纤维素燃料乙醇被认为是一种重要的化石燃料可再生替代能源[1-2]。二代纤维素乙醇是指以农作物废弃物为原料,通过对原料进行预处理和纤维素酶解得到可发酵糖,经微生物发酵生产得到的乙醇,因其原料来源广泛而受到关注。从20世纪初至今,纤维素乙醇技术的发展日渐成熟,然而距离实现大规模工业化生产仍然有一定的距离,尤其是木质纤维素水解过程中产生的多种抑制物对后续的酶解和发酵过程带来的负面影响,是纤维素乙醇发展所面临的瓶颈问题之一[3-4]。
由于木质纤维素原料内部结构成网状紧密排列,组成复杂,木质纤维原料未经预处理时酶解得率不到20%,效率低而且非常缓慢。因此,预处理是酿酒酵母利用木质纤维原料发酵生产燃料乙醇必不可少的环节[5-7]。通过预处理,在一定浓度化学试剂、温度、压力下可有效破坏木质纤维素的致密结构,降低聚合度和结晶度,增加酶与底物的接触面积,从而提高酶解效率[8]。然而木质纤维原料在预处理过程中,特别是在典型的稀酸预处理条件下,生物质原料会降解生成一系列结构复杂的抑制物(见图1)。这些发酵抑制物的种类和浓度与原料和预处理条件密切相关,随着抑制物浓度的增加,严重影响细胞活力和生长速度,延长生长延滞期,降低酶解和发酵过程中葡萄糖和木糖的转化率[9-14]。
酿酒酵母(Saccharomyces cerevisiae)作为传统生产乙醇的研究最广泛的微生物,提高其对纤维素水解液中抑制物耐受性已成为当前燃料乙醇研究的热点。近年来,研究者在酿酒酵母抵御水解液抑制物方面进行了研究探索,围绕抑制物对酵母的抑制机理,代谢抑制物的生化途径,以及构建抑制物抗性提高的酵母菌株等方面开展了一系列工作,取得了很大的研究进展。本文针对木质纤维素预处理水解液抑制物,综述了其来源,抑制机理以及提高酿酒酵母对抑制物的耐受性方法,旨在为选育耐受性良好的酿酒酵母提供参考。
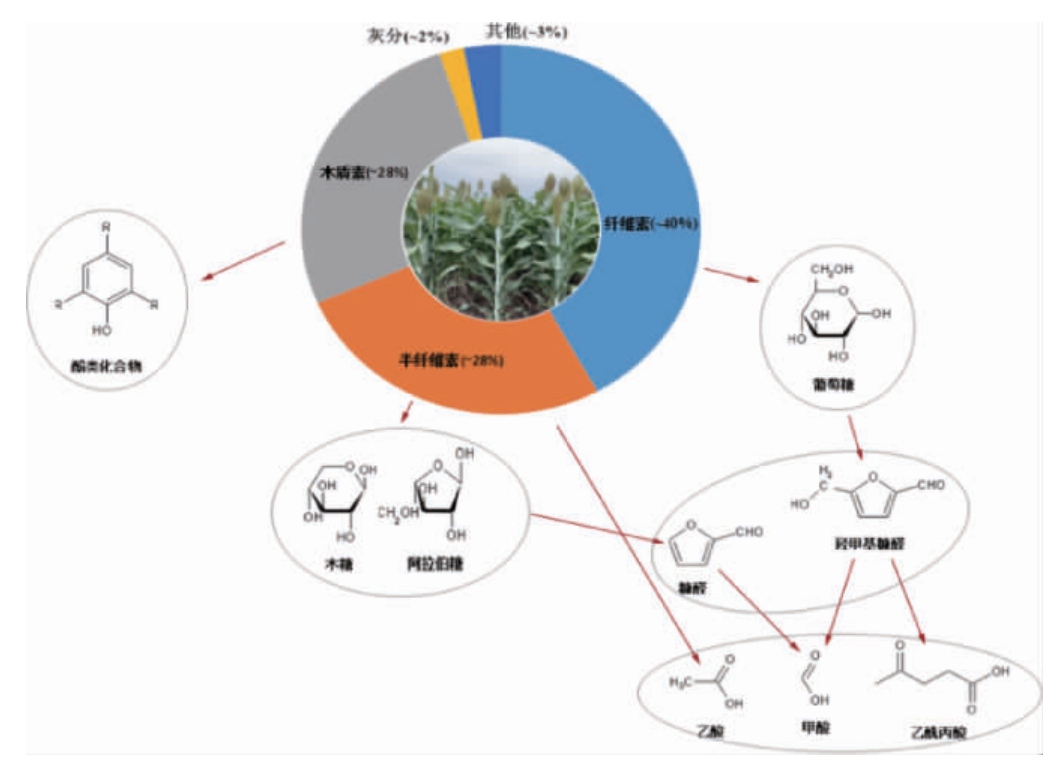
图1 木质纤维素原料的组成及主要水解抑制物
Fig.1 Composition of lignocellulosic biomass and main hydrolysis products
1 木质纤维素原料的预处理与发酵抑制物的形成机理
1.1 酸处理
木质纤维素酸预处理包括稀酸预处理和浓酸预处理两种,为了避免设备腐蚀以及考虑酸的回收问题,稀酸预处理被认为具有更高的经济可行。木质纤维素经稀酸预处理后,纤维素的平均聚合度下降,反应能力增强,影响稀酸预处理的因素主要包括酸浓度、温度和反应时间[15-16]。与其他预处理方法相比,稀酸预处理方法使半纤维素以单糖形式的溶出率更高。然而,酸预处理过程中产生的己糖和戊糖会降解生成5-羟甲基糠醛(5-hydroxymethyl furfural,5-HMF)和糠醛,进而降解成甲酸,乙酰丙酸等对后续发酵微生物有强烈抑制甚至有致死毒性的物质。随着酸浓度的增大,水解液中抑制物的浓度也上升[17]。因此,为了降低这些抑制物对后续发酵过程的影响,木质纤维素水解液必须经过脱毒处理才能进入发酵阶段[9]。
1.2 碱处理
与酸处理相比,碱处理可削弱纤维素和半纤维素之间的氢键,引起木质素和半纤维素间的酯键发生皂化,破坏木质素的结构,得到更高的木质素溶出率和较低的纤维素、半纤维素溶出率,此时与木质素连接的侧链基团断裂释放出酚类物质,生成阿魏酸、香草醛、丁香醛等抑制物,其中一些低分子并且含有脂肪族官能团的的酚类单体抑制物对后续酶解和酵母的生长抑制作用最强[18-19]。丁驰等[20-21]对经过不同浓度的氢氧化钠溶液预处理后的稻草秸秆水解液中抑制物成分进行了分析研究,较未经预处理的对照样,经过碱预处理后的水解液中酚类和酸类抑制物种类明显增多且分布非常集中,成为最主要的抑制物,且抑制物的含量也随碱浓度上升而上升,其中以阿魏酸为主的酚类物质含量占绝对优势。
1.3 蒸汽爆破处理
蒸汽爆破预处理可以显著降低原料中半纤维素的含量和改变木质素的结构,提高纤维素酶的可及度,提高材料的酶解效率,是一种应用前景十分广阔的预处理方法。然而,在高温高压或化学物质催化作用下,同时伴随有许多副反应发生,半纤维素部分过度降解,产生乙酸、糠醛等发酵抑制物[22]。汽爆条件的不同,对不同材料的酶解效率以及抑制物生成的影响程度也不同,影响因素包括蒸汽爆破压力、温度、时间等[23-25]。王风芹等[26]采用不同的蒸汽爆破条件对玉米芯进行预处理,研究了蒸汽爆破玉米芯中的有毒物质含量,结果表明随着蒸汽爆破强度的增强,半纤维素水解的低聚糖进一步被分解破坏,甲酸、乙酸、糠醛、5-HMF和总酚的含量显著增多。
2 抑制物的种类和作用
2.1 酸类物质
木质纤维素水解液中的酸类毒性副产物主要包含甲酸和乙酸,甲酸是由糠醛和5-HMF进一步降解形成的,而乙酸则主要是在半纤维素中的乙酰基裂解之后生成的,其中乙酸的浓度相对较高。对于弱酸类物质对微生物的抑制机理,一般认为甲酸和乙酸都属于酸性弱电解质,纤维素水解液通常为弱酸性,pH值低于甲酸和乙酸的酸度系数(pKa)值,使得两种物质呈现未解离的小分子状态,可通过细胞膜进入细胞内部;当弱酸进入接近中性的细胞质环境后,甲酸和乙酸分子开始解离,形成酸根离子(RCOO-)和氢离子(H+),由于胞内H+大量积累,引起细胞质酸化[27],破坏细胞的跨膜电势,降低代谢活性。同时为维持正常的生长环境,细胞会激活细胞膜上的三磷酸腺苷(adenosine triphosphate,ATP)酶,通过水解ATP获得足够能量驱动质子泵,从而排出H+。由于ATP大量消耗而又得不到及时的补充,用于细胞代谢的ATP就会供应不足,细胞生长一些必需的酶,辅酶以及一些营养物质得不到及时的供应和运输,从而导致细胞活性降低,并最终影响微生物的发酵过程[28]。
2.2 醛类物质
糠醛和5-HMF是水解液中两种主要的醛类毒性抑制物,其中糠醛主要是由木糖、阿拉伯糖等戊糖脱水环化形成,而5-HMF则主要是由葡萄糖、甘露糖等己糖脱水生成。糠醛和5-HMF对微生物的抑制机理相似,但糠醛对细胞生长和代谢的抑制作用较5-HMF更强,通常会抑制细胞糖酵解和三羧酸循环等重要碳代谢过程中相关的酶(如己糖激酶,乙醇脱氢酶,乙醛脱氢酶等)活性,降低细胞的比生长速率,同时可降低乙醇得率和产率[29-30]。此外,进入细胞的醛类抑制物还会导致活性氧含量的上升,引起线粒体,核染色体的损伤。虽然微生物自身可将糠醛和5-HMF还原为糠醇、羟甲基糠醇等毒性较小的物质来减少醛类抑制物对自身的影响,但这个转化过程需要消耗大量的ATP,同时会使细胞内的还原力水平降低,还与乙醛共同竞争乙醇脱氢酶,从而延迟酵母代谢活动,抑制乙醇生成[31-32]。糠醛和5-HMF也可与脂肪酸类抑制物产生协同效应降低酵母的生理性能和发酵性能[33]。
2.3 酚类化合物
酚类物质主要来源于木质素的降解,主要包括以阿魏酸和香草醛为代表的酚类抑制物,虽然这些酚类抑制物在纤维素水解液中的浓度很低,但它们对微生物的毒性作用却很大。有关酚类化合物对微生物的抑制机制还没有完全阐明,一般认为酚类化合物可渗透到细胞膜内,引起细胞活性氧的积累,而且可通过改变细胞膜蛋白和脂质的比例,引起细胞膜的不可逆的损伤来影响细胞正常的生长,且分子质量和酚单体上取代基的位置也影响酚类物质的毒性[34-35]。
3 提高酿酒酵母对抑制物耐受性的方法
为了降低纤维素水解液抑制物对后续酶解以及酿酒酵母发酵的影响,并提高乙醇的生产效率,水解液抑制物的脱毒处理是常用的方法之一。但是脱毒处理工序往往会造成水解液中糖类的损失以及增加纤维素乙醇发酵的成本。因此只有提高发酵菌株的抑制物耐受性,使其适应未脱毒的水解液环境,才能从根本上解决水解液抑制物对酵母产生的毒害影响。通过菌种筛选,诱变育种,基因工程改造以及长期适应性驯化是提高酿酒酵母对水解液抑制物耐受性得到有效措施。
3.1 自然选育
发酵菌种的自然选育就是从自然或者工业环境当中收集微生物,筛选,鉴定对抑制剂具有高抗性的菌株。采用传统分离筛选的方法简单实用,目前仍是筛选高耐受性酵母菌株的有效方法之一。FAVARO L等[36]从酿酒厂葡萄渣里筛选到40株酿酒酵母菌株,并对这些菌株进行了脂肪族羧酸、呋喃醛以及含有混合抑制剂的甘蔗渣水解液的耐受性评价,发现这些菌株的发酵能力和抑制物抗性均大于普通的工业和商业酿酒酵母菌株。WIMALASENA T T等[37]从自然环境、葡萄酒厂、啤酒厂等筛选到了90株酿酒酵母菌株,并就目前木质纤维素水解液乙醇发酵过程中的一些胁迫条件(高温、高渗透压、高乙醇浓度和抑制物)做了表型评价,发现许多菌株对多种抑制剂具有耐受性。
3.2 诱变筛选
纤维素水解液中的多种抑制物对细胞的毒害作用机理是非常复杂的,很多基因在细胞中作用机制以及作用靶点尚不清楚。诱变及筛选是一种传统的菌种选育手段,具有简便、快捷、高效等特点,因此一直是菌种选育普遍使用的方法之一[38]。陈胜杰等[39]以酿酒酵母XP为出发菌株,通过常温等离子诱变技术,得到突变体库,并以玉米秸秆水解液为筛选压力,经过多代连续传代,梯度增加抑制物浓度,驯化培养突变株,最终筛选出能够在玉米秸秆水解液中高产酒精的改造菌XP2,其生长性能优势明显,转化糠醛和乙酸的能力较原菌有明显提升;董健等[40]以酿酒酵母AY12为出发菌株进行紫外诱变获得突变群体,再与酿酒酵母反复产孢与杂交筛选得到最优菌株LYQ-F1;郭雪娇等[41]通过诱变育种结合驯化工程选育了一株具有对复合抑制剂高耐受性的酿酒酵母XYJ003,在未脱毒的秸秆纤维素水解液中发酵,乙醇产量达到4.16 g/(L·h),而对照菌株无乙醇产出。林贝等[42]以酿酒酵母Sc4126作为出发菌株,在2 g/L糠醛、5 g/L乙酸、1 g/L香草醛组成的复合抑制剂存在下进行紫外诱变筛选,而后逐渐提高复合抑制剂浓度进行驯化,发酵对比实验结果显示其在复合抑制剂中的耐受性有效提高,在复合抑制剂存在下,优势菌株Sc4126-1发酵时间为48 h,乙醇平均产率0.19 g/(L·h),而原始菌株Sc4126发酵时间138 h,乙醇平均产率0.06 g/(L·h),相比原始菌株,优势菌株发酵时间缩短65.22%,乙醇平均产率提高2.17%。
3.3 基因工程改造
基于不同微生物对环境胁迫耐受能力的差异及转录组学和蛋白表达分析的基础上,挖掘新的靶点基因和代谢通路,进行过表达是强化酵母耐受力的有效手段之一。通过过表达相关代谢关键酶蛋白,可开发出对木质纤维素水解抑制物具有更好抗性和代谢能力的重组微生物。基因工程改造方法针对性和目的性强,随着对细胞耐受机理的分析,相关基因改造策略和合理的基因线路已经被成功设计去强化菌株对单一抑制剂和混合抑制剂的耐受性。张克俞等[43]在硫酸锌添加条件下转录组分析揭示其与转录调控、碳水化合物代谢、核苷酸代谢及氨基酸代谢等途径相关基因的变化,筛选分析可能关键基因ADE17、SSZ1、SET5、PPR1、OGG1和YKL222C过表达对酿酒酵母环境胁迫耐受性的影响,同时发现这些基因过表达不仅提高了酵母乙酸耐受性,而且赋予了其应对其他多种胁迫的耐受性(糠醛、苯酚、丙酸);吴宇等[44]以原始酵母菌BY4741为出发菌株,通过表达酿酒酵母自身的谷氨酰胺合成酶基因GLN1,成功构建了重组菌株YEA9,使得胞内谷胱甘肽抗氧化系统的水平得到提升,进而降低酿酒酵母中活性氧的含量,从而增强了酿酒酵母的耐受糠醛胁迫能力和乙醇发酵速率,最终乙醇浓度提高了9.2倍;细胞膜蛋白具有物质运输,细胞识别以及细胞防御等多项功能,向瑞娟[45]利用基因工程改造相关手段将膜转运蛋白基因ADP1,MDRI过表达于酿酒酵母S.cerevisiae 280/959,并通过甲酸,乙酸,糠醛等抑制物胁迫条件下,进行生长情况比较和发酵性能考察,结果表明过表达菌株较对照菌株表现出一定的抗性,在生长速率,糖耗速率,乙醇产率等方面有明显的优势;LUO P等[46]研究发现来自耐辐射球菌(Deinococcus radiodurans)RI的IrrE调控基因的异源表达不仅赋予了酿酒酵母对单一或者多种抑制剂(糠醛、5-HMF、甲酸和乙酸)更好的耐受性,而且增强了其对活性氧的清除能力,使得菌种在乙醇、酸、渗透压等多重压力下仍然保持旺盛的生长和代谢活力。
3.4 适应性驯化
进化工程是开发用于工业生产燃料和化学品的高性能酵母菌株的一种有效手段,通过模拟自然进化中的生物变异和选择过程,在人工提供选择压力的条件下使微生物进化,然后从进化的菌群中筛选出性状优良的菌株[47-48],它可以加速酵母基因组和特定基因的体内突变率获得表型稳定的菌株。TIAN S等[49]在软木水解液中对S.cerevisiae Y5进行了适应性驯化,通过提高水解液抑制物浓度的方法,将对数生长期的酿酒酵母逐渐转移到新的适应环境,直到能够在未稀释的水解液中稳定连续传代培养,结果显示驯化之后的酿酒酵母对1~4 g/L不同质量浓度的糠醛和5-HMF都有很高的耐受能力。HAWKINS G M等[50]以一株工业酵母菌株XR122N为基础,利用松树水解液进行连续传代驯化得到菌株AJP50,结果表明菌株AJP50很明显地缩短了发酵延滞期,可以快速地将糠醛和5-HMF转化为低毒性的醇类衍生物,从而减少了细胞内活性氧对细胞的毒害作用;QURESHI A S等[51]通过将S.cerevisiae DQ1每隔12 h,依次转移到含有抑制物的玉米秸秆水解液中进行适应性驯化,最终在65 d的连续适应后获得稳定的酵母菌株,适应性酵母菌株在30%的固体含量下,发酵得到71.40 g/L的乙醇含量和80.34%的乙醇产率,显著地改善了酵母的发酵性能。LI W C等[52]以可利用木糖发酵的S.cerevisiae E7为出发菌株,将其在浓度从40%~100%不断提高的含有复合抑制剂的培养基中进行驯化,最终得到的驯化菌株S.cerevisiae E7-403缩短了延滞期,更有效地去除了糠醛对酵母生长和发酵的影响,增强了对混合糖的利用和乙醇得率。
4 展望
利用木质纤维素作为原料生产燃料乙醇,是实现由传统化石能源到清洁型能源转变的重要发展方向。酿酒酵母因其独有的乙醇产率高,耐受性好的特性,这使得其广泛用于燃料乙醇的工业生产,但是距离纤维素乙醇能够大规模地商业化应用仍然有众多瓶颈问题亟需解决。
目前,利用酿酒酵母进行乙醇发酵主要以下几个问题;①酿酒酵母不能利用半纤维素水解产生五碳糖;②酿酒酵母生长和乙醇生产受预处理副产物和发酵物的抑制;③酿酒酵母高温、高糖浓度发酵性能不佳。尽管在增强菌体对纤维素水解液中戊糖的利用以及单一环境压力的耐受性和作用机制方面已有了较多的研究,但是选择和育种抗多重应力的工业酵母是仍当前研究的重点。此外,目前还缺少工程菌株在纤维素生物质水解液发酵实际应用过程中的评价和放大研究。随着对抑制物形成,作用机制及酿酒酵母耐受机制的研究不断深入,构建本身具有抑制物代谢活性的工业发酵菌株,将菌株的代谢能力提升和耐受能力强化进行耦合是未来解决木质纤维素水解液抑制物问题的理想手段,但是微生物对抑制物的耐受和代谢是一个复杂的调控体系,目前对抑制物代谢及耐受的基因背景尚未清晰了解,针对复杂的抑制物环境,利用基因工程和代谢工程定向改造微生物受到限制,另一方面,不同预处理方法的处理效果跟原料的组分也有很大的关系,因此,在木质纤维素深加工过程中,应根据原料的类型探索合适的预处理方式,以减少抑制物的产生和环境污染,提高整体的生产效率和经济性。
综上所述,加强酿酒酵母对木质纤维素乙醇发酵过程中的研究和评价,进行菌株构建和优化,进一步提高纤维素乙醇生产的高效性和经济性,是未来酵母菌株选择的重要研究方向。面对乙醇生产工业复杂的环境,只有提高酿酒酵母对多种环境压力胁迫下的耐受性及发酵效率才是未来能够大规模高效利用木质纤维素水解液的关键。
[1]宁艳春,陈希海,王硕,等.纤维素乙醇研发现状与研究趋势分析[J].化工科技,2020,28(1):65-68.
[2]黄伊婷,黄清妹,杨亚会,等.大型藻类发酵燃料乙醇的研究进展[J].中国酿造,2017,36(8):26-30.
[3]杨莉,谭丽萍,刘同军.木质纤维素预处理抑制物产生及脱除方法的研究进展[J].生物工程学报,2021,37(1):15-29.
[4]孙慧敏,邹丽花,郑兆娟,等.应用生物技术降解木质纤维素水解液中呋喃醛[J].生物工程学报,2021,37(2):473-485.
[5]LIU C G,XIAO Y,XIA X X,et al.Cellulosic ethanol production:Progress,challenges and strategies for solutions[J]. Biotechnol Adv,2019,37:491-504.
[6]REZANIA S,ORYANI B,CHO J,et al.Different pretreatment technologies of lignocellulosic biomass for bioethanol production:An overview[J].Energy,2020,199:117457.
[7]彭姿,谭兴和,熊兴耀,等.木质纤维素糖化前预处理新技术研究进展[J].中国酿造,2013,32(1):1-4.
[8]CHUNDAWAT S P S,BECKHAM G T,HIMMEL M E,et al.Deconstruction of lignocellulosic biomass to fuels and chemicals[J].Annu Rev Chem Biomol Eng,2011,2:121-145.
[9]王新明,肖林,杨建,等.纤维素乙醇发酵方法及发酵抑制物[J].中国酿造,2013,32(S1):1-4.
[10]DU C,LI Y,ZONG H,et al.Production of bioethanol and xylitol from nondetoxified corn cob via a two-stage fermentation strategy[J]. Bioresource Technol,2020,310:123427.
[11]QI F,KITAHARA Y,WANG Z,et al.Novel mutant strains of Rhodosporidium toruloides by plasma mutagenesis approach and their tolerance for inhibitors in lignocellulosic hydrolyzate[J].J Chem Technol Biotechn,2014,89(5):735-742.
[12]WU J,ZHOU Y J,ZHANG W,et al.Screening of a highly inhibitor-tolerant bacterial strain for 2,3-BDO and organic acid production from non-detoxified corncob acid hydrolysate[J].AMB Express,2019,9(1):153.
[13]LIU Z H,QIN L,ZHU J Q,et al.Simultaneous saccharification and fermentation of steam-exploded corn stover at high glucan loading and high temperature[J].Biotechnol Biofuel,2014,7(1):167.
[14]DIJK M V,ERDEI B,GALBE M,et al.Strain-dependent variance in shortterm adaptation effects of two xylose-fermenting strains of Saccharomyces cerevisiae[J].Bioresource Technol,2019,292:121922.
[15]杨盛茹,邹建,丁长河,等.稀酸预处理玉米芯酶解工艺响应面优化研究[J].中国酿造,2017,36(1):111-115.
[16]HENDRIKS A T W M,ZEEMAN G.Pretreatments to enhance the digestibility of lignocellulosic biomass[J]. Bioresource Technol,2009,100(1):10-18.
[17]RAJAN K,CARRIER D J.Effect of dilute acid pretreatment conditions and washing on the production of inhibitors and on recovery of sugars during wheat straw enzymatic hydrolysis[J].Biomass Bioenergy,2014,62(352):222-227.
[18]SHAO L Y,CHEN H,LI Y L,et al.Pretreatment of corn stover via sodium hydroxide-urea solutions to improve the glucose yield[J]. Bioresource Technol,2020,doi:10.1016/j.biortech.2020.123191.
[19]顾翰琦,刘冉,邵玲智,等.酿酒酵母对酚类抑制物耐受性研究[J].生物技术通报,2020,36(6):136-142.
[20]丁驰,黄慧琴,张树栋,等.不同浓度NaOH 预处理对稻秸水解液中抑制物组分的影响[J].食品与发酵工业,2015,41(9):51-56.
[21]丁驰,张树栋,张秋卓,等.碱处理对稻秸水解液中抑制物成分的影响[J].环境科学与技术,2015,38(10):21-26.
[22]李国栋,赵圣国,张养东,等.秸秆饲料化预处理方式及其发酵抑制化合物的作用机理[J].动物营养学报,2016,28(10):3051-3058.
[23]BISWAS R,UELLENDAH H,AHRING B K.Wet explosion:a universal and efficient pretreatment process for lignocellulosic biorefineries[J].Bioenerg Res,2015,8:1101-1116.
[24]KAAR W E,HOLTZAPPLE M T.Benefits from tween during enzym ic hydrolysis of corn stover[J].Biotechnol Bioeng,2015,59(4):419-427.
[25]KIM Y,KREKE T,HENDRICKSON R,et al.Fractionation of cellulase and fermentation inhibitors from steam pretreated mixed hardwood[J].Bioresour Technol,2013,135(3):30-38.
[26]王风芹,谢慧,仝银杏,等.蒸汽爆破预处理对玉米芯酶水解的影响[J].太阳能学报,2018,39(6):1675-1680.
[27]郭凯原,石海强,熊学东,等.木质纤维素水解过程中发酵抑制物的产生与脱毒[J].黑龙江造纸,2016,44(4):16-21.
[28]王永伟,王异静,张五九.生物质原料稀酸预处理水解液中发酵抑制物研究进展[J].酿酒科技,2009(10):91-94.
[29]PETERSSON A,ALMEIDA J R M,MODIG T,et al.A 5-hydroxymethyl furfural reducing enzyme encoded by the Saccharomyces cerevisiae ADH6 gene conveys HMF tolerance[J].Yeast,2010,23(6):455-464.
[30]JÖNSSON L J,MARTÍN C.Pretreatment of lignocellulose:Formation of inhibitory by-products and strategies for minimizing their effects[J].Bioresource Technol,2016,199:103-112.
[31]WANG S Z,HE Z J,YUAN Q P.Xylose enhances furfural tolerance in Candida tropicalis by improving NADH recycle[J].Chem Eng Sci,2016,158:37-40.
[32]赵孝阳.乙酸抗性菌株选育及混菌发酵生产乙醇[D].大连:大连理工大学,2019.
[33]BAKKER R R,BAETS P,EGGINK G,et al.By-products resulting from lignocellulose pretreatment and their inhibitory effect on fermentations for(bio)chemicals and fuels[J].Appl M icrobiol Biotechn,2014,98(23):9579-9593.
[34]PALMQVIST E,HAHN-HAGERDAL B.Fermentation of lignocellulosic hydrolysates.II:inhibitors and mechanisms of inhibition[J]. Bioresource Technol,2000,74(1):25-33.
[35]何北海,林鹿,孙润仓,等.木质纤维素化学水解产生可发酵糖研究[J].化学进展,2007(Z2):1141-1146.
[36]FAVARO L,BASAGLIA M,TRENTO A,et al.Exploring grape marc as trove for new thermotolerant and inhibitor-tolerant Saccharomyces cerevisiae strains for second-generation bioethanol production[J].Biotechnol Biofuel,2013,6:168.
[37]WIMALASENA T T,GREETHAM D,MARVIN M E,et al.Phenotypic characterisation of Saccharomyces spp.yeast for tolerance to stresses encountered during fermentation of lignocellulosic residues to produce bioethanol[J].M icrobial Cell Factor,2014,13:47.
[38]温晓瑜,王靖,王金玲,等.酵母菌利用木糖发酵生产乙醇的研究进展[J].中国酿造,2011,30(12):12-16.
[39]陈胜杰,高翔,袁戎宇.常温常压等离子诱变结合玉米秸秆水解液驯化酿酒酵母生产生物乙醇[J].食品与发酵工业,2020,46(4):167-171.
[40]董健,李月强,陈叶福.传统诱变与基因组重排技术相结合选育耐高温酿酒酵母菌株[J].酿酒科技,2013(8):50-53.
[41]郭雪娇,查健,姚坤,等.选育耐受复合抑制剂酿酒酵母提高乙醇产量[J].中国生物工程杂质,2016,36(5):37-105.
[42]林贝,李健秀,刘雪凌.紫外诱变结合驯化提高酿酒酵母对抑制物耐受性[J].生物技术,2018,28(1):85-91.
[43]张克俞,张明明,赵心清,等.关键基因过表达提高酿酒酵母抑制剂耐受性及乙醇发酵性能[J].应用与环境生物学报,2018,24(3):541-546.
[44]吴宇,王金华,赵筱.GLN1 基因过表达对提高酿酒酵母糠醛耐受性的研究[J].生物技术通报,2020,36(8):69-78.
[45]相瑞娟.木质纤维素水解液抑制物高抗性酵母的选育[D].大连:大连理工大学,2016.
[46]LUO P,ZHANG Y,SUO Y,et al.The global regulator IrrE from Deinococcus radiodurans enhances the furfural tolerance of Saccharomyces cerevisiae[J].Biochem Eng J,2018,136:69-77.
[47]柳洋,汤晓玉,刘义,等.进化工程选育乙醇发酵酵母菌株研究进展[J].中国酿造,2016,35(11):26-30.
[48]SCALCINATI G,OTERO J M,VLEET J R,et al.Evolutionary engineering of Saccharomyces cerevisiae for efficient aerobic xylose consumption[J]. FEMS Yeast Res,2012,12(5):582-597.
[49]TIAN S,ZHU J,YANG X.Evaluation of an adapted inhibitor-tolerant yeast strain for ethanol production from combined hydrolysate of softwood[J].Appl Energy,2011,88(5):1792-1796.
[50]HAWKINS G M,DORAN-PETERSON J.A strain of Saccharomyces cerevisiae evolved for fermentation of lignocellulosic biomass displays improved growth and fermentative ability in high solids concentrations and in the presence of inhibitory compounds[J].Biotechnol Biofuel,2011,4(1):49.
[51]QURESHI A S,ZHANG J,BAO J.High ethanol fermentation performance of the dry dilute acid pretreated corn stover by an evolutionarily adapted Saccharomyces cerevisiae strain[J].Bioresource Technol,2015,189:309-404.
[52]LI W C,ZHU J Q,ZHAO X,et al.Improving co-fermentation of glucose and xylose by adaptive evolution of engineering xylose-fermenting Saccharomyces cerevisiae and different fermentation strategies[J]. Renewable Energy,2019,139:1176-1183.