玉米作为主要的粮食作物,一直以来是商品市场上的大品种,玉米深加工产品主要有玉米淀粉、玉米蛋白粉、变性淀粉、玉米淀粉糖、玉米油、食用酒精、谷氨酸、赖氨酸、木糖醇等数百个品种[1]。微生物油脂也可采用玉米淀粉糖发酵生产[2],具有潜在商业化价值,可应用于营养保健品、药物、水产养殖饲料和生物柴油原料等方面[3-8]。但目前国内生产淀粉糖的原料大都采用玉米淀粉,生产成本高,作为发酵用糖液会造成资源浪费[9]。与复杂的湿法玉米淀粉生产技术相比,玉米粉是将玉米籽粒通过磨碎、筛分、风选等简单方法,分出胚芽和纤维,而得到低脂肪的玉米粉。玉米粉水解糖液含有葡萄糖、蛋白质、脂肪及多种维生素、矿物质和微量元素等,是发酵工业物美价廉的重要原料[10-11]。玉米粉液化、糖化工艺优化的方法有双酶法、复合糖化酶法、喷射液化法、挤压酶解法等[12-15],目的是提高液化液质量,为糖化创造有利条件,缩短糖化时间,提高糖液质量,节约能耗,降低生产成本。
本研究以玉米粉为原料,以葡萄糖当量(dextrose equivalent,DE)值作为评价指标,通过单因素试验与正交试验对玉米粉水解糖液液化、糖化工艺条件进行优化,旨在为微生物油脂的工业化生产提供参考。
1 材料与方法
1.1 材料与试剂
玉米粉(水分含量为13.85%,粗淀粉含量为71.10%):市售;α-淀粉酶(酶活4 000 U/g):天津市光复精细化工研究所;糖化酶(酶活100 000 U/g):上海源叶生物科技有限公司;无水氯化钙(分析纯):西陇化工股份有限公司;3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)(分析纯):阿拉丁试剂(上海)有限公司;丙三醇、葡萄糖(均为分析纯):北京化工厂;氢氧化钠(分析纯):天津市光复科技发展有限公司。
1.2 仪器与设备
BGT-8A糖化仪:杭州博日科技有限公司;GT10-1型高速台式离心机:北京时代北利离心机有限公司;UV5100B紫外可见分光光度计:上海元析仪器有限公司;LH-T55数显折光仪:杭州陆恒生物科技有限公司。
1.3 试验方法
1.3.1 玉米糖液制备工艺流程

1.3.2 分析方法
(1)还原糖的测定
采用DNS法[16],待测液5 000 r/min离心10 min,取上清液稀释至适宜倍数待测;葡萄糖标准曲线的制备,取配制好的不同含量得标准葡萄糖溶液0.5 mL,再加入3,5-二硝基水杨酸(DNS)试剂1.5 mL,轻摇混匀,沸水浴5 min显色,冷却后加4 mL去离子水,振荡均匀。在波长540 nm处比色,以去离子水为空白,测出各管的吸光度值。以吸光度值(y)为纵坐标,葡萄糖含量(x)为横坐标,绘制葡萄糖标准曲线,得到回归方程为y=0.000 7x+0.021 9,相关系数R2=0.992 1。取适当稀释后的样品0.5 mL,按上述方法测吸光度值,按照标准曲线回归方程计算待测液还原糖含量。
(2)干物质含量的测定
采用折光法[17]测定料液的干物质含量(°Bx)。
(3)葡萄糖当量值
DE值计算公式如下[18]:
1.3.3 玉米粉糖液液化工艺优化
液化液的DE值控制一般在15%~20%[19-20]。液化DE值过低,料液易老化、黏度较高、不宜操作,还会将一些液化不完全的大分子糊精带入糖化过程,直接影响糖化质量;液化程度过高不利于糖化过程酶与底物形成络合结构,影响催化效率。
单因素试验:以玉米粉为原料,按料液比分别为1∶8、1∶5、1∶4、1∶3、1∶2(g∶mL)配制不同浓度的粉浆,pH值为6.2,无水氯化钙含量0.2%,α-淀粉酶添加量分别为2 U/g、4 U/g、6 U/g、8 U/g、10 U/g玉米粉,液化温度分别为70 ℃、75 ℃、80 ℃、85 ℃、90 ℃,液化时间分别为20 min、40 min、60 min、80 min、100 min,酶解结束沸水浴10 min灭酶,5 000 r/min离心取上清液,测定还原糖含量与干物质含量,计算DE值。分别考察料液比、α-淀粉酶添加量、液化温度及液化时间对玉米粉糖液液化的影响。
正交试验:根据单因素试验所得结果,使用L9(34)正交设计,以DE值为评价指标,进行3因素3水平正交试验确定最优液化工艺条件。
1.3.4 玉米粉糖液糖化工艺优化
单因素试验:液化液调pH值为4.3,糖化温度分别为50 ℃、55 ℃、60 ℃、65 ℃、70 ℃,糖化酶添加量分别为50 U/g、100 U/g、150 U/g、200 U/g、250 U/g、300 U/g,糖化时间分别为2 h、4 h、6 h、8 h、10 h、12 h、14 h,糖化液沸水浴10 min灭酶,5 000 r/min离心取上清液,测定还原糖含量与干物质含量,计算DE值。糖化酶添加量、糖化温度及糖化时间对玉米粉糖液糖化的影响。
正交试验:根据单因素试验所得结果,使用L9(34)正交设计,以DE值为评价指标,进行3因素3水平正交试验确定最优糖化工艺条件。
1.3.5 数据处理方法
本研究测定试验均重复3次,结果为平均值的方式表示。使用OEA3.1软件进行正交试验设计,SAS 9.1进行数据处理。
2 结果与分析
2.1 玉米粉糖液最佳液化工艺条件的确定
2.1.1 料液比对液化效果的影响
由图1可知,随着玉米粉浆中含水量的降低,DE值先逐渐增加后又降低,料液比为1∶4(g∶mL)时DE值最大;料液比过小即料液浓度过低,淀粉水解产物糊精浓度低使酶活力稳定性降低[17],料液中还原糖产生的少,DE值较低;料液比过大即料液浓度过高,理论上可产生较多的糊精对增加酶活力稳定性有提高作用,但料液含水量过低,原料玉米粉吸水不充分,流动性较差,黏度较高,不利于酶与底物结合,故产生的还原糖较少,造成料液DE值较低[21-22]。因此,最适料液比为1∶4(g∶mL),此时料液淀粉水解产物糊精浓度可使酶活力稳定性增加,同时有利于酶与底物结合,产生短链糊精和少量低分子糖类,从而还原糖增加、DE值最大。
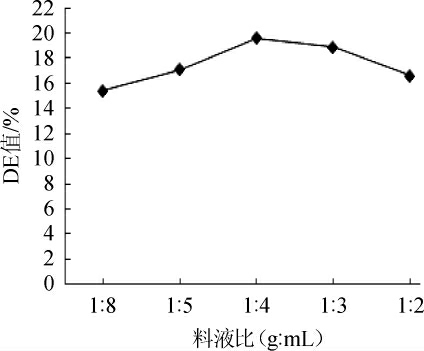
图1 料液比对葡萄糖当量值的影响
Fig.1 Effect of solid-liquid ratio on dextrose equivalent value
2.1.2 液化时间对液化效果的影响
液化开始时首先是α-淀粉酶分解淀粉分子中的α-1,4糖苷键产生糊精和低聚糖,此酶促反应速度较快。但α-淀粉酶不能水解α-1,6糖苷键,也不能水解紧靠分支点的α-1,4糖苷键,所以水解支链淀粉的速度较直链淀粉慢。此时酶解产物的积累与α-1,6糖苷键相对比例的增大会使得酶促反应速度下降[23]。由图2可知,液化时间为40 min时,DE值达到一个高点,其原因是最初还原糖含量的增加速度比干物质含量增加的速度要快,但是此时的还原糖含量却没有达到最大值。而当液化时间为60 min时,DE值稍有降低,是因为还原糖的含量平稳,干物质量略有升高[18]。之后随着时间增加DE值逐渐升高。考虑液化醪DE值在15%~20%对后序糖化有利,因此,选择最适液化时间为60 min。

图2 液化时间对葡萄糖当量值的影响
Fig.2 Effect of liquefaction time on dextrose equivalent value
2.1.3 α-淀粉酶添加量对液化效果的影响
在酶促反应中,底物浓度足够高时,酶促反应速度随着酶添加量的增加而提高。由图3可知,随着α-淀粉酶添加量的增大,液化醪DE值逐渐提高。当液化醪液化程度(DE值)控制在15%~20%时,利于后续糖化与发酵。α-淀粉酶添加量>8 U/g时,DE值过高,生成的糊精分子太小,不利于后续糖化酶构成络合结构,影响糖化酶的催化效率[24]。因此,最适α-淀粉酶添加量为6 U/g。
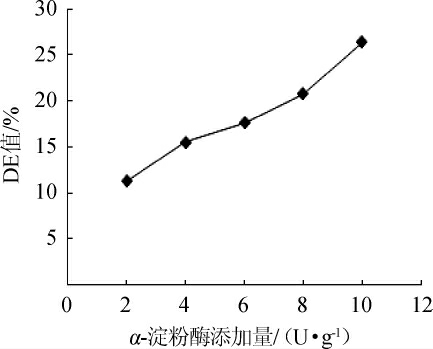
图3 α-淀粉酶添加量对葡萄糖当量值的影响
Fig.3 Effect of α-amylase addition on dextrose equivalent value
2.1.4 液化温度对液化效果的影响
玉米淀粉的糊化温度是65~75 ℃,糊化过程淀粉颗粒吸水膨胀,晶体结构破坏,有利于液化过程酶与底物作用,淀粉分子形成低分子糊精溶液。由图4可知,在液化温度为80 ℃时DE值最高,在温度高于80 ℃后DE值有所降低。这是因为在一定温度范围内,酶促反应速度随温度的升高而增快,至最适反应温度后,继续升高温度会造成部分酶的失活,使反应速度下降[25]。因此,最适液化温度为80 ℃。

图4 液化温度对葡萄糖当量值的影响
Fig.4 Effect of liquefaction temperature on dextrose equivalent value
2.1.5 液化条件优化正交试验
根据单因素试验所得结果,考察液化时间、α-淀粉酶量、液化温度3个因素对玉米粉液化程度的影响,选择合适的水平范围,以DE值为考察指标,进行正交试验确定最优液化条件。正交试验结果与分析见表1,方差分析见表2。
表1 玉米粉液化条件优化正交试验结果与分析
Table 1 Results and analysis of orthogonal experiments for liquefaction conditions optimization of corn flour
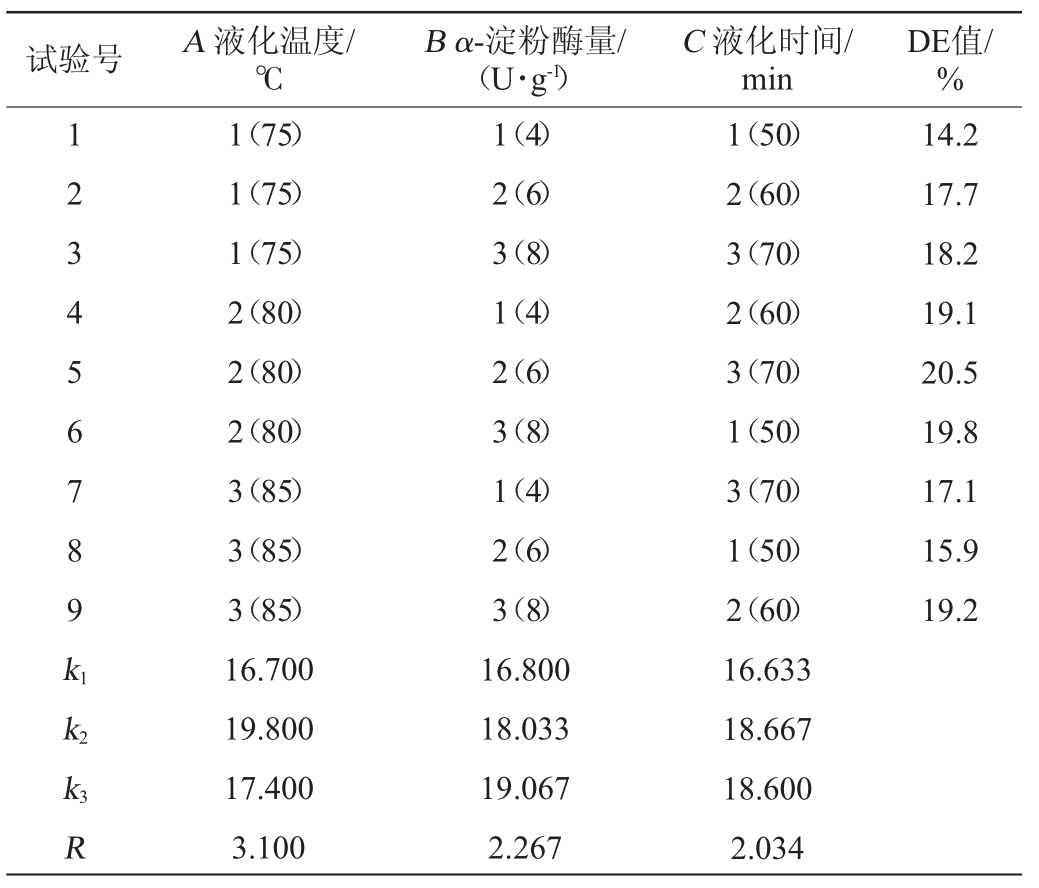
表2 玉米粉液化条件优化正交试验结果方差分析
Table 2 Variance analysis of orthogonal experiments results for liquefaction conditions optimization of corn flour

注:“*”表示对结果影响显著(P<0.05)。
由表1可知,液化工艺条件对于液化程度的影响主次顺序为A>B>C,即液化温度>α-淀粉酶量>液化时间,最优液化工艺条件组合为A2B3C2,即液化温度80 ℃、α-淀粉酶量8 U/g、液化时间60 min。在此最佳液化条件下进行3次平行验证试验,液化液DE值为20.6%。
从表2可以看出,液化条件对液化程度的影响均达到了显著水平(P<0.05)。因此在玉米粉糖液液化时,液化温度、α-淀粉酶量和液化时间这3个因素都要考虑。
2.2 玉米粉糖液最佳糖化工艺条件的确定
2.2.1 糖化时间对糖化效果的影响
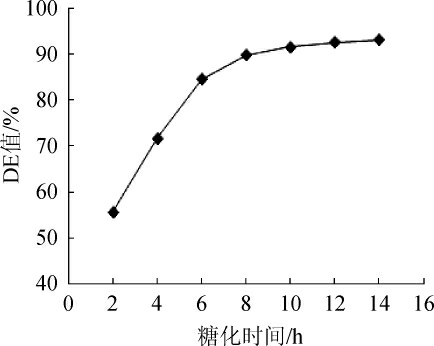
图5 糖化时间对葡萄糖当量值的影响
Fig.5 Effect of saccharification time on dextrose equivalent value
由图5可知,糖化时间8 h之前,随着时间的推移糖化醪的DE值大幅度提高;在糖化时间8~14 h时DE值提高不大,逐渐趋于平缓;糖化时间>14 h之后,DE值增加不明显,其原因是糖化酶底物专一性很低,除能从淀粉分子非还原末端切开α-1,4糖苷键之外,也能切开α-1,6糖苷键和切开α-1,3糖苷键,但前者的速度要快于后两种糖苷键;而糖化酶作用于支链淀粉时,从非还原末端顺次切下葡萄糖单位,遇到α-1,6糖苷键分支处,先将α-1,6糖苷键切开,再将α-1,4糖苷键水解,故水解支链淀粉的速度受水解α-1,6糖苷键速度的控制[26]。因此,考虑提高设备利用率和节约时间,选择最优糖化时间为10 h。
2.2.2 糖化酶添加量对糖化效果的影响

图6 糖化酶添加量对葡萄糖当量值的影响
Fig.6 Effect of glucoamylase addition on dextrose equivalent value
糖化醪底物浓度足够高时,随着加酶量的增加糖化程度也随之增加[27]。由图6可知,随着糖化酶添加量的增加,糖化醪DE值逐渐增加,当糖化酶加量为200 U/g原料,DE值达到高峰,之后随着加酶量增加,DE值增加量趋于平衡,这是因为糖化酶添加量低时,浆液中酶没达到饱和,酶促反应不充分,还原糖产量较低,当酶量达到饱和后,加酶量的增加对反应影响不大,还原糖的增加量变化不明显,因此,综合考虑成本和糖化酶解效果,选择最适加酶量为200 U/g。
2.2.3 糖化温度对糖化效果的影响
糖化温度能显著影响酶促反应,在适宜的温度范围内,酶促反应随着温度的升高加快,至最适反应温度时到达最快。若温度继续升高,会导致酶失活,使得酶促反应速度降低[28]。由图7可知,DE值在糖化温度低于60 ℃范围内逐渐升高,但糖化温度高于65 ℃后糖化酶失活严重,DE值降低。因此,选择最适糖化温度为60 ℃。
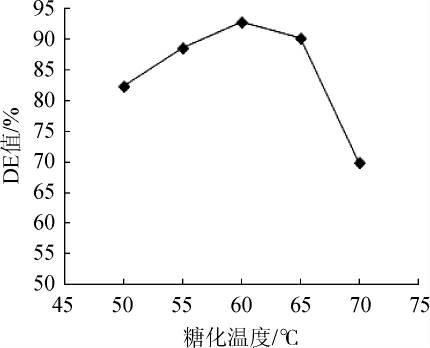
图7 糖化温度对葡萄糖当量值的影响
Fig.7 Effect of saccharification temperature on dextrose equivalent value
2.2.4 糖化条件优化正交试验
根据单因素试验所得结果,以DE值为考察指标,进行正交试验确定最优糖化工艺条件。正交试验结果与分析见表3,方差分析见表4。
表3 玉米粉糖化条件优化正交试验结果与分析
Table 3 Results and analysis of orthogonal experiments for saccharification conditions optimization of corn flour
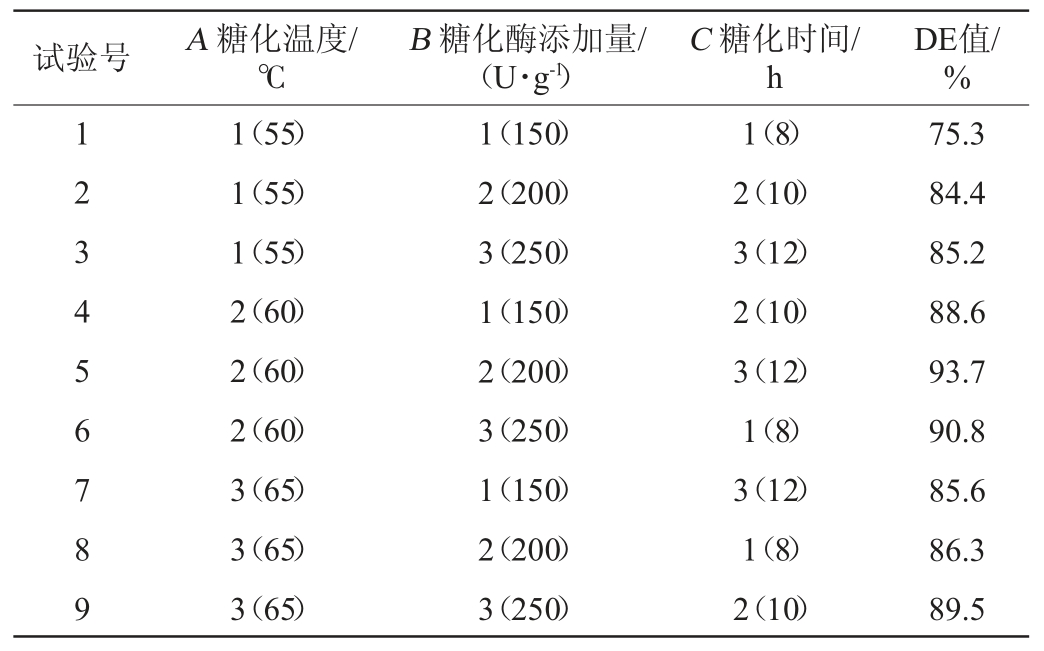
续表
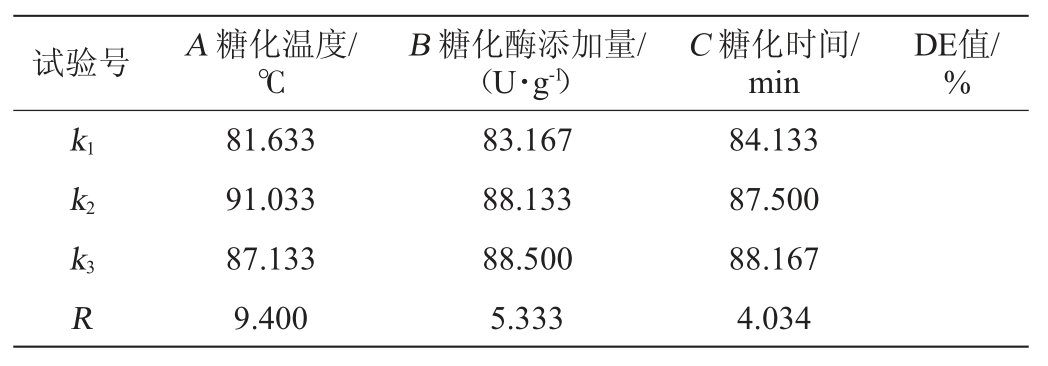
表4 玉米粉糖化条件优化正交试验结果方差分析
Table 4 Variance analysis of orthogonal experiments results for saccharification conditions optimization of corn flour
注:“*”表示对结果影响显著(P<0.05),“**”表示对结果影响极显著(P<0.01)。
由表3可知,糖化工艺条件的主次顺序为糖化温度>糖化酶添加量>糖化时间;得到最佳糖化工艺条件组合为A2B3C3,即糖化温度60 ℃,糖化酶添加量250 U/g,糖化时间12 h。在此优化工艺条件下进行3次平行验证试验,糖化液DE值为93.1%。由表4可知,糖化酶添加量和糖化时间对结果均有显著的影响(P<0.05),糖化温度对结果有极显著的影响(P<0.01)。因此,在玉米粉糖液糖化时,温度、糖化酶添加量和时间这三个因素都要考虑。
3 结论
通过单因素与正交试验确定了玉米粉糖液的最佳液化和糖化工艺条件,即最佳液化工艺条件为液化温度80 ℃、α-淀粉酶添加量为8 U/g、液化时间60 min;最佳糖化条件为糖化温度60 ℃、糖化酶添加量250 U/g、糖化时间12 h。在此最佳工艺条件下,制备的玉米粉糖液DE值达93.1%,且糖液澄清度高,提高了玉米粉糖液的质量和得率。本研究及结果可为玉米粉糖液双酶法的工业化提供理论依据。
[1]尤新.玉米深加工技术(第二版)[M].北京:中国轻工业出版社,2009:15-241.
[2]马丽娟,王海明,温玉凤,等.丝状真菌发酵产油脂培养基及发酵条件的优化研究[J].长春工业大学学报(自然科学版),2008,29(4):459-463.
[3]王瑞元.发展微生物油脂前景广阔[J].粮食与食品工业,2014,21(4):1-2.
[4]李翔,黎冬明,郭晓敏,等.微生物油脂产业化应用研究进展[J].中国油脂,2010,35(11):10-14.
[5]张燕鹏,黄凤洪,杨湄,等.发酵法生产多不饱和脂肪酸[J].中国生物工程杂志,2007,27(4):139-145.
[6]JANG H D,LIN Y Y,YANG S S.Effect of culture media and conditions on polyunsaturated fatty acids production by Mortierella alpina[J].Bioresource Technol,2005,96(15):1633-1644.
[7]EROSHIN V K,DEDYUKHINA E G,CHISTYAKOVA T I,et al.Arachidonic-acid production by species of Mortierella[J]. World J Microbiol Biotechn,1996,12(1):91-96.
[8]LI Q,DU W,LIU D.Perspectives of microbial oils for biodiesel production[J].Appl Microbiol Biotechnol,2008,80(5):749-756.
[9]杨志强,于涛,张春泓.以玉米粉为原料生产淀粉糖可节能降耗、降低成本[J].中小企业管理与科技(下旬刊),2013,6(8):323-324.
[10]王丽娟,许婷婷,何冰芳,等.双酶法制备玉米粉水解糖液的工艺优化[J].粮食与饲料工业,2008,32(6):25-27.
[11]姚妙爱.双酶直接催化玉米粉中的淀粉糖化工艺参数的研究[J].粮油加工,2009,40(8):104-106.
[12]TOMASIK P,HORTON D.Enzymatic conversion of starch[J].Adv Carbohydr Chem Biochem,2012,432-436.
[13]蒋宝航.全营养型玉米啤酒糖浆的研制[D].大连:大连工业大学,2017.
[14]杨志强,孟悦.玉米粉喷射液化工艺优化[J].食品科技,2018,43(3):159-164.
[15]叶玲玲,肖志刚,王利民,等.挤压玉米粉制备高麦芽糖浆工艺优化化[J].农业工程学报,2012,28(23):277-285.
[16]赵凯,许鹏举,谷广烨.3,5-二硝基水杨酸比色法测定还原糖含量的研究[J].食品科学,2008,29(8):534-536.
[17]姜锡瑞,段钢.新编酶制剂实用技术手册[M].北京:中国轻工业出版社,2002:145-147.
[18]刘浩,任贵兴.液化法酿造燕麦黄酒工艺条件优化[J].中国酿造,2014,33(8):67-74.
[19]刘亚伟.玉米淀粉生产及转化技术[M].北京:化学工业出版社,2003:296-297.
[20]李祥,刘玉婷,冯立庄,等.液体葡萄糖生产工艺及酶作用研究[J].中国酿造,2008,27(5):51-53.
[21]柯旭清.双酶法玉米淀粉糖化反应的影响因素研究[J].粮食与油脂,2019,32(2):63-66.
[22]LI Z,LIU W,GU Z,et al.The effect of starch concentration on the gelatinization and liquefaction of corn starch[J].Food Hydrocolloid,2015,48:189-196.
[23]张旺,林松毅,刘静波,等.玉米葡萄糖全糖粉生产关键技术中液化条件的优化研究[J].食品工业科技,2009,30(2):180-183.
[24]付丙勇.双酶法制糖生产工艺中易忽视的四个环节[J].发酵科技通讯,2010,39(4):22-24.
[25]贾新成,陈红歌.酶制剂工艺学[M].北京:化学工业出版社,2008:136-143.
[26]孙俊良.酶制剂生产技术[M].北京:科学出版社,2004:167-175.
[27]王鹤,陈晓平.糯米酒最佳糖化工艺的优选[J].农产品加工(学刊),2014,10(1):22-24.
[28]付艳丽,周霞,苏畅.荞麦黑米酒液化及糖化工艺的研究[J].食品工业,2013,34(5):100-103.