我国农作物秸秆的产量高,利用率低,焚烧和堆放在田间地头会造成巨大的资源浪费和环境污染。秸秆主要含有纤维素、半纤维素、木质素、蛋白质及灰分物质,前三种的含量占80%以上,纤维素类物质在自然状态下降解率不高,往往降低了秸秆的再利用水平[1-2]。
目前秸秆的综合利用有多种途径。秸秆能源化会产生二次污染并且总利用率低。直接还田的降解周期长,还会增加来年耕作难度;作为动物饲料,由于其纤维素、半纤维素和木质素的含量高,蛋白含量低,适口性差,使得秸秆的消化率低和营养价值低,有效提高消化率和营养价值可以改善秸秆的再利用价值[4];堆沤还田是利用微生物将大部分有机质转化为腐殖质,使秸秆中的氮磷钾等被转化为可利用的状态再应用于土壤中[5]。
微生物发酵秸秆可以降低其纤维素、木质素含量,并提高蛋白含量,提高秸秆饲料的营养价值和利用率。微生物的生长和繁殖会分泌大量酸类、酶类,酶类可以将秸秆中的木聚糖链和木质素聚合物酯链进行酶解[6-8],酸类可以软化秸秆[9]。发酵过程中有益微生物的繁殖还会抑制其他有害细菌的生长。自然环境中秸秆降解缓慢,纤维素酶活力低限制着纤维素的降解,制约着秸秆的再利用,在秸秆中加入微生物有助于加快秸秆的降解[10-11]。本研究为了提高秸秆的发酵效果,通过测定复合微生物发酵秸秆过程中的酶活,筛选出纤维素酶活和木聚糖酶活力高的复合微生物,将其应用于秸秆发酵,测定秸秆成分(粗纤维、中性洗涤纤维、酸性洗涤纤维、木质素、粗蛋白)的变化,为复合微生物应用于秸秆发酵提供科学依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
供试菌株黑曲酶(Aspergillus niger)0002、黑曲酶(Aspergillus niger)0007、黑曲酶(Aspergillus niger)0011、米曲酶(Aspergillus oryzae)0008、白腐菌(white rot fungi)0126、芽孢杆菌(Bacillus)0136和放线菌(Actinomyces)0057等:山东宝来利来生物工程股份有限公司菌种保藏中心保存;玉米秸秆、小麦秸秆:泰安市农业科学院的种植基地。
1.1.2 化学试剂
硫酸(分析纯):天津市致远化学试剂有限公司;氯化钠、硫酸亚铁、硝酸钾、磷酸氢二钾、氢氧化钠(均为分析纯):天津凯通化学试剂有限公司;酒石酸钾钠(分析纯):天津北辰方正试剂厂;木糖、葡萄糖(均为分析纯):天津大茂化学试剂厂;3,5-二硝基水杨酸(dinitrosalicylic acid,DNS):上海中秦化学试剂有限公司;无水亚硫酸钠、羧甲基纤维素钠(carboxymethy cellulose-Na,CMC-Na)(均为分析纯):天津市科密欧化学试剂有限公司;木聚糖(分析纯):国药集团化学试剂有限公司;醋酸、醋酸钠(均为分析纯):青岛捷世康生物科技有限公司;硫酸镁(分析纯):济南汇丰达化工有限公司;蛋白胨(生化试剂):北京奥博星生物技术有限责任公司;酵母膏(生化试剂):天津市英博生化试剂有限公司。
1.1.3 培养基
黑曲霉和米曲霉培养基:称量麸皮30 g,加入20 mL水,121 ℃灭菌30 min。
芽孢杆菌培养基:葡萄糖0.2%,蛋白胨1.0%,氯化钠0.5%,酵母膏0.5%,pH调至7.0,121 ℃灭菌30 min。
放线菌培养基:可溶性淀粉2%,硝酸钾0.1%,磷酸氢二钾0.05%,硫酸镁0.05%,氯化钠0.05%,硫酸亚铁0.001%,pH调至7.2~7.4,121 ℃灭菌30 min。
白腐菌培养基:马铃薯(去皮)200 g/L,葡萄糖20 g/L,121 ℃灭菌30 min。
刚果红纤维素鉴别培养基:CMC-Na 10 g,KNO31 g,K2HPO40.5 g,MgSO40.5 g,NaCl 1.5 g,刚果红0.2 g,水1 L,121 ℃灭菌30 min。
1.2 仪器与设备
DHP-9082数显恒温培养箱:上海一恒科学仪器有限公司;DHG-9140A电热鼓风干燥箱:常州诺基仪器有限公司;KDN-103F自动定氮仪、HYP308消化炉:上海纤检仪器有限公司;LD5-2A低速离心机:北京京立离心机有限公司;HH-4数显恒温水浴锅:国华电器有限公司;722E型可见分光光度计:上海光谱仪器有限公司;YXQ-LS-50S11压力蒸汽灭菌锅:上海博讯实业有限公司医疗设备厂;pHS-3C型pH计:上海精密科学仪器有限公司。
1.3 方法
1.3.1 菌株的培养及其筛选
分别用接种环取黑曲酶、米曲霉、芽孢杆菌、白腐菌、放线菌斜面于装有对应培养基的三角瓶中,芽孢杆菌于37 ℃、180 r/min摇床培养24 h。黑曲酶和米曲霉于30 ℃培养箱中静置培养72 h。白腐菌和放线菌于30 ℃、180 r/min摇床培养72 h。
将制备的菌液滴到刚果红培养基上进行培养,培养菌落至周围出现透明圈后,用0.02%刚果红溶液染色20 min,1 mol/L氯化钠溶液脱色20 min后计算透明圈直径D、菌落直径d。根据透明圈直径(D)与菌落直径(d)的比值(H=D/d)来初步判断该待测菌株降解纤维素的能力,H值越大表明该待测菌株降解纤维素的能力越强,初筛H值大的菌株。
1.3.2 复合菌株的筛选及发酵玉米秸秆
在初筛菌株的基础上,将发酵菌株组合分别设计为:①白腐菌0126+黑曲酶(0007、0011、0002)[1∶1(0.33∶0.33∶0.33)];②白腐菌0126+米曲霉0008(1∶1);③白腐菌0126+黑曲霉(0007、0011、0002)+米曲霉0008[1∶1(0.33∶0.33∶0.33)∶1];④白腐菌0126+黑曲霉(0007、0011、0002)+米曲霉0008+芽孢杆菌0136+放线菌0057[1∶1(0.33∶0.33∶0.33)∶1∶1∶1]。
将玉米秸秆剪碎至3~5 cm长度,加入培养基(秸秆∶麸皮=7∶3,(NH4)2SO41%,KH2PO40.2%,料水比1∶4(g∶mL))后在密封袋中充分混匀,于121 ℃灭菌30 min,冷却后分别按照接菌量1%接入4种组合的菌,于30 ℃条件下发酵,保持通风,根据腐化程度于第15天时结束发酵。同时设置自然发酵对照组(不接菌)。发酵不同的时间(1d、3d、6d、9d、12d、15 d)进行取样测定纤维素酶活、木聚糖酶活。木聚糖酶是半纤维素复合酶的主要成分,木聚糖酶活越高则半纤维素酶活越高,因此,可以用木聚糖酶活来反映半纤维素酶活的情况。
1.3.3 复合菌株发酵田间大堆小麦秸秆
在田间用小麦秸秆堆成圆锥形堆体,堆体高度约1.2 m,直径约2.0 m,每个堆体约50 kg干秸秆。堆体的底部、表面都用塑料布铺盖。秸秆中加入玉米面6.1%,尿素1%,料水比1∶1(g∶mL),按照1%的接菌量分别接入白腐菌、黑曲霉、米曲霉、芽孢杆菌和放线菌(1∶1∶1∶1∶1)。每天记录堆体的温度,分别在发酵第5、10、15、20天时翻堆补水(以手握时指缝有水但不下滴为宜)。观察堆体的形貌变化,定期取样测定pH、中性洗涤纤维、酸性洗涤纤维、木质素、粗纤维和粗蛋白,发酵38 d时外观腐化程度良好,即可结束发酵。
1.3.4 粗酶液的制备
取发酵秸秆样品3 g,加30 mL蒸馏水,在室温下浸提4 h后用4层纱布过滤,于转速为3 500 r/min条件下离心10 min,上清液即为粗酶液,置于4 ℃冰箱备用。
1.3.5 分析检测
(1)纤维素酶活测定
纤维素酶酶活采用羧甲基纤维素糖化力法[12]。纤维素酶酶活定义:在40 ℃、pH 4.6的条件下,1 min水解羧甲基纤维素产生1.0 μg葡萄糖的酶量定义为1个酶活单位(U/g)。
(2)木聚糖酶活测定
木聚糖酶酶活测定参考国标GB/T 23874—2009《饲料添加剂木聚糖酶活力的测定分光光度法》。木聚糖酶酶活定义:在37 ℃、pH 5.5的条件下,每分钟从质量浓度为5 mg/mL的木聚糖溶液中降解释放1 mol还原糖所需要的酶量为1个酶活力单位(U/g)。
(3)组分及pH值测定
粗纤维含量:参照国标GB/T 6434—2006《饲料中粗纤维的含量测定过滤法》;中性洗涤纤维含量:参照国标GB/T 20806—2006《饲料中中性洗涤纤维(NDF)的测定》;酸性洗涤纤维含量:参照农业行业标准NY/T 1459—2007《饲料中酸性洗涤纤维的测定》;木质素含量:参照国标GB/T 20805—2006《饲料中酸性洗涤木质素(ADL)的测定》;粗蛋白含量:参照国标GB/T 6432—1994《饲料中粗蛋白测定方法》;pH的测定:采用玻璃电极pHS-3C型pH计。
1.3.6 统计分析
使用Excel 2007软件对原始数据进行处理,采用SPSS 17.0统计软件(One-Way ANOVA)进行显著性分析,并采用最小显著差异(least significant difference,LSD)法进行多重比较,结果用平均值±标准误差表示,以P<0.05作为差异显著性判断标准。
2 结果与分析
2.1 纤维素分解能力菌株的筛选
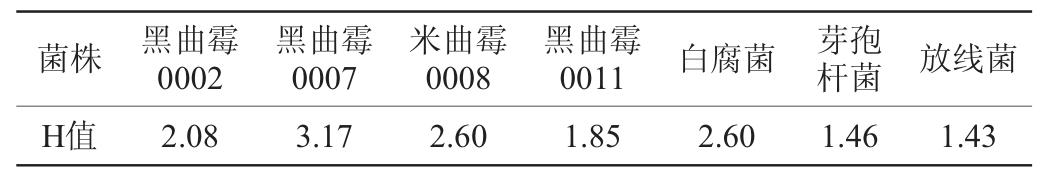
通过刚果红纤维素鉴别培养基培养后,只有纤维素分解菌周围才会形成透明圈。本实验对本公司菌种库中的7株菌进行筛选,结果见表1。由表1可知,7株菌均能观察到透明圈,可以产降解纤维素酶,能够用于降解秸秆的试验。
表1 不同菌株的透明圈直径D与菌落直径d的比值H
Table 1 Ratio value H of transparent ring diameter D to colony diameter d of different strains
2.2 不同组合复合株菌发酵玉米秸秆的纤维素酶活和木聚糖酶活
纤维素酶可以将纤维素分解成寡糖或单糖。木聚糖是植物中半纤维素的重要组成部分,在植物细胞壁中的含量仅次于纤维素。木聚糖酶能够降解木聚糖生成木寡糖、木糖等低聚木糖混合物及葡萄糖等[13],这两种酶活力越高,越有利于降解秸秆中的纤维素和半纤维素。木聚糖酶和纤维素酶可以通过物理或化学作用直接或间接使秸秆的纤维结构得到膨胀甚至破坏[14]。
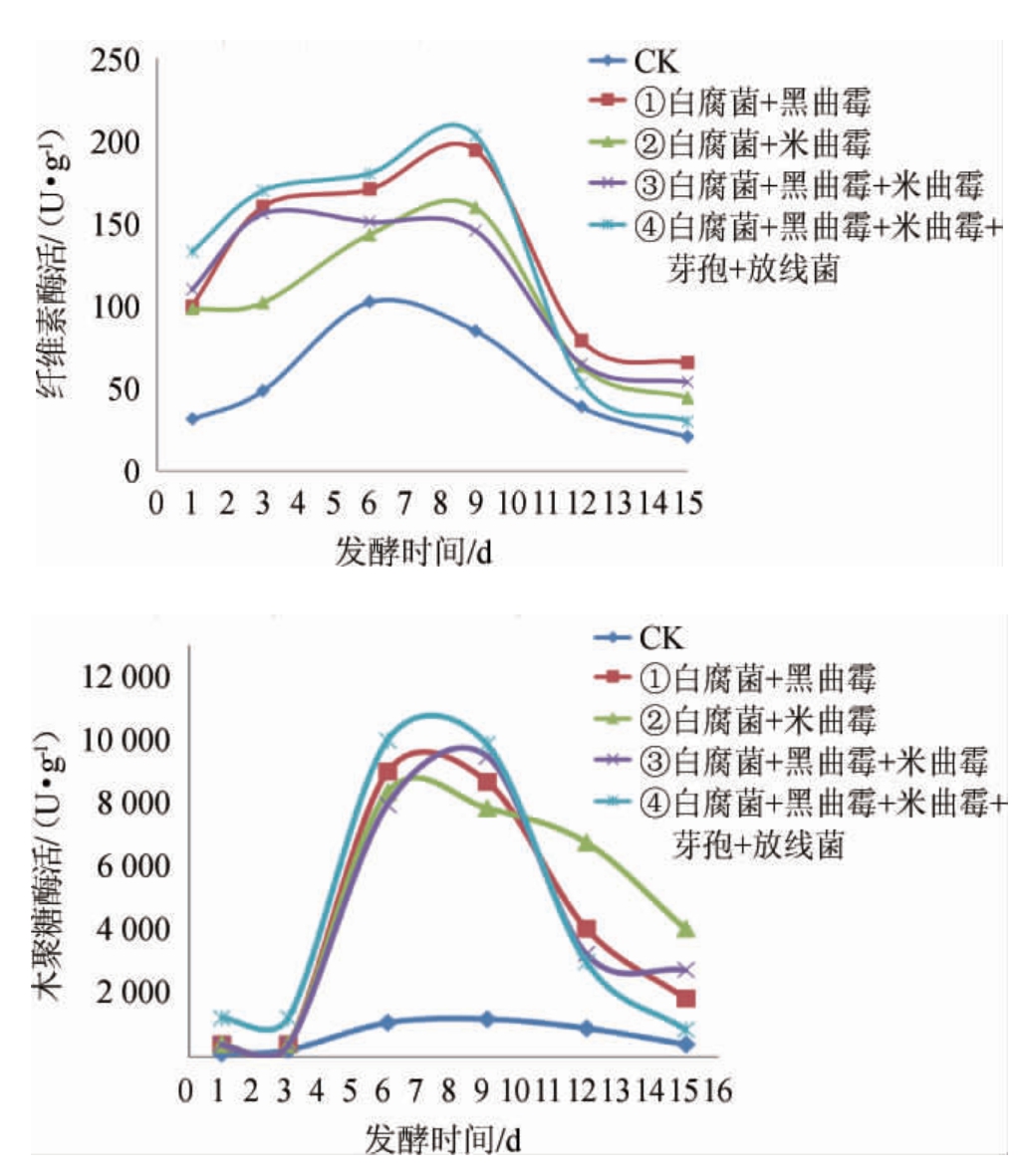
图1 不同菌株组合发酵玉米秸秆的纤维素酶活(A)及木聚糖酶活(B)
Fig.1 Cellulase (A) and xylanase (B) activities of corn straw fermented by different combinations of strains
由图1A可知,添加复合菌株的试验组在发酵秸秆1~9 d时,各组纤维素酶酶活随时间增加呈持续升高趋势,第9天后开始下降。①组的纤维素酶酶活在发酵第9天时最高,为194.73 U/g。②组的纤维素酶酶活在发酵第9天时最高,为159.80 U/g。③组的纤维素酶酶活在发酵第3天时最高,为155.92 U/g。④组的纤维素酶酶活在发酵第9天时最高,为203.64 U/g。自然发酵对照组纤维素酶酶活在第6天时,酶活最高,为102.47 U/g。试验组的纤维素酶活均显著高于对照组(P<0.05)。结果表明,④组(白腐菌+黑曲霉+米曲霉+芽孢+放线菌)的纤维素酶活最佳(203.64 U/g)。
由图1B可知,试验组不同的复合菌株在发酵1~9 d时,各组木聚糖酶酶活随时间增加呈先升高后下降趋势。①组的木聚糖酶酶活在发酵第6天时最高,为9 021.33 U/g。②组的木聚糖酶酶活在发酵第6天时最高,为8 376.55 U/g。③组的木聚糖酶酶活在发酵第9天时最高,为9 503.88 U/g。④组的木聚糖酶酶活在发酵第6、9天时最高,为100 17.41 U/g。对照组在第9天时木聚糖酶活最高,为1 189.43 U/g。试验组的木聚糖酶活均显著高于对照组(P<0.05)。结果表明,④组(白腐菌+黑曲霉+米曲霉+芽孢+放线菌)的木聚糖酶活最佳(100 17.41 U/g)。
综上所述,白腐菌+黑曲霉+米曲霉+芽孢+放线菌菌株组合可以应用于秸秆发酵。
2.3 田间大堆发酵小麦秸秆的情况
温度为堆肥过程中微生物生命活动的重要参数,也是判断发酵产品能否达到无害化条件的重要指标之一,发酵初期微生物的繁殖等大量活动释放热量,使温度上升。高温发酵过程能杀死其中的病菌、虫卵和杂草种子,部分嗜温菌受到抑制甚至死亡,需要及时降温[15],各温度阶段的微生物群和酶系存在着差异。白腐菌+黑曲霉+米曲霉+芽孢+放线菌菌株组合应用于小麦秸秆田间大堆发酵,发酵过程中温度的变化见图2,pH值变化见表2,组分变化见表3,外观变化见图3。
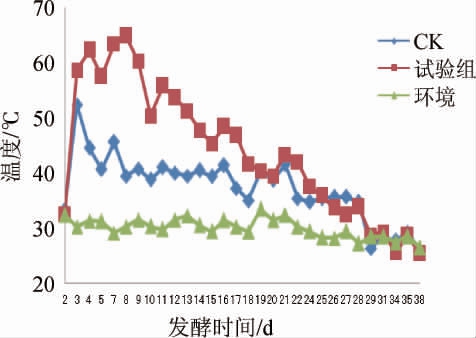
图2 小麦秸秆发酵过程中温度的变化
Fig.2 Changes of temperature during wheat straw fermentation
由图2可知,本次发酵过程中温度有高温期、中温期和低温期。试验组从第3天开始迅速升温,第4天升至60 ℃以上,第5天温度有所下降。整个发酵过程中,温度超过60 ℃以上的时间有4 d,超过50~60 ℃的时间有6 d,40~50 ℃的时间有8 d。基本上第24天开始,温度都低于40 ℃。对照组从第3天开始迅速升温,第3天升至50 ℃以上,第4天温度有所下降。整个发酵过程中,温度超过50 ℃以上的时间有1 d,40~50 ℃的时间有10 d。第21天开始,温度都低于40 ℃。在第5、10、15、20天时进行翻堆补水,试验组和对照组每翻堆一次温度有小幅度升高。
本研究中采用翻堆来改善通风状况,每次翻堆后温度都有小幅度升高,有助于提高秸秆的发酵腐熟。李春燕等[16]研究发现,翻堆可延长好氧发酵高温期。在高温期进行翻堆2~3次,能够更有效促进可挥发性固体的降解,提高秸秆腐殖化程度。
表2 小麦秸秆发酵过程中pH值的变化
Table 2 Changes of pH during wheat straw fermentation
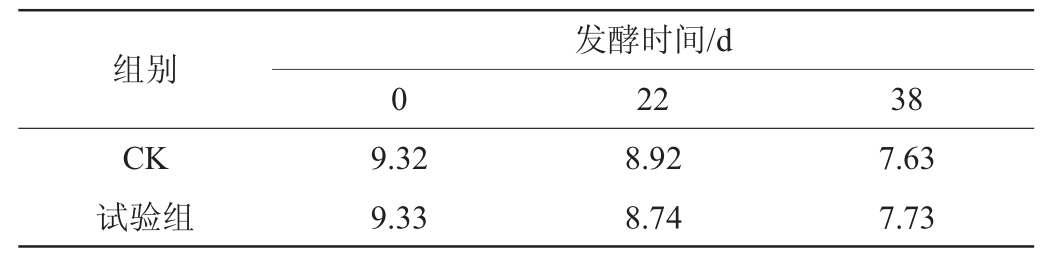
由表2可知,小麦秸秆堆肥初始pH值为9.33,发酵22 d后pH略微降低,仍为碱性,至发酵38 d时pH为微碱性。可能是由于发酵过程中微生物的繁殖和代谢产物产生了少量酸性物质,使pH有所下降。发酵结束秸秆pH为微碱性,符合腐熟堆肥的pH为7.5~8.5[17-18]。王琼瑶等[19]研究了不同腐熟剂对水稻秸秆的腐熟效果,发现强微堆肥快速腐熟剂处理后,在42 d时腐熟液pH值达7.5,与本研究结果一致。
表3 小麦秸秆发酵过程中组分变化
Table 3 Changes of compositions during wheat straw fermentation
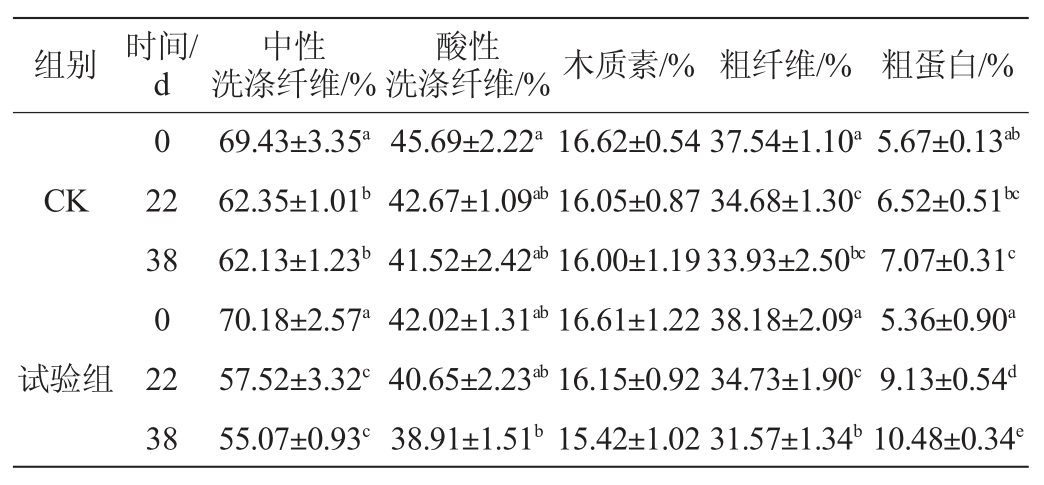
注:所有指标测定结果均以干物质计。同列数据肩不同字母表示显著差异(P<0.05);相同字母表示差异不显著(P>0.05)。下同。
由表3可知,对照组和试验组的小麦秸秆的中性洗涤纤维、酸性洗涤纤维、木质素、粗纤维随着发酵时间的增加而逐渐降低,粗蛋白逐渐升高。
对照组发酵38 d的小麦秸秆,中性洗涤纤维、粗纤维比发酵前秸秆显著降低(P<0.05),粗蛋白显著升高(P<0.05)。
试验组发酵38 d的小麦秸秆,中性洗涤纤维比发酵前显著降低21.53%(P<0.05),粗纤维显著降低17.31%(P<0.05),粗蛋白显著升高95.52%(P<0.05)。试验组发酵38 d的秸秆中酸性洗涤纤维和木质素与未发酵时无显著性差异(P>0.05),酸性洗涤纤维降低7.4%,木质素降低7.16%。
试验组发酵38 d的小麦秸秆的中性洗涤纤维、酸性洗涤纤维、木质素、粗纤维分别比对照组发酵38 d的小麦秸秆降低了11.36%、6.29%、3.63%、6.95%,粗蛋白显著升高了48.23%(P<0.05)。
目前发现能够降解小麦秸秆的微生物主要有细菌、真菌和放线菌,它们能够降解纤维素、半纤维素和木质素,还会影响蛋白质的含量[20-21]。乔君毅等[22]利用黑曲霉3.3148菌株发酵玉米秸秆,粗蛋白含量提高了11.26%,粗纤维、中性洗涤纤维、酸性洗涤纤维含量分别下降了24.45%、45.24%、37.04%;黑曲霉产生的羧甲基纤维素酶活力为29.94 IU/g。
由图3可知,添加复合微生物的发酵秸秆比自然发酵对照组外观腐化程度高。可能微生物发酵改变了秸秆内部的分子结构和表观形态。赵方圆等[23]筛选了纤维素高效降解菌曲霉YN1,并进行了降解滤纸、秸秆和稻壳的微观形态上的观察,对照组的稻壳表面光滑有排列整齐的突起,接菌发酵后稻壳表面呈现瓦解溃烂状。秸秆原来是光滑的表面,发酵后菌丝定殖于秸秆的纤维表面,破坏了秸秆原有的光滑表面。

图3 小麦秸秆发酵38 d的外观
Fig.3 Appearance of wheat straw fermentation for 38 d
3 结论
本研究筛选出复合菌株:白腐菌+黑曲霉+米曲霉+芽孢杆菌+放线菌(1∶1∶1∶1∶1),该复合菌株产纤维素酶活和木聚糖酶活较高,分别可达203.64 U/g、10 017.41 U/g。添加该复合菌株发酵秸秆,显著降低了中性洗涤纤维、粗纤维水平(P<0.05),显著提高了粗蛋白水平(P<0.05),该复合菌株可以用于秸秆发酵该复合菌有助于提高秸秆发酵效果,为秸秆的再利用提供了一种处理方法,具有广泛的应用前景。
[1]鲁宇橦.玉米秸秆专用复合微生物发酵剂的研制[D].长春:吉林农业大学,2019.
[2]LYND L R,WEIMER P J,ZYL W H V,et al.Microbial cellulose utilization:Fundamentals and biotechnology[J].Microbiol Mol Biol Rev,2002,66(3):506-577.
[3]董祥洲,陈亚奎,任立伟,等.微生物转化在秸秆还田中的应用进展[J].生物加工过程,2020,18(5):604-611.
[4]EASTRIDGE M L,STARKEY R A,GOTT P N,et al.Dairy cows fed equivalent concentrations of forage neutral detergent fiber from corn silage,alfalfa hay,wheat straw,and corn stover had similar milk yield and total tract digestibility[J].Anim Feed Sci Technol,2017,225:81-86.
[5]LIU C H,LIU Y,FAN C,et al.The effects of composted pineapple residue return on soil properties and the growth and yield of pineapple[J].J Soil Sci Plant Nutr,2013,13(2):433-444.
[6]谢永生.玉米秸秆发酵原理及其特点[J].畜牧兽医科技信息,2012(3):117.
[7]DING C,LI M,HU Y.High-activity production of xylanase by Pichia stipitis:Purification,characterization,kinetic evaluation and xylooligosaccharides production[J].Int J Biol Macromol,2018,117(1):72-77.
[8]毛婷,朱瑞清,牛永艳,等.纤维素降解芽孢菌的筛选及产酶条件优化[J].中国酿造,2020,39(1):71-76.
[9]袁建国.常见微生物发酵饲料的利用[J].营养与日粮,2011,268(6):32-33.
[10]刘晓飞,宋洁,马京求,等.产纤维素酶放线菌的筛选鉴定及其对玉米秸秆的降解[J].精细化工,2020,37(8):1657-1664,1671.
[11]许富强,王曙阳,董妙音,等.可高效降解甜高粱秸秆产糖的纤维素酶研究[J].中国酿造,2018,37(5):126-129.
[12]李兰晓,杜金华,李军训,等.CMC糖化力法测定纤维素酶活性条件的研究[J].饲料工业,2006,27(24):49-52.
[13]OTTENHEIM C,VERDEJO C,ZIMMERMANN W,et al.Hemicellulase production by Aspergillus niger DSM 26641 in hydrothermal palm oil empty fruit bunch hydrolysate and transcriptome analysis[J].J Biosci Bioeng,2014,118(6):696-701.
[14]李红亚,李文,李术娜,等.解淀粉芽孢杆菌复合菌剂对玉米秸秆的降解作用及表征[J].草业学报,2017,26(6):153-167.
[15]张从军,胥清君,刘庆,等.小麦秸秆静态堆肥技术总结[J].磷肥与复肥,2015,30(11):34-35.
[16]李春燕,张曦,沈玉君,等.翻堆策略对猪粪沼渣好氧发酵特性的影响[J/OL].环境工程:1-14[2020-10-26].http://kns.cnki.net/kcms/detail/11.2097.X.20200615.1822.052.html.
[17]于子旋,杨静静,王语嫣,等.畜禽粪便堆肥的理化腐熟指标及其红外光谱[J].应用生态学报,2016,27(6):2015-2023.
[18]朱凤香,王卫平,杨友坤,等.固体废弃物堆肥的腐熟度评价指标[J].浙农业科学,2010(1):159-163.
[19]王琼瑶,赵源,朱艳婷,等.水稻秸秆的腐熟剂筛选研究[J].安徽农业科学,2018,46(14):68-70.
[20]史彬,黄魏魏,付丹妮,等.秸秆降解放线菌GC的筛选及其应用基础研究[J].微生物学杂志,2018,38(2):43-49.
[21]江北,吕梦霞,蒋冬花.曲霉属真菌活性代谢产物及在农业生产中的应用研究进展[J].微生物学杂志,2019,39(2):103-110.
[22]乔君毅,亢晋,张福元,等.黑曲霉发酵玉米秸秆产纤维素酶的研究[J].饲料研究,2008(12):63-66.
[23]王砚,李念念,朱端卫,等.水稻秸秆预处理对猪粪高温堆肥过程中磷素形态变化的影响[J].植物营养与肥料学报,2019,25(6):963-971.