水果具有生产上市时间较为集中,货架期短、不耐贮存的特点,极易出现旺季滞销的问题[1]。果醋属于水果精深加工产品[2],选择适宜品种进行果醋加工是解决水果滞销的一个有效途径。果醋既具有传统醋的酸味物质,又具有水果的果香味和营养成分,被誉为第四代饮料[3]。传统的果醋发酵主要分为两个阶段,第一个阶段是利用酿酒酵母(Saccharomyces cerevisiae)将水果汁中的糖分发酵成酒精,第二个阶段是利用醋酸菌将酒精转化成醋酸。采用这种发酵方式生产的果醋存在酸味单一、口感刺激的问题。添加乳酸菌发酵是改善果醋风味的一个途径,果醋中不挥发酸的主要成分是乳酸,乳酸与其他成分一起能赋予果醋圆润和棉柔的风味[4]。醋醅中有丰富的乳酸菌菌种资源,高产酸乳酸菌在食醋酿造过程中具有一定的应用价值。许女等[5]从山西老陈醋发酵过程中分离筛选得到1株高产酸、高产乙偶姻的植物乳杆菌(Lactobacillus plantarum)和1株发酵挥发性成分含量丰富的戊糖片球菌(Pediococcus pentosaceus),并将其应用于山西老陈醋发酵,大幅度提升了山西老陈醋总酸、不挥发性酸和总酯的含量;余永建[6]从镇江香醋醋醅中分离得到一株瑞士乳杆菌(Lactobacillus helveticus),并将其应用于食醋强化发酵,能有效缩短醋酸发酵周期、提高乳酸相对含量、改善食醋口感。然而目前关于从果醋醋醅分离高产酸乳酸菌的研究鲜见报道。
本研究采用MRS培养基从桃果醋醋醅中分离具有强产酸能力的乳酸菌,通过形态观察、生理生化试验及分子生物学技术对其进行鉴定,并研究其乙醇耐受能力、产酸能力和抗生素敏感性,从而筛选出具有改善果醋风味品质的乳酸菌菌株。
1 材料与方法
1.1 材料与试剂
桃果醋醋醅:大竹鹏程果业农民专业合作社;MRS肉汤培养基、MRS固体培养基:北京奥博星生物技术有限公司;乙醇(分析纯)、浓硫酸(分析纯)、琼脂粉(生化试剂):成都市科龙化工试剂厂;DL-苹果酸、D-酒石酸、琥珀酸、富马酸、草酸、柠檬酸、乙酸、L-乳酸、奎宁酸标准品:美国Sigma公司;抗生素纸片:杭州微生物试剂有限公司;土壤基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)快速抽提试剂盒、2×Taq聚合酶链式反应(polymerase chain reaction,PCR)Master Mix、引物27F(5'-AGAGTTTGATCMTGGCTCAG-3')、引物1492R(5'-GGYTACCTTGTTACGACTT-3'):生工生物工程(上海)股份有限公司;BHI乳酸菌生化鉴定条:青岛高科技工业园海博生物技术有限公司。
1.2 仪器与设备
HPX-87H液相分析柱:美国伯乐公司;AC2-6S1二级生物安全柜:新加坡Esco公司;CP153分析天平:奥豪斯仪器(上海)有限公司;YXQ-LS-50SII立式压力蒸汽灭菌器:上海博迅实业有限公司;1260高效液相色谱(high performance liquid chromatography,HPLC)仪:美国安捷伦科技公司;FlexCycle PCR仪:德国耶拿分析仪器有限公司;SUP-250生化培养箱:上海精宏实验设备有限公司;HBM-400拍击式均质器:天津恒奥科技发展有限公司;5810R台式冷冻离心机:德国Eppendorf公司;Synergy HTX多功能微孔板检测仪:美国伯腾仪器有限公司。
1.3 方法
1.3.1 乳酸菌菌株的分离纯化
称取10 g桃果醋醋醅到100 mL无菌生理盐水中,用拍击式均质器拍打混匀,取1 mL均质液到9 mL无菌生理盐水进行梯度稀释,取10-6、10-7、10-8倍稀释液100 μL到含1%CaCO3的MRS固体平板,涂布,37 ℃培养48 h,挑取具有最大溶钙圈的菌落接种到含1%CaCO3的MRS固体平板反复划线纯化获得纯菌株。
1.3.2 分离菌株的鉴定
形态观察:将分离菌株接种到MRS固体平板上,37 ℃培养48 h,观察菌落形态和显微形态。
生理生化试验:将分离菌株划线接种到MRS固体平板上,37 ℃培养24 h长出单菌落,随机挑取2个平板上的单菌落分别用生理盐水制成菌悬液,根据说明书接种到BHI乳酸菌生化鉴定条,37 ℃培养24 h,记录实验结果。
分子生物学鉴定:将分离菌株D2接种到MRS肉汤培养基,37 ℃培养24 h,取1 mL菌液12 000×g离心5 min后,弃上清,取菌体沉淀用作DNA提取,具体操作按照土壤基因组DNA快速抽提试剂盒说明书进行。以提取的基因组DNA为模板对分离菌株的16S rDNA基因序列进行PCR扩增。PCR扩增体系:DNA 1 μL,PCR引物27F(10 μmol/L)和1492R(10 μmol/L)各1 μL,2×Taq PCR Master Mix 25 μL、双蒸水(ddH2O)22 μL;PCR扩增程序参照王志山等[7]的方法进行。PCR扩增产物送到上海生工生物工程股份有限公司进行纯化和测序。测序结果提交至美国国立生物技术信息中心(national center for biotechnology information,NCBI)的GenBank数据库中进行比对搜索[8],选取与分离菌株同源性较高的10株模式菌株的16S rDNA基因序列,利用MEGA 6.06软件中的邻接(neighbor-joining,NJ)法构建系统发育树[9]。
1.3.3 分离菌株对乙醇的耐受性
将分离菌株接种到30 mL MRS肉汤培养基中,37 ℃静置培养24 h。分别取以上培养液600 μL接种到30 mL含0、2%、4%、6%、8%、10%、12%、14%(V/V)乙醇的MRS肉汤培养基中,接种3个平行,37 ℃静置培养24 h,取200 μL培养液到96孔板,用Synergy HTX多功能微孔板检测仪测定OD600nm值。
1.3.4 分离菌株的产酸能力
取300 μL分离菌株培养液接种到30 mL MRS液体培养基,接种3个平行,37 ℃静置培养24 h、48 h、72 h,将培养液12 000×g离心10 min,取上清液测定总酸和有机酸组成。总酸含量(以乳酸计)测定:参照文献[10]采用滴定法测定。有机酸含量测定:以MRS肉汤培养基为空白,参照文献[11]采用高效液相色谱法测定。
1.3.5 分离菌株对抗生素的敏感性
将100 μL分离菌株培养液涂布到MRS固体平板,将抗生素纸片放在MRS固体平板上,37 ℃培养24 h,每种抗生素纸片做3个平行,观察抑菌圈情况[12-13]。
2 结果与分析
2.1 乳酸菌菌株的分离纯化
通过MRS固体培养基从桃果醋醋醅中分离纯化得到一株溶钙圈最大的菌株,编号为D2,保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为CGMCC No:1.16283
2.2 菌株D2的鉴定
2.2.1 形态观察结果
菌株D2在MRS固体培养基上培养48 h的菌落及细胞形态见图1。由图1可知,菌株D2的菌落突起、表面光滑、边缘整齐、乳白色、不透明,菌落大小为1~2 mm,与胡博等[14]鉴定的鼠李糖乳杆(Lactobacillus rhamnosus)菌菌落形态一致。用革兰氏染色液染色后,在油镜下观察细胞形态,其为短杆状、单个或线性排列,这与COLLINS M D等[15]报道的鼠李糖乳杆菌标准菌株的细胞形态一致。
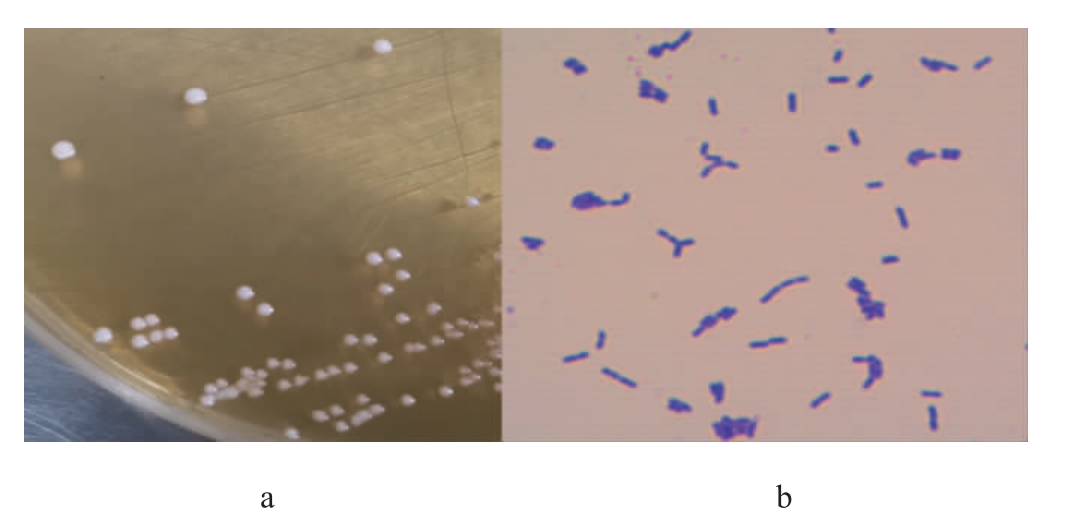
图1 菌株D2的菌落(a)及细胞(b)形态
Fig.1 Colonial (a) and cell (b) morphology of strain D2
2.2.2 生理生化试验结果
挑取1个单菌落到2 mL无菌生理盐水制成菌悬液,采用海博生物HBI乳酸菌生化鉴定条进行生理生化鉴定,发酵七叶苷、纤维二糖、麦芽糖、甘露醇、水杨苷、山梨醇、蔗糖、菊糖和乳糖均为阳性,发酵棉籽糖为阴性,与鼠李糖乳杆菌标准菌株(JCM1136)[16-17]糖发酵能力一致。
2.2.3 分子生物学鉴定结果
菌株D2的16S rDNA基因序列碱基长度为1 491 bp,其序列与鼠李糖乳杆菌(Lactobacillus rhamnosus)JCM 1136相似性最高,相似性为98.21%,其次与干酪乳杆菌(Lactobacillus casei)ATCC 393相似性为97.31%。选取与菌株D2 16S rDNA基因序列相似性最高的10株模式菌株的16S rDNA基因序列构建系统发育树,结果见图2。由图2可知,菌株D2与鼠李糖乳杆菌(Lactobacillus rhamnosus)JCM 1136聚于一支,亲缘关系最近,因此,结合形态观察、生理生化试验结果,鉴定菌株D2为鼠李糖乳杆菌(Lactobacillus rhamnosus)。鼠李糖乳杆菌已被列为《可用于食品的菌种名单》,是公知的无毒、无副作用的益生菌,可用于食品发酵。

图2 基于16S rDNA基因序列菌株D2的系统发育树
Fig.2 Phylogenetic tree of strain D2 based on 16S rDNA gene sequences
2.3 菌株D2对乙醇的耐受性试验结果
菌株D2在含不同体积分数乙醇的MRS肉汤培养基中的生长情况见图3。
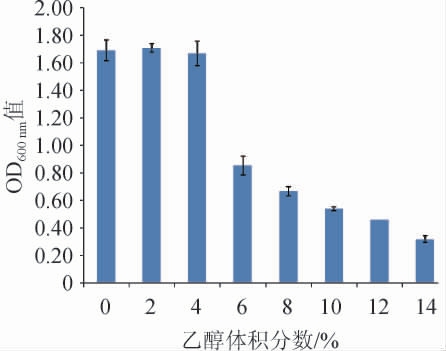
图3 菌株D2的乙醇耐受性试验结果
Fig.3 Results of ethanol tolerance tests of strain D2
由图3可知,菌株D2在所有接种的培养基中都有生长,且在含体积分数0~4%乙醇的MRS肉汤培养基中生长能力基本一致,OD600nm值明显比体积分数6%~14%乙醇的高,说明0~4%乙醇体积分数对菌株D2生长没有表现出抑制现象。当乙醇体积分数为6%~14%,随着乙醇体积分数的增加,菌株D2的OD600nm值逐渐减少,说明乙醇体积分数越高,对菌株D2的生长抑制性越强。金丹等[18]研究了12株乳酸菌的乙醇耐受能力,仅有3株菌在乙醇体积分数14%下还能存活,存活率≤2%,其中有一株存活率为2%的菌株为鼠李糖乳杆菌;刘威良等[19]研究了10株不同乳酸菌菌种的乙醇耐受能力,其中嗜酸乳杆菌(Lactobacillus acidophilus)、鼠李糖乳杆菌、副干酪乳杆菌(Lactobacillus paracasei)相比其他7株乳酸菌具有更强的乙醇耐受能力;本研究中菌株D2在乙醇含量14%下还具有一定的生长能力,且菌株D2也为鼠李糖乳杆菌,推测鼠李糖乳杆菌类可能带有乙醇耐受基因。
2.4 菌株D2产酸能力分析结果
菌株D2发酵液中的总酸含量见图4。
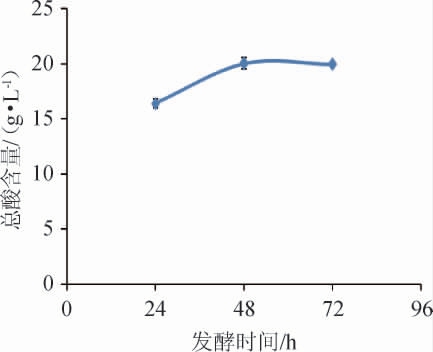
图4 菌株D2发酵液中的总酸含量
Fig.4 Total acid content in fermentation broth of strain D2
由图4可知,菌株D2发酵24 h时,发酵液中总酸含量为16.4 g/L,发酵48 h时总酸含量为20.03 g/L,发酵72 h时总酸含量为19.97 g/L,表明发酵48 h时,发酵液中总酸含量基本趋于稳定。采用高效液相色谱仪检测发酵48 h的发酵液中草酸、柠檬酸、酒石酸、苹果酸、奎宁酸、琥珀酸、乳酸、乙酸、富马酸等有机酸含量,具体结果见表1。由表1可知,发酵液中乳酸含量最高,为(17.45±0.06)g/L,其次是乙酸(4.06±0.04)g/L和柠檬酸(1.35±0.07)g/L,乳酸含量增加最多,其次是苹果酸和琥珀酸。柠檬酸含量低于MRS肉汤培养基,酒石酸、奎宁酸和富马酸未检出。可能是由于乳酸菌在厌氧条件下将丙酮酸代谢成乙酸和H+,H+将延胡索酸还原成琥珀酸,导致发酵液中乙酸和琥珀酸含量增加[20]。草酸、琥珀酸和苹果酸是三羧酸循环途径的中间代谢物,其在发酵过程中不会积累太多[21]。菌株D2发酵液中总酸含量为20.03 g/L,陈卓等[22]从四川麸醋醋醅中分离到的鼠李糖乳杆菌总酸含量仅为1.97 g/L。
表1 菌株D2 48 h发酵液中有机酸检测结果
Table 1 Determination results of organic acids in fermentation broth of strain D2 at 48 h g/L

注:“-”表示未检出。
2.5 菌株D2对抗生素的敏感性试验结果
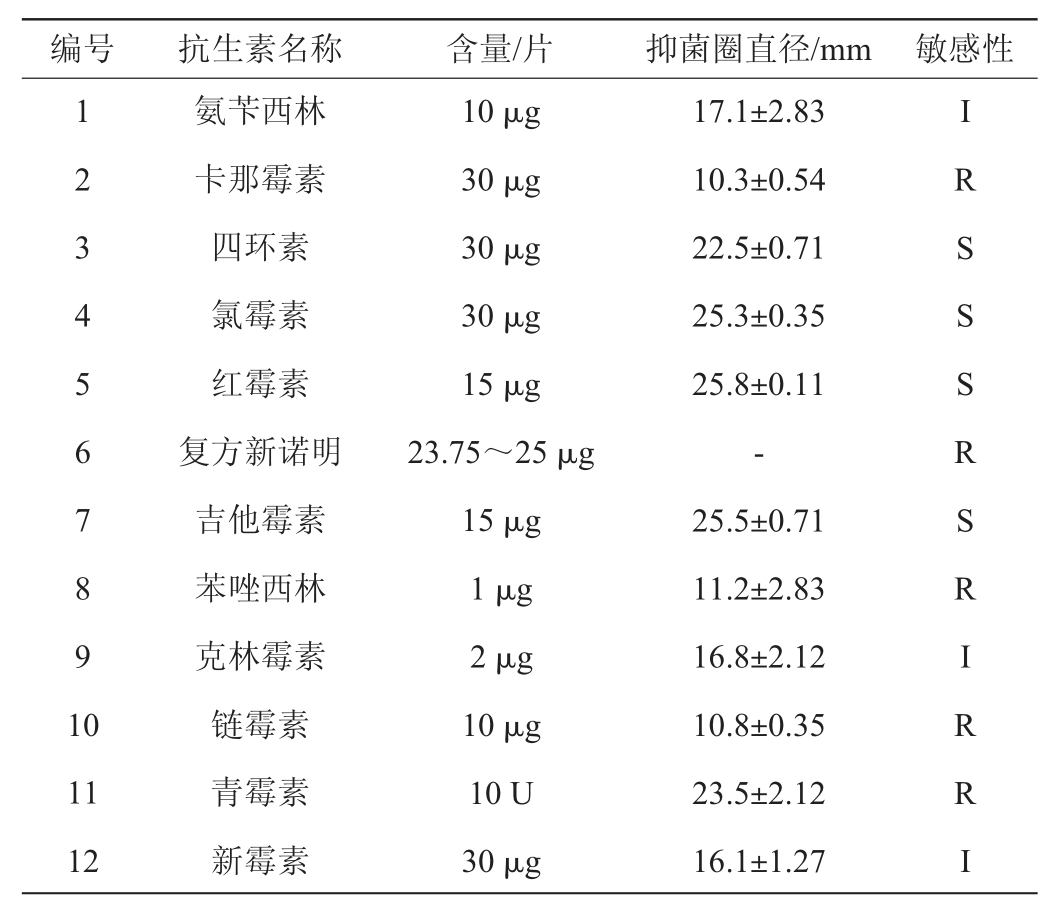
菌株D2对抗生素的敏感试验结果见表2和图5。由表2及图5可知,菌株D2对四环素、酰胺醇类(氯霉素)、大环内酯类(红霉素、吉他霉素)敏感,对氨基糖苷类(链霉素、卡那霉素)、青霉素类(青霉素、苯唑西林)和黄胺类(复方新诺明)具有抗性。菌株D2对氨基糖苷类敏感这一试验结果与NAWAZ M等[23]的研究结果一致,乳酸菌类对链霉素和卡那霉素具有抗性。菌株D2对四环素具有抗性,而SHARMA P等[24]研究了9株鼠李糖乳杆菌的抗生素敏感性,其中仅有一株对四环素具有抗性,说明菌株对四环素类抗生素的敏感性存在个体差异。
表2 菌株D2抗生素敏感试验结果
Table 2 Results of antibiotic susceptibility tests of strain D2
注:“R”表示具有耐药性;“I”表示具有中介;“S”表示具有敏感性。
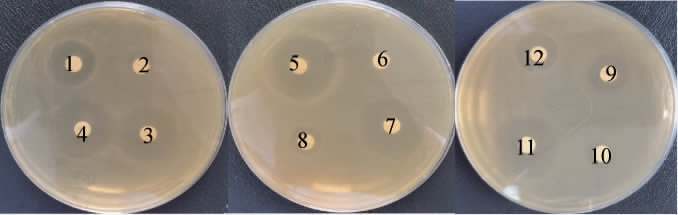
图5 菌株D2抗生素敏感效果
Fig.5 Effect of antibiotic susceptibility of strain D2
1~12为表2中抗生素相应的编号。
3 结论
通过MRS固体培养基从桃果醋醋醅中分离到1株具有强产酸能力的乳酸菌,编号为D2,经形态观察、生理生化试验及分子生物学技术鉴定为鼠李糖乳杆菌(Lactobacillus rhamnosus)。该菌株在体积分数4%乙醇下能够正常生长,在体积分数14%乙醇下能够存活,具有较强乙醇耐受力;在MRS肉汤培养基中发酵48 h时,总酸含量达到20.03 g/L,其中乳酸含量增加最多,其次是苹果酸和琥珀酸;对四环素、酰胺醇类(氯霉素)、大环内酯类(红霉素、吉他霉素)敏感,对氨基糖苷类(链霉素、卡那霉素)、青霉素类(青霉素、苯唑西林)和黄胺类(复方新诺明)具有耐药性。该菌株具有较强的乙醇耐受能力和产乳酸能力,安全性高,有一定的开发利用价值。
[1]柯炳生.我国水果产业有哪些重要变化趋势?[J].中国果业信息,2020,37(5):2.
[2]向进乐,罗磊,郭香凤,等.果醋功能性研究进展[J].食品科学,2013,34(13):356-360.
[3]王彦安.果醋研究现状[J].中国调味品,2015,40(9):109-112.
[4]畅功民,张春杰,张敏,等.高乳酸食醋酿造技术研究进展[J].中国酿造,2016,35(9):1-4.
[5]许女,王如福,贾瑞娟,等.建立在菌种互作基础上的优良土著复合乳酸菌直投式发酵剂及其强化山西老陈醋生产的方法:CN 109749963 A[P].2019-05-14.
[6]余永建.镇江香醋有机酸组成及乳酸合成的生物强化[D].无锡:江南大学,2014.
[7]王志山,李苗,陈文浩,等.一株芝麻香型白酒高温大曲细菌Q2B1 的鉴定及其产酶活性研究[J].中国酿造,2020,39(2):51-55.
[8]YOON S H,HA S M,KWON S,et al.Introducing EzBioCloud:A taxonomically united database of 16S rRNA and whole genome assemblies[J].Int J Syst Evolut Microbiol,2017,67(5):1613-1617.
[9]TAMURA K,STECHER G,PETERSON D,et al.MEGA6:molecular evolutionary genetics analysis version 6.0[J].Mol Biol Evolut,2013,30(12):2725-2729.
[10]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 12456—2008 食品中总酸的测定[S].北京:中国标准出版社,2008.
[11]于江,刘永轩,于贞.有机酸对酱油品质的影响[J].中国调味品,2019,44(9):90-93.
[12]郭凤茹,刘元雪,施文正,等.罗非鱼肠道乳酸菌对抗生素的药敏性[J].中国食品学报,2020,20(6):287-294.
[13]Clinical and Laboratory Standards Institute.M100-S25 Performance standards for antimicrobial susceptibility testing:twenty-eighth informational supplement[S].CLSI,2018.
[14]胡博,教戈,梁金钟.鼠李糖乳杆菌L7-13 株生物学特性[J].农业工程,2014,4(5):66-69.
[15]COLLINS M D,PHILLIPS B A,ZANONI P.Deoxyribonucleic acid homologystudies of Lactobacillus casei,Lactobacillus paracasei sp.nov.,subsp.paracasei and subsp.tolerans,and Lactobacillus rhamnosus sp.nov.,comb.nov[J].Int J Syst Bacteriol,1989,39:105-108.
[16]凌代文,东秀珠.乳酸细菌分类鉴定及实验方法[M].北京:中国轻工业出版社,1999:10-11.
[17]孙丽慧,王云晓,吕诗文,等.1 株高产L-乳酸菌株的分离鉴定及其发酵培养基优化[J].食品科学,2018,39(6):135-140.
[18]金丹,蒋彩虹,蒋艾廷,等.塔城地区酸马奶中耐乙醇乳酸菌的筛选与鉴定[J].中国酿造,2017,36(3):44-48.
[19]刘威良,毛瑞霞,王雪峰,等.乙醇降解菌种的筛选及其发酵乳产品解酒功效评价[J].食品科学,2020,41(2):107-113.
[20]李华,王华,袁春龙,等.葡萄酒化学[M].北京:中国青年出版社,2005:90-104.
[21]方冠宇,穆晓静,蒋予箭.浙江玫瑰醋发酵过程中细菌菌群结构变化与有机酸形成相关性分析[J].食品科学,2019,40(22):177-184.
[22]陈卓,毛祥,于华,等.四川麸醋醋醅中乳酸菌的分离鉴定及产酸特性研究[J].中国调味品,2018,43(4):103-106,113.
[23]NAWAZ M,WANG J,ZHOU A,et al.Characterization and transfer of antibiotic resistance in lactic acid bacteria from fermented food products[J].Curr Microbiol,2011,62:1081-1089.
[24]SHARMA P,ANAND S,TOMAR S K,et al.Antibiotic susceptibility of Lactobacillus sp.isolated from commercial probiotic products by e-test strip method[J].Int J Curr Microbiol Appl Sci,2018,7(4):3499-3517.