中国传统的浓香型白酒酿造以窖池中的窖泥为基础,窖池中丰富的微生物菌群在发酵过程中进行着复杂的能量与物质代谢,从而促进了窖泥的老熟以及白酒品质的提高[1-2]。近年来研究发现,真菌菌群在白酒酿造过程中起到至关重要的作用,是产酒精、产香的主要功能菌,也具有很高的糖化酶及酯化酶活力[3-4]。因此,对窖泥中真菌群落结构组成的分析有助于了解浓香型白酒酿酒微生物菌群代谢特征,为白酒风味形成及品质保证提供必要的依据。
传统的平板培养或聚合酶链式反应-变性梯度凝胶电泳(polymerase chain reaction-denaturing gel gradient electrophoresis,PCR-DGGE)等技术存在分析数据量小,覆盖率低等弊端,而高通量测序(high-throughput sequencing,HTS)技术具有通量高、覆盖广泛、耗时短等特点,能够更加准确、全面地揭示或预测微生物的群落结构及功能,是微生物群落深入解析的强有力手段[5]。目前,对窖泥真菌菌群结构研究的方法主要集中在可培养菌的分离筛选以及磷酸脂肪酸(phosphor lipid fatty acid,PLFA)生物标记和PCR-DGGE技术[6-8],高通量测序技术更多的被应用于分析白酒窖泥原核微生物[9-11],而真菌群落结构解析研究较少。于春涛等[12]研究发现河北某知名酒厂窖泥变质前后真菌的种类和丰度均有显著差异;孟雅静等[13]分析了安徽某知名浓香型白酒企业新老窖泥的真核菌群结构,发现属水平上新老窖池窖底泥中假丝酵母(Candida)占绝对优势,新老池窖壁泥的真菌组成更接近且更丰富,Ca2+含量对窖底泥的真核菌群组成具有重要作用;LIU M K等[14]研究了不同窖龄窖泥内部转录间隔区(internal transcribed spacer,ITS)基因序列多样性,结果显示5年窖龄窖泥样品中根霉菌(Rhizopus)、茎点菌(Phoma)和毛孢子菌(Trichosporon)相对较多,100年窖龄窖泥样品中曲霉(Aspergillus)和假丝酵母的比例最高;王福桢[15]研究发现内蒙古河套酒业集团浓香型白酒窖泥真菌的群落组成较为简单,而沈毅等[16]研究发现郎酒公司酱香型白酒窖泥中真核微生物丰富度和多样性远高于高温大曲和酒醅。
微生物群落分布特征与其环境因素息息相关,生产实践表明,窖泥越老,窖泥富集的有利微生物越多,参与形成的呈香物质也越多,相同窖龄窖池的窖壁泥和窖底泥所处环境因子差异较大,这些因素势必都会对真核微生物群落分布产生不同程度的影响[17],因此针对不同窖龄窖壁泥和窖底泥中真菌群落特征及其分布情况的研究十分必要。宋河酒业是河南省浓香型白酒的代表,对其窖泥中真菌微生物的调查研究非常薄弱,本研究以宋河浓香型白酒不同窖龄窖壁泥和窖底泥为研究对象,采用高通量测序技术对其真菌群落结构进行全面分析,以期更加深入的认知酿酒微生物的作用机理,揭示“老窖产好酒”的秘密,为更好的稳定白酒品质提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
窖泥样品:取自河南宋河酒业股份有限公司浓香型白酒生产厂,所选窖池窖龄分别为6年和16年。窖壁泥采用四点取样法,4面池壁分别取距窖口约50 cm处的泥样约50 g,充分混匀作为1个窖壁泥样本,分别编号为W1(6年窖壁泥)和Y1(16年窖壁泥);窖底泥采用五点取样法,窖池底部中心点及四个角点分别取泥样约50 g,充分混匀作为1个窖底泥样本,分别编号为W2(6年窖底泥)和Y2(16年窖底泥)。所有样品放入无菌采样袋中低温运回实验室。
1.1.2 主要试剂
E.Z.N.ATM Mag-Bind 土壤脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:美国OMEGA公司;2×Taq聚合酶链式反应(polymerase chain reaction,PCR)Master Mix:南京诺唯赞生物科技有限公司;琼脂糖(生化试剂):西格玛奥德里奇(上海)贸易有限公司;Agencourt AMPure XP核酸纯化试剂盒:美国Beckman公司;Qubit3.0 DNA检测试剂盒:美国Life公司。
1.2 仪器与设备
Illumina Miseq PE250高通量测序仪:美国Illumina公司;T100 Thermal Cycler PCR仪:美国BIO-RAD公司;Invitrogen Qubit3.0荧光计:美国Life公司;凝胶成像系统:美国UVP公司。
1.3 方法
1.3.1 DNA提取及PCR扩增
窖泥总DNA的具体提取步骤参照E.Z.N.ATM Mag-Bind土壤DNA提取试剂盒的使用说明书,采用1%琼脂糖凝胶电泳对所提样本DNA进行完整性检测。以DNA为模板,采用Illumina Miseq测序平台的通用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2R(5'-GCTGCGTTCTTCATCGATGC-3')对窖泥样品中真菌的内部转录间隔区(internal transcribed spacer,ITS)序列进行PCR扩增。PCR扩增体系及扩增条件参照文献[18]。
1.3.2 Illumina MiSeq高通量测序及数据分析
PCR扩增产物经电泳检测、纯化回收后,利用Qubit3.0 DNA检测试剂盒对回收的DNA精确定量。定量后的DNA样品各取10 ng,1∶1等量混合后,依托生工生物工程(上海)股份有限公司进行Illumina MiSeq高通量测序。测序结果首先按照标签序列(barcode)识别区分各样本序列,并对其进行质量控制,得到各样本的有效数据,调用Usearch软件去除非特异性扩增序列和嵌合体。按照97%序列相似性标准划分操作分类单元(operational taxonomic unit,OTU),使用R软件的VennDiagram制作OTU分布韦恩图。使用QIIME软件,对样本的多样性指数、丰富度指数以及覆盖率(Coverage)进行计算。
2 结果与分析
2.1 高通量测序结果及Alpha多样性分析
利用Illumina Miseq测序平台得到窖泥样品W1、W2、Y1、Y2的原始序列数分别为67 962条、69 530条、139 774条和45 165条。剔除嵌合体和靶区域外序列后最终得到的有效序列数分别为67787条、69 350条、139573条和45063条,其平均碱基长度分别为240.95 bp、238.50 bp、267.62 bp和257.42 bp。在97%序列相似性水平下划分OTU,4个窖泥样品共得到2 238个OTUs,对其进行Alpha多样性分析,结果见表1。
表1 窖泥样品真菌的序列数、OTU数及Alpha多样性指数
Table 1 Sequence number,OTU number and Alpha diversity index of fungi in pit mud samples
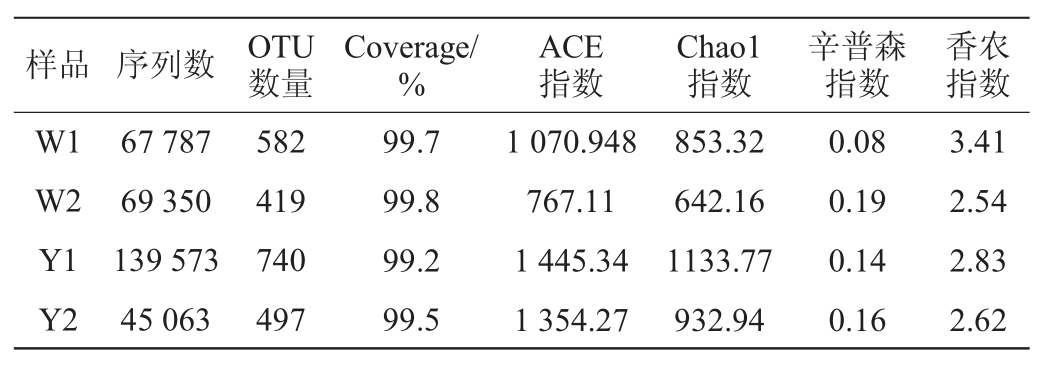
由表1可知,4个窖泥样品的覆盖率均>99.0%,表明试验的取样合理,测序结果能真实反映样本的实际情况。Alpha多样性指数中香农(Shannon)和辛普森(Simpson)指数是物种多样性和均匀度的综合指标,Chao1和ACE指数是物种丰富度指数,对稀有物种更为敏感。本研究中6年窖龄窖池窖壁泥样品W1的香农指数(3.41)最高,辛普森指数(0.08)最低,说明其真菌群落的多样性最高,16年窖龄窖池窖壁泥样品Y1的ACE指数(1 445.34)及Chao1指数(1 133.77)最高,说明其真菌群落物种的丰富度最大。进一步在OTU水平上对窖泥中真菌菌群的构成进行解析,基于OTU水平的Venn图见图1。
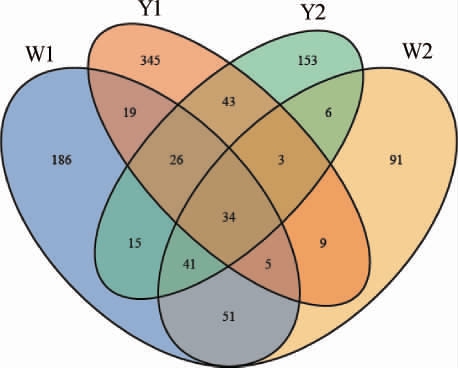
图1 基于OTU水平的Venn图
Fig.1 Venn diagram based on OTU level
由图1可知,4个样品的核心OTU为34个,独有OTU分别为186(W1)、91(W2)、345(Y1)和153(Y2),结果表明随着窖龄的增加,窖泥中稀有真菌物种均有所提高,这与丰富度指数计算结果相一致。以上数据分析还发现无论多样性还是丰富度,窖泥样品W1高于W2,Y1高于Y2,由此可见,相同窖龄的窖壁泥真菌多样性及丰富度均高于窖底泥,这与孟雅静等[13]的研究结果相一致。这可能是由于窖底泥常年处于黄水的浸泡中,更偏向为厌氧环境,从而不利于好氧型真菌的生存,而窖壁泥中氧气的含量相对更多,这为真菌群落呈现更加丰富的多样性提供了可能。
2.2 基于门水平窖泥真菌群落结构分析
对OTU注释,共得到5个门,其中优势菌门(相对丰度≥1%)共4个,其余门和未注释到门的OUT归为others,结果见图2。由图2可知,子囊菌门(Ascomycota)在4个窖泥样品中占据绝对优势,且在6年窖龄窖池窖壁泥、窖底泥中相对丰度(69.1%、68.7%)均小于16年(86.2%、81.1%),同样的随着窖龄的增加,毛霉菌门(Mucoromycota)在窖壁泥、窖底泥中相对丰度分别从1.9%和0.3%增加至4.4%和5.8%。被孢霉门(Mortierellomycota)有着不同的变化趋势,6年窖龄窖池窖壁泥、窖底泥的相对丰度高达6.7%和13.8%,16年窖龄窖池窖泥中却消失未检出,担子菌门(Basidiomycota)仅在16年窖龄窖池窖壁泥中占据优势(2.5%),其他样品均未检出。相较于孟雅静等[13-14]的相关研究结果,宋河酒业窖泥中绝对优势菌门相同,毛霉菌门和被孢霉门是特有菌门,担子菌门的丰度显著偏少。
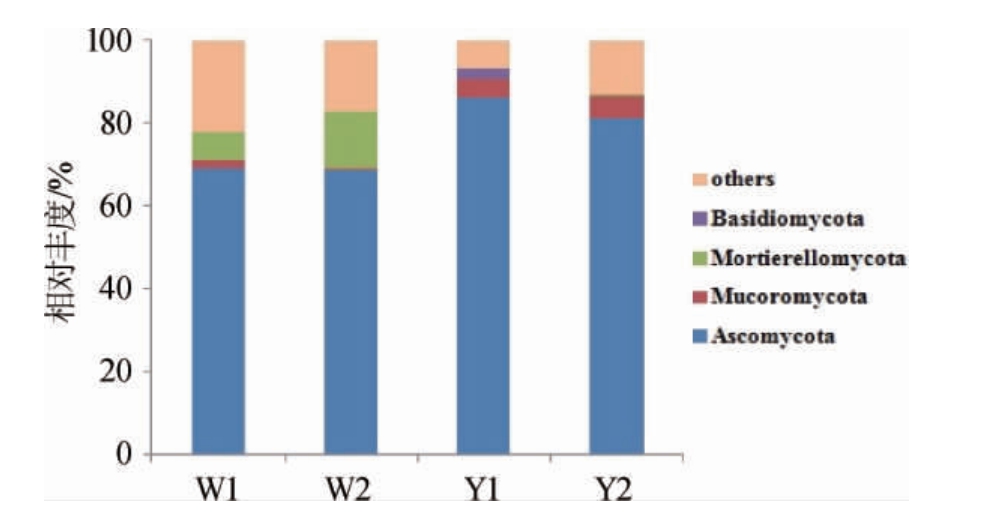
图2 基于门水平窖泥真菌群落结构分析
Fig.2 Analysis of fungi community structure in pit mud based on phylum level
2.3 基于属水平窖泥真菌群落结构分析
对OTU注释,共得到124个属,其中优势菌属(相对丰度≥1%)共15个,其余非优势菌属和未注释到属的OTU归为others,结果见图3。由图3可知,窖泥中的真核微生物主要由酵母菌和霉菌组成。6年窖龄窖池窖壁泥、窖底泥中青霉属(Penicillium)、毡盘菌属(Byssonectria)、被孢霉属(Mortierella)和伽穆孢属(Gamsia)作为优势菌属,其相对丰度分别为26.1%和40.3%、8.7%和16.3%、6.7%和13.8%、5.0%和1.5%。随着窖龄的延长,16年窖龄窖池窖泥中青霉属相对丰度显著下降,低至5.1%和4.5%,毡盘菌属、被孢霉属和伽穆孢属在16年窖龄窖池窖壁泥中消失未被检出,在16年窖龄窖池窖底泥中有检出但相对丰度均<1%成为非优势菌。相反的,嗜热真菌属(Thermomyces)、曲霉菌属(Aspergillus)和根毛霉属(Rhizomucor)在6年窖龄窖池窖壁泥、窖底泥的相对丰度较低,分别为1.7%和0.4%、3.8%和5.4%、0.9%和0.2%,16年窖龄窖池窖龄窖泥中相对丰度显著增加至20.2%和21.7%、10.9%和14.3%以及2.6%和4.6%,成为16年窖龄窖池窖龄窖泥的优势真菌属。除此之外,高通量测序结果显示嗜热子囊菌属(Thermoascus)、绿僵菌属(Metarhizium)和根霉属(Rhizopus)仅为16年窖壁泥的优势属,而在其他3个样品中相对丰度极低。孟雅静等[13]研究发现,窖池的真菌群落结构主要由窖壁泥和窖底泥所处的理化环境差异所决定,窖壁泥与窖底泥真菌组成差异较大,而新老窖泥差异并不显著。LIU M K等[14]的研究有着不同的结论,实验结果揭示低龄和百年窖泥优势真核菌群结构存在显著差异。本研究结果表明,相同窖龄窖池窖壁泥和窖底泥的真菌群落结构分布较为接近,不同窖龄窖池窖泥在优势真菌类别上存在较大差异,窖池内不同位置的环境差异可能会导致“稀有种”的出现,但是绝对优势菌的类别没有显著区别。由此可见,窖龄及窖泥位置的理化环境均可不同程度的影响真菌群落结构分布,本研究中窖龄是影响的主导因素。
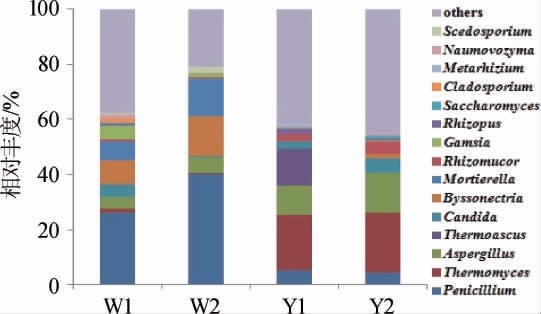
图3 基于属水平窖泥中真菌群落结构分析
Fig.3 Analysis of fungi community structure in pit mud based on genus level
真菌是窖泥微生物的重要组成部分,已报道的不同窖泥样本中的真菌多样性有高有低,本研究窖泥呈现出丰富的真核微生物多样性,与该样本的细菌群落中少数几个优势菌属相对含量>80%的现象存在显著差异[19]。6年窖龄窖池窖泥的优势真菌主要为青霉属、毡盘菌属和被孢霉属等,16年窖龄窖池窖泥为未分类酵母菌、嗜热真菌属和曲霉菌属,这些优势真菌属同样存在于已报道的其他白酒真核微生物组成中[12,15],是白酒酿造过程中复杂的物质能量代谢的重要参与者。酵母菌对于酒精发酵以及相关酶系的产生起着重要作用[20],曲霉、根霉等具有较强的产酶能力,能够分泌葡萄糖氧化酶、糖化酶和蛋白酶,促进酵母菌的生长繁殖,进而产生更多的酒精,这对白酒品质、风味的提升有着积极的影响[21],而有些菌类(如青霉菌等)通过消耗酒精底物产生相应代谢产物,导致酒糟pH值增加,从而影响酒类口味[22-23]。于春涛等[12]对浓香型白酒窖泥变质前后真菌群落差异分析发现,变质后的窖泥中青霉属成为主要调节者(相对丰度为76.56%)。本研究中出酒品质相对较差的6年窖龄窖池窖泥中青霉属相对丰度占据绝对优势,而出酒品质较好的16年窖龄窖池窖泥中青霉属相对丰度显著降低,青霉属相对丰度的变化可能成为窖泥质量变化的指示性真核微生物,这有待于认识窖泥微生物全貌再作综合分析。
3 结论
本研究运用Illumina MiSeq高通量测序技术分析了河南宋河浓香型白酒新(6年)老(16年)窖池窖壁泥和窖底泥的真菌群落结构特征。结果表明,老窖池窖壁泥和窖底泥中真菌菌群物种丰富度均高于新窖池,老窖池窖底泥真菌菌群多样性高于新窖池,但窖壁泥多样性低于新窖池;窖壁泥中真菌菌群物种多样性和丰富度均高于窖底泥。在门水平上,新老窖池窖泥的绝对优势菌门均为子囊菌门,相对含量为68.7%~86.2%。在属水平上,相同窖龄窖池窖壁泥和窖底泥的真菌群落结构分布较为接近,不同窖龄窖泥真菌微生物在优势物种组成上发生了改变,新窖池窖泥的优势真菌群(相对丰度≥1%)主要有青霉属、毡盘菌属和被孢霉属等,老窖池窖泥的优势真菌群为嗜热真菌属、曲霉菌属和根毛霉属等。相较于其他3个样本,嗜热子囊菌属、绿僵菌属和根霉属仅为老窖池窖壁泥的优势属。窖龄及窖泥位置的理化环境均可不同程度的影响真菌群落结构分布,本研究中窖龄可能是影响的主导因素。
[1]蔡雪梅,蒋英丽,吴联海,等.不同区域酱香型白酒人工窖底泥细菌多样性及其影响因子[J].食品科学,2017,38(10):87-91.
[2]高占争,吴正云,张文学.浓香型白酒窖泥微生物群落研究进展[J].中国酿造,2020,39(6):1-7.
[3]刘雯雯,孙剑秋,平文祥,等.中国白酒窖池真菌的研究进展[J].中国酿造,2012,31(6):1-5.
[4]刘茂柯,唐玉明,赵珂,等.浓香型白酒窖泥微生物群落结构及其选育应用研究进展[J].微生物学通报,2017,44(5):1222-1229.
[5]MARGULIES M,EGHOLM M,ALTMAN W E,et al.Genome sequencing in microfabricated high-densitypicolitre reactors[J].Nature,2005,437:376-380.
[6]李永博,邓波,刘燕梅,等.基于PLFA 分析不同窖龄窖泥微生物群落结构[J].中国酿造,2017,36(9):74-77.
[7]ZHENG J,LIANG R,ZHANG L Q,et al.Characterization of microbial communities in strong aromatic liquor fermentation pit muds of different agesassessedbycombinedDGGEandPLFAanalyses[J].Food Res Int,2013,54(1):660-666.
[8]DING X F,WU C D,HUANG J,et al.Interphase microbial community characteristics in the fermentation cellar of Chinese Luzhou-flavor liquor determined by PLFA and DGGE profiles[J].Food Res Int,2015,72:16-24.
[9]叶光斌,罗惠波,杨晓东,等.基于免培养法研究泸州地区浓香型白酒窖泥原核微生物群落结构[J].食品科学,2013,34(17):176-181.
[10]唐贤华.高通量测序技术初步解析浓香型白酒窖泥细菌群落结构[J].中国酿造,2020,39(1):160-164.
[11]杨小丽,尚雪娇,余海忠,等.基于Miseq 高通量测序技术的古襄阳酒窖泥细菌多样性评价[J].中国酿造,2018,37(7):26-30.
[12]于春涛,刘超,陈瑞玲,等.浓香型白酒窖泥变质前后真菌群落差异分析[J].酿酒科技,2016(10):40-44.
[13]孟雅静,张会敏,王艳丽,等.浓香型白酒新老窖池池壁泥与池底泥理化性质与真核菌群结构分析[J].现代食品科技,2020,36(5):1-8.
[14]LIU M K,TANG Y M,ZHAO K,et al.Determination of the fungal community of pit mud in fermentation cellars for Chinese strong-flavor liquor,using DGGE and Illumina MiSeq sequencing[J].Food Res Int,2017,91:80-87.
[15]王福桢.北方浓香型白酒发酵微生物多样性分布模式解析[D].呼和浩特:内蒙古大学,2014.
[16]沈毅,程伟,邓小波,等.酱香高温大曲、酒醅和窖泥的真菌多样性分析[J].酿酒科技,2019(3):17-23.
[17]张会敏,王艳丽,孟雅静,等.浓香型白酒发酵新老窖泥理化因子和原核微生物群落结构差异分析[J].食品科学,2020,41(6):207-214.
[18]李斌,胡俊杰,张兰兰,等.基于高通量测序浓香型和芝麻香型白酒酒曲真菌群落结构的分析[J].中国酿造,2019,38(10):96-100.
[19]王春艳,宋建阳,吕慧鑫,等.基于高通量测序的宋河浓香型白酒不同窖龄窖泥细菌群落结构分析[J].中国酿造,2019,38(9):163-166.
[20]WU Q,ZHU W,WANG W,et al.Effect of yeast species on the terpenoids profile of Chinese light-style liquor[J].Food Chem,2015,168(2):390-395.
[21]戴奕杰,李宗军,田志强.酱香型白酒大曲和糟醅的真菌多样性分析[J].现代食品科技,2018,34(7):97-104.
[22]李兵,张超,王玉霞,等.白酒大曲功能微生物与酶系研究进展[J].中国酿造,2019,38(6):7-12.
[23]刘绪,张磊,王超凯,等.窖泥中优势丝状真菌的分布规律及分类鉴定[J].食品与发酵工业,2012,48(1):16-19.