泡桐(Paulownia fortunei)属于双子叶植物纲中的玄参目玄参科,其资源丰富,分布广泛,种类繁多,常见的有毛泡桐、兰考泡桐、白花泡桐等种类,在黄河流域被用作传统医药数百年[1]。近年来研究发现,泡桐花主要含有总黄酮类、多糖、萜类、生物碱、有机酸、氨基酸等活性成分[2-3],具有清热解毒、疏风散热、燥湿止痢、清肝明目之功能[4-5],多用于治疗慢性支气管炎、肺炎等疾病[6]。目前,对泡桐的研究主要集中在栽培技术和幼苗培育技术上,而对有效部位泡桐花的研究主要集中在提取分离黄酮类、多糖、多酚,熊果酸等有效成分,研究其最佳提取工艺及药理作用,为工业化生产及开发应用于临床提供一定的参考依据。
研究发现,黄酮类物质具有抗炎[7]、抗肿瘤[8]、抗氧化[9]、抗病毒[10]、降血糖[11]等药理作用,在食品和制药行业应用广泛。泡桐花黄酮的常用提取方法有溶剂回流提取法、微波提取和超声波提取法,张青青等[12-13]采用乙醇加热回流法提取工艺泡桐花总黄酮,该种提取方法提取温度稳定,利于总黄酮类物质溶出,但是溶剂消耗量大、耗时耗能、提取率低。孟志芬等[14-15]分别采用微波法和超声法提取泡桐花总黄酮,这两种提取方法相较于回流提取法具有操作简单、提取效率高且提取时间短的优点。本试验拟采用超声辅助纤维素酶法提取泡桐花总黄酮,在单因素试验的基础上,结合响应面法对泡桐花总黄酮提取工艺参数进行优化,并对其体外抗氧化能力进行研究,以期为开发天然抗氧化剂应用于功能性食品、化妆品及制药行业提供依据。
1 材料与方法
1.1 材料与试剂
泡桐花:购自河南兰考的中草药市场,经鉴定属于玄参科泡桐属植物。
1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)、纤维素酶(酶活力20 U/mg):南京奥多福尼生物科技有限公司;芦丁(纯度>98%)、抗坏血酸、2,2'-联氮双(3-乙基苯并噻唑啉-6-磺酸)二铵盐(diammonium 2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonate),ABTS)(均为分析纯):上海如吉生物科技发展有限公司;过硫酸钾、亚硝酸钠、硝酸铝、氢氧化钠、乙醇等试剂均为国产分析纯。
1.2 仪器与设备
HX-200A多功能粉碎机:中国永康市五金医疗器械厂;UV1800紫外检测器:日本岛津有限公司;HH-2数显恒温水浴锅:国华电器有限公司;BSA电子天平:赛多利斯科学仪器(北京)有限公司;PS-60型超声波清洗器:苏州市创惠电子有限公司;PHS-25精密酸度计:上海精密仪器有限公司。
1.3 方法
1.3.1 样品处理方法
泡桐花样品干燥至恒质量,用多功能粉碎机粉碎成300目,收集,保存备用。
1.3.2 泡桐花总黄酮提取工艺
依照超声波辅助酶法提取泡桐花总黄酮[16]:
称取泡桐花粉末→添加pH4.5醋酸-醋酸钠缓冲液→按照1.0 mg/g加入纤维素酶→45 ℃酶解30 min→灭酶(80 ℃,10 min)→加入体积分数为60%乙醇溶液→超声处理→离心(4 000 r/min,10 min)→上清液过滤浓缩
1.3.3 泡桐花总黄酮含量的测定
参照文献[17],采用硝酸铝法绘制标准曲线,取芦丁对照品5.0 mg,置于25 mL容量瓶中,用蒸馏水定容至刻度,配成0.20 mg/mL的对照品溶液。精密量取对照品溶液1.0 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL,依次加入0.3 mL 5%NaNO2,摇匀,静置6 min,再各加0.3 mL 10%Al(NO3)3,摇匀,静置6 min,各加3.0 mL 1.0 mol/L NaOH溶液,用蒸馏水定容至10 mL,放置15 min,以空白试剂作为参比,于510 nm波长处测定吸光度值。芦丁标准曲线回归方程为:y=9.315x-0.035 3,相关系数R2=0.999 8。
取适量样品,配制成一定质量浓度的溶液,按上述方法测定总黄酮含量,重复3次,按照式(1)计算总黄酮得率。
式中:Y为泡桐花总黄酮提取得率,%;C为提取液中总黄酮的质量浓度,mg/mL;V为提取液定容体积,mL;D为稀释倍数;m为泡桐花样品称取质量,g。
1.3.4 泡桐花总黄酮提取条件优化单因素试验
分别考察纤维素酶的用量(0.5 mg/g、1.0 mg/g、1.5 mg/g、2.0 mg/g、2.5 mg/g)、酶解温度(40 ℃、45 ℃、50 ℃、55 ℃、60 ℃)、酶解时间(20 min、30 min、40 min、50 min、60 min)、pH(4.0、4.5、5.0、5.5、6.0)、液料比(10∶1、20∶1、30∶1、40∶1、50∶1(mL∶g))、乙醇体积分数(40%、50%、60%、70%、80%)、超声功率(100 W、150 W、200 W、250 W、300 W)和超声时间(13 min、16 min、19 min、22 min、25 min)对总黄酮产率的影响,每个水平平行测定3次,取平均值。
1.3.5 响应面试验设计
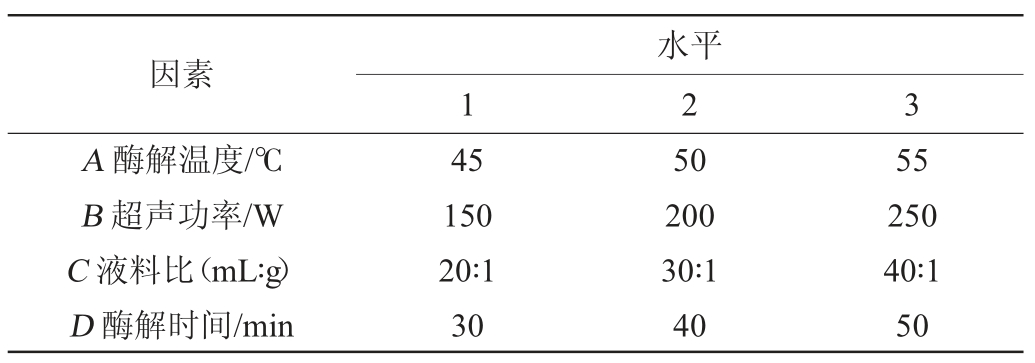
在单因素试验结果的基础上,选择对总黄酮提取得率影响较大的4个因素,酶解温度(A)、超声功率(B)、液料比(C)和酶解时间(D)进行Box-Benhnken试验设计,响应面试验因素与水平见表1。
表1 黄酮提取工艺优化响应面试验设计因素与水平
Table 1 Factors and levels of response surface tests for flavonoid extraction process optimization
1.3.6 泡桐花总黄酮抗氧化活性研究
(1)泡桐花总黄酮对DPPH自由基清除率的测定
提取的泡桐花总黄酮用无水乙醇配成质量浓度为50 μg/mL、70 μg/mL、90 μg/mL、110 μg/mL、200 μg/mL、300 μg/mL、500 μg/mL、800 μg/mL的样品溶液,根据文献[18]的试验方法测定总黄酮的抗氧化活性。以抗坏血酸作为对照,按式(2)计算清除率及半抑制浓度(half maximal inhibitory concentration,IC50)值。
式中:A0为无水乙醇和DPPH乙醇溶液混合均匀后吸光度值;A1为泡桐花样品溶液与DPPH乙醇溶液混合均匀后吸光度值;A2为泡桐花样品溶液与无水乙醇混合均匀后吸光度值。
(2)泡桐花总黄酮对羟自由基(·OH)清除活性的测定
参照文献[19]的试验方法并稍作修改,分别量取已配制质量浓度不同的样品溶液与抗坏血酸对照品溶液各1.0 mL置于10mL容量瓶中,分别加入5mmol/L的水杨酸溶液1.0mL、5 mmol/L的FeSO4溶液1.0 mL,摇匀,使之充分混合,再加入5 mmol/L的H2O2 1.0 mL,蒸馏水定容至刻度,于37 ℃水浴放置30 min后,冷却,在波长510 nm处测定吸光度值A1,用1.0 mL蒸馏水代替样品溶液反应,按同样的方法测定吸光度值A0,用1.0 mL蒸馏水代替H2O2,按同样的方法测定吸光度值A2。按式(3)计算清除率及IC50。
式中:A0为不加样品溶液的吸光度值;A1为加样品溶液的吸光度值;A2为不加H2O2的吸光度值。
(3)泡桐花总黄酮对ABTS·清除活性的测定
参照文献[20]的试验方法并稍作修改,将配制好的7 mmol/L ABTS溶液与2.45 mmol/L的过硫酸钾溶液按照1∶1的比例混合均匀,室温避光放置12 h,制成ABTS储备液。使用前用无水乙醇稀释使其在734 nm的吸光度值为0.7~0.8。
分别量取已配制质量浓度不同的样品溶液与抗坏血酸对照品溶液各0.4 mL,加入4.0 mL ABTS储备液,充分混匀,在室温下避光反应8 min,测定波长734 nm处吸光度值A1,0.4 mL乙醇代替样品溶液与4.0 mL ABTS储备液混合,测定吸光度值A0,0.4 mL样品溶液与4.0 mL乙醇混合,测定吸光度值A2。按式(4)计算清除率及IC50。
式中:A0为不加样品溶液的吸光度值;A1为加样品溶液的吸光度值;A2为不加ABTS的吸光度值。
1.3.7 数据处理
使用Design-Expert 8.0.6、OriginPro 2016、SPSS 22.0软件进行数据处理和分析。
2 结果与分析
2.1 泡桐花总黄酮提取工艺优化单因素试验
纤维素酶用量、酶解温度、酶解时间、pH、液料比、乙醇体积分数、超声功率、超声时间对总黄酮得率的影响见图1。
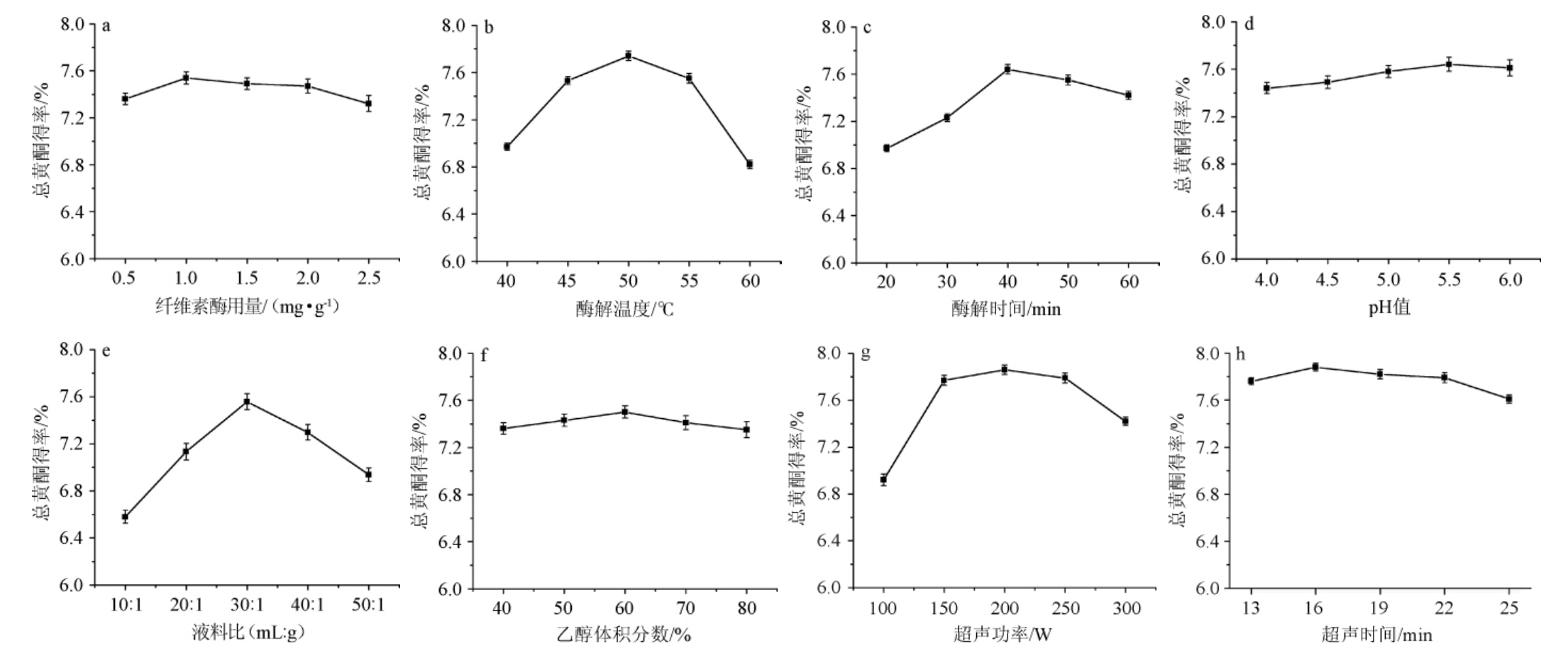
图1 纤维素酶用量(a)、酶解温度(b)、酶解时间(c)、pH(d)、液料比(e)、乙醇体积分数(f)、超声功率(g)、超声时间(h)对总黄酮得率的影响
Fig.1 Effect of cellulase dosage (a),enzymolysis temperature (b),enzymolysis time (c),pH (d),liquid-solid ratio (e),ethanol volume fraction (f),ultrasonic power (g),ultrasonic time (h) on the yield of total flavonoids
如图1a所示,随着纤维素酶的增加,总黄酮提取得率先升高后降低,这可能是因为细胞壁是由纤维素构成,纤维素酶添加量为1.0 mg/g时,细胞壁纤维素水解较彻底,促进总黄酮从细胞中溶出,当纤维素酶添加量继续增大时,会抑制酶的活力,导致总黄酮提取得率降低,因此选择酶添加量1.0 mg/g较为适宜。由图1b可以得出,当酶解温度为50 ℃时,总黄酮得率最大,可能是50 ℃时酶的活力达到最大,温度过低时,酶未被完全活化,不能充分发挥水解的作用,当温度过高时,酶的活性受到抑制,因此选择50 ℃为最佳酶解温度。由图1c可见,总黄酮的得率随着酶解时间的延长呈现先升高后降低的趋势,说明在40 min时,酶解效果较好,低于40 min时,纤维素酶未能完全水解细胞壁,导致总黄酮未能充分溶出,高于40 min时,可能会导致部分黄酮分子结构遭到破坏,还会促使其他非黄酮类物质的溶出,导致总黄酮得率降低,因此,适宜的酶解时间为40 min。如图1d所示,随着pH的增加,总黄酮得率呈现先增后减的趋势,但变化不大,应选择5.5为最佳的pH。如图1e所示,液料比30∶1(mL∶g)时,总黄酮得率最大,当液料比大于30∶1(mL∶g),总黄酮提取得率降低。可能是因为液料比过大时,提取溶剂较大会加大其他杂质的溶出,致使降压浓缩过程延长,会使部分总黄酮降解,使得提取率下降。因而选择液料比30∶1(mL∶g)较为适宜。由图1f可知,当乙醇体积分数为60%时,泡桐花总黄酮得率最大,这可能是因为乙醇体积分数太低,未能将泡桐花中的总黄酮完全浸出,而浓度太大时,醇溶性杂质又开始析出,导致总黄酮得率下降[21-22]。故选用乙醇体积分数60%较为适宜。由图1g可知,超声功率为200 W时,总黄酮提取得率达到最大,可能原因是功率较大时,超声波及剪切力作用下,使得总黄酮的结构遭到破坏,造成总黄酮得率下降[23],故选用200 W为最佳的超声功率。由图1h可知,当超声时间16 min时,总黄酮得率达到最大,这可能是因为超声时间超过30 min,总黄酮类物质可能会发生降解,导致得率下降[24],故选用16 min为最佳的超声时间。
2.2 泡桐花总黄酮提取工艺优化响应面试验
2.2.1 响应面试验结果及分析
以总黄酮得率(Y)为响应值,选取酶解温度(A)、超声功率(B)、液料比(C)和酶解时间(D)4个因素为评价因素,设计4因素3水平的响应面优化试验,试验设计及结果见表2。
表2 黄酮提取工艺优化响应面试验设计及结果
Table 2 Design and results of response surface tests for flavonoid extraction process optimization
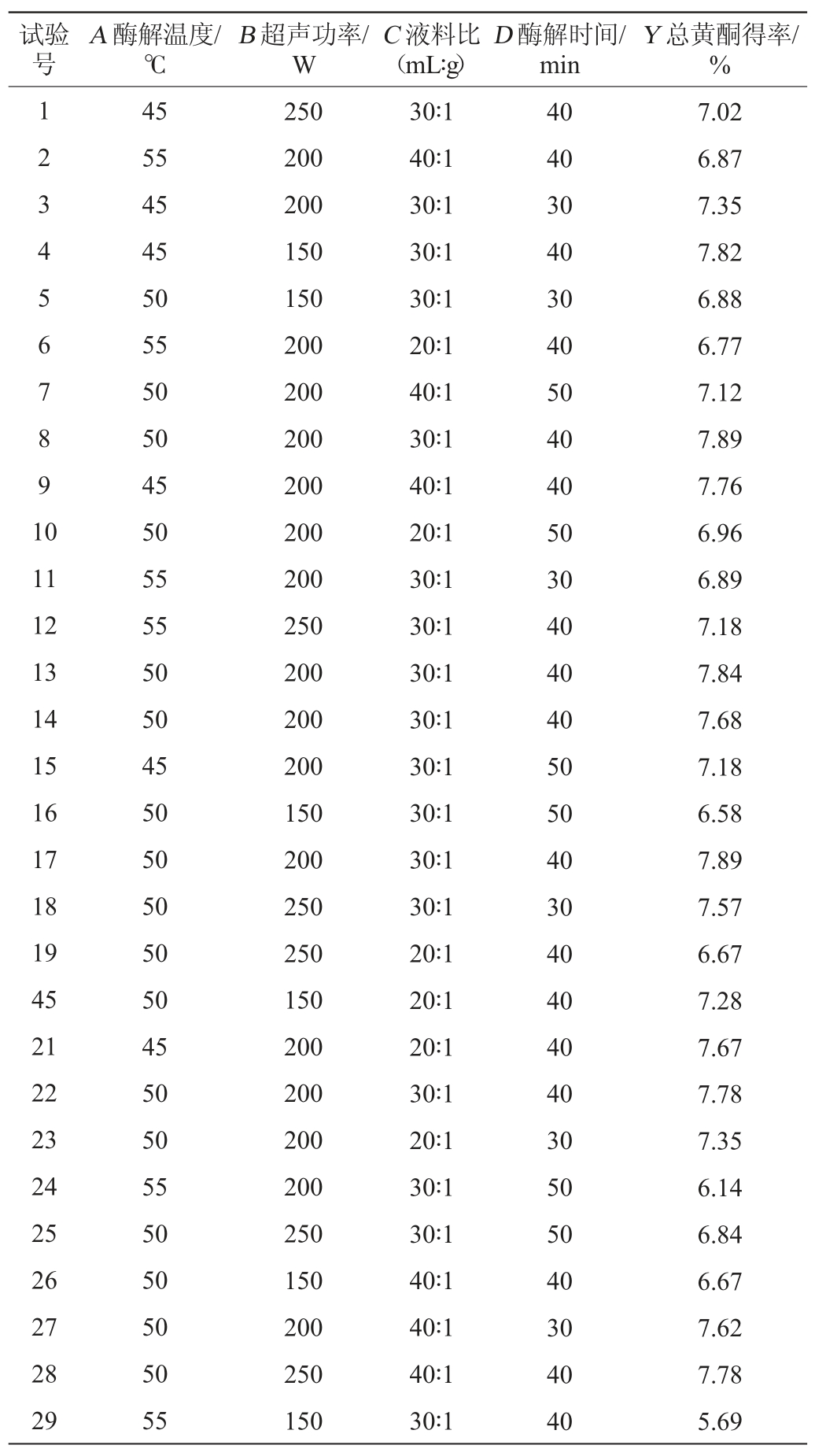
运用Design-Expert 8.0.6软件对表2结果进行回归拟合,所得二次回归方程为:Y=7.82-0.44A+0.18B+0.093C-0.24D+0.57AB+0.0025AC-0.15AD+0.43BC-0.11BD-0.027CD-0.43A2-0.48B2-0.16C2-0.42D2。回归方程方差分析如表3所示。
表3 响应面试验二次模型方差分析
Table 3 Variance analysis of response surface quadratic model
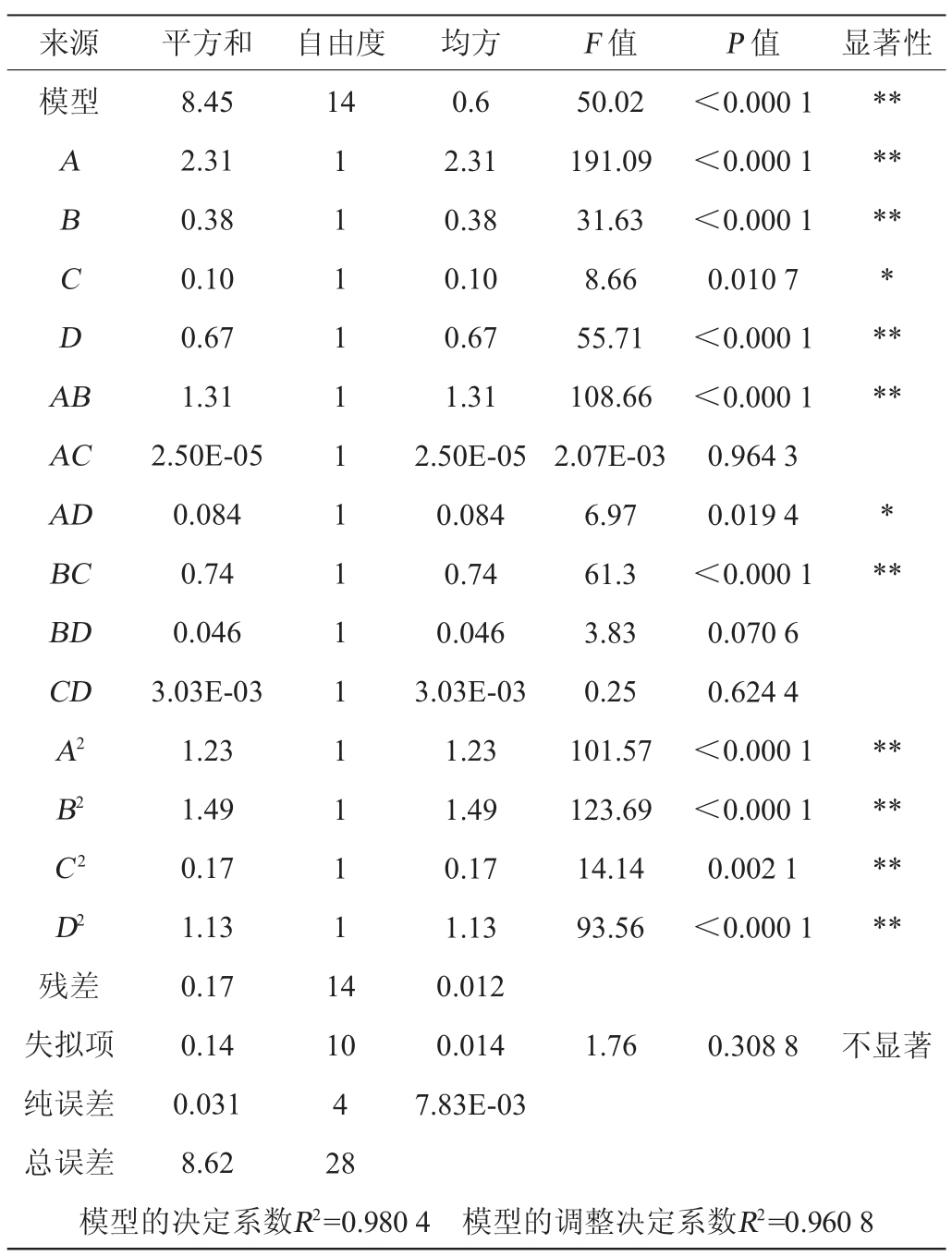
注:“*”表示差异显著(P<0.05);“**”表示差异极显著(P<0.01)。
由表3可知,总模型P<0.000 1,可知本试验所选取的模型具有高度的显著性,失拟项P值为0.308 8>0.05,故失拟项不显著,说明模型选取是无误的;模型的决定系数R2=0.980 4,模型可以解释98.04%实验中总黄酮得率的变化,说明方程的拟合度较好。模型的调整决定系数R2=0.960 8,表明试验误差小,可用该模型进行试验预测。因素A、B、D、AB、BC、A2、B2、C2、D2对试验结果的影响极显著(P<0.01),因素C、AD对试验结果的影响显著(P<0.05),由F值可知,各因素对总黄酮得率的影响主次顺序为:酶解温度(A)>酶解时间(D)>超声功率(B)>液料比(C)。
2.2.2 响应面图分析
各因素对泡桐花总黄酮得率影响的响应面图如图2所示,响应曲面图中图形陡峭程度越大代表相互作用越大,反之则越小。观察响应面的陡峭程度可以看出,酶解温度对泡桐花总黄酮提取得率影响最大,其次是酶解时间、超声功率,影响最小的是液料比,这与表3分析结果一致。

图2 各因素交互作用对泡桐花总黄酮得率影响的响应面和等高线
Fig.2 Response surface plots and contour lines of effects of interaction between each factor on the yield of flavonoids in Paulownia fortunei flowers
2.2.3 提取工艺优化及验证试验
通过Design-Expert 8.0.6软件分析得到最佳工艺条件为:酶解温度50.13 ℃,超声功率243.74 W,液料比40∶1(mL∶g),酶解时间35.89 min,在此优化提取条件下,总黄酮得率预测值可达8.01%。为便于试验操作,将最佳提取工艺条件修正为:酶解温度50 ℃,超声功率240 W,液料比40∶1(mL∶g),酶解时间36 min,并在此优化提取条件下进行3次平行试验的验证,得到泡桐花总黄酮的平均得率实际值为7.82%,与预测值接近,表明该模型具有较好的预测性能,响应面法优化泡桐花总黄酮提取工艺具有可行性。
2.3 泡桐花总黄酮抗氧化活性研究
2.3.1 泡桐花总黄酮对DPPH·清除活性的测定
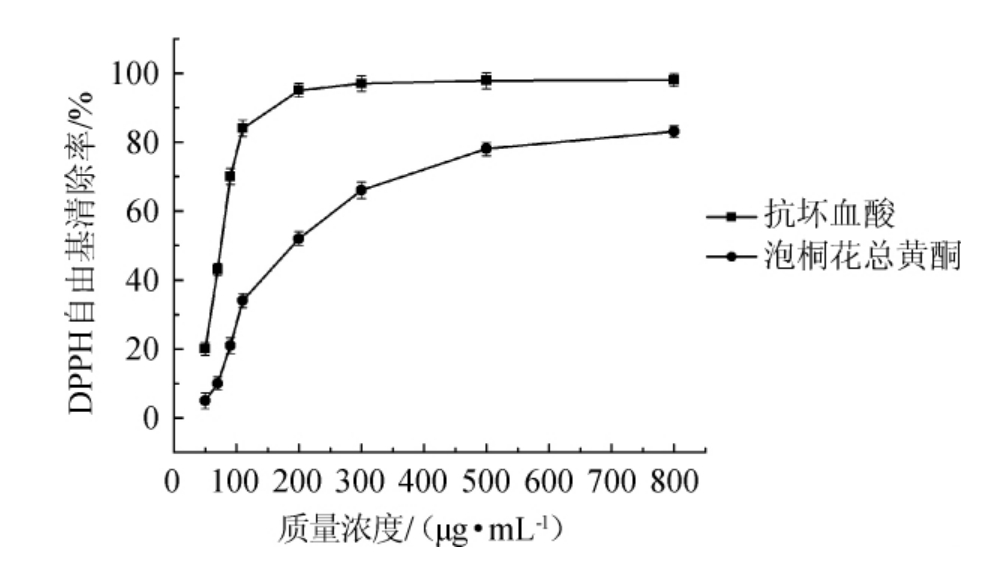
图3 不同质量浓度的泡桐花总黄酮和抗坏血酸对DPPH自由基的清除活性
Fig.3 Scavenging activities of different concentrations of Paulownia fortunei flowers total flavonoids and ascorbic acid on DPPH radical
不同质量浓度的泡桐花总黄酮和抗坏血酸对DPPH自由基的影响见图3。如图3所示,泡桐花总黄酮具有清除DPPH·的能力,且泡桐花总黄酮对DPPH·的清除率随着质量浓度的增加而增大,最后趋于平衡,在质量浓度800μg/mL时,DPPH·清除率达到83.1%。由SPSS22.0软件得出,泡桐花总黄酮的IC50值为214.2 μg/mL,抗坏血酸的IC50值为72.6 μg/mL,说明相同质量浓度下泡桐花总黄酮对DPPH·的清除率弱于抗坏血酸。
2.3.2 泡桐花总黄酮对·OH清除活性的测定
不同质量浓度的泡桐花总黄酮和抗坏血酸对羟自由基的影响见图4。如图4所示,泡桐花总黄酮具有清除羟的能力,且随着质量浓度的增加,泡桐花总黄酮对羟的清除率先升高,最后趋于平衡,在质量浓度800 μg/mL时,清除率达到75.4%。泡桐花总黄酮的IC50值为200.7 μg/mL,与此同时抗坏血酸的IC50值为68.6 μg/mL,说明相同质量浓度下泡桐花总黄酮对·OH的清除能力弱于抗坏血酸。
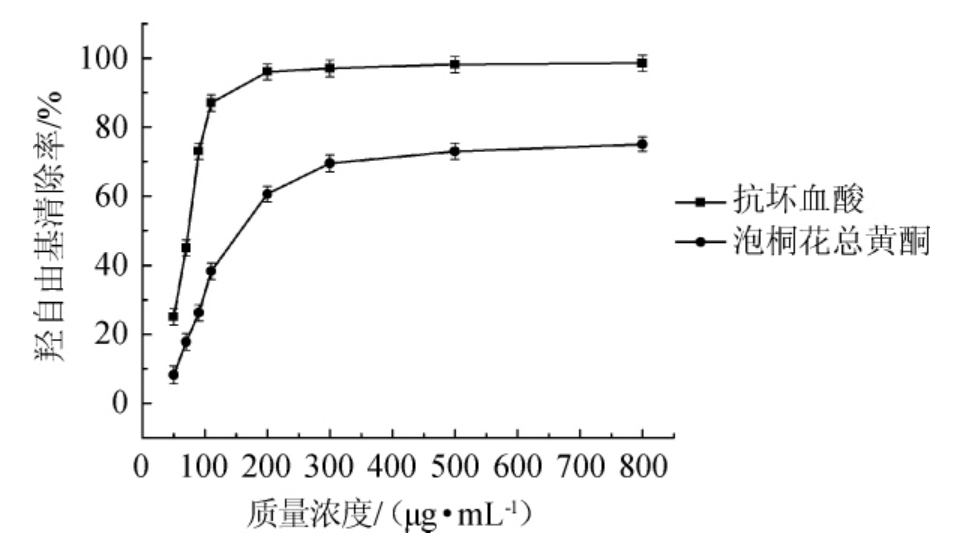
图4 不同质量浓度的泡桐花总黄酮和抗坏血酸对羟自由基的清除活性
Fig.4 Scavenging activities of different concentrations of Paulownia fortunei flowers total flavonoids and ascorbic acid on OH radical
2.3.3 泡桐花总黄酮对ABTS·清除活性的测定
不同质量浓度的泡桐花总黄酮和抗坏血酸对ABTS自由基的影响见图5。如图5所示,泡桐花总黄酮具有清除ABTS·的能力,在质量浓度800 μg/mL时,清除率达到64.3%。由SPSS22软件得出,泡桐花总黄酮的IC50值为328.5 μg/mL,抗坏血酸的IC50值为100.1 μg/mL,说明相同浓度下抗坏血酸对ABTS·的清除能力强于泡桐花总黄酮。
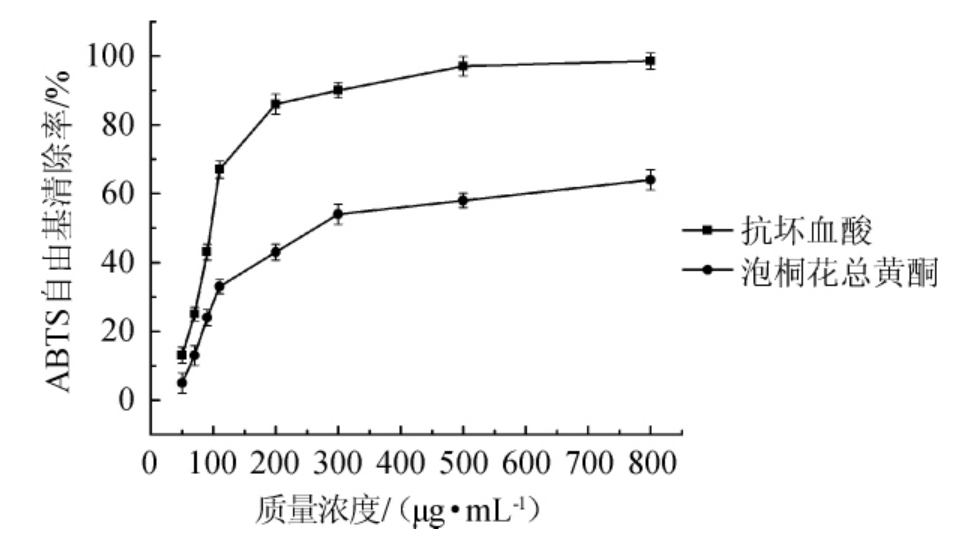
图5 不同质量浓度的泡桐花总黄酮和抗坏血酸对ABTS自由基的清除活性
Fig.5 Scavenging activities of different concentrations of Paulownia fortunei flowers total flavonoids and ascorbic acid on ABTS radical
3 结论
本试验采用超声波辅助酶法提取泡桐花总黄酮,在单因素试验的基础上,采用响应面法优化泡桐花总黄酮的提取工艺。优化后的最佳提取条件为酶解温度50 ℃,超声功率240 W,液料比40∶1(mL∶g),酶解时间36 min,通过3次平行试验验证得到泡桐花总黄酮的平均提取得率为7.82%,与预测值8.01%接近,表明该模型拟合度较好,为泡桐花总黄酮类化合物工业化生产提供一定的参考依据。泡桐花总黄酮抗氧化活性研究表明,泡桐花总黄酮对DPPH·、·OH和ABTS·均具有明显的清除活性,未来可能被开发为一种新型的抗氧化剂应用在食品、药品及化妆品等领域。在此基础上,后续可以对泡桐花总黄酮体内抗氧化活性及抗氧化活性机理进行深入研究。
[1]邢雅丽,毕良武,赵振东,等.泡桐植物资源分布及化学成分研究进展[J].林产化学与工业,2013,33(6):135-140.
[2]冯卫生,张靖柯,吕锦锦,等.泡桐花化学成分研究[J].中国药学杂志,2018,53(18):1547-1551.
[3]钱建中,张雨梅,丁丽军.泡桐花的活性成分及其药理作用综述[J].江苏农业科学,2013,41(5):7-9.
[4]姚焕英,高志勇,王君龙.泡桐属植物生物学及药用价值研究[J].渭南师范学院学报,2016,31(16):29-34.
[5]冯卫生,吕锦锦,张靖柯,等.泡桐花中糖苷类成分及其抗氧化活性[J].中成药,2020,42(2):369-374.
[6]屈枫锦,张晓珍,姚默,等.泡桐属药学研究新进展[J].安徽农业科学,2011,39(32):19809-19810.
[7]KAWAI Y.β-glucuronidase activity and mitochondrial dysfunction:the sites where flavonoid glucuronides act as anti-inflammatory agents[J].J Clin Biochem Nutr,2014,54(3):145-150.
[8]PHAM D C,NGUYEN H C,NGUYEN T H L,et al.Optimization of ultrasound-assisted extraction of flavonoids from Celastrus hindsii leaves using response surface methodology and evaluation of their antioxidant and antitumor activities[J].Biomed Res Int,2020,1(6):9.
[9]CEN X,TENG Y,YAO C,et al.Antioxidant properties of flavonoid derivatives and their hepatoprotective effects on CCl4 induced acute liver injury in mice[J].Rsc Adv,2018,8(28):15366-15371.
[10]MIN N,LEONG P T,LEE R C H.A flavonoid compound library screen revealed potent antiviral activity of plant-derived flavonoids on human Enterovirus A71 replication[J].Antivir Res,2018,150:60-68.
[11]杨玉玲,王莹,马红梅,等.德国洋甘菊总黄酮对糖尿病小鼠的降血糖作用研究[J].食品安全质量检测学报,2020,11(5):1524-1528.
[12]张青青.泡桐花总黄酮提取工艺的研究[D].杨凌:西北农林科技大学,2014.
[13]孟志芬,董彩霞,吕丹丹.毛泡桐花中总黄酮的含量测定及提取工艺研究[J].光谱实验室,2008(2):273-276.
[14]孟志芬,乔梅英,刘耀民,等.微波法提取毛泡桐花总黄酮的工艺研究[J].化学世界,2009,50(11):675-677,680.
[15]宋扬.泡桐花总黄酮类化合物的提取及其对肉鸡生长性能和肉品质的影响[D].洛阳:河南科技大学,2012.
[16]NAG S,SIT N.Optimization of ultrasound assisted enzymatic extraction of polyphenols from pomegranate peels based on phytochemical content and antioxidant property[J].J Food Meas Char,2018,12(3):1734-1743.
[17]李欣燃,朱淼,韩世明,等.刺梨叶总黄酮超声辅助提取工艺优化[J].食品研究与开发,2019,40(12):189-193.
[18]钱慧琴,秦晶晶,魏婧,等.线叶旋覆花总黄酮的提取工艺优化及其抗氧化活性分析[J].食品工业科技,2019,40(22):151-156,162.
[19]张鹏,张蝶,唐森,等.羊蹄甲果荚总黄酮提取工艺优化及抗氧化性研究[J].当代化工,2019,48(12):2717-2722,2726.
[20]张意笠,程汝滨,黄真,等.响应面法优化结香花总黄酮提取工艺及其抗氧化活性[J].食品工业科技,2020,41(19):192-197.
[21]陈建福.响应面优化超声辅助提取黄槿叶总黄酮工艺及其亚硝酸盐清除能力[J].食品工业科技,2019,40(6):193-197,204.
[22]朱盼,谢娟平,向纪明.Box-Behnken 响应面法优化秦巴山区粉葛中总异总黄酮的提取工艺[J].食品工业科技,2020,41(1):165-170.
[23]唐婷范,黄芳丽,朱家庆,等.超声波辅助提取葛根异总黄酮的工艺优化及其抑菌活性研究[J].食品研究与开发,2020,41(12):30-36.
[24]项昭保,伍晓玲,钟雪.响应面优化超声波辅助乙醇提取橄榄叶总黄酮的工艺研究[J].食品工业科技,2018,39(10):211-215,221.