螺旋藻也被称作节旋藻,是属于蓝藻门、藻殖段纲、颤藻科、螺旋藻属(节旋藻属)的一类原始生物[1-3]。人们已经发现30多个螺旋藻种[4]。目前中国允许产业化的螺旋藻种只有钝顶螺旋藻和极大螺旋藻[5-6]。
螺旋藻因其能量低、蛋白质适中、脂肪、碳水化合物含量低的特性以健康食品的形式进入人们的餐桌,在最少的脂肪、碳水化合物及能量摄入前提下补充优质蛋白质[7-8],提高人们的免疫力[9-10]、抗感染力[11-13]、抗病毒力[14],也可避免肥胖[15-16]和高血压等慢性病[17]。螺旋藻含有藻蓝蛋白、多糖、超氧化物歧化酶(superoxide dismutase,SOD)、γ-亚麻酸、叶绿素等具有改善健康功能的多种有用物质[18-22]。
内蒙古鄂尔多斯市鄂托克旗部分企业从2002年开始养殖螺旋藻,产量逐年增加,生产工艺不断优化和改善,产品质量不断提升[23]。2010年,鄂托克旗螺旋藻产业园建立后,26家企业全部入驻螺旋藻产业园区。现园区年生产螺旋藻粉3 500 t,占国内螺旋藻粉产量的40%以上[24]。为推动当地螺旋藻获得保健功能认证,按照《保健食品注册与备案管理办法》(国家食品药品监督管理总局令第22号)要求,注册保健食品要求提供毒理学试验报告,对产品进行安全性评价,研究了鄂尔多斯钝顶螺旋藻急性毒性、小鼠骨髓细胞微核试验、Ames试验、小鼠精子畸形试验,评价鄂尔多斯钝顶螺旋藻摄入的危险性,为保健食品剂量设计提供参考。
1 材料与方法
1.1 材料与试剂
墨绿色螺旋藻:产自鄂尔多斯市新宇力藻业公司,粉碎,研磨过55目筛备用。试验所用美国癌症研究所(institute of cancer research,ICR)小鼠:来自于浙江省试验动物中心,属清洁级,试验动物生产许可证号编号为SCXK(浙)2008-0033,试验动物使用许可证编号为SYXK(浙)2005-0074。试验动物所用饲料来自于浙江省试验动物中心,执行标准为GB 14924—2010《实验动物配合饲料营养成分》。检测环境温度为20~25 ℃,相对湿度为40%~70%。在试验前所有试验动物均在动物房设定环境条件下适应3 d。
鼠伤塞沙门氏菌(组氨酸营养缺陷型)四株:TA97a、TA98、TA100、TA102,来自于上海市疾病预防控制中心,经生物学试验鉴定为合格。
羧甲基纤维素、二甲基亚砜(dimethylsulfoxide,DMSO)、叠氮钠、敌克松、2-乙酰氨基芴、1,8-二羟基蔥醌、S9、环磷酰胺、甲醇、Giemsa、丝裂霉素C、伊红等试剂(分析纯):上海起发实验试剂有限公司。
1.2 仪器与设备
奥林巴斯CX21显微镜:奥林巴斯(北京)销售服务有限公司;JOYNTYJS-Ⅱ菌落计数器:上海乔越电子科技有限公司。
1.3 方法
1.3.1 小鼠急性经口毒性试验
选用雌雄各10只健壮、成熟的美国癌症研究所(institute of cancer research,ICR)小鼠,体质量应为18~22 g 之间。遵从最大耐受量试验的要求,设置20.0 g/kg小鼠重量试验剂量组,称取螺旋藻样品20 g,以1%浓度的羧甲基纤维素为溶媒配制40 mL样品混悬液。对雌雄各10只小鼠按20 mg/kg体质量灌胃容量灌胃(灌胃前停止供食16 h),间隔6 h后同灌胃容量条件下二次灌胃。观察记录试验小鼠灌药后的基本状况、中毒的情况基表现以及死亡状况,观察时长设置为7 d。
1.3.2 Ames试验
试验采用平板掺入的方法。准确称取钝顶螺旋藻样品0.50 g用DMSO研磨稀释到10.0 mL,在0.103 MPa压力条件下灭菌20 min,备用。用非代谢活化的TA100菌株系统开展预备试验,5 000 μg/皿剂量未出现明显的增菌和抑菌情况,在正式试验过程中选取8 μg/皿、40 μg/皿、200 μg/皿、1 000 μg/皿、5000 μg/皿五个剂量组设定为试验的浓度,对照组为空白、溶剂和阳性组(叠氮钠、敌克松、2-乙酰氨基芴与1,8-二羟基蔥醌),每一种试验菌株的每一个试验浓度均设置三皿平行,均在加与不加S9的条件下开展试验。试验均重复一次。直接计数培养基上的各个菌株发生的回变菌落数。
1.3.3 小鼠骨髓细胞微核试验
将体质量均在25~28 g之间的小鼠随机分成三个剂量组:2.5、5.0、10.0 g/kg体质量,分别称取试验螺旋藻样品2.5 g、5.0 g、10.0 g,配制20 mL混悬液,以1%羟甲基纤维素为溶媒。一个阴性对照组用1%浓度羟甲基纤维素,一个阳性对照组用40 mg/kg体质量环磷酰胺,每组选取10只小鼠,雄雄各5只。对小鼠间隔24 h分别灌胃2次,灌胃容量为20 mL/kg体质量,第二次灌胃后6 h将试验小鼠脱臼处死。用小鼠胸骨的骨髓制骨髓片,用甲醇溶液进行固定,然后采用Giemsa染色。在显微镜检时,分别对每只小鼠计数1 000个嗜多染红细胞,计算其微核千分率和PCE/NCE数值。
1.3.4 小鼠精子畸形试验
将25只体质量在25~30 g之间的ICR雄性小鼠随机分为三个剂量组:分别为2.5、5.0、10.0 g/kg体质量,然后分别称取试验样品5.0、10.0、20.0 g,配制成40 mL混悬液,以1%羧甲基纤维素为溶媒。设置一个阴性对照组:1%羧甲基纤维素,一个阳性对照组:1.5 mg/kg体质量丝裂霉素C,每组选取5只小鼠。用灌胃方式给予样品,灌胃容量为20 mL/kg小鼠体质量,连续灌胃5 d,毎天一次,给予对照组同样处理。首次灌胃后第35天将试验小鼠脱臼处死,在取得每组试验小鼠的两侧附睾后,用吸滤液制片,在自然条件下干燥,用甲醇溶液固定,采用1%伊红染色后,备用。用高倍显微镜观察涂片上精子的形态,对每只小鼠均计数完整精子1 000条,并计算发生畸形精子的百分数(%)。
2 结果与分析
2.1 小鼠急性经口毒性试验
试验小鼠死亡的统计结果见表1。在整个试验期限内,所有试验小鼠均未发现明显中毒症状和死亡现象。鄂尔多斯钝顶螺旋藻对试验雌雄小鼠经口最大耐受量(maximum-tolerated dose,MTD)都不小于20 g/kg体质量,故此鄂尔多斯钝顶螺旋藻样品属于无毒级。
表1 鄂尔多斯钝顶螺旋藻小鼠经口急性毒性死亡情况
Table 1 Oral acute toxicity death of Spirulina platensis from Ordos in mice

2.2 Ames试验
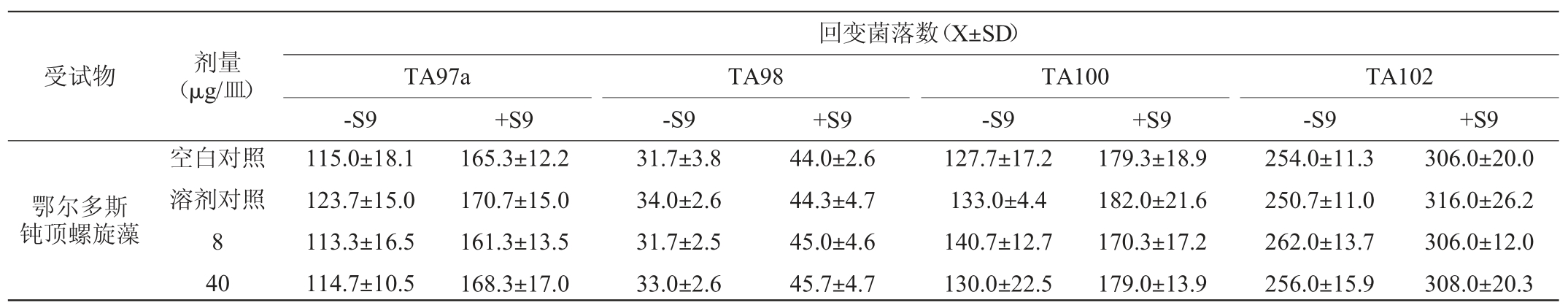
表2 鄂尔多斯钝顶螺旋藻Ames试验结果
Table 2 Result of Ames tests of Spirulina platensis from Ordos
续表
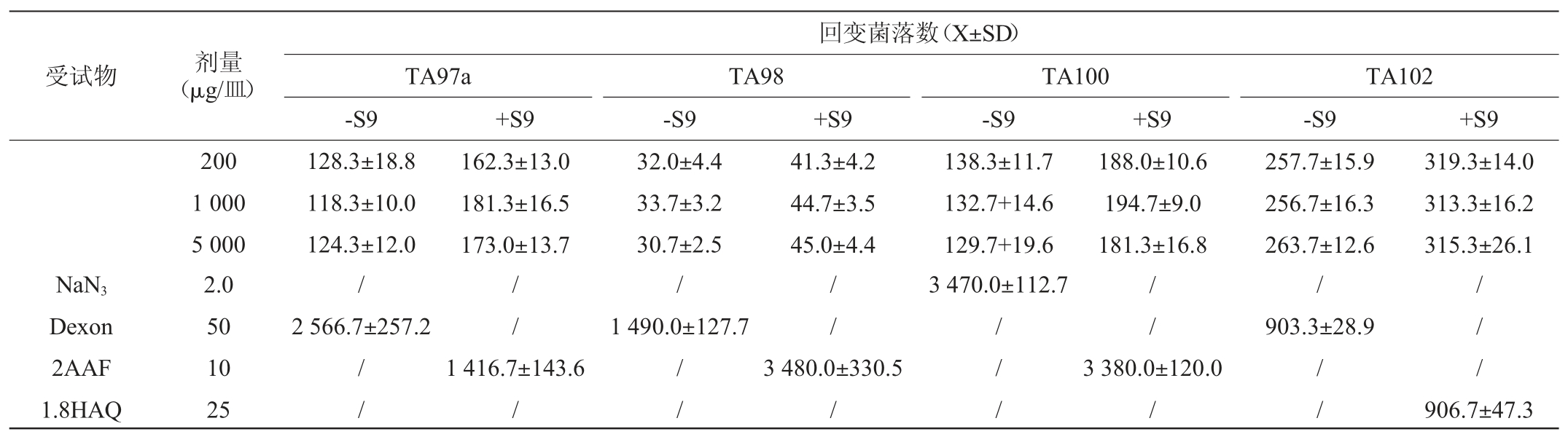
NaN3:叠氮钠;Dexon:对二甲基氨基苯重氮磺酸钠(敌克松);2AAF:2-乙酰氨基芴;1.8HAQ:1.8-二羟基蔥醌。下同。
表3 鄂尔多斯钝顶螺旋藻Ames试验重复试验结果
Table 3 Result of repeated Ames test of Spirulina platensis from Ordos
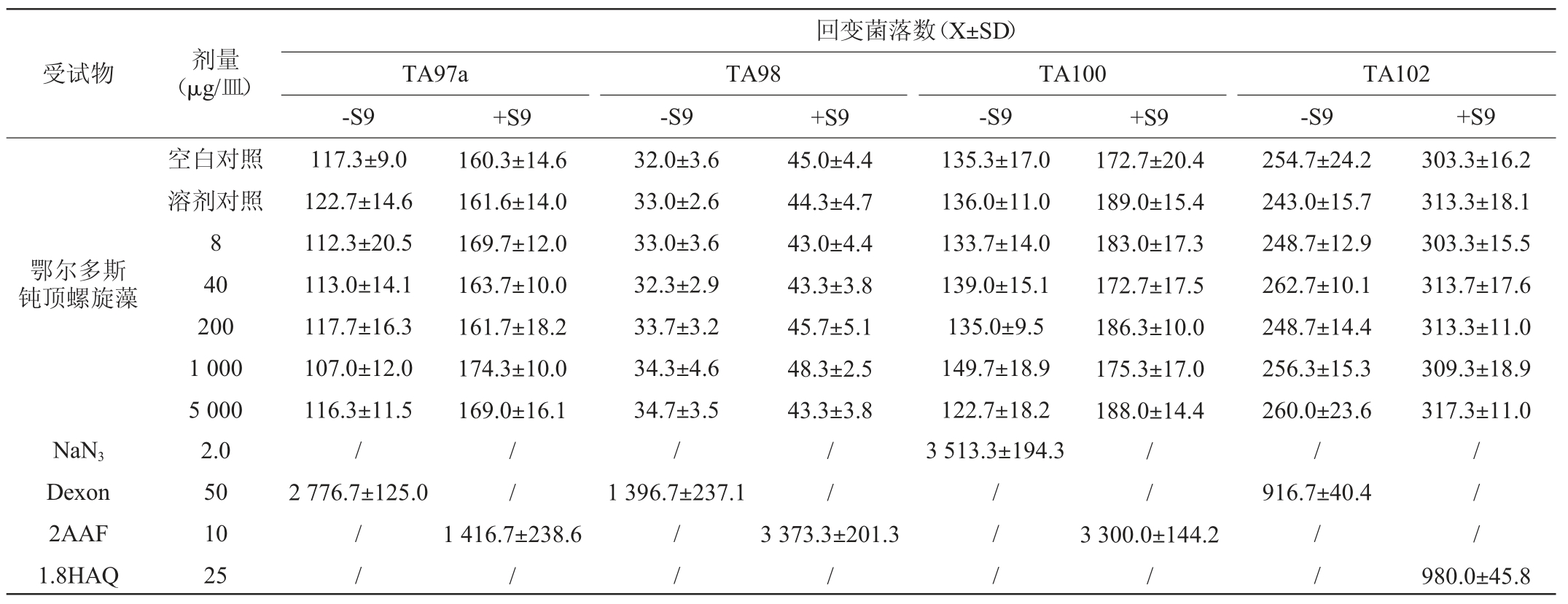
表2、表3为各试验菌株的回变菌落数。由表2和表3可知,无论加与不加S9,各浓度受试物回变菌落数均与阴性对照试验组结果趋于近似,而各阳性对照回变菌落数均超过阴性对照回变菌落数2倍以上。鄂尔多斯钝顶螺旋藻Ames试验结果呈阴性。
2.3 小鼠骨髓细胞微核试验
鄂尔多斯钝顶螺旋藻样品对试验小鼠骨髓细胞微核率的影响情况见表4。
表4 鄂尔多斯钝顶螺旋藻对小鼠微核的影响
Table 4 Effect of Spirulina platensis from Ordos on micronucleus in mice
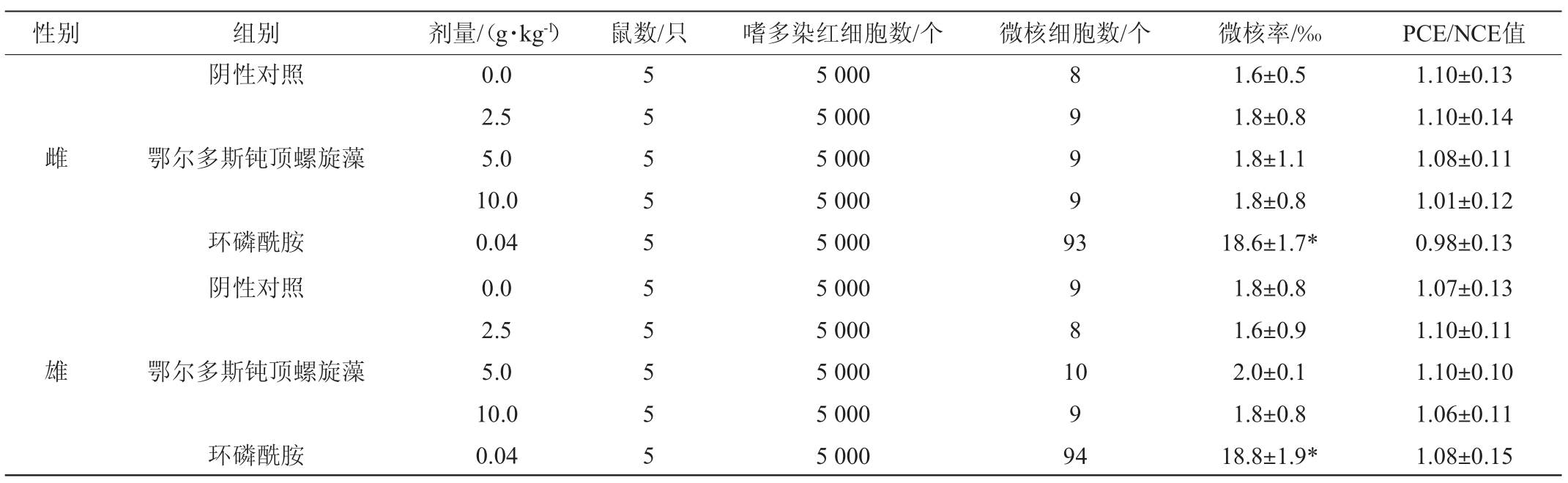
注:“*”表示差异极显著(P<0.01)(与阴性对照组比)。下同。
由表4可知,运用卡方检验对数据进行统计,各试验剂量组的微核千分率与阴性对照组相比均无显著差异(P>0.05),而阳性试验对照组骨髓细胞微核率则极显著超过阴性试验对照组(P<0.01)。试验数据表明鄂尔多斯钝顶螺旋藻样品对小鼠骨髓嗜多染红细胞微核率无显著影响。
2.4 小鼠精子畸形试验
鄂尔多斯钝顶螺旋藻样品对试验小鼠精子发生畸形比率的数据见表5。各剂量组试验小鼠精子畸形发生率与阴性对照组比较均无显著性差异(P>0.05),而阳性试验对照组小鼠精子畸形发生率则极显著高于阴性对照组(P<0.01),数据表明鄂尔多斯钝顶螺旋藻样品对小鼠精子畸形发生率无显著影响(P>0.05)。
表5 鄂尔多斯钝顶螺旋藻对小鼠精子畸形发生率的影响
Table 5 Effect of Spirulina platensis from Ordos on the incidence of sperm abnormalities in mice
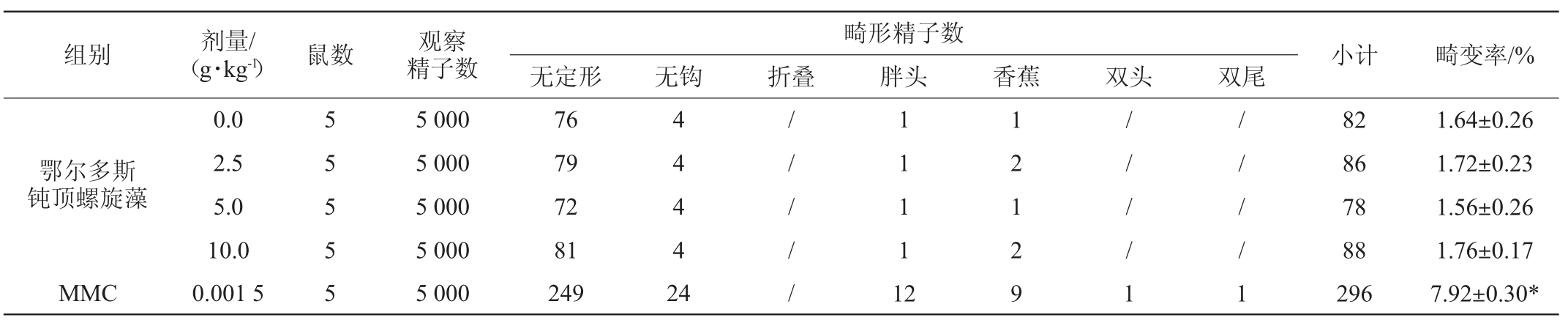
注:MMC为丝裂霉素C。
3 讨论
鄂尔多斯钝顶螺旋藻其藻种也来自于当地碱湖,虽然藻种经鉴定属于钝顶螺旋藻品系,且针对钝顶螺旋藻的营养和功能已有多项研究成果,但其毕竟为一中国新记录种[23],其毒理学试验并未开展,其安全性也未得到验证,所以对鄂尔多斯钝顶螺旋藻开展急性毒性试验非常必要。
试验结果表明,鄂尔多斯钝顶螺旋藻对雌雄小鼠经口MTD均大于20 g/kg体质量,属于无毒级产品,且证明对试验小鼠没有发生突变,对小鼠骨髓嗜多染红细胞微核百分率也未见明显的影响,对试验小鼠精子发生畸形比率无显著影响,可以证明鄂托克旗产钝顶螺旋藻无急性毒性。这与李晓玉等[25]检测的北海生巴达生物科技有限公司提供螺旋藻粉的急性毒性检测结果相同。李凤文等[26]对昆明某技术有限公司提供的螺旋藻精片开展了急性毒性、Ames、小鼠骨髓细胞微核试验和小鼠精子畸形试验,也得出了无毒性、无致突变等与本研究一致性的结果。本研究结果与刘用国等[27]对福清市新大泽产螺旋藻粉对小鼠急性毒性的研究结果也相一致,由此可见,内蒙古鄂托克旗产钝顶螺旋藻的急性毒性、致突变和致畸的结果与广西、云南、福建产螺旋藻的结果相一致,说明此四地的螺旋藻基本毒理学属性相一致,但广西、云南、福建螺旋藻是否为钝顶螺旋藻且其是否产自上述三地均有待于进一步考证和验证。从上述试验结果来看,鄂托克旗产钝顶螺旋藻是无毒和无致突变的,可以作为人们放心食用的食品或保健食品。
4 结论
鄂尔多斯钝顶螺旋藻小鼠经口急性毒性最大耐受量(MTD)都大于20.0 g/kg体质量(雌雄两性别),根据急性毒性分级的判定标准进行判定,本试验受试样品应属于无毒级别;Ames试验、小鼠骨髓细胞微核试验与小鼠精子畸形试验结果都为阴性,显示在本次试验设定的条件下,鄂尔多斯钝顶螺旋藻未显示有致突变性和致精子畸形特性。
[1]胡鸿钧.微藻分类学[M].北京:中国轻工业出版社,1999:1-10.
[2]B.福迪,罗迪安译.藻类学[M].上海:上海科学技术出版社,1980:24.
[3]GLADE M J,SIST M D.Dietary yeast culture supplementation enhances urearecyclingintheequinelargeintestine[J].Nutr Rep Int,1988,37(1):11-17.
[4]KAJI T,OKABE M,SHIMADA S.Sodium spirulina as a potent inhibitor of arterial smooth muscle cell proliferation in vitro[J]. Life Sci,2004,74:2431-2439.
[5]胡鸿均.国外螺旋藻生物技术的现状及发展趋势[J].武汉植物学研究,1997,15(4):369-374.
[6]DESIKACHARY T V,BAI N J.The identification of Arthrospira(Spirulina)strains and natural samples of different geographical regions[J]. Taxonom stud Spirulina II,1996(83):163-178.
[7]FLACHOWSKY G,MEYER U,SUDEKUM K.Land use for edible protein of animal origin-a review[J].Animals,2017,7(3):2-19.
[8]BLEAKLEY S,HAYES M.Algal proteins:extraction,application,and challenges concerning production[J].Foods,2017,6(5):1-34.
[9]JUSZKIEWICZ A,BASTA P,PETRICZKO E,et al.An attempt to induce an immunomodulatory effect in rowers with Spirulina extract[J]. J Int Soc Sport Nutr,2018,15(1):9.
[10]WU Q H,LIU L,MIRON A,et al.The antioxidant,immunomodulatory,and anti-inflammatory activities of Spirulina:an overview[J].Arch Toxicol,2016,90(8):1817-1840.
[11]SAUDAGAR R B,SAOKAR S N.Anti-inflammatory natural compounds from herbal and marine origin[J].J Drug Deliver Ther,2019,9(3):669-672.
[12]FERNANDO I P,NAH J,JEON Y,et al.Potential anti-inflammatory natural products from marine algae[J].Environ Toxicol Phar,2016,48:22-30.
[13]JANG H,CHOI E Y.Effects of Spirulina platensis extract,the act of which are anti-inflammation,anti-aging,as well as suppressing melanin synthesis[J].Kor J Aesthet Cosmetol,2015,13(2):243-249.
[14]CHEN Y,CHANG G,KUO S,et al.Well-tolerated Spirulina extract inhibits influenza virus replication and reduces virus-induced mortality[J].Sci Rep,2016,6:24253.
[15]SAJJAD M,RAHELE Z,SAHAR F,et al.Effects of Spirulina supplementation on obesity:a systematic review and meta-analysis of randomized clinical trials[J].Complement Ther Med,2019,47:102211.
[16]HERNANDEZLEPE M A,WALLMEDRANO A,LOPEZDIAZ J A,et al.Hypolipidemic effect of Arthrospira (Spirulina) maxima supplementation and a systematic physical exercise program in overweight and obese men:a double-blind,randomized,and crossover controlled trial[J]. Mar Drugs,2018,16(10):364.
[17]SZULINSKA M,GIBASDORNA M,MILLERKASPRZAK E,et al.Spirulina maxima improves insulin sensitivity,lipid profile,and total antioxidant status in obese patients with well-treated hypertension:a randomized double-blind placebo-controlled study[J]. Eur Rev Med Pharmacol Sci,2017,21:2473-2481.
[18]CIFERRI O,TIBONI O.The biochemistry and industrial potential of Spir-ulina[J].Ann Rev Microbiol,1985,39:503.
[19]李神州,李岳.浅谈螺旋藻的开发价值及应用[J].科技资讯,2008(14):208-209.
[20]ERIKSEN N T.Production of phycocyanin-a pigment with applications in biology,biotechnology,foods and medicine[J].Appl Microbilol Biot,2008,80(1):1-14.
[21]吴文龙,杨志娟.螺旋藻保健食品的功能因子与研究开发进展[J].食品研究与开发,2006,27(2):129-131.
[22]赵琪,李宗磊,吴昊,等.超声-微波协同提取螺旋藻中的叶绿素[J].中国酿造,2016,35(2):106-108.
[23]乔辰,栗淑媛.鄂尔多斯高原碱湖螺旋藻[M].北京:科学出版社,2013:26-41.
[24]王志忠.鄂尔多斯高原碱湖钝顶螺旋藻生产加工关键因子研究[D].呼和浩特:内蒙古农业大学,2015.
[25]李晓玉,陈忠伟,赵武,等.螺旋藻的急性和亚慢性毒性试验[J].畜牧与饲料科学,2018,39(9):4-9.
[26]李凤文,赵鹏,苏爱荣,等.螺旋藻精片毒性试验研究[J].应用预防医学,2008(1):8-11.
[27]刘用国,王江融,李菊芬,等.螺旋藻粉的药理和毒性研究[J].海峡药学,1999(3):31.