辣椒(Capsicum frutescence L.)属茄科(Solanaceae)辣椒属(Capsicum),是能结辣椒浆果的一年生或多年生草本植物[1]。辣椒不仅能增强食欲,还具有多种保健功,如能够预防心血管疾病、改善消化功能,具有减肥和促进血液循环等功效[2-5]。剁辣椒是具有地域特色明显的产品,但由于新鲜辣椒的季节性较强,一般采用高盐进行保坯发酵,然后在经过脱盐、调味、杀菌成为商品化产品。在此加工过程中会产生大量的盐渍辣椒汁无法处理,直接排放造成大量营养成分的浪费[9-10],而且环境污染严重,不利于行业的可持续发展,因此开发利用辣椒汁成为企业和研究者的一个热点[11-13]。盐渍辣椒汁不仅营养丰富,含有较高的盐度,同时也含有一些耐盐的微生物,风味独特。由于干辣椒无季节性问题,且原料方便控制[14-16]。本研究将盐渍辣椒汁和一定比例的干辣椒混合进行发酵制备辣椒酱,探讨强化接种发酵提升其品质的可能性。将16%盐度的辣椒汁以无菌水平衡盐度至10%左右后,加入干辣椒,分别接入5株菌株(凝结芽孢杆菌1.3220、植物乳杆菌1.555、植物乳杆菌1.3919、鲁氏接合酵母2.1913、鲁氏接合酵母2.371)发酵制备辣椒酱,利用顶空-固相微萃取(head space solid-phase micro-extractions,HS-SPME)结合气质联用(gaschromatography-massspectrometry,GC-MS)法对发酵30 d后辣椒酱进行风味物质的检测,且采用Upset软件及主成分分析(principalcomponentanalysis,PCA)研究其挥发性风味成分的共同点和差异性,探讨接种发酵对辣椒酱的影响,并为盐渍辣椒汁的综合利用提供参考,促进产业良性发展。
1 材料与方法
1.1 材料与试剂
1.1.1 原料和菌株
盐度为16%盐渍辣椒水、干辣椒:长沙坛坛香调料食品有限公司;凝结芽孢杆菌(Bacillus coagulans)1.3220、植物乳杆菌(Lactobacillus plantarum)1.555、1.3919、鲁氏接合酵母(Zygosaccharomyces rouxii)2.1913、2.371:中国普通微生物菌种保藏管理中心。
1.1.2 化学试剂
MRS肉汤培养基、营养肉汤培养基、麦芽汁培养基:北京奥博星生物技术有限责任公司。实验所用试剂均为分析纯。
1.1.3 培养基
营养肉汤液体培养基:牛肉膏5.0 g/L,蛋白胨10 g/L,氯化钠5.0 g/L,pH 7.2~7.5。
MRS液体培养基:蛋白胨10 g/L,牛肉膏10 g/L,酵母提取物5.0 g/L,磷酸氢二钾2.0 g/L,柠檬酸二铵2.0 g/L,乙酸钠5.0 g/L,葡萄糖20 g/L,吐温80 1.0 mL,硫酸镁0.5 g/L,硫酸锰0.25 g/L,pH6.2~6.4。
麦芽汁液体培养基:麦芽汁70 mL,pH 6.4。
培养基灭菌条件:121 ℃高压灭菌20 min。
1.2 仪器与设备
CP114电子天平:奥豪斯仪器有限公司;KQ3200E超声波清洗器:昆山市超声仪器有限公司;FE20K pH计:梅特勒-托利多仪器有限公司;20133419 超纯水机:贝徕美生物科技有限公司;QP2010 SE气相色谱质谱联用仪:日本岛津公司;HS-SPME固相微萃取装置:美国Supelco公司;DHP120恒温培养箱:上海实验仪器厂有限公司;HY45恒温摇床:深圳汇成科技有限公司。
1.3 试验方法
1.3.1 菌种扩大培养
从斜面上分别将凝结芽孢杆菌1.3220,植物乳杆菌1.555、1.3919,鲁氏接合酵母2.1913、2.371挑出后,接入营养肉汤液体培养基、MRS液体培养基、麦芽汁液体培养基中,除凝结芽孢杆菌置于30 ℃摇床中以外,其余的均放置于28 ℃培养箱中培养。3~5 d后,各取3%菌液,接入相应液体培养基进行扩大培养,当微生物培养数量细菌数达到107 CFU/mL、酵母菌数量106 CFU/mL以上数量级时,放入4 ℃冰箱保存备用。
1.3.2 样品制备
干辣椒切碎成片状,盐渍辣椒水用无菌水将盐度稀释至10%,将稀释后的盐渍辣椒水∶干辣椒以3∶1的质量比混匀,再接入3%的单一菌种,放入食品级白色塑料桶中,根据所选微生物的适宜生长温度,选择在30 ℃条件下密封发酵一个月。样品编号详情为:空白(P-KB)、PB-1.3220(凝结芽孢杆菌1.3220)、PZ-2.371(鲁氏接合酵母2.371)、PZ-2.1913(鲁氏接合酵母2.1913)、PL-1.5559(植物乳杆菌1.555)、PL-1.3919(植物乳杆菌1.3919)。
1.3.3 HS-SPME-GC-MS分析条件
HS-SPME:首先将萃取头(85 μmPA)在GC进样口温度为240 ℃条件下老化40 min,备用;将6种发酵辣椒样品取10 g分别放置于15 mL顶空瓶中,60 ℃预热20 min备用,将已老化的萃取头穿过密封垫插入顶空进样瓶内后推出纤维头,露出纤维头距离样品液面约10 mm,顶空吸附30 min,插入GC进样口解吸5 min。
气相色谱条件:CD-WAX石英毛细管柱(30m×0.25 mm,0.25 μm);载气:高纯氦气(He),流速1 mL/min;进样口温度:240 ℃;不分流进样。程序升温:柱温50 ℃;进样时间:1 min,起始温度为50 ℃保持2 min后,以5 ℃/min的速度升温至200 ℃保持14 min,再以15 ℃/min的速度升至240 ℃。
质谱条件:电子电离(electron ionization,EI)源,接口温度220 ℃,离子源温度200 ℃,电子能量70 eV,质量扫描范围45~500 m/z。
定性定量方法:采用美国国家标准技术研究所(national institute of standards and technology,NIST)谱库和Wiley谱库对挥发性成分进行定性分析(匹配度>80,最大值为100)。
1.3.4 数据处理
每次样品重复3次,主成分分析是一种使用最广泛的数据降维算法,用以解释数据的方差,证明数据可靠性,同时通过样品点与横坐标的距离,可以反映样品组之间的差异;Upset软件作图来呈现样品数较多时,样品组之间各物质的异同。
2 结果与分析
2.1 不同菌种发酵辣椒酱中挥发性香气成分的测定
通过GC-MS法对6种发酵辣椒样品挥发性香气成分进行检测,其总离子流色谱图见图1,各样品检出风味成分见表1。
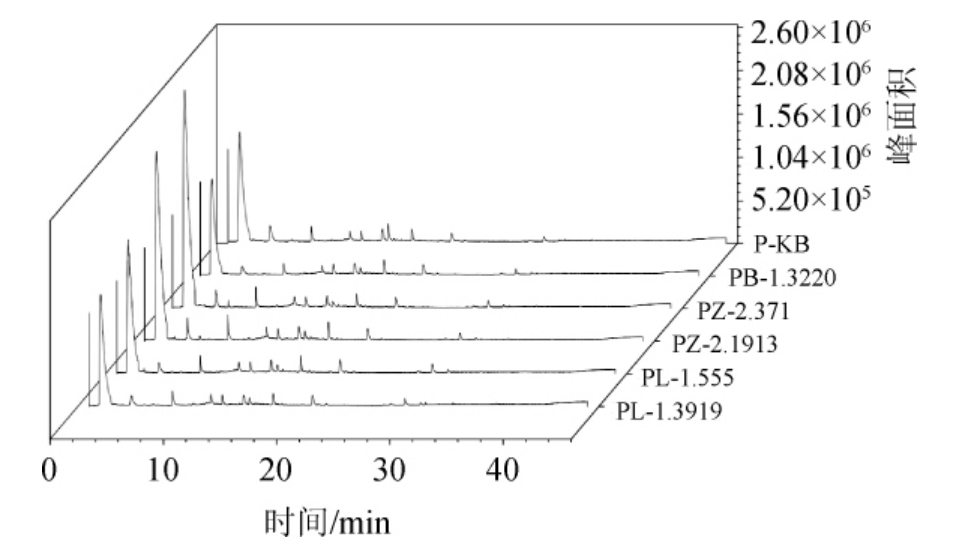
图1 发酵辣椒酱挥发性成分GC-MS分析总离子流色谱图
Fig.1 Total ion chromatogram of volatile components in fermented pepper sauce analysis by GC-MS
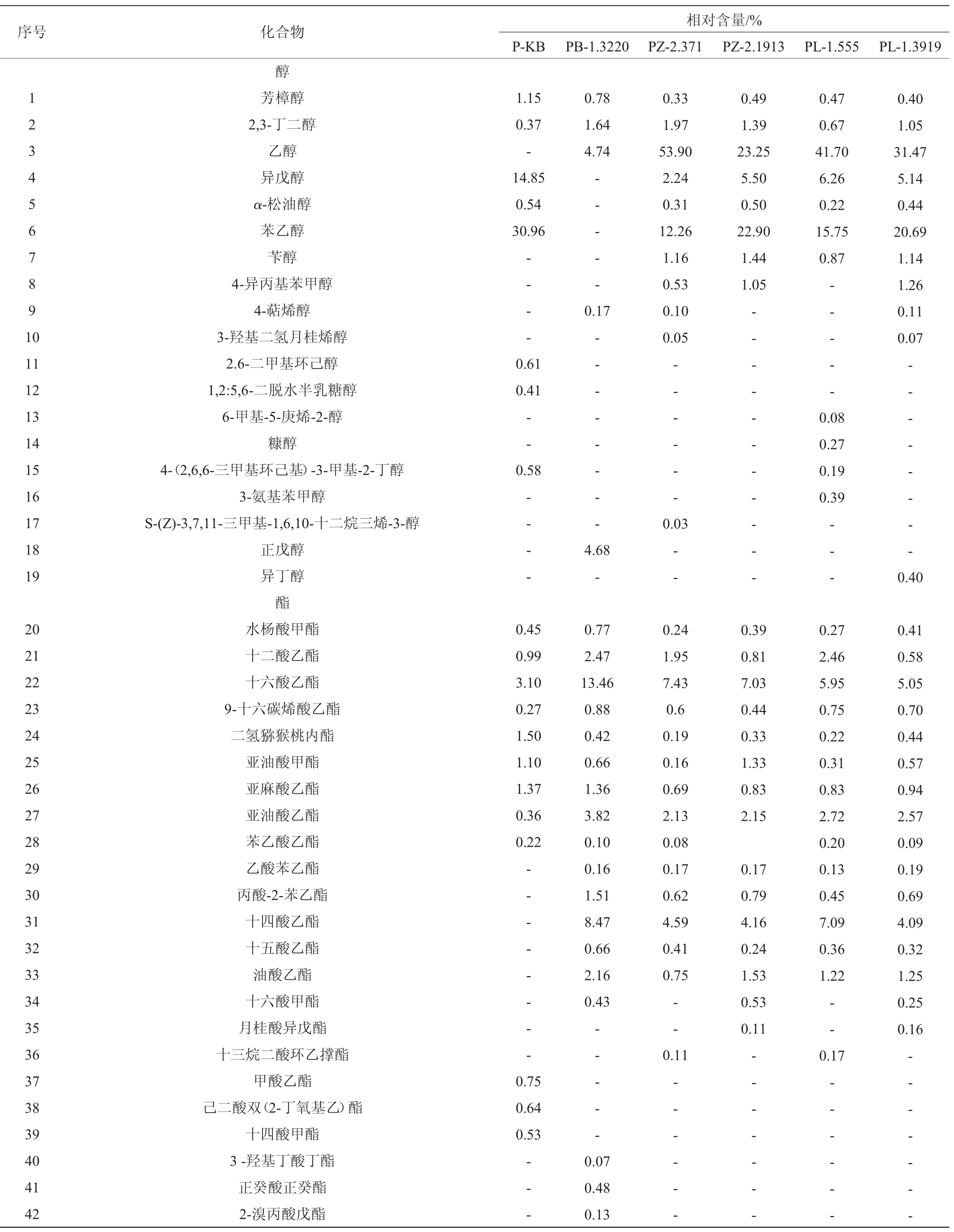
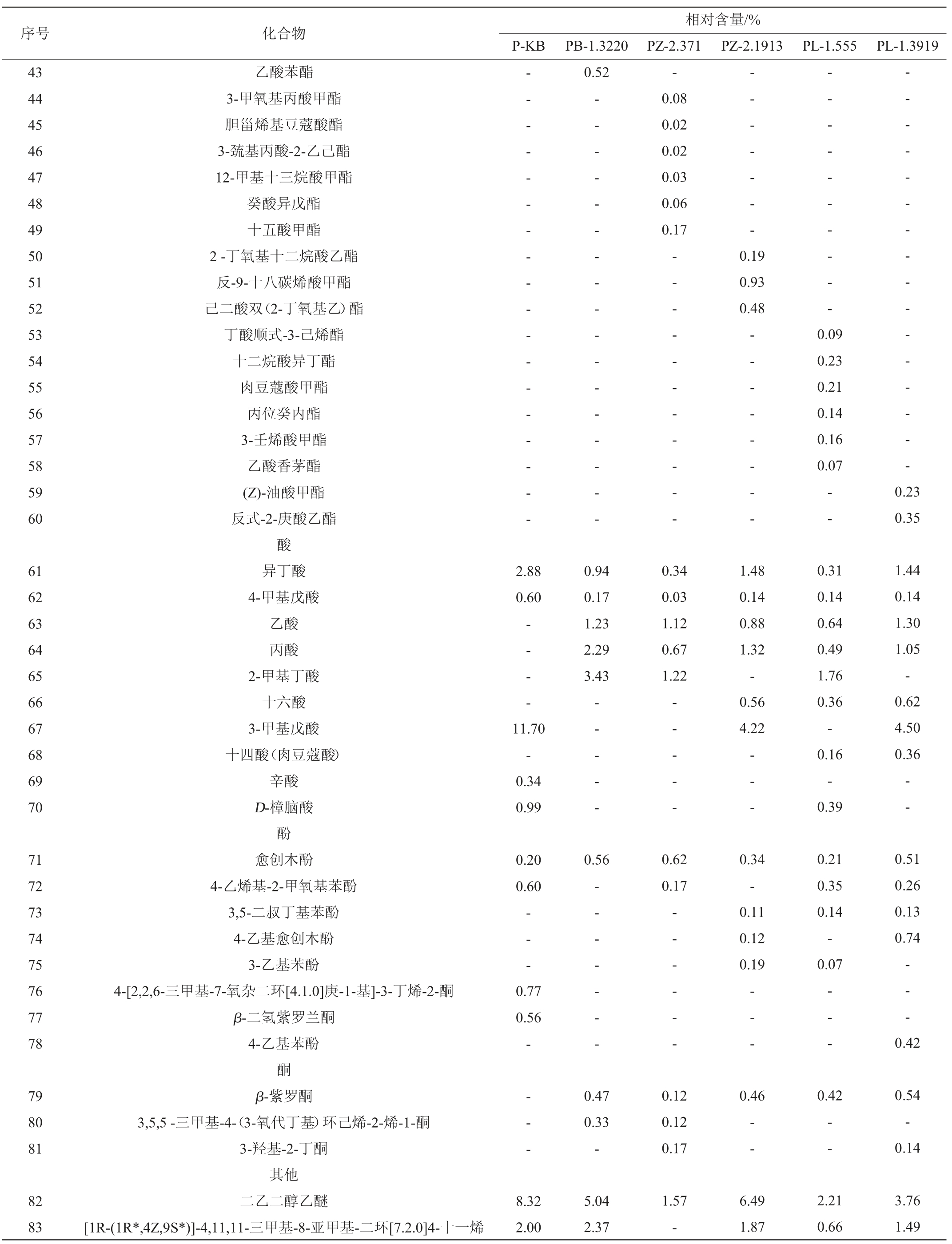
表1 发酵辣椒酱挥发性成分含量测定结果
Table 1 Determination results of volatile components contents in fermented pepper sauce
续表
续表
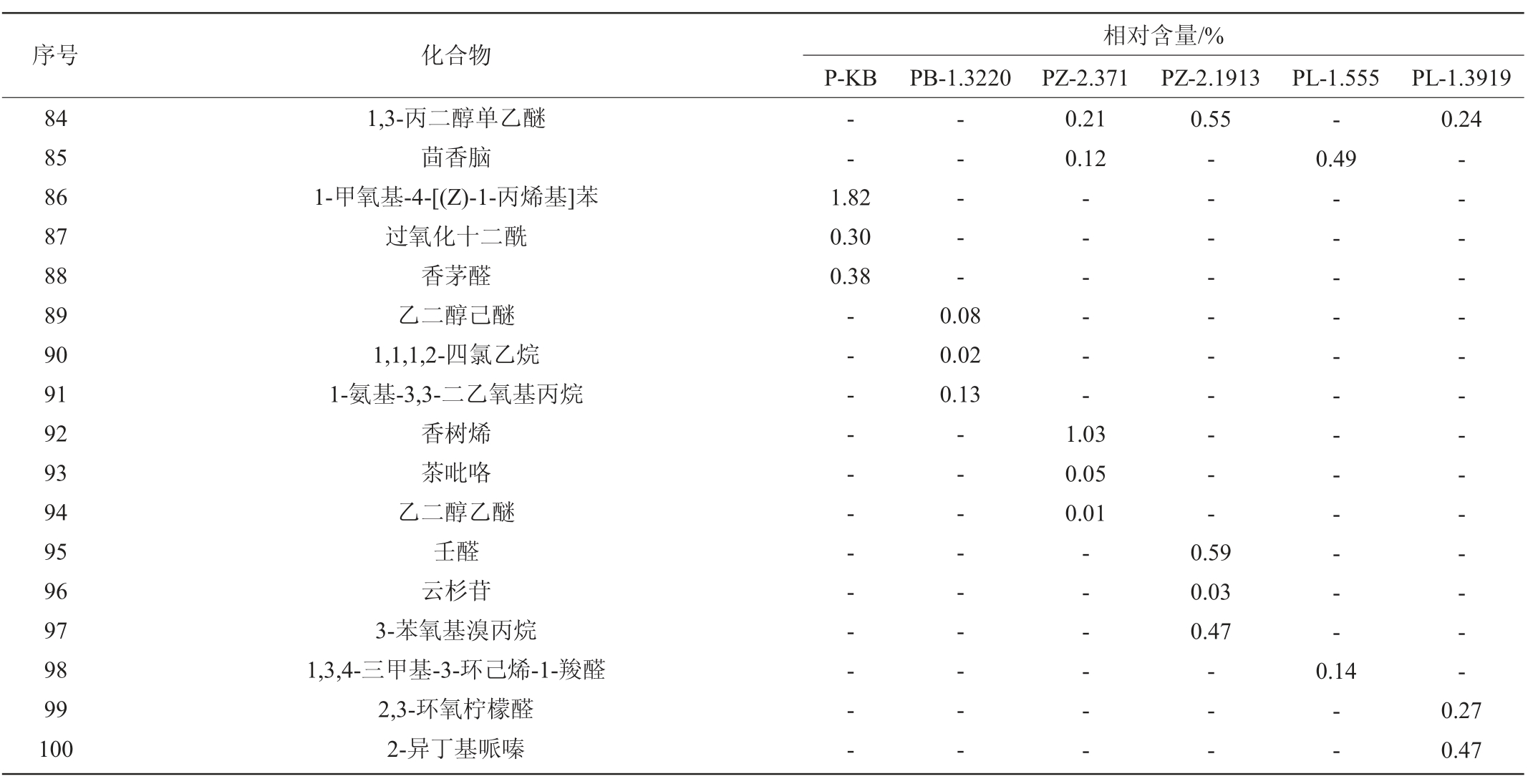
由表1可知,6种发酵辣椒样品共检测出100种物质,说明发酵辣椒酱中气味成分物质丰富,其中包括醇(19种)、酯(41种)、酸(10种)、酚(8种)、酮(3种)、其他(19 种)。
2.1.1 不同菌种发酵辣椒酱挥发性成分种类比较
不同菌株发酵辣椒酱样品中挥发性物质的种类比较结果见图2。由图2可知,醇类和酚类物最为丰富的样品为PL-1.3919,分别有11种、5种,酯类物质在样品PL-1.555(20种)和样品PL-1.3919(19种)中种类均较多,说明样品PL-1.3919呈现出的风味物质最为丰富。虽然P-KB中挥发性成分相对含量较高,但各类别种类数量较低,表明未接菌样品的风味会较为单一。
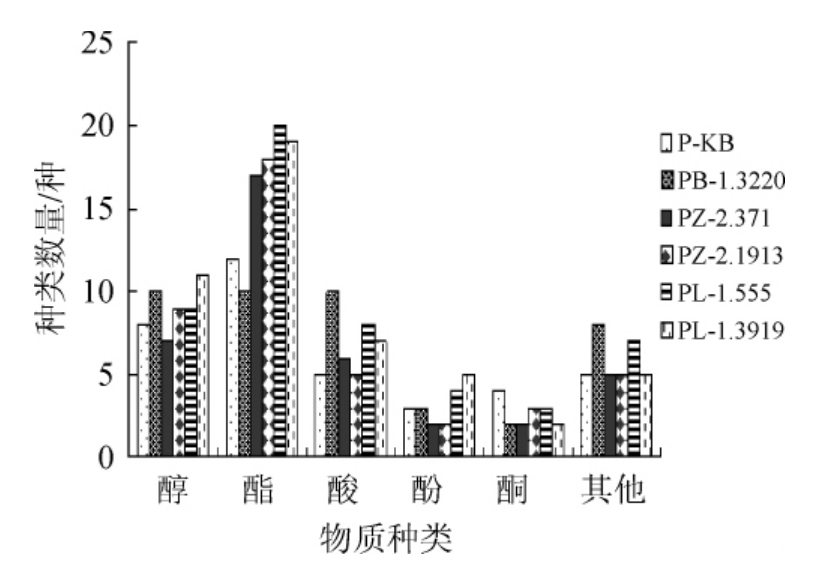
图2 不同发酵辣椒酱样品中挥发性成分的种类
Fig.2 Types of volatile components in different fermented pepper sauce samples
2.1.2 不同菌株发酵辣椒组之间同异性分析
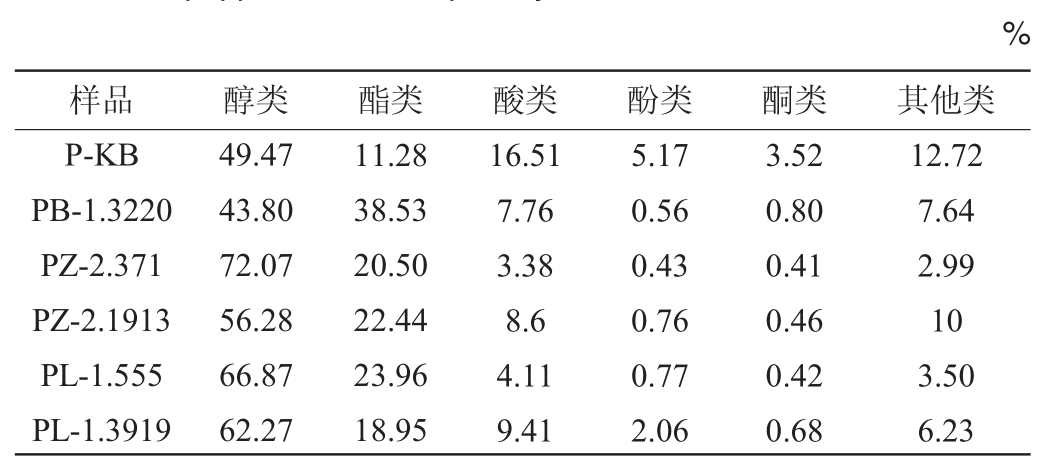
各辣椒酱样品中挥发性物质种类含量差异比较结果见表2。由表2可知,P-KB样品中的酸类、酚类以及其他类相对含量均为最高,经过接菌后的5组发酵辣椒样品的醇类与酯类挥发性气味物质的相对含量都较P-KB(空白组)样品有所增加,其中PZ-2.371样品中挥发性醇类物质相对含量最高(72.07%),最低的则是PB-1.3220样品(43.8%),酯类物质最高的样品是PB-1.322样品(38.35%),P-KB样品中的酸类、酚类以及其他类较其他样品相对含量均为最高。结合表2可得,接入菌种的样品组中乙醇是导致醇类物质上升的主要成分,PZ-2.371样品中乙醇的相对含量最高达到53%,其次是PL-1.555样品(41.7%),此外如异戊醇这类具有不良风味的物质较P-KB样品(14.85%)有所下降,但至于为何接如菌株后,乙醇存在大幅度上升,还需进一步研究讨论。酯类物质中增加幅度较大的有十四酸乙酯、油酸乙酯、亚油酸乙酯、十六酸乙酯等,其中十四酸乙酯又称肉豆蔻酸乙酯,是由肉豆蔻酸与乙醇酯化反应而来,具有有鸢尾油香气,并带有油脂气息[17],亚油酸乙酯还具有降低血液中胆固醇和血脂的作用。
表2 菌种发酵辣椒酱样品中挥发性成分的种类和含量
Table 2 Types and contents of volatile components in fermented pepper sauce samples by different strains
不同发酵辣椒酱样品挥发性香气成分的UpSet软件分析结果见图3。由图3可知,左边水平柱状图表示各分组的元素统计数值,中间矩阵中的单个点表示某个分组特有的元素,点和点之间的连线表示不同分组特有的交集,竖直柱状图中则分别表示对应的交集元素数值。由图3亦可知,6个样品中共有的挥发性物质14种,PL-1.555、PL-1.3919、PZ-2.371、PZ-2.1939、PB-1.3220、P-KB发酵各样品中所特有的物质分别有11种、8种、6种、10种、6种、10种,各原始物质数量以PL-1.555样品最多(49种),其次则是PL-1.3919和PZ-2.371样品均为48种。结果表明,通过接入不同菌株发酵后的盐渍辣椒,在发酵过程中都形成了各自独特的风味物质,且风味物质种类均多于未接菌的样品(P-KB),证明接菌发酵有助于产品的风味的形成。
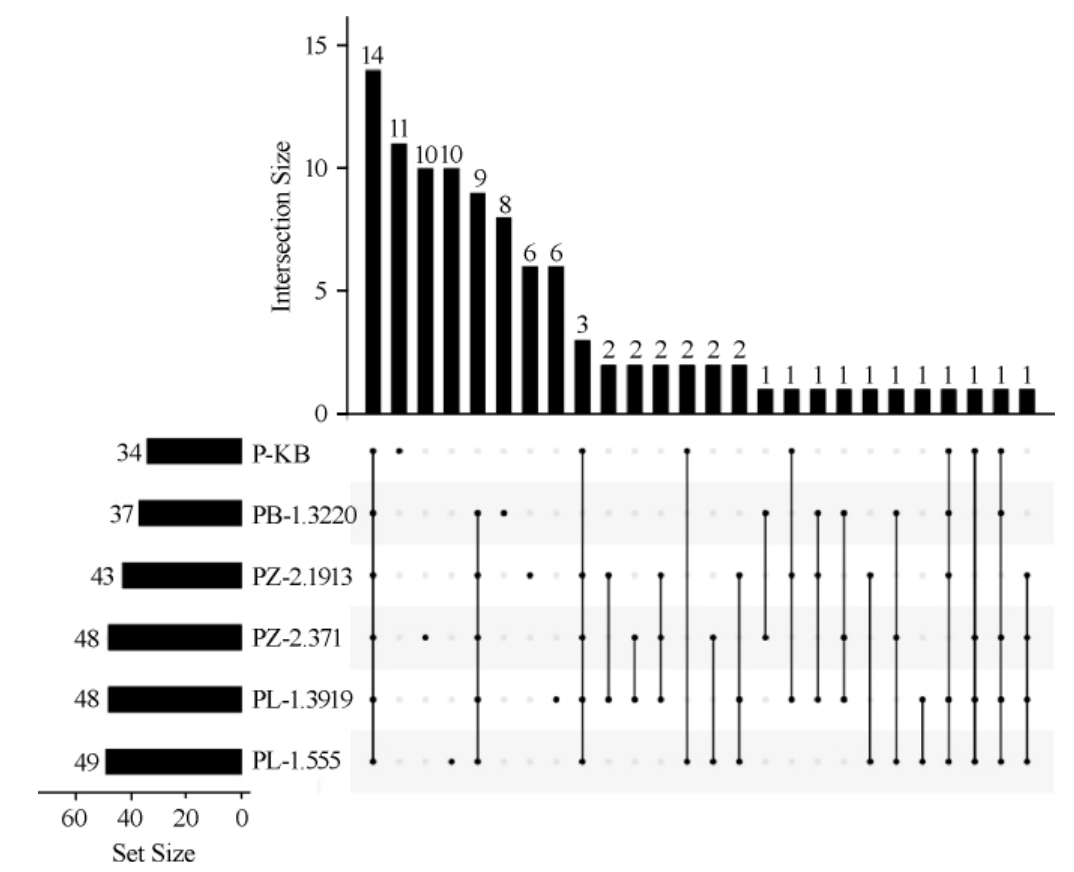
图3 不同发酵辣椒酱样品挥发性香气成分的UpSet分析结果
Fig.3 UpSet analysis results of volatile components in different fermented pepper sauce samples
共有的14种挥发性气味物质中,其中以酯香物质种类(8种)最为丰富,说明发酵辣椒中酯类挥发性物质担任关键的角色,5组接菌发酵的辣椒样品中,醇类和酯类较空白组样品(P-KB)明显增加,这表明接入的菌种通过代谢加强了发酵辣椒中醇类和酯类挥发性物质的释放。共同的醇类物质中芳樟醇具有花香、木香、柑橘香、浆果香、玫瑰香,2,3-丁二醇则具有甜香、奶香[17];酯类化合物气味浓郁,香气持久,低分子质量的酯类一般具有芳香气味或特定水果香味,共有的酯类物质有水杨酸甲酯、十二酸乙酯、十六酸乙酯、9-十六碳烯酸乙酯、二氢猕猴桃内酯、亚油酸甲酯、亚麻酸乙酯、亚油酸乙酯,其中水杨酸甲酯具有果香和花香的气味,亚油酸乙酯具有降血脂功效,这类物质常在发酵后期中由酸和醇经酯化反应生成[18-19];异丁酸、4-甲基戊酸是共有酸类物质为,酸类物质不仅对发酵辣椒提供了酸味,同时也提供了香气,其中PB-1.3220、PZ-2.371、PL-1.555样品中的2-甲基丁酸拥有果香、奶酪、酸性的乳制品的香气[20];共有酚类物质为愈创木酚,其具有烟熏香、焦香、蒸粮香香味[21],PZ-2.371和PL-1.3919样品中含量较高。
2.2 主成分分析
由图4可知,PC1解释了数据集中总方差贡献率的69.7%,而PC2解释了17.25%。由于横纵坐标的刻度线表示样品之间的距离,P-KB与PB-1.3220样品相距较远以外,其余4个样品均聚集在横坐标(0.5-1.0)纵坐标(0.0-1.0)的区域,其中样品PZ-2.1913与PL-1.3919、样品PL-1.555与PZ-2.371两两相近,说明靠近的样品在挥发性物质种类和含量方面均相似。另外植物乳杆菌是同型乳酸发酵,酵母菌是产香型菌株,一般以用于酱料发酵中产生酱香。
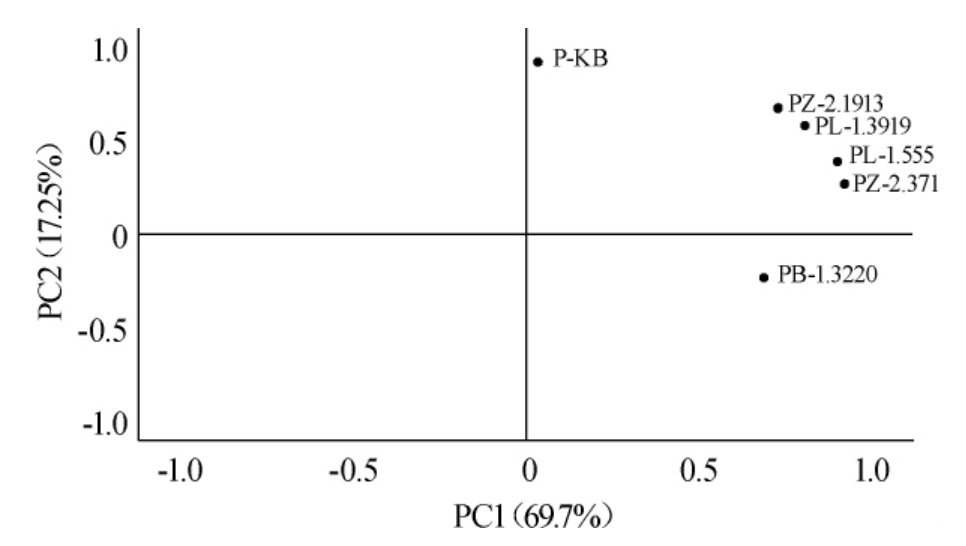
图4 挥发性香气成分的主成分分析
Fig.4 Principal component analysis of volatile components
3 结论
综上所述,发酵辣椒酱中气味成分物质丰富,在所有样品中共检测出100种挥发性物质,其中包括醇(19种)、酯(41种)、酸(10种)、酚(8种)、酮(3种)、其他(19种)。接菌后的所有样品中挥发性物质种类均高于未接菌样品P-KB,以PL-1.555样品最多(49种),其次为样品PL-1.3919和PZ-2.371均为48种,共有的挥发性物质为14种,以酯类物质种类(8种)最为丰富。样品PL-1.3919中的醇类和酚类物最为丰富,样品PL-1.555(20种)中酯类物质数量最多,其次为样品PL-1.3919(19种)。由于挥发性物质种的多少是构成发酵辣椒产品具有优良风味的重要因素之一,此外醇类和酯类物质也在发酵辣椒中起到关键性的作用,因此认为菌株1.3919更适合接入盐渍辣椒汁发酵干辣椒。
[1]邢玉晓,刘方菁,丁涌波,等.石柱主栽朝天红辣椒腌制加工适性研究[J].食品工业科技,2015,36(12):113-121.
[2]赵玲艳,黄嘉欣,杨剑,等.盐渍辣椒细菌多样性分析[J/OL].食品科学,2020,41(20):105-111.
[3]LAMA K,ALKALAI-TUVIA S,PERZELA Y,et al.Nutritional qualities and aroma volatiles of harvested red pepper fruits stored at suboptimal temperatures[J].Sci Hortic-Amsterdam,2016,213:42-48.
[4]LEE D E,SHIN G R,LEE S,et al.Metabolomics reveal that amino acids are the main contributors to antioxidant activity in wheat and rice gochujangs(Korean fermented red pepper paste)[J].Food Res Int,2016,87:10-17.
[5]TANIA A C,ISMAEL D S G,DE MELO L A M P,et al.Carotenoid and total vitamin C content of peppers from selected Brazilian cultivars[J].J Food Compos Anal,2017,57:73-79.
[6]龚永强,甘增鹏,廖卢艳,等.市售剁辣椒脆性品质评价研究[J].中国酿造,2019,38(10):40-43.
[7]WANG J,WANG R,XIAO Q,et al.Analysis of bacterial diversity during fermentation of Chinese traditional fermented chopped pepper[J].Lett Appl Microbiol,2019,69(5):346-352.
[8]韩俊燕,赵国忠,赵建新,等.发酵辣椒细菌多样性的16S rDNA 测序分析[J].中国食品学报,2018,18(5):246-251.
[9]MORALES-SORIANO E,KEBEDE B,UGÁS R,et al.Flavor characterization of native Peruvian chili peppers through integrated aroma fingerprinting and pungency profiling[J].Food Res Int,2018,109:250-259.
[10]罗凤莲,夏延斌,王燕,等.脱盐盐渍辣椒发酵工艺优化及风味品质研究[J].湖南农业大学学报(自然科学版),2017,43(1):71-78.
[11]王万程,赵玲艳,邓放明.红线椒与盐渍辣椒汁复合发酵工艺优化[J].食品与机械,2018,34(3):211-219.
[12]杜卫华,陈移平,鲍华军,等.陈泡辣椒汁接种腌渍辣椒的发酵工艺[J].浙江农业科学,2018,59(2):318-321.
[13]卢星军.辣椒汁工业化生产技术研究及应用[D].长沙:湖南农业大学,2015.
[14]韩亚楠,程方方,武亚婷,等.辣椒酱发酵菌肠膜明串珠菌C27 高密度培养条件优化[J].中国酿造,2020,39(3):99-103.
[15]李文青,罗凤莲,曾希珂,等.多菌种接种发酵生产低盐剁辣椒的工艺优化[J].现代食品科技,2019,35(1):206-214.
[16]IRANMANESH M I,EZZATPANAH H,AKBARI-ADERGANI B,et al.SPME/GC-MS characterization of volatile compounds of Iranian traditional dried Kashk[J].Int J Food Prop,2017,21(1):1067-1079.
[17]孙宝国.食用调香术[M].北京:化学工业出版社,2003:690-740.
[18]梁娟.湖南省发酵碎鲜辣椒香气成分的检测与分析[D].长沙:湖南农业大学,2014.
[19]杨芳,杨莉,粟立丹.基于电子鼻和气相-离子迁移谱对美人椒酱的风味分析[J].食品工业科技,2019,40(23):193-206.
[20]王雪梅,孙文佳,李亚隆,等.不同产地鲜辣椒发酵郫县豆瓣的品质分析[J].食品科学,2020,41(10):213-221.
[21]孙小静,王雪雅,蓬桂华,等.不同辣椒品种对辣椒酱发酵品质的影响[J].中国酿造,2017,36(9):55-59.