北五味子性温,可收敛固涩、益气生津与补肾宁心[1],果实中有大量的多糖、木脂素、花色苷、多酚等功能性成分[2-3],其具有治疗代谢综合征、辅助睡眠等作用[4-7]。由于北五味子特殊的药用价值,已成为国内外研究的热点,关于五味子低醇饮料[8]、五味子米酒[9]、五味子麦芽酵素[10]、五味子发酵果酱[11]以及五味子发酵物的抗炎作用[12]等更是进行了深入的研究。但是,由于北五味子过高的酸度[13-15],使得其相关产品的开发受到了很大程度的限制。目前,化学降酸法被广泛的应用于北五味子果汁的降酸,虽然其降酸的效果显著,但严重制约了其口感、色泽与气味等,还未见报道关于北五味子汁的生物降酸法。
苹果酸-乳酸发酵(malolactic fermentation,MLF)主要是在乳酸菌(lactic acid bacteria,LAB)作用下,通过苹果酸-乳酸酶将更为酸涩的L-苹果酸脱羧基降解为更加柔和的L-乳酸,同时伴随二氧化碳的产生[16],从而降低发酵饮品的酸度。
本研究将酒酒球菌(Oenococcus oeni)应用在北五味子汁的苹果酸-乳酸发酵过程中,研究了接种量、发酵温度、发酵时间及初始pH对其降酸的影响,并对比降酸前后的抗氧化指标,旨在最大限度保留北五味子功能成分,同时更加安全与有效地降低其果汁酸度。
1 材料与方法
1.1 材料与试剂
北五味子鲜果:吉林长白山制药有限责任公司;酒酒球菌(Oenococcus oeni)6066:中国工业微生物菌种保藏管理中心;NaHCO3(食品级):市售;活化培养基、无水醋酸钠、2,4,6-三吡啶基三嗪、浓盐酸、氯化铁、硫酸亚铁:哈尔滨盛世天泽生物科技有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)、2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(2,2'-azinobis-(3-ethylbenzthiazo line-6-sulphonate,ABTS)、2-D-脱氧核糖:美国Sigma公司;L-苹果酸测定试剂盒:北京百奥康生物技术有限公司。本研究所用试剂均为食品级或分析纯。
1.2 仪器与设备
PHS-3C数显台式pH计:安徽赛科环保科技有限公司;SW-CJ-1D超净工作台:上海舍岩仪器有限公司;LRH-70F生化培养箱:无锡玛瑞特科技有限公司;723N可见分光光度计:杭州俊升科学器材有限公司。
1.3 方法
1.3.1 北五味子汁苹果酸-乳酸发酵工艺流程及操作要点
北五味子→榨汁→调节pH→灭菌→冷却→接种酒酒球菌→发酵→发酵液
操作要点:
北五味子果汁制备:选取新鲜北五味子,除去霉烂部位与次果,去籽,以1∶1比例加入饮用水,使用榨汁机打浆。
初始pH调节:使用1.0mol/LNaHCO3溶液调节pH达到3.4。灭菌:将其置于水浴环境为65 ℃条件下处理30 min。接种:将购买的酒酒球菌6066接种到制备的斜面培养基上,37 ℃培养12 h,连续传代3次,随后接入液体培养基中,按平板菌落计数法测得其活菌数约为2×108 CFU/mL。按照果汁7%的体积接种。
发酵:将样品置于24 ℃条件下发酵8 d,得到成品。
1.3.2 北五味子汁苹果酸-乳酸发酵工艺参数优化单因素试验
(1)接种量对北五味子汁MLF的影响
将北五味子汁pH调整为3.4,分别接种3%、5%、7%、9%、11%的酒酒球菌,24 ℃条件下发酵8 d,发酵结束后检测苹果酸含量,探究不同接种量对发酵结果的影响。
(2)发酵温度对北五味子汁MLF发酵结果的影响
将北五味子汁pH调整为3.4,接种量为7%,调整发酵温度分别为20 ℃、22 ℃、24 ℃、26 ℃、28 ℃,发酵8 d,发酵结束后检测苹果酸含量,探究不同发酵温度对发酵结果的影响。
(3)发酵时间对北五味子汁MLF发酵结果的影响
将北五味子汁pH调整为3.4,接种量为7%,调整发酵温度为24 ℃,选取发酵时间为6 d、7 d、8 d、9 d、10 d进行MLF发酵,发酵结束后检测苹果酸含量,探究不同发酵时间对发酵结果的影响。
(4)初始pH对北五味子汁MLF发酵结果的影响
将北五味子汁pH调整为3.4,接种量为7%,发酵温度为24℃时,分别调整初始pH为2.8、3.1、3.4、3.7、4.0发酵8d,发酵结束后检测苹果酸含量,探究不同初始pH对发酵结果的影响。
1.3.3 北五味子汁苹果酸-乳酸发酵工艺参数优化正交试验
按照Box-Behnken的试验设计原理,以苹果酸降解率(R)为响应值,选择五味子汁MLF的接种量(A)、发酵温度(B)、发酵时间(C)、初始pH(D)为影响因素,进行3因素3水平Box-Behnken试验,因素与水平见表1。
表1 Box-Behnken试验因素与水平
Table 1 Factors and levels of Box-Behnken experiments

1.3.4 指标检测
(1)L-苹果酸的检测
总苹果酸的检测通过L-苹果酸测定试剂盒测定,苹果酸降解率计算公式如下:
苹果酸降解率=(1-C/C0)×100%
式中:C为发酵后苹果酸含量(以苹果酸计),mg/L;C0为空白组,即未经发酵的五味子汁中L-苹果酸含量,mg/L。
(2)DPPH自由基清除率的测定
取0.2 mL溶液,添加2.8 mL的0.2 mmol/L DPPH溶液,混匀,室温放置30 min,波长517 nm处测定吸光度值。甲醇作为调零管,样品加DPPH为样品组AS,甲醇替代提取液作为空白组A0[17]。DPPH自由基清除率计算公式如下:
(3)还原力的测定
取相同体积待测样品、1%的铁氰化钾溶液与0.02 mol/L的磷酸缓冲盐溶液(phosphate buffer saline,PBS)(pH 6.6),将其充分混匀,50 ℃处理20 min。待其冷却后,添加10%的三氯乙酸(trichloroacetic acid,TCA)溶液0.5mL,离心(3000r/min,8 min),取上清液、蒸馏水0.1%的三氯化铁溶液,以1∶1∶1体积充分混匀,静置5min,在波长700nm处测定吸光度值。以L-半胱氨酸盐酸盐(50~300 μmol/L)标准曲线计算,以μmol/L表示[18]。
(4)铁离子还原能力的测定
取0.3 mmol/L的醋酸钠缓冲液(pH 3.6)、0.01 mmol/L的2,4,6-三(2-吡啶基)三嗪(2,4,6-tripyridin-2-yl-1,3,5-triazine,TPTZ)-HCl溶液、0.02 mmol/L的FeCl3溶液以10∶1∶1混合配成工作液。添加0.1 mL待测样品,3 mL铁离子还原法(ferric ion reducing antioxidant power,FRAP)工作液(提前37 ℃水浴处理),添加0.3 mL去离子水,立即混匀,37 ℃水浴7 min,在波长593 nm处测定其吸光度值,以FeSO4(0.025~0.400 mmol/L)作为标准曲线,以mmol/L FeSO4表示[18]。
(5)ABTS自由基清除率的测定
取7 mmol/L的ABTS溶液10 mL与7.35 mmol/L的过硫酸钾溶液5 mL避光放置16 h,作为ABTS+·溶液。利用无水乙醇稀释适当浓度,波长734 nm处测定其吸光度值Ac,要求在0.70±0.02左右。将15 μL样品与2.8 mL的ABTS+·溶液混匀,放置6 min后,波长734 nm处测定吸光度值As[17]。
1.3.5 数据分析
通过Origin8.6绘制图,SPSS V17.0软件进行显著性分析(P<0.05),每组试验重复3次。
2 结果与分析
2.1 接种量对北五味子汁发酵的影响
由图1可知,随着酒酒球菌接种量的增大,苹果酸降解率呈现出先增大后减小的趋势,在接种量为7%时达到最大,接种量继续增大则苹果酸降解率有轻微下降趋势。可能是由于北五味子汁中的营养素含量有限,接种量过大在MLF前期可使得菌种迅速增加,但后期会由于体系中的养分无法充分提供,进而使得菌株大量死亡,造成降解率有所下降。因此最佳接种量为7%。
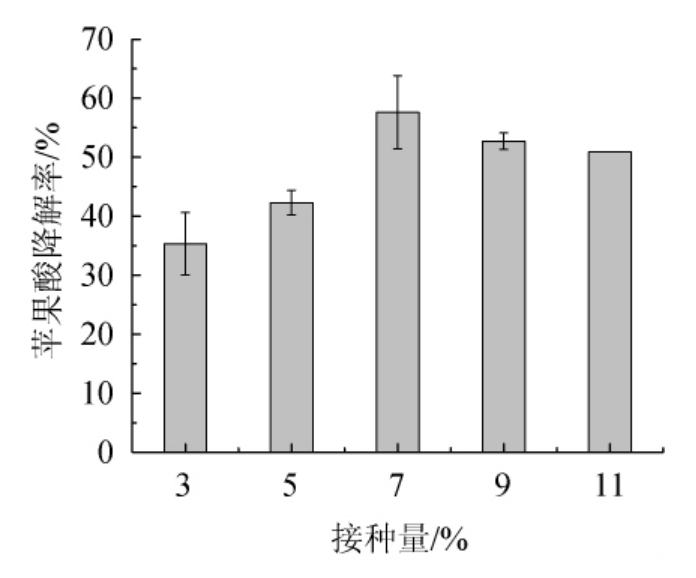
图1 接种量对苹果酸降解率的影响
Fig.1 Effect of inoculum on malic acid degradation rate
2.2 发酵温度对北五味子汁发酵的影响
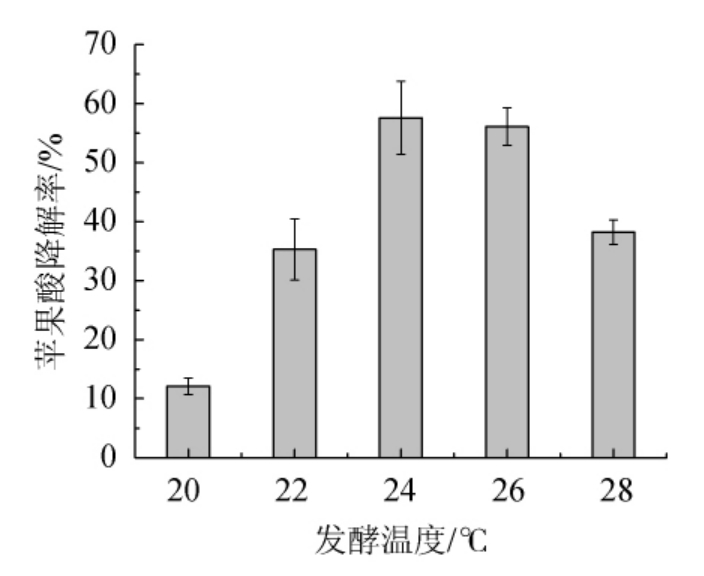
图2 发酵温度对苹果酸降解率的影响
Fig.2 Effect of fermentation temperature on malic acid degradation rate
由图2可知,随着发酵温度升高,苹果酸降解率增大,发酵温度达到24 ℃时,降解率最大,继续升高发酵温度苹果酸降解率呈减小趋势。可能是因为酒酒球菌的生长对温度较为敏感,环境温度较低时,菌株无法充分的生长,使得产酶量与酶活力都较低,导致降酸效果不理想。随着温度升高,酶活力也同样升高,但环境因为温度过高和过低都不是乳酸菌的适宜生长和代谢温度进而导致其MLF发酵效果变差。因此最佳发酵温度为24 ℃。
2.3 发酵时间对北五味子汁发酵的影响
由图3可知,随着发酵时间的延长,苹果酸降解率呈先增大后减小的趋势,当发酵时间为8 d时,苹果酸降解率最高,当发酵时间超过8 d时,降解率有所下降,过长时间的MLF会使得其他微生物污染反而会增加风险,因此,选择发酵时间为8 d。
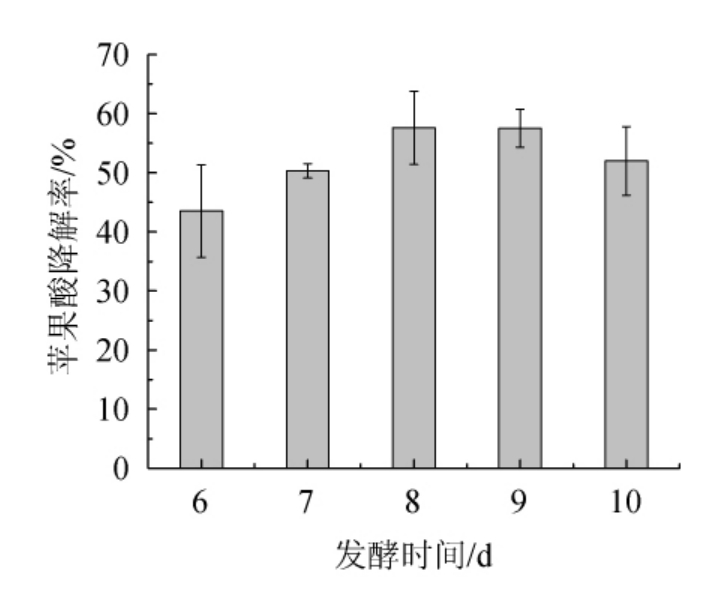
图3 发酵时间对苹果酸降解率的影响
Fig.3 Effect of fermentation time on malic acid degradation rate
2.4 初始pH对北五味子汁发酵的影响
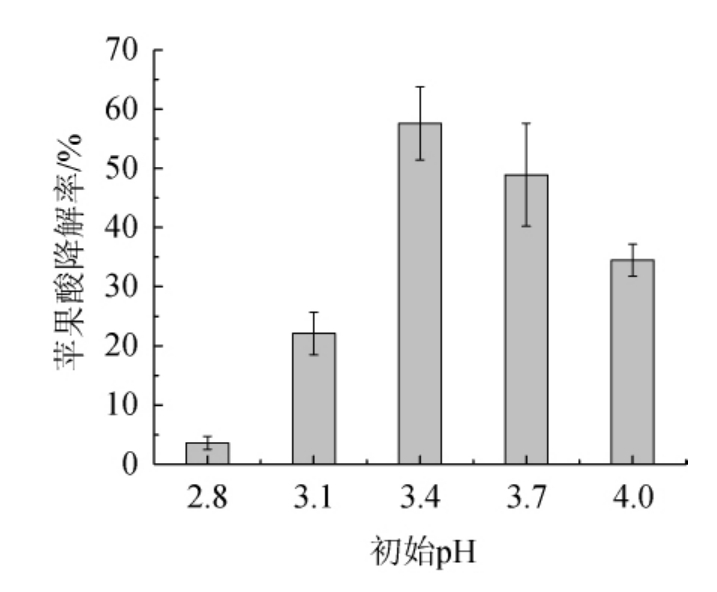
图4 初始pH对苹果酸降解率的影响
Fig.4 Effect of initial pH on malic acid degradation rate
由图4可知,随着初始pH的增大苹果酸降解率呈现出先增大后减小的趋势,且初始pH为3.4时降解率达最大,过低的初始pH会抑制酒酒球菌的生长,使得苹果酸降解率下降,而过高的初始pH可能会影响酒酒球菌产酶的能力[19-20],使得苹果酸的降解率有所下降。因此最佳初始pH为3.4。
2.5 北五味子汁苹果酸-乳酸工艺参数优化正交试验
在单因素试验的基础上,选取酒酒球菌接种量(A)、发酵温度(B)、发酵时间(C)、初始pH(D)为影响因素,以苹果酸降解率(R)为响应值,采用4因素3水平的响应曲面试验考察各发酵条件对发酵效果的影响,试验设计与结果见表2。
通过统计分析软件Design-Expert 8.0.6对表2数据进行分析,建立回归模型如下:
R=58.72-3.19A-1.34B-1.14C+2.33D+0.050AB+3.05AC+4.82AD-1.10BC+3.43BD+2.12CD-20.80A2-14.25B2-7.33C2-7.10D2
由表3可知,响应面优化拟合出的方程回归项极显著(P<0.000 1),且失拟项0.164 6>0.05,说明响应值预测良好。拟合模型方程的决定系数R2=97.28%,表明所建立的模型可以用来解释97.28%的响应变化,调整决定系数R2Adj=94.55%,说明该模型能解释94.55%响应值的变化,拟合程度较好,以上指标均能证明该拟合方程有较好的拟合效果。由F值大小得出影响因素影响程度由高至低依次为A>D>B>C,即接种量>初始pH>发酵温度>发酵时间。两两因子的相互作用对于响应值影响的响应面分析如图5所示。
表2 发酵条件优化响应面试验设计及结果
Table 2 Design and results of response surface experiments for fermentation condition optimization
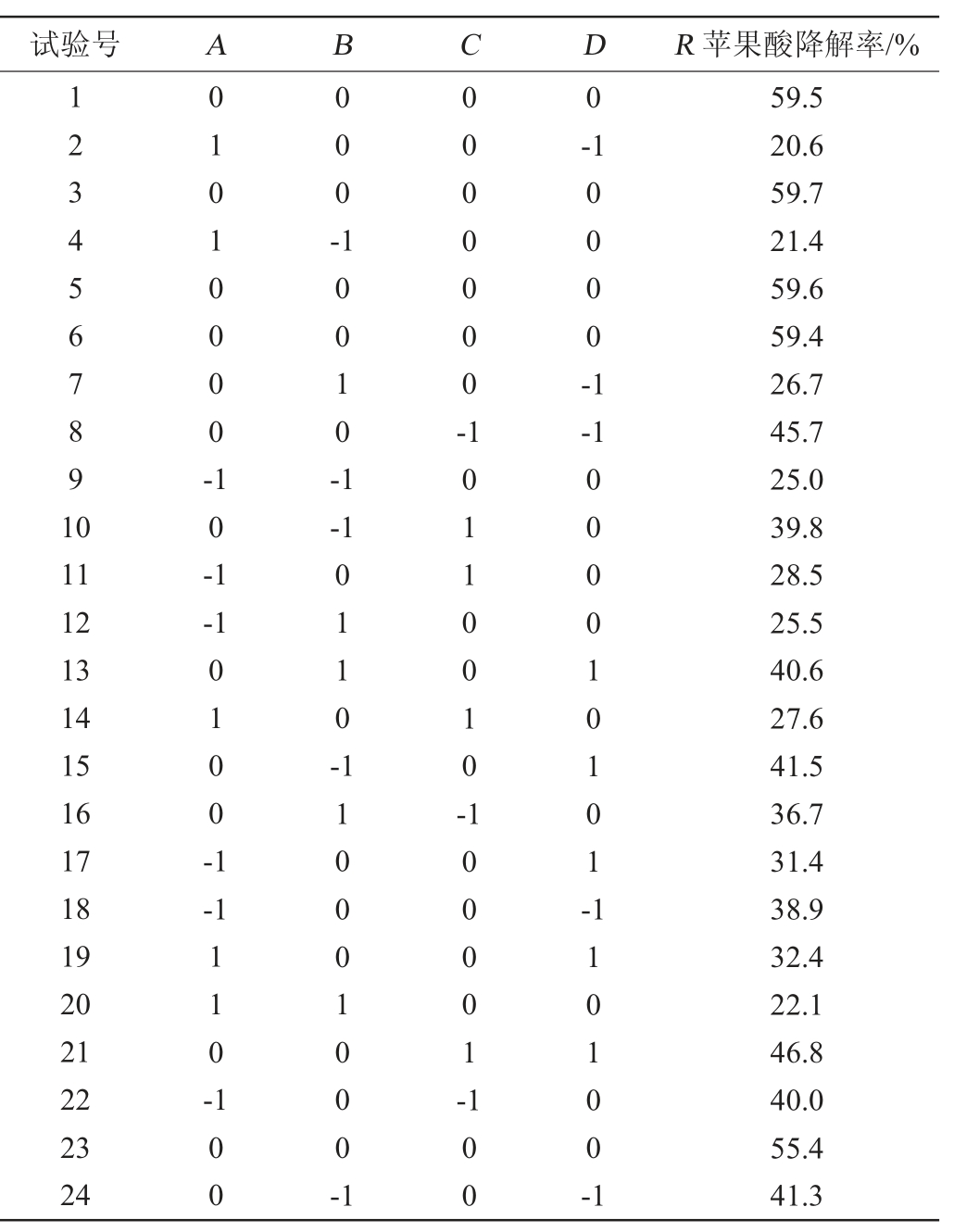
续表
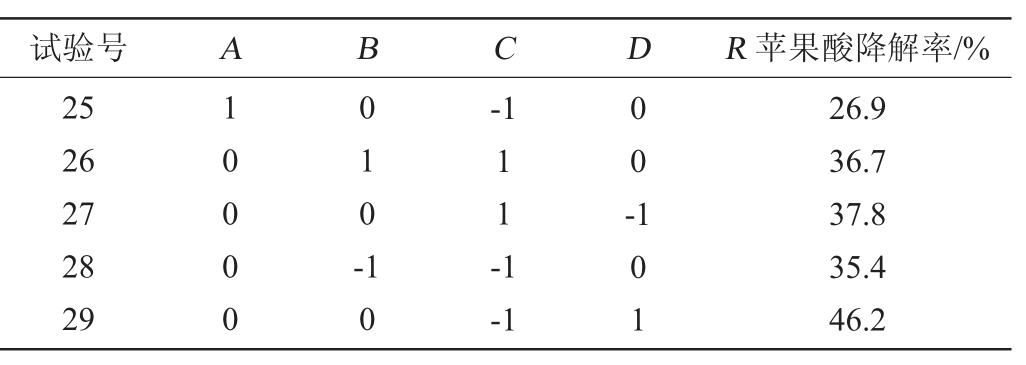
表3 响应面试验结果方差分析
Table 3 Variance analysis of response surface experiment results
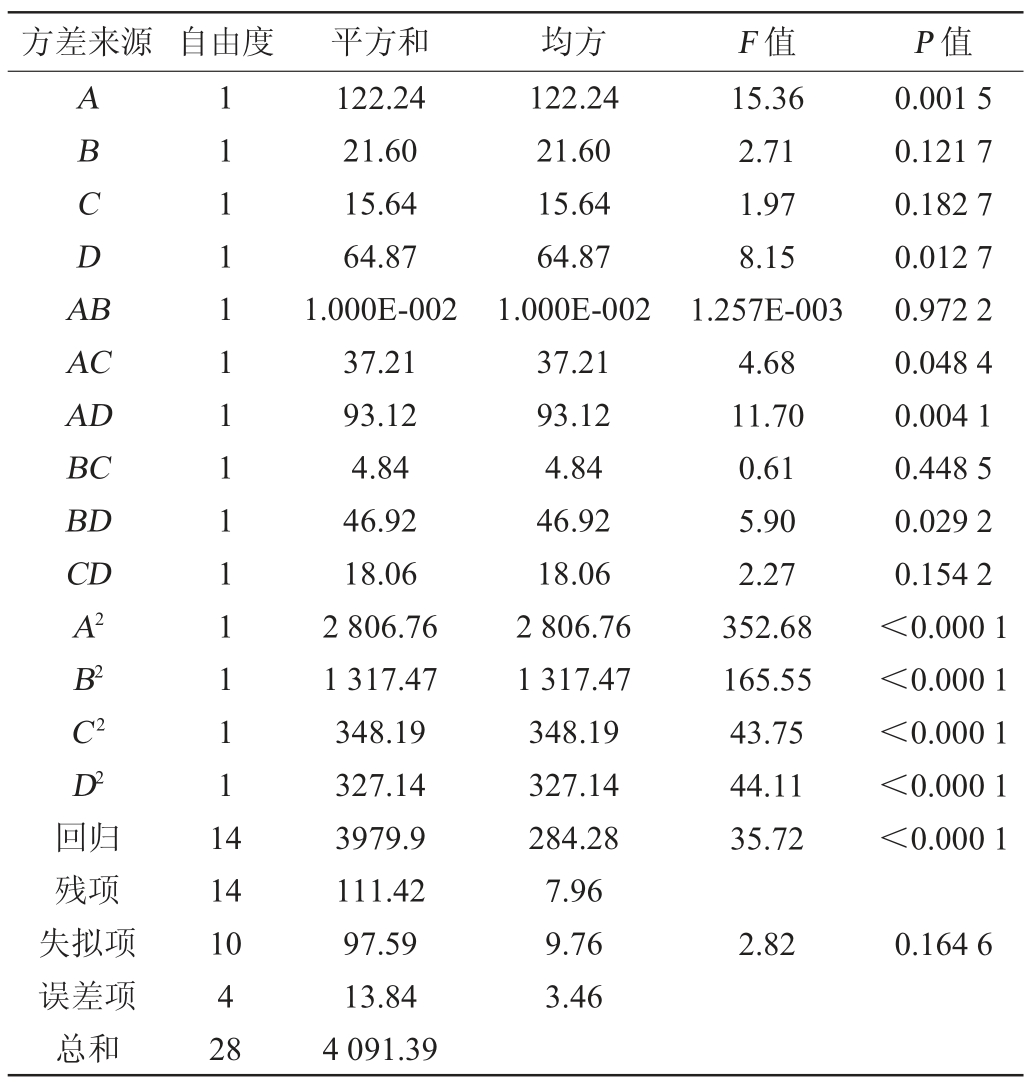

图5 各因素交互作用对苹果酸降解率影响的响应面和等高线
Fig.5 Response surface plots and contour lines of effects of interactions between each factors on malic acid degradation rate
应用响应面寻优分析方法对回归模型进行描述,接种量、发酵温度、发酵时间、初始pH和对应的编码值分别为-0.068、-0.030、-0.073和0.122。寻找最优发酵工艺参数为:酒酒球菌接种量6.93%、发酵温度23.97 ℃、发酵时间7.46 d、初始pH 3.44,在此条件下,苹果酸降解率预测值为59.03%。但考虑实际的操作情况,将发酵工艺参数调整为酒酒球菌接种量7%、发酵温度24 ℃、发酵时间8 d、初始pH 3.4。
根据拟合条件进行验证性试验,3组平行试验的苹果酸降解率实际值为59.00%,与理论预测值仅相差0.03%。因此,采用响应面分析法优化得到的北五味子汁MLF工艺条件参数准确可靠,实用价值较高。
2.6 北五味子汁MLF前后抗氧化活性对比
通过以上最优工艺进行北五味子汁MLF,检测发酵前后DPPH自由基清除率、还原力、铁离子还原能力(ferric ion reducing antioxidant power,FRAP)、ABTS自由基清除率等指标的变化,结果见表4。
表4 苹果酸-乳酸发酵前后抗氧化活性对比
Table 4 Comparison of antioxidant activity before and after malolactic fermentation
注:“**”表示MLF后与MLF前相比差异极显著(P<0.01)。
由表4可知,当北五味子汁经过MLF后,DPPH自由基清除率是发酵前的1.22倍,还原力是发酵前的1.444倍,FRAP是发酵前的1.03倍,ABTS自由基清除率是发酵前的1.10倍。除还原力提高不显著外(P>0.05),其余均显著性提高(P<0.01)。
当北五味子汁经过MLF后,酚酸物质含量有所增加,由于在酚酸分子结构上的羟基具有较强的还原力与亲核力,使得其具备了抗氧化活性,其分子中羟基的数量决定了其抗氧化能力的高低[20];不仅如此,经过MLF发酵后,部分黄酮类化合物的含量也会有所增加,而存在于北五味子汁中的一些游离花色苷可以与其他多酚类物质相结合而产生的辅色素同样使得北五味子汁黄酮类化合物的含量增加。因此,MLF可通过提高北五味子汁中黄酮类物质的含量来发挥对人体有益的作用。
需要进一步探究的是,有大量的多酚类物质、非多酚类物质、矿物质和酶存在于北五味子中,酒酒球菌究竟是如何与这些物质相互作用的还有待研究。
3 结论
在北五味子汁苹果酸-乳酸发酵过程中,发酵温度、发酵时间、初始pH会对其降酸工艺有一定影响,可以通过苹果酸的降解率判定降酸效果;通过响应面优化可以得出最优工艺条件为酒酒球菌接种量7%、发酵温度24 ℃、发酵时间8 d、初始pH 3.4。此优化条件下,北五味子汁经过苹果酸-乳酸发酵后,苹果酸降解率为59%。通过对比北五味子汁苹果酸-乳酸发酵前后的抗氧化指标,得出北五味子汁通过苹果酸-乳酸发酵更有利于其抗氧化活性成分的保持与提高抗氧化能力。
[1]闫舒,仰榴青,赵婷,等.五味子多糖的最新研究进展[J].江苏大学学报(医学版),2009,19(4):366-368.
[2]KWAK H J,PARK S,YOO G,et al.Chemical constituents from the fruits of Schisandra sphenanthera and their cytotoxicity activity[J].Rev Bras Farmacogn,2019,29(5):578-581.
[3]吴夏,张盛,景浩.随机质心映射优化法在五味子多酚优化提取中的应用[J].食品科学,2012,33(22):341-347.
[4]解琦,张群,谷烨,等.北五味子药用价值研究进展[J].特种经济动植物,2020,23(3):25-26.
[5]陶雪,车金营,杨硕,等.五味子多糖对2 型糖尿病大鼠肝脏的保护作用[J].北华大学学报(自然科学版),2019,20(1):43-46.
[6]LASIK M.The application of malolactic fermentation process to create goodquality grape wine produced in cool-climate countries:a review[J].Eur Food Res Technol,2013,237(6):843-850.
[7]常世敏,李乾丽,谢婵媛,等.黑米与欧洲越橘花色苷抗氧化活性比较研究[J].食品工业科技,2019,40(9):57-61,67.
[8]张晟,马雪,李杨,等.五味子果渣低醇饮料发酵工艺优化[J].食品工业,2020,41(6):175-179.
[9]董佳萍,颜飞翔,牛广财,等.北五味子麦芽酵素发酵工艺优化及其生物活性初探[J].食品工业,2020,41(5):31-34.
[10]刘洋.响应面优化北五味子米酒发酵工艺研究[J].中国酿造,2019,38(7):194-199.
[11]王晨.五味子皮渣乳酸发酵复合果酱发酵工艺及品质特性研究[D].长春:吉林农业大学,2017.
[12]NAM H H,KIM H J,CHOI N J,et al.A comparison of antioxidant activity from Schisandra chinensis water extracts depending on stir-frying and stirfrying with liquids process[J].Kor J Organ Agr,2015,23(4):987-997.
[13]杨炳友,郑桂雪,郭江涛,等.五味子藤茎的化学成分研究[J].中医药信息,2016,33(4):7-10.
[14]杜庆波.中药五味子的化学成分研究新进展[J].河套学院学报,2015,12(2):92-95.
[15]李丽,肖永庆,于定荣,等.HPLC 测定五味子中3 种有机酸的含量[J].中国中药杂志,2011,36(23):3286-3289.
[16]ASSAR S H,MOLONEY C,LIMA M,et al.Determination of N (E>)-(Carboxymethyl) lysine in food systems by ultra performance liquid chromatography-mass spectrometry[J].Amino Acids,2009,36(2):317-326.
[17]李小娟,李明笑,聂钰洪,等.外源h_2s 对货架及低温下采后草莓果实抗氧化活性的影响[J].食品工业科技,2019,40(11):291-296.
[18]RICE-EVANS C A,MILLER N J,PAGANGA G.Structure-antioxidant activity relationships of flavonoids and phenolic acids[J]. Free Rad Biol Med,1996,20(7):933-956.
[19]李维新.优良MLF 乳酸菌选育及其产酶特性研究与应用[D].福州:福建农林大学,2012.
[20]刘晓娇.不同因素对酒酒球菌苹果酸—乳酸发酵的影响[D].杨凌:西北农林科技大学,2011.