中国酒文化源远流长,自酒问世以来,始终作为一种情感交流的载体,展现独特的消费理念和神奇魅力。随着社会经济的发展进步,物质文化水平的提高,人们对白酒的消费更加走向理性化,对白酒品质提出了更高的要求,不仅要满足饮时激活人体精神,而且更加注重饮后的体征感受,具体来说要“饮时爽口,饮后醉的慢,醒得快,酒后不干口、不上头”[1-2]。对于白酒饮用舒适度的研究主要方式为专家评判,但人工评判主观性过强,效率较低。张梦妍等[3]已初步建立白酒饮用舒适度评价模型,根据醉酒昏睡期小鼠的醉酒时间、醒酒时间对白酒饮用舒适度进行了评价,并成功应用于多种白酒的测定,但是由于醉酒阶段指标测定的影响因素较多,实验结果的准确度、精密度较差,因此该评价模型的进一步优化问题亟待解决。目前有研究依据乙醇在体内的代谢差异,将急性醉酒分为三个阶段:兴奋期、共济失调期及醉酒昏睡期[4-5],提示针对醉酒不同阶段进行研究的可能性,有研究者以此为基础对白酒饮用舒适度评价模型进行了优化[6]。
在急性醉酒的三个阶段中,共济失调期常伴随明显的肢体不稳、动作不协调等症状[5]。研究表明,急性醉酒共济失调是由于过量摄入乙醇造成的脑组织氧化损伤[7],但共济失调发生机制复杂,影响因素较多,且我国复杂的白酒酿造工艺赋予了酒体除乙醇外的众多有利微量成分[8]。相比于静态昏睡期,共济失调阶段动态的行为学表现则更能直观准确地体现实验动物的生理状态,展现白酒饮用舒适度,且目前未见不同白酒对共济失调效应是否会产生不同影响的研究。故本研究以优化的动物行为学实验为基础,结合乙醇代谢、急性损伤、氧化损伤等生理生化指标,在共济失调阶段比较分析不同白酒对醉酒小鼠的影响,探究白酒饮用舒适度评价指标灵敏度,弥补研究空白,为进一步优化白酒饮用舒适度动物评价模型提供数据支撑,奠定实验基础,同时对不同白酒导致不同共济失调效应的原因进行初步探索。
1 材料与方法
1.1 材料与试剂
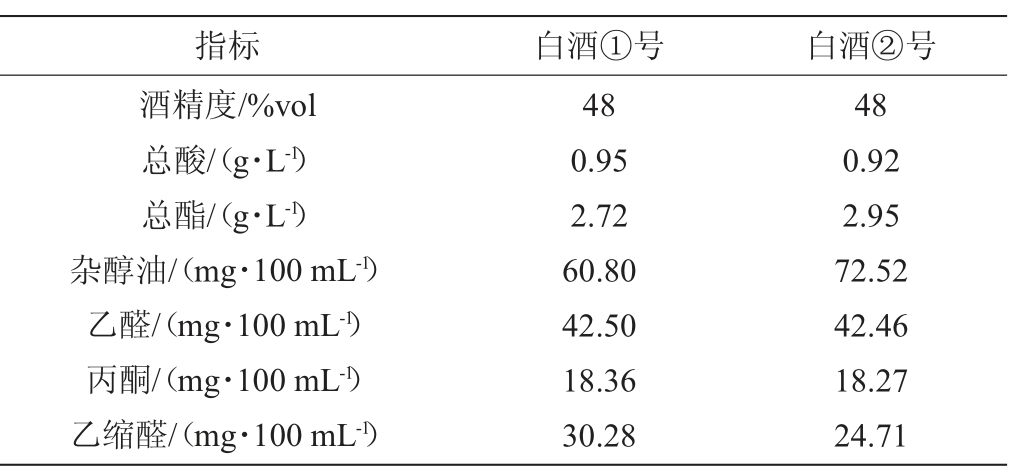
2种白酒(酒精度48%vol)(编号分别为①号、②号):由四川省绵阳市丰谷酒业有限公司提供,主要理化指标分析结果见表1。
表1 2种白酒主要理化指标分析结果
Table 1 Results of main physical and chemical indexes analysis of 2 Baijiu samples
无特定病原体(specific pathogen free,SPF)级Balb/c小鼠(雄性,日龄(42~48 d)):由北京维通利华实验动物有限技术公司提供(许可证号:SCXK(京)2016-0011)。独立通风笼具(individually wentilate cagesdul,IVC)饲养,环境温度20~22℃,相对湿度60%~70%,由四川大学华西公共卫生学院实验动物中心提供(使用许可证号:SYXK(川)2018-011)。
乙醇(分析纯):成都海兴化工试剂厂;乙醛测定试剂盒:爱尔兰Megazyme公司;神经特异性烯醇化酶(neuronspecific enolase,NSE)酶联免疫检测试剂盒:上海酶联科技生物有限公司;肝素试剂、超氧化物歧化酶(superoxide dismutase,SOD)测定试剂盒、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-PX)测定试剂盒、脂质过氧化物(lipid peroxidation,LPO)测定试剂盒、丙二醛(malondialdehyde,MDA)测定试剂盒:南京建成生物工程研究所。
1.2 仪器与设备
平衡木装置(60 cm×2 cm×2 cm):实验室自制;7890B气相色谱仪:美国Agilent公司;7697A顶空进样器:美国Agilent公司;ECTM-WAX色谱柱(30m×0.53mm×1.2μm):美国Alltech公司;HeraeusTMFrescoTM21微量离心机:美国ThermoScientific公司;Multiskan Go全波长酶标仪:美国Thermo Scientific公司;手持式匀浆器:美国Kimble公司。
1.3 方法
1.3.1 动物分组与处理
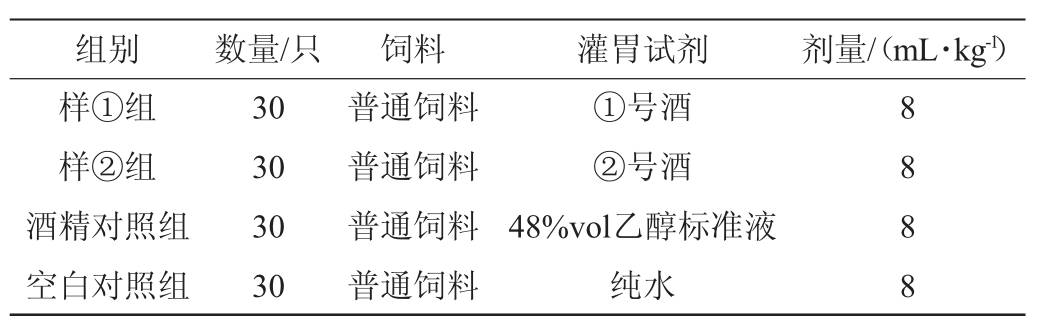
120只Balb/c小鼠适应性饲养后,按体质量分层后随机分组,分为样①组、样②组、酒精对照组及空白对照组,分组情况见表2。
表2 实验动物分组情况
Table 2 Grouping of experimental animals
1.3.2 平衡木实验
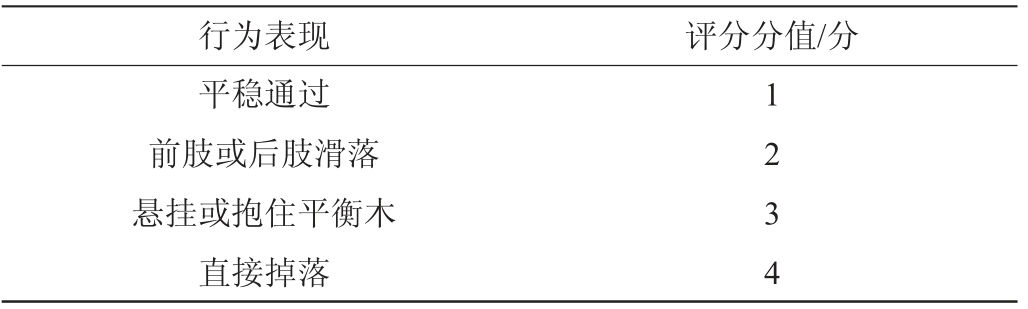
参考CRABBE J C等方法[9],正式实验前1天需要进行过梁训练,将小鼠放置于平衡木一端,推动臀部或轻柔摇动尾部使其过梁,每只小鼠训练两次。禁食不禁水12 h,不同组别小鼠进行称质量并计算灌胃量。正式实验前将小鼠移入测试房间适应2 h,每只小鼠灌胃10 min后置于平衡木一端,观察小鼠过梁情况,行走评分标准见表3。
表3 行走试验评分标准
Table 3 Score standards of walking tests
1.3.3 标本采集及检测
不同组别小鼠过梁结束后,立即抓取固定使其眼球突出充血,用弯头眼科镊迅速钳取眼球,使血液流入抗凝离心管(肝素钠溶液100 μL)中,颠倒混匀后4 ℃、3 000 r/min离心15 min,取上清,-20 ℃冰箱保存。小鼠摘眼球取血后,颈椎脱臼处死,置于冰盘上,医用解剖剪剪开颈部皮肤、人字缝,医用直头镊剥开颅骨,轻轻取出脑组织,剔除结缔组织和脂肪组织后,用预冷过的生理盐水漂洗血迹,吸水纸吸干后电子天平称质量。按体料液比1∶1(g∶mL)加入生理盐水在冰浴中进行匀浆,4 ℃、10 000 r/min离心30 min,取上清,-20 ℃冰箱保存。顶空气相色谱法测定小鼠血浆中乙醇含量,酶联免疫吸附法测定小鼠血浆中NSE含量,化学显色法测定小鼠脑匀浆中乙醛、LPO、MDA含量、SOD、GSH-PX活力,操作步骤严格按照说明书进行。
1.3.4 数据的统计及处理
采用SPSS 21.0软件进行统计分析和处理,正态分布数据采用均值±标准差(X±S)表示,方差齐时进行单因素方差分析(one-way ANOVA),LSD检验进行组间两两比较;方差不齐时使用Kruskal-Wallis检验。
2 结果与分析
2.1 行为学指标
共济失调的发生与大脑、小脑及前庭系统等的损害密切相关,主要表现为机体运动的协调不良、平衡障碍等。研究表明,乙醇暴露剂量控制在2.5~3.5 g/kg范围内能使小鼠产生明显的共济失调现象[10-11],故根据前期预实验,本研究采用8 mL/(kg·体质量)(约3.0 g/kg)的单次灌胃剂量进行有效造模。平衡木实验是评估小鼠肢体平衡以及肌肉运动协调能力的行为学方法。本研究参考崔海等[12-13]研究方法对平衡木行走评分标准进行了适当调整,即行走评分越高,共济失调现象越严重。不同组别平衡木实验行为学指标检测结果见表4。
表4 平衡木实验行为学指标检测结果
Table 4 Determination results of behavioral indicators by balance beam device tests

注:“aa”表示与空白对照组比较差异极显著(P<0.01);“bb”表示与酒精对照组比较差异极显著(P<0.01);“c”表示与样②组比较差异显著(P<0.05)。下同。
由表4可知,样①组、样②组、酒精对照组行走评分高于空白对照组,差异极显著(P<0.01);样②组行走评分低于酒精对照组,差异极显著(P<0.01);样①组行走评分高于样②组,差异显著(P<0.05);其余组间差异无统计学意义(P>0.05)。酒精暴露组较空白对照组均出现明显的共济失调现象,提示乙醇在致共济失调中的关键作用,但样①组、样②组较酒精对照组行走评分偏低,说明酒样中除乙醇、水外的微量成分可能对小鼠机体具有一定的保护作用。白酒中杂醇、醛类、羧酸、酯类、酸类等微量成分约占1%~2%,其种类与比例的变化都会影响白酒的质量和风味[14],本研究发现样①组与样②组诱导产生的共济失调程度不同,且差异具有统计学意义,提示平衡木实验行为学指标能有效反映不同白酒引起的共济失调效应大小。
2.2 乙醇代谢指标
乙醇是亲脂性小分子化合物,能迅速通过血脑屏障作用于脑组织。乙醛是乙醇的代谢产物,动物实验证明摄入酒精的小鼠脑部乙醛含量明显增加,且小脑含量更高,小脑是平衡中枢,由于乙醛其较强还原性,会致使脑部缺氧,出现站立不稳等现象[15]。不同组别乙醇、乙醛含量检测结果见表5。
表5 不同浓香型白酒对急性酒精中毒小鼠乙醇代谢的影响
Table 5 Effect of different strong-flavor Baijiu on ethanol metabolism in mice with acute alcoholism
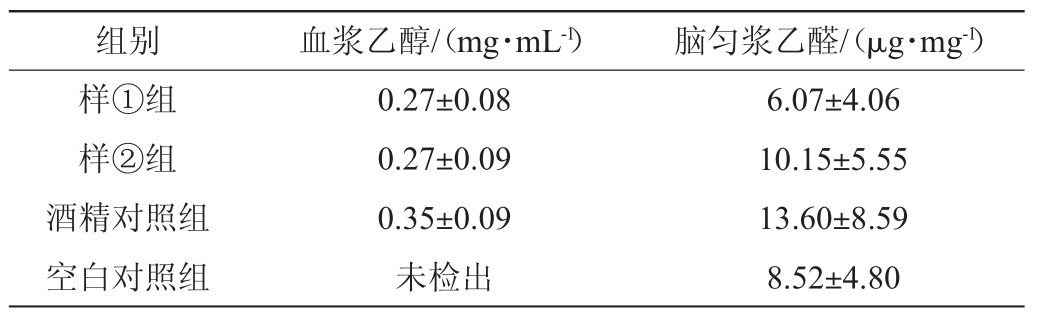
由表5可知,各组间血浆乙醇、脑匀浆乙醛含量差异不显著(P>0.05),与上述行为学结果不一致。由于乙醛的浓度与乙醇摄入量、乙醛加和物的形成、体内代谢酶的活性等密切相关[16],结合酒样主要理化指标分析结果(即乙醇、乙醛、乙缩醛含量相近),可得出乙醛含量不能有效反映共济失调的程度。
2.3 急性脑损伤指标
NSE是细胞能量代谢活动的关键酶,主要分布于中枢神经系统神经元与神经内分泌细胞中,当神经元损伤或坏死后,NSE通过血脑屏障进入血液中,致使血清(或血浆)NSE水平升高,其含量可灵敏、特异地反映神经元受损的程度[17-18]。不同组别神经特异性烯醇化酶含量检测结果见表6。
表6 血浆中神经特异性烯醇化酶检测结果
Table 6 Determination results of neuron-specific enolase in plasma

由表6可知,样①组、样②组、酒精对照组血浆NSE含量高于空白对照组,差异极显著(P<0.01);其余组间无统计学差异(P>0.05)。结果显示,样②组NSE含量稍低于样①组、酒精对照组,提示②号酒样所致的急性脑损伤程度更小,且NSE检测水平趋势与行走评分结果保持一致,提示血浆NSE含量可能与共济失调水平呈正相关趋势。由于样①组、样②组、酒精对照组小鼠酒精摄入量及血浆乙醇含量并无显著差异,提示酒样②中的微量成分可能有减轻乙醇对神经元损伤的作用。
2.4 氧化损伤指标
酒精诱导的脑损伤与脑组织发生氧化应激和脂质过氧化等反应有关[19]。MDA和LPO是脂质过氧化的重要产物,常用作反映机体细胞氧化损伤程度的指标,由于SOD和GSH-PX活力高低可间接反映机体清除自由基的能力,故常联合使用进行氧化损伤评价。不同组别氧化损伤相关指标检测结果见表7。
表7 氧化损伤相关指标检测结果
Table 7 Determination results of indicators related to oxidative damage
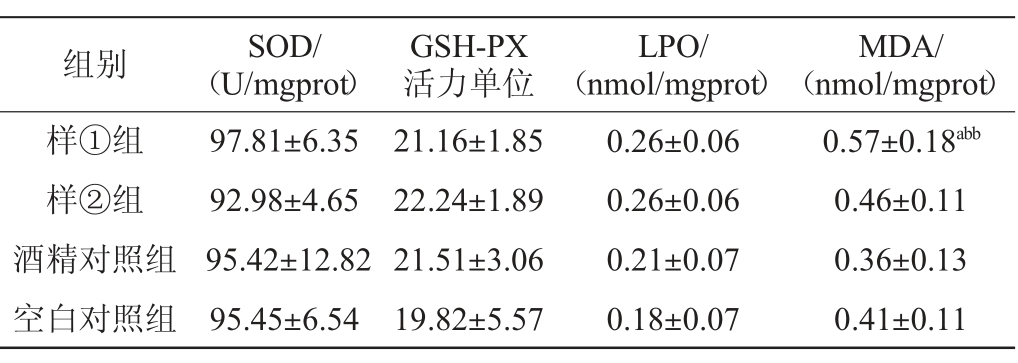
注:“a”表示与空白对照组比较差异显著(P<0.05)。
由表7可知,样①组脑匀浆MDA含量高于酒精对照组、空白对照组,差异具有统计学意义(P<0.01或0.05);其余组间差异无统计学意义;各组间脑匀浆SOD、GSH-PX活力、LPO含量无统计学差异(P>0.05)。研究发现不同组别间氧化损伤指标无统计学差异(P>0.05),考虑到实验动物采用的是单次中剂量酒精暴露,且段玉香等[19-20]研究结果显示,单次大剂量或者长期酒精暴露均可产生明显的脑部氧化损伤,故提示可能与作用剂量大小或者酒精暴露时间长短有关。且由于白酒中的微量成分组成及比例十分复杂,酒体中的某一种或某一类微量成分会对氧化应激造成不同的影响,具体的影响方式与程度需要进一步的实验研究。
3 结论
本研究结果显示,同酒精浓度酒精暴露组(不同白酒以及乙醇溶液)将造成实验动物不同程度的共济失调效应,具体可能是通过调控NSE的含量水平来产生影响。即饮用舒适度越高的酒饮后体内生成的NSE含量水平越低,急性脑损伤越轻,产生的共济失调效应越小。提示可通过优化的平衡木实验测定动物行为学指标结合急性脑损伤指标来评价白酒的饮用舒适度。
本研究结果提示,同酒精浓度酒精暴露组(不同白酒以及乙醇溶液)引起的共济失调效应有明显差异,且不同组间乙醇代谢、氧化应激指标与行为学实验结果并不完全一致,结合白酒的理化成分检测结果分析,可能与白酒中微量成分组成和比例不同有关;但具体的原因与机制值得深入探究,后续研究将对该内容继续开展。
[1]曾祖训.白酒醉酒度低的产品是消费者的新追求[J].酿酒科技,2008(10):115-116.
[2]郝飞克,刘蓉,韩兴林,等.饮料酒饮用舒适度及健康评价体系的研究与应用[J].食品科学技术学报,2019,37(2):10-16.
[3]张梦妍,郑露,党好,等.浓香型白酒醉酒度评价动物模型的建立[J].现代预防医学,2010,37(19):3623-3625.
[4]MARCZINSKI C A,FILLMORE M T.Acute alcohol tolerance on subjective intoxication and simulated driving performance in binge drinkers[J].Psychol Addict Behav,2009,23(2):238-247.
[5]张文玲,文亚男,郑红,等.酒精暴露与中枢神经系统的损伤[J].河南大学学报(医学版),2013,32(4):285-289.
[6]胡力文,杨飞,赵婉妤,等.浓香型白酒对急性酒精中毒小鼠宿醉头痛指标的影响[J].中国酿造,2019,38(6):128-131.
[7]张学武.银杏叶提取物联合纳洛酮对急性酒精中毒共济失调患者认知和运动功能的影响[J].中国中医急症,2010,19(4):556-559.
[8]丁海龙,敖灵,邓波,等.中国白酒微量健康成分分析[J].中国酿造,2018,37(2):11-14.
[9]CRABBE J C,METTEN P,YU C,et al.Genotypic differences in ethanol sensitivity in two tests of motor incoordination[J]. J Appl Physiol,2003,95(4):1338-1351.
[10]METTEN P,BEST K L,CAMERON A J,et al.Observer-rated ataxia:rating scales for assessment of genetic differences in ethanol-induced intoxication in mice[J].J Appl Physiol,2004,97(1):360-368.
[11]郑露,张梦妍,彭彦卿,等.不同醉酒度浓香型白酒对小鼠血中乙醇代谢的影响[J].现代预防医学,2010,37(19):3626-3628.
[12]崔海.低强度超声联合微泡开放大鼠血脑屏障的研究[D].重庆:第三军医大学,2015.
[13]李榕,罗春霞,迟路湘.重组人生长激素对局灶性脑缺血大鼠神经功能恢复的影响[J].中国临床药理学与治疗学,2007(11):1288-1291.
[14]海超.白酒中微量成分的变化及其利用[J].酿酒科技,2010(5):72-77.
[15]童国强,杨强,乐细选.白酒饮用舒适度的影响因素及应对措施[J].酿酒科技,2011(8):91-92.
[16]李芳芳,张宇,陈韶华,等.酒精灌胃大鼠全血乙醛浓度变化[J].浙江预防医学,2004(1):13-14.
[17]吴春,魏光辉.血清神经元特异性烯醇化酶水平的研究进展[J].重庆医学,2010,39(21):2985-2987.
[18]王琨,李彦敏.NSE、S-100 蛋白与脑损伤关系的研究[J].脑与神经疾病杂志,2009,17(5):396-398.
[19]段玉香,王彦,张瑞荣.大鼠慢性酒精性脑损害及额区MDA、MT 含量变化的研究[J].医学动物防制,2012,28(7):721-722.
[20]韩光顺,梁华益,焦雯,等.茴香提取液对酒精中毒小鼠的解酒及脑组织抗氧化作用的研究[J].中国医学创新,2018,15(2):42-45.