苹果酸是葡萄果实成熟过程中形成的一种重要的有机酸,它的含量因葡萄品种以及葡萄成熟的条件不同而不同,过量苹果酸会影响葡萄酒的酸度和感官品质[1]。葡萄中的苹果酸异构体为L型[2],L-苹果酸不仅影响葡萄酒的酸度及感官品质,而且影响葡萄酒中微生物稳定性,因其它微生物可利用L-苹果酸为底物进行生长,进而造成葡萄酒腐败变质[3-4]。降解葡萄酒中过量的L-苹果酸可提高葡萄酒的风味品质。用于葡萄酒发酵的酿酒酵母并不能有效降解L-苹果酸,因此需要采用具有降解苹果酸能力菌株进行降酸。
一直以来,多采用乳酸菌(lactic acid bacteria,LAB)进行苹果酸-乳酸发酵(malolactic fermentation,MLF),将L-苹果酸转化为L-乳酸,降低葡萄酒酸度、改善葡萄酒感官特性。然而,乳酸菌在葡萄酒的特殊环境(如低pH值、高SO2、高乙醇、中链脂肪酸等)生长和发酵缓慢[5],且可能会产生生物胺(如腐胺、组胺、酪胺和尸胺)、氨基甲酸乙酯等有害物质[6-8]。MLF结束后,如果乳酸菌发酵终止不彻底,葡萄酒可因乳酸菌生长而产生生物浑浊,进而降低葡萄酒品质[9]。
实际上,一些非酿酒酵母也可降解L-苹果酸,利用降酸酵母代替乳酸菌进行降酸发酵可在某种程度上解决乳酸菌发酵存在的问题[10-13]。项目组前期已从宁夏贺兰山东麓葡萄产区的自然发酵赤霞珠葡萄汁中分离了7种,共计299株酵母菌株。为了分析已分离酵母菌降解L-苹果酸的能力,本研究采用L-苹果酸降解指示培养基显色法和高效液相色谱法(high performance liquid chromatography,HPLC)分析其降解L-苹果酸的性能,为葡萄酒降酸提供了新的菌种资源,为酵母菌开发和利用提供借鉴。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
实验所用酵母菌均分离自贺兰山东麓葡萄产区的自然发酵赤霞珠葡萄酒,见表1。
表1 实验用酵母菌株
Table 1 Yeast strains used in the experiment

注:“a”为176株酵母中随机选了4株进行测定。
1.1.2 试剂
无氨基酵母氮源(yeastnitrogenbasewithoutaminoacids,YNB)、硫酸铵、溴甲酚绿(均为化学纯)、磷酸(分析纯):国药集团化学试剂有限公司;L-苹果酸(化学纯):北京索莱宝科技有限公司;L-苹果酸(色谱纯):上海源叶生物科技有限公司。
1.1.3 培养基
酵母浸粉蛋白胨葡萄糖(yeast extract peptone dextrose,YPD)培养基:蛋白胨2%,酵母浸粉1%,葡萄糖2%,蒸馏水配制,121 ℃灭菌20 min。
酵母浸粉蛋白胨葡萄糖琼脂(yeast extract peptone dextrose agar,YPDA)培养基:蛋白胨2%,酵母浸粉1%,葡萄糖2%,琼脂粉1.5%,蒸馏水配制,121 ℃灭菌20 min。
苹果酸降解指示培养基:YNB 1.7 g/L,硫酸铵5 g/L,L-苹果酸20 g/L,溴甲酚绿0.1 g/L,以双蒸水配制,0.45 μm滤膜过滤除菌。
1.2 仪器与设备
SZ-93自动双重纯水蒸馏器:上海亚荣生化仪器厂;LC-20A高效液相色谱仪:日本岛津公司;HZ200L恒温摇床:武汉瑞华仪器设备有限责任公司;SHZ-D循环水式多用真空泵:郑州特尔仪器设备有限公司。
1.3 实验方法
1.3.1 酵母菌降L-苹果酸的定性分析
采用苹果酸降解指示培养基显色法进行降酸酵母的初筛,参照OSOTHSILP C等[14]的方法。用接种环取2环YPDA斜面培养基上的酵母菌,接种到装液量为30 mL/100 mLYPD培养基中,28 ℃、120 r/min恒温摇床培养24 h进行活化。活化后的酵母菌以106 CFU/mL接种到装有30 mL苹果酸降解指示培养基的100 mL三角瓶中,25 ℃、120 r/min恒温摇床培养10 d,以空白指示培养基作为对照,每株菌做2个平行。自培养第1天开始每天观察和记录培养基的颜色。
培养基中添加L-苹果酸作为主要碳源,溴甲酚绿作为酸碱指示剂,若待测菌株具有代谢L-苹果酸的能力,则随着菌株代谢能力的增强,培养基中L-苹果酸逐渐被消耗,pH值随之升高,则培养基的颜色呈现从黄色到蓝色的转变,当培养基pH 3.3时呈黄色,pH 4.5时开始出现颜色的明显变化,pH 5.4时呈蓝色。
1.3.2 酵母菌降L-苹果酸的定量分析
根据GB 5009.157—2006《食品中有机酸的测定》,采用HPLC对苹果酸降解指示培养基中的苹果酸含量进行定量检测,方法如下:
0.1%磷酸溶液配制:磷酸1 mL,加水至1 000 mL并混匀,用0.22 μm滤膜过滤备用。HPLC的流动相为0.1%磷酸溶液和甲醇,二者体积比例为97.5∶2.5。
标准L-苹果酸溶液配制:准确称取L-苹果酸标准品0.5 g,加入0.1%的磷酸溶液并定容至10 mL以配制50 mg/mL苹果酸的储备液;然后用0.1%的磷酸溶液稀释储备液,分别使L-苹果酸质量浓度达1 mg/mL、2 mg/mL、4 mg/mL、10 mg/mL、20 mg/mL和30 mg/mL,于4 ℃保存。
样品处理:将培养10 d的苹果酸降解指示培养基倒入50 mL离心管离心10 min(4 ℃、8 000 r/min),取上清并用0.22 μm滤膜过滤并进行检测。
色谱条件:色谱柱为inertsilODS-3C18柱(4.6 mm×250mm),流动相使用前用超声波脱气5 min,总流速0.7 mL/min,检测波长为210nm,柱温40℃,进样量为20μL,检测时间为20min。
1.3.3 数据统计处理与分析
采用Microsoft Office 2016和GraphPad Prism 6对数据进行处理。
2 结果与分析
2.1 不同酵母菌株降L-苹果酸的定性分析
为了解不同酵母菌株的L-苹果酸降解能力,将不同酵母菌按106 CFU/mL接种于苹果酸降解指示培养基,以不接种酵母的空白指示培养基为对照,28 ℃培养10 d,观察其降酸能力,若酵母培养液呈蓝色,则表示其降酸能力强,呈绿色表示其降酸能力较强,呈黄绿色表示其降酸能力弱,若酵母培养液不变色(黄色),则表示其不降酸。显色结果表示,304株酵母菌中有21株具有降L-苹果酸能力的酵母菌株。其中有19株酵母菌降酸能力强,分别是菌株HI-5、HI-6、HII-17、H-II-2、H-II-13、H-II-16、YI-1-1、YI-1-2、YI-2、YI-9-1、YI-9-2、YI-9-3、YII-1、YIII-9、LI-6、LI-9、LI-10、LI-13、L-II-8。菌株G-II-18降酸能力较强,菌株Hlast-35降酸能力弱,而其余菌株均无降酸能力。对降L-苹果酸的酵母菌株的定性分析结果表明不同酵母菌株的降酸能力不同。前期研究表明,拜耳接合酵母(Zygosaccharomyces bailii)、异常汉逊酵母(Hansenula anomala)、东方伊萨酵母(Issatchenkia orientalis)、园球形假丝酵母(Candida sphaerica)、嗜鞣管囊酵母(Pachysolen tannophilus)、树干毕赤酵母(Pichia stipitis)、解苹果酸裂殖酵母(Schizosaccharomyces malidevorans)和粟酒裂殖酵母(Schizosaccharomyces pombe)等菌株均具有降解L-苹果酸的能力,且不同种酵母菌株的降酸能力不同[15-17]。
2.2 L-苹果酸标准曲线
采用高效液相色谱分别分析1mg/mL、2mg/mL、4mg/mL、10 mg/mL、20 mg/mL和30 mg/mL的L-苹果酸标准溶液。以标准液的质量浓度(x)为横坐标,以色谱峰面积(y)为纵坐标,绘制标准曲线,结果见图1。由图1可知,L-苹果酸标准曲线回归方程为y=1.2523x+1.1093,R2=0.9992,二者线性关系良好。
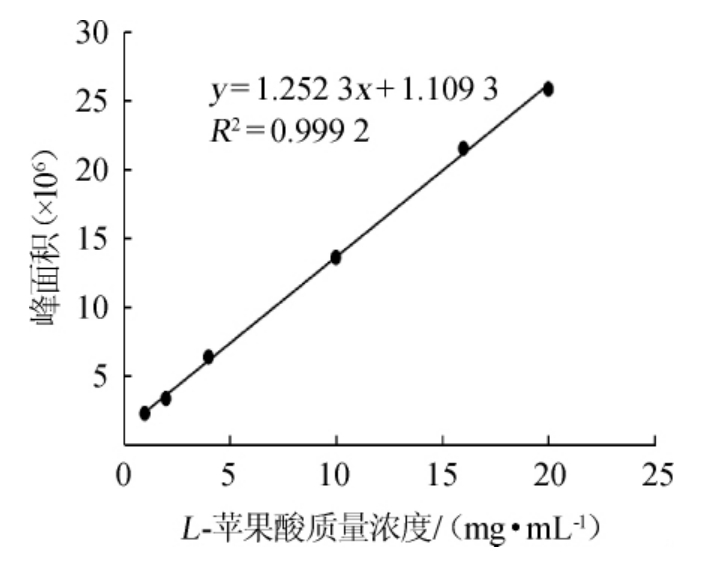
图1 L-苹果酸标准曲线
Fig.1 Standard curve of L-malic acid
2.3 酵母菌株降L-苹果酸的定量分析
为了进一步定量分析不同种酵母菌株的L-苹果酸降解能力,采用HPLC对发酵10 d的上清液中L-苹果酸的含量进行分析,以空白培养基为对照,计算其降酸率。
2.3.1 不同美极梅齐酵母降L-苹果酸能力的定量分析
不同美极梅齐酵母(Metschnikowia pulcherrima)菌株降酸能力的定量分析结果见图2。由图2可知,菌株GI-1的降酸率为24.05%,菌株YII-1的降酸率为89.48%,而其他11株M.pulcherrima的降酸率均>90%,这说明M.pulcherrima菌株均可降解L-苹果酸,且多数菌株降酸能力较强。前期研究表明,M.pulcherrima可有效改善葡萄酒的风味和品质。BENITOME等[18]将M.pulcherrima与酿酒酵母序列接种于雷司令葡萄汁中,可显著提高葡萄酒的果香风味。RODRIGUEZ M E等[19]将M.pulcherrima与酿酒酵母序列接种于马斯喀特葡萄汁中,酿造的葡萄酒中α-松油醇含量增加,提高了葡萄酒的花香风味。但关于降解L-苹果酸的M.pulcherrima菌株研究尚未见报道。
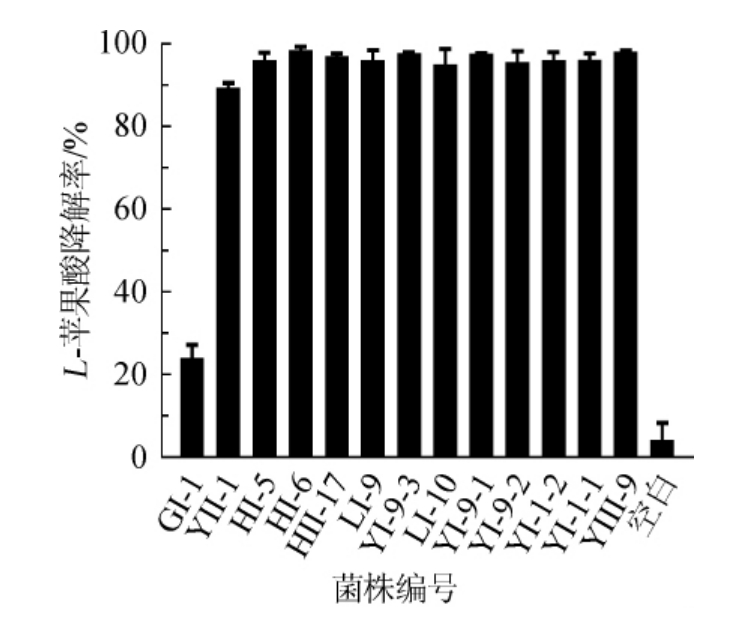
图2 不同美极梅齐酵母降L-苹果酸能力的分析
Fig.2 Analysis of L-malic acid degradation ability of different strains of Metschnikowia pulcherrima
2.3.2 不同星形假丝酵母菌株降L-苹果酸能力的定量分析
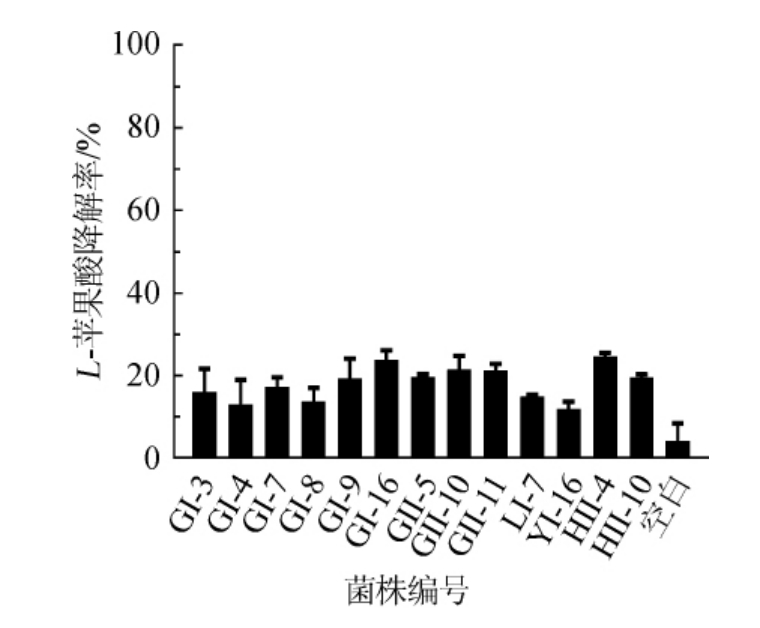
图3 不同星形假丝酵母降L-苹果酸能力的分析
Fig.3 Analysis of L-malic acid degradation ability of different strains of Candida zemplinina
不同星形假丝酵母(Candida zemplinina)菌株降L-苹果酸能力的定量分析结果见图3。由图3可知,13株酵母降酸能力均低于30%。然而,APONTE M等[20]在用艾格尼科葡萄进行微发酵评估时发现C.zemplinina能产生大量甘油,且能够代谢所有的果糖和苹果酸。筛选结果与文献报道不符,可能与同种酵母不同菌株之间的降酸差异性不同有关。
2.3.3 戴尔有孢圆酵母、加利福尼亚假丝酵母及不同库德毕赤酵母降L-苹果酸能力的定量分析
戴尔有孢圆酵母(Y-III-2-1)、加利福尼亚假丝酵母(Hlast-35)及不同库德毕赤酵母(LI-6、LI-13、YI-2)菌株降L-苹果酸能力的定量分析结果见图4。由图4可知,戴尔有孢圆酵母的降酸率为6.13%,加利福尼亚假丝酵母的降酸率为34.77%。库德毕赤酵母(P.kudriavzevii)YI-2的降酸率为85.46%,P.kudriavzevii LI-6和P.kudriavzevii LI-13降酸率分别为99.55%及99.21%。事实上,SEO S等[21]从韩国葡萄酒渣中分离到一株具有降解L-苹果酸的P.kudriavzevii KMBL 5774,降酸率为95.5%,DEL MÓNACO S M等[22]分离出一株降酸菌株P.kudriavzevii NNI15,且在发酵过程中高产甘油、低产乙醇,能显著提高葡萄酒果香。
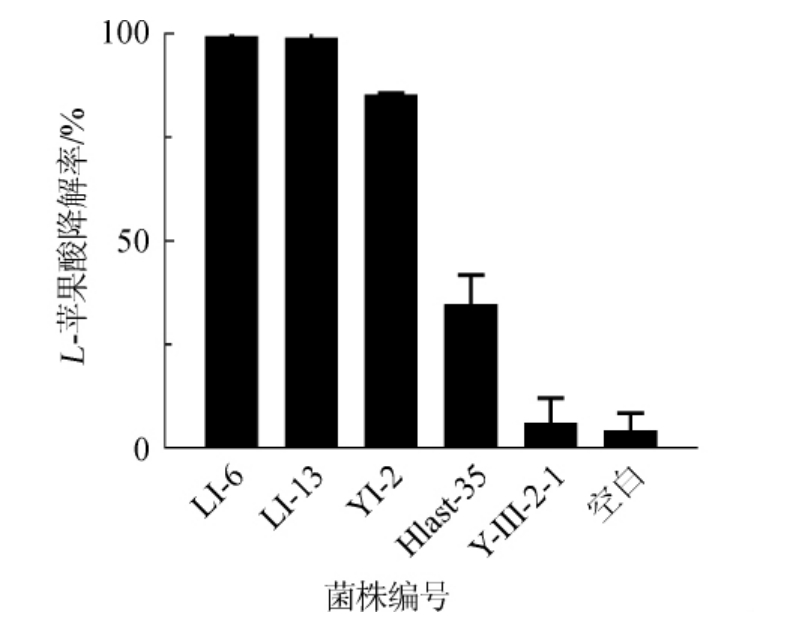
图4 戴尔有孢圆酵母、加利福尼亚假丝酵母及不同库德毕赤酵母降L-苹果酸能力的分析
Fig.4 Analysis of L-malic acid degradation ability of Torulaspora delbrueckii, Candida californica and different strains of Candida zemplinina
2.3.4 不同葡萄有孢汉逊酵母菌株降L-苹果酸能力的定量分析
不同葡萄有孢汉逊酵母(Hanseniaspora uvarum)菌株降L-苹果酸能力的定量分析结果见图5。由图5可知,菌株G-II-18、L-II-8、H-II-2、H-II-13和H-II-16降解L-苹果酸能力较强,其降酸率分别为71.20%、86.30%、85.88%、86.62%和81.44%,其余均低于30%。根据HUK等[23]的报道,将H.uvarum与酿酒酵母序列接种应用于黑比诺葡萄酒的酿造,葡萄酒中几种C13-异戊二烯化合物和一些萜烯物质的浓度增加,增加了葡萄酒“热带水果”、“浆果”、“花香”和“坚果香”的风味特征。HERNANDEZ-ORTE P 等[24]研究发现,H.uvarum释放的糖苷酶能促进萜烯类糖苷的水解,释放出风味活性成分,改善葡萄酒的风味品质。然而,关于将H.uvarum应用于葡萄酒酿造降解其中L-苹果酸的研究尚未见报道。
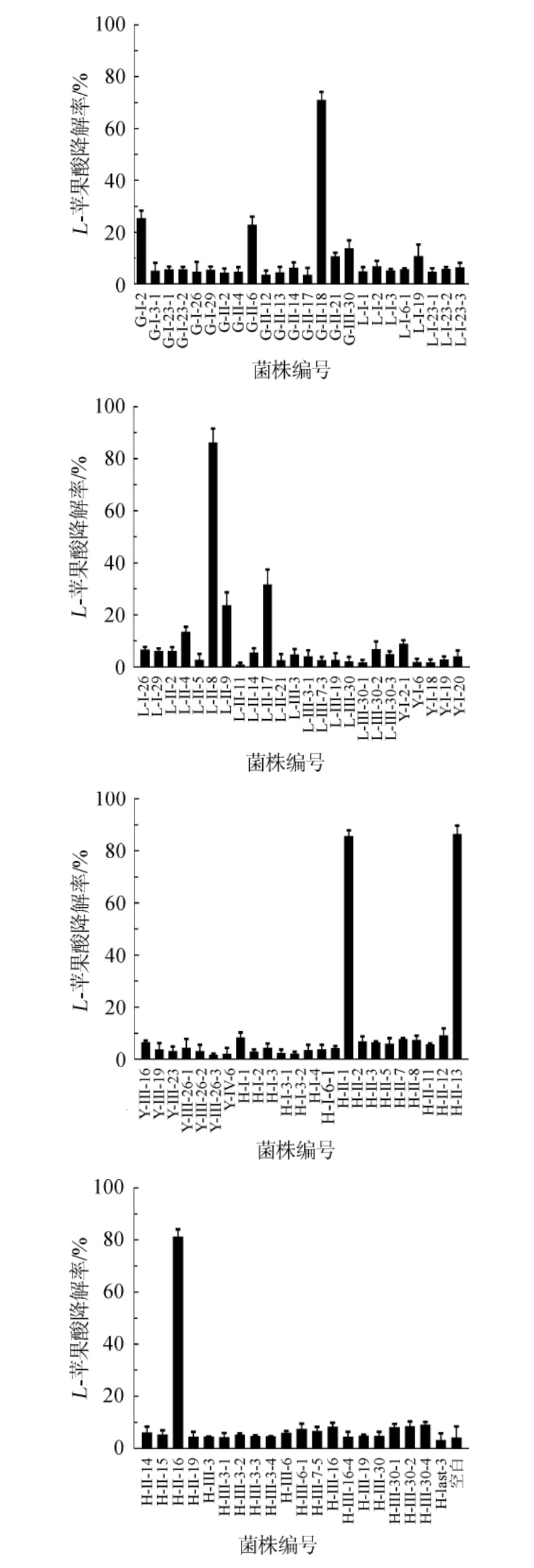
图5 不同葡萄有孢汉逊酵母降L-苹果酸能力的分析
Fig.5 Analysis of L-malic acid degradation ability of different strains of Hanseniaspora uvarum
2.3.5 不同酿酒酵母菌株降L-苹果酸能力的定量分析
据文献报道,酿酒酵母(Saccharomyces cerevisiae)因不含苹果酸通透酶而不具有代谢L-苹果酸的能力[25],为了验证鉴定保藏的S.cerevisiae是否具有降酸能力,从鉴定的176株S.cerevisiae随机选取4株进行降L-苹果酸定量分析。结果见图6。由图6可知,菌株LIII-7、Glast-33-1、Hlast-2和GIII-16的降酸率分别为5.93%、13.91%、0.86%和12.03%,这说明S.cerevisiae降解L-苹果酸的能力较低,与文献报道相符。

图6 不同酿酒酵母降L-苹果酸能力的分析
Fig.6 Analysis of L-malic acid degradation ability of different strains of Saccharomyces cerevisiae
2.4 不同种酵母降L-苹果酸能力统计分析
对不同种酵母菌株降L-苹果酸性能进行统计分析,结果见表2。由表2可知,不同种酵母菌株降解L-苹果酸的能力存在明显差异,即使同一种内,不同菌株降解苹果酸的能力也不尽相同。M.pulcherrima、P.kudriavzevii和H.uvarum中的部分菌株降解苹果酸能力较强。其中P.kudriavzevii降解苹果酸的能力较强,而M.pulcherrima和H.uvarum降解苹果酸的能力则出现了明显的种内差异,产生这个现象的原因还有待探究。此外,在C.zemplinina、T.delbrueckii、C.californica和S.cerevisiae中并未发现能够明显降解L-苹果酸的菌株。
表2 不同种的酵母菌株降L-苹果酸能力统计分析
Table 2 Statistical analysis of L-malic acid degradation ability of different yeast species
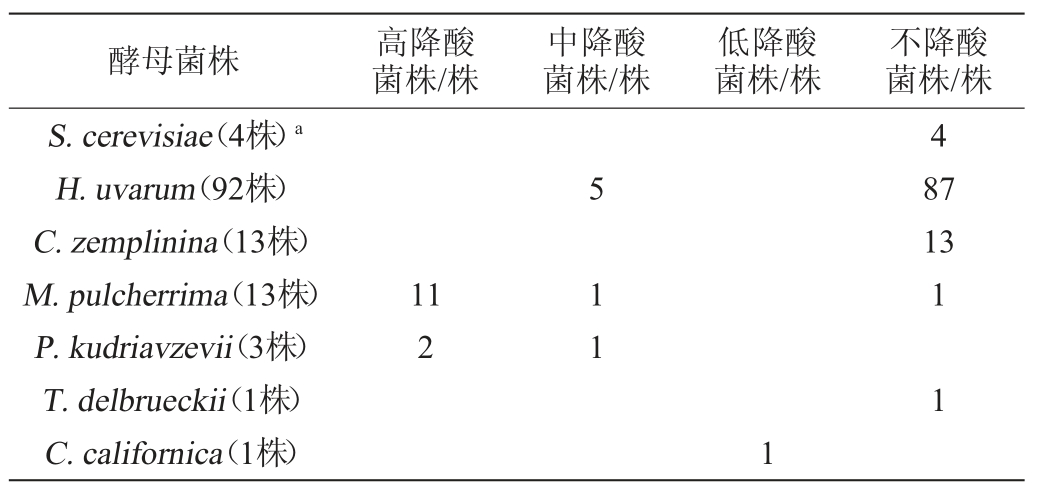
注:降酸率介于90%~100%为高降酸菌株,60%~90%为中降酸菌株,30%~60%为低降酸菌株,0~30%为不降酸菌株。“a”为176株酿酒酵母中随机选取4株进行测定。
3 结论
采用苹果酸降解指示培养基显色法和HPLC对自然发酵液中分离、鉴定的酵母菌株的降解L-苹果酸能力进行定性和定量分析,共分离到13株强降酸酵母,降酸率均在90%以上。其中菌株HI-5、HI-6、HII-17、LI-9、LI-10、YI-1-1、YI-1-2、YI-9-1、YI-9-2、YI-9-3、YIII-9属于M.pulcherrima,LI-6、LI-13属于P.kudriavzevii的。然而不同种酵母菌株间呈现出L-苹果酸降解能力的明显差异,且同一种的不同酵母菌株间也存在降酸能力的明显差异。降L-苹果酸酵母菌株的获得为葡萄酒降酸提供新的菌种资源,为酵母菌开发利用提供借鉴。然而,筛选得到的降解L-苹果酸的酵母菌株属于非酿酒酵母,该类酵母发酵糖产生酒精的能力较弱,所以在用于葡萄酒酿造时,需与酿酒酵母混合发酵才能同时达到降酸和发酵产酒的目的[26],但关于二者混合发酵降酸工艺需要进一步探究。
[1]PICARIELLO L,RINALDI A,MARTINO F,et al.Modification of the organic acid profile of grapes due to climate changes alters the stability of red wine phenolics during controlled oxidation[J].Vitis:J Grapevine Res,2019,58(5):127-133.
[2]莫燕霞,殷居易,顾晓俊,等.葡萄酒有机酸研究现状及应用展望[J].食品工业科技,2015,36(6):380-384.
[3]SWIEGERS J H,BARTOWSKY E J,HENSCHKE P A,et al.Yeast and bacterial modulation of wine aroma and flavour[J].Aust J Grape Wine Res,2005,11(2):139-173.
[4]TOIT M D,PRETORIUS I S.Microbial spoilage and preservation of wine:using weapons from nature's own arsenal-a review[J].South Afr J Enol Viticult,2000,21(1):74-96.
[5]MARTINO C D,TESTA B,LETIZIA F,et al.Effect of exogenous proline on the ethanolic tolerance and malolactic performance of Oenococcus oeni[J].J Food Sci Technol,2020,57(11):3973-3979.
[6]SMIT A Y,ENGELBRECHT L,TOIT M D.Managing your wine fermentation to reduce the risk of biogenic amine formation[J]. Front Microbiol,2012,3:76.
[7]POLO L,FERRER S,PEÑA-GALLEGO A,et al.Biogenic amine synthesis in high quality Tempranillo wines.Relationship with lactic acid bacteria and vinification conditions[J].Ann Microbiol,2011,61(1):191-198.
[8]RESTUCCIA D,LOIZZO M R,SPIZZIRRI U G,et al.Accumulation of biogenic amines in wine:role of alcoholic and malolactic fermentation[J].Fermentation,2018,4(1):6.
[9]SUMBY K M,GRBIN P R,JIRANEK V.Implications of new research and technologiesformalolacticfermentationinwine[J].Appl Microbiol Biotechn,2014,98(19):8111-8132.
[10]HEINRICH D P,MARET D T,HÉLÉNE N,et al.Modulation of wine flavor using Hanseniaspora uvarum in combination with different Saccharomyces cerevisiae,lactic acid bacteria strains and malolactic fermentation strategies[J].Fermentation,2019,5(3):64.
[11]王玉华,盛文军,李敏,等.耐热克鲁维酵母和粟酒裂殖酵母顺序接种发酵对美乐干红葡萄酒品质的影响[J].食品科学,2019,40(8):102-111.
[12]HONG S K,LEE H J,PARK H J,et al.Degradation of malic acid in wine by immobilized Issatchenkia orientalis cells with oriental oak charcoal and alginate[J]. Lett Appl Microbiol,2010,50(5):522-529.
[13]KIM D H,HONG Y H.Co-fermentation of grape must by Issatchenkia orientalis and Saccharomyces cerevisiae reduces the malic acid content in wine[J].Biotechnol Lett,2008,30(9):1633-1638.
[14]OSOTHSIL P C,SUBDEN R E.Isolation and characterization of Schizosaccharomyces pombe mutants with defective NAD-dependent malic enzyme[J].Revue Canad Microbiol,1986,32:481-486.
[15]SU J,WANG T,WANG Y,et al.The use of lactic acid-producing,malic acid-producing,or malic acid-degrading yeast strains for acidity adjustment in the wine industry[J].Appl Microbiol Biotechn,2014,98(6):2395-2413.
[16]REDZEPOVIC S,ORLIC S,MAJDAK A,et al.Differential malic acid degradation by selected strains of Saccharomyces during alcoholic fermentation[J].Int J Food Microbiol,2003,83(1):49-61.
[17]VOLSCHENK H,VUUREN H J,VILJOEN-BLOOM M.Malo-ethanolic fermentation in Saccharomyces and Schizosaccharomyces[J].Curr Genet,2003,43(6):379-391.
[18]BENITO S,HOFMANN T,LAIER M,et al.Effect on quality and composition of Riesling wines fermented by sequential inoculation with non-Saccharomycesand Saccharomycescerevisiae[J].Eur Food Res Technol,2015,241(5):707-717.
[19]RODRIGUEZ M E,LOPES C A,BARBAGELATA R J,et al.Influence of Candida pulcherrima Patagonian strain on alcoholic fermentation behaviour and wine aroma[J].Int J Food Microbiol,2010,138(1):19-25.
[20]APONTE M,BLAIOTTA G.Potential role of yeast strains isolated from grapes in the production of Taurasi DOCG[J].Front Microbiol,2016:809-809.
[21]SEO S,RHEE C,PARK H,et al.Degradation of malic acid by Issatchenkia orientalis KMBL 5774,an acidophilic yeast strain isolated from Korean grape wine pomace[J].J Microbiol,2007,45(6):521-527.
[22]DEL MÓNACO S M,BARDA N B,RUBIO N C,et al.Selection and characterization of a Patagonian Pichia kudriavzevii for wine deacidification[J].J Appl Microbiol,2014,117(2):451-464.
[23]HU K,QIN Y,TAO Y,et al.Potential of glycosidase from Non-Saccharomyces isolates for enhancement of wine aroma[J].J Food Sci,2016,81(4):M935-M943.
[24]HERNANDEZ-ORTE P,CERSOSIMO M,LOSCOS N,et al.The development of varietal aroma from non-floral grapes by yeasts of different genera[J].Food Chem,2008,107(3):1064-1077.
[25]BOLES E,DE JONGGUBBELS P,PRONK J T,et al.Identification and characterization of MAE1,the Saccharomyces cerevisiae structural gene encoding mitochondrial malic enzyme[J].J Bacteriol,1998,180(11):2875-2882.
[26]VARELA C,BORNEMAN A R.Yeasts found in vineyards and wineries[J].Yeast,2017,34(3):111-128.