拐枣(Hovenia acerba),学名枳椇,系鼠李科(Rhamnaceae)枳椇属(Hovenia)植物的果实,又名鸡爪连、甜半夜等,其果实形态似万字符,有万寿果的美誉[1]。拐枣含糖量高,且果香浓郁,是制备果酒的优良原料[2]。拐枣果酒的加工不仅可以实现拐枣资源高效利用,也符合我国当前酒类从烈性型酒向营养型酒转变和从粮食类酒向果酒转变的消费结构调整趋势。我国很多农村地区都有利用拐枣制酒的传统,将拐枣加入到一定量的白酒中进行泡制,制成拐枣露酒,或将拐枣破碎处理接种发酵剂得到拐枣发酵酒。《滇南本草》中就曾提到,拐枣泡酒服之,具有舒通筋络、安神保健等功效[3]。
自由基是人体内的正常代谢产物,在常态下,人体内的自由基处于动态平衡中,然而该平衡一旦被打破,就会对机体造成损害,从而引发诸如高血压、糖尿病等一系列相关疾病。摄入一定量的抗氧化食物,对人体的保健作用已得到证实[4-5],果酒的抗氧化能力是果酒的重要功能特性,流行病学调查和动物实验证明,葡萄酒由于富含多种天然抗氧化剂而具有很强的抗氧化能力,能起到保护心脑血管的作用[6]。拐枣富含酚类、多糖、生物碱等活性成分[7-8],具有解酒保肝、抗氧化、降血糖、免疫调节多种保健功能[9-10]。将拐枣加工成拐枣发酵酒或拐枣露酒,是否仍能保持其强抗氧化性能还有待研究,且酒中多酚、黄酮含量与其抗氧化能力的关系,目前也鲜见报道。
本研究拟比较拐枣发酵酒与拐枣露酒中总酚、总黄酮、总糖、抗坏血酸等成分的含量差异,采用氧自由基吸收能力(oxygen radical absorbance capacity,ORAC)、铁离子还原能力(ferric ion reducing antioxidant power,FRAP)、1,1-二苯基-2-苦肼基(1,1-diphenyl-2-picrylhydrazyl,DPPH)与2,2'-联氨-双(3-乙基苯并噻唑啉-6-磺酸)二铵盐(2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)自由基清除能力4种抗氧化体系评价其抗氧化活性,以期为拐枣酒的加工提供理论指导和技术参考。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
拐枣:采自浏阳市大围山;邵阳大曲(酒精度为52%vol):湖南湘窖酒业有限公司。
1.1.2 试剂
芦丁标准品(纯度≥98%)、没食子酸标准品(纯度为99.04%):成都曼思特生物科技有限公司;荧光素钠、奎诺二甲基丙烯酸(水溶性维生素E)(纯度为97%)、偶氮二异丁脒盐酸盐(纯度为97%)、葡萄糖分析对照品(纯度≥99%)、抗坏血酸标准品(纯度≥99.9%):上海麦克林生化科技有限公司;DPPH(纯度>97%):梯希爱(上海)化成工业发展有限公司;ABTS(纯度≥98%)、2,4,6-三吡啶基三嗪(纯度≥98%)、2,6-二氯靛酚钠盐(纯度≥97%)、果胶酶(500 U/mg):上海瑞永生物科技有限公司;其他试剂均为国产分析纯。
1.2 仪器与设备
AL204电子天平:梅特勒-托利多仪器(上海)有限公司;TGW16台式高速微量离心机:长沙英泰仪器有限公司;H-8数显恒温水浴锅:上海浦东物理光学仪器厂;WFJ-7200型可见分光光度计:尤尼柯(上海)仪器有限公司;Varioskan Lux多功能微孔读数仪:美国赛默飞世尔科技有限公司。
1.3 试验方法
1.3.1 拐枣酒制备工艺
(1)拐枣发酵酒
拐枣前处理→破碎→酶解→主发酵→过滤→后发酵→澄清→成品
操作要点:
拐枣前处理:挑选完好无损伤的拐枣,洗净沥干,剪去拐枣枝;
破碎:加入拐枣等质量的纯净水进行破碎处理,装入发酵容器;
酶解:加入0.6 g/L果胶酶溶液,室温(20~25 ℃)酶解8 h;
主发酵:按0.05 g/L加入5%的食品级亚硫酸与0.4 g/L温水活化的安琪酵母,室温(20~25 ℃)主发酵10~15 d,当酒精度不再变化,即主发酵完成;
后发酵:用纱布过滤除渣,于室温下后发酵15 d,澄清,即得拐枣发酵酒。
(2)拐枣露酒
拐枣前处理→加酒浸泡→过滤→成品
操作要点:拐枣果皮具有一定涩味,为保证口感,在制备露酒时拐枣与酒的比例不宜过大。将洗净沥干的拐枣,以邵阳大曲为酒基,液料比(mL∶g)为2.5∶1.0、3.5∶1.0、4.5∶1.0分别进行泡制,室温(20~25 ℃)避光放置45 d,过滤除去拐枣,即得拐枣露酒。
1.3.2 拐枣酒理化指标测定
参照GB/T 15038—2006《葡萄酒、果酒通用分析方法》,测定样品酒精度及抗坏血酸含量[11];采用福林酚法,测定样品中总多酚含量[12];采用亚硝酸钠-硝酸铝比色法,测定样品中总黄酮含量[13];采用3,5-二硝基水杨酸法测定样品总糖与还原糖含量[14]。
1.3.3 拐枣酒体外抗氧化试验
ORAC值的测定:参照文献[15]测定拐枣酒的ORAC值,以浓度为12.5 μmol/L、25 μmol/L、50 μmol/L、100 μmol/L、200μmol/L、400μmol/L的水溶性维生素E代替样品作荧光衰退曲线,计算曲线下净面积(the area under the curve,AUC),以水溶性维生素E浓度(x)为横坐标,AUC(y)为纵坐标绘制标准曲线,标准曲线的回归方程为:y=36.988x+376.39,相关系数R2=0.995 3,线性关系良好。样品的抗氧化能力最终由ORAC值,即水溶性维生素E当量浓度(mmol/L)表示。
FRAP值的测定:参照文献[16]测定拐枣酒的FRAP值,以硫酸亚铁标准溶液绘制标准曲线,样品最终的总抗氧化能力以硫酸亚铁当量浓度(mmol/L)表示。
ABTS自由基清除能力的测定:参照文献[17],配制7 mmol/L的ABTS甲醇溶液与2.45 mmol/L的过硫酸钾溶液,等体积混合避光反应12 h,得ABTS混合液,吸取适量ABTS混合液,甲醇稀释至其在波长734 nm处的吸光度值为0.700±0.050,得ABTS工作液。准确吸取ABTS工作液2.7 mL与0.3 mL样品溶液混合,摇匀,室温避光反应10 min,采用分光光度计在波长734 nm处测其吸光度值As。对照组以0.30 mL甲醇溶液代替样品,测其吸光度值Ac,计算ABTS自由基清除率,其计算公式如下:
ABTS自由基清除率=![]()
DPPH自由基清除能力的测定:参照文献[18],配制100 μmol/L的DPPH甲醇溶液,准确吸取0.5 mL样品溶液与3.0 mL DPPH溶液混合,摇匀,室温避光反应30 min,采用分光光度计在波长517 nm处测其吸光度值Aj。对照组以0.5 mL甲醇溶液代替样品,测其吸光度值Ai,计算DPPH自由基清除率,其计算公式如下:
DPPH自由基清除率=![]()
自由基清除能力通常由样品的半抑制浓度(halfinhibitory inhibitory concentration,IC50)值表示。本试验以维生素C(vitamin C,VC)作为阳性对照,其清除ABTS与DPPH自由基的IC50值由SPSS软件进行曲线拟合所得。拐枣酒对两种自由基清除能力的IC50值,根据其稀释倍数,最终结果以VC质量浓度(μg/mL)当量抗氧化能力表示。
1.3.4 数据分析
试验数据均采用Excel 2007、SPSS19.0与Origin 8.5进行分析处理。数据用“平均值±标准偏差”表示,采用最小显著差数法(least significance difference,LSD)进行显著性分析(P<0.05),Pearson法进行相关性分析。
2 结果与分析
2.1 不同拐枣酒理化指标测定结果
不同拐枣酒理化指标测定结果见表1。
表1 拐枣露酒与发酵酒理化指标测定结果
Table 1 Determination results of physicochemical indexes of blended and fermented Hovenia acerba alcoholic beverage
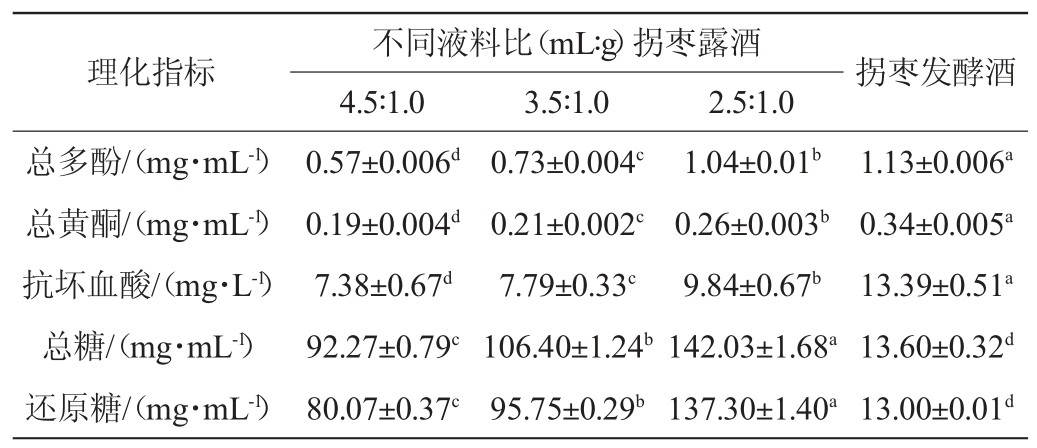
注:同一行数据不同小写字母表示差异显著(P<0.05)。
植物多酚、黄酮类物质具有抗氧化、抗炎、抑菌等功能活性[19-20]。由表1可知,拐枣露酒及发酵酒均含有一定量的多酚与黄酮,且含量差异显著(P<0.05)。拐枣露酒中多酚、黄酮含量随着液料比的减小而增大,以液料比为2.5∶1.0(mL∶g)的拐枣露酒含量最高,其总多酚含量为(1.04±0.01)mg/mL,总黄酮含量为(0.26±0.003)mg/mL。拐枣发酵酒中总多酚含量为(1.13±0.006)mg/mL,总黄酮含量为(0.34±0.005)mg/mL,显著高于拐枣露酒(P<0.05)。多酚和黄酮的溶出大大增强了拐枣酒的抗氧化能力,提高了酒的营养价值。
抗坏血酸含量与抗氧化能力关系密切,但成熟拐枣的抗坏血酸含量较低。由表1可知,拐枣露酒与发酵酒中均含有少量抗坏血酸,且含量差异显著(P<0.05)。拐枣露酒中抗坏血酸含量随拐枣液料比的减小而增大,以液料比为2.5∶1.0(mL∶g)的拐枣露酒含量最高,为(9.84±0.67)mg/L,拐枣发酵酒的抗坏血酸含量为(13.39±0.51)mg/L,显著高于拐枣露酒(P<0.05)。拐枣发酵酒中抗坏血酸含量与文献报道的欧李果酒中抗坏血酸含量接近[21]。
由表1可知,随着液料比的减小,拐枣露酒中糖类溶出增加,以液料比为2.5∶1.0(mL∶g)的拐枣露酒总糖及还原糖含量最高,分别为(142.03±1.68)mg/mL、(137.30±1.40)mg/mL,显著高于拐枣发酵酒(13.60±0.32)mg/mL、(13.00±0.01)mg/mL(P<0.05)。糖的溶出,不仅了改善酒的口感,也提高了酒的营养价值,4种拐枣酒中总糖含量与还原糖含量均差异显著(P<0.05)。
2.2 拐枣酒体外抗氧化试验结果
2.2.1 不同拐枣酒氧自由基吸收能力比较
ORAC法是目前检测抗氧化剂抗氧化能力的标准方法,被广泛应用于食品、药品等抗氧化能力的检测[22]。不同拐枣酒的ORAC值见图1。
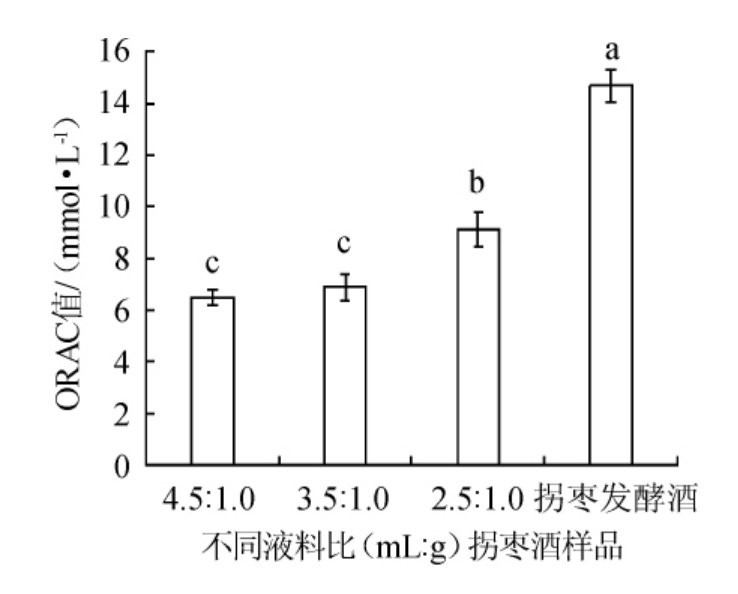
图1 不同拐枣酒的氧自由基吸收能力值
Fig.1 Oxygen radical absorption capacity value of different Hovenia acerba alcoholic beverage samples
不同小写字母表示差异显著(P<0.05)。下同。
由图1可知,拐枣露酒的ORAC值随液料比的减小而增大,当液料比为2.5∶1.0(mL∶g)时,拐枣露酒的ORAC值最大达(9.12±1.48)mmol/L,而拐枣发酵酒的ORAC值为(14.69±1.31)mmol/L,显著大于拐枣露酒(P<0.05),表明拐枣发酵酒的抗氧化能力更强。CAO G等[23]对水果的总抗氧化能力进行研究,结果表明葡萄汁的ORAC值约为15 mmol/L,葡萄酒的ORAC值为(12.34±0.47)mmol/L,与拐枣发酵酒的ORAC值相近;拐枣露酒的ORAC值大于该文献报道的橘子汁、苹果汁等常见果汁的ORAC值。李拥军等[24]在研究单枞茶酒抗氧化作用中表明,单枞茶酒ORAC值在30 mmol/L左右,约为拐枣发酵酒的2倍。
2.2.2 不同拐枣酒Fe3+还原能力比较
FRAP值越大,表明样品的Fe3+还原力越强。不同拐枣酒的FRAP值见表2。
表2 不同拐枣酒的铁离子还原能力值
Table 2 Ferric ion reducing antioxidant power value of different Hovenia acerba alcoholic beverage samples
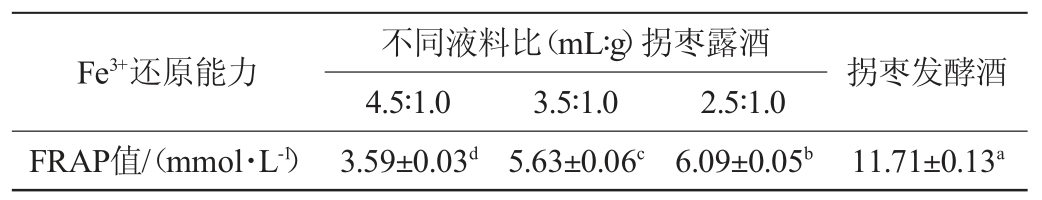
由表2可知,不同拐枣酒之间的FRAP值均存在显著差异(P<0.05),拐枣露酒的FRAP值随液料比的减小而增大,当料液比为2.5∶1.0(mL∶g)时,拐枣露酒的FRAP值最高,为(6.09±0.05)mmol/L。拐枣发酵酒的FRAP值为(11.71±0.13)mmol/L,显著高于拐枣露酒(P<0.05),表明拐枣发酵酒的Fe3+还原能力比拐枣露酒更强。
2.2.3 不同拐枣酒清除ABTS与DPPH自由基能力比较
DPPH与ABTS自由基清除能力的测定是常见的体外抗氧化方法,两种自由基被清除的机制不同,前者主要涉及氢转移,后者是一种带正电荷的自由基,它的清除过程主要涉及电子转移。拐枣酒对ABTS、DPPH自由基的清除作用见图2,IC50值见表3。
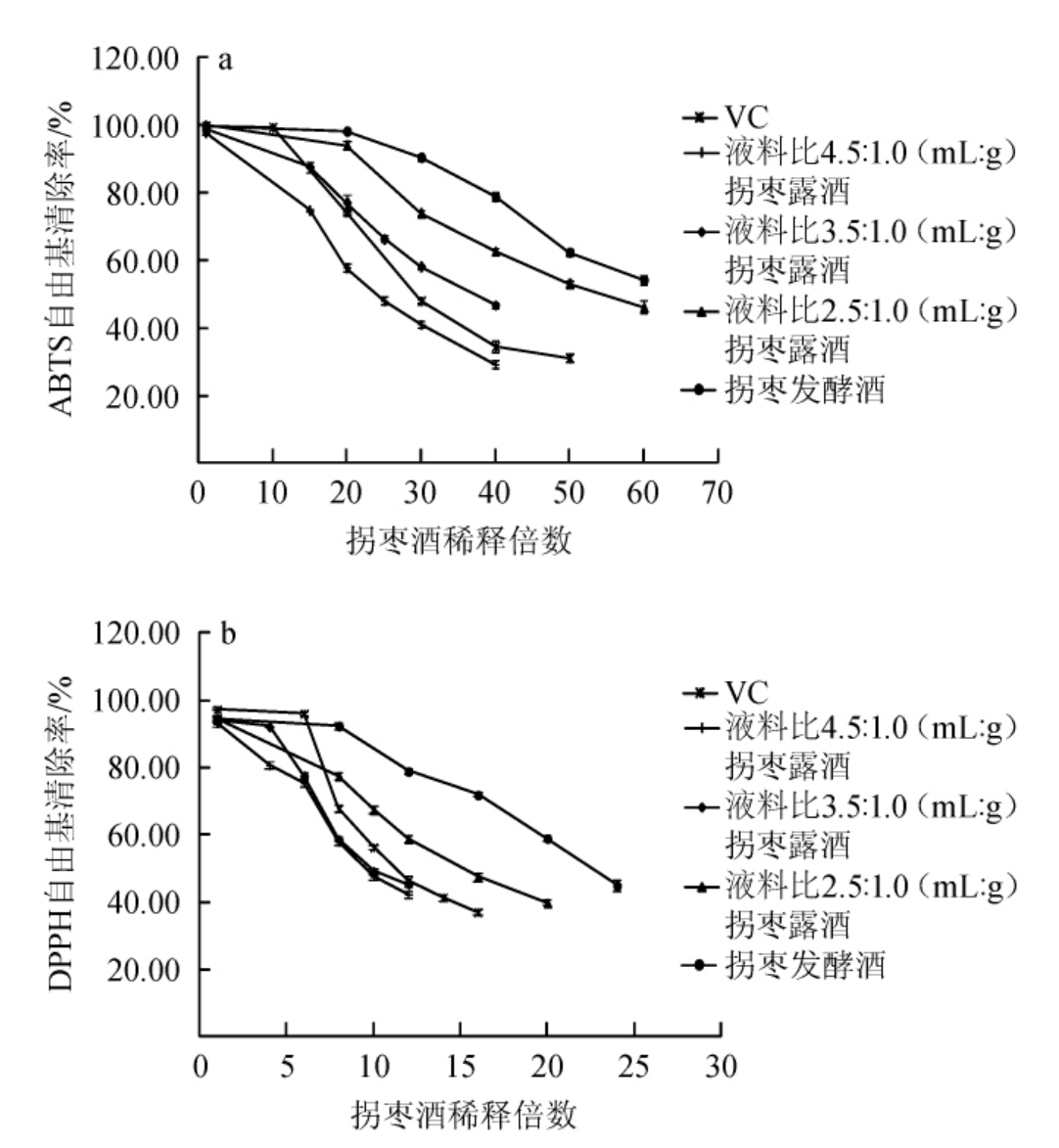
图2 拐枣酒对2,2'-联氨-双(3-乙基苯并噻唑啉-6-磺酸)二铵盐(a)及1,1-二苯基-2-苦肼基(b)自由基的清除作用
Fig.2 2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonate) (a) and 1,1-diphenyl-2-picrylhydrazyl (b) free radical scavenging ability of different Hovenia acerba alcoholic beverage samples
由图2可知,不同拐枣酒对ABTS、DPPH自由基均表现出强清除率,未稀释的4种拐枣酒对ABTS自由基的清除率接近100%,对DPPH自由基的清除率达90%以上。在两类自由基清除试验中,清除效果均以拐枣发酵酒最突出,拐枣发酵酒在稀释60倍、24倍后,对ABTS、DPPH自由基的清除率分别达50%、40%以上。将0.5 mg/mL的VC溶液按不同稀释倍数进行试验,作为拐枣酒抗氧化能力的阳性对照,随着稀释倍数增大,VC溶液对两种自由基的清除率下降迅速。在稀释50倍,即VC质量浓度为0.01 mg/mL 时,其对ABTS自由基的清除率为31.13%;在稀释16倍,即VC质量浓度为0.031 25 mg/mL时,其对DPPH自由基的清除率为37.57%。
表3 拐枣酒清除2,2'-联氨-双(3-乙基苯并噻唑啉-6-磺酸)二铵盐与1,1-二苯基-2-苦肼基自由基的IC50值
Table 3 IC50 of different Hovenia acerba alcoholic beverage samples scavenging 2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonate) and 1,1-diphenyl-2-picrylhydrazyl free radical
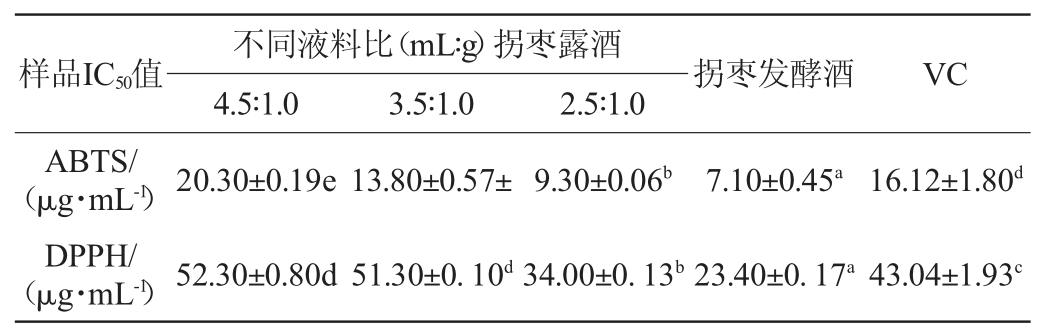
由表3可知,在DPPH自由基清除试验中,VC溶液的IC50值为(43.04±1.93)μg/mL,大于液料比为2.5∶1.0(mL∶g)的拐枣露酒和拐枣发酵酒的IC50值,表明这两种拐枣酒对DPPH自由基的清除能力要高于VC。在ABTS自由基清除能力中,VC溶液的IC50值为(16.12±1.80)μg/mL,仅低于液料比为4.5∶1.0的拐枣露酒,这表明VC对ABTS自由基的清除能力仅高于4.5∶1.0的拐枣露酒,液料比为3.5∶1.0、2.5∶1.0的拐枣露酒与拐枣发酵酒的ABTS自由基清除能力均高于VC。拐枣酒清除ABTS自由基的能力远大于DPPH自由基,与MAIEVES H A等[25]研究的拐枣多糖趋势一致。
2.3 拐枣酒中活性成分与抗氧化相关性分析
植物的抗氧化作用与其含有的活性成分如多酚、黄酮类物质的含量、种类、结构密切相关[26]。拐枣酒中总多酚、总黄酮、抗坏血酸含量与4种抗氧化试验结果的相关系数见表4。
由表4可知,3种活性成分的含量与抗氧化活性的相关性强。总多酚含量与Fe3+还原能力、氧自由基吸收能力相关性显著(P<0.05),与DPPH、ABTS自由基清除能力相关性呈极显著(P<0.01)。总黄酮与抗坏血酸含量对4种抗氧化试验都呈现出极显著的正相关影响(P<0.01)。ABTS试验中,3种活性成分对其影响大小为:总黄酮>抗坏血酸>总多酚;DPPH、FRAP、ORAC试验中,3种活性成分对其影响大小均表现为:抗坏血酸>总黄酮>总多酚。
表4 拐枣酒中总黄酮、总多酚、抗坏血酸与抗氧化活性的相关系数
Table 4 Correlations between antioxidant activities and total phenols,total flavonoids and ascorbic acid contents in Hovenia acerba alcoholic beverage samples
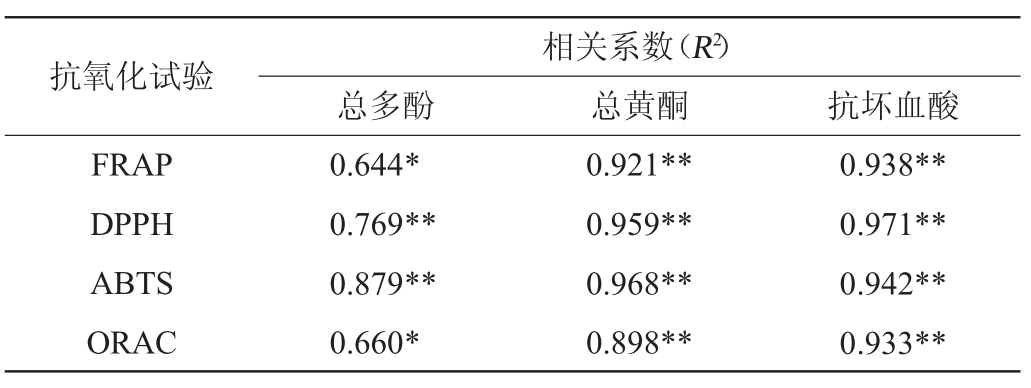
注:“*”表示显著相关(P<0.05);“**”表示极显著相关(P<0.01)。
3 结论
拐枣露酒与拐枣发酵酒中都含有较高含量的多酚、黄酮、抗坏血酸活性成分,且口感、风味良好,具有较高的营养价值,适当饮用对人体大有裨益。拐枣酒中多酚、黄酮、抗坏血酸含量均以拐枣发酵酒更高,含量分别为1.13 mg/mL、0.34mg/mL、13.39mg/L,而糖含量则以液料比为2.5∶1.0(mL∶g)的拐枣露酒更高,其总糖含量达142.03 mg/mL,还原糖含量达137.30 mg/mL。两种工艺拐枣酒均具有很强的体外抗氧化能力,其总抗氧化能力与之含有的抗坏血酸、总多酚、总黄酮含量密切相关。拐枣露酒总体风味依赖于酒基,可改善酒基风味,拐枣露酒以液料比为2.5∶1.0(mL∶g)进行泡制为宜,其口感醇和,抗氧化能力强;与拐枣露酒相比,拐枣发酵酒中活性成分含量更高,抗氧化能力更强,其ORAC值与FRAP值分别达14.69 mmol/L、11.71 mmol/L,对ABTS、DPPH自由基的清除率均>90%,清除ABTS与DPPH自由基的IC50值以VC当量抗氧化能力表示分别为7.10 μg/mL、23.40 μg/mL。
我国拐枣资源丰富,以拐枣为原料加工成拐枣发酵酒或拐枣露酒,是拐枣资源高值化利用的良好途径,对开发山区资源,带动农民致富具有积极的意义。此外,充分利用拐枣浓郁的果香,将拐枣与其他水果进行混合发酵,制成复合果酒,也将具有广阔前景。
[1]HYUN T K,EOM S H,YU C Y,et al.Hovenia dulcis-An Asian traditional herb[J].Planta Med,2010,76(10):943-949.
[2]白小琼.拐枣果梗酿酒最佳工艺条件研究初报[J].南方农业,2019,13(22):83-86.
[3]谢宗万,余友军.全国中草药名鉴[M].上册.北京:人民卫生出版社,1996
[4]廉翠翠,查圣华,王俊亮,等.雪莲培养物保健食品的抗氧化功能研究[J].食品研究与开发,2020,41(13):43-49.
[5]YANG B,WU Q J,LUO Y X,et al.Japanese grape(Hovenia dulcis)polysaccharides:New insight into extraction,characterization,rheological properties,and bioactivities[J].Int J Biol Macromol,2019,134:631-644.
[6]常甜甜,李记明,阮仕立,等.橡木桶陈酿对红葡萄酒抗氧化性的影响[J].中国酿造,2020,39(5):65-70.
[7]LIU Y,QIANG M,SUN Z,et al.Optimization of ultrasonic extraction of polysaccharides from Hovenia dulcis peduncles and their antioxidant potential[J].Int J Biol Macromol,2015,80:350-357.
[8]MORALES P,MAIEVES H A,DIAS M I,et al. Hovenia dulcis Thunb.pseudofruits as functional foods:Phytochemicals and bioactive properties in different maturity stages[J].J Funct Food,2017,29:37-45.
[9]凌圣宝.拐枣醋及其功能性研究[D].咸阳:西北农林科技大学,2012.
[10]WANG M,JIANG C,MA L,et al.Preparation,preliminary characterization and immunostimulatory activity of polysaccharide fractions from the peduncles of Hovenia dulcis[J].Food Chem,2013,138(1):41-47.
[11]郭新光,马佩选,王晓红,等.GB/T 15038—2006 葡萄酒果酒通用分析方法[S].北京:中国标准出版社,2007.
[12]李巨秀,王柏玉.福林—酚比色法测定桑椹中总多酚[J].食品科学,2009,20(18):292-295.
[13]叶兴乾,沈淑妤,黄睿,等.谷物食品总黄酮比色法定量的问题及选用原则[J].中国食品学报,2018,18(2):1-14.
[14]杨宁,王伟明,姚琳,等.3,5-二硝基水杨酸法测定发酵型果露酒中总糖含量[J].中国酿造,2018,37(1):181-184.
[15]李苇舟,李福香,何晓琴,等.酿造啤酒大麦发芽前后多酚组分变化及抗氧化活性[J].食品科学,2019,40(18):15-21.
[16]RUPASINGHE H P V,CLEGG S.Total antioxidant capacity,total phenolic content,mineral elements,and histamine concentrations in wines of different fruit sources[J].J Food Compos Anal,2007,20(2):133-137.
[17]CHENG H,FENG S,JIA X,et al.Structural characterization and antioxidant activities of polysaccharides extracted from Epimedium acuminatum[J].Carbohyd Polym,2013,92(1):63-68.
[18]JAGTAP U B,BAPAT V A.Phenolic composition and antioxidant capacity of wine prepared from custard apple(Annona squamosa L.)fruits[J].J Food Process Pres,2015,39(2):175-182.
[19]徐蔓.无花果多酚和黄酮类物质的提取及活性测定[D].太原:山西大学,2018.
[20]许亮,师俊玲,任健,等.枸杞果酒发酵过程中黄酮含量的变化[J].食品科学,2011,32(5):100-103.
[21]王菁,赵璐,肖世娣,等.不同工艺制作欧李果酒的品质比较[J].食品工业科技,2019,40(14):42-48,55.
[22]张迪,籍保平,周峰,等.食品体外抗氧化能力评价方法探讨[J].北京工商大学学报(自然科学版),2012,30(1):20-25.
[23]CAO G,PRIOR R L.Total antioxidant capacity of fruits[J].J Agr Food Chem,1996,44(3):701-705.
[24]李拥军,孙远明.单枞茶酒的抗氧化活性评价[J].中国食品添加剂,2019,30(2):104-110.
[25]MAIEVES H A,LÓPEZ-FROILÁN R,MORALES P,et al.Antioxidant phytochemicals of Hovenia dulcis Thunb.peduncles in different maturity stages[J].J Funct Food,2015,18:1117-1124.
[26]钱骅,赵伯涛,陈斌,等.桑黄子实体多糖、黄酮和多酚含量与抗氧化活性相关性[J].食品工业科技,2015,36(12):104-108.