亚麻(Linum usitatissimum L.)是一种油料作物,在食品和饲料工业中扮演着重要作用[1-2]。亚麻在世界的栽培历史可追溯到5 000年前,中国亦有600多年[3]。在河北省北部、西北各省、黑龙江和云南等地大量种植,年产量约50万t[4]。亚麻籽经过溶剂浸提法或机械压榨法制油后的产物称为亚麻籽饼粕,亚麻籽饼粕中蛋白质含量在32%~49%之间[5]。
目前蛋白质的提取方法主要有碱溶酸沉法和酶法[6]。碱溶酸沉法工艺操作简单,但是高浓度碱液会加深产品色泽,破坏产品风味,可能导致蛋白质营养价值损失,还会使赖氨酸和丙氨酸生产有毒化合物,降低赖氨酸的营养价值[7-9]。酶法反应条件较温和,能够更多保留蛋白质营养价值,而且能够降低碱溶酸沉法提取蛋白质产生的不利影响[10]。于雷等[11]对碱溶酸沉法和超声辅助双酶法提取的米糠蛋白的功能性质进行研究,考察pH值对米糠蛋白溶解度、起泡性、起泡稳定性、乳化性、乳化稳定性等功能性质的影响,以及温度对黏度的影响,结果表明,超声辅助双酶法提取的米糠蛋白的功能性质较碱法有所改善;张薇[12]将双酶复合法和碱法提取的米糠蛋白功能性质进行比较,结果也表现为双酶复合法提取的米糠蛋白的功能性质较碱溶酸沉法有所改善。因此,酶法提取的米糠蛋白质的功能性质较好。但是在亚麻蛋白方面,仅有单种提取方法研究功能性质的报道[13-14]。
本试验对碱溶酸沉法和双酶复合酶解法提取的亚麻蛋白的功能性质进行比较,同时,为了满足亚麻蛋白在各类食品中的应用,考察pH值、温度、亚麻蛋白含量及NaCl浓度四个因素对亚麻蛋白起泡性和起泡稳定性、乳化性及乳化稳定性、黏度的影响,为亚麻蛋白产品的研发及亚麻蛋白的贮藏提供理论研究基础。
1 材料与方法
1.1 材料与试剂
亚麻籽饼粕:康保光明粮油有限公司;碱性蛋白酶(50 U/mg)、α-淀粉酶(酶活性3 700 U/g):北京奥博星生物技术有限公司;大豆油(食品级):九三粮油工业集团有限公司;正己烷、氢氧化钠(均为分析纯):天津市科密欧化学试剂有限公司;盐酸(分析纯):北京化工厂。
1.2 仪器与设备
HC-3018高速离心机:安徽中科中佳科学仪器有限公司;HH-S数显恒温水浴锅:金坛市医疗仪器厂;PHS-3C酸度计:上海佑科仪表有限公司;79-1磁力加热搅拌器、HY-4A调速振荡器:常州澳华仪器有限公司;JYL-C50T九阳料理机:九阳股份有限公司;NDJ-5S旋转黏度计:上海力辰仪器科技有限公司。
1.3 方法
1.3.1 脱胶、脱脂亚麻籽饼粕的制备
亚麻籽饼粕粉碎过筛(80目),称取20 g亚麻籽饼粕粉加入400 mL水、在75 ℃的水浴锅中水浴90 min,并不断搅拌,洗胶3次,进行脱胶[15]。称脱胶后的亚麻籽饼粕的质量,加入30倍的正己烷,置于通风橱,不断振荡6 h后,静置,回收正己烷,于通风橱晾12 h即为脱胶、脱脂亚麻籽饼粕。
1.3.2 双酶复合酶解法提取亚麻蛋白
经过前期试验得到亚麻蛋白的最佳提取工艺,根据最佳工艺条件制备亚麻蛋白。取脱胶、脱脂亚麻籽饼粕,按料液比1∶15加入蒸馏水,添加2.5%的α-淀粉酶,在pH 6.0、60 ℃条件下酶解4 h,再添加1%的碱性蛋白酶,在pH 10.1、47.5 ℃条件下酶解3 h,100 ℃条件下灭酶,4 000 r/min离心15 min,取上清液壳聚糖沉淀蛋白质,4000 r/min离心15 min,蛋白质沉淀物冷冻干燥。
1.3.3 碱溶酸沉制备亚麻蛋白
脱胶、脱脂亚麻籽饼粕,按料水比1∶15加入蒸馏水,在pH 9.5、60 ℃条件下提取1.5 h,4 000 r/min离心10 min,取上清液调节pH值至4.4,静置1.5 h,4 000 r/min离心15 min,水洗蛋白质沉淀,冷冻干燥即可[14,16]。
1.3.4 亚麻蛋白等电点的确定
取等体积的9份双酶复合酶解法制备的亚麻蛋白上清液,调pH值范围为3.6~5.2,静置30 min后4 000 r/min离心20 min,吸取0.5 mL上清液,测定其蛋白质含量,吸光度值越小,上清液中的蛋白质含量越少,即沉淀中的蛋白质就越多,吸光度值最小值对应的pH值为亚麻蛋白的等电点[16]。
1.3.5 不同条件对亚麻蛋白功能性质的影响
分别测定不同pH值(2、3、4、5、6、7、8、9、10、11)、温度(20 ℃、40 ℃、60 ℃、80 ℃、100 ℃)、亚麻蛋白含量(1%、1.6%、2.2%、2.8%、3.4%)、NaCl浓度(0.25 mol/L、0.5 mol/L、1.0 mol/L、1.5 mol/L、2.0 mol/L)对亚麻蛋白乳化性和乳化稳定性、起泡性和起泡稳定性的影响。
分别测定不同pH值(2、4、6、8、10、12)、温度(20 ℃、40 ℃、60 ℃、80 ℃、100 ℃)、亚麻蛋白含量(1%、1.6%、2.2%、2.8%、3.4%)、NaCl浓度(0.25 mol/L、0.5 mol/L、1.0 mol/L、1.5 mol/L、2.0 mol/L)对亚麻蛋白黏度的影响。
1.3.6 测定方法
乳化性:取25 mL 1%的亚麻蛋白溶液与等量大豆油混合,以2 000 r/min的速度均质10 min。将乳浊液以4 000 r/min离心10 min,转入100 mL量筒,记录总体积和乳化层体积,计算乳化活性,其计算公式如下[14]:
乳化稳定性:取25 mL 1%的亚麻蛋白溶液与等量大豆油混合,以2 000 r/min的速度均质10 min。在85 ℃水浴中加热15 min破乳,然后冷却至室温,2 000 r/min离心5 min后,转移至量筒内,读取乳化层高度,计算乳化稳定性,其计算公式如下[14]:
起泡性:配制1%的亚麻蛋白溶液,以7 000 r/min的速度均质4 min,迅速转入量筒,记录泡沫总体积,计算起泡性,其计算公式如下[14]:
起泡稳定性:将均质形成的泡沫静置10 min、30 min、60 min、90 min、120 min后,分别读取剩余泡沫的体积,以10 min时的起泡稳定性为例,计算起泡稳定性,其计算公式如下[14]:
黏度:配制1%的亚麻蛋白溶液,立即采用NDJ-5S旋转式黏度计,调整转速为60 r/min,选择2号转子,测定亚麻蛋白的黏度[14]。
1.3.8 数据处理
采用SPSS 20.0软件进行数据分析,分别对双酶复合酶解法和碱溶酸沉法提取亚麻蛋白在不同条件下的结果进行显著分析,再对同一条件下,双酶复合法提取亚麻蛋白和碱溶酸沉法提取的亚麻蛋白的结果进行显著性分析。
2 结果与分析
2.1 亚麻蛋白等电点的测定
亚麻蛋白等电点的测定结果见图1。
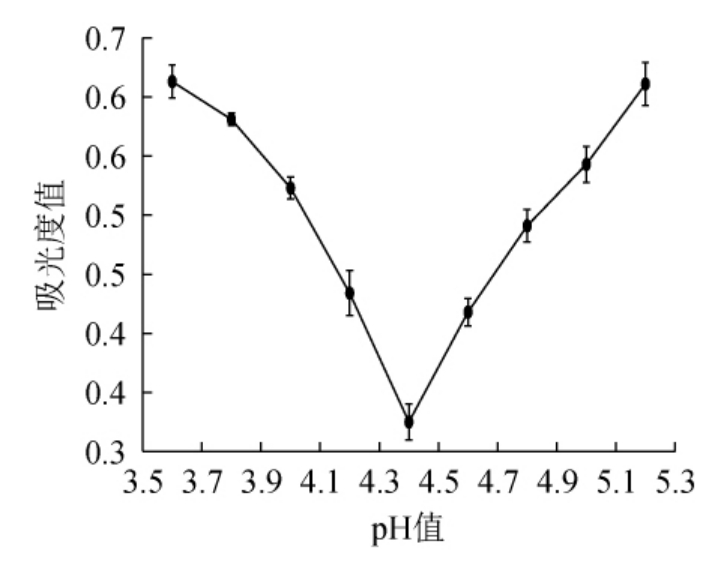
图1 亚麻蛋白等电点的测定结果
Fig.1 Determination results of isoelectric point of flax protein
由图1可知,吸光度值随着pH值的增大,呈现先下降后上升的趋势,当pH=4.4时,吸光度值最低,亚麻蛋白沉淀量最大,所以亚麻蛋白的等电点为4.4。施树[14]采用碱溶酸沉法制备亚麻蛋白,测定其等电点为4.4,与本研究测定的双酶复合酶解法制备亚麻蛋白的结果相一致。
2.2 不同影响因素对亚麻蛋白乳化性及乳化稳定性的影响
2.2.1 pH值对亚麻蛋白乳化性及乳化稳定性的影响

图2 pH值对亚麻蛋白乳化性(a)及乳化稳定性(b)的影响
Fig.2 Effect of pH on emulsifying property (a) and emulsifying stability(b) of flax protein
不同小写字母表示同一提取方法不同pH间结果差异显著(P<0.05),“*”表示不同提取方法在同一pH下的结果差异显著(P<0.05)。下同。
由图2可知,随着pH值的增加,两种方法提取的亚麻蛋白的乳化性和乳化稳定性呈现先下降后上升的趋势。于雷等[11]在测定pH值对米糠蛋白乳化性及乳化稳定性时,表现出相同的趋势。在等电点附近两种方法制备的亚麻蛋白的乳化性和乳化稳定性最差,分析原因可能是在等电点附近,蛋白质所带电荷为零,且等电点附近蛋白质的溶解度也是最低的,吸附在油-水界面的蛋白质较少,所以乳化能力表现较差[14]。在同一pH值条件下,双酶复合酶解法提取的亚麻蛋白的乳化性和乳化稳定性均显著优于碱溶酸沉法(P<0.05)。
2.2.2 温度对亚麻蛋白乳化性及乳化稳定性的影响

图3 温度对亚麻蛋白乳化性(a)及乳化稳定性(b)的影响
Fig.3 Effect of temperature on emulsifying (a) and emulsifying stability(b) of flax protein
由图3可知,两种提取方法制备的亚麻蛋白的乳化性和乳化稳定性随着温度升高均呈现先上升后下降的趋势。双酶复合酶解法提取的亚麻蛋白的乳化性优于碱溶酸沉法,而乳化稳定性仅在40 ℃时表现为双酶复合酶解法提取的亚麻蛋白显著优于碱溶酸沉法(P<0.05)。在40 ℃时,双酶复合酶解法提取的亚麻蛋白的乳化性和乳化稳定性均优于碱溶酸沉法(P<0.05)。
2.2.3 亚麻蛋白含量对亚麻蛋白乳化性及乳化稳定性的影响
由图4可知,两种方法提取的亚麻蛋白的乳化性和乳化稳定性均随着亚麻蛋白含量的增加,呈现逐渐上升的趋势。在蛋白质吸附油-水界面,蛋白质的推动力增大,能够吸附更多的蛋白质,所以形成乳状液油滴粒径减小,反而数目增多,油-水界面的面积增大,吸附更多的油,因而乳化性增大[17]。在同一亚麻蛋白含量下,双酶复合酶解法提取的亚麻蛋白的乳化性和乳化稳定性均优于碱溶酸沉法,且当亚麻蛋白含量为2.8%时,差异均显著(P<0.05)。

图4 亚麻蛋白含量对亚麻蛋白乳化性(a)及乳化稳定性(b)的影响
Fig.4 Effect of flax protein content on emulsifying (a) and emulsifying stability (b) of flax protein
2.2.4 NaCl浓度对亚麻蛋白乳化性及乳化稳定性的影响

图5 NaCl浓度对亚麻蛋白乳化性(a)及乳化稳定性(b)的影响
Fig.5 Effect of NaCl concentration on emulsifying (a) and emulsifying stability (b) of flax protein
由图5可知,亚麻蛋白的乳化性及乳化稳定性均随着NaCl浓度的增大,呈现先增大后减小的趋势。最适NaCl浓度为1.5 mol/L,低浓度的NaCl溶液能够加速蛋白质溶解,提高油-水体系中蛋白质的质量,增加油-水界面的面积,过高浓度的NaCl溶液会使蛋白质乳化液胶体的水化层变薄,降低蛋白质与水的作用,蛋白质与蛋白质分子间的疏水作用加强,吸附油-水界面的能力减弱,油滴的粒径变大,导致界面面积减小,乳化性则出现下降的趋势[18]。在同一NaCl浓度下,双酶复合酶解法提取的亚麻蛋白的乳化性及乳化稳定均优于碱溶酸沉法,且当NaCl浓度为0.5 mol/L,差异均显著(P<0.05)。
2.3 不同影响因素对亚麻蛋白起泡性及起泡稳定性的影响
2.3.1 pH值对亚麻蛋白起泡性及起泡稳定性的影响
pH值对亚麻蛋白起泡性及起泡稳定性的影响见图6。由图6可知。在等电点附近,两种方法制备的亚麻蛋白的起泡性和起泡稳定性较差。可能原因是等电点附近蛋白质的溶解度最低,形成泡沫的蛋白质减少,仅少量蛋白质被溶解参与泡沫的形成,所以亚麻蛋白的起泡性较差。并且等电点附近,蛋白质分子间的相互作用,蛋白质膜在气液界面上变厚变硬,所以起泡稳定性变差[19]。在同一pH值下,双酶复合酶解法提取的亚麻蛋白的起泡性和起泡稳定性均显著优于碱溶酸沉法(P<0.05)。
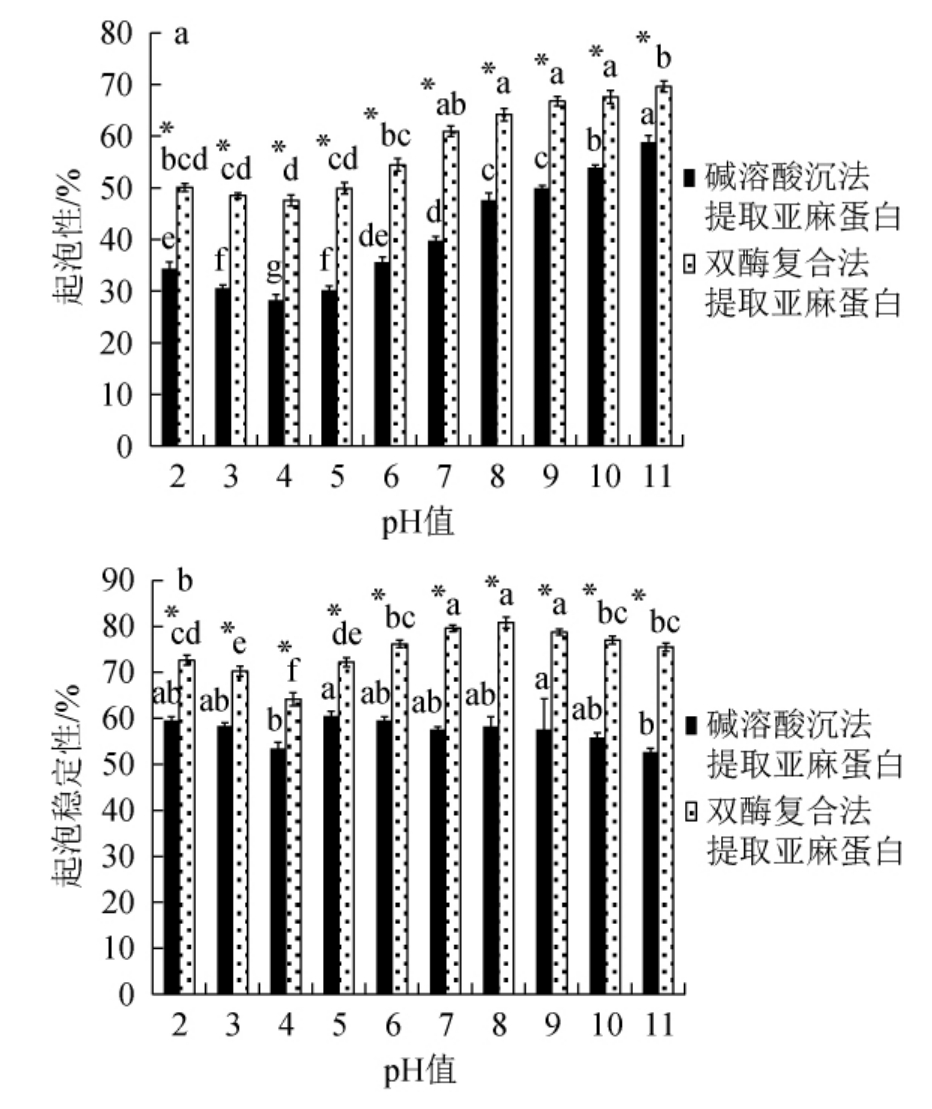
图6 pH值对亚麻蛋白起泡性(a)及起泡稳定性(b)的影响
Fig.6 Effect of pH on foaming property (a) and foaming stability (b) of flax protein
2.3.2 温度对亚麻蛋白起泡性及起泡稳定性的影响
温度对亚麻蛋白起泡性及起泡稳定性的影响见图7。由图7可知,随着温度的升高,两种方法提取的亚麻蛋白的起泡性和起泡稳定性均呈现先上升后下降的趋势,最适温度均为60 ℃。仅在40 ℃、60 ℃、100 ℃时,双酶复合酶解法提取的亚麻蛋白的起泡性显著优于碱溶酸沉法(P<0.05);同一温度下,双酶复合酶解法提取的亚麻蛋白的起泡稳定性均显著优于碱溶酸沉法(P<0.05)。
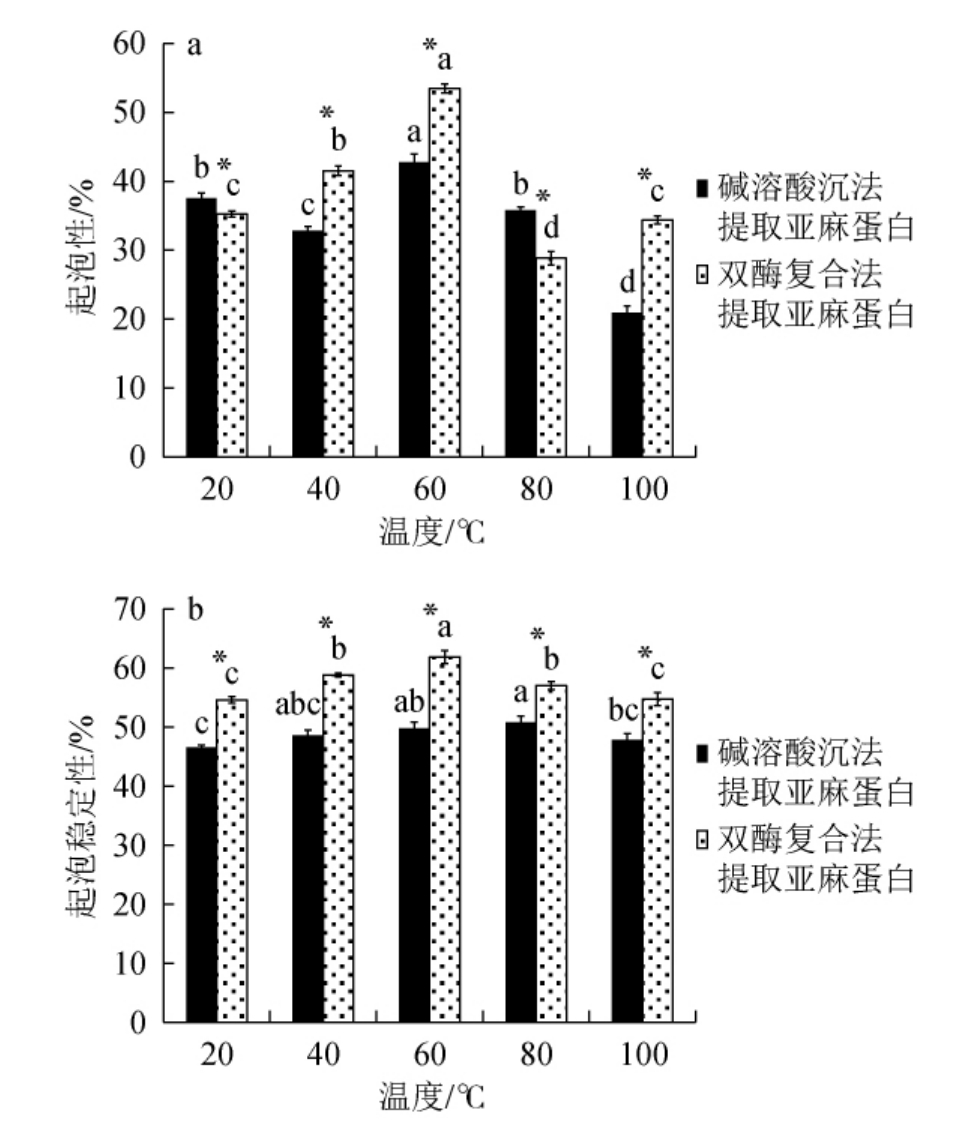
图7 温度对亚麻蛋白起泡性(a)及起泡稳定性(b)的影响
Fig.7 Effect of temperature on foaming property (a) and foaming stability (b) of flax protein
2.3.3 亚麻蛋白含量对亚麻蛋白起泡性及起泡稳定性的影响
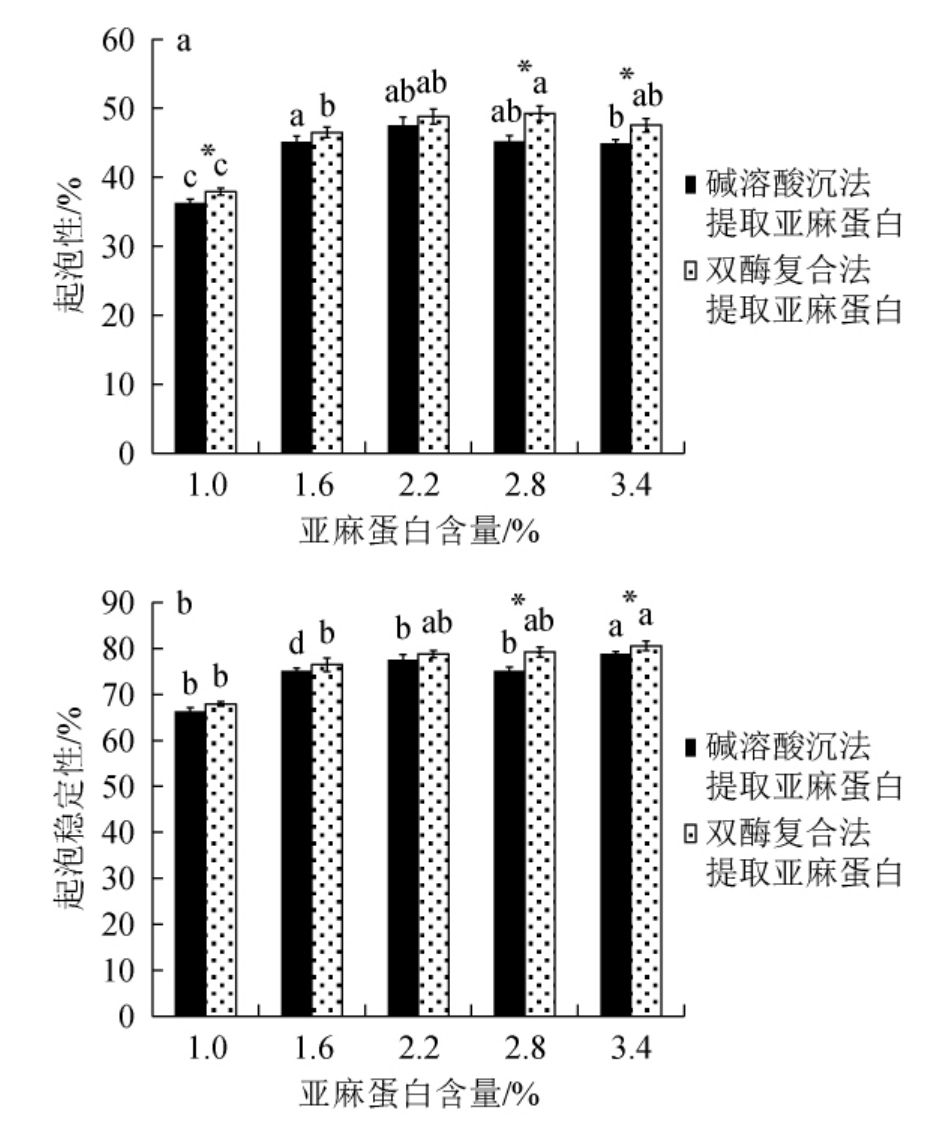
图8 亚麻蛋白含量对亚麻蛋白起泡性(a)及起泡稳定性(b)的影响
Fig.8 Effect of flax protein contents on foaming property (a) and foaming stability (b) of flax protein
亚麻蛋白含量对亚麻蛋白起泡性及起泡稳定性的影响见图8。由图8可知,随着亚麻蛋白含量的增加,亚麻蛋白的起泡性及起泡稳定性逐渐增大。在同一亚麻蛋白含量下,双酶复合酶解法提取的亚麻蛋白的起泡性及起泡稳定性均优于碱溶酸沉法,且当亚麻蛋白含量为2.8%时,差异均显著(P<0.05)。
2.3.4 NaCl浓度对亚麻蛋白起泡性及起泡稳定性的影响
NaCl浓度对亚麻蛋白起泡性及起泡稳定性的影响见图9。由图9可知,起泡性和起泡稳定性随着NaCI浓度增加出现先上升后下降趋势,虽然趋势相同,但是起泡性变化趋势较起泡稳定性趋势更陡峭。可能原因是,随着NaCI浓度的增加,亚麻蛋白的溶解度增加,所以提高了亚麻蛋白的起泡性。当NaCI浓度在0.25~1.00 mol/L范围内对亚麻蛋白的起泡性及起泡稳定性有促进作用[20],当NaCl浓度>0.5 mol/L之后,有抑制作用;当NaCl浓度在1.00 mol/L时,两种方法制备的亚麻蛋白的乳化性和乳化稳定性最佳。在同一NaCl浓度下,双酶复合酶解法提取的亚麻蛋白的起泡性及起泡稳定性均优于碱溶酸沉法,且当NaCl浓度为0.25 mol/L、0.5 mol/L时,差异均显著(P<0.05)。
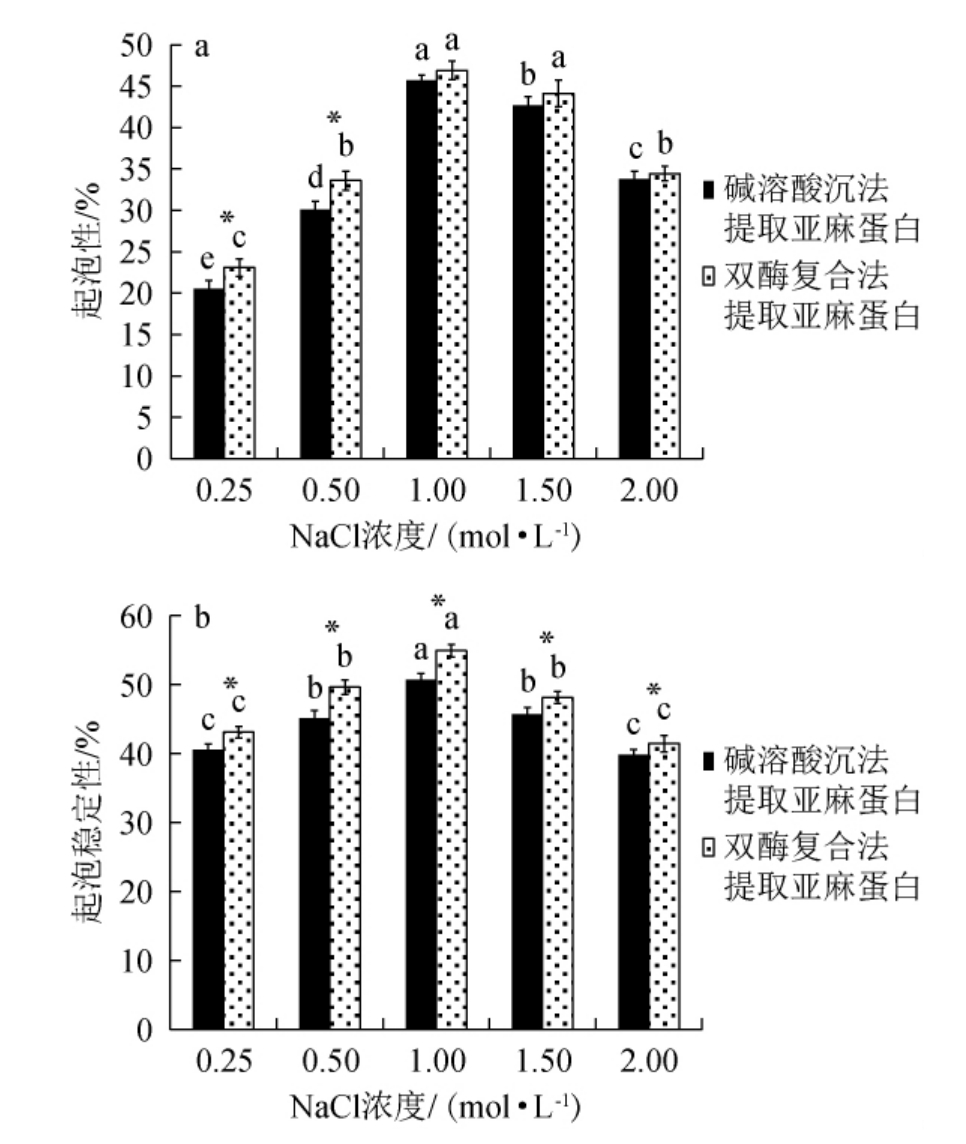
图9 NaCl浓度对亚麻蛋白起泡稳定性的影响
Fig.9 Effect of NaCl concentration on stability of flax protein foam
2.4 不同影响因素对亚麻蛋白黏度的影响
2.4.1 pH值对亚麻蛋白黏度的影响
黏度是指溶液流动的快慢程度,其不仅可以使食品中各组分更加稳定,还可以为改善产品的口感。影响流体或半流体黏度的主要因素有蛋白质分子的表面直径、温度等。pH值对亚麻蛋白黏度的影响见图10。
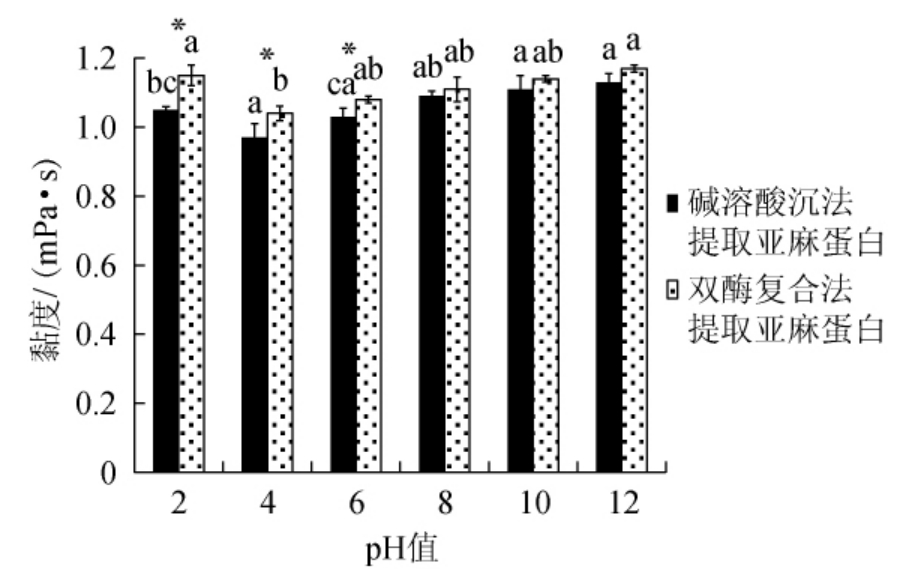
图10 pH值对亚麻蛋白黏度的影响
Fig.10 Effect of pH value on flax protein viscosity
由图10可知,亚麻蛋白的黏度在等电点附近,黏度较差,主要是因为在等电点附近,蛋白质的溶解度降低,蛋白质之间和蛋白质与溶剂之间的作用力减弱,使得阻力下降,以致亚麻蛋白黏度下将[21]。在同一pH值时,双酶复合酶解法提取的亚麻蛋白的黏度优于碱溶酸沉法,且当pH为2、4、6时,双酶复合酶解法提取的亚麻蛋白的黏度显著优于碱溶酸沉法(P<0.05)。
2.4.2 温度对亚麻蛋白黏度的影响
温度对亚麻蛋白黏度的影响见图11。

图11 温度对亚麻蛋白黏度的影响
Fig.11 Effect of temperature on flax protein viscosity
由图11可知,随着温度的升高,亚麻蛋白黏度出现下降趋势,分析原因可能是高温可增加蛋白质间能量,产生的作用力难以控制逐渐变强的分子运动,间距增大导致吸引力减小,所以黏度出现下降趋势[20]。在20 ℃黏度最佳,且在同一温度下,双酶复合酶解法提取的亚麻蛋白的黏度优于碱溶酸沉法,但差异性不显著(P>0.05)。
2.4.3 亚麻蛋白含量对亚麻蛋白黏度的影响
蛋白质分子是影响蛋白质黏度的主要因素,这与蛋白质分子固有特性、蛋白质与溶剂间的作用还有蛋白质间的作用有关,它们决定了黏度的大小。亚麻蛋白含量对亚麻蛋白黏度的影响见图12。
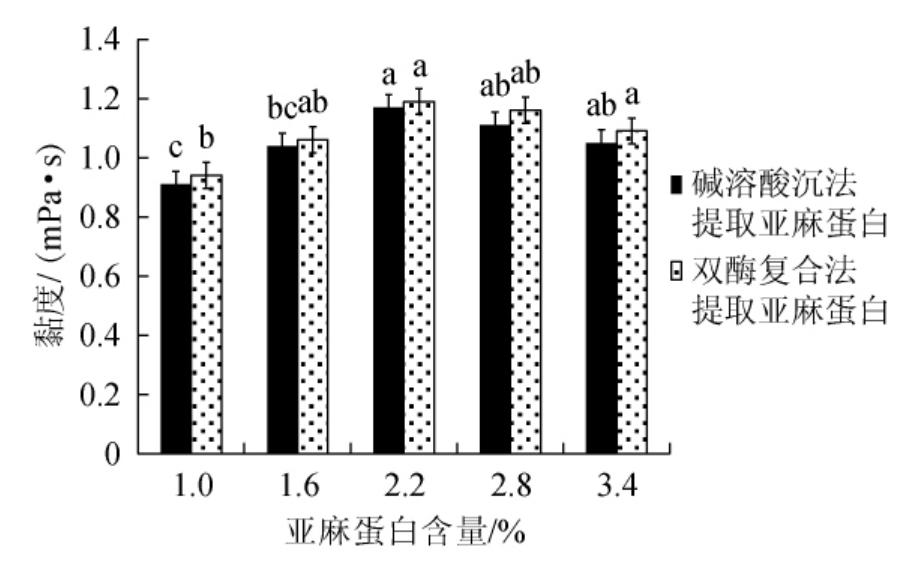
图12 亚麻蛋白含量对亚麻蛋白黏度的影响
Fig.12 Effect of flax protein contents on flax protein viscosity
由图12可知,两种方法提取的亚麻蛋白的黏度随着亚麻蛋白含量的增加出现先上升后下降的趋势,当亚麻蛋白含量为2.2%时,亚麻蛋白的黏度最大。当亚麻蛋白含量在1.0%~2.2%时,黏度出现上升的趋势,随着亚麻蛋白含量的增加,蛋白质与溶剂和蛋白质与蛋白质间的作用增加,黏度也随着增大。当亚麻蛋白含量>2.2%之后,大量蛋白质不利于蛋白质的充分展开所以抑制蛋白质摩擦力,从而黏度下降[20]。在同一亚麻蛋白含量下,双酶复合酶解法提取的亚麻蛋白的黏度优于碱溶酸沉法,但差异不显著(P>0.05)。
2.4.4 NaCl浓度对亚麻蛋白黏度的影响
NaCl浓度对亚麻蛋白黏度的影响见图13。

图13 NaCl浓度对亚麻蛋白黏度的影响
Fig.13 Effect of NaCl concentration on flax protein viscosity
当NaCl浓度在0.25~1.00 mol/L之间,亚麻蛋白黏度随NaCl浓度的增加出现上升趋势。原因可能是低浓度的NaCl溶液加速蛋白质的溶解,增加蛋白质之间、蛋白质与溶剂之间连结的网络,使阻力变大,黏度增大;当NaCl浓度>1.00 mol/L之后,蛋白质与蛋白质的结合物质发生沉淀,溶液中的蛋白质分子减少,所以黏度下降[20-21];当NaCl浓度为1.00 mol/L时,两种方法提取的亚麻蛋白的黏度最高。在同一NaCl浓度下,双酶复合酶解法提取的亚麻蛋白的黏度优于碱溶酸沉法,且在NaCl浓度为1.00 mol/L时,具有显著性差异(P<0.05)。
3 结论
本研究利用双酶复合酶解法提取的亚麻蛋白的乳化性、乳化稳定性、起泡性、起泡稳定性和黏度较碱溶酸沉法更优,且不同因素对亚麻蛋白功能性质具有一定的影响。双酶复合酶解法提取的亚麻蛋白的等电点为4.4,当pH值11、温度60 ℃、亚麻蛋白含量3.4%和NaCl浓度1.5 mol/L时,亚麻蛋白乳化性最佳;当pH值11、温度40 ℃、亚麻蛋白含量3.4%和NaCl浓度1.5 mol/L,亚麻蛋白乳化稳定性最佳;当pH值11、温度60 ℃、亚麻蛋白含量2.8%和NaCl浓度1.0 mol/L时,亚麻蛋白起泡性最佳;当pH值8、温度60 ℃、亚麻蛋白含量3.4%和NaCl浓度1.0 mol/L时,亚麻蛋白起泡稳定性最佳;当pH值2、温度20 ℃、亚麻蛋白含量2.2%和NaCl浓度1.0 mol/L时,亚麻蛋白黏度最佳。
[1]KAJLA P,SHARMA A,SOOD D R.Flaxseed-a potential functional food source[J].Food Sci Technol,2015,52(4):1857-1871.
[2]GOYAL A,SHARMA V,UPADHYAY N,et al.Flax and flaxseed oil:an ancient medicine &modem functional food[J]. Food Sci Technol,2014,51(9):1633-1653.
[3]帅瑞艳,刘飞虎.亚麻起源及其在中国的栽培与利用[J].中国麻业科学,2010,32(5):282-286.
[4]王玉富,邱财生,龙松华,等.中国纤维亚麻生产现状与研究进展及建议[J].中国麻业科学,2013,35(4):214-218.
[5]翟双双,李孟孟,冯佩诗,等.四川白鹅、樱桃谷肉鸭对不同产地亚麻饼粕养分利用率的影响[J].动物营养学报,2016,28(7):2147-2153.
[6]曹阔.小米谷糠蛋白的分离提取及功能性质研究[D].张家口:河北北方学院,2019.
[7]郝文来.基于碱溶酸沉法的亚麻籽油蛋白分离工艺优化[J].当代化工,2019,48(10):2285-2287.
[8]SHIH F F,DAIGLE K W.Preparation and characterization of rice protein isolates[J].JAm Oil Chem Soc,2000,77(8):885-889.
[9]王萍,位治国,郭金英,等.碱溶酸沉法提取梧桐子蛋白质的工艺[J].食品工业,2019,40(10):110-113.
[10]王雪飞,于国萍,徐红华.不同酶类提取米糠蛋白的研究[J].中国粮油学报,2004,19(1):8-11.
[11]于雷,张薇,乔筱童,等.超声波辅助双酶法与碱法提取米糠蛋功能特性的比较研究[J].食品科技,2014,39(11):256-261.
[12]张薇.超声波辅助双酶法提取米糠蛋白及其应用的研究[D].长春:吉林农业大学,2014.
[13]许晖,郑桂富.金属离子和pH 对亚麻蛋白溶解性和持水力的影响[J].食品工业科技.2013(4):21-23.
[14]施树.胡麻分离蛋白及其性质的研究[D].重庆:西南大学,2008.
[15]张泽生,张兰,徐慧,等.亚麻粕中亚麻胶的提取与纯化[J].食品研究与开发,2010,31(9):234-236.
[16]许光映,胡晓军,李群,等.亚麻分离蛋白提取工艺的研究[J].中国粮油学报,2013,28(3):45-48.
[17]杨柳,江连洲,李杨,等.水酶法提取的大豆蛋白功能特性研究[J].大豆科技,2019(S1):174-178.
[18]许尨.大米蛋白降解改性及起泡性能的研究[D].武汉:湖北工业大学,2013.
[19]李娟.非水溶性茶叶蛋白质提取及理化性质研究[D].乌鲁木齐:新疆农业大学,2003.
[20]李雪,白新鹏,曹君,等.仙人掌果籽蛋白提取及功能性质研究[J].中国油脂,2018,43(5):39-43.
[21]莫重文.蛋白质化学与工艺学[M].北京:北京化工业出版社,2007:87-92.