2,4,6-三氯苯甲醚(2,4,6-trichloroanisole,TCA)是造成葡萄酒软木塞污染的主要成分之一,它是由一类生长在软木塞内的霉菌,为了去除其生长环境中的2,4,6-三氯苯酚,作为一种脱毒机制而产生的物质[1-2]。因其具有强烈的泥土和发霉气味[3-4],痕量的TCA便会令人不悦。美国食品药品监督管理局的研究报告表明,消费者对于TCA的阈值水平一般在3.1 ng/L[5]。瓶装后经木塞迁移到葡萄酒中的TCA比葡萄酒本身还稳定,而且该过程基本是不可逆的[6-7],根据测算,全球每年因TCA污染而造成的葡萄酒损失可达100亿美元[8]。
TCA在软木塞和葡萄酒中的含量都非常低(ng/L水平),因此,高效的前处理萃取技术和灵敏度极高的检测方法是必不可少的,应用最多的是顶空固相微萃取结合气相色谱-质谱联用法或气相色谱-电子捕获检测器法[9-10]。目前,国家尚未明确规定软木塞中TCA的限量标准,但各葡萄酒企业对木塞中TCA的限量比较低,基本都在2 ng/L,有些天然塞要求在1 ng/L。通常使用分析结果作为决策依据时,必须对结果的可靠性有所了解[11]。因此,木塞中TCA的迁移量不仅要求检测准确,而且在限量值附近的结果可靠。不确定度是对测定结果的信息补充,反映了测量结果可信程度的高低;它一方面便于评定结果的可靠性,另一方面也可增强实验室间或实验室内部测量结果间的可比性[12]。
本研究参照中国合格评定国家认可委员会CNASGL006:2019《化学分析中不确定度的评估指南》[12]、中华人民共和国国家计量技术规范JJF1059.1—2012《测量不确定度评定与表示》[13]及国际标准化组织ISO 20752—2014《cork stoppers—determination of releasable 2,4,6-trichloroanisol(TCA)》[14],对软木塞中TCA检测的不确定度进行评定,旨在为评价测量数据的准确性、可靠性提供科学依据,并通过分析不确定度的主要影响因素,后期重点把控以确保检测结果的准确、可靠。
1 材料与方法
1.1 材料与试剂
试验所用软木塞由某生产厂商提供,每批次取样40个,密封包装后备用。
本方法使用符合GB/T 6682—2008《分析实验室用水规格和试验方法》规定的一级水;四无乙醇(色谱纯):天津市光复精细化工研究所;无水乙醇、氯化钠(分析纯):国药集团化学试剂有限公司;2,4,6-三氯苯甲醚(TCA)标品(纯度99.5%)、2,4,6-三氯苯甲醚(TCA)-D5标品(纯度98.8%):Dr.EhrenstorferGmbh公司。固定相为5%二苯基95%二甲基聚硅氧烷共聚物:美国瑞斯泰克公司。
1.2 仪器与设备
GC-MS QP2010Ultra气相色谱-质谱联用仪:日本岛津公司;固相微萃取(solid phase micro-extraction,SPME)装置;100 μm PDMS SPME萃取头:上海安谱实验科技股份有限公司;低极性石英毛细管柱(30 m×0.25 mm×0.25 μm)。
1.3 实验方法
1.3.1 TCA系列标准溶液配制
准确称取TCA标品10 mg,用四无乙醇定容至100 mL容量瓶,质量浓度为100 mg/L,作为TCA标准储备液。用12%乙醇溶液逐级稀释至质量浓度为100 ng/L,再分别配制质量浓度为20 ng/L、10 ng/L、5 ng/L、2.5 ng/L、1 ng/L、0.5 ng/L系列标准溶液。
1.3.2 TCA-D5内标工作液配制
准确称取TCA-D5标品10mg,用四无乙醇定容至100mL容量瓶,质量浓度为100 mg/L,作为TCA-D5内标储备液。用12%乙醇溶液逐级稀释至质量浓度为1 000 ng/L,作为TCA-D5内标工作液。
1.3.3 样品处理
在室温下将20个软木塞置于1 L广口瓶内,倒入乙醇溶液直至充满广口瓶,浸泡24 h后取出浸提液,作为样品溶液。称取1.5 g氯化钠于20 mL顶空样品瓶中,加入5 mL样品溶液和0.1 mL的TCA-D5内标工作液,压盖,备用。
1.3.4 仪器参数设置
固相微萃取:平衡温度40 ℃,平衡时间5 min,搅拌速度250 r/min;萃取温度40 ℃,萃取时间30 min;解吸温度250 ℃,解吸时间5 min;萃取头老化温度260 ℃,老化时间1 min。
进样口温度:250℃。升温程序:初始柱温70℃,以10℃/min升温至160 ℃;再以25 ℃/min升温至250 ℃,保持3 min。进样方式:不分流进样,1 mL/min。载气:高纯氦气(He)。色谱与质谱接口温度:250 ℃;离子源温度:230 ℃;溶剂延迟时间7 min。
1.3.5 数学模型的建立
根据ISO 20752—2014的测定原理及检测过程,并参考CNAS-GL006:2019[12]和JJF1059.1—2012[13],待测物中TCA含量(ng/L)的计算公式如下:
式中:X为样品中TCA的质量浓度,ng/L;f为TCA的相对校正因子;A为样品中TCA的峰面积;Ai为添加于样品中内标TCA-D5的峰面积;I为内标物的质量浓度(添加在样品中),ng/L;Asi为标样f值测定时内标TCA-D5的峰面积;As为标样f值测定时TCA的峰面积;c为标样中TCA的质量浓度,ng/L;csi为内标物TCA-D5的浓度(添加在标样中),ng/L。
1.3.6 不确定度来源分析
通过对检测过程和数学模型的分析,影响木塞中TCA含量不确定度的因素有:(1)重复性测定引入的不确定度;(2)样品加标回收率产生的不确定度;(3)标准系列配制引入的不确定度(包括:标准物质和内标物质纯度、标准物质和内标物质称量、标准物质和内标物质稀释、标准溶液系列配制)[15-17];(4)标准曲线拟合引入的不确定度;(5)样品制备引入的不确定度(包括:12%乙醇溶液配制、样品取样、添加内标物)。木塞中TCA含量测定不确定度分量因果关系见图1。

图1 不确定度分量因果关系图
Fig.1 Causality diagram of uncertainty components
2 结果与分析
2.1 各分量不确定度的计算
2.1.1 重复性测定引入的不确定度
与测量结果直接相关的重复性测量过程,包括样品的均匀性测量、设备的重复性以及样品前处理过程的重复性,这一分量可由测量结果的重复性表示。在重复条件下对某一木塞浸提液进行8次平行试验,测量数据见表1。
表1 重复性试验测量结果
Table 1 Determination results of repeated tests

测量结果重复性引入的标准不确定度![]()
![]() ,相对标准不确定度
,相对标准不确定度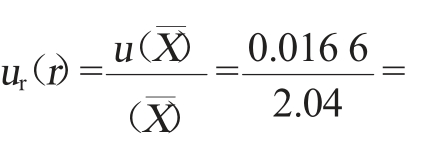 0.008 1。
0.008 1。
2.1.2 样品加标回收率引入的不确定度
在本底值为2.04 ng/L的样品溶液中加入TCA标准溶液,加入量为2.00 ng/L,并重复测定6次,测得值及回收率如表2所示。
表2 样品回收率测定结果
Table 2 Determination results of recovery rates of samples
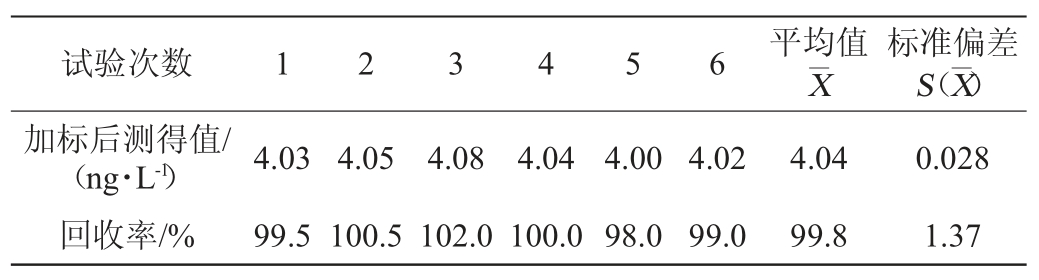
回收率平均值的标准不确定度u(r′)=![]() 0.559 3,其相对标准不确定度为ur(r′)=
0.559 3,其相对标准不确定度为ur(r′)=![]() 0.005 6。
0.005 6。
2.1.3 标准溶液配制引入的相对不确定度
(1)标准物质和内标物质纯度引入的相对不确定度
TCA标准品的纯度为99.5%,扩展不确定度为0.5%(k=2);TCA-D5标准品的纯度为98.8%,扩展不确定度为1.0%(k=2)。则由标品纯度引入的相对不确定度[18-19]分别为:

(2)标准物质和内标物质称量引入的相对不确定度
配制TCA与TCA-D5标准储备液时需称量标品各0.01 g,要求使用的天平最小分度为0.01 mg。JJG 1036—2008《电子天平检定规程》[20]规定,该准确级的天平在0.01~5.00 g称量的最大允差为±0.05 mg,与天平检定证书结果一致。属均匀分布,所以相对不确定度分别为:
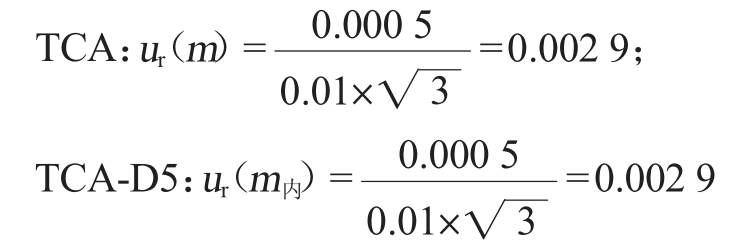
(3)标准物质和内标物质稀释引入的相对不确定度
标品:称取TCA标品0.01 g,用四无乙醇定容至100 mL容量瓶,TCA标准储备液质量浓度为100mg/L;之后用12%乙醇溶液逐级稀释至TCA质量浓度为100ng/L(1mL→100 mL,1mL→100 mL,1 mL→100 mL)。
第一步所使用的100 mL容量瓶,经校准符合A 级[21],其允差为±0.10 mL,以三角分布计![]() ,由此引入的不确定度为
,由此引入的不确定度为![]() =0.04,相对不确定度为:ur(d0)=
=0.04,相对不确定度为:ur(d0)=![]() 实验室温度控制在(20±2)℃,乙醇的体积膨胀系数为7.5×10-4/℃,假设温度变化呈均匀分布,k=
实验室温度控制在(20±2)℃,乙醇的体积膨胀系数为7.5×10-4/℃,假设温度变化呈均匀分布,k=![]() ,则由温度引起体积变化的不确定度[22]为:u(t0)=
,则由温度引起体积变化的不确定度[22]为:u(t0)=![]() =0.09,相对不确定度为:ur(t0)=
=0.09,相对不确定度为:ur(t0)=![]() 0.000 9。则TCA标品定容引入的相对不确定度为:ur(D0)=
0.000 9。则TCA标品定容引入的相对不确定度为:ur(D0)=![]()
第二步逐级稀释引入的相对不确定度分量见表3。
表3 2,4,6-三氯苯甲醚标准储备液逐级稀释引入的不确定度
Table 3 Uncertainty introduced by successive dilution of 2,4,6-trichloroanisole standard reserve solution

注:实验所用容量瓶、吸量管、移液器经检定全部合格,符合相应级别,因此其最大容量允差均参照相应规程[21,23-24]。12%乙醇溶液的体积膨胀系数根据乙醇和水(2.08×10-4/℃)的近似换算,为2.73×10-4/℃。
由表3可知,一级稀释引入的相对不确定度为:
同理,二级稀释引入的相对不确定度为:
三级稀释引入的相对不确定度为:ur(D3)=0.002 9。
综上,标准物质TCA稀释引入的相对不确定度ur(D)=![]()
内标:称取TCA-D5标品0.01 g,用四无乙醇定容至100mL容量瓶,TCA标准储备液质量浓度为100 mg/L;之后用乙醇溶液逐级稀释至TCA-D5质量浓度为1 000 ng/L(2 mL→100 mL,2 mL→100 mL,2.5 mL→100 mL)。
由表4可知,TCA-D5标品定容引入的相对不确定度为:
表4 2,4,6-三氯苯甲醚内标物质逐级稀释引入的不确定度
Table 4 Uncertainty introduced by successive dilution of 2,4,6-trichloroanisole-D5 internal standard reserve solution
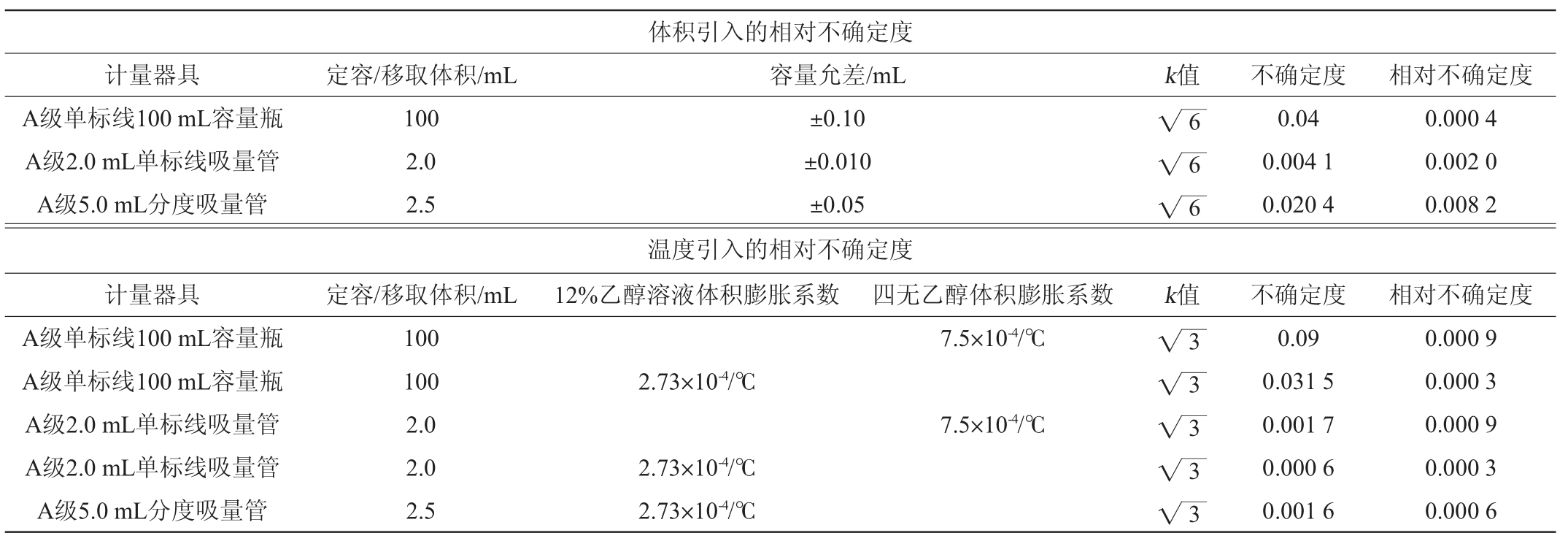
一级稀释引入的相对不确定度为:
同理,二级稀释引入的相对不确定度为:
三级稀释引入的相对不确定度为:ur(D3内)=0.008 2。
综上,内标物质TCA-D5稀释引入的相对不确定度![]()
(4)标准溶液系列配制引入的相对不确定度
配制20 ng/L的标准溶液引入的相对不确定度为ur(p20)=![]() 同理ur(p10)=0.012 5,ur(p5)=0.014 8,ur(p2.5)=0.021 8,ur(p1)=0.016 7,ur(p0.5)=0.036 5。因此,标准溶液系列配制引入的相对不确定度为:ur(p)=
同理ur(p10)=0.012 5,ur(p5)=0.014 8,ur(p2.5)=0.021 8,ur(p1)=0.016 7,ur(p0.5)=0.036 5。因此,标准溶液系列配制引入的相对不确定度为:ur(p)=![]()
表5 2,4,6-三氯苯甲醚系列标准溶液配制引入的不确定度
Table 5 Uncertainty introduced in the preparation of 2,4,6-trichloroanisole series standard solution

由于标准溶液配制完成后,需分别取5 mL标液、100 L内标加入样品瓶。则:
(a)标准溶液取样引入的相对不确定度
用A级5 mL单标线吸量管移取标准溶液,最大容量允差为±0.015 mL,按均匀分布考虑,k=![]() ,由此引入的相对不确定度为ur(V)=
,由此引入的相对不确定度为ur(V)=![]() =0.001 7。实验室温度控制在(20±2)℃,12%乙醇溶液的体积膨胀系数为2.73×10-4/℃,假设温度变化呈均匀分布,k=
=0.001 7。实验室温度控制在(20±2)℃,12%乙醇溶液的体积膨胀系数为2.73×10-4/℃,假设温度变化呈均匀分布,k=![]() ,则由温度引起体积变化的相对不确定度为:ur(t)=
,则由温度引起体积变化的相对不确定度为:ur(t)=![]() 。则标准溶液取样引入的相对不确定度
。则标准溶液取样引入的相对不确定度![]() 0.001 7。
0.001 7。
(b)添加内标物质引入的相对不确定度
用100 μL移液器移取内标液100 μL,最大容量允差为±2.0 μL,按均匀分布考虑,k=![]() ,由此引入的相对不确定度为ur(V)=
,由此引入的相对不确定度为ur(V)=![]() =0.011 5。实验室温度控制在(20±2)℃,12%乙醇溶液的体积膨胀系数为2.73×10-4/℃,假设温度变化呈均匀分布,k=
=0.011 5。实验室温度控制在(20±2)℃,12%乙醇溶液的体积膨胀系数为2.73×10-4/℃,假设温度变化呈均匀分布,k=![]() ,则由温度引起体积变化的相对不确定度为:ur(t)=
,则由温度引起体积变化的相对不确定度为:ur(t)=![]() 。则添加内标物质引入的相对不确定度ur(V内)=
。则添加内标物质引入的相对不确定度ur(V内)=![]() 0.011 5。
0.011 5。
综上可知,标准系列溶液上仪器之前,因取标样和添加内标物引入的相对不确定度为:
所以,标准溶液系列配制这一步最终引入的相对不确定度为:
由2.1.3(1)~(4)可知,标准溶液系列配制全过程引入的相对不确定度为:ur(P总)=![]()
![]() 0.060 9。
0.060 9。
2.1.4 标准曲线拟合引入的相对不确定度
以TCA与TCA-D5的峰面积比为纵坐标,TCA浓度为横坐标,所得标准曲线回归方程为:Y=0.066 3X;线性相关系数R2为:0.999 9。标准曲线产生的不确定度源于标准曲线残差的标准偏差,残差为测量值Y与标准曲线拟合值Y′之差的绝对值![]() 。TCA标准曲线残差计算见表6。
。TCA标准曲线残差计算见表6。
表6 2,4,6-三氯苯甲醚标准曲线残差计算
Table 6 Calculation of residuals for 2,4,6-trichloroanisole standard curve
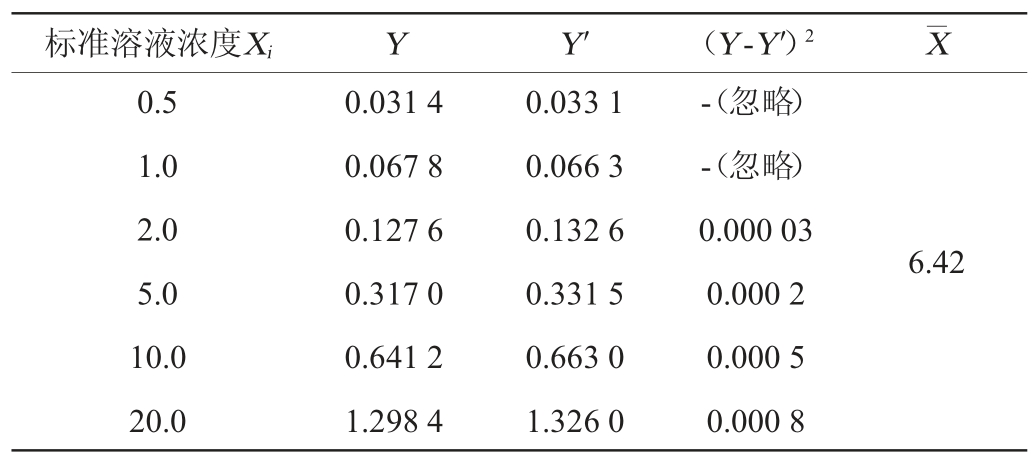
标准曲线峰面积比残差的标准差![]() 0.000 4,n为标准样品测试次数6。
0.000 4,n为标准样品测试次数6。
标准曲线拟合引入的标准不确定度根据公式u(f)=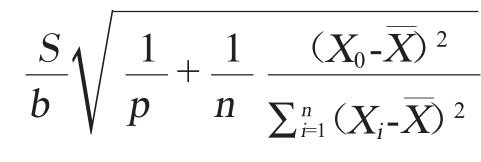 计算,b为斜率,p为样品X0的测试次数(本实验测定8次),X¯为标准溶液的平均质量浓度。则u(f)=0.003 6(X0=2.04 ng/L),由标准曲线拟合引入的相对标准不确定度ur(f)=
计算,b为斜率,p为样品X0的测试次数(本实验测定8次),X¯为标准溶液的平均质量浓度。则u(f)=0.003 6(X0=2.04 ng/L),由标准曲线拟合引入的相对标准不确定度ur(f)=![]()
2.1.5 样品制备引入的相对不确定度
(1)12%乙醇溶液配制引入的相对不确定度
由于TCA的迁移量与乙醇浓度有关,因此应考虑12%乙醇溶液配制引入的相对不确定度。用250 mL量筒移取乙醇240 mL,容量允差为±1.0 mL,按均匀分布考虑,k=![]() 由此引入的相对不确定度为ur(V)=
由此引入的相对不确定度为ur(V)=![]() =0.002 4;实验室温度控制在(20±2)℃,乙醇的体积膨胀系数为7.5×10-4/℃,假设温度变化呈均匀分布,k=
=0.002 4;实验室温度控制在(20±2)℃,乙醇的体积膨胀系数为7.5×10-4/℃,假设温度变化呈均匀分布,k=![]() ,则由温度引起体积变化的相对不确定度为:ur(t)=
,则由温度引起体积变化的相对不确定度为:ur(t)=![]() 。因此,由量筒移取引入的相对不确定度ur(量筒)=
。因此,由量筒移取引入的相对不确定度ur(量筒)=![]() 0.002 6。
0.002 6。
将乙醇定容至A级2000mL容量瓶,容量允差为±0.6mL,按均匀分布考虑,k=![]() ,由此引入的相对不确定度为
,由此引入的相对不确定度为![]() =0.000 2;实验室温度控制在(20±2)℃,12%乙醇溶液的体积膨胀系数为2.73×10-4/℃,假设温度变化呈均匀分布,k=
=0.000 2;实验室温度控制在(20±2)℃,12%乙醇溶液的体积膨胀系数为2.73×10-4/℃,假设温度变化呈均匀分布,k=![]() ,则由温度引起体积变化的相对不确定度为:ur(t)=
,则由温度引起体积变化的相对不确定度为:ur(t)=![]() 。因此,由定容引入的相对不确定度ur(定容)
。因此,由定容引入的相对不确定度ur(定容)![]()
12%乙醇溶液配制引入的相对不确定度ur(溶)=![]()
(2)样品取样引入的相对不确定度
由2.1.3(4)(a)可知,样品取样引入的相对不确定度ur(样)![]()
(3)添加内标物质引入的相对不确定度
由2.1.3(4)(b)可知,添加内标物质引入的相对不确定度ur(内)![]()
综上,样品制备引入的相对不确定度ur(s)=![]() 0.011 9。
0.011 9。
2.2 合成标准不确定度
TCA检测过程相对不确定度分量见表7。
表7 2,4,6-三氯苯甲醚相对不确定度分量
Table 7 Relative uncertainty subscale of 2,4,6-trichloroanisole

合成相对标准不确定度为
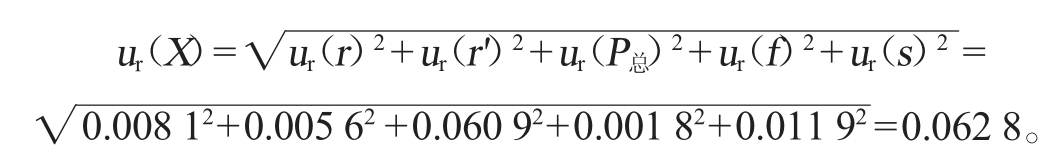
试样中TCA含量的平均值X=2.04 ng/L,则标准不确定度![]()
2.3 扩展不确定度的评定
根据CNAS-GL006:2019[12],取置信区间P=95%,包含因子k=2;根据公式扩展不确定度U=uc(X)×2,则TCA的扩展不确定度为UTCA=0.26。最终检测结果可表示为:TCA含量X=(2.04±0.26)ng/L,k=2。
3 结论
本文采用顶空固相微萃取结合气相色谱-质谱联用仪对木塞中TCA含量进行测定,并对该过程可能引入不确定度的因素进行深入考量、评定。结果表明,标准溶液系列配制过程引入的不确定度最大,其次是内标物质添加过程;而重复性测定、加标回收率、标品稀释等过程引入的不确定度相对较小,标品称量、样品取样、乙醇溶液配制等引入的不确定度可忽略不计。当木塞中TCA迁移量为2.04 ng/L时,其扩展不确定度为0.26 ng/L(k=2)。因此,实验过程中可通过提高实验人员的操作水平、定期校准玻璃仪器、严格控制操作环境温度、定期核查气质联用仪等来减小测量不确定度,从而提高检测结果的准确度、可靠性。
[1]PRAK S,GUNATA Z,GUIRAUD J P,et al.Fungal strains isolated from cork stoppers and the formation of 2,4,6-trichloroanisolse involved in the cork taint of wine[J].Food Microbiol,2007,24(3):271-280.
[2]钟其顶,刘明,熊正河,等.红葡萄酒中2,4,6-三氯苯甲醚(TCA)感官阈值的研究[J].中外葡萄与葡萄酒,2010(9):13-16.
[3]潘秋红,段长青,王军,等译.葡萄酒化学[M].北京:科学出版社,2019:164-167.
[4]RIU M,MESTRES M,BUSTO O,et al.Determination of 2,4,6-trichloroanisole in wines by headspace solid-phase microextraction and gas chromatography-electron-capture detection[J].J Chromatogr A,2002,977(1):1-8.
[5]PRESCOTT J,NORRIS L,KUNST M,et al.Estimating a"Consumer Rejection Threshold"for cork taint in white wine[J].Food Qual Prefer,2005,16(4):345-349.
[6]SEFTON M A,SIMPSON R F.Compounds causing cork taint and the factors affecting their transfer from natural cork closures to wine-a review[J].Aust J Grape Wine Res,2005,11:226-240.
[7]余蕾.葡萄酒酿造与品鉴[M].成都:西南交通大学出版社,2017:34-36.
[8]FULLER P.Cork taint-closing in on an industry problem[J]. Aust New Zealand Wine Ind J,1995,10:58-60.
[9]张亚莲,柳菡,王岁楼,等.葡萄酒和软木塞中2,4,6-三氯苯甲醚检测方法的研究进展[J].食品科学,2014,35(15):304-308.
[10]张哲琦.葡萄酒软木塞中TCA 检测方法的建立及迁移规律研究[D].石家庄:河北科技大学,2015.
[11]中国合格评定国家认可委员会.化学分析中不确定度的评估指南:CNAS-GL006:2019[S].北京:中国计量出版社,2019.
[12]李静,张居舟,余晓娟,等.超高效液相色谱-串联质谱法测定豆芽中植物生长调节剂残留量的不确定度评定[J].食品科学,2019,40(10):293-296.
[13]国家质量监督检验检疫总局.测量不确定度评定与表示:JJF 1059.1—2012[S].北京:中国计量出版社,2012.
[14]International Standard for Standardization.Cork stoppers-Determination of releasable 2,4,6-trichloroanisol (TCA):ISO 20752-2014[S].Geneva:ISO,2014.
[15]图雅,张海燕,董长征.液质联用法测定水产品中氯霉素残留量的不确定度评定[J].职业与健康,2017,6(33):753-755.
[16]梁桂娟,寻思颖,李清伟,等.高效液相色谱-质谱联用法测定酱油中三氯蔗糖的不确定度评估[J].中国酿造,2016,35(8):66-68.
[17]宁霄,金绍明,梁瑞强,等.超高效液相色谱-串联质谱法测定猪肉中β-受体激动剂残留量的不确定度分析[J].食品科学,2017,38(6):315-319.
[18]官咏仪,邱志超,宋阳,等.高效液相色谱法测定葡萄酒中山梨酸含量的不确定度评定[J].食品科学,2015,36(16):231-235.
[19]韩德娟,高艾英,高大山.液相色谱串联质谱内标法测定猪肉中沙丁胺醇及莱克多巴胺残留量的不确定度分析[J].食品安全质量检测学报,2020,11(1):223-229.
[20]国家质量监督检验检疫总局.电子天平检定规程:JJG 1036—2008[S].北京:中国计量出版社,2008.
[21]国家质量监督检验检疫总局.实验室玻璃仪器单标线容量瓶:GB/T 12806—2011[S].北京:中国标准出版社,2011.
[22]卫星,华李卓,张亚锋,等.高效液相色谱法测定黄酒中纽甜的不确定度评定[J].中国酿造,2017,36(10):167-170.
[23]国家质量监督检验检疫总局.常用玻璃量器检定规程:JJG 196—2006[S].北京:中国计量出版社,2006.
[24]国家质量监督检验检疫总局.移液器检定规程:JJG 646—2006[S].北京:中国计量出版社,2006.