葡萄酒酿造使用的葡萄通常破碎后直接发酵,但在夏季高温多雨的葡萄种植区,葡萄容易爆发霜霉病、白粉病、炭疽病等病害,为了不影响葡萄的正常收获,果农们会喷洒杀虫剂、杀菌剂和除草剂等农药,导致葡萄皮上有一定的农药残留[1]。研究发现,残留的农药会影响葡萄酒酿造过程中酵母的生长代谢,延迟发酵,产生一些不良代谢产物和异味物质,影响到葡萄酒的口感、香味等感官质量[2-3]和食用的安全性[4-5]。另外,葡萄皮上残留的有害微生物在葡萄发酵过程中与酿酒酵母菌群争夺养分,影响发酵并且会产生有害的副产物,比如醋酸菌可产生大量醋酸,引起葡萄酒的酸败味,霉菌可使果酒产生霉味等[6-8]。减少葡萄皮上农药残留和有害微生物,对葡萄酒正常发酵、质量及饮用安全性将有一定积极作用。
通常葡萄酿酒不需要清洗原料,主要是利用葡萄表皮附着的微生物进行发酵。对于泥沙较多的葡萄原料在酿酒前需要对原料进行清洗沥干处理[9],但尚鲜见关于清洗葡萄的研究报道。本研究采用1%盐水、1%淀粉液和自来水对赤霞珠葡萄进行清洗,以不清洗的葡萄原料为对照,通过不同的清洗方法造成葡萄不同的洁净度,旨在研究不同洁净度葡萄发酵的效果,并监测不同清洗条件下发酵过程的菌群生长、还原糖消耗、可溶性固形物变化、乙醇含量、乙酸含量及香气物质含量变化等,考察不同洁净度葡萄对葡萄酒发酵效果的影响,为酿酒葡萄原料的状态控制提供理论依据,以保证正常良好的葡萄酒发酵过程和终产物葡萄酒质量。
1 材料与方法
1.1 材料与试剂
1.1.1 原料与菌株
赤霞珠葡萄:河北昌黎卢龙华夏基地中粮集团华夏葡萄酒公司;ST活性干酵母:辽宁本溪桓仁五女山米兰酒业有限公司。
1.1.2 化学试剂
牛肉膏、蛋白胨、酵母浸粉(均为生化试剂):北京奥博星生物技术责任有限公司;氯化钠、硝酸钠、磷酸二氢钾、柠檬酸三铁、硫酸亚铁、硫酸锰、苯酚、3,5-二硝基水杨酸(dinitrosalicylic acid,DNS)、葡萄糖(均为分析纯):天津市天河化学试剂厂;玉米淀粉:南京甘汁园糖业有限公司;亚硫酸(分析纯):天津市科密欧化学试剂有限公司。
1.1.3 培养基[10-13]
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YEPD)培养基:酵母浸粉1%,蛋白胨2%,葡萄糖2%,琼脂2%,3.2×104 U/L青霉素和4×104 U/L的链霉素(用孔径为0.22 μm的水系膜过滤除菌),调pH至6.0。
肉汤培养基:牛肉膏0.5%,蛋白胨1%,氯化钠0.5%,琼脂2%,纳他霉素25%,调pH至7.2~7.4。
察氏培养基:硝酸钠0.3%,硫酸镁0.05%,磷酸氢二钾0.1%,硫酸亚铁0.001%,氯化钾0.05%,蔗糖3%,琼脂2%,3.2万单位/L青霉素与4万单位/L的链霉素(用孔径为0.22 μm的水系膜过滤除菌),调pH至6.7。
1.2 仪器与设备
UV-5200型分光光度计:上海元析仪器有限公司;PHS-3C型精密pH计:上海仪电科学仪器股份有限公司;H1750R离心机:湘仪离心机仪器有限公司;78-1磁力加热搅拌器:金坛市金城翔龙仪器厂;DNP-9082型恒温培养箱:上海精宏实验设备有限公司;DW-86L-386立式超低温冰箱:青岛海尔特种电器有限公司;LERD-TECH高压蒸汽灭菌器、Memmert低温培养箱:北京五洲东方科技发展有限公司;Agilent7697A顶空进样器、AgilentGC6850气相色谱仪:美国安捷伦公司;KT-2000恒温摇床:常州市中贝仪器有限公司。
1.3 方法
1.3.1 活性干酵母的活化及培养
将1 g ST活性干酵母溶于10 mL无菌水,40 ℃恒温水浴培养15 min,每5 min轻微摇动一次,培养完成后得到一级活化液;随后将10 mL稀释到20°Bx左右的模拟葡萄汁,加入到一级活化液中,25 ℃恒温水浴培养1 h,每30 min轻微摇动一次,培养完成后得到20 mL二级活化液,取20 mL的40°Bx左右的模拟葡萄汁,加入到二级活化液中,20 ℃恒温水浴培养2 h,每30 min轻微摇动一次。最后得到40 mL 0.25 g/L的酵母种子液。
1.3.2 葡萄原料的预处理
将1.8 kg成串的赤霞珠葡萄分成3等份,分别浸没于4 L的1%盐水、1%淀粉水及自来水中,在90 r/min摇床清洗10 min,捞出后,分别用4 L自来水在90 r/min的摇床清洗3次,每次清洗5 min,自然晾干后将果粒剪下,手带一次性手套挤压2层纱布包裹的葡萄果粒,将破碎处理后的葡萄皮和葡萄汁液装入500 mL三角瓶内,添加亚硫酸,使SO2含量为60 mg/L,每个处理3个平行。
1.3.3 葡萄酒的制备
将上述清洗处理的葡萄的葡萄浆,接种活化的酵母液,使接入的酵母量为102个/mL。接种后,混合均匀,瓶口安装发酵栓,以排放发酵产生的气体,在15~18 ℃静置发酵26 d,以还原糖不再降低视为发酵结束。发酵过程中定期取样测定微生物菌群、理化指标及主要香气物质。
1.3.4 取样及样品预处理
发酵过程中每3天取样一次,在取样前将带有发酵栓的玻璃锥形瓶以顺时针摇匀。将用于测定还原糖、可溶性固形物和挥发性物质的样品离心(4 ℃、8 000 r/min条件下离心5 min)以除去菌群细胞,保存于-20 ℃冰箱中待测。
1.3.5 分析检测
(1)菌群的测定[14]
采用稀释涂平板法测定微生物菌群。将发酵液适当稀释后,分别在YEPD培养基、肉汤培养基和察氏培养基接种0.2 mL于30 ℃静置培养至菌落不再增加为止,进行酵母菌、细菌和霉菌落计数。
(2)还原糖含量和可溶性固形物的测定[15-16]
用DNS法测定还原糖含量。用手持糖量折光仪直接测定可溶性固形物含量[17]。
(3)挥发性物质含量测定[18-19]
乙醇、乙酸和香气成分含量都采用气相色谱测定。
样品前处理:依次将1.4 g NaCl、磁力搅拌转子和7 mL发酵上清液加入15 mL顶空气相瓶中,用聚四氟乙烯(polytetrafluoroethylene,PTFE)垫密封,放置在磁力搅拌器上,在250 r/min下搅拌10 min。
顶空进样条件:Agilent 7697A顶空进样器;样品平衡温度90 ℃;样品平衡时间30 min;进样口温度250 ℃;检测器温度250 ℃。
气相色谱条件:Agilent DB-FFAP毛细管色谱柱(30 m×0.25 mm×0.25 μm);色谱柱初始温度40 ℃,稳定10 min,以5 ℃/min 升温至180 ℃,稳定1 min,然后以20 ℃/min升温至230℃,稳定2min;空气流量300mL/min,氢气流量30mL/min,载气为氮气(N2)流量10 mL/min,分流比10∶1,进样量2 μL。
1.3.6 统计分析
所有实验均进行3次平行,数值表示为3次独立实验的“平均值±标准偏差”。使用IBM SPSS Statistics 19.0软件进行显著性分析,然后以P<0.05的水平确定Duncan。
2 结果与分析
2.1 不同清洗方法的葡萄发酵过程中的菌群变化
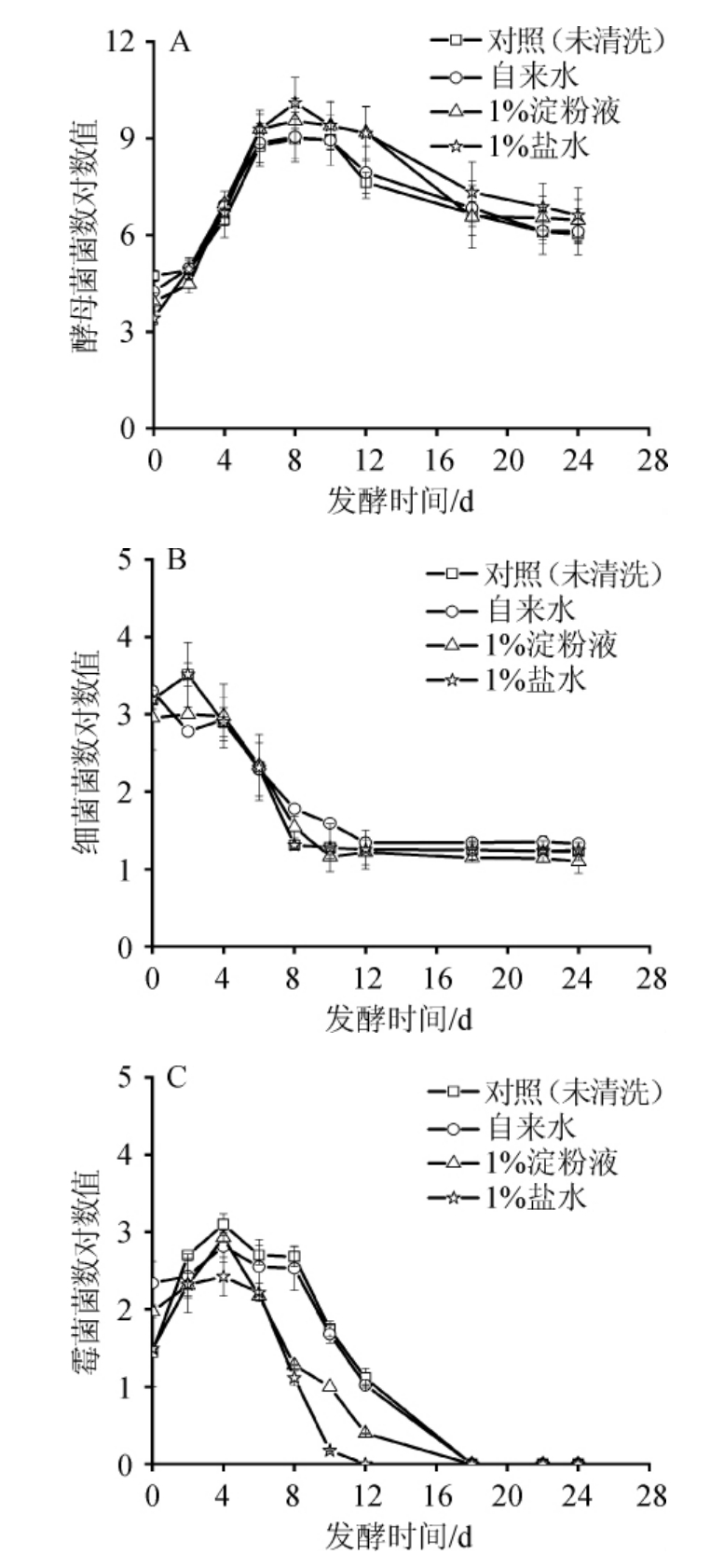
图1 不同清洗方法的葡萄发酵过程中的菌群变化
Fig.1 Change of microflora in the fermentation process of grape washed by different methods
由图1A可知,经不同方式清洗的葡萄初始酵母菌数量为对照组>自来水>1%淀粉液>1%盐水;发酵0~6 d各实验组的酵母数量差别很小,8 d后盐水处理组酵母菌数量最多,达到约1.26×1010个/mL,其次为淀粉液处理组,酵母菌数量达到3.47×109个/mL,自来水处理组和对照组酵母菌数量最少,酵母菌数量分别是1.10×109和1.26×108个/mL。由图1B可知,初始细菌数以淀粉液和盐水处理较少,细菌数分别为9.00×102和1.00×103个/mL,整个发酵过程中只有第8天的细菌数量高于对照组(可能是测量误差引起的),其余时间均低于对照组。由图1C可知,在发酵过程中,各实验组的霉菌数均表现为发酵4 d达到最大值后降低,清洗组霉菌数量一直低于对照组,盐水处理组的霉菌在第12天全部消失,淀粉液处理组比对照组和自来水处理组的霉菌数量下降快。
产生这些现象的原因主要是在发酵过程中,随着营养物质的消耗,酵母逐渐占据优势。盐水处理组能够清洗掉较多的细菌和霉菌,整个发酵过程中的细菌和霉菌数量比其他组少,与酵母的营养竞争弱,更有利于酵母的生长,发酵后期的酵母数量也就比其他实验组多。淀粉液处理组的细菌和霉菌虽然前期略多,但后期较少,所以发酵后期的酵母菌数量也比较多,可能与清洗去除葡萄表皮的化学物质(比如农药)有关。
综上分析,用1%盐水或1%淀粉液清洗葡萄有助于减少霉菌和细菌数量,提高葡萄洁净度,提高发酵过程中酵母数量,从而有利于葡萄酒的酿造。
2.2 不同清洗方法的葡萄发酵过程中的还原糖及可溶性固形物含量变化

图2 不同清洗方法的葡萄发酵过程中的还原糖及可溶性固形物含量变化
Fig.2 Change of reducing sugar and soluble solid contents in the fermentation process of grape washed by different methods
由图2A和图2B可知,发酵过程中的还原糖和可溶性固形物的变化趋势相同。各实验组的还原糖和可溶性固形物均在发酵的前10 d快速下降,下降速度和幅度依次为盐水处理组>淀粉液处理组>自来水处理组>对照组;发酵12 d后各实验组的还原糖和可溶性固形物含量基本稳定并且很接近。经盐水处理的葡萄初始微生物数量较少,而发酵过程中酵母数量较多,因此其发酵效率较高,表现出还原糖和可溶性固形物的消耗较多较快。这与PRETORIUS I S等[20]用柠檬酸盐清洗液清洗葡萄明显减少有害微生物提高发酵效率的研究结果类似。
结果表明,用1%盐水、1%淀粉液或自来水清洗的酿酒葡萄,仅在葡萄酒发酵过程中表现出还原糖和可溶性固形物消耗的差别,但发酵终点的含量很相近。用1%盐水或1%淀粉液清洗葡萄能有效的去除果皮上的微生物,从而更有利于发酵过程中酵母菌的生长和代谢,促进还原糖和可溶性固形物的消耗,提高葡萄酒发酵效率。
2.3 不同清洗方法的葡萄发酵过程中的乙醇和乙酸含量变化
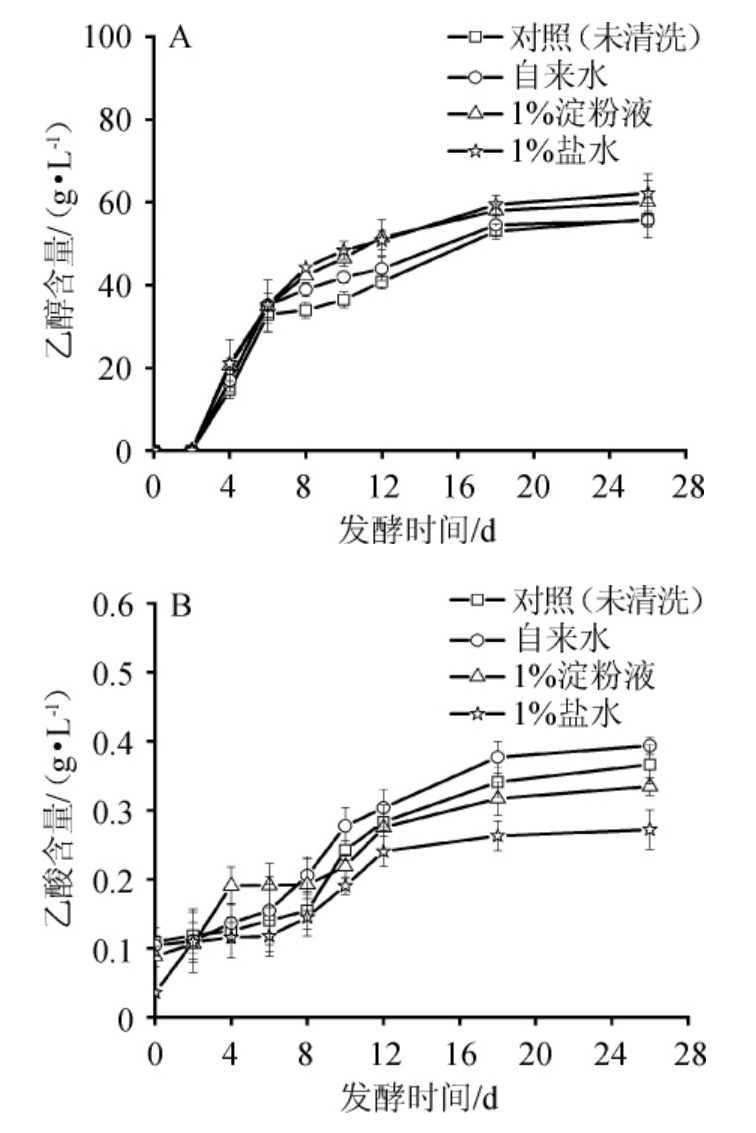
图3 不同清洗方法的葡萄发酵过程中的乙醇(A)和乙酸(B)含量变化
Fig.3 Change of ethanol (A) and acetic acid (B) contents in the fermentation process of grape washed by different methods
由图3A可知,不同实验组的葡萄在发酵过程中乙醇生成规律基本一致。在发酵的前2 d均未产生乙醇;随后快速产生乙醇,对照组和自来水处理组在发酵6 d和12 d开始出现产乙醇减慢。20 d后原料逐渐消耗殆尽,乙醇含量开始趋向平稳。在整个发酵过程中,清洗组的乙醇含量都要高于对照组,其中1%盐水处理组的乙醇含量最高,对照组的乙醇含量最低。在发酵初期葡萄浆内有较多溶解氧,酵母主要进行生长和繁殖。细胞生长繁殖消耗大量的溶解氧,随后酵母菌在相对厌氧的环境下代谢产乙醇。由于清洗组比对照组的细菌和霉菌数量少,酵母在竞争中迅速占据优势,能够更快更多产乙醇,其中,盐水处理组最终的乙醇含量最高。
由图3B可知,在葡萄酒发酵过程中,乙酸含量逐渐升高。在发酵前3 d,淀粉处理组迅速生成乙酸,在发酵3~5 d保持稳定;在发酵后期,自来水处理组的乙酸含量最高,其次为对照组;在2~26 d发酵过程中,1%盐水处理组的乙酸生成量一直比其他组低。
综上分析,1%盐水清洗葡萄可提高发酵过程中乙醇的生成速率和葡萄酒中的乙醇含量,1%淀粉液处理的效果次之。1%盐水清洗能够更好的清洗掉葡萄上的醋酸菌,减少发酵过程中醋酸的产生,1%淀粉液清洗的效果次之。
2.4 不同清洗方法的葡萄发酵过程中的香气物质含量变化
由图4A~4D可知,高级醇的生成主要集中在发酵的前期和中期。在发酵过程中,异丁醇一直处于上升状态,异戊醇、β-苯乙醇和2,3-丁二醇含量先升高后降低。在发酵过程中的大多数时段,自来水处理组的异丁醇、异戊醇和β-苯乙醇的生成量最高,其次为1%盐水处理组,处理组中1%淀粉液处理组的异丁醇生成量最低,对照组异戊醇和β-苯乙醇的生成量最低。葡萄在发酵过程中异戊醇含量均高于其他高级醇,分别占高级醇含量的67%~81%。对照组、自来水、1%盐水及1%淀粉液处理组的葡萄所酿的葡萄酒中总高级醇含量依次为63.89 mg/L、105.37 mg/L、98.73 mg/L和142.79 mg/L。当葡萄酒中高级醇的总量≤300 mg/L时,高级醇的含量越高,葡萄酒的风味就越复杂。对比四组高级醇总量,发现对葡萄进行清洗能够提高葡萄酒的风味复杂性。其中淀粉液处理的效果最好,其次是自来水和盐水。
由图4E和图4F可知,清洗过的葡萄酿造的葡萄酒中乳酸乙酯和乙酸乙酯的产量明显比对照组低,自来水处理组是所有清洗组中酯类化合物生成量较多的,这可能与清洗过的葡萄上细菌数量少,产生的乙酸或乙醇的产量少有关。与高级醇相比,酯类物质的形成过程更为复杂,酯类物质的合成可能受有机酸和高级醇的影响,有机酸经酯化反应生成相应的酯,乙酸乙酯就是其中的一种,因其独特的甜味和果香味,被作为葡萄酒中重要的风味物质,但葡萄酒中乙酸乙酯含量也不宜过高,浓度过高时容易产生刺激性气味。葡萄酒酿造过程中乙酸乙酯含量与乙酸含量正相关。盐水处理组乙酸产生量最低,所以乙酸乙酯的生成量也最低,葡萄酒中的总酯含量也就最低。
综上分析,清洗葡萄能够提高葡萄酒的异丁醇、异戊醇、β-苯乙醇以及总高级醇含量,但会降低2,3-丁二醇含量和酯类化合物总含量。1%淀粉清洗有助于提高葡萄酒中高级醇的含量,最有利于提高葡萄酒的风味复杂性。

图4 不同清洗方法的葡萄发酵过程中的香气物质含量变化
Fig.4 Change of aroma compounds contents in the fermentation process of grape washed by different methods
3 结论
采用1%盐水、1%淀粉液和自来水清洗赤霞珠葡萄,发现经不同清洗方式处理的葡萄在发酵过程中酵母菌、细菌和霉菌数量、还原糖消耗量、可溶性物质含量以及乙醇、乙酸和典型香气物质的含量差异显著(P<0.05)。清洗或者提高葡萄清洁度都有助于提高发酵过程中酵母菌数量、糖和可溶性固形物消耗速率、乙醇生成速率和产量以及高级醇产量,减少霉菌和细菌数量、乙酸生成速率和产量,1%盐水和1%淀粉液清洗的葡萄发酵效果更突出。足以见得,葡萄的清洁度对葡萄酒发酵过程和最终的葡萄酒质量均有影响。因此,很好地控制葡萄的清洁度是提高葡萄酒质量的重要保证。
[1]孙彩霞,姜遥,于国光,等.国内外葡萄农药最大残留限量比对研究[J].农产品质量与安全,2019(3):77-80.
[2]BRIZ-CID N,RIAL-OTERO R,CAMARA M A,et al.Dissipation of three fungicides and their effects on anthocyanins and color of monastrell red wines[J].Int J Mol Sci,2019,20(6):1447.
[3]GONZALEZ-RODRÍGUEZ R M,NOGUEROL-PATO R,GONZALEZBARREIRO C,et al.Application of new fungicides under good agricultural practices and their effects on the volatile profile of white wines[J].Food Res Int,2011,44(1):397-403.
[4]杨晨露,曹佩佩,单文龙,等.葡萄酒质量安全影响因素及酿造过程中的质量管理[J].食品安全质量检测学报,2019,10(6):1573-158.
[5]CHIOTTA M L,PONSONE M L,SOSA D M,et al.Biodiversity of Aspergillus section Nigri populations in Argentinian vineyards and ochratoxin A contamination[J].Food Microbiol,2013,36(2):182-190.
[6]MARZANO M,FOSSO B,MANZARI C,et al.Complexity and dynamics of the winemaking bacterial communities in berries,musts,and wines from apulian grape cultivars through time and space[J].PLoS One,2016,11(6):e0157383.
[7]张建华,李敏,张波,等.8 种单体多酚对葡萄酒微生物的抑菌活性比较[J].食品与发酵工业,2016,42(7):101-106.
[8]VARZAKAS T,ZAKYNTHINOS G,VERPOORT F.Plant food residues as a source of nutraceuticals and functional foods[J].Foods,2016,5(4):88.
[9]李华,王华,袁春龙,等.葡萄酒工艺学[M].北京:科学出版社,2007:32-35.
[10]MELO A T,MARTHO K F,ROBERTO T N,et al.The regulation of the sulfur amino acid biosynthetic pathway in Cryptococcus neoformans:the relationship of Cys3,calcineurin,and Gpp2 phosphatases[J]. Sci Rep,2019,9(1):11923.
[11]张丽娜,孙玉梅.不同SO2 添加量的草莓发酵微生物种群及理化特性动态测定[J].大连工业大学学报,2012,31(2):99-102.
[12]张中华.绍兴黄酒麦曲中微生物群落结构的研究[D].无锡:江南大学,2012.
[13]蒋春美,师俊玲,刘延琳.赭曲霉毒素产生菌筛选方法的对比与优选[J].西北农林科技大学学报,2012,57(3):169-174.
[14]龚军辉,王晶.稀释涂布平板法计数活菌的方法简介[J].生物学教学,2018,61(2):70-71.
[15]兰丰,刘传德.柱前衍生-液相色谱-串联质谱法测定葡萄和樱桃中单氰胺残留[J].色谱,2018,36(1):78-82
[16]高文军,李卫红,王喜明,等.3,5-二硝基水杨酸法测定蔓菁中还原糖和总糖含量[J].中国药业,2020,26(9):113-116.
[17]刘旭,陈敏,武轩,等.“赤霞珠”葡萄转色后不同成熟度指标的变化[J].食品科学,2016,37(22):230-236.
[18]陈霞.葡萄酒中乙醇含量的气相色谱法测定[J].中国酿造,2010,29(9):152-154.
[19]赵婉珍,祝霞,陈霞,等.不同浸渍工艺对蛇龙珠干红葡萄酒香气成分的影响[J].食品工业科学,2017,39(13):237-247.
[20]PRETORIUS I S.Tailoring wine yeast for the new millennium:novel approaches to the ancient art of winemaking[J].Yeast,2000,16(8):675-729.