山药酒是以山药为主要原料,经酵母菌发酵而成的蒸馏酒、发酵酒,或经蒸馏酒浸提后制成的山药配制酒,因其可使山药丰富的营养物质更加完全的溶入酒体,将药物活性成分最大限度的保留,具有一定滋养强壮,助消化,敛虚汗,止泻之保健功效,越来越受到消费者喜爱[1-3]。甾醇又称固醇,是广泛存在于生物体内的一种重要的天然活性物质,可分为动物性甾醇、植物性甾醇和菌类甾醇等三类[4-5],动物性甾醇以胆固醇为主,植物性甾醇主要为谷甾醇、豆甾醇和菜油甾醇等,而麦角甾醇则属于菌类甾醇,其中,植物甾醇可降低心血管、癌症发病率,降胆固醇、促进生长等功效,也是各种植源性食品主要抗氧化活性成分之一[6]。
甾醇作为山药的标志性活性成分之一,目前其酒类产品的测定方法和含量水平,均未见文献报导[1],因此急需建立山药酒中甾醇含量的测定方法,并对其抗氧化功能进行评价。食品中甾醇类化合物的测定方法有分光光度计法[7]、液相色谱法[8-9]、气相色谱法[10]、气相色谱-质谱法[11]等。分光光度计法和液相色谱法易受样品中其他类化合物干扰,气相色谱法和单级质谱能得到准确定量结果,但灵敏度不够高。本研究采用气相色谱串联质谱法,利用三重四级杆质谱技术的高特异性和强抗干扰能力,大大提升方法灵敏度[12-14],建立了4种常见植物甾醇和胆固醇同时测定的方法,并以DPPH自由基清除能力为评价指标,对其抗氧化能力进行评价,为深入研究山药酒的保健功效、提升产品品质,提供技术手段和数据支撑。
1 材料与方法
1.1 材料与试剂
山药酒(1#山药蒸馏酒、2#~5#发酵酒、6#~12#露酒):市售。
5α-胆甾烷醇(内标,纯度≥97%)、豆甾醇(纯度98.09%)、β-谷甾醇(纯度98.05%)、菜油甾醇(纯度96.12%)、豆甾烷醇(纯度≥98%)、正己烷(色谱纯):上海安谱实验科技股份有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH):美国Sigma公司;胆固醇(纯度97.2%):德国Dr.Ehrenstorfer公司;石油醚、氢氧化钠、无水硫酸钠(均为分析纯):北京化工试剂厂。
1.2 仪器与设备
TQ8040气相色谱串联质谱(gas chromatography tandem mass spectrometer,GC-MS)联用仪(配备AOC-20i+s自动进样器):日本岛津公司;Milli-Q Reference超纯水系统:美国Millipore公司;Rxi-5MS毛细管色谱柱(30 m×0.25 mm×0.25 μm):美国Restek公司;T6新世纪紫外-可见分光光度计:北京普析通用仪器有限公司。
1.3 方法
1.3.1 样品处理
取一定体积酒样于蒸发皿中,蒸发浓缩至10 mL转移到皂化瓶中,依次加入内标物(5α-胆甾烷醇),2 mol/L氢氧化钠-乙醇溶液50 mL,置于80 ℃恒温水浴锅中皂化60 min[15],冷却后,转移至250 mL分液漏斗中,分别用50 mL、50 mL、30 mL石油醚萃取3次,合并有机相,每次加入30 mL去离子水洗涤,直至洗至中性,再经无水硫酸钠脱水后,于35 ℃水浴中旋转蒸发至近干,加入200 μL衍生剂(三氟乙酰胺∶三甲基氯硅烷=99∶1,V/V)60 ℃衍生30 min,正己烷定容至1 mL,上机分析。
1.3.2 GC-MS/MS条件
色谱条件[15]:Rxi-5 MS毛细管色谱柱(30 m×0.25 mm×0.25 μm);升温程序:柱温200 ℃,以20 ℃/min升至300 ℃,以5 ℃/min升至320 ℃,保持4 min;进样口温度250 ℃;载气为高纯氦气(He)(纯度≥99.999%),流速1 mL/min;进样量1 μL;不分流进样。
质谱条件:电子电离(electron ionization,EI)源,能量70 eV;离子源温度250 ℃;质谱接口温度280 ℃;溶剂延迟时间5 min;碰撞气:高纯氩气(Ar)(纯度≥99.999%);多反应监测(multiple reaction monitoring,MRM)模式。
1.3.3 标准溶液的配制
称取甾醇类标准品10 mg(精确至0.01 mg)至10 mL容量瓶中,以正己烷溶解并定容,配制成质量浓度为1.0 mg/mL的甾醇类化合物标准储备液,再逐级稀释至一系列质量浓度梯度的混合标准溶液,每一质量浓度梯度的混合标准溶液中加入5 μL 5α-胆甾烷醇内标使用液,使其最终质量浓度均为0.5 μg/L。
1.3.4 清除二苯代苦味酰基自由基(DPPH·)能力测定
取不同体积的酒样,加入1 000 μL DPPH·(浓度为100 μmol/L的乙醇溶液),将其充分混匀后暗处放置30 min后,在波长517 nm处测定吸光度值,同时以2,6-二叔丁基对甲酚(butylated hydroxytoluene,BHT)作阳性对照。计算DPPH·清除率[16-17]。
式中:A0为DPPH溶液+同体积乙醇溶液的吸光度值;Ai为DPPH溶液+样液的吸光度值;Aj无水乙醇+样液的吸光度值。
2 结果与分析
2.1 质谱条件优化
采用GC-MS/MS MRM模式,设定多个时间段和扫描通道实现对6种甾醇类化合物的同时测定。多反应监测条件见表1。
表1 甾醇类化合物多反应监测条件
Table 1 Monitoring conditions for multiple reactions of sterols compounds

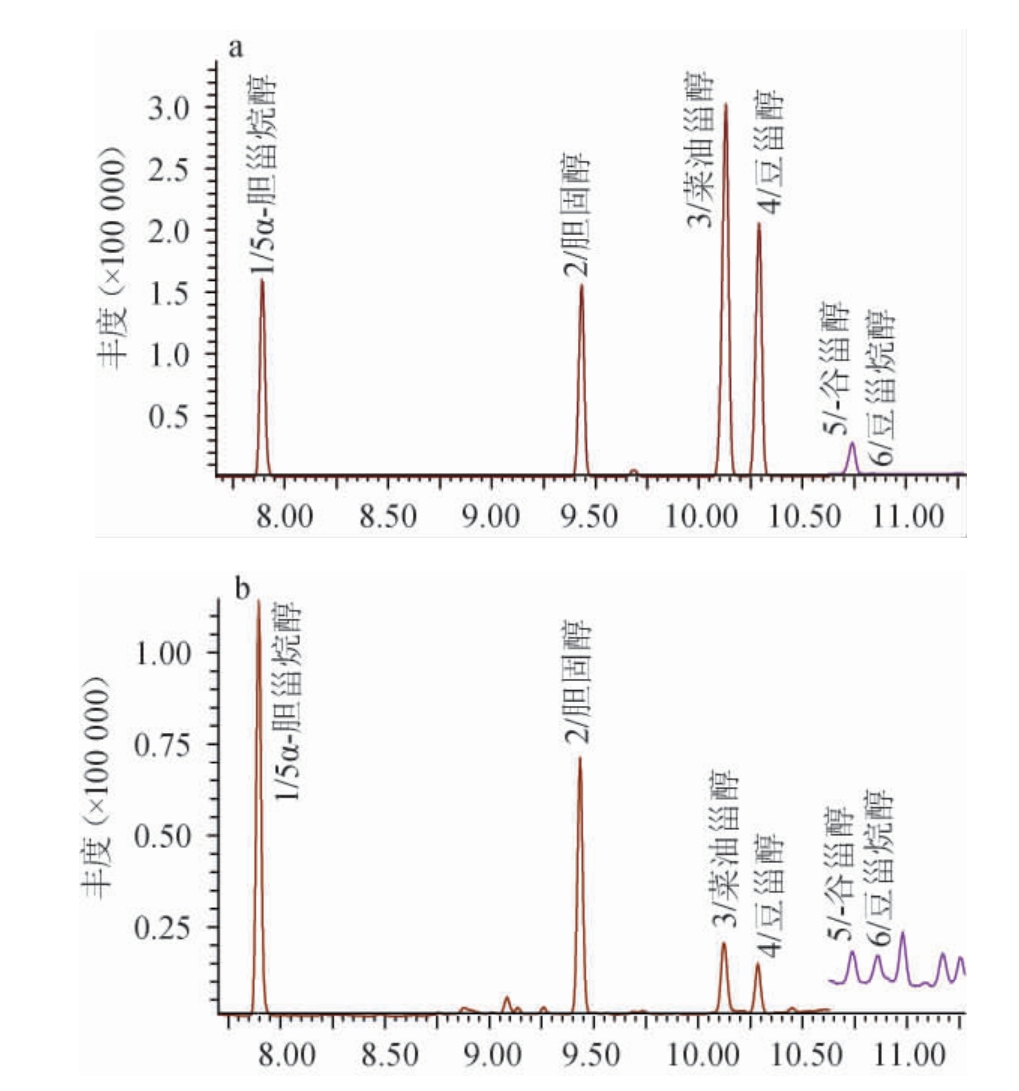
图1 标准溶液(a)及典型样品(b)的MRM谱图
Fig.1 MRM chromatogram of standard solution (a) and typical samples (b)
由表1可知,通过气相色谱分离和单级质谱全扫描方式确定各甾醇化合物的出峰顺序及保留时间。以多反应监测模式(MRM)为扫描模式,根据目标化合物的保留时间分为3个扫描窗口,使每个时间段的扫描离子对数量适中,调整离子对扫描时间,保证6种甾醇类化合物的同时检测。标准溶液及样品的MRM谱图见图1。由图1可知,胆固醇和植物甾醇各组分在11 min内实现良好分离。
2.2 方法学考察
通过线性范围及相关系数、检出限和定量限以及相对标准偏差和回收率,对方法进行综合评估,结果见表2。
表2 甾醇类化合物含量测定方法学评价结果
Table 2 Methodological evaluation results of sterols contents determination

由表2可知,各甾醇类化合物标准曲线线性范围在103.5~57 500 μg/L,相关系数R2均大于0.991,具有较好的线性关系;分别以信噪比为3和信噪比为10时的质量浓度作为检出限和定量限,其检出限为0.230~14.48 μg/L,定量限为0.775~48.29 μg/L,高于气相色谱法和单级气质联用技术的灵敏度;分别采用该方法对样品平行测定6次,其相对标准偏差为0.4%~1.2%;通过添加近等量的标准品,平行测定6次,加标回收率为98.74%~101.3%。上述结果显示该方法灵敏度高,结果准确可靠,可满足山药酒中甾醇化合物定量分析要求。
2.3 样品分析
利用本研究所建立的方法对山药酒进行分析,其中包括1种山药蒸馏酒,4种以山药为原料的发酵酒和7种山药露酒,化合物类别和含量详见表3。
表3 样品中甾醇类化合物含量测定结果
Table 3 Determination results of sterols contents in samples
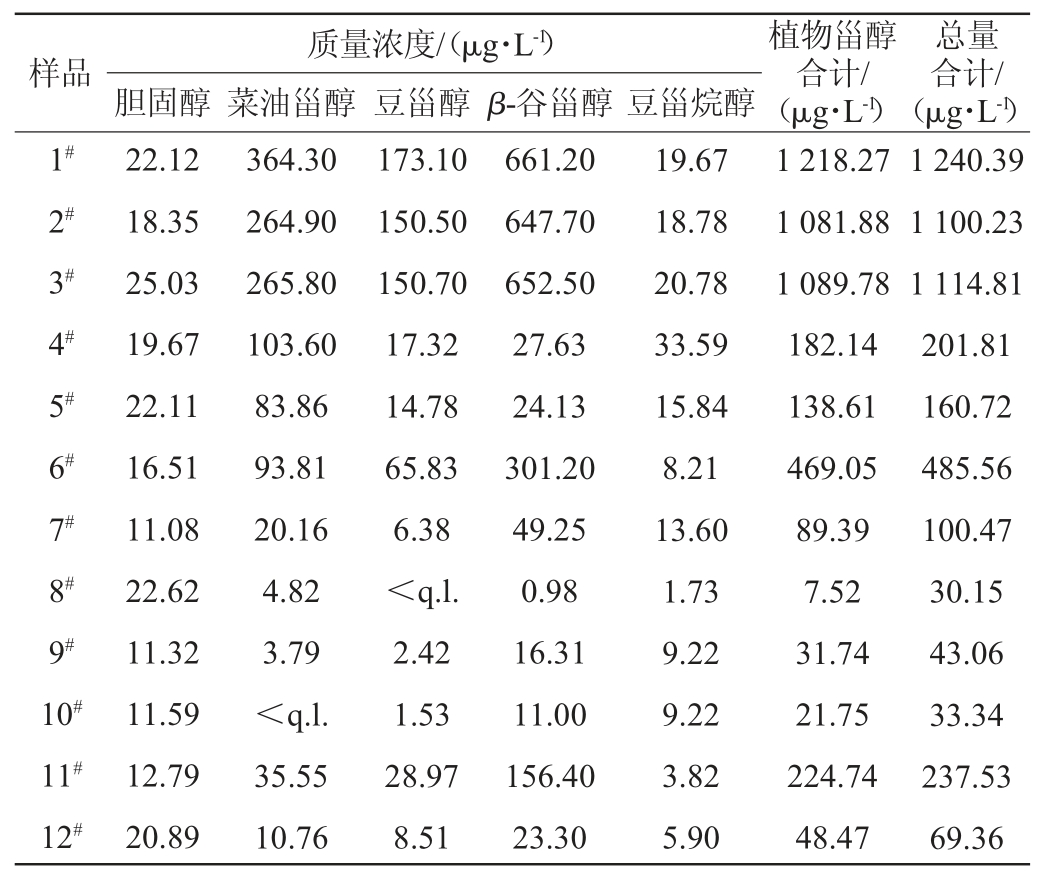
注:<q.l.表示低于定量限。
结果显示,不同种类山药酒,其甾醇组成特点相似,均以β-谷甾醇或菜油甾醇含量最高;豆甾醇在山药发酵酒中含量较高,而其饱和形式——豆甾烷醇在山药发酵酒中含量较低;山药酒中均存在一定量的胆固醇,含量为11.08~25.03 μg/L,远低于牛乳(15 mg/100 g)、瘦牛肉(58 mg/100 g)和鲫鱼(130 mg/100 g)等食品中胆固醇含量[18]。以甾醇含量进行比较,不同类山药酒存在明显差异:甾醇类化合物总量最高的是山药蒸馏酒(1#),为1 240.39 μg/L,其中植物甾醇总量为1 218.27 μg/L,胆固醇为22.12 μg/L,发酵酒中甾醇类化合物含量普遍高于配制酒,发酵酒为160.72~1 114.81 μg/L,而配制酒仅为30.15~237.53 μg/L,这可能与酒种的不同工艺(发酵、浸泡)及山药原料的使用量有关,甾醇含量测定结果可为进一步对山药酒中甾醇的功效评价提供一定的数据基础。
2.4 山药酒DPPH·清除能力的测定
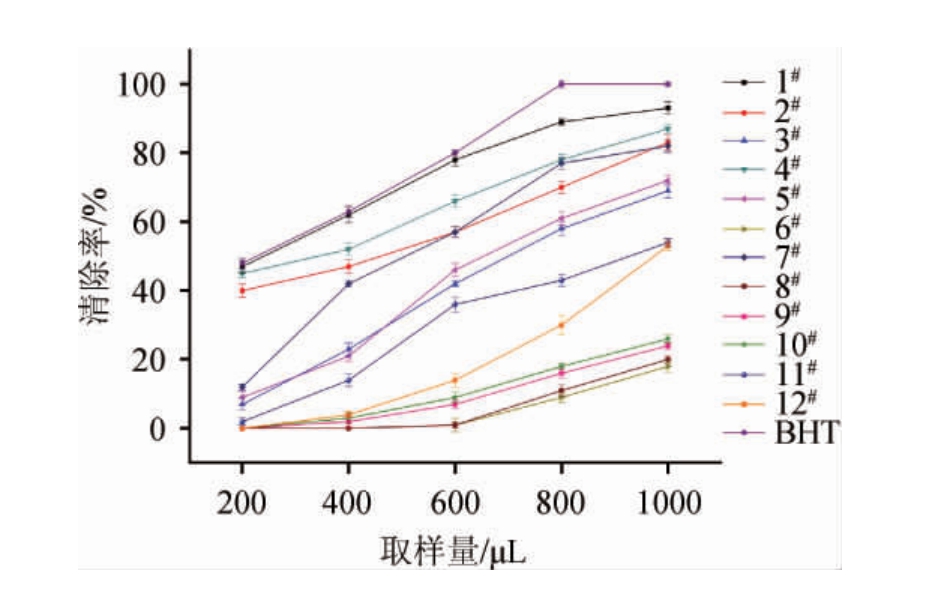
图2 山药酒DPPH自由基清除率测定结果
Fig.2 Determination results of DPPH free radical scavenging rate in yam alcoholic drinks
利用DPPH法[19-20]对1种山药蒸馏酒,4种山药发酵酒和7种山药露酒进行分析,如图2所示。结果表明,山药酒对DPPH自由基均有清除作用,且随着取样量增加,清除能力增强,具有良好的量效关系,清除率为0~93.12%;本实验用半抑制浓度(50%inhibiting concentration,IC50)值来反映样液清除DPPH自由基的能力,IC50表示清除自由基50%时溶液的取样量,其与清除能力呈负相关,IC50值越低,表明清除自由基能力越强,由图2可知,基酒1#清除DPPH自由基活性能力最强,明显高于其他样品,其IC50值为213 μL,接近对照组BHT的IC50值(200 μL),而6#样品取样量为1 000 μL时,清除率仅为18.34%,抗氧化能力较低,12种山药酒抗氧化能力排序为1#>4#>2#>7#>5#>3#>11#>12#>10#>9#>8#>6#。
3 结论
本研究建立了同时测定山药酒中4种常见植物甾醇和胆固醇的GC-MS/MS方法,该方法对甾醇类化合物进行皂化提取,气相色谱串联质谱的多反应监测模式测定,对方法进行评估,其相关系数R2≥0.991,检出限为0.23~14.48 μg/L,定量限为0.775~48.29 μg/L,相对标准偏差小于1.2%,加标回收率为98.74%~101.3%,该方法灵敏度高,可满足山药酒中胆固醇和植物甾醇快速同时测定的分析要求。经对部分市售山药酒中甾醇化合物进行分析和体外抗氧化评价,其甾醇类化合物组成相似,含量存在差异,含量范围7.52~1 218.27 μg/L。以清除DPPH自由基为指标对山药酒体外抗氧化能力进行评价,山药酒均具有一定的抗氧化能力,其中山药蒸馏酒和发酵酒的抗氧化活性高于山药配制酒。
[1]林英男.复合酶法制备发酵型山药酒及其澄清工艺的研究[D].济南:齐鲁工业大学,2014.
[2]王晨慧,饶静,辛鹏,等.复合酶法结合液相色谱技术测定山药酒中薯蓣皂苷的含量[J].中国酿造,2018,37(1):127-130.
[3]GARY P,ZALOGA M D.Phytosterols,lipid administration,and liver disease during parenteral nutrition[J].J Parent Enteral Nutr,2015,39(1 Suppl):39S.
[4]陈月晓,何涛,唐凌轩,等.气相色谱法同时测定食品中的胆固醇和植物甾醇[J].食品科学,2016,37(14):180-183.
[5]曹龙辉,李晓珺,赵文红,等.麦角甾醇的研究进展[J].中国酿造,2014,33(4):14-17.
[6]RONG S,XU R,LI W F.Phytosterols and dementia[J].Plant Food Human Nutr,2016,71(4):1-8.
[7]陈刘杨,刘玉兰,张晓丽.米糠油脱臭馏出物中甾醇的分析检测[J].中国油脂,2010,35(4):57-62.
[8]刘凤萍,戴华,李拥军,等.高效液相色谱-蒸发光散射检测器测定五种甾醇含量[J].分析科学学报,2002,18(3):230-232.
[9]赵海燕,詹未,李兵,等.超高效液相色谱法同时测定食用植物油中的4 种植物甾醇[J].中国食品卫生杂志,2016,28(2):223-226.
[10]SIVAKUMAR G,BATI C B,PERRI E,et al.Gas chromatography screening of bioactive phytosterols from mono-cultivar olive oils[J].Food Chem,2006,95(3):525-528.
[11]AHMIDA H S M,BERTUCCI P,FRANZÒ L,et al.Simultaneous determination of plasmatic phytosterols and cholesterol precursors using gas chromatography-mass spectrometry(GC-MS)with selective ion monitoring(SIM)[J].J Chromatogry B,2006,842(1):43-47.
[12]王晓丽,袁宜霖,李非凡,等.鹰嘴豆中植物甾醇的鉴定及生物接近度研究[J].中国食物与营养,2019(10):33-38.
[13]郑庆霞,刘萍萍,陈千思,等.气相色谱-串联质谱检测新鲜烟叶中的萜类成分[J].烟草科技,2019(7):61-68.
[14]支荣荣,周会芹,郑灏.GC-MS/MS 法测定桂丁香中β-谷甾醇含量[J].药学与临床研究,2019(6):437-439.
[15]SANTOS R,LIMAS E,SOUSA M,et al.Optimization of analytical procedures for GC-MS determination of phytosterols and phytostanols in enriched milk and yoghurt[J].Food Chem,2007,102(1):113-117.
[16]陈冰丹.应用DPPH 建立啤酒还原力检测方法的研究[J].中外酒业·啤酒科技,2018(1):40-42.
[17]张玲,左广垒,刘子菱,等.比较蓝莓发酵酒、浸泡酒和蓝莓果间总酚、总黄酮及DPPH 的差异[J].食品科技,2015(1):68-72.
[18]江松敏,孙庆文,曹立环,等.营养健康与疾病预防[M].北京:军事医学科学出版社,2015:222-223.
[19]韦献雅,殷丽琴,钟成,等.DPPH 法评价抗氧化活性研究进展[J].食品科学,2014,35(9):317-322.
[20]邱妍川,韦丽佳,李琳,等.基于1,1-二苯基-2-三硝基苯肼检测中药抗氧化成分的方法及其原理研究进展[J].中国药房,2016(27):2721.