新疆维吾尔自治区的红枣种植面积约46.67万km2,年产量在300万t左右,种植面积和产量均约占全国的1/3[1]。目前新疆地区红枣加工以干果和枣片等粗加工为主,以红枣果汁(浆)饮料、醋和酵素加工为辅,存在深加工程度不高、加工链条短和附加值低等问题[2]。作为高附加值产品,红枣酒是利用酵母菌将原料中的糖分转化为酒精制成的一类发酵型果酒,具有口感清爽和香气怡人的特点[3]。工业化生产的红枣酒需接入活性干酵母进行发酵,较之自然发酵的果酒其品质更为稳定且安全性更高[4]。然而,红枣酒加工中使用的活性干酵母多为国外进口,且多为葡萄酒酿造专用,具有自主知识产权且专门针对红枣酒发酵的酵母菌菌株尚少。酿酒文化在我国具有几千年的历史,白酒[5]、黄酒[6]和米酒[7]不仅产品种类繁多,其酒曲[8]、酒醅[9]或窖泥[10]中亦蕴含了宝贵的酵母菌微生物资源,因而从中分离、鉴定和筛选适合于红枣酒加工用的酵母菌株具有较强的可行性和微生物资源开发保护价值。
作为中国地理标识产品,孝感凤窝酒曲真菌以淀粉霉(Amylomyces)、复膜孢酵母属(Saccharomycopsis)和曲霉属(Aspergillus)为主,其中酵母菌的含量占到了真菌总量的1/3[11],具有较高的多样性,为红枣酒加工用酵母菌菌株的筛选提供了良好的素材。扣囊复膜酵母(Saccharomycopsis fibuligera)又称扣囊复膜孢酵母或扣囊拟内孢霉,在我国各类酒曲中大量存在[12],具有高产β-葡萄糖苷酶、淀粉酶和酸性蛋白酶等特性[13],在红枣酒中应用可显著提升酒体中乙酸乙酯的含量[14]。红枣富含丰富的氨基酸,其不仅参与人体正常的新陈代谢,具有生物活性与功能,同时对果酒的滋味品质具有重要的影响[15]。
本研究从湖北省孝感市采集了15个凤窝酒曲样品,采用纯培养和分子生物学技术相结合的手段对其中蕴含的酵母菌菌株进行了分离鉴定,同时选取扣囊复膜酵母(Saccharomycopsis fibuligera)和酿酒酵母(Saccharomyces cerevisiae)进行了红枣酒制备,并对其氨基酸种类和含量进行了分析,以期为后续红枣加工用酵母菌的筛选提供菌株支持和数据支撑。
1 材料与方法
1.1 材料与试剂
米酒曲:市售。
M13F(-47)/M13R(-48)和NL1/NL4:均由武汉天一辉远生物有限公司合成;脱氧核糖核苷三磷酸、rTaq酶、10×聚合酶链式反应(polymerase chain reaction,PCR)缓冲液和pMD18-T载体:大连宝生物技术有限公司;Axygen清洁试剂盒:康宁生命科学有限公司;马铃薯葡萄糖琼脂培养基(potato dextrose agar,PDA)、酵母浸出粉胨葡萄糖培养基(yeast extract peptone dextrose medium,YPD)合成培养基:北京奥博星生物技术有限责任公司;氨基酸分析仪配套缓冲溶液1、缓冲液2、缓冲液5和缓冲液6:英国Biochrom公司。其中引物为NL1/NL4(NL1:5'-GCATATCAATAAGCGGAGGAAAAG-3';NL4:5'-GGTCCGTGTTTCAAGACGG-3')和M13F(-47)/M13R(-48)(M13F:5'-CGCCAGGGTTTTCCCAGTCACGAC-3';M13R:5'-AGCGGATAACAATTTCACACAGGA-3')。
骏枣:新疆维吾尔自治区石河子市;白砂糖(食品级):柳州市柳冰食品厂;果胶酶(5万U/g):和氏璧生物科技有限公司;偏重亚硫酸钾(食品级):意大利ESSECO集团;酒石酸:南祥瑞食品添加有限公司。
1.2 仪器与设备
ECLIPSSE Ci-L显微镜:日本NiKon公司;PTC-100PCR仪:美国ABI公司;FluorChem FC3化学发光凝胶成像系统:美国ProteinSimple公司;WZS手持式折射仪:上海仪电物理光学仪器有限公司;PHS-25型数显pH计:上海仪电科学仪器股份有限公司;Biochrom 30+全自动氨基酸分析仪:英国Biochrom公司。
1.3 实验方法
1.3.1 样品的采集
于湖北省孝感市云梦县的城北菜市场、珍珠坡菜市场以及大悟县的三里菜市场选取无霉变、无虫眼及无异味的米酒曲样品,共采集15 份,其编号依次为HB1~HB15。
1.3.2 酵母菌的分离与鉴定
用生理盐水对研碎后的米酒曲分别进行倍比稀释,取10-1~10-5稀释液100 μL涂布于PDA固体培养基上,30 ℃培养18~30 h,根据菌落形态与大小进行单菌落挑选,纯化3次后镜检,冻存备用。按照下述方法对酵母菌基因组进行提取和26S rDNA PCR扩增[16]。扩增体系:10×PCR 缓冲溶液2.5 μL、脱氧核糖核苷三磷酸2.0 μL、DNA聚合酶0.5 μL、引物NL1和NL4各0.5 μL、无菌水18.5 μL和DNA模板0.5 μL。扩增程序:94 ℃预变性5 min;94 ℃变性1 min,55 ℃退火1 min,72 ℃延伸2 min,30个循环;72 ℃延伸10 min,4 ℃保温。
PCR扩增产物经2%的琼脂糖凝胶电泳检测后,使用清洁试剂盒进行纯化,连接和转化并挑阳性克隆子送武汉天一辉远生物有限公司测序。序列切除引物后,在美国国立生物技术信息中心(nationalcenter for biotechnology information,NCBI)网站上的GenBank数据库进行同源序列比对,进而明确酵母菌的分类地位[17]。
1.3.3 红枣酒的制作
取100 g去核骏枣加入500 mL蒸馏水和0.036 g偏重亚硫酸钾后破壁打浆,枣浆静置30 min,加入0.18 g果胶酶,45 ℃酶解2 h后,使用白砂糖将其可溶性固形物调至24°Bx并用酒石酸调pH值至3.80,68 ℃水浴杀菌1 h,备用[18]。将
1.3.2 中鉴定为酿酒酵母和扣囊复膜酵母的菌株,在YPD培养基中活化三代后离心收集菌体,按照5×107CFU/mL红枣浆的比例接入菌体,发酵罐罐口4 层纱布封口后,20 ℃发酵,若发酵液的糖度在48h内保持不变,则判定为发酵结束。红枣酒用纱布袋过滤后4 ℃、10 000 r/min离心10 min,上清液备用。
1.3.4 红枣酒中氨基酸含量的测定
参照GB/T 5009.124—2016《食品中氨基酸的测定》中约束方法对红枣酒样品进行预处理。测试条件:色谱柱为磺酸型阳离子树脂,检测波长为440 nm和570 nm,温度梯度为38 ℃、50 ℃和93 ℃,缓冲液1、2、5和6分别洗脱9 min、12 min、20 min和6 min,流速为35 mL/h。
1.3.5 统计分析
使用PAST3.0软件计算香农指数和超1指数;使用MEGA 7.0软件绘制系统发育树,其他图使用Origin 2017绘制。
2 结果与分析
2.1 孝感地区米酒曲中酵母菌的分离与鉴定

图1 部分疑似酵母菌菌落特征及细胞形态
Fig.1 Colony characteristics and cell morphology of some suspected yeast strains
由图1可知,菌株HBUAS61076的菌落偏小、呈乳白色圆形、表面湿润光滑且中间凸起,菌体为卵形;菌株HBUAS61089的菌落亦偏小、呈乳黄色圆形、表面湿润光滑且中间凸起,菌体为椭圆形;菌株HBUAS61093的菌落偏大、呈白色圆形、表面粗糙干燥且中间凸起,菌体为椭圆形并能形成假菌丝。
本研究采用分子生物学方法对疑似酵母菌分离株26S rDNA基因序列进行了扩增及测序,并构建了系统发育树,其结果如图2所示。

图2 基于26S rDNA基因的部分酵母菌菌株系统发育树
Fig.2 Phylogenetic tree of partial yeast strains based on 26S rDNA gene
每个酵母种仅选取1 株菌株用于系统发育树的构建。
由图2可知,HBUAS61116等15 株菌株与模式菌株Saccharomycopsis fibuligera ATCC 36309聚在一支且相似度≥99%,被鉴定为扣囊复膜酵母(Saccharomycopsis fibuligera);HBUAS61081等8 株菌株与模式菌株Pichia anomala NRRL Y-366聚在一支且相似度≥99%,被鉴定为皮希亚诺姆拉酵母(Pichia anomala);HBUAS61079等8 株菌株与模式菌株Candida glabrata ATCC 2001聚在一支且相似度≥99%,被鉴定为光滑假丝酵母(Candida glabrata);HBUAS61080等7株菌株与模式菌株Cyberlindnera fabianii NRRL 1871聚在一支且相似度≥99%,被鉴定为弗比恩酵母(Cyberlindnera fabianii);HBUAS61108等3株菌株与模式菌株Saccharomyces cerevisiae NRRL Y-12632聚在一支且相似度等于100%,被鉴定为酿酒酵母(Saccharomyces cerevisiae);HBUAS61110等2 株菌株与模式菌株Candida tropicalis ATCC 750聚在一支且相似度≥99%,被鉴定为热带假丝酵母(Candida tropicalis);HBUAS61107菌株与模式菌株Pichia kudriavzevii CBS5147聚在一支且相似度等于100%,被鉴定为库德毕赤酵母(Pichia kudriavzevii);HBUAS61120菌株与模式菌株Clavispora lusitaniae NRRL Y-11827聚在一支且相似度等于100%,被鉴定为葡萄牙棒孢酵母(Clavispora lusitaniae)。各米酒曲样品酵母菌分离鉴定情况如表1所示。
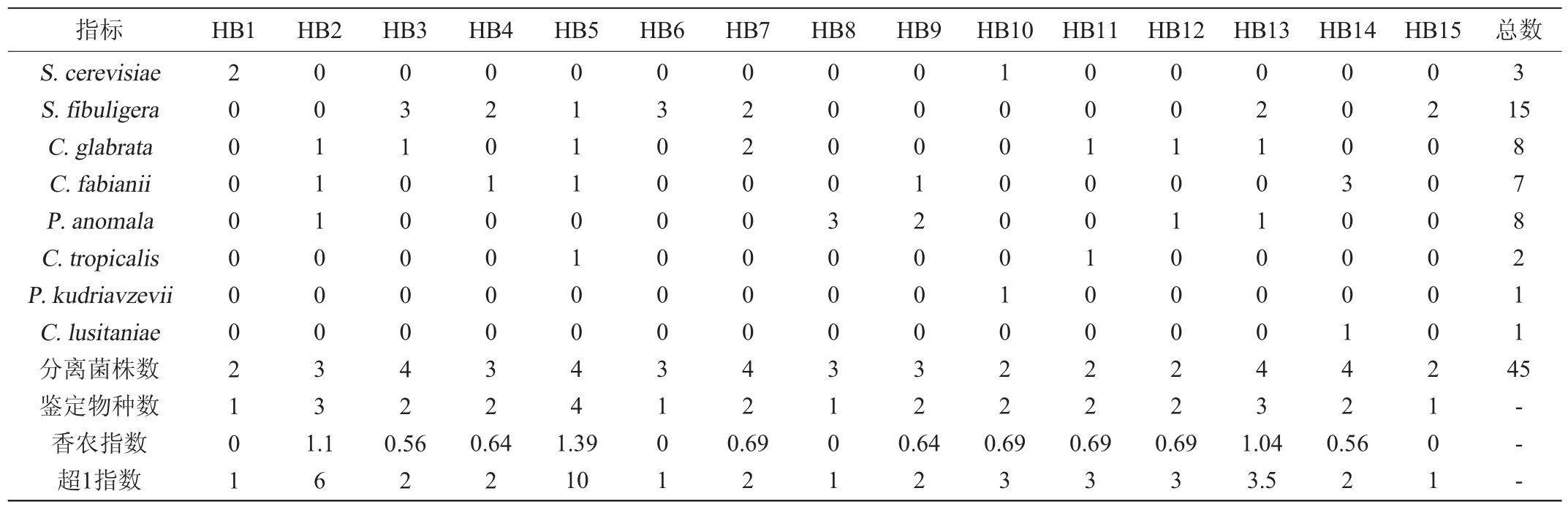
由表1可知,45 株酵母菌共被鉴定为8 个种,其中15 株为S.fibuligera,占分离株总数的33.33%。样品HB2和HB5分别分离出3株和4株酵母菌,被鉴定为3个和4个物种,香农指数分别为1.1和1.39,超1指数分别为6和10,而样品HB1、HB6、HB8和HB15分别分离出2 株或3 株酵母菌,但均被鉴定为1个种,其香农和超1指数均为0和1。由此可见,S.fibuligera为孝感地区米酒曲中的优势酵母菌,且不同米酒曲间酵母菌丰度和多样性存在较大的差异。
表1 凤窝酒曲样品酵母菌分离鉴定统计
Table 1 Isolation and identification statistics of yeast strains from Fengwo Jiuqu
2.2 红枣酒氨基酸种类及含量分析
由表2可知,红枣酒中共检测到12种氨基酸,氨基酸总量为3.019 mg/mL,其中必需氨基酸有5种,累计含量为0.282 mg/mL,非必需氨基酸有7种,累计含量为2.737mg/mL。红枣酒中含量最多的氨基酸为脯氨酸,含量为1.662 mg/mL,其次为天冬氨酸,含量为0.737 mg/mL。由此可见,红枣酒中的氨基酸以脯氨酸和天冬氨酸等非必需氨基酸为主。黄酒中富含丰富的氨基酸,因而本研究结合参考文献[17]将红枣酒与丹阳封缸酒的氨基酸构成进行了比较分析。
由表2亦可知,丹阳封缸酒中氨基酸的总量为2.497mg/mL,共检测出7 种必需氨基酸和10种非必需氨基,甘氨酸、丙氨酸、蛋氨酸、半胱氨酸和缬氨酸仅在丹阳封缸酒中检测到。此外,红枣酒中必需氨基酸所占的比例为9.3%,而丹阳封缸酒中这一比例高达42.4%。由此亦可知,较之丹阳封缸酒,虽然氨基酸的种类和必需氨基酸构成均明显偏少,但红枣酒氨基酸总量明显偏高。
表2 红枣酒中氨基酸组成分析
Table 2 Analysis of amino acid composition of jujube wine
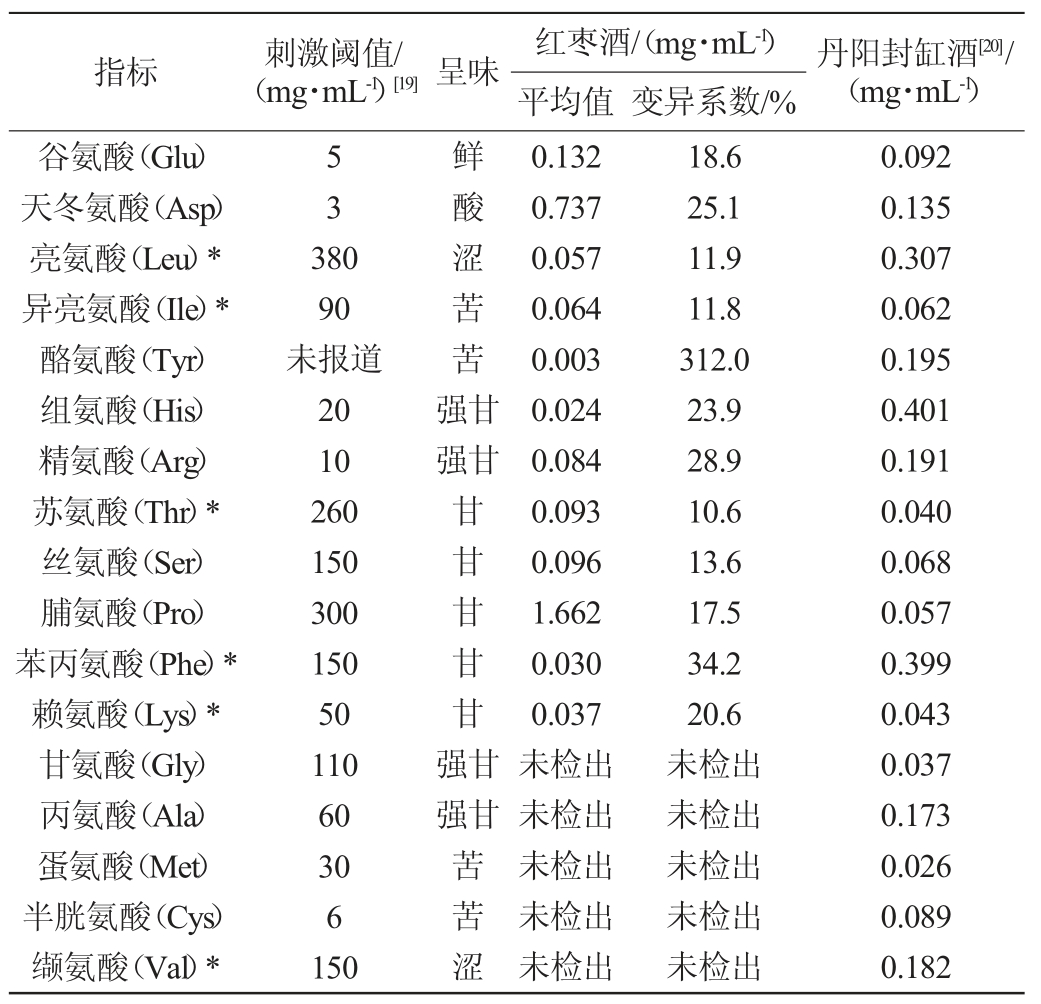
注:“*”为必需氨基酸。
本研究进一步对红枣酒中鲜、酸、涩、苦和甘5种呈味氨基酸的构成进行了分析与比较,结果见表2。由表2可知,红枣酒中鲜味呈味氨基酸平均含量为0.132 mg/mL,占氨基酸总量的4.4%,变异系数为18.6%;酸味呈味氨基酸平均含量为0.737 mg/mL,占氨基酸总量的24.4%,变异系数为25.1%;涩味呈味氨基酸平均含量为0.057 mg/mL,占氨基酸总量的1.9%,变异系数为11.8%;苦味呈味氨基酸平均含量为0.067 mg/mL,占氨基酸总量的2.2%,变异系数为16.3%;甘味呈味氨基酸平均含量为2.026 mg/mL,占氨基酸总量的67.1%,变异系数为15.5%。由所测数据可得,红枣酒中甘味呈味氨基酸含量最多,其次为酸味呈味氨基酸,而鲜、苦和涩味呈味氨基酸的含量均相对较少。相较之丹阳封缸酒,其甘味呈味氨基酸占总氨基酸的56.4%,为其主要呈味氨基酸,涩味和苦味呈味氨基酸的含量亦较高,分别占19.6%和14.9%,而酸味和鲜味呈味氨基酸含量较少,分别占5.4%和3.7%。由此可见,红枣酒以甘味和酸味氨基酸为主,与丹阳封缸酒存在明显的差异。
3 结论
S.fibuligera为孝感地区米酒曲中的优势酵母菌,且不同米酒曲间酵母菌丰度和多样性存在较大的差异。以S.fibuligera和S.cerevisiae分离株进行红枣酒制备,结果发现红枣酒中的氨基酸以脯氨酸和天冬氨酸等非必需氨基酸为主,呈味氨基酸以甘味和酸味为主。
[1]王雨,李占林,斯琴,等.新疆红枣产业发展现状及今后发展思路[J].农村科技,2019,36(3):60-64.
[2]陈晓丽.新疆特色林果产品市场营销策略研究[D].石河子:石河子大学,2019.
[3]LEE J E,YUN J H,LEE A R,et al.Volatile components and sensory properties of jujube wine as affected by material preprocessing[J]. Int J Food Prop,2018,21(1):2052-2061.
[4]LI S,MAO Z,WANG P,et al.Brewing jujube Brandy with Daqu and yeast by solid-state fermentation[J].J Food Proc Eng,2016,39(2):157-165.
[5]沈馨,马佳佳,刘文汇,等.浓香型白酒窖泥中乳酸菌的分离鉴定及其在柑橘酒中的应用[J].中国酿造,2018,37(7):42-46.
[6]LV X C,CHEN Z C,JIA R B,et al.Microbial community structure and dynamics during the traditional brewing of Fuzhou Hong Qu glutinous rice wine as determined by culture-dependent and culture-independent techniques[J].Food Control,2015,57(11):216-224.
[7]向凡舒,邓风,魏冰倩,等.不同来源酒曲酿制米酒中乳酸菌的分离与鉴定[J].中国酿造,2019,38(5):67-72.
[8]JI Z,JIN J,YU G,et al.Characteristic of filamentous fungal diversity and dynamics associated with wheat Qu and the traditional fermentation of Chinese rice wine[J].Int J Food Sci Tech,2018,53(7):1611-1621.
[9]马红玉.清香型白酒酒醅测定及核心真菌特性研究[D].太原:山西大学,2019.
[10]LIU M,TANG Y,ZHAO K,et al.Determination of the fungal community of pit mud in fermentation cellars for Chinese strong-flavor liquor,using DGGE and Illumina MiSeq sequencing[J]. Food Res Int,2017,91(1):80-87.
[11]王丹丹,沈馨,董蕴,等.孝感凤窝酒曲真菌多样性评价[J].中国酿造,2017,36(11):38-42.
[12]苏畅,马莹莹,杨建刚.扣囊复膜酵母在酿酒中的应用研究进展[J].食品研究与开发,2018,39(1):205-209.
[13]WANG S K,WANG X,TIAN Y T,et al.Direct utilization of starch for heterotrophic cultivation of Chlorella pyrenoidosa by co-culture with immobilized Saccharomycopsis fibuligera[J].Algal Res,2018,33(7):406-411.
[14]和东芹,张伟.大枣干红生产工艺研究[J].食品科学,2002,23(12):74-76.
[15]NIU Y,ZHANG X,XIAO Z,et al.Characterization of taste-active compounds of various cherry wines and their correlation with sensory attributes[J].J Chromatogr B,2012,902(8):55-60.
[16]DESIYE A,ABEGAZ K.Isolation,characterization and identification of lactic acid bacteria and yeast involved in fermentation of teff (Eragrostis tef)batter[J].Adv Ecol Res,2013,1(3):36-44.
[17]唐玲,刘平,黄瑛,等.酵母的分子生物学鉴定[J].生物技术通报,2008,24(5):84-87.
[18]蔡文超,单春会,杨丽萍,等.红枣复合甜酒的发酵工艺初探[J].中国酿造,2018,37(6):199-204.
[19]LAMBRECHTS M,PRETORIUS I.Yeast and its importance to wine aroma-a review[J].S Afr J Enol Viticult,2000,21(Special Issue):97-129.
[20]邓娜娜,马永昆,王亚超,等.超高压催陈对丹阳封缸酒中游离氨基酸的影响[J].食品工业科技,2014,35(18):149-152.