谷类杂粮制品主要是指以玉米、黑米、小米、薏米、高粱、燕麦、大麦、红米、红稗等杂粮蒸煮或者粉碎制得的食品,营养丰富,富含多种维生素、矿物质和膳食纤维。但是,同样这些杂粮在生长过程中也会受到易病虫害危害产生真菌毒素,从而影响产品产量和质量、埋下食品安全隐患[1]。目前对粮谷的真菌毒素报道很多[2-6],对谷类杂粮制品的研究较少,特别是在3种呕吐毒素类-脱氧雪腐镰刀菌烯醇(deoxynivalenol,DON)、3-乙酰脱氧雪腐镰刀菌烯醇(3-acetyldeoxynivalenol,3-ADON)、15-乙酰脱氧雪腐镰刀菌烯醇(15-acetyldeoxyn-ivalenol,15-ADON)以及玉米赤霉烯酮(zearalenone,ZON)等真菌毒素方面鲜有报道。CASTILLO M D等[7]研究发现,黑豆可能存在链格孢霉毒素、玉米赤霉烯酮(zearalenone,ZEN)和单端孢霉烯族毒素的污染风险;TSENG T C等[8]在赤豆和绿豆中检测到了伏马菌素B1(fumonisin B1,FB1)。
目前,真菌毒素检测的方法主要有薄层色谱法、酶联吸附免疫法、高效液相色谱法和高效液相色谱-质谱联用法(high performance liquid chromatography mass spectrometry,HPLC-MS/MS)[9-12]。薄层色谱法对检测仪器及人员要求较低,但是此方法精度较差、实验步骤冗长繁多、重现性不好[13];酶联免疫吸附试验法具有灵敏、快速等优点,但是存在交叉污染反应的缺点[14];高效液相色谱法应用较为广泛,检测稳定性较好,但样品中基质易对目标物产生干扰,前处理过程繁琐,对操作人员要求高,且采用的免疫亲和柱成本较昂贵[15]。鉴于上述方法存在的前处理中有些步骤和条件的缺陷,或者易定性误判等不足,本研究尝试运用QuEChERS前处理净化技术,简化提取过程,建立快速、容易、便宜、有效、稳定和可靠(Quick Easy Cheap Effective Rugged Safe,QuEChERS)的净化技术结合高效液相色谱-质谱联用法检测谷类杂粮制品中DON、3-ADON、15-ADON 和ZON同时检测的方法,该研究对评价此类食品的安全具有重要意义,也为谷类杂粮制品中真菌毒素的分析和监控提供技术支持。
1 材料与方法
1.1 材料与试剂
DON溶液标准品(100 μg/mL)、3-ADON溶液标准品(100 μg/mL)、15-ADON溶液标准品(100 μg/mL)、ZON溶液标准品(100 μg/mL):中国计量科学研究院;甲醇、乙腈(色谱纯):德国Merck公司;甲酸(色谱纯):上海安谱实验科技股份有限公司。
1.2 仪器与设备
2695型高效液相色谱仪:美国Waters公司;API 3500 QTrap超高压液相色谱-三重四级杆串联质谱仪:美国AB公司;Milli-Q纯水仪:美国Millipore公司。
1.3 实验方法
1.3.1 色谱条件
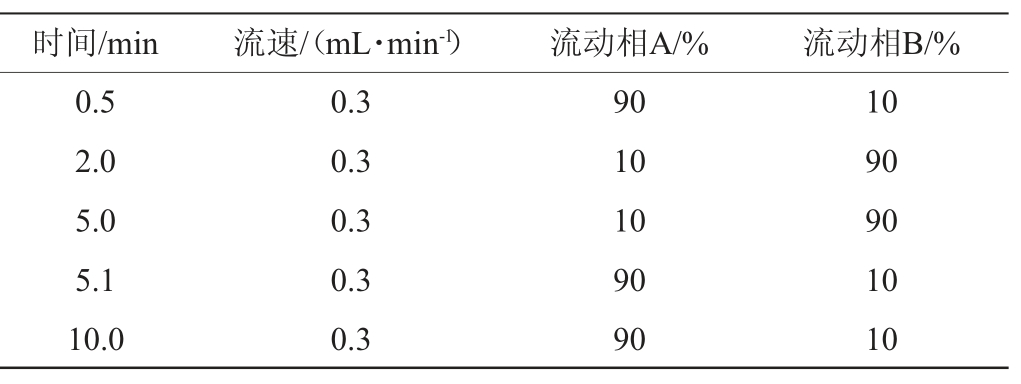
色谱柱:Zorba-C18柱(2.1 mm×150 mm,3 μm);流速:0.3 mL/min;进样量:20 μL;柱温:30 ℃;流动相:A为0.10%甲酸溶液,B为乙腈;洗脱条件见表1。
表1 HPLC-MS/MS梯度洗脱条件
Table 1 Gradient elution conditions of HPLC-MS/MS
1.3.2 样品的提取与净化
称取1.0 g混合盐析剂置于10 mL离心管中,加入2.0 g样品,加入4.0 mL提取溶液。取1 mL上清液于2.0 mL PE管中,加入吸附剂后涡旋10 s,离心取上清液,过膜后上机进样分析。实验分别比较不同的提取溶液以及吸附剂组合,对4种真菌毒素检测的影响。其中提取液分别比较了提取溶液Ⅰ(甲醇∶水=20∶80,V/V)、提取溶液Ⅱ(甲醇∶水=10∶90,V/V)、提取溶液Ⅲ(乙腈∶水=20∶80,V/V)、提取溶液Ⅳ(乙腈∶水=10∶90,V/V)共4种,对目标物提取的影响;吸附剂比较了C18、Florial、SAX、GCB、Al2O3、PSA共6种以及未使用吸附剂时对目标物提取的影响,并在上述优化基础上比较C18+无水硫酸镁粉末(100 mg+300 mg)、Florisil+无水硫酸镁粉末(100 mg+300 mg)和Florisil+C18+无水硫酸镁粉末(50 mg+50 mg+300 mg)共3种配比,来优化QuEChERS吸附剂组合。
1.3.3 标准溶液的配制
DON、3-ADON、ZON用乙腈配制成1.0 μg/mL的标准储备液,15-ADON用乙腈配制成10.0 μg/mL的标准储备液,置于4 ℃冰箱中储存。
1.3.4 方法的精密度、重复性与回收率
以未检出4种真菌毒素的谷类杂粮样品为空白基质,加入不同浓度的DON、3-ADON、15-ADON、ZON混合标液,使用QuEChERS提取后,上机检测计算回收率。
2 结果与分析
2.1 QuEChERS前处理方法的优化
2.1.1 提取溶液的选择
呕吐毒素类(DON、3-ADON、15-ADON)的提取溶液一般采用纯水,而玉米赤霉烯酮(ZON)的提取一般采用甲醇-水或者乙腈-水体系,且在实验中发现,提取溶液与试样比为2∶1(mL∶g)时,加入盐析剂样品高速均质后不易产生乳浊液,上层提取液易过滤分层[16-18]。因此,采用4种提取溶液分别提取加标样品中的4种真菌毒素,实验结果以样品中4种真菌毒素的加标回收率来比较提取溶液效果,结果见图1。

图1 提取溶液对4种真菌毒素回收率的影响
Fig.1 Effect of extraction solution on recovery rates of four mycotoxins
由图1可知,含20%有机相的提取液对呕吐毒素类提取效果不佳,含10%的有机相提取液效果较好,其中提取溶液Ⅳ(乙腈∶水=10∶90,V/V)的提取效果最优,4种真菌毒素的加标回收率都能达到90%以上,在此比例的提取溶液条件下,既能保证呕吐毒素类毒素的活性,又能提高4种目标物在提取液中的分配系数。
2.1.2 吸附剂的优化
本试验对比了混合标准溶液经过6种不同吸附剂和未使用吸附剂时各真菌毒素的回收率[19-20],结果见图2。
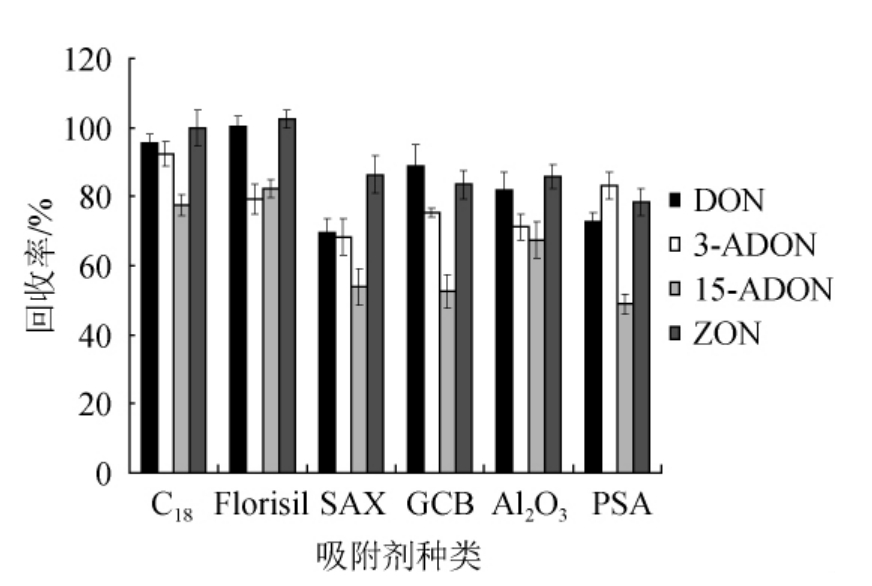
图2 4种真菌毒素经不同吸附剂处理后的回收率
Fig.2 Recovery of four mycotoxins treated with different adsorbent
由图2可知,C18和Florisil对4种真菌毒素的回收率均较好,均在70%以上,而其他4种吸附剂净化后的真菌毒素回收率较低,因此,本试验选择C18和Florisil填料作为QuEChERS净化的吸附剂。
一般QuEChERS净化处理中会添加无水硫酸镁粉末,起到除水的作用,以提高目标物的响应值,所以试验比较了3种QuEChERS吸附剂组合对回收率的影响,结果见图3。
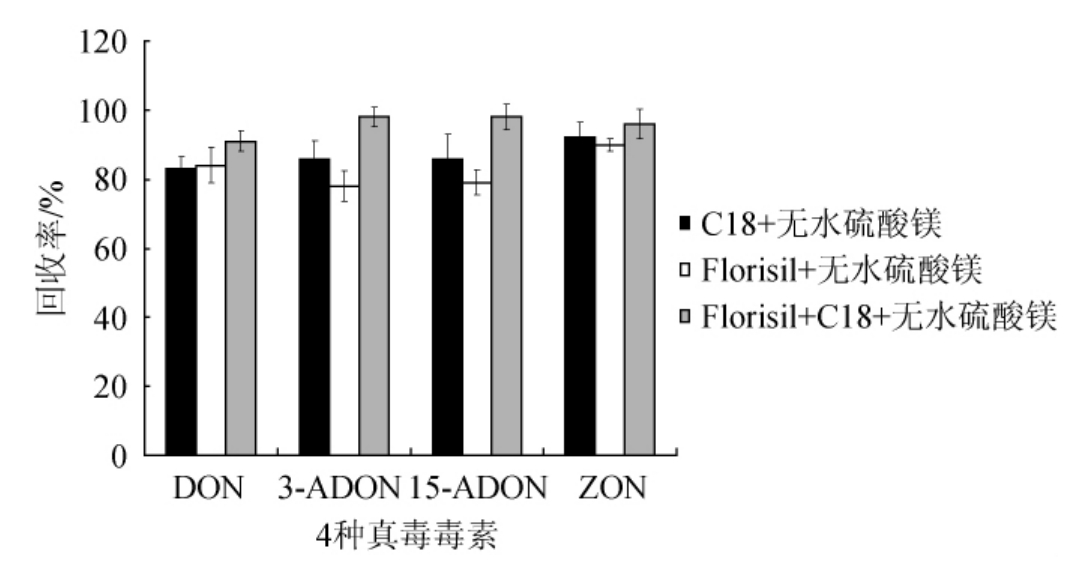
图3 4种真菌毒素经不同吸附剂组合处理后的回收率
Fig.3 Recovery of four mycotoxins treated with different adsorbent combination
由图3可知,Florisil+C18+无水硫酸镁粉末(50 mg+50 mg+300 mg)组合对4种真毒毒素的回收率较高,主要因为Florisil能吸附强极性组分与C18能吸附弱极性组分,两者形成互补,并添加了无水硫酸镁,起到除水的作用,所以本试验选择该组合作为吸附剂组成。
2.2 流动相的选择
呕吐毒素类以及玉米赤霉烯酮属于极性化合物,因此选择水和乙腈作为流动相的基础溶剂,为了促进样品的离子化,本实验比较了水相分别为0.1%甲酸、0.1%乙酸和10 mmol/L乙酸铵对4种真菌毒素分离效果的影响。实验结果发现,加入0.1%甲酸时,4种目标物的离子丰度最强,分离度较好,因此选择浓度为0.1%甲酸为水相,与乙腈组合组成流动相进行梯度洗脱,得到ZON、DON、与3-ADON和15-ADON在色谱分析图上有很好的分离度,4种目标物的离子丰度都较强,无杂质干扰,色谱图见图4。

图4 混合标准溶液色谱图
Fig.4 Chromatogram of mixture standard solution
由图4可知,4种目标化合物得以很好的分离。
2.3 质谱条件的选择
用质量浓度为50 ng/mL的混合标准溶液,对目标物进行一级和二级质谱扫描,并优化质谱参数。依据目标物的分子式和碎片离子信息拟合出理论精确质量数,采用多反应监测扫描模式进行优化参数,4种化合物优化后的质谱分析参数见表2。
表2 4种真菌毒素的多反应监测扫描模式的质谱参数
Table 2 Mass spectrometric parameters for monitoring the scanning patterns of four mycotoxins with multiple reactions

注:“*”表示定量离子。
2.4 方法的线性范围、检出限与定量限
在0.10%甲酸-乙腈流动相体系中,按照1.3.2方法进行前处理,得到空白基质提取液,用空白基质提取液稀释,配制混合标准溶液,以表1梯度洗脱的步骤,经仪器进行分析,绘制标准曲线,结果见表3。
表3 4种真菌毒素的保留时间、标准曲线、相关系数、检出限与定量限
Table 3 Retention time,standard curve,correlation coefficient,detection limit and quantitative limit of four mycotoxins
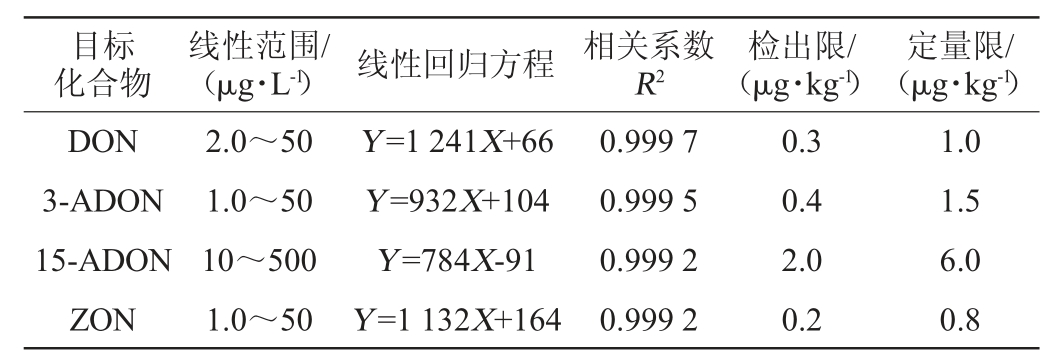
由表3可知,4种真菌毒素在上述各自的质量浓度范围内均具有良好的线性关系,相关系数R2均大于0.999。4种真菌毒素的检出限分别为DON 0.3 μg/kg、3-ADON 0.4 μg/kg、15-ADON 2.0 μg/kg、ZON 0.2 μg/kg,定量限分别为DON 1.0 μg/kg、3-ADON 1.5 μg/kg、15-ADON 6.0 μg/kg、ZON 0.8 μg/kg。
2.5 方法的回收率与精密度
在加标回收实验中,选用杂粮粥、杂粮饭、杂粮代餐粉3种空白基质的样品,分别添加1倍限量、5倍限量和10倍限量低、中、高的三个水平的标准品,每个结果测定5次,进行加标回收的试验,计算相对标准偏差(relative standard deviation,RSD),结果见表4。
表4 方法的回收率试验结果
Table 4 Results of recovery rate of the method
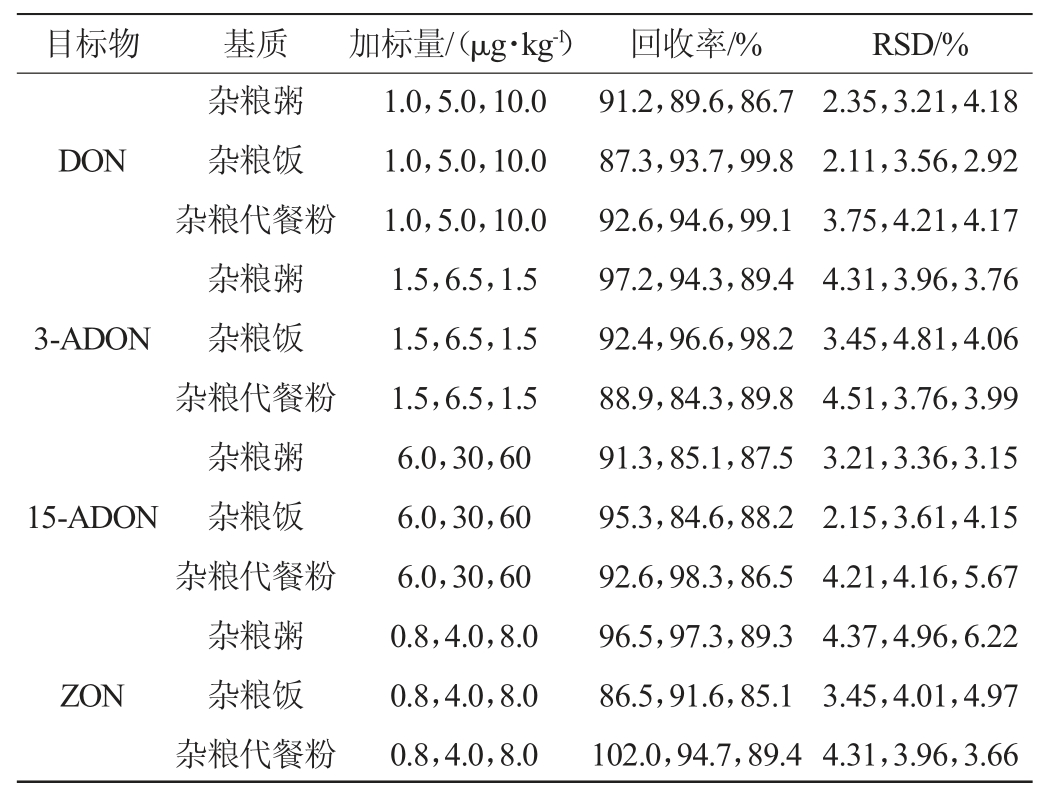
由表4可见,4种真菌毒素DON、3-ADON、15-ADON、ZON在不同基质中的回收率范围为85.1%~102.0%,RSD为2.11%~6.22%,说明本实验的检测数据的准确度和精密度可行。
2.6 实际样品的检测
应用本方法对10份谷类杂粮制品进行检测,以保留时间和碎片离子定性,外标法定量。结果表明,其中2份样品均有检出不同浓度的DON,含量分别110.3 μg/kg和260.5 μg/kg,均未超过国家标准规定的限量要求,除此以外的3种真菌毒素均未检出。
3 结论
本研究建立了一种QuEChERS-HPLC-MS/MS检测谷类杂粮制品中DON、3-ADON、15-ADON、ZON 4种真菌毒素的分析方法。实验结果表明,样品经乙腈/水(10∶90,V/V)进行提取后,经Florisil+C18+无水硫酸镁组合吸附剂处理后,可有效去除谷类杂粮制品中的干扰物对目标峰的影响,实现对4种真菌毒素的净化,在质谱检测器的多反应监测模式下,可实现同时对谷类杂粮制品中4种真毒毒素的定性和定量分析。在3种谷类杂粮样品基质中的加标回收率为85.1%~102.0%之间,相对标准偏差(RSD)在2.11%~6.22%之间,所建立的方法具有可靠的准确度和精密度,能准确快速有效地检测谷类杂粮样品基质中的4种真菌毒素的含量。
[1]侯广月,杜营,杨帆,等.谷物及其制品中真菌毒素的前处理及检测技术研究进展[J].食品科学,2019,40(8):306-310.
[2]赵英莲,张梓琪,赵鑫,等.QuEChERS 技术在食品真菌毒素检测中的研究进展[J].中国酿造,2020,39(1):1-5.
[3]TURNER NW,BRAMHMBHATT H,SZABOVEZSE M,et al.Analytical methods for determination of mycotoxins:An update(2009-2014)[J].Anal Chim Acta,2015,901(2):12-33.
[4]庞世琦,刘青,李志勇.胶体金技术快速测定葡萄酒中赭曲霉毒素A[J].食品安全质量检测学报,2016,7(8):3073-3076.
[5]张思思,陆继伟,王少敏,等.国内外真菌毒素检测方法研究现状及进展[J].食品安全质量检测学报,2016,7(7):2575-2586.
[6]王文珺,刘怡菲,韩霄,等.玉米赤霉烯酮一步ELISA 法的建立及应用[J].食品工业科技,2016,37(14):78-82.
[7]CASTILLO M D,GONZÁLEZ H H,MARTÍNEZ E J,et al.Mycoflflora and potential for mycotoxin production of freshly harvested black bean from the Argentinean main production area[J].Mycopathologia,2004,158(1):107-112.
[8]TSENG T C,TU J C,TZEAN S S.Mycoflflora and mycotoxins in dry bean (Phaseolus vulgaris) produced in Taiwan and in Ontario,Canada[J].Botanical Bulletin of Academia Sinica,2005,36(4):229-234.
[9]DUARTE S C,LINO C M,PENA A.Food safety implications of ochratoxin A in animal derived food products[J].Veterin J,2012,192(3):286-292.
[10]耿霞,赵强.基于结构转换适配体荧光法检测赭曲霉素A[J].分析科学学报,2013,29(2):164-168.
[11]梁桂娟,张琼,杨波.高效液相色谱-荧光检测法检测大米中的赭曲霉毒素A[J].中国酿造,2008,8(5):136-138.
[12]孙雪,郗存显,唐柏彬,等.复合免疫亲和柱净化-液相色谱-串联质谱法测定动物源食品中6 种黄曲霉毒素和6 种玉米赤霉醇类真菌毒素残留量[J].分析化学,2016,44(6):970-978.
[13]孙伟华,杨欢,曹赵云,等.基于分散固相萃取液相色谱-串联质谱法测定大米中8 种真菌毒素[J].分析测试学报,2017,36(1):47-53.
[14]刘青,曾广丰,王志元.QuEChERS 净化技术结合高效液相色谱-串联质谱法测定食用贝类产品中4 种脂溶性贝类毒素[J].现代食品科技,2015,31(12):338-344.
[15]林琳.QuEChERS-HPLC-MS/MS 法检测谷物源性食品中3 种赭曲霉毒素[J].食品工业,2019,40(12):311-314.
[16]VICTOR M D,LARA F J,GARCIA M,et al.Evaluation of dispersive liquid-liquid microextraction for the determination of patulin in apple juices using micellar electrokinetic capillary chromatography[J]. Food Control,2013,31(2):353-358.
[17]ANTEP H M,MERDIVAN M.Development of new dispersive liquidliquid microextraction technique for the identification of zearalenone in beer[J].Anal Meth,2012,12(4):4129-4134.
[18]ANDRADE P D,DANTAS R R,MOURA-ALVES TLDS D,et al.Determination of multi-mycotoxins in cereals and of total fumonisins in maize products using isotope labeled internal standard and liquid chromatography/tandem mass spectrometry with positive ionization[J].J Chromatogr A,2017,1490:138-147.
[19]ALASSANE-KPEMBI I,SCHATZAMYR G,TARANU I,et al.Mycotoxins contamination:Methodological aspects and biological relevance of combined toxicity studies[J].Crit Rev Food SciNutr,2016,57(16):3489-3507.
[20]周健,许娇娇,金米聪,等.响应面试验优化QuEChERS 法提取鸡蛋中杂色曲霉毒素工艺及方法学验证[J].食品科学,2017,38(24):288-295.