近些年来与米香型白酒风味相关的研究方兴未艾,主要集中在白酒发酵工艺与原料的探索[1]、酒体后期催陈效果研究[2]、不良苦味的消除[3]以及功能菌的增香效果评估[4]等。本课题组前期也针对性地做了产香酵母的筛选与产酯规律研究[5],为米香型白酒的风味改善提供了技术支撑,但均未对改善风味的工艺进行进一步分析和优化。
酒曲是富含微生物的发酵引物,素有“曲是酒中骨”的说法[6]。米曲是指以大米粉、米糠等为原料,经接种种曲后制备得到的一类优质酿酒小曲,有以生料制曲的邛崃米曲,以熟料制作颗粒曲与散曲的厦门白曲,以及绍兴酒药、宁波白药等[7-8]。
国外在酿酒领域对于产香酵母的利用较为深入,普遍将其作为生物香料以增加产品的香气多样性,而相关的研究也不断证实了产香酵母对于酿酒的积极作用[9]。将产香酵母用于制曲,丰富微生物的种系,对于酒体质量的提升有良好促进作用。
本研究将异常维克汉逊酵母(Wickerhamomycesanomalus)、扣囊复膜酵母(Saccharomycopsis fibuligera)、克鲁维毕赤酵母(Pichia kudriazevii)与酿酒酵母(Saccharomyces cerevisiae)共培养制作复配酵母种,通过对米曲制备中影响因素进行研究,利用单因素试验及响应面法对风味米曲的制备工艺进行优化,并评估了风味米曲的酿造可行性。旨在通过丰富酒曲中的功能性微生物来改善米香型白酒酒体风味。
1 材料与方法
1.1 材料与试剂
1.1.1 试验原料与菌株
一级籼米:金健米业股份有限公司;生麦芽:泉州市麦芽有限公司;小曲(广西小曲样品A、四川小曲样品B、厦门小曲样品C):满盅花酿酒设备厂;米根霉(Rhizopus oryzae)、酿酒酵母(Saccharomyces cerevisiae,SC)、克鲁维毕赤酵母(Pichia kudriazevii,PK)、异常维克汉逊酵母(Wickerhamomyces anomalus,WA)、扣囊复膜酵母(Saccharomycopsis fibuligera,SF):本实验室筛选鉴定得到并保藏的菌种。
1.1.2 化学试剂
重铬酸钾、无水乙醇、酚酞、氢氧化钠:国药集团化学试剂有限公司;盐酸、硫酸:广州凯茵化工有限公司。所用试剂均为分析纯。
1.1.3 培养基
米曲汁培养基:参照黄慧芬等[5,10]的方法制备;麦芽汁培养基:参照陈小龙等[11]的方法制备,于115 ℃下高压灭菌30 min。
1.2 仪器与设备
LRH-150生化培养箱:上海一恒科技有限公司;HZQ-C气浴恒温摇床:常州恒隆仪器有限公司;YXQ-LS-75G全自动数显高压灭菌器:上海博迅医疗生物仪器股份有限公司;BM1000生物显微镜:江南永新光学仪器有限公司;UV-2600紫外可见光分光光度计:日本岛津公司;DK-98-2电热恒温水浴锅:上海虔钧科学仪器有限公司;5804R台式高速冷冻离心机:艾本德中国有限公司;JH-H5快速水份测定仪:泰州市宜信得仪器仪表有限公司。
1.3 方法
1.3.1 风味米曲制曲工艺流程及操作要点[12]

操作要点:
粉碎过筛:取籼米粉碎后过60目筛,作为米曲培养的原料。
灭菌、打散:将米粉在121 ℃高压蒸汽灭菌30 min后,趁热打散。
米根霉固体米粉种曲制备:用米根霉制备纯种固体米粉种曲[13]。
复配酵母共培养种子液的制备:取SC及3株产香酵母PK、WA、SF菌株试管种,挑取一环接种于装有50 mL YPD液体培养基的100 mL三角瓶中,于30 ℃、150 r/min气浴摇床中活化24 h,将上述3株产香酵母种子活化液以106∶106∶106(CFU/mL)的比例接种到米曲汁培养基中,于30 ℃培养8 h后,再以106 CFU/mL的浓度接种SC种子活化液,继续共培养24 h,制得复配酵母共培养种子液。
接种培养:在灭菌后打散的米粉中加入25%无菌水,接种5%米根霉种,再接种酵母共培种,32 ℃培养72 h至米粉结块良好,翻曲培养至米曲成熟后出箱,得到风味米曲。
1.3.2 风味米曲试饭的制备[13]
米香型白酒原料为大米,根霉曲直接接种米饭作为糖化发酵剂,采用试饭的方法来检测风味米曲的质量。
试饭的制备:取籼米50 g,按米水比1∶1.2(g∶mL)加水,115 ℃高压灭菌15 min,用无菌药匙趁热搅散,要求饭质量等于大米和所加水量之和,不足部分用无菌水补足,待米饭凉至35 ℃左右,以大米质量1%的比例(即0.5 g)称取风味米曲均匀地拌和到米饭中,在30 ℃固态糖化24 h后,以大米质量的150%加水密闭发酵3 d。测定其试饭的感官评分、酯和乙醇含量。
1.3.3 风味米曲制备工艺优化单因素试验
在接种根霉固体种曲后8 h再接种液体酵母种共培养制备米曲的基础上,分别考察培养温度(26 ℃、28 ℃、30 ℃、32 ℃、34 ℃)、培养时间(36 h、48 h、60 h、72 h、84 h)以及酵母添加量(0.6%、0.8%、1.0%、1.2%、1.4%)对风味米曲制备的影响。
1.3.4 响应面法优化风味米曲制备工艺
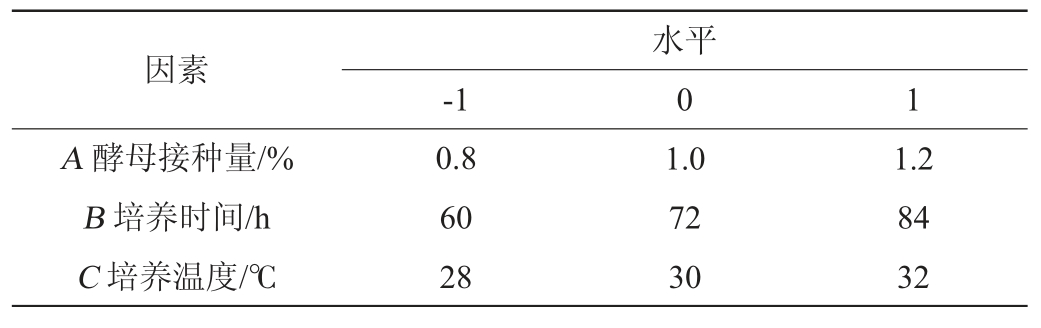
在单因素试验的基础上,选取风味米曲制备的关键影响因素酵母接种量(A)、培养时间(B)、培养温度(C)进行考察,以试饭酯含量(Y)为响应指标进行Box-Behnken响应面设计优化,Box-Behnken试验因素与水平见表1。
表1 Box-Behnken试验设计因素与水平
Table 1 Factors and levels of Box-Behnken experiments design
1.3.5 分析检测
(1)试饭指标
试饭酯含量的测定参照卢亭等[14]的方法;试饭乙醇含量的测定参照吴琼燕[15]的方法;按国标GB/T 33405—2016《白酒感官品评术语》[16]中白酒中风味评价的标准并参照吴琼燕[15]等的品评方法进行试饭感官评价。
(2)风味米曲理化指标
采用快速水分测定仪测定风味米曲水分含量;参照马歌丽等[17]的方法测定风味米曲糖化力;参照QB/T 4257—2011《酿酒大曲通用分析方法》[18]测定风味米曲的发酵能力。
1.3.6 风味米曲的半固态发酵验证
对响应面优化制曲工艺进行试饭验证后,以市场上的3种小曲样品A、B、C作为对照,将风味米曲作为酿造酒曲进行半固态发酵验证。取籼米1 000 g,按照1.3.2中的方法进行处理并摊凉后,按米质量的1%取酒曲均匀地拌和到米饭中,在30 ℃固态糖化24 h后,加水150%,密闭发酵7 d。将发酵繆取出进行常压蒸馏,截取头酒后,将中段酒接至56%vol后停止接酒,并测定酒体总酸总酯含量,同时参照米香型白酒品评方法对酒体进行感官评价[5]。
2 结果与分析
2.1 风味米曲制备工艺优化单因素试验
2.1.1 不同培养温度对风味米曲试饭指标的影响
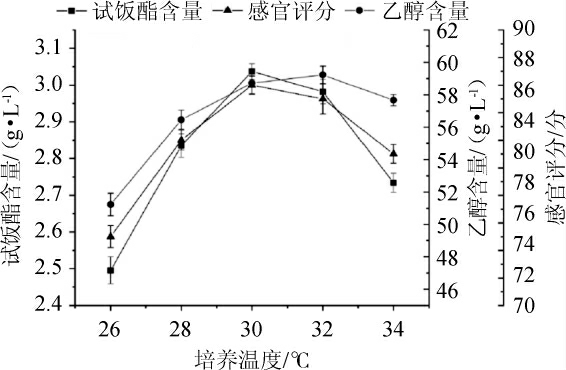
图1 培养温度对试饭指标的影响
Fig.1 Effect of culture temperature on testing indicators of steamed rice
由图1可知,随着培养温度的不断上升,试饭指标均呈现出先升后降的趋势,其中试饭酯含量与感官评分变化趋势一致,在26~30 ℃的培养温度范围内逐渐增高,在30 ℃时达到峰值,分别为3.04 g/L与86分,继续升温会导致两者均出现大幅度下降。试饭乙醇含量随着温度在26~33 ℃范围增加逐渐升高,并在32 ℃达到最大值(59.23 g/L),继续升温试饭乙醇含量减少。综合考虑,选择最适培养温度为30 ℃。
温度是影响微生物生长的重要因素,但菌体生长的最适温度与代谢产物累积的最佳温度通常并不相符,这可能与发酵体系中的物质基础相关,代谢产物的生成会受到发酵体系中的物质调控,与ROLLERO S等[19]的研究结果一致。
2.1.2 不同培养时间对风味米曲试饭指标的影响
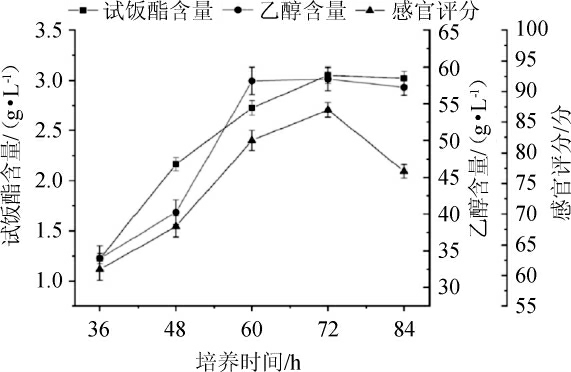
图2 培养时间对试饭指标的影响
Fig.2 Effect of culture time on testing indicators of steamed rice
由图2可知,培养时间在36~72 h内,试饭酯含量、乙醇含量与感官评分3个试饭指标均随着培养时间的延长逐渐增高,并在72 h出现了峰值,分别为3.05 g/L、58.37 g/L以及87分。培养时间>72 h之后,试饭酯含量、乙醇含量稍微下降,感官评分出现了较大程度的降低。综合考虑,选择最适培养时间为72 h。
2.1.3 不同酵母接种量对风味米曲试饭指标的影响
酒曲微生物的菌群多样性与酒体中各种微量成分的形成密切相关,不同的接种比例会直接影响到代谢物质的含量[20]。
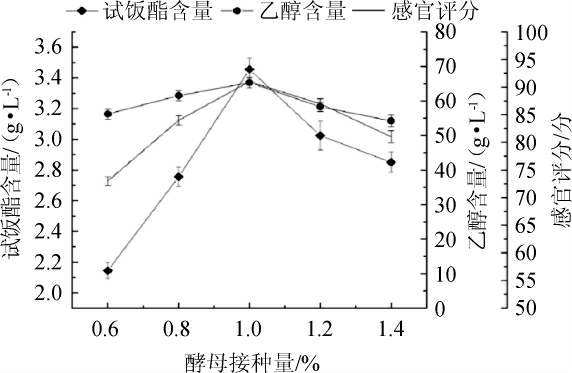
图3 酵母接种量对试饭指标的影响
Fig.3 Effect of yeasts inoculum on testing indicators of steamed rice
由图3可知,酵母接种量在0.6%~1.0%范围内增加,试饭酯含量、乙醇含量及感官评分也随之升高,3个指标均在1.0%的接种比例下达到峰值,分别为3.46 g/L、65.35 g/L以及91分。随着接种量的进一步增加,3个试饭指标均随之降低,继续加大酵母接种量不利于发酵平衡以及产物的代谢。综合考虑,选择最适酵母接种量为1.0%。
产香酵母可通过生物转化形成芳香酮以及酯类物质[21],在一定范围内,增大产香酵母的接种比例可增加其代谢产物的浓度,但超出适宜范围之后,会对根霉的生长造成不利影响,这可能是引起试饭指标下降的一个重要原因。
2.2 风味米曲制备工艺优化的Box-Behnken响应面试验
2.2.1 Box-Behnken 响应面设计与结果
根据单因素试验结果,以试饭酯含量(Y)为响应值,选择显著影响试饭指标的因素酵母接种量(A),培养温度(B)、培养时间(C)进行Box-Behnken响应面优化,结果见表2。
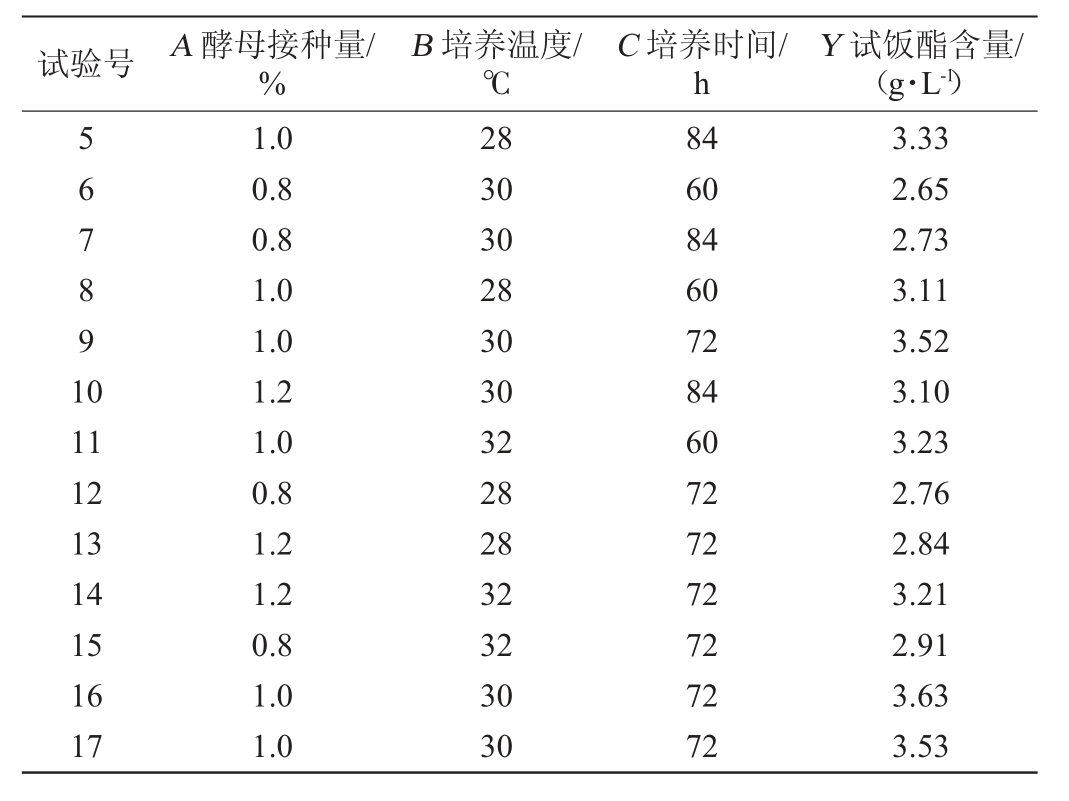
表2 Box-Behnken试验设计结果
Table 2 Results of Box-Behnken experiments design
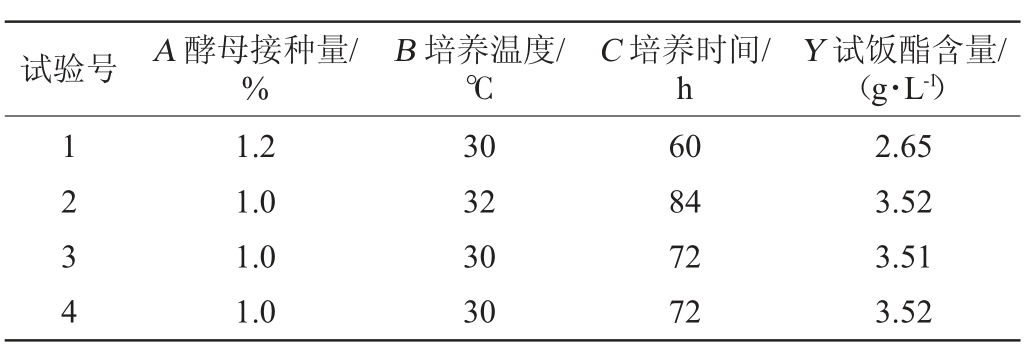
续表
对试饭酯含量(Y)进行二次项模型的回归拟合分析,得到回归方程为:
2.2.2 试饭酯含量的方差与可信度分析
进一步对表2各组试验的结果进行方差分析,结果见表3。
由表3可知,针对试饭酯含量选用二次项模型进行回归拟合,模型P值<0.000 1,具有极显著差异,拟合精度良好,可用该模型进行后续的优化分析;同时失拟项P值>0.05,差异不显著,说明该二次项模型在整个回归区域类拟合较好[22],试饭酯含量的模型拟合成功。同时,从各因素在模型拟合中的P值来看,一次项A、B、C,二次项A2与C2对试饭酯含量有极显著的影响(P<0.01);交互项AB、AC对试饭酯含量有显著性的影响(P<0.05)。
表3 回归模型方差分析
Table 3 Variance analysis of regression model
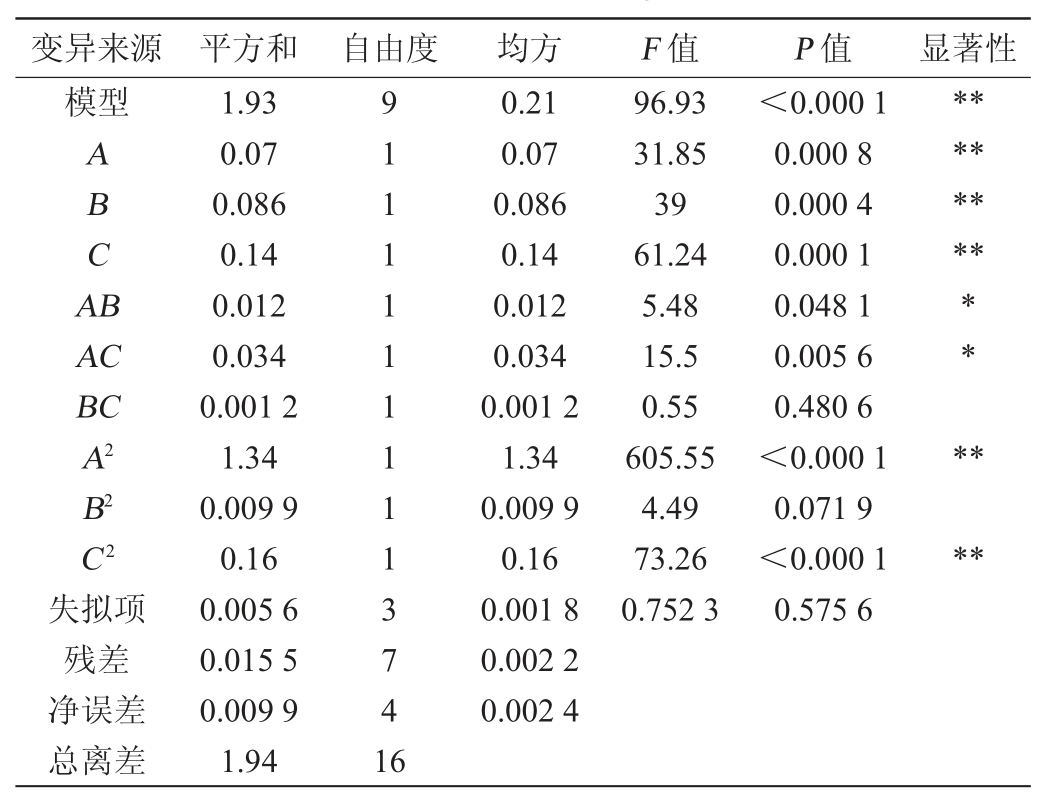
注:“*”表示对结果影响显著(P<0.05);“**”表示对结果影响极显著(P<0.01)。
模型的决定系数R2与调整决定系数R2adj分别为0.992 6、0.981 8,证明拟合后99.26%的试饭酯含量可由模型解释,98.18%的变化来源于考察的变量,调整优化后的模型能充分说明工艺情况。变异系数为1.486 1%,在实验范围内的变异较小,数据的离散程度在可接受范围内。
2.2.3 试饭酯含量的响应面分析及验证试验
对风味米曲试饭指标的响应面进行分析,各因素交互作用对试饭酯含量影响的响应面及等高线见图4。
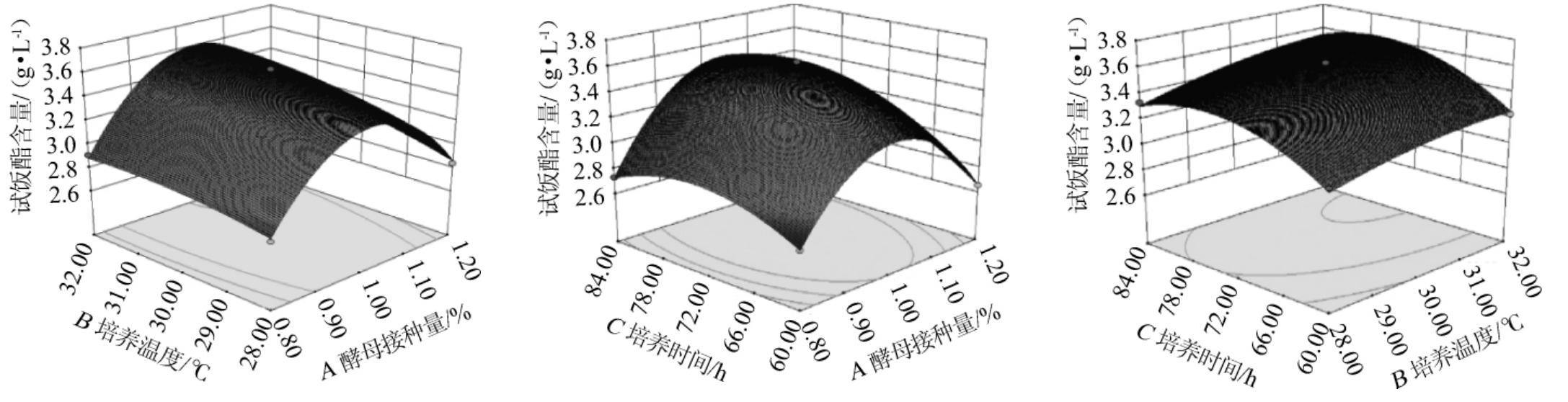
图4 酵母接种量、培养温度、培养时间交互作用对试饭酯含量影响的响应面及等高线
Fig.4 Response surface plots and contour lines of effects of interaction between inoculum,culture temperature and time on ester contents of steamed rice
由图4可知,AB、AC交互作用对于试饭酯含量均有显著影响,以试饭酯含量为响应指标,拟合出的最佳制备工艺参数为酵母接种量1.03%、培养温度30 ℃、培养时间72.98 h,此优化条件下试饭酯含量预测值为3.64 g/L。为了便于实际操作,将理论最优的风味米曲制备工艺修正为酵母接种量1.0%,培养时间73 h,培养温度30 ℃。在此优化制备工艺条件下,得试饭的酯含量实际值为3.65 g/L,与理论值基本一致,表明响应面拟合成功,可为实际的制曲提供参考。
2.3 风味米曲的质量指标检测
由图5可知,4种小曲的水分含量均≤13%,其中小曲A的水分含量最高,与其余3种小曲相比差异具有显著性(P<0.05),而小曲C、小曲B、自制风味米曲则无明显区别(P>0.05)。风味米曲的糖化力达到423.77 U/g,与小曲A、小曲B无明显差异(P>0.05),但显著高于小曲C(P<0.05)。而从发酵力指标可看出,风味米曲达到2.24 g/(g·72 h),与其余小曲相比具有显著性差异(P<0.05),具备良好的发酵能力。
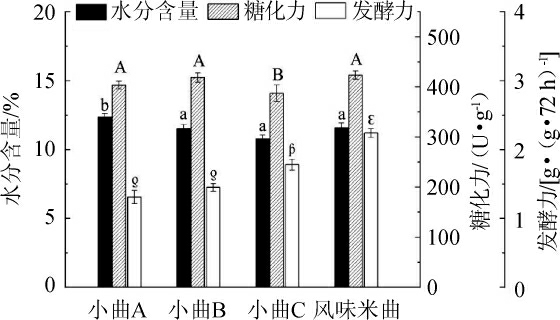
图5 风味米曲的半固态发酵结果
Fig.5 Semi-solid fermentation results of flavor rice starter
不同字母表示同指标差异显著(P<0.05)。下同。
2.4 风味米曲的半固态发酵制备米香型白酒验证
选择了不同产区的优质小曲样品A、B、C作为对照,进行实际酿造,研究了最优拟合工艺下制备出的风味米曲的酿造效果,结果见图6。
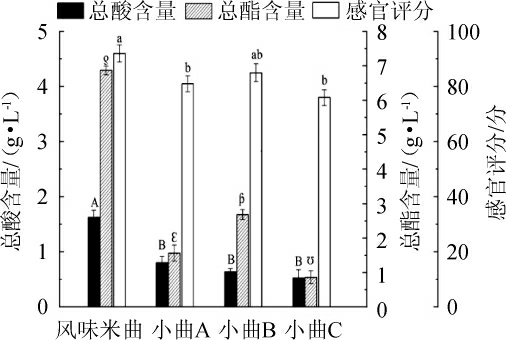
图6 风味米曲的半固态发酵验证试验结果
Fig.6 Verification tests results of semi-solid fermentation results of flavor-producing rice starter
由图6可知,4种酒曲的酿造效果具有明显差异。其中风味米曲的总酯含量与其余3种小曲具有显著性差异(P<0.05),产量最高,达到了6.87 g/L;此外总酸含量、感官评分值分别为1.63 g/L、92分,同样与其余酒曲具有显著性差异,均为最优。产香酵母的添加,使得风味米曲的产酯能力与产酸能力明显提升,这对酒体感官品质起到了很大的贡献作用,极大的改善了米香型白酒香气。为优质米曲的工业化生产提供了参考。
3 结论
用3株产香酵母与1株酿酒酵母制备复配酵母种,与纯种米根霉菌共培养制备风味米曲,以试饭感官评价分值、试饭酯含量、试饭乙醇含量为评价指标,针对酵母接种比例、培养温度、培养时间进行单因素试验。在此基础上,以米曲的试饭酯含量为响应指标,采用响应面法优化了制曲工艺,建立了风味米曲制作工艺的二次项回归模型,拟合出的理论最优工艺为酵母接种量1.0%,培养时间73 h,培养温度30 ℃。在此优化制备工艺条件下,试饭的酯含量为3.65 g/L。
风味米曲的质量指标检测与半固态发酵酿酒实验结果显示,风味米曲水分含量为10.58%,糖化力为423.77 U/g,发酵力为2.24 g/(g·72 h)。经半固态法实际酿酒后,酒体总酯含量达到了6.87 g/L,总酸与感官评分分别为1.63 g/L、92分,具备米香型白酒典型风格,且风味明显提升。利用产香酵母制备风味米曲,对米香型白酒起到了明显的增香作用。
[1]李明球,彭松林.低度小曲米香型白酒生产过程中几个问题的探讨[J].酿酒,2018,45(1):50-52.
[2]魏群舒,杨勇,陈雨,等.超声波催陈米香型白酒的研究[J].中国酿造,2017,36(10):66-70.
[3]肖丽琼.米香型白酒苦味物质形成机理及控制措施研究[D].广州:仲恺农业工程学院,2014.
[4]吴金燕,梁振荣,韦文宁,等.提升米香型原酒总酯的功能菌研究[J].酿酒科技,2017(11):50-53,56.
[5]黄慧芬.米香型白酒酿造产香酵母的筛选鉴定及其产酯规律研究[D].长沙:中南林业科技大学,2018.
[6]王俏.白酒大曲贮存过程中主要微生物活性快速检测方法的研究[D].乌鲁木齐:新疆农业大学,2015.
[7]张和笙.闽南地区小曲酒工艺特点及香味成分剖析[J].酿酒科技,2003(2):20-21.
[8]景泉.酒曲生产实用技术[M].北京:中国食品出版社,1988:58-62.
[9] BASSO R F,ALCARDE A R,PORTUGAL C B.Could non-Saccharomyces yeasts contribute on innovative brewing fermentations?[J].Food Res Int,2016,86:112-120.
[10]毛宜祥,郑翠萍.怎样制好米曲汁培养基[J].上海调味品,1990(1):31.
[11]陈小龙,王远山,郑裕国,等.腺苷蛋氨酸发酵条件及发酵培养基的优化[J].中国生物工程杂志,2004(11):64-68.
[12]张和笙.谈谈厦门白曲[J].酿酒,2003,30(1):14-16.
[13]吴健,祝贺,蓝彩红,等.响应面法优化纯种根霉米粉种曲制作工艺[J].中国酿造,2019,38(9):86-90.
[14]卢亭,何计龙,夏慧丽,等.水浴静置皂化法测定白酒中的总酯[J].食品研究与开发,2016,37(23):154-156.
[15]吴琼燕.中草药对甜酒曲微生物发酵性能及酒酿香气成分研究[D].广州:华南农业大学,2016.
[16]中华人民共和国国家质量监督检验检疫总局.GB/T 33405—2016 白酒感官品评术语[S].北京:中国标准出版社,2016.
[17]马歌丽,魏泉增,张志刚.分光光度法测定大曲糖化酶活力探讨[J].中国酿造,2008,27(17):73-75.
[18]中华人民共和国工业和信息化部.QB/T 4257—2011 酿酒大曲通用分析方法[S].北京:中国标准出版社,2011.
[19]ROLLERO S,BLOEM A,ORTIZ-JULIEN A,et al.Fermentation performances and aroma production of non-conventional wine yeasts are influenced by nitrogen preferences[J].Fems Yeast Res,2018,18(5):1-11.
[20]刘昕,吴天祥,赵群丽,等.基于Kriging 代理模型对产不饱和脂肪酸的酒曲微生物混菌比例优化[J].酿酒科技,2016(9):23-27.
[21]CONTENTE M L,MOLINARI F,ZAMBELLI P,et al.Biotransformation of aromatic ketones and ketoesters with the non-conventional yeast Pichia glucozyma[J].Tetrahed Lett,2014,55(51):7-8.
[22]李莉,张赛,何强,等.响应面法在试验设计与优化中的应用[J].实验室研究与探索,2015,34(8):41-45.