清香型大曲白酒是我国的四大白酒之一,它以高粱为主要原料酿造而成。在酿造过程中,高粱品种的质量直接影响着白酒的产量和品质。高粱的理化品质不仅包括淀粉、脂肪、蛋白质等,同时还包括其他重要的物质如单宁。单宁又称多酚,是植物的次生代谢产物。单宁根据其化学性质分为水解单宁和缩合单宁。水解单宁的相对分子质量为500~3 000 Da,主要分布在茶、水果、豆类和坚果中;缩合单宁的相对分子质量为2 900~28 000 Da,通常存在于谷物、菜籽、双子叶植物等体内。缩合单宁是高粱中单宁的主要存在形式。已有研究表明,不同品种高粱中的单宁含量不同,若单宁含量过高,则会阻碍白酒发酵的正常进行,使成品酒香气不足、口感苦涩[1];相反若单宁含量过低,则会导致成品酒因缺少主要成味物质而口感寡淡[2]。而适量的单宁除了可赋予白酒特殊的香气和提升口感[3-5]之外,更重要的是部分微生物能分泌单宁酶而降解单宁[6-7];因此,高粱单宁能通过影响白酒酿造过程中微生物的生长来间接影响出酒率[1-2,8-9]。而目前国内外的相关研究尚非常少,蒋兰等[1,10]研究发现,适量单宁能抑制白酒发酵中部分有害微生物的生长。
适中的单宁含量是优质高粱的必备条件[11]。本研究利用高通量测序技术比较了含单宁高粱和不含单宁高粱对清香型大曲白酒酒醅中细菌种群的影响,并分析了高粱单宁含量与细菌种群的关系,旨在为选育具有合理单宁含量的高粱品种提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 样品
采自山西省汾阳市某清香型大曲白酒厂的酒醅,其酿造原料分别是同种高粱的含单宁品种和不含单宁品种。
1.1.2 主要试剂
琼脂糖凝胶回收试剂盒:日本宝生物工程株式会社;2×Phusion High-Fidelity PCR Master Mix:美国纽英伦生物技术公司;Ion Plus建库试剂盒:美国赛默飞世尔公司。其余试剂均为分析纯。
1.2 仪器与设备
ALS 1296聚合酶链式反应(polymerase chain reaction,PCR)仪、Gel Doc 2000 UV凝胶成像系统:美国Bio-Rad公司;5417R高速冷冻离心机:德国Eppendorf公司;HH数显恒温水浴锅:江苏金坛市金城国胜实验仪器厂;SIM-F123制冰机:日本三洋电子有限公司;SK-1国华快速混匀器:常州国华电器有限公司;DYY-6C型电泳仪:北京六一仪器厂;Nova-Seq6000测序仪:美国Illumina公司。
1.3 方法
1.3.1 酿造阶段操作条件
酿造过程共21 d,分别经历以下3个阶段:①升温阶段(1~7 d):起始温度约15 ℃,每天升温2 ℃,约第7天达到28 ℃;②稳定阶段(8~15 d):在28 ℃维持8 d;③降温阶段(16~21 d),每两天降温1 ℃,约6 d后降至25 ℃。在升温阶段的初期(第1天)、中期(第3天)、末期(第7天)和降温阶段的末期(第21天)分别取样,含单宁的样品编号为A、B、C和D,而不含单宁的样品编号为a、b、c和d。每个样品3个平行。
1.3.2 样品基本理化指标测定
温度的测定:在发酵缸内距离表层30 cm处的中心点测定。含水量的测定:依据GB 5009.3—2016《食品中水分的测定》进行。单宁含量的测定:依据GB/T 15686—2008《高粱单宁含量的测定》进行。
1.3.3 样品细菌基因组DNA的提取及检测
用磷酸缓冲液(0.1 mol/L)洗涤样品3次,收集菌体。利用十六烷基三甲基溴化铵法(cetyl trimethyl ammonium bromide,CTAB)法提取细菌的基因组DNA[12],用0.7%琼脂糖凝胶电泳检测。
1.3.4 样品16SrDNAV4区的PCR扩增及测序
扩增引物515F:5'-TGCCAGCMGCCGCGGTAA-3'和806R:5'-GGACTACHVGGGTTCTAAT-3'。PCR反应体系(30μL):2×Mix,15μL;515F(2μmol/L),3μL;806R(2μmol/L)3 μL;基因组DNA,10μL(5~10ng);ddH2O补至30μL。PCR反应条件:预变性94℃、5 min;变性94 ℃、30 s;退火55℃、30 s;延伸72℃、90 s;35个循环后,72 ℃保温10 min。扩增产物经1%的琼脂糖凝胶电泳检测。
将扩增产物使用建库试剂盒构建文库,经Thermofisher的IonS5XL上机测序。由北京诺禾致源生物公司完成。
1.3.5 生物信息分析
将测序得到的原始序列进行质控、过滤、去嵌合体,得到有效序列。将有效序列按97%的相似度进行操作分类单元(operational taxonomic units,OTU)聚类,即分子水平分类的“种”[13]。选取每一个OTU中的代表序列进行物种注释。
1.3.6 多样性分析和统计分析
对OTU进行丰度分析,计算样品的多样性指数。利用Edge R软件进行统计分析以比较差异性。
2 结果与分析
2.1 高粱样品基本理化指标的测定
表1 高粱样品基本理化指标的测定
Table 1 Determination of normal physicochemical index of sorghum samples
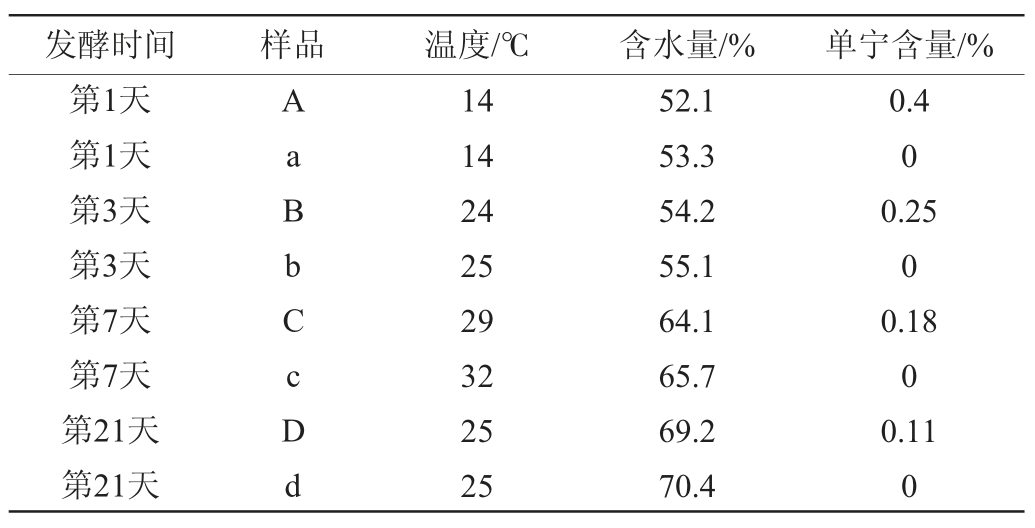
由表1可知,在发酵旺盛阶段,含单宁样品温度略低于不含单宁样品的温度;在整个发酵阶段,不含单宁样品的含水量较高,这表明不含单宁高粱样品更有利于产生水分的微生物的生长。两种样品的单宁含量在整个发酵过程中不断下降,这表明单宁参与了整个发酵过程,对样品的理化特性有一定的影响。
2.2 不同单宁含量高粱样品中细菌多样性的丰度
表2 不同高粱样品的原始序列数、有效序列数和OTU数
Table 2 Original sequence number,effective sequence number and OTU number of different sorghum samples
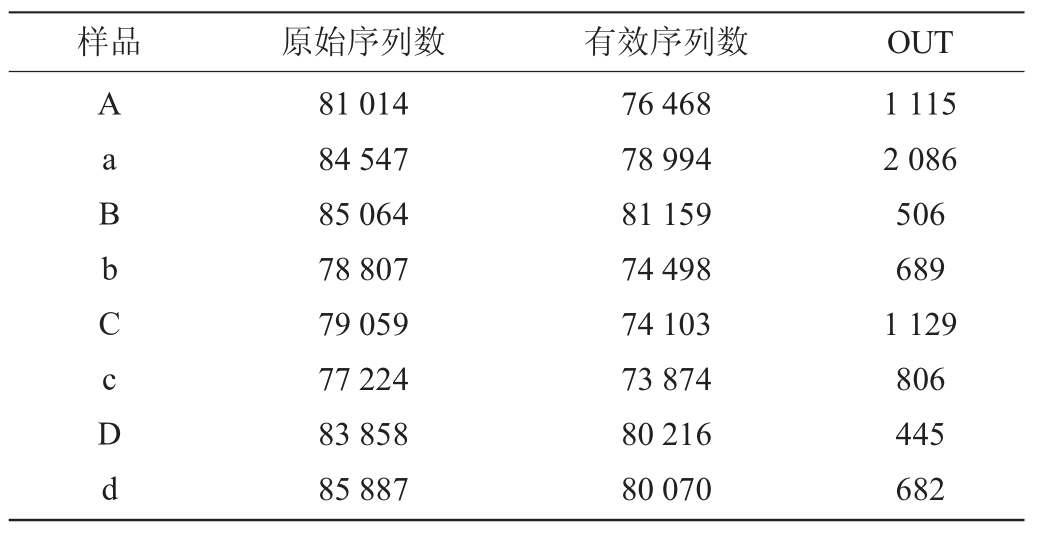
由表2可知,在发酵第1、3、7和21天,含单宁样品中的OTU分别是1 115、506、1 129和445个;不含单宁样品中的OTU分别是2 086、689、806和682个。在发酵初期,不含单宁样品的OTU数量多于含单宁样品的;但是在发酵中期情况相反,这可能是由于发酵中期单宁含量降低,对细菌的抑制作用降低,从而增加了细菌的数量。
稀释曲线可直接反映测序数据量的合理性,当曲线趋向平坦时,说明测序深度基本可以覆盖样品中的所有物种。丰度等级聚类曲线可直观地反映样本中物种的丰富度和均匀度,在横轴方向上,曲线的跨度越大,表示物种的丰富度越高;在纵轴方向上,曲线越平缓,表示物种分布越均匀[14]。
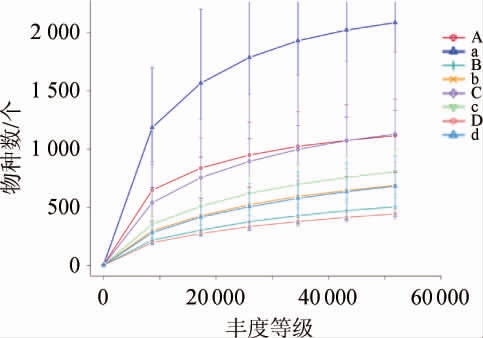
图1 不同高粱样品的稀释曲线
Fig.1 Rarefaction curves of different sorghum samples
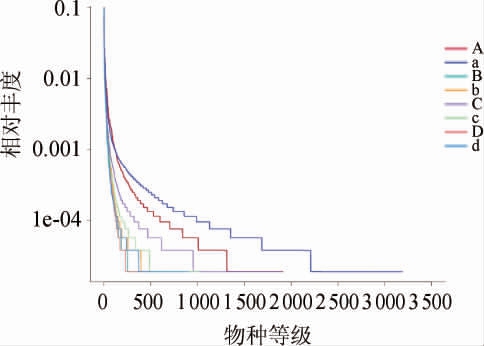
图2 不同高粱样品的丰度等级聚类曲线
Fig.2 Rank-abundance curves of different sorghum samples
由图1可知,8个样品的稀释曲线均趋于平缓,表明测序量可以较好地反映酒醅中的物种信息。由图2可知,在发酵的初期和末期,不含单宁的样品比含单宁的样品的细菌种类丰富、均匀。
2.3 不同单宁含量高粱样品中细菌的多样性分析
2.3.1 α-多样性分析
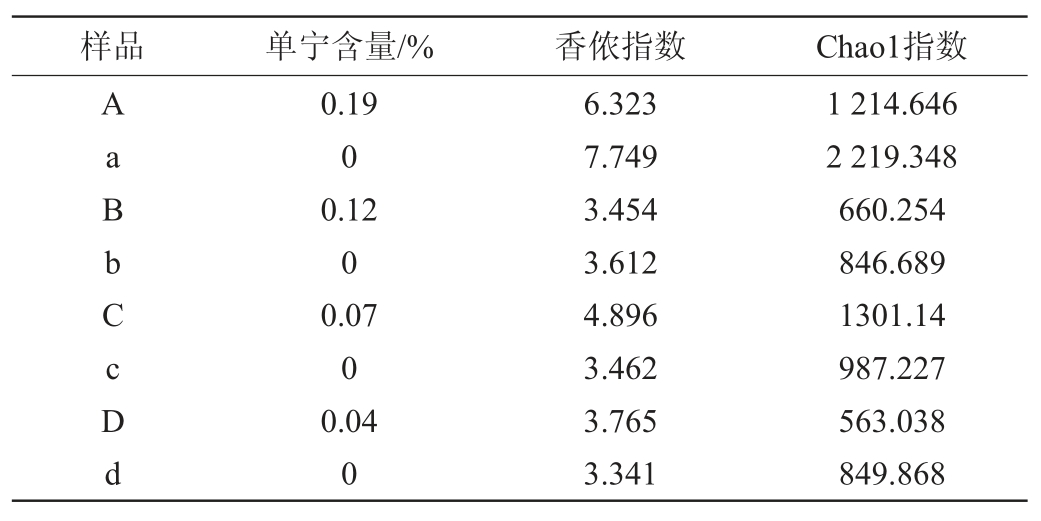
香侬指数可以反映样品的物种多样性,香侬指数越大,说明样品内物种丰度越多[15]。Chao1指数即物种丰富度指数,可以预测样品中细菌的总种类数[16]。不同样品OTU的α-多样性分析结果见表3。
由表3可知,在发酵的第1天和第3天,不含单宁样品的香侬指数高于含单宁样品的;但在第7和第21天,情况却完全相反。说明在发酵中后期,样品中的单宁含量影响了细菌种群的丰度。由Chao1指数预测值OTU数(表3)与实际OTU数(表2)相比结果可知,OTU的预测值与实际值有80%~90%的符合度,说明测序结果基本可以代表样品的种类数。
表3 不同高粱样品的OTU的α-多样性指数
Table 3 α-diversity indexes of OUT of different sorghum samples
2.3.2 β-多样性分析
主成分分析(principal component analysis,PCA)是一种对多维数据进行降维后提取出最主要元素的方法。不同样品OTU的PCA分析结果见图3。由图3可知,主成分1和主成分2的样品中细菌种群的差异性贡献率分别为40.50%和9.99%。对于含单宁和不含单宁的样品来说,除了发酵第1天外,其余每个发酵时间的细菌均能较好地聚集在一起,说明除了发酵第1天外,每个样品的3个平行之间的细菌种群相似。在整个发酵过程中,含单宁的样品和不含单宁的样品之间均有间隔,说明二者的细菌种群有差异。
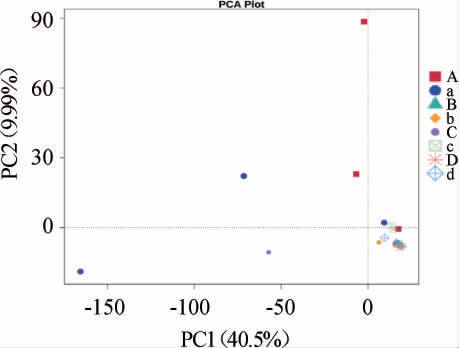
图3 不同高粱样品的细菌种群主成分分析
Fig.3 PCA analysis of bacteria community of different sorghum samples
2.4 细菌种群结构分析
2.4.1 不同单宁含量高粱样品细菌种群在门水平上的组成
由图4可知,含单宁样品和不含单宁样品中的细菌类群排名前10的是厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、拟杆菌门(Bacteroidetes)、蓝藻门(Cyanobacteria)、放线菌门(Actinobacteria)、酸杆菌门(Acidobacteria)、梭杆菌门(Fusobacteria)、疣微菌门(Verrucomicrobia)、绿弯菌门(Chloroflexi)和螺旋体门(Spirochaetes)。
在整个发酵过程中,含单宁样品和不含单宁样品中的细菌类群差异很大。在发酵第1天,含单宁样品和不含单宁样品中的优势类群分别为厚壁菌门和其他类群。在发酵第3天,含单宁样品和不含单宁样品中的优势类群分别为变形菌门和厚壁菌门,可见样品的单宁含量在发酵初期对样品细菌类群的影响很大。造成这一差别的原因可能是样品中一定浓度的单宁可以被微生物分泌的单宁酶分解[3],而过高浓度的单宁则会抑制微生物的生长[1,10]。而白酒发酵是多种微生物混合发酵的过程,因此,部分微生物的生长情况会直接影响群体的结构,从而导致了细菌类群的差异。在发酵第7天和第21天,含单宁样品和不含单宁样品中的优势类群均为厚壁菌门。
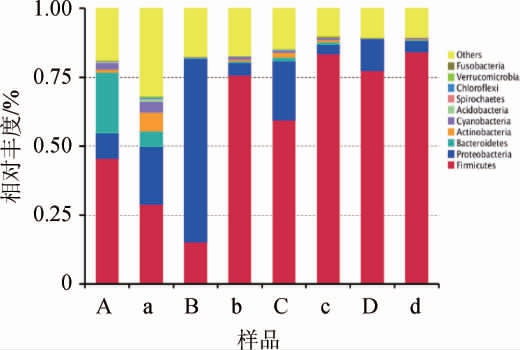
图4 不同高粱样品的细菌种群在门水平上的分布
Fig.4 Distribution of bacterial community of different sorghum samples at phylum level
王青山[17]对不同地域清香型白酒发酵微生物种群结构的比较结果中,厚壁菌门和变形菌门是主要种群,且发酵中期后,厚壁菌门占主要地位,这与其他香型白酒微生物的研究结果相吻合[18-21]。李晓然[22]发现汾酒发酵过程中的主要细菌也是厚壁菌门。这与该研究结果是一致的。
2.4.2 不同单宁含量高粱样品细菌种群在属水平上的组成
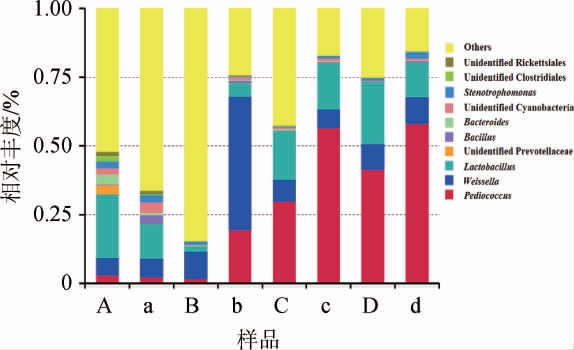
图5 不同样品的细菌种群在属水平上的分布
Fig.5 Distribution of bacterial community of different samples at genus level
由图5可知,含单宁样品和不含单宁样品中的细菌类群主要为片球菌属(Pediococcus)、魏斯氏菌属(Weissella)、乳杆菌属(Lactobacillus)、芽孢杆菌属(Bacillus)、拟杆菌属(Bacteroides)和窄食单胞菌属(Stenotrophomonas)等。
在整个发酵过程中,含单宁样品和不含单宁样品中的细菌类群在属水平上差异很大。在发酵第1天,含单宁样品和不含单宁样品中的第一优势类群均为其他属。在发酵第3天,含单宁样品中的绝对优势类群依然是其他属,而不含单宁样品中的优势类群则为魏斯氏菌属。在发酵第7天,含单宁样品中的优势类群还是其他属,只是比例大幅度降低,不含单宁样品中的优势类群变成了片球菌属。在发酵第21天,含单宁样品和不含单宁样品中的优势类群均为片球菌属,比例均高于第7天样品的。
综上,本实验中清香型大曲白酒酒醅的优势类群为片球菌属、乳杆菌属和魏斯氏菌属,这与其他研究者的结果部分相符[17]。乳杆菌属、魏斯氏菌属存在于多种香型白酒的发酵过程中,也是白酒发酵中主要的功能种群[17-19,21,22],为白酒中风味物质的合成提供前体物质[18,23]。
2.5 不同单宁含量高粱样品的细菌种群在属水平上的区别
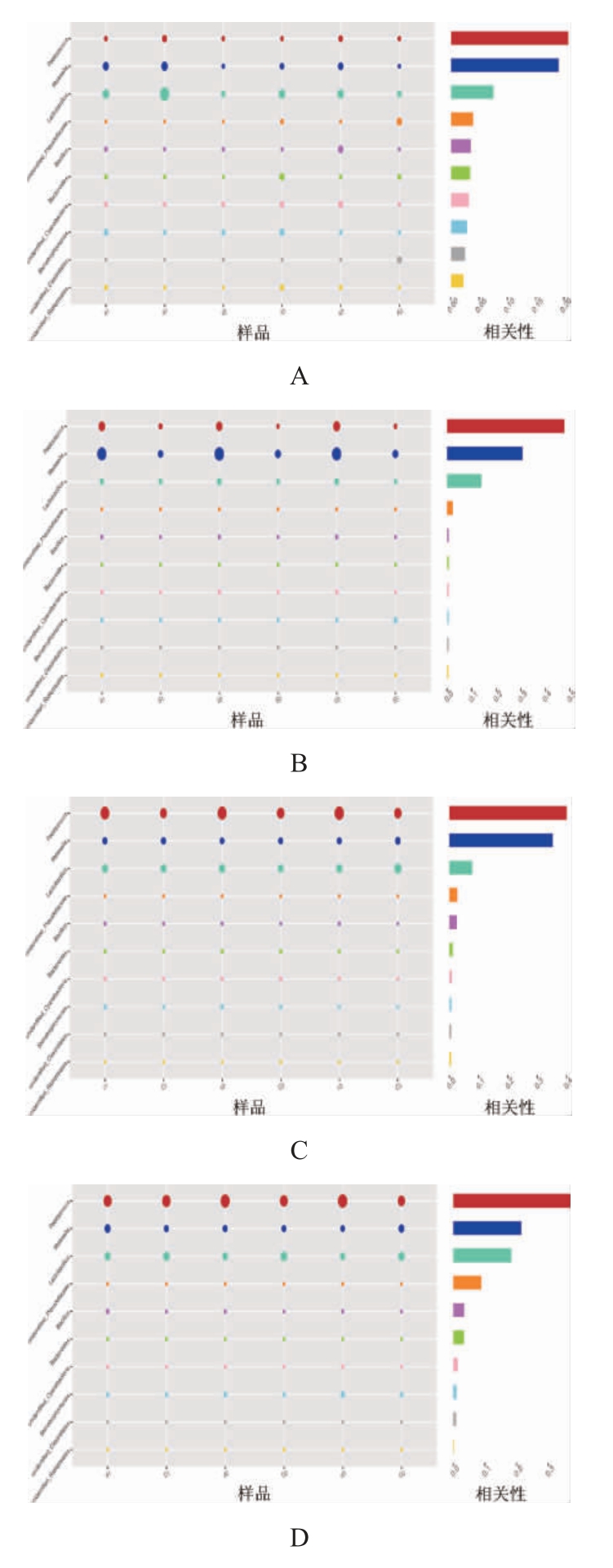
图6 含单宁和不含单宁的高粱样品在属水平上的细菌种群比较
Fig.6 Comparison of bacteria community of sorghum samples with and without tannin at genus level
圆圈的大小代表该属所占比例的大小,A、B、C和D分别指发酵第1天、3天、7天和21天样品。
由图6可知,在发酵第1天,在对两种样品物种差异贡献度排名前10的物种中,乳杆菌属在含单宁样品中的丰度大于不含单宁样品中的丰度;其次是魏氏菌属(见图6A);但是它们的丰度差异在统计学上不显著。在发酵第3天,魏氏菌属在含单宁样品中的丰度远低于不含单宁样品中的丰度;其次是片球菌属;乳杆菌属在含单宁样品中的丰度略低于不含单宁样品中的丰度(见图6B)。在发酵第7天,片球菌属在含单宁样品中的丰度低于不含单宁样品中的丰度;魏氏菌属和乳杆菌属在二者中的丰度差别不大(见图6C)。在发酵第21天,片球菌属在含单宁样品中的丰度低于不含单宁样品中的丰度;相反,乳杆菌属在含单宁样品中的丰度高于不含单宁样品中的丰度;魏氏菌属在含单宁样品中的丰度低于不含单宁样品中的丰度(见图6D)。总之,单宁含量对乳杆菌属在整个发酵过程中丰度的影响较大,而对于魏氏菌属和片球菌属在整个发酵过程中丰度的影响则较小。
2.6 发酵时间和单宁含量与样品中细菌种群分布的关联性
2.6.1 VPA分析
方差划分标准对应分析(variance partitioning canonical correspondence analysis,VPA)[24]用于表示造成微生物群落分布差异的各环境因子的贡献度大小,本研究中导致样品细菌种群的差异的环境因子见图7。由图7可知,发酵时间和单宁含量对样品中细菌种群分布差异的贡献度分别为31.87%和22.39%;二者共同对细菌种群分布差异的贡献度为10.58%。
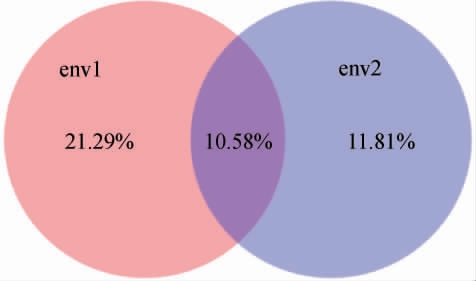
图7 环境因子对群落差异贡献率的方差划分标准对应分析
Fig.7 Variance partitioning canonical correspondence analysis of contribution rates of environmental factors to community differences
env1 为发酵时间,env2 为单宁含量。
2.6.2 Spearman相关性分析
Spearman相关性分析可以研究环境因子与物种之间的相关性[25]。本研究中环境因子发酵时间与样品中物种之间的相关性见图8和9,单宁含量与样品中物种之间的相关性见图8和10。
由图8和图9可知,有5个属与发酵时间显著相关(P<0.05),分别是片球菌属、蓝细菌纲的未知属、拟杆菌属、立克次氏体目的未知属、Roseovarius;其中片球菌属与发酵时间呈正相关,立克次氏体目的未知属与发酵时间呈极显著相关(P<0.05)。由图8和图10可知,有3个属与单宁含量呈显著负相关(P<0.05),分别是芽孢杆菌属、肠球菌属、类芽孢杆菌属,其中类芽孢杆菌属与单宁含量呈极显著负相关(P<0.01)。

图8 发酵时间和单宁含量与细菌属水平种群相关性分析
Fig.8 Analysis of correlation of fermentation time and tannin content and bacteria community at genus level
纵向为环境因子,横向为物种,中间热图对应值为相关系数r,r介于-1到1之间,r<0为负相关,r>0为正相关,*表示P<0.05。
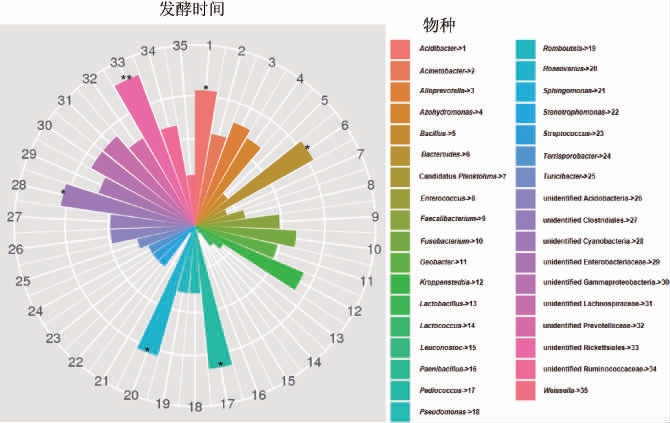
图9 发酵时间与细菌属水平种群相关性分析
Fig.9 Analysis of correlation of fermentation time and bacteria community at genus level
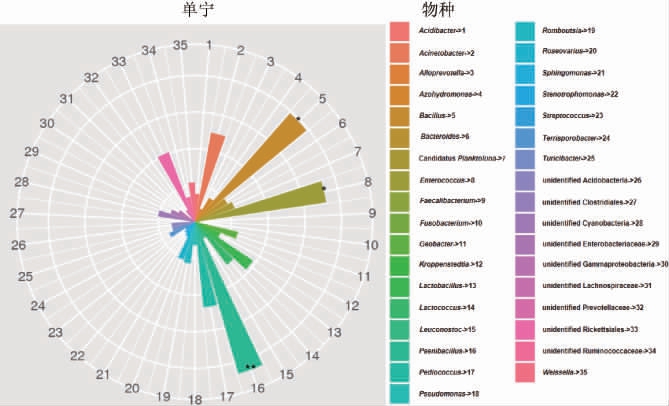
图10 单宁含量与细菌属水平种群相关性分析
Fig.10 Analysis of correlation of tannins content and bacteria community at genus level
郭旭凯等[26]利用纯培养方法研究了山西老陈醋酒化阶段高粱单宁对乳酸菌和醋酸菌生长的影响,结果发现,当高粱单宁含量为0~1.5%时,所有乳酸菌和醋酸菌的生长均被促进;当单宁含量为2.0%时,对不同菌的生长影响不同;而当单宁含量为3.0~6.0%时,所有乳酸菌和醋酸菌的生长均被抑制,且单宁浓度越高抑制作用越强;直到浓度为6.0%时菌株彻底不生长。对于清香型大曲白酒,高粱单宁含量在1.0%左右时,不会影响出酒率;但超过1.4%时,有可能会降低出酒率,但却可能提高白酒的品质[2]。综上可知,高粱中的单宁含量与细菌的种群有一定的关系,具体机理还需要深入研究。
3 结论
本实验利用高通量测序技术对清香型大曲白酒含单宁高粱和不含单宁高粱酒醅中的细菌种群进行了分析,研究了高粱单宁含量对细菌种群的影响。多样性分析结果显示,在发酵的第1天和第3天,不含单宁酒醅的细菌种群多样性高于含单宁酒醅的;但在发酵第7天和第21天的酒醅中却完全相反。两种酒醅中的细菌类群有:片球菌属(Pediococcus)、魏斯氏菌属(Weissella)、乳杆菌属(Lactobacillus)、芽孢杆菌属(Bacillus)、拟杆菌属(Bacteroides)、窄食单胞菌属(Stenotrophomonas)等。单宁含量对细菌种群差异的贡献率为22.39%,芽孢杆菌属(Bacillus)、肠球菌属(Enterococcus)、类芽孢杆菌属(Paenibacillus)与单宁含量呈显著负相关(P<0.05)。
单宁广泛存在于高粱中,而高粱是是清香型大曲白酒酿造的主要原料。因此,单宁含量的高低直接影响整个酿造过程中的细菌种群,从而进一步影响到发酵的走向,并最终影响白酒的品质。因此,本研究对选育具有合理含量单宁的高粱、促进清香型大曲白酒酿造工业的发展具有重要的指导意义。
[1]蒋兰.酿酒高粱淀粉含量测定及性质研究[D].重庆:重庆大学,2013.
[2]焦少杰,王黎明,姜艳喜,等.高粱与固态白酒关系的研究综述[J].酿酒,2015,42(1):13-16.
[3]郭旭凯,杨玲,张福耀,等.高粱子粒理化特性与清香型大曲白酒酿造关系的研究[J].中国酿造,2016,35(12):40-43.
[4]王恭堂.白兰地工艺学[M].北京:中国轻工业出版社,2002:57-63.
[5]康三江,张永茂,曾朝珍,等.苹果白兰地发酵工艺技术研究进展[J].中国酿造,2015,34(1):10-12.
[6]PUECH J L.Phenolic compounds in oak wood extracts used in the ageing of brandies[J].J Sci Food Agr,1998,42(2):165-172.
[7]MOSEDALE J R,PUECH J L.Wood maturation of distilled beverages[J].Food Sci Technol,1998,9(3):95-101.
[8] ORTEGA-HERAS M,GONZÁLEZ-HUERTA C,HERRERA P,et al.Changes in wine volatile compounds of varietal wines during age ing in wood barrels[J].Anal Chim Acta,2004,513(1):341-350.
[9]刘聪,王琪,杨玲,等.山西老陈醋酿造过程中真菌的分离、鉴定及高粱单宁对其生长的影响[J].食品科技,2019,44(2):19-26.
[10]刘娟.不同品种高粱淀粉、赖氨酸和单宁含量的比较[J].陕西农业科学,2019,65(3):5-9,16.
[11]唐玉明.高粱籽粒的酿酒品质研究[J].酿酒,2000,27(4):45-47.
[12]ZHOU J,BRUNS M A,TIEDJE J M.DNA recovery from soils of diverse composition[J].Appl Environ Microbiol,1996,62:316-322.
[13]田维平,陈学民,周鹏,等.蚯蚓粪净化硫化氢恶臭气体[J].环境工程,2018,12(11):169-176.
[14]LUNDBERG D S,YOURSTONE S,MIECZKOWSKI P,et al.Practical innovations for high-throughput amplicon sequencing[J].Nat Meth,2013,10(10):999-1002.
[15]庄林杰,夏超,田晴,等.高通量测序技术研究典型湖泊岸边陆向深层土壤中厌氧氨氧化细菌的群落结构[J].环境科学学报,2017,37(1):261-271.
[16] CHAO A.Estimating the population size for capture-recapture data with unequal catchability[J].Biometrics,1987,43:783-791.
[17]王青山.不同环境清香型白酒发酵微生物种群结构比较及溯源解析[D].无锡:江南大学,2018.
[18]ZHANG W X,QIAO Z W,SHIGEMATSU T,et al.Analysis of the bacterial community in Zaopei during production of Chinese Luzhou-flavor liquor[J].J Inst Brew,2005,111(2):215-222.
[19]WANG X,DU H,XU Y.Source tracking of prokaryotic communities in fermented grain of Chinese strong-flavor liquor[J].Int J Food Microbiol,2017,244:27-35.
[20]WANG H Y,ZHANG X J,ZHAO L P,et al.Analysis and comparison of the bacterial community in fermented grains during the fermentation for two different styles of Chinese liquor[J].J Ind Microbiol Biotechn,2008,35(6):603.
[21] WANG L,WANG Y Y,WANG D Q,et al.Dynamic changes in the bacterial community in Moutai liquor fermentation process characterized by deep sequencing[J].J I Brewing,2015,121(4):603-608.
[22] LI X R,MA E B,YAN L Z,et al.Bacterial and fungal diversity in the traditional Chinese liquor fermentation process[J].Int J Food Microbiol,2011,146(1):31-37.
[23]WANG P,WU Q,JIANG X,et al.Bacillus licheniformis affects the microbial community and metabolic profile in the spontaneous fermentation of Daqu starter for Chinese liquor making[J].Int J Food Microbiol,2017,250:59-67.
[24]李晓谦,朱京海,宋有涛.景观遗传学中Mantel 检验和dbRDA 统计方法的对比分析[J].辽宁大学学报,2015,42(4):289-295.
[25] SEGATA N,IZARD J,WALDRON L,et al.Metagenomic biomarker discovery and explanation[J].Genome Biol,2011,12(6):R60.
[26]郭旭凯,杨玲,刘聪,等.山西老陈醋酿造过程中乳酸菌和醋酸菌的分离、鉴定及高粱单宁对其生长的影响[J].中国酿造,2018,37(8):37-44.