啤酒是人们日常生活中的重要饮品,是以啤酒花和麦芽为原料,经糊化、糖化、液态发酵后酿制而成的酒精饮料[1-4]。啤酒酿制过程中会产生多种糖类、糖醇、醇类,它们是啤酒中重要的营养物质和风味物质,直接影响啤酒的口感、风味和品质。糖类化合物是一类多羟基醛或酮,是人体生命活动的能源物质,是许多食品和饮料的重要成分[5-7]。糖醇是糖类的醛基或者酮基被还原后的物质,通常是由对应的糖经过催化氢化而生成的甜味剂,具有预防糖尿病、热量低、口感好等优点[8-10]。醇类是某些发酵食品中的重要组分,某些醇类有益于人体健康,但是某些醇类如丁二醇,具有一定的毒性[11-12]。因此,啤酒中糖类、糖醇和醇类组分含量的测定具有重要的现实意义。
目前,糖类、糖醇、醇类的检测方法主要有液相色谱法[13]、液相色谱质谱联用法[14]、气相色谱法[15-16]、酶电极法[17]、离子迁移谱法[18]、离子色谱法[19]。液相色谱法通用方便,但灵敏度低,对复杂基质的样品测定困难;气相色谱法灵敏度高,但是需要衍生,定量重复性差,不适宜做准确定量分析;酶电极法一般仅对一种糖类进行测定,具有较好的特异性,但是不能进行多组分同时测定;液相色谱质谱联用法和离子迁移谱法成本较高,广泛普及应用的难度较大。离子色谱法,是一种简便、灵敏、准确、可同时分析多类别多组分的技术方法,在食品检测领域应用广泛。OWEN B等[20]采用脉冲安培检测-离子色谱法测定了甘露醇、山梨醇、葡萄糖三种物质;张水锋等[21]采用脉冲安培-离子色谱方法分析了婴幼儿乳粉中麦芽糖醇、半乳糖、葡萄糖、蔗糖、果糖、乳糖6种组分,但是研究组分数量较少。
本研究采用积分脉冲安培检测(integrated pulse amperometric detection,IPAD)-离子色谱(ion chromatography,IC)法,通过深入研究色谱分离的影响因素,优化色谱分析条件,建立了啤酒中23种糖类、糖醇、醇类同时测定的方法,该方法快速、灵敏、准确、选择性好,解决了当前啤酒中多类别多组分测定时人力物力成本高、检测效率低的技术难题,且无有毒有害试剂使用,具有良好的经济价值和环保效益。
1 材料与方法
1.1 材料与试剂
2,3-丁二醇、乙醇、甲醇、丙三醇、赤藓糖醇、岩藻糖、麦芽糖醇(纯度均>98%):上海安谱实验科技股份有限公司;木糖醇、阿拉伯糖醇、山梨醇、海藻糖、核糖醇、甘露醇、甘露糖、蜜二糖、葡萄糖、果糖、乳糖、核糖、蔗糖、棉子糖、麦芽糖(纯度均>98%):德国Dr.Ehrenstorfer GmbH公司;2-脱氧-D-葡萄糖(纯度>98%):加拿大Toronto Research Chemicals公司;氢氧化钠(色谱纯)Fisher Chemical公司;盐酸(色谱纯):美国Merck公司;超纯水(电阻率18.2 MΩ·cm)、IC-RP10柱(1 cc)和IC-H10柱(1 cc):美国Agela Technologies公司;所测样品为随机抽取的市售啤酒。
1.2 仪器与设备
ICS5000离子色谱仪(配备电化学检测器和自动进样器):美国Thermo Scientific公司;Milli-Q超纯水仪:美国Millipore公司;DL-360E智能超声波清洗器:上海之信仪器有限公司;ML802/02电子天平:瑞士梅特勒公司。
1.3 方法
1.3.1 离子色谱条件
Dionex CarboPacTM MA1色谱分离柱(4 mm×250 mm),Dionex CarboPacTM MA1保护柱(4 mm×50 mm);积分脉冲安培检测模式;工作电极:Gold(Au);参比电极:AgCl电极;电位波形:Gold,Carbo,Quad;流动相:NaOH淋洗液;流速:0.45 mL/min;柱温:29 ℃;进样量:10 μL。NaOH溶液淋洗液条件,0~75 min:480 mmol/L;75~80 min:480 mmol/L增至600 mmol/L;80~105min:600 mmol/L;105~110 min:600 mmol/L降至480 mmol/L;110~120 min:480 mmol/L。
1.3.2 前处理方法
移取啤酒样品约10 g,超声30 min(去除二氧化碳)。准确取超声后待检样品0.100 g,加入去离子水约150 mL,摇匀静置15 min,全部转移至200 mL容量瓶中,采用去离子水定容至刻度,摇匀、静置15 min,取10.0 mL溶液,先过已预活化的IC-H10柱(去除重金属离子),再过0.22 μm水相滤膜,最后过已预活化的IC-RP柱(去除有机物和其他杂质离子),弃去前3 mL,收集清液,待上机测定。
2 结果与分析
2.1 色谱条件优化
2.1.1 梯度淋洗液的选择
先后采用了NaOH溶液、NaAc溶液、NaOH溶液和NaAc溶液的梯度淋洗溶液这三种淋洗液,进行分析测定对比,发现采用单纯的NaOH溶液淋洗液测定23种糖类、糖醇、醇类的分离效果最好。而后进行了NaOH溶液的等度和梯度淋洗液浓度条件下分离实验,发现在梯度淋洗条件下,组分分离并不理想,随着淋洗溶液中氢氧化钠浓度的变化,基线出现不同程度的漂移,直接影响了定性定量分析;等度淋洗条件下,基线平衡较好,组分分离良好。因此,选取等度NaOH淋洗液进行组分分离实验(80 min后采用高浓度NaOH淋洗液冲洗色谱柱),23种组分混合标准溶液的离子色谱图见图1。由图1可知,23种组分检出的主要顺序依次是醇类、糖醇类、糖类,各组分分离良好。

图1 23种组分混合标准溶液的离子色谱图
Fig.1 Ion chromatogram of mixed standards solution of 23 kinds of components
1.2,3-丁二醇;2.乙醇;3.甲醇;4.丙三醇;5.赤藓糖醇;6.木糖醇;7.岩藻糖;8.阿拉伯糖醇;9.山梨醇;10.海藻糖;11.核糖醇;12.甘露醇;13.2-脱氧-D-葡萄糖;14.甘露糖;15.蜜二糖;16.葡萄糖;17.麦芽糖醇;18.果糖;19.乳糖;20.核糖;21.蔗糖;22.棉子糖;23.麦芽糖。
2.1.2 流速的选择
考察了0.40 mL/min、0.45 mL/min、0.50 mL/min流速条件下组分分离状况,结果表明,流速越大,压力越大,组分保留时间缩短,流速从0.40 mL/min增至0.50 mL/min,23种组分总保留时间由80 min降至62 min,而系统初始压力由8.1MPa增至10.0MPa。在0.40mL/min流速时,因为流速较低,压力较小,导致组分峰宽较大,总保留时间较长。0.50 mL/min流速时,系统压力较大,组分总保留时间缩短,但在75 min后使用600 mmol/L NaOH淋洗液冲洗色谱柱,系统压力由10.0 MPa升至12.7 MPa,接近色谱柱最高操作压力13.8 MPa,对色谱柱的使用寿命和系统的整体稳定性不利。0.45mL/min流速时,初始压力为9.0 MPa,最高压力为11.5 MPa,压力适中,而且分离度比较理想,23种组分在70 min内全部出峰。由此可见,增大流速可以提高色谱柱的压力和理论塔板数,从而缩短保留时间,但是不能改变分离度和组分的洗脱顺序,从减少分析时间、提高色谱柱寿命、维持系统稳定角度考虑,选择在0.45 mL/min流速条件下进行实验。
2.1.3 NaOH淋洗液浓度的选择
为了提高23种组分的分离度和灵敏度,进行了初始NaOH淋洗液浓度分别为450 mmol/L、470 mmol/L、480 mmol/L、490 mmol/L、500 mmol/L条件下的对比实验,结果见图2。由图2可知,随着淋洗浓度逐步增大,多数组分保留时间逐步减小,但是醇类和糖醇组分受淋洗液浓度的影响较小,如组分1~6、8、11和12。这是因为醇类和糖醇含有羟基,在水溶液中几乎呈中性,而糖类是多羟基(2个或以上)的醛类或酮类化合物,易发生水解,糖类的分子结构和物化特性决定了其在MA1离子色谱柱上的保留较糖醇和醇类更强,受氢氧化钠淋洗液浓度的变化影响更大。恰好能利用23种糖类、糖醇、醇类组分在不同浓度的氢氧化钠溶液淋洗条件下,在色谱柱上保留特性的差异,来优化改进组分间的整体分离度。

图2 不同NaOH淋洗液浓度下混合标准溶液的离子色谱图
Fig.2 Ion chromatogram of mixed standard solution at various NaOH eluate concentrations
淋洗浓度为450 mmol/L时,组分7和8、组分19和20的分离度不高,组分10和11几乎重叠;淋洗浓度为470 mmol/L时,组分10和11分离度不高;淋洗浓度分别为490 mmol/L、500 mmol/L时,组分14和15分离度明显下降,而组分18和19未完全实现分离;而淋洗浓度为480 mmol/L时,这23种组分的整体分离度和灵敏度最为理想。因此,从整体分离效果来看,选择淋洗浓度480 mmol/L进行实验测定。
2.1.4 柱温的选择
考察了26 ℃、28 ℃、29 ℃、30 ℃、32 ℃色谱柱温度条件下组分分离情况,结果见图3。
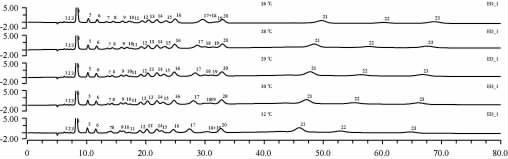
图3 不同柱温下混合标准溶液的离子色谱图
Fig.3 Ion chromatogram of mixed standard solution at different column temperature
由图3可知,随着柱温的升高,组分总保留时间缩短,其中组分7和8、组分9和10的之间分离度越来越小,而组分17和18分离度越来越大。从分析温度点看,26 ℃时,组分10和11、组分17和18这两对组分几乎重叠;28 ℃时,组分10和组分11之间的分离度不高;30 ℃时,组分18和19之间的分离度较小,不能满足定量分析的要求;32 ℃时,组分18和19完全重叠,组分7和8、组分9和10、组分14和15这三对组分分离度较小;29 ℃时,23种组分的分离度和灵敏度均比较理想。由此可见,温度对23种组分同时测定具有显著的影响,每一摄氏度的变化就会导致两种或几种组分不能有效分离。从提高方法的分离度、灵敏度、选择性角度考虑,选取在29 ℃柱温条件下进行实验分析。
2.2 线性范围与检出限
配制7个不同浓度水平的混合标准工作液,其中甲醇质量浓度范围在10.0~1 000 mg/L、乙醇质量浓度范围在2.0~200 mg/L,其他组分浓度范围在0.025~10.0 mg/L之间,以各待测物质质量浓度(X)为横坐标,峰面积(Y)为纵坐标,进行检测和校准曲线拟合,并计算待测组分的检出限(S/N=3),结果见表1。由表1可知,23种组分线性相关系数R2均>0.999,其中有18种组分相关系数R2>0.999 5,同时23种组分线性方程截距的绝对值均<0.008,这充分说明在此实验条件下,23种组分同时测定的方法稳定、线性良好。除了甲醇和乙醇外,其他21种组分检出限在0.011~0.197 mg/L之间。
表1 测定组分的线性范围、线性方程、相关系数及检出限
Table 1 Linear ranges,linear equations,correlation coefficient and limits of detection of determination components

2.3 回收率与精密度试验
抽取1种啤酒样品,依次向样品中添加质量浓度水平分别为0.20 mg/L、1.00 mg/L、2.00 mg/L的混合标准溶液,每个浓度水平进行6次平行实验,来验证方法的回收率和精密度,根据基质浓度、添加浓度和添加后测定浓度来计算回收率及相对标准偏差(relative standard deviation,RSD),结果见表2。由表2可知,23种糖类、糖醇、醇类组分在三个添加浓度水平下的回收率在81.27%~106.12%之间,精密度试验结果RSD在1.53%~10.52%范围内。回收率、精密度试验结果均符合食品理化检测要求[22],表明该检测方法精密度和准确性良好。
表2 回收率及精密度试验结果
Table 2 Results of recovery rates and precisions tests

2.4 实际样品的检测
依次抽取5种代表性啤酒(1-黄啤酒、2-黄啤酒、3-黄啤酒、4-黑啤酒、5-黑啤酒),按照离子色谱条件和前处理步骤,进行了实际样品中23种糖类、糖醇、醇类组分含量的检测分析,各样品离子色谱图见图4,检测结果见表3。

图4 5种啤酒样品中23种糖、糖醇及醇测定的离子色谱图
Fig.4 Ion chromatogram of 23 carbohydrates,sugar alcohols and alcohols in beer samples
表3 啤酒样品的23种糖、糖醇及醇测定结果
Table 3 Determination results of 23 carbohydrates,sugar alcohols and alcohols in beer samples

注:“ND”表示未检出。
由图4可知,测定基线稳定,组分分离效果好,受其他干扰较小,这说明此方法稳定性好、适用性强。由表3可知,五种啤酒中检出的糖类、糖醇、醇类组分总数量依次是13、16、14、17、15种,啤酒中检出有益组分的种类越多、含量越大,该啤酒的品质就越好,实验测定结果与样品实际品质状况完全相符。从检出组分来看,检出含量较大的组分依次是丙三醇、乙醇、乳糖、葡萄糖、海藻糖、山梨醇、甘露醇等。从啤酒种类来看,黑啤酒中糖类、糖醇比黄啤酒中的种类和含量更加丰富。
3 结论
本研究通过对流速、淋洗液浓度、色谱柱温度等实验影响因素的分析讨论,探索出了适于23种糖、糖醇及醇类同时检测的色谱分析条件,建立了积分脉冲安培-离子色谱法同时测定啤酒中23种糖、糖醇及醇类的分析方法。当流速为0.45 mL/min,淋洗浓度为480 mmol/L,柱温为29 ℃时,23种组分在各自的质量浓度范围内具有良好的线性关系(R2>0.999)。除了甲醇和乙醇外,其他21种组分检出限(LOD)在0.011~0.197 mg/L;在0.20 mg/L、1.00 mg/L、2.00 mg/L三个添加浓度水平下,23种组分的回收率为81.27%~106.12%,精密度试验结果相对标准偏差(RSD)为1.53%~10.52%。该方法简便、快速、灵敏、准确,完全适于啤酒酿制加工、质量控制和安全监管等过程中多种糖、糖醇及醇类的快速筛查分析。
[1]张海梦,张皓哲,崔云前.采用CDR BeerLab 分析仪检测啤酒理化指标的研究[J].中国酿造,2019,38(4):174-178.
[2]翟乃明,邓鸿钰,谭兆顺,等.利用废啤酒蒸馏回收酒精及风味物质的研究[J].中国酿造,2019,38(12):125-129.
[3]NARDINI M,GARAGUSO I.Characterization of bioactive compounds and antioxidant activity of fruit beers[J].Food Chem,2020,305(1):15-16.
[4]洪凯,马长伟.酒花与啤酒中单萜化合物的研究进展[J].食品科学,2019,40(7):328-330.
[5]KAZALAKI A,MISIAK M,SPYROS A,et al.Identification and quantitative determination of carbohydrate molecules in Greek honey by employing C-13 NMR spectroscopy[J].Anal Meth,2015,7(14):5962-5965.
[6]蒲小秋,白红进,马倩倩,等.HPLC-ELSD 法同时测定鲜枣果实中不同种类可溶性糖含量[J].食品科学,2017,38(14):170-174.
[7]曾杜文,牛亚平,徐丽丽,等.大豆渣提取L-阿拉伯糖及辅助玉米秸秆酶解液发酵产乙醇的研究[J].中国酿造,2019,38(3):70-75.
[8]余义,刘艳,周玉.LC-ESI-MS/MS 测定白酒中山梨糖醇的方法研究[J].酿酒科技,2019(2):117-120.
[9]王凤梅,张邦建,岳泰新,等.转木糖还原酶基因XYL1 酿酒酵母的构建及产木糖醇能力研究[J].中国酿造,2018,37(12):66-70.
[10]王超,李玉鑫,刘朦朦,等.木糖醇绿茶饼干的研制[J].食品研究与开发,2019,40(14):131-135.
[11]唐开永,周鸿翔,刘彩婷,等.米酒中6 种醇的气相色谱外标法测定研究[J].中国酿造,2019,38(4):183-187.
[12]李惠民,冯锁民,张博,等.气相色谱法测定桑葚酒中甲醇限度及乙醇含量[J].中国食品添加剂,2019,12(7):204-208.
[13]李开,曾鸣,宋昊,等.浓缩果汁中游离糖的组成分析[J].食品研究与开发,2019,40(16):129-134.
[14]赵孟欣,王泽岚,孟哲,等.温和条件下柱前标记-高效液相色谱-质谱法测定枸杞多糖中单糖组成[J].色谱,2019,37(11):1162-1172.
[15]杨珍,贺立东.反吹-气相色谱法快速检测啤酒中的主要风味物质[J].中国酿造,2019,38(10):171-174.
[16]张耀海,赵其阳,张雪莲,等.柱前衍生-气相色谱法同时测定不同柑橘汁中的糖和肌醇[J].食品科学,2012,33(10):173-178.
[17]王子辉,楚杰,王君高,等.酶电极法测定海藻糖含量[J].食品工业科技,2010,31(11):366-368.
[18]BROWNE C A,FORBES T P,SISCO E.Detection and identification of sugar alcohol sweeteners by ion mobility spectrometry[J].Anal Meth,2016,28(8):5611-5618.
[19]沈燕飞,朱仙娜,姚澄,等.阀切换离子色谱技术同时检测饮料中的糖类、甜味剂和防腐剂[J].食品科学,2018,39(16):311-313.
[20]OWEN B,JAMES F,JOHN S.Analytical protocol for the sensitive determination of mannitol,sorbitol and glucose containing powders in pharmaceutical workplaces by ion chromatography using a pulsed amperometric detector[J].J Pharmaceut Biomed Anal,2015,106(15):204-209.
[21]张水锋,盛华栋,姜侃,等.梯度洗脱优化-离子色谱-脉冲安培法分析婴幼儿配方乳粉中的糖和糖醇[J].色谱,2016,34(10):946-950.
[22]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 27404—2008 实验室质量控制规范食品理化检测[S].北京:中国标准出版社,2008.