青梅广泛分布于我国广东、浙江、江苏、广西、云南、福建等地。青梅果不仅营养丰富还具有独特的药用价值,有研究表明青梅有抗菌、抗病毒、抗肿瘤、代谢调节、抗骨质疏松、免疫增强等作用[1];除此之外青梅是天然的保健剂,用八九成熟的青梅发酵的酒能促进新陈代谢,延缓衰老,清除体内自由基,抗氧化能力强[2-3]。青梅酒是一种风靡中国、韩国和日本的饮料,因其营养价值高,风味淳朴,香气宜人,深受广大消费者的喜爱。大量研究表明,青梅酒品质在发酵过程和保存中都受到各种因素的影响,如酵母、品种、原料地、发酵条件、澄清方法,不同条件澄清方法以及酵母筛选的方法都比较局限性。国内近几年对青梅酒的研究偏重于产品工艺研发,不断提高其主要分析检测、药用价值和提取鉴定的工艺优化[4],国外注重于研究青梅酒工艺优化发酵条件以及发酵产品的风味成分[5]。目前已有关于产品工艺条件对青梅酒的品质和成分含量影响的报道,如张超等[6]利用菌株RC212、PRLWVER和DV10研究青梅酒酵母的筛选,严红光等[7]采用明胶、酪蛋白、硅藻土、皂土作为澄清剂研究对青梅酒澄清的影响,多数以复合澄清剂为主。本研究充分利用阳江市阳春地区的特色农产品青梅,酿造出口感独特的青梅果酒,为提升青梅果酒的品质和稳定性,在单因素试验基础上,采用响应面法对青梅酒进行澄清工艺优化的研究,探索最佳的澄清工艺参数,为青梅的工业化生产提供参考。
1 材料与方法
1.1 材料与试剂
青梅:阳江市阳春地区果园;青梅酒:本食品加工实验室发酵。
壳聚糖、柠檬酸:宏大生物科技有限公司;果胶酶、维生素C、纤维素酶:上海源叶生物科技有限公司;RC212酵母、焦亚硫酸钾:烟台帝伯仕自酿机有限公司。
1.2 仪器与设备
I3紫外可见分光光度计:济南海能仪器有限公司;FA224电子天平:上海舜宇恒平科技仪器有限公司DK-S24恒温水溶锅:上海精宏实验设备有限公司;TGL-18台式高速冷冻离心机:上海卢湘仪离心机仪器有限公司;KQ-250E超声清洗器:昆明市超声仪器有限公司;PHSJ-3F pH计:上海仪电科学仪器股份有限公司。
1.3 方法
1.3.1 青梅酒的加工工艺流程及操作要点

原料预处理:挑选无病虫害、无霉变、无落地果、果实饱满,果肉形体完整,肉质爽口,略带苦涩、七八分熟的青果,青梅果香味纯正,关于成熟的青梅会使果酒变浑浊,且影响果酒的芳香;将挑选好的鲜果用清水细心清果皮上的泥土、杂质,清洗时对青梅进行再次挑选,清洗好的青梅果要用凉白开漂洗2次[8]。
破碎打浆:人工卫生去核,迅速将青梅果肉投入含0.5%维生素C(抗氧化,防褐变)的凉白开水浸泡,按照青梅和水料液比1∶2(g∶mL)加凉白开水,再加入焦亚硫酸钾(防止氧化,抑制杂菌生长)混合打浆1 min左右得到青梅汁[9]。
酶解处理:添加0.12%的复合酶(果胶酶、纤维素酶比例为1∶1),在室温条件下协同处理青梅汁8 h,进行酶解[10]。
RC212酵母的活化[11]:酵母粉按照料液比1∶20(g∶mL)溶于2%糖水中,38 ℃恒温水浴活化30 min后,投入发酵使用。
成分调配:添加白砂糖对青梅汁的糖度和酸度进行调配,使其酸甜适中,使可溶性固形物含量达到18%,控制pH值为3.5条件下发酵,可抑制其他杂菌繁殖。
主发酵:将调配好的青梅汁以1 000 mL的三角瓶为发酵容器,装液量为70%,酵母菌的接种量为5%,将接好酵母的青梅汁于28 ℃恒温培养箱中进行主发酵,定时观察,以确保发酵正常进行。主发酵时间15 d。
后发酵:将过滤好的青梅果酒在20 ℃的恒温恒湿箱条件下,密闭容器中贮藏(陈酿)1个月。
澄清、过滤:在陈酿好的青梅酒中加入壳聚糖,澄清后再次过滤。
调配:利用白砂糖和碳酸钙进行青梅果酒的酸甜调配。
贮藏:将调配过滤好的青梅果酒罐装,密封,在60~70℃热水杀菌30 min,冷却取出,即得青梅果酒成品,在10 ℃低温贮藏[12]。
1.3.2 澄清工艺优化单因素试验[13-15]
以青梅酒透光率为评价指标,在壳聚糖添加量分别为0、4 g/L、8 g/L、12 g/L、16 g/L、20 g/L,pH值分别为3.0、3.5、4.0、4.5、5.0、5.5,澄清时间分别为1 d、2 d、3 d、4 d、5 d、6 d,在澄清温度为25 ℃条件下,考察壳聚糖添加量、pH值、澄清时间对青梅酒品质的影响。
1.3.3 澄清工艺优化响应面试验设计
根据单因素试验的结果,应用响应面法优化澄清工艺,以壳聚糖添加量(A)、澄清时间(B)、pH值(C)3个因素为自变量,以透光率(Y)为响应值,根据Box-Behnken试验设计原理,进行3因素3水平的优化设计,Box-Behnken试验设计因素与水平见表1。
表1 Box-Behnken试验设计因素与水平
Table 1 Factors and levels of Box-Behnken experiments design

1.3.4 数据处理与分析
试验做3次平行测定,结果以均值±标准误差的形式表示,数据采用Origin Pro 2019b绘图,响应面法采用Design Expert 10.0.3软件进行设计和统计分析,SPSS 21.0统计软件进行方差分析和显著性检验(P<0.05)。
2 结果与分析
2.1 青梅酒澄清工艺优化单因素试验
2.1.1 壳聚糖添加量对青梅酒澄清的影响
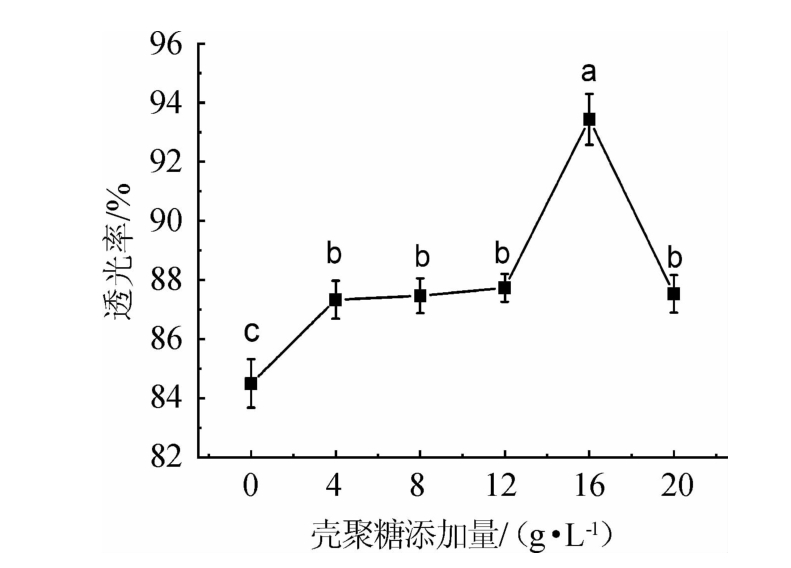
图1 壳聚糖添加量对青梅酒透光率的影响
Fig.1 Effect of chitosan addition on transmittance of plum wine
由图1可知,青梅酒的透光率随着壳聚糖添加量在4~16 g/L范围内的增加而增大,当壳聚糖添加量为16 g/L时,透光率达到最高值为93.4%,但当壳聚糖添加量>16 g/L之后,青梅酒透光率反而下降,这是由于壳聚糖是天然的阳离子性絮凝剂,而果酒中含有大量带负电荷的纤维素、果胶、单宁等微小颗粒,混合后依靠静电作用,果酒中的微小颗粒会缠绕于有线性分子结构的壳聚糖,使微小颗粒变成大颗粒逐渐沉降,从而使果酒澄清,若浓度过低形成颗粒物少,沉降速度则慢;若浓度过高,易使体系中黏度增大,果酒中悬浮的颗粒物难以沉降[16]。因此,壳聚糖的最佳添加量为16 g/L。
2.1.2 pH值对青梅酒澄清的影响

图2 pH值对青梅酒透光率的影响
Fig.2 Effect of pH on transmittance of plum wine
由图2可知,pH值在3.0~4.5范围时,其透光率随着pH增加而增大,在pH值4.5时透光率达到最大值91.3%,pH值再提高,该酒的透光率下降。因为壳聚糖分子氨基在酸性环境中带正电荷,与青梅酒中的负电荷物质产生中和作用[17],产生凝聚作用从而使青梅酒澄清,青梅酒中的pH值的高低还会影响壳聚糖分子中的游离氨基的数量,从而影响壳聚糖对青梅酒胶体物质的絮凝效果。因此,最佳pH值为4.5。
2.1.3 澄清时间对青梅酒澄清的影响

图3 澄清时间对青梅酒透光率的影响
Fig.3 Effect of clarification time on transmittance of plum wine
由图3可知,青梅酒透光率随着澄清时间在1~4 d范围内的延长逐渐增大,在澄清时间第4天透光率达到最高92.1%后,澄清时间超过4 d之后,透光率反而下降。这是由于壳聚糖与青梅酒中的负电荷物质相互作用产生絮凝沉淀物质需要一段时间[18-19],但放置时间过长,又会有部分絮凝物重新溶于溶液。因此,最佳澄清时间为4 d。
2.2 响应面试验优化设计与结果分析
2.2.1 响应面模型建立及显著性分析
在单因素试验基础上,以壳聚糖添加量、pH值、澄清时间3个因素进行响应面试验设计。以壳聚糖添加量(A)、澄清时间(B)及pH(C)为自变量,以透光率(Y)为响应值。响应面优化试验方案及结果见表2,模型方差分析见表3。
对试验数据进行回归拟合,得到自变量与透光率(Y)的二次多项回归方程,Y=96.18-2.11A+3.45B-4.39C+3.17AB+2.35AC-0.13BC-3.62A2-2.79B2-5.56C2
表2 Box-Behnken试验设计结果
Table 2 Design and results of Box-Behnken experiments

表3 回归模型方差分析
Table 3 Variance analysis of regression model
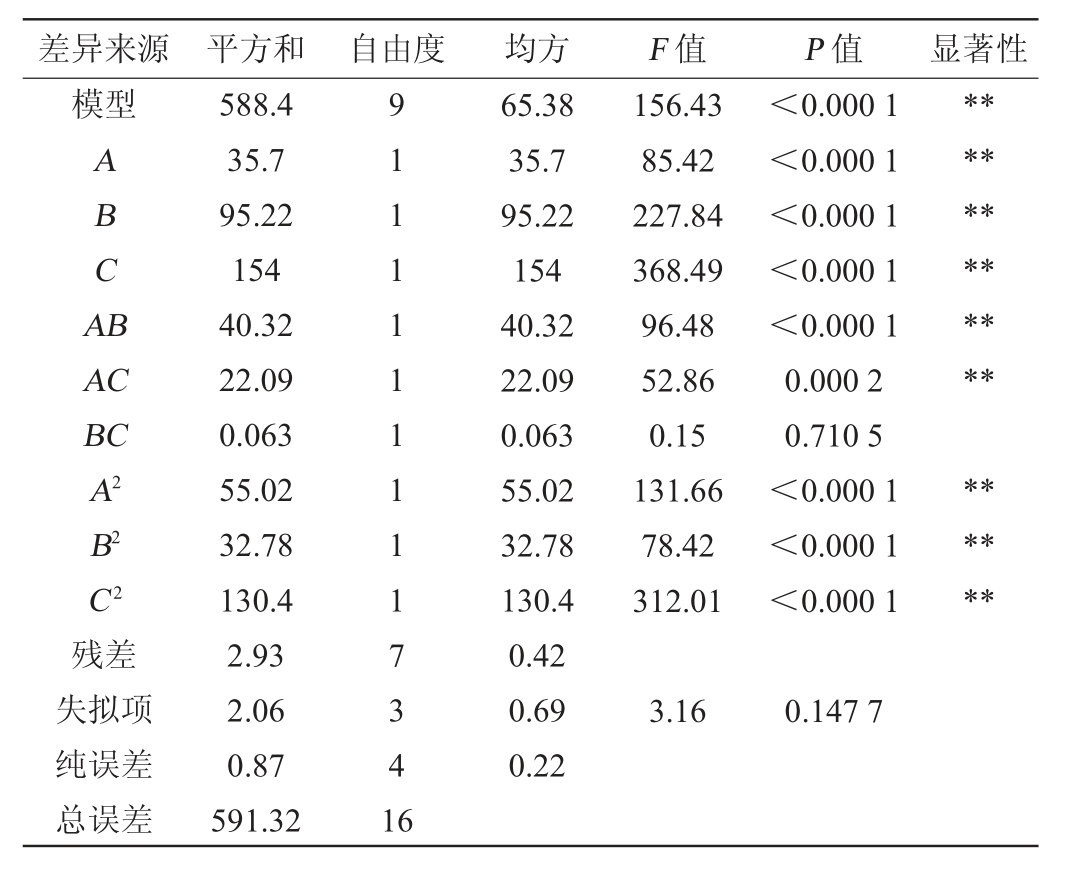
注:“**”表示对结果影响差异极显著(P<0.01);“*”表示对结果影响差异显著(P<0.05)。
由表3可知,模型的P<0.000 1,达到极显著,说明响应面法得到的模型可靠;失拟项P值为0.147 7>0.05,表明失拟项不显著,没有失拟现象;A、B、C、AB、AC、A2、B2、C2对结果影响达到极显著性水平(P<0.01),BC对结果影响不显著(P>0.05),由F值可知影响青梅酒壳聚糖不同条件澄清的因素大小顺序为C(pH)>B(澄清时间)>A(壳聚糖添加量),在因素交互作用的条件中,AB的交互作用对青梅酒澄清的效果最好,该模型的决定系数R2=0.995 1,模型调整决定系数R2Adj=0.988 7,说明该模型拟合程度高,预测值能较好反映实际值[20]。
2.2.2 各影响因素的交互作用分析
壳聚糖添加量(A)、澄清时间(B)、pH值(C)3各因素之间交互作用的响应面及等高线见图4。响应面越陡表示交互作用越强,等高线形状呈椭圆;响应面越平表示交互作用越弱,等高线形状越圆[21]。由图4a、图4b可以看出,响应面的曲面坡度陡峭,等高线呈椭圆形,说明AB、AC之间的交互作用对青梅酒透光率的影响极显著(P<0.01),由图4c可以看出,响应面的曲面坡度较平,等高线较圆,BC的交互作用对青梅酒透光率的影响不显著(P>0.05)[22]。

图4 壳聚糖添加量、澄清时间及pH值交互作用对青梅酒透光率影响的响应面及等高线
Fig.4 Response surface plots and contour lines of effects of interaction between chitosan addition,clarification time and pH on transmittance of plum wine
2.2.3 最优澄清工艺与验证
经Design-Expert10.0.3优化,采取软件优化得出在所选试验因素最优条件为壳聚糖添加量为15.505 0 g/L,澄清时间4.852 9 d,pH值为4.312 5,在此条件下青梅酒的透光率预测值为98.0%。考虑实际操作的可行性,修正最优澄清条件为壳聚糖添加量15.5 g/L,澄清时间5 d,pH值为4.3。在此优化条件下,进行3次平行验证试验,青梅酒透光率的均值为97.4%,与预测值接近,说明响应面优化法模型可靠[23]。
3 结论
通过单因素试验和响应面试验确定了发酵型青梅酒的澄清最佳工艺条件为壳聚糖添加量15.5 g/L、澄清时间5 d、pH值为4.3。在此优化条件下,透光率为97.4%。通过响应面试验进行澄清工艺优化,得到一种营养价值高、保健效果和口感俱佳的青梅酒,帝伯仕RC212酵母可作为青梅酒发酵工业化的一种参考发酵剂。
[1]赵维薇,申元英.青梅果药理学作用研究进展[J].安徽农业科学,2017,45(4):128-131.
[2]刘功德,苏艳兰,黄富宇,等.青梅的功能价值及加工研究进展[J].农业研究与应用,2018,31(4):1-8.
[3]林钥铭.青梅果酒发酵菌株筛选及工艺研究[D].合肥:安徽农业大学大学,2014.
[4]袁竹连.中国青梅酒研究文献的计量分析[J].食品与机械,2013,29(2):49-53.
[5]TIAN T T,YANG H,YANG F,et al.Optimization of fermentation conditions and comparison of flavor compounds for three fermented greengage wines[J].LWT-Food Sci Technol,2018,89:542-550.
[6]张超,谭平,王玉霞,等.青梅果酒酿造酵母菌筛选研究[J].酿酒科技,2015(4):22-27.
[7]严红光,姚平伟,郭红莉,等.不同澄清剂对青梅果酒澄清效果的影响[J].凯里学院学报,2016,34(6):60-63.
[8]赵文红,钱敏,白卫东,等.发酵青梅酒的研制[J].中国酿造,2009,28(1):169-171.
[9]钱敏,白卫东,沈棚,等.发酵型全果青梅酒的研制[J].中国酿造,2013,32(11):156-160.
[10]杨玉霞,康超,段振华,等.响应面法优化百香果酒发酵工艺研究[J].食品工业科技,2018,39(8):167-172.
[11]陈铭中,钟旭美,陈勇,等.青梅酒发酵工艺的优化[J].农产品加工,2019,485(8):27-29.
[12]王嘉祥,韩希凤.沂州木瓜酒酿造工艺技术研究[J].食品科学,2008,29(11):731.
[13]夏兵兵,张学锋,刘达玉,等.桔子果酒的澄清及稳定性研究[J].中国酿造,2009,28(1):118-121.
[14]曾湛慧,杨志娟,黄和,等.壳聚糖对火龙果汁澄清效果的影响[J].农产品加工,2015,380(3):21-24.
[15]章斌,罗志,凡芳华.活性炭负载壳聚糖对苹果汁的澄清效果研究[J].食品研究与开发,2013,34(17):15-19.
[16]韩希凤,金晓辉,郭志鹏,等.澄清方法对发酵型大枣果酒澄清效果的比较分析[J].食品工业,2018,39(4):141-144.
[17]黄武营.壳聚糖对枇杷汁的澄清效应[J].轻工科技,2016,212(7):1-2.
[18]艾克拜尔·艾海提,许艳顺,姜启兴,等.红枣汁澄清工艺研究[J].食品与机械,2013,29(1):209-212.
[19]吴兵.壳聚糖对樱桃汁澄清效果的影响[J].安徽农业科学,2010,38(27):14950-14954.
[20]谭红军,李红,杨勇,等.响应面法优化壳聚糖澄清药酒工艺及其效果评价[J].食品与发酵科技,2016,52(2):77-81.
[21]夏天奇,高新亚,刘小琳,等.红树莓果酒澄清工艺的优化及理化指标的测定[J].中国酿造,2018,37(8):138-142.
[22]苏龙,吕凤丹,王雪儒,等.响应面优化杨梅果酒发酵工艺及其抗氧化性[J].食品工业科技,2017,38(20):146-170.
[23]王芳,邓启,段伟丽,等.响应面法优化复合澄清剂对蓝莓果酒的澄清效果[J].中国食品学报,2016,16(8):149-158.