非酿酒酵母(non-Saccharomyces)通常存在于葡萄醪、发酵停滞或迟缓的葡萄酒,或者具有异常分析和感官特征的葡萄酒中,被认为是“野生”酵母或“腐败”酵母[1]。尽管经常被视作果酒微生物腐败变质的主要原因,但是目前已有较多研究表明,部分非酿酒酵母对果酒的发酵过程及品质控制具有积极作用[2]。酸度是影响果酒质量的重要因素[3-4],其种类和含量直接或间接影响果酒的口感和品质[5]。果酒中有机酸含量在合适的范围内时,可以有效地平衡果酒中的甜味和苦味[6],而有机酸过量时会使酒味酸涩,造成酒体粗糙等[3-4,7],苹果酸和柠檬酸是影响果酒口感的两种重要有机酸。有研究表明,利用非酿酒酵母酿造果酒,可以有效降低果酒中的有机酸含量,将其与酿酒酵母(Saccharomyces cerevisiae)混合发酵时可以改善果酒风味与口感[8-12]。李旋等[13-14]研究发现,粟酒裂殖酵母(Schizosaccharomyces pombe)能减少葡萄酒中苹果酸的含量;王立芳等[15]从葡萄园土壤中分离得到一株既能降解L-苹果酸又能降解柠檬酸的菌株,经鉴定为陆生伊萨酵母(Issatchenkia terricola),对其有机酸代谢能力进行研究发现,该菌株对L-苹果酸和柠檬酸的代谢能力受两种酸含量的影响。不同的酵母对有机酸的利用率不同[16],因此研究非酿酒酵母对有机酸的代谢特征以及选择合适的酵母菌株改善果酒中有机酸含量对指导果酒酿造具有积极意义。
碳源在发酵过程中主要有两种生理功能,一是构成细胞物质以及各种代谢产物的碳架,二是提供细胞活动所需要的能量[17]。在发酵过程中,碳源会经酵母分解代谢产生能量和一系列重要的中间代谢产物,供合成代谢所需。酵母菌的碳源来源非常广泛,包括醇类、有机酸和氨基酸等,目前研究较多的有糖类,包括已糖、二糖以及二碳化合物[18]。在酵母对果酒中碳源代谢方面,现有研究多是集中于酿酒酵母,对非酿酒酵母碳源代谢尤其是对有机酸类碳源的代谢研究比较少见。培养基中含有不同碳源时,对有机酸的代谢会产生不同的影响[17]。
本研究以酿酒酵母(Saccharomyces cerevisiae)RV002为对照,将发酵毕赤酵母(Pichia fermentans)JT-1-3和季也蒙毕赤酵母(Meyerozyma guilliermondii)JP-4-2分别接种于以L-苹果酸、柠檬酸、葡萄糖和乙醇为单一碳源或双碳源的培养基中培养,测定酵母生物量及碳源代谢动态变化,以期探讨非酿酒酵母对碳源尤其是有机酸类碳源的代谢规律,为非酿酒酵母改善果酒中有机酸含量提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
葡萄酒酿酒活性干酵母RV002(酿酒酵母):安琪酵母股份有限公司;发酵毕赤酵母(Pichia fermentans)JT-1-3、季也蒙毕赤酵母(Meyerozyma guilliermondii)JP-4-2(非酿酒酵母):由本实验室从柑橘皮、柠檬皮、橘树土和烂橘堆中筛选分离鉴定得到。
1.1.2 培养基
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD)培养基、无氨基酵母氮源(yeast nitrogen base without amino acids,YNB)培养基:北京酷来搏科技有限公司;马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基:青岛高科技工业园海博生物技术有限公司。
YNB-M培养基:苹果酸2 g/L,YNB 6.7 g/L;YNB-C培养基:10 g/L柠檬酸,YNB 6.7 g/L;YNB-G培养基:葡萄糖10 g/L,YNB 6.7 g/L;YNB-E培养基:乙醇5%,YNB 6.7 g/L。
YNB-M-G培养基:苹果酸2 g/L,葡萄糖10 g/L,YNB 6.7 g/L;YNB-C-G培养基:柠檬酸2 g/L,葡萄糖10 g/L,YNB 6.7g/L;YNB-M-E培养基:苹果酸2 g/L,乙醇5%,YNB6.7 g/L;YNB-C-E培养基:柠檬酸2 g/L,乙醇5%,YNB 6.7 g/L。
1.1.3 试剂
葡萄糖(分析纯)、L-苹果酸(分析纯)、柠檬酸(分析纯):上海阿拉丁生化科技股份有限公司;无水乙醇(分析纯):国药集团化学试剂有限公司。
1.2 仪器与设备
SPX-250B生化培养箱:天津市泰斯特仪器有限公司;TGL-16g离心机:飞鸽仪器有限公司;UV-1700紫外可见分光光度计:日本岛津公司;e2695高效液相色谱(highperformance liquid chromatography,HPLC)仪:美国WATERS公司。
1.3 实验方法
1.3.1 菌种活化
取3株酵母菌(JT-1-3、JP-4-2、RV002)冻存液(50%甘油保存)各1管于YPD培养基中,于28 ℃、120 r/min条件下培养24 h后,在PDA培养基上进行划线分离,并于28 ℃培养2 d。在PDA培养基上挑取菌落特征明显的菌株接种于YPD培养基中,于28 ℃、120 r/min条件下培养24 h制成种子液。
1.3.2 碳源代谢特征的研究
为探究2株非酿酒酵母对单碳源(L-苹果酸、柠檬酸、葡萄糖和乙醇)的消耗利用情况以及葡萄糖或乙醇的存在对非酿酒酵母消耗利用有机酸的影响,本实验以酿酒酵母为对照,将3株酵母菌的种子液分别接种于YNB-M、YNB-C、YNB-G、YNB-E、YNB-M-G、YNB-M-E、YNB-C-G 和YNBC-E培养基,接种量为3%(V/V),于28 ℃条件下发酵9 d,在发酵1 d、3 d、5 d、7 d、9 d时,取样,测定生物量、L-苹果酸、柠檬酸、葡萄糖和乙醇含量。
1.3.3 检测方法
生物量的测定:采用分光光度计在波长600 nm处测定各发酵时期发酵液的吸光度值,以OD600nm值表示酵母生物量[19]。葡萄糖含量的测定:采用3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)法[20]。乙醇含量的测定:采用重铬酸钾氧化法[21]。有机酸(L-苹果酸、柠檬酸)含量的测定:采用高效液相色谱(HPLC)法测定有机酸的含量[5]。
2 结果与分析
2.1 单碳源代谢特征的研究
由图1A可知,在以L-苹果酸为唯一碳源的YNB培养基中,3种酵母均能正常生长,对L-苹果酸的代谢能力为酵母JT-1-3>RV002>JP-4-2,且酵母JT-1-3所在培养基中的L-苹果酸含量显著降低(P<0.05),由1.91 g/L降至0.96 g/L。由图1B可知,在以柠檬酸为唯一碳源的YNB培养基中,非酿酒酵母JP-4-2和JT-1-3也能够较好地生长,而酿酒酵母RV002基本不生长;3种酵母对柠檬酸的代谢能力为酵母JP-4-2>JT-1-3>RV002,且酵母JP-4-2所在培养基中的柠檬酸含量显著降低(P<0.05),由9.86 g/L降至7.07 g/L。由图1C可知,在以葡萄糖为唯一碳源的YNB培养基中,3种酵母均能很好地生长,3种酵母对葡萄糖的代谢能力为酵母RV002>JP-4-2>JT-1-3。由图1D可知,在以乙醇为唯一碳源的YNB培养基中,3种酵母均可以生长,3种酵母对乙醇的代谢能力为酵母JT-1-3>JP-4-2>RV002。结果表明,酵母JT-1-3具有很强的代谢L-苹果酸的能力,酵母JP-4-2具有很强的代谢柠檬酸的能力,而酿酒酵母RV002不能利用柠檬酸。

图1 3种酵母在YNB-M(A)、YNB-C(B)、YNB-G(C)及YNB-E(D)培养基中的生物量及相应碳源含量的变化
Fig.1 Changes of biomass and corresponding carbon source contents of three yeasts in YNB-M (A),YNB-C (B),YNB-G (C) and YNB-E (D) media
实线表示生物量,虚线表示L-苹果酸、柠檬酸、葡萄糖及乙醇含量。
2.2 双碳源代谢特征的研究
2.2.1 葡萄糖存在下L-苹果酸的代谢特征
由图2可知,在以L-苹果酸和葡萄糖为双碳源的培养基中,3种酵母均能够较好地生长。其中,酿酒酵母RV002在第1天时生物量达到最大值,且消耗完培养基中的葡萄糖,L-苹果酸含量呈现先降低后回升的现象;非酿酒酵母JT-1-3所在培养基中L-苹果酸含量显著降低(P<0.05),由1.90 g/L降至1.58 g/L,且消耗葡萄糖的速度最慢,至发酵第9天时,培养基中仍有葡萄糖剩余;非酿酒酵母JP-4-2基本不消耗L-苹果酸(P>0.05)。结果表明,当培养基中同时含有葡萄糖和L-苹果酸两种碳源时,3种酵母都会优先消耗葡萄糖,非酿酒酵母JP-4-2基本不利用L-苹果酸,非酿酒酵母JT-1-3可以利用部分L-苹果酸,且相对于单碳源培养基,有机酸消耗量减少,这与高卫卫[16,22]的研究结果一致,即酵母会优先利用葡萄糖,且葡萄糖的存在阻碍了其他酵母对有机酸的利用。
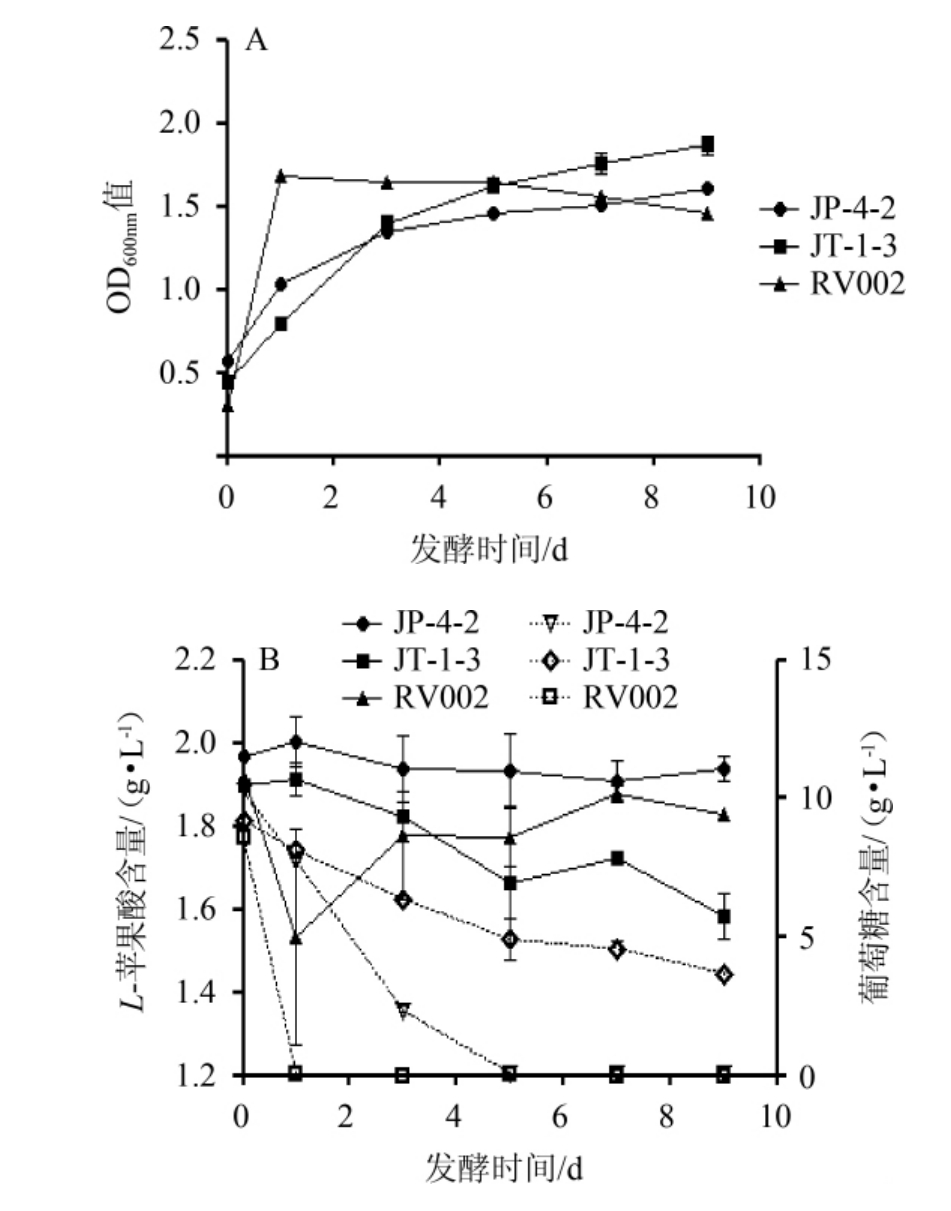
图2 3种酵母在YNB-M-G培养基中的生物量(A)、L-苹果酸及葡萄糖含量(B)的变化
Fig.2 Changes of biomass (A),L-malic acid and glucose content (B)of three yeasts in YNB-M-G medium
图B中实线为L-苹果酸,虚线为葡萄糖。
2.2.2 葡萄糖存在下柠檬酸的代谢特征
由图3可知,在以柠檬酸和葡萄糖为双碳源的培养基中,3种酵母均能很好地生长,且非酿酒酵母JP-4-2的生长优于非酿酒酵母JT-1-3;3种酵母所在培养基中柠檬酸的含量变化情况基本类似,均在第1天时含量显著性下降(P<0.05),随后变化幅度不大(P>0.05);葡萄糖消耗情况为酵母RV002>JP-4-2>JT-1-3。结果表明,当培养基中同时含有葡萄糖和柠檬酸两种碳源时,酿酒酵母会消耗葡萄糖,葡萄糖含量发生极显著性变化(P<0.01),但基本不利用柠檬酸。赵玉平等[23]对筛选出的毕赤酵母(Pichia pastoris)进行碳源代谢研究表明,其会先利用还原糖再利用柠檬酸,柠檬酸的利用会受到还原糖的阻碍,本实验结果与其研究结果一致,非酿酒酵母JP-4-2会利用葡萄糖以及部分的柠檬酸;非酿酒酵母JT-1-3利用大部分葡萄糖以及小部分柠檬酸,且与单碳源培养相比,两株非酿酒酵母对柠檬酸的利用率均显著降低(P<0.05)。
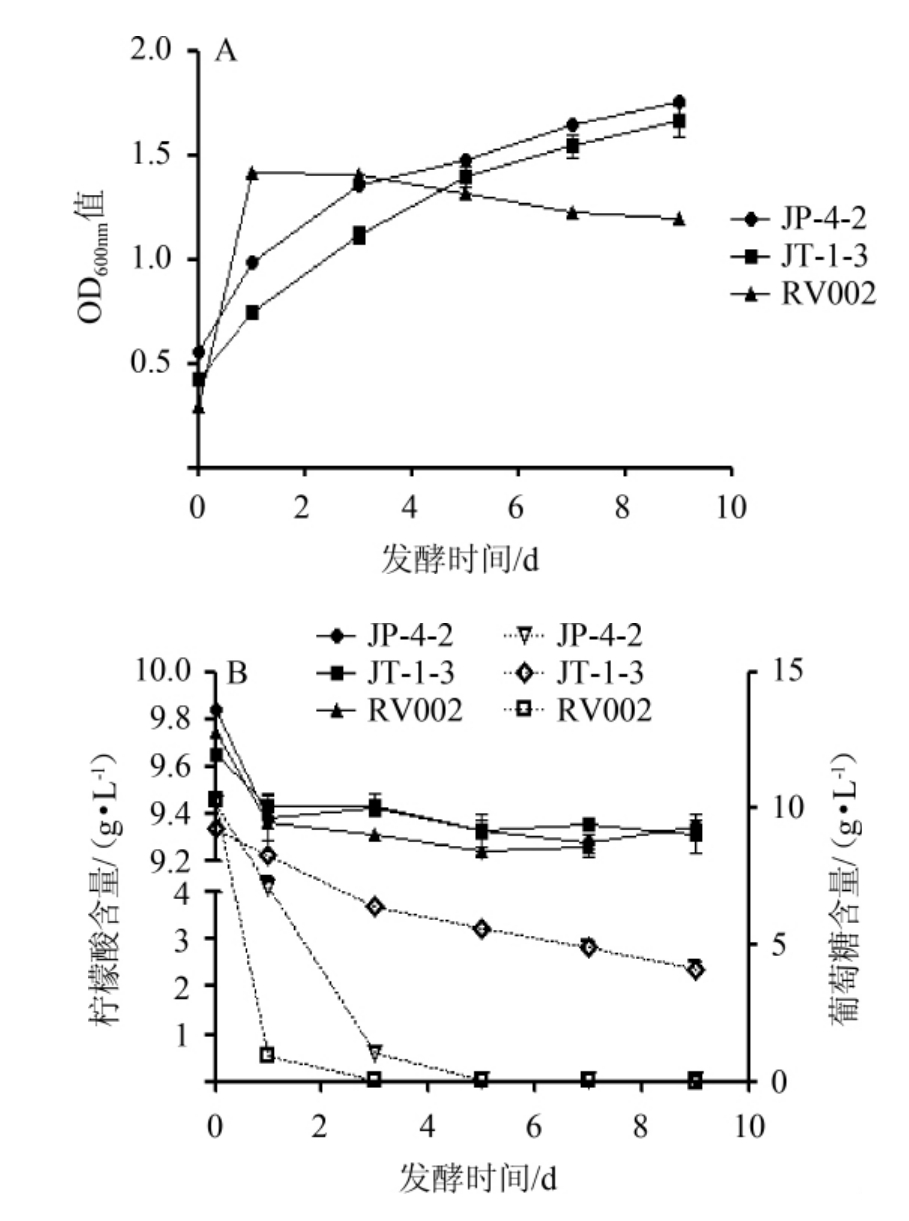
图3 3种酵母在YNB-C-G培养基中的生物量(A)、柠檬酸及葡萄糖含量(B)的变化
Fig.3 Changes of biomass (A),citric acid and glucose content (B) of three yeasts in YNB-C-G medium
图B中实线为柠檬酸,虚线为葡萄糖。
2.2.3 乙醇存在下L-苹果酸的代谢特征
由图4可知,在以乙醇和L-苹果酸为双碳源的培养基中,非酿酒酵母JT-1-3的生长情况最好,JP-4-2的生长情况次之,酿酒酵母RV002的生长情况最差;酿酒酵母RV002和非酿酒酵母JP-4-2所在培养基中L-苹果酸的含量无显著变化(P>0.05),而非酿酒酵母JT-1-3所在培养基中L-苹果酸的含量显著降低(P<0.05),由1.97 g/L降至0.81 g/L;3种酵母所在培养基中乙醇含量除在第1天时有所减少外(P<0.05),后续发酵过程中酿酒酵母RV002所在培养基中乙醇含量无显著变化(P>0.05),而非酿酒酵母JP-4-2和JT-1-3所在培养基中乙醇含量又有减少的趋势。结果表明,当培养基中同时含有乙醇和L-苹果酸两种碳源时,非酿酒酵母JT-1-3既可以利用L-苹果酸又可以利用部分乙醇,而非酿酒酵母JP-4-2与酿酒酵母RV002只能利用部分乙醇,基本不利用L-苹果酸。
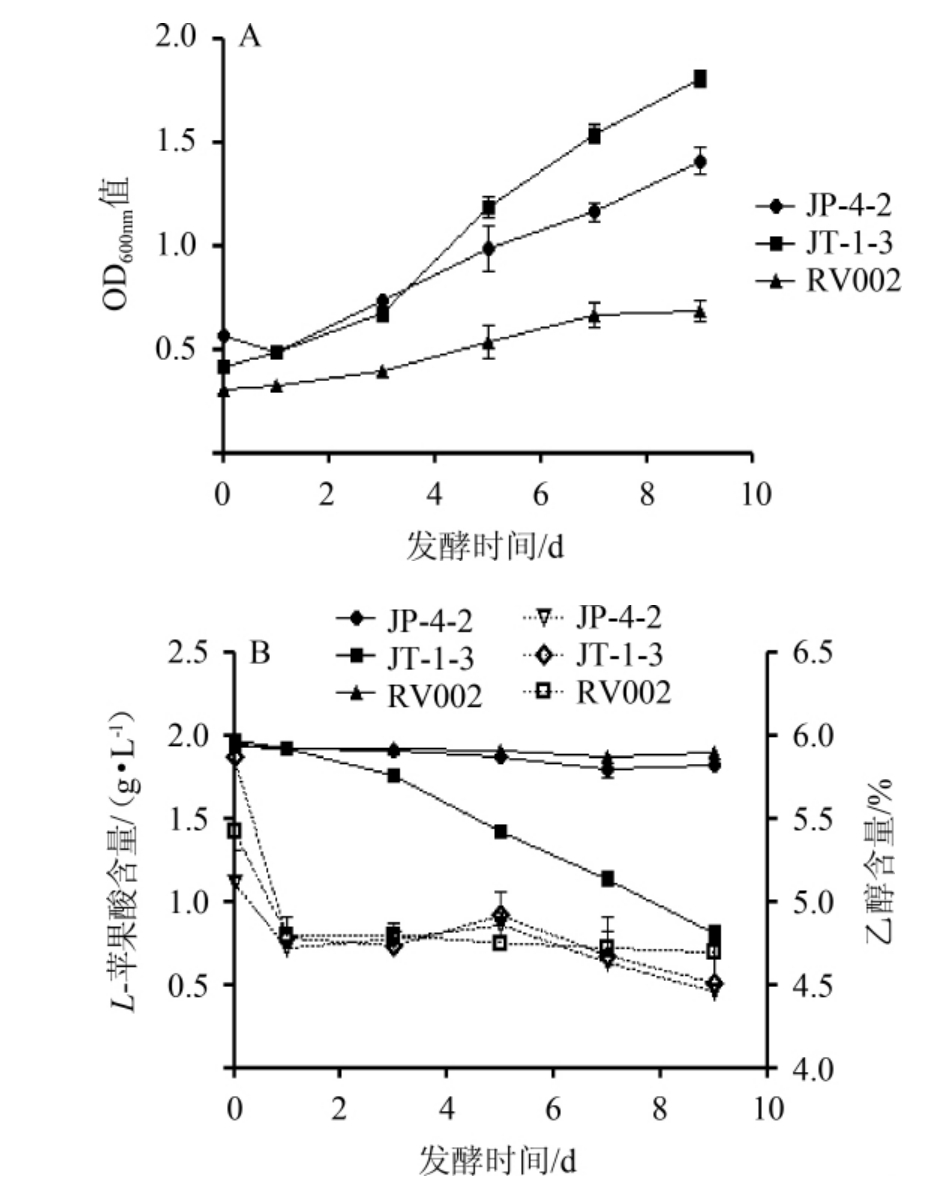
图4 3种酵母在YNB-M-E培养基中的生物量(A)、L-苹果酸及乙醇含量(B)的变化
Fig.4 Changes of biomass (A),L-malic acid and ethanol content (B)of three yeasts in YNB-M-E medium
图B中实线为L-苹果酸,虚线为乙醇。
2.2.4 乙醇存在下柠檬酸的代谢特征
由图5可知,在以乙醇和柠檬酸为双碳源的培养基中,非酿酒酵母JP-4-2可以生长,非酿酒酵母JT-1-3可以微弱地生长,而酿酒酵母RV002基本不生长,且3种酵母所在培养基中柠檬酸的含量无显著变化(P>0.05);非酿酒酵母JP-4-2所在培养基中乙醇含量降低幅度最大(P<0.01),由6.35%降至5.16%,非酿酒酵母JT-1-3所在培养基中乙醇含量小幅度降低(P<0.05),由6.50%降至5.64%,而酿酒酵母RV002所在培养基中乙醇含量无显著变化(P>0.05)。结果表明,当培养基中同时含有乙醇和柠檬酸两种碳源时,3种酵母基本不消耗柠檬酸,非酿酒酵母JP-4-2可以利用部分乙醇,非酿酒酵母JT-1-3只能利用极少量乙醇,而酿酒酵母RV002基本上不利用乙醇。

图5 3种酵母在YNB-C-G培养基中的生物量(A)、柠檬酸及乙醇含量(B)的变化
Fig.5 Changes of biomass (A),citric acid and ethanol content (B) of three yeasts in YNB-C-G medium
图B中实线为柠檬酸,虚线为乙醇。
3 结论
不同酵母对不同碳源的代谢能力有所差异,酿酒酵母RV002代谢葡萄糖的能力较强,代谢率达99.80%,基本不代谢柠檬酸;P.fermentans JT-1-3代谢L-苹果酸的能力较强,代谢率达49.74%,代谢葡萄糖能力较弱;M.guilliermondii JP-4-2代谢柠檬酸的能力较强,代谢率达28.30%,且代谢葡萄糖的能力优于P.fermentans。此外,培养基中的碳源成分葡萄糖和乙醇会影响酵母对有机酸类碳源代谢的能力,与以有机酸为唯一碳源的培养基相比,当培养基中同时含有葡萄糖或乙醇以及有机酸(L-苹果酸或柠檬酸)时,除P.fermentans JT-1-3在L-苹果酸与乙醇共存的培养基中L-苹果酸消耗量略有增加外,其余情况下,2株非酿酒酵母对有机酸的利用率会降低。
[1]CIANI M,COMITINI F,MANNAZZU I,et al.Controlled mixed culture fermentation:a new perspective on the use of non-Saccaromyces yeasts in winemaking[J].FEMS Yeast Res,2010,10:123-133.
[2]JOLLY N P,AUGUSTYN O P H,PRETORIUS I S.The role and use of non-Saccharomyces yeasts in wine production[J].S Afr J Enol Viticult,2006,27(10):15-39.
[3]郝爱玲,冯莉,秦义,等.降解柠檬酸酵母菌的筛选及其发酵性能研究[J].中国食品学报,2018,18(11):72-80.
[4]SU J,WANG T,WANG Y,et al.The use of lactic acid-producing,malic acid-producing,or malic acid-degrading yeast strains for acidity adjustment in the wine industry[J].Appl Microbiol Biot,2014,98(6):2395-2413.
[5]赵鹤然.葡萄酒酿造过程中的苹果酸和乳酸的变化[D].大连:大连工业大学,2016.
[6]杨春霞,苟春林,单巧玲.葡萄酒酿造过程中有机酸变化规律研究[J].中国酿造,2017,36(4):83-86.
[7]MEDINA-PLAZA C,GARCIA-CABEZON C,GARCIA-HERNONDEZ C,et al.Analysis of organic acids and phenols of interest in the wine industry using Langmuir-Blodgett films based on functionalized nanoparticles[J].Anal Chim Acta,2015,853:572-578.
[8]崔艳,刘金福.非酿酒酵母在葡萄酒酿造中应用的研究现状[J].中国酿造,2010,29(11):13-16.
[9]IRIS L,ANTONIO M,PIERGIORGIO C,et al.Use of Schizosaccharomyces pombe and Torulaspora delbrueckii strains in mixed and sequential fermentations to improve red wine sensory quality[J].Food Res Int,2015,76:325-333.
[10]PEDOR M,IZQUIERDO C,ESTEBAN G,et al.Influence of sequential inoculation of Wickerhamomyces anomalus and Saccharomyces cerevisiae in the quality of redwines[J].Eur Food Res Technol,2014,239(2):279-286.
[11]LIU S X,LAAKSONEN O,YANG B.Volatile composition of bilberry wines fermented with non-Saccharomyces and Saccharomyces yeasts in pure,sequential and simultaneous inoculations[J].Food Microbiol,2019,80:25-39.
[12]RENAULT P,COULON J,DE REVEL G,et al.Increase of fruity aroma during mixed T.delbrueckii/S.cerevisiae wine fermentation is linked to specific esters enhancement[J].Int J Food Microbiol,2015,207:40-48.
[13]李旋,亓桂梅,王超萍.非酿酒酵母在葡萄酒生产中的作用及研究进展[J].中外葡萄与葡萄酒,2019(1):52-56.
[14]ROCA-DOMENECH G,CORDERO-OTERO R,ROZES N,et al.Metabolism of Schizosaccharomyces pombe under reduced osmotic stress conditions afforded by fed-batch alcoholic fermentation of white grape must[J].Food Res Int,2018,113:401-406.
[15]王立芳,张微,文连奎.可降解L-苹果酸和柠檬酸菌株的筛选及鉴定[J].食品科学,2010,31(21):279-282.
[16]高卫卫.产朊假丝酵母利用有机酸及其发酵苹果渣生产菌体蛋白的研究[D].泰安:山东农业大学,2009.
[17]杨文洲,薛永常,窦少华,等.不同碳源对酵母代谢有机酸的影响[J].中国酿造,2007,26(10):20-22,61.
[18]ROSA C,PÉTER G.Biodiversity and Ecophysiology of Yeasts[M].New York:Springer,2006:101-122.
[19]潘婷.模拟汁中可同化氮和还原糖对酵母酒精发酵和香气成分的影响[D].咸阳:西北农林科技大学,2015.
[20]王靖,李智敏,谢纯良,等.毕赤酵母发酵不同单糖产乙醇的研究[J].湖北农业科学,2016,55(3):716-719.
[21]王晓昌.宁夏贺兰山东麓非酿酒酵母的分离鉴定与发酵特性研究[D].银川:宁夏大学,2016.
[22]BERTHELS N J,OTREO R R C,BAUER F F,et al.Discrepancy in glucose and fructose utilisation during fermentation by Saccharmyces cerevisiae wine yeast strains[J].FEMS Yeast Res,2004,4(7):683-689.
[23]赵玉平,杜连祥,刘丽丽,等.降解山楂汁中柠檬酸酵母菌的筛选及其降酸特性研究[J].微生物学报,2004,44(2):235-239.