γ-氨基丁酸(γ-aminiobutyric acid,GABA)是一种天然非蛋白质组成成分的氨基酸,广泛存在于动物、植物和微生物中[1]。GABA具有降低血压、治疗癫痫、改善脑细胞、增强记忆和促进睡眠等多种生理功能[2-4],它不仅在哺乳动物中枢神经系统中充当重要的抑制性神经递质,还参与多种生命代谢活动,对生物体正常的生命活动起着重要的调节作用,在非神经的组织中发挥激素或营养因子的作用[5-6]。在微生物体内,GABA的合成原理是以L-谷氨酸(L-glutamic,L-Glu)为底物,谷氨酸脱羧酶(glutamate decarboxylase,GAD)为催化酶制剂将L-Glu或L-谷氨酸单钠盐(L-glutamic acid monosodium salt,L-MSG)脱羧获得[7-8]。2009年,由生物法制备的GABA被批准为“新资源食品”,目前GABA作为一种新型的功能性因子,在食品及医药领域都具有良好的应用前景[9-10]。
为了更方便、快捷的检测GABA含量,建立适应复杂转化液中定量分析GABA的方法是微生物法制备GABA的前提条件。由于GABA本身对紫外光吸收小,一般需要衍生化后才能使用紫外检测器检测[11]。目前常用的衍生试剂有苯二醛-2-巯基乙醇、丹磺酰氯以及邻苯二甲醛(O-phthalaldehyde,OPA)等[12-15],其中OPA是最为常用的一般实验选用的衍生试剂,具有衍生时间短、价格便宜、简单易操作等优点。目前GABA定量分析方法主要有高效液相色谱(high performance liquid chromatography,HPLC)法、电泳法和纸层析法等[16-19],其中高效液相色谱法应用最为广泛。然而,由于GABA需要衍生化后才能检测,加上出峰时间较长,目前面对大批量样品时仍无法快速检测。超高效液相色谱(ultra performance liquid chromatography,UPLC)与传统的HPLC相比,UPLC的速度、灵敏度及分离度均优于HPLC。目前,UPLC多应用于代谢组学分析及其他一些生化领域,在天然产物的分析方面运用也逐渐兴起,因为在这些领域深入研究需要更高的分析精度。目前,利用UPLC法与HPLC法测定微生物制备液中GABA含量的研究鲜有报道,本试验采用邻苯二甲醛(OPA)柱前衍生-紫外检测UPLC法与HPLC法进行方法学验证和对比研究,旨在寻求一种快速准确测定乳酸菌发酵液中GABA含量的方法,以期为大通量筛选产GABA的乳酸菌提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
乳酸菌:本研究室保存的乳酸菌菌种。
1.1.2 化学试剂
γ-氨基丁酸标品(纯度>99.9%):上海源叶生物科技有限公司;谷氨酸钠(纯度>98.0%):生工生物工程股份有限公司;甲醇(色谱纯):国药集团化学试剂有限公司;正丁醇、茚三酮、丁二酸钠、硼酸、无水乙酸钠(均为分析纯):广州化学试剂厂;冰醋酸(分析纯):上海陆都化学试剂厂;β-巯基乙醇、邻苯二甲醛:酷尔化学科技有限公司。
1.1.3 培养基
MRS培养基(固体培养基中加2%琼脂):蛋白胨1%、牛肉膏1%、酵母提取物0.5%、柠檬酸胺0.2%、葡萄糖2.0%、吐温-80 0.1%、乙酸钠0.5%、磷酸氢二钾0.2%、硫酸镁0.058%、硫酸锰0.025%、调pH值为6.2~6.6。121 ℃条件下灭菌20 min,用于菌种的培养。
TYG液体培养基:胰蛋白胨0.5%、酵母提取物0.5%、葡萄糖1.0%、丁二酸钠0.5%,调pH值为6.5。121 ℃条件下灭菌20 min,用于发酵培养。
1.2 仪器与设备
岛津LC-2030高效液相色谱仪、UV-1800紫外可见分光光度计:日本岛津仪器有限公司;ACQUITY UPLC I-Class超高效液相色谱:美国Waters公司;Millipore纯水仪:默克密理博(中国)有限公司;5417R离心机:德国Eppendorf公司。
1.3 方法
1.3.1 样品制备
种子培养液制备:从MRS平板上挑取适量经纯化后的乳酸菌菌株,接种到种子培养基(MRS液体培养基中)中,37 ℃条件下静置培养16 h。
发酵培养液制备:按体积分数3%的接种量取上述种子培养液接入到添加了1%谷氨酸的TYG液体培养基中,37 ℃条件下静置培养24 h,备用。
1.3.2 HPLC操作条件
参考李鹏等[20]的测量方法。衍生处理:取200 μL乳酸菌发酵液或GABA标准品溶液于5 mL的EP管中,加入600 μL的OPA衍生剂,混匀,然后再加入800 μL磷酸二氢钾缓冲液,避光反应1 min,经0.22 μm过滤膜过滤后立刻进样,整个衍生过程控制在3 min内。
HPLC条件:Luna-C18色谱柱(250 mm×4.6 mm,5 μm);流速0.8 mL/min;柱温27 ℃;进样量10 μL;检测波长333 nm;流动相为醋酸-醋酸钠缓冲液∶甲醇=55∶45,V/V。
1.3.3 UPLC操作条件
衍生处理同1.3.2。
UPLC条件:Acquity UPLC Waters BEH C18色谱柱(2.1 mm×50 mm,1.7 μm);流速0.8 mL/min;柱温27 ℃;进样量10 μL;检测波长333 nm;流动相为醋酸-醋酸钠缓冲液∶甲醇=55∶45,V/V。
2 结果与分析
2.1 检测波长的选择
分别吸取400 μg/mL和1 000 μg/mL的γ-氨基丁酸标准准溶液各200 μL,分别按1.3.3中的衍生处理对GABA标准溶液进行衍生,取衍生后的反应液进行全波长扫描(200~800 nm),扫描结果见图1。
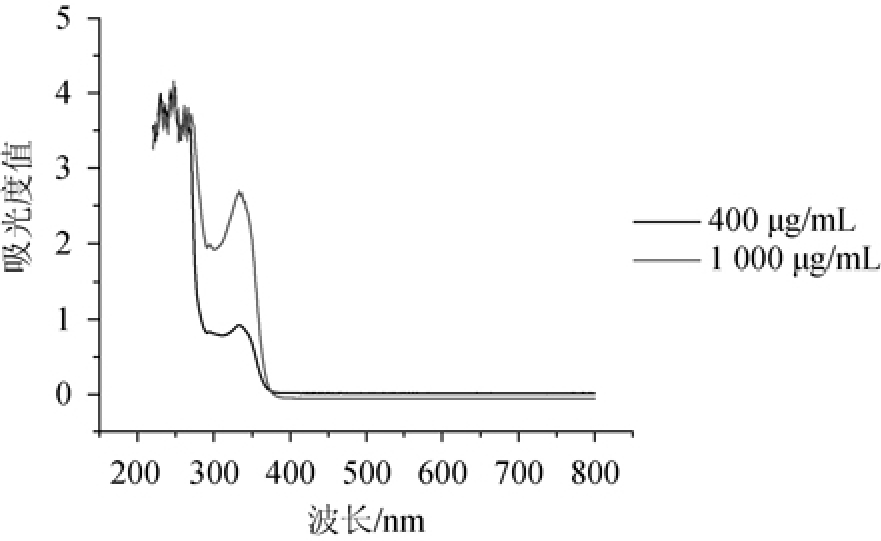
图1 γ-氨基丁酸标准品全波长扫描结果
Fig.1 Full-wavelength scanning results of γ-aminobutyric acid standard
由图1可知,220~278 nm干扰峰过多,峰值接近,无法明确区分,且不随γ-氨基丁酸标准溶液浓度的变化而改变,主要是由于样品中衍生剂的影响而导致的。γ-氨基丁酸标准溶液的最大吸收峰在波长310~370 nm处,且吸收峰区分明显,周围无干扰,最大吸收波长为333 nm。因此,进行UPLC和HPLC分析时以333 nm作为检测波长。
2.2 GABA标准品的HPLC法和UPLC法测定
GABA标准品HPLC法和UPLC法分析结果见图2。由图2A可知,在1.3.3色谱条件下,标准液在高柱效Acquity UPLC Waters BEH C18色谱柱上得到了良好的洗脱和分离,GABA在柱上的保留时间是0.837 min。由图2B可知,在1.3.2色谱条件下,标准液在Luna-C18色谱柱上得到了良好的洗脱和分离,GABA在柱上的保留时间是23.034 min。与HPLC法比,UPLC法的出峰时间明显缩短,检测效率有了显著的提高,并且其他杂质对测定没有干扰,HPLC法和UPLC法都能很好的对GABA进行分离。
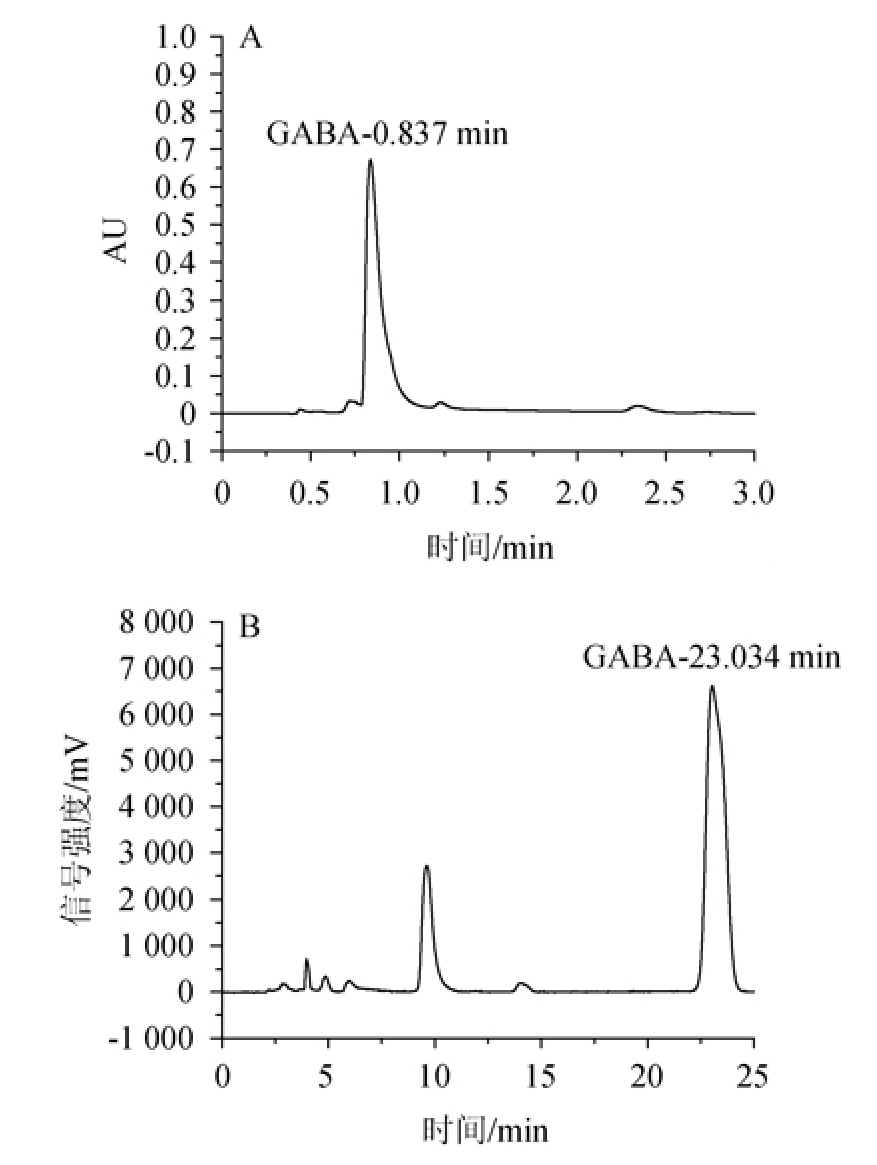
图2 γ-氨基丁酸标准品分析UPLC(A)和HPLC(B)色谱图
Fig.2 Chromatogram of γ-aminobutyric standard by UPLC (A) and HPLC (B)
2.3 反应时间对衍生反应的影响
吸取200 μL γ-氨基丁酸标准准溶液,按1.3.2方法进行衍生,再分别放置0、1 min、2 min、3 min、4 min、5 min、6 min后采用UPLC法检测,考察不同放置时间对GABA峰面积的影响,并作色谱图和峰面积的变化曲线,结果见图3。由图3可知,γ-氨基丁酸标准溶液经过柱前衍生反应后,其响应值(峰面积)会随着放置时间的增加而明显减小。6 min内峰面积从8 900 216下降至4 561 646,可见γ-氨基丁酸衍生物极其不稳定,其衍生产物会随着衍生时间的延长而逐渐分解,因此衍生时间对试验结果有显著地影响,应该严格控制衍生时间相同,以确保得到最大响应值的同时降低误差,保证试验具有好的准确性和重现性,本试验将整个衍生反应过程控制在3 min。
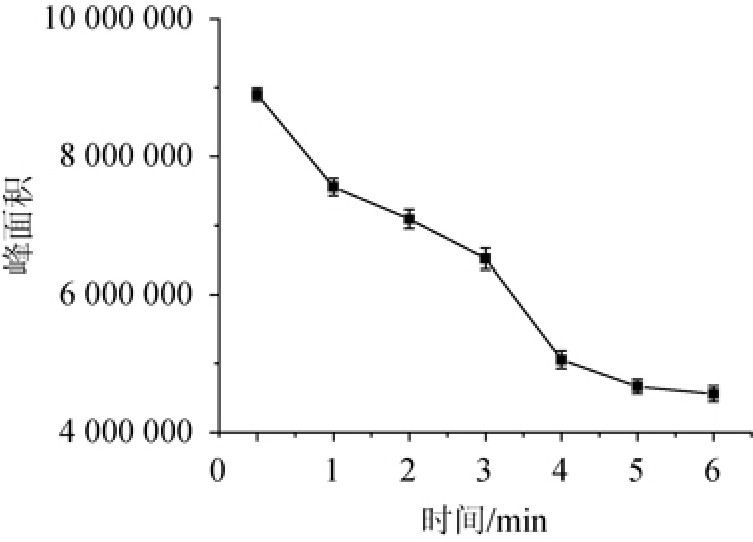
图3 衍生时间对γ-氨基丁酸峰面积的影响
Fig.3 Effect of derivation time on γ-aminobutyric peak area
2.4 γ-氨基丁酸标准曲线
将配制1000.0μg/mL的GABA标准品溶液稀释成质量浓度为100.0 μg/mL、200.0 μg/mL、400.0 μg/mL、600.0 μg/mL、800.0 μg/mL的标准工作液,衍生后进样。以峰面积(y)为纵坐标,标准液质量浓度(x)为横坐标绘制标准曲线,得到标准曲线回归方程及相关系数见表1。由表1可知,HPLC法和UPLC法在GABA质量浓度为100.0~1 000.0 mg/mL范围内线性关系良好(相关系数R2均>0.998)。
表1 γ-氨基丁酸标准曲线回归方程
Table 1 Regression equation of standard curve of γ-aminobutyric acid

2.5 精密度试验
配制质量浓度为800 μg/mL的γ-氨基丁酸标准溶液,采用UPLC和HPLC两种方法对γ-氨基丁酸标准品和香蕉上初筛到的乳酸菌发酵液进行定量检测,每个样品在不同时间段各重复测量5次,并根据γ-氨基丁酸标准曲线计算样品中的GABA含量,结果见表2。由表2可知,HPLC法的平均相对标准偏差(relative standard deviation,RSD)为1.175%,UPLC法RSD为0.529%,2种检测方法的日内精密度与日间精密度的RSD均<1.5%,表明这2种方法均具有良好的精密度,并且UPLC法测量的结果更为精确。
表2 γ-氨基丁酸检测精密度试验结果
Table 2 Results of precision tests of γ-aminobutyric acid determination

分别吸取不同编号乳酸菌发酵液各100 μL,再分别加入400.0 μg/mL的γ-氨基丁酸标准液100 μL。按1.3.3方法进行衍生,再采用UPLC法和HPLC法两种方法测量GABA含量,计算回收率,结果见表3。
表3 γ-氨基丁酸检测加标回收率试验结果
Table 3 Results of standard recovery rate tests of γ-aminobutyric determination

由表3可知,UPLC法和HPLC法的平均回收率在98.28%~99.36%,超高效液相色谱法的RSD(0.680%)低于高效液相色谱的RSD(1.053%),说明UPLC法测量GABA时准确度更高。
2.6 乳酸菌发酵液中γ-氨基丁酸含量测定结果
取离心后的不同乳酸菌发酵液各200 μL,经OPA柱前衍生后,采用UPLC法分别测定各发酵液样品,每个发酵液测定5次,得到γ-氨基丁酸的峰面积。根据标准工作曲线的回归方程计算,得到样品中γ-氨基丁酸的含量,结果见表4。
表4 乳酸菌发酵液中γ-氨基丁酸含量测定结果
Table 4 Determination results of γ-aminobutyric acid contents in lactic acid bacteria fermentation broth

由表4可知,通过UPLC法对5株产GABA的乳酸菌发酵液进行定量分析,最后筛出产γ-氨基丁酸最高的菌株编号为CT4-1,其γ-氨基丁酸的产量为928.095 μg/mL。
3 结论
本实验对超高效液相色谱(UPLC)与高效液相色谱(HPLC)两种方法进行对比研究,采用邻苯二甲醛(OPA)柱前衍生-紫外测定乳酸菌发酵液中的γ-氨基丁酸(GABA)含量。试验结果表明,GABA经UPLC法与HPLC法2种方法测定的含量在所需质量浓度范围内均具有良好的线性关系(R2>0.998)。UPLC法的平均相对标准差为0.529%,平均回收率为99.59%;HPLC法的平均相对标准差为1.175%,平均回收率为98.06%。精密度和回收率试验表明,2种检测方法均可准确定量分析乳酸菌发酵液中GABA含量。2种方法相比较,UPLC法的操作更为简单、出峰时间短,色谱峰具有较好的分离度,测定结果准确,精密度好,灵敏度高,能够满足检测大批量乳酸菌发酵液中的γ-氨基丁酸含量。
[1]UENO H.Enzymatic and structural aspects on glutamate decarboxylase[J].J Mol Catal B-Enzym,2000,10(1-3):67-79.
[2]朱广跃,杨卫,吴健,等.HPLC 法定量分析微生物法制备液中产物γ-氨基丁酸和底物L-谷氨酸[J].食品科学,2015,36(24):190-194.
[3]PEARL P L,HARTKA T R,CABALZA J L,et al.Inherited disorders of GABA metabolism[J].J Inherit Metab Dis,1993,16(4):704-715.
[4]WONG C G T,BOTTIGLIERI T,SNEAD O C.GABA,γ-hydroxybutyric acid,and neurological disease[J].Ann Neurol,2003,54(S6):3-12.
[5]SANDMEIER E.Multiple evolutionary origin of pyridoxal-5'-phosphatedependent amino acid decarboxylases[J].Febs J,2010,221(3):997-1002.
[6]吴慧,崔本来.柱前衍生-高效液相色谱法检测运动型饮料中γ-氨基丁酸的含量[J].中国酿造,2018,37(11):154-158.
[7]杨胜远,陆兆新,吕风霞,等.γ-氨基丁酸的生理功能和研究开发进展[J].食品科学,2005,26(9):546-551.
[8]毕金丽,刘娅,王建平,等.大肠杆菌L-谷氨酸脱羧酶定点突变及其酶学性质初步研究[J].食品工业科技,2014,35(19):162-167.
[9]杨帆.微生物转化法产γ-氨基丁酸[D].无锡:江南大学,2008.
[10]金红星,田楠,成文玉,等.微生物发酵合成γ-氨基丁酸的研究进展[J].安徽农业科学,2012,52(11):6385-6386,6470.
[11]MATSUO A,SATO K,PARK E Y,et al.Control of amylase and protease activities in a phytase preparation by ampholyte-free preparative isoelectric focusing for unrefined cereal-containing bread[J].J Funct Foods,2012,4(2):513-519.
[12]KIM H.Functional foods and the biomedicalisation of everyday life:a case of germinated brown rice[J].Sociol Heal Illness,2012,35(6):842-857.
[13]KARLADEE D,SURIYONG S.γ-Aminobutyric acid(GABA)content in different varieties of brown rice during germination[J].Scienceasia,2012,38(13):13-17.
[14]邵金良,杨东顺,樊建麟,等.DABS-Cl 柱前衍生-HPLC 测定稻米中γ-氨基丁酸方法优化[J].作物杂志,2016(1):135-140.
[15]王丽群,潘媛媛,孟庆虹,等.基于柱后衍生发芽糙米中γ-氨基丁酸HPLC 检测方法的建立及应用[J].中国酿造,2016,35(2):144-147.
[16]刘铁兵,龚金炎,朱银邦,等.柱前衍生化法农产品中γ-氨基丁酸的检测方法研究[J].中国粮油学报,2014,29(10):118-128.
[17]汤彩云,王涛,屠洁,等.比色法与HPLC 法对比测定桑叶茶中γ-氨基丁酸的含量[J].食品科学,2018,39(24):256-260.
[18]GAO Q,DUAN Q,WANG D,et al.Separation and purification of γ-amino butyric acid from fermentation broth by flocculation and chromatographic methodologies[J].J Agr Food Chem,2013,61(8):1914-1919.
[19]程威威,周婷,吴跃,等.高效液相色谱法测定发芽糙米中γ-氨基丁酸含量[J].食品科学,2014,35(12):98-101.
[20]李鹏.代谢工程改造大肠杆菌生产γ-氨基丁酸的含量[J].杭州:浙江工商大学,2017.