白酒是世界六大蒸馏酒之一,其独特的酿造方式造就了白酒不同的风格与特征,其显著特点是固态纯粮混菌发酵[1]。在白酒生产过程中,酿酒微生物主要包括霉菌、酵母菌、细菌三大类[2]。其中乳酸菌贯穿白酒生产的始终,是白酒生产中一类十分重要的微生物,乳酸菌可以促进发酵过程中的美拉德反应[3],有研究发现乳酸菌对酿酒酵母(Saccharomyces cerevisiae)的生长有抑制作用[4-7],但是乳酸菌可以促进酿酒酵母风味物质的代谢[8-9]。乳酸菌产生的乳酸能使白酒的刺激性气味减少,增加白酒的风味[10],而且乳酸可以与乙醇酯化形成乳酸乙酯,乳酸乙酯是各种白酒中十分重要的香味物质。无论是在制曲还是发酵过程中,都可以检测到乳酸菌,乳酸菌中又以乳杆菌居多[11-12],这和乳杆菌对高温、高酒精度和酸度的良好耐性有关系[13-14]。
我国白酒的生产需要依靠酒曲及环境中多种微生物的共同作用,其中酵母菌在发酵过程中起主导作用[15]。酵母菌分为酿酒酵母和非酿酒酵母,在白酒生产过程中,酿酒酵母是负责酒精发酵的主体菌,非酿酒酵母虽然酒精发酵能力不如酿酒酵母[16],但大多数能够高产乙酸酯类。酵母代谢产生的乙酸乙酯是很多香型白酒的主体香味物质,乙酸异戊醇和乙酸异丁酯具有水果的芳香。而高级醇是酵母酒精发酵的副产物,常见的高级醇主要包括正丙醇、异丁醇、异戊醇、活性戊醇、苯乙醇,白酒中适量的高级醇能使酒体丰满协调,给人柔和的香气,高级醇含量较低时就会导致酒中香气较淡而且酒体显得单薄;当高级醇含量过高时,会导致酒体中有不愉快的异杂味,并且更容易使人“上头”[17]。
白酒生产是微生物相互作用的结果,研究微生物相互作用对白酒酿造技术的进步有着重要的意义[18]。实验室前期通过分子生物学手段构建了一株高产酯酿酒酵母MY-15,能够高产乙酸酯类,且酒精发酵能力与普通酿酒酵母相当。将高产酯酿酒酵母与植物乳杆菌(Lactobacillus plantarum)在高粱汁中混合发酵,采用同步接种的方法,研究植物乳杆菌对高产酯酿酒酵母酯醇代谢的影响,为白酒生产中高产酯酿酒酵母的实际应用提供理论依据,探明高产酯酿酒酵母与植物乳杆菌协同发酵的代谢机制。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种和原料
植物乳杆菌(Lactobacillus plantarum):本实验室从老白干酒醅中分离获得;高产酯酿酒酵母(Saccharomyces cerevisiae)MY-15(CGMCC No.5635):天津市工业微生物重点实验室保存。玉米粉:市售;澳洲高粱:北京红星二锅头有限公司。
1.1.2 化学试剂
硫酸镁、硫酸铵、磷酸氢二钾(均为分析纯):天津市北方天医化学试剂厂;牛肉膏、酵母膏、蛋白胨(均为生化试剂):北京奥博星生物技术有限公司;一水葡萄糖(分析纯):天津光复精细化工有限公司;耐高温α-淀粉酶(酶活1×105 U/mL)、糖化酶(酶活2.9×105 U/mL)、酸性蛋白酶(酶活5×104 U/mL):诺维信(中国)生物技术有限公司。
1.1.3 培养基
酿酒酵母种子培养基(玉米水解液):玉米粉与水按照料液比1∶4(g∶mL)混合,添加耐高温α-淀粉酶(10 U/g原料)90 ℃水浴作用1 h,然后继续加热煮沸30 min,之后补水至原体积,立即降温到60 ℃,添加糖化酶(250 U/g原料)在60 ℃水浴作用4 h,然后用4层纱布过滤,调节糖度为12°Bx,添加硫酸铵6 g/L,硫酸镁1.2 g/L,磷酸氢二钾2.4 g/L,115 ℃高温灭菌20 min,备用。
酿酒酵母发酵培养基:高粱粉与水按照料水比1∶3(g∶mL)混合,液化糖化步骤同玉米粉水解液,糖化完成后降温到40 ℃,添加酸性蛋白酶(30 U/g原料),水浴作用4 h,然后用4层纱布过滤,得澄清高粱汁,调节到所需糖度,115℃高温灭菌20 min,备用。
乳酸菌种子培养基:MRS培养基[19]。
乳酸菌发酵培养基:葡萄糖质量分数为4%的MRS培养基。
1.2 仪器与设备
MS204S电子天平:梅特勒-托利多仪器有限公司;1200系列高效液相色谱仪、7890B型气相色谱仪:美国安捷伦科技有限公司;XMTB型电热恒温水浴锅:天津市中环实验器材有限公司;H1650-W型高速冷冻离心机:湖南湘仪科技有限公司;BX43型生物显微镜:日本OLYMPUS会社。
1.3 试验方法
1.3.1 植物乳杆菌的培养
植物乳杆菌的活化:取一环保藏于斜面上的植物乳杆菌接种于装有5 mL MRS液体培养基的试管中,30 ℃条件下静置培养24 h。
植物乳杆菌种子液的制备:将活化植物乳杆菌培养液转接于装液量为100 mL/250 mL MRS液体培养基中,30 ℃条件下静置培养24 h。
将植物乳杆菌种子液按10%(V/V)的接种量转接于装有葡萄糖质量分数为4%的MRS培养基三角瓶中,装液量为100 mL/250 mL,30 ℃条件下静置培养3 d,得植物乳杆菌发酵液。
1.3.2 高产酯酿酒酵母种子液的培养
高产酯酿酒酵母的活化:取一环保藏于斜面上的高产酯酿酒酵母接种于装有5 mL玉米水解液的试管中,30 ℃条件下静置培养24 h。
高产酯酿酒酵母种子液的制备:将活化好的酿酒酵母培养液转接于装液量为100 mL/250 mL玉米水解液中,30 ℃条件下静置培养16 h。
1.3.3 植物乳杆菌菌悬液对酿酒酵母酒精发酵及酯醇代谢的影响
取植物乳杆菌二级种子培养液150mL,于4℃、7000r/min条件下离心5 min,弃上清液,向沉淀中加入16°Bx高粱汁至总体积150 mL,振荡混匀,制成植物乳杆菌菌悬液。然后将植物乳杆菌菌悬液按照4.0%、8.0%、12.0%、16.0%的接种量接种到装有高粱汁培养基的三角瓶中,高产酯酿酒酵母种子液接种量均为8.0%,装液量为130 mL/250 mL,30 ℃静置发酵72 h。
1.3.4 植物乳杆菌种子培养液对酿酒酵母酒精发酵及酯醇代谢的影响
将培养好植物乳杆菌种子液按照4.0%、8.0%、12.0%、16.0%的接种量接种到装有高粱汁培养基的三角瓶中,高产酯酿酒酵母种子液接种量均为8.0%,装液量为130 mL/250 mL,30 ℃静置发酵72 h。
1.3.5 不同乳酸质量浓度对酿酒酵母酒精发酵及酯醇代谢的影响
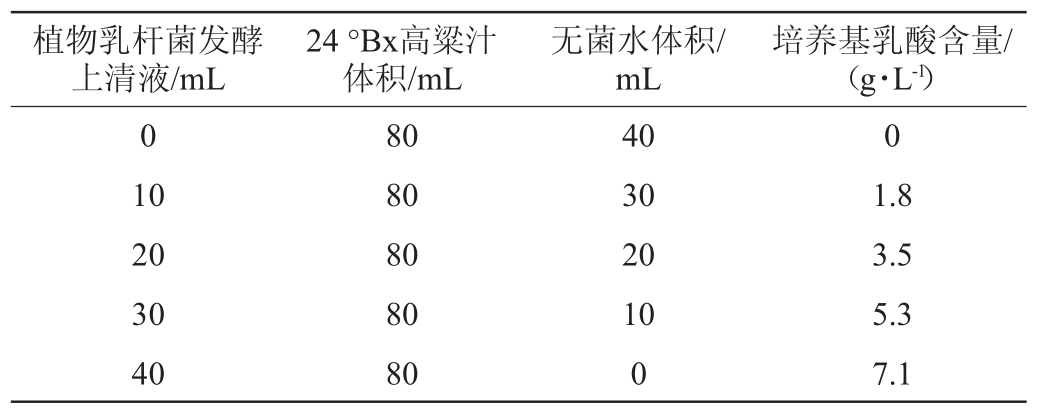
取培养好的植物乳杆菌发酵液300 mL,4 ℃、7 000 r/min离心5 min取上清液,用上清液配制成不同乳酸含量的高粱汁发酵培养基(见表1),高产酯酿酒酵母种子液接种量均为8.0%,装液量为130 mL/250 mL,30 ℃静置发酵72 h。
表1 含有不同乳酸含量的高粱汁发酵培养基配方
Table 1 Formula of sorghum juice fermentation medium with different lactic acid contents
1.3.6 分析方法
乳酸检测:采用高效液相色谱法。其色谱条件如下:HPX-87H色谱柱(300 mm×7.8 mm×9 μm),紫外(ultra violet,UV)检测器,流动相为5 mmol/L的稀硫酸溶液,柱温60 ℃,流速为0.6 mL/min,检测波长210 nm,检测时间23 min,进样量20 μL。
高级醇、乙酸酯检测:采用气相色谱法。其色谱条件如下:氢火焰离子检测器(flame ionization detector,FID),载气为高纯氮气(N2),LZP930白酒分析专用毛细管柱(50 m×0.32 mm×0.25 μm),进样量1 μL,分流比10∶1,进样口温度200 ℃,检测器温度230 ℃,氢气流量40 mL/min,空气流量300 mL/min,柱流量0.8 mL/min。程序升温,50 ℃保持8 min,然后以5 ℃/min速率升温至200 ℃保持5 min。
残糖量的测定:菲林试剂法[20];酵母菌数:血球计数板法[21-22]。
2 结果与分析
2.1 植物乳杆菌菌悬液对高产酯酿酒酵母酒精发酵及酯醇代谢的影响
植物乳杆菌菌悬液对高产酯酿酒酵母MY-15生长和酒精发酵的影响结果见表2。由表2可知,不同植物乳杆菌菌悬液添加量对高产酯酿酒酵母发酵过程的酵母细胞数、最终乙醇产量和发酵残糖量没有明显差异,乙醇含量在73.77~74.20 g/L,残糖量在4.01~4.21 g/L,说明植物乳杆菌对高产酯酿酒酵母的生长及酒精发酵没有直接影响。
表2 不同植物乳杆菌菌悬液添加量对高产酯酿酒酵母生长和酒精发酵的影响
Table 2 Effects of different suspension addition of Lactobacillus plantarum on the growth of high-yield ester Saccharomyces cerevisiae and alcoholic fermentation

植物乳杆菌菌悬液对高产酯酿酒酵母MY-15主要风味物质的影响结果见图1。由图1可知,植物乳杆菌菌悬液对高产酯酿酒酵母MY-15酯代谢有一定影响,与对照(植物乳杆菌菌悬液接种量为0时)相比,植物乳杆菌菌悬液接种量为4.0%、8.0%、12.0%、16.0%,乙酸乙酯分别减少了4.45%、15.83%、12.94%、15.31%;乙酸异戊酯分别减少了10.12%、17.74%、8.41%、15.54%;植物乳杆菌菌悬液各接种量下乙酸异丁酯的影响不明显,乙酸异丁酯含量在11.32~12.11 mg/L。可能原因与其含量相对较低有关。植物乳杆菌菌悬液对高产酯酿酒酵母MY-15高级醇代谢的影响各有不同,这与各高级醇不同的代谢途径有关。其中对苯乙醇和活性戊醇的影响最为明显,与对照(植物乳杆菌菌悬液接种量为0时)相比,植物乳杆菌菌悬液接种量为4.0%、8.0%、12.0%、16.0%时,苯乙醇含量分别下降了34.58%、36.78%、39.45%、42.17%,活性戊醇含量分别下降了21.58%、23.52%、26.97%、34.83%;对正丙醇和异丁醇含量的影响相对较低,植物乳杆菌菌悬液接种量为4.0%、8.0%、12.0%、16.0%时,正丙醇分别下降了14.89%、21.77%、17.16%、14.76%,异丁醇分别下降了9.34%、14.55%、19.52%、17.15%;各添加量对异戊醇的影响不明显。
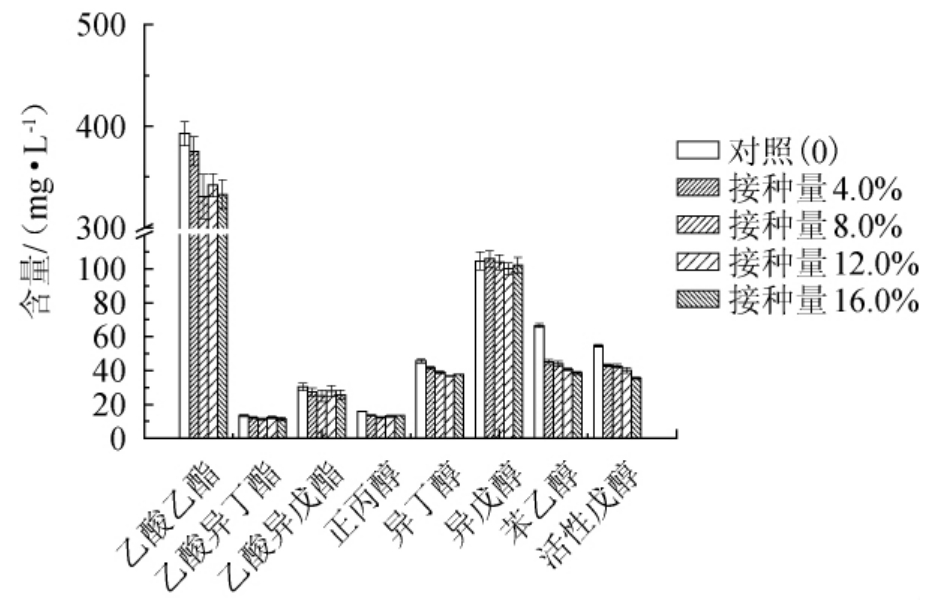
图1 不同植物乳杆菌菌悬液添加量对高产酯酿酒酵母主要风味物质的影响
Fig.1 Effects of different suspension addition of Lactobacillus plantarum on major flavor substances of high-yield ester Saccharomyces cerevisiae
2.2 植物乳杆菌种子液对高产酯酿酒酵母酒精发酵及酯醇代谢的影响
植物乳杆菌种子培养液对高产酯酿酒酵母生长和酒精发酵的影响结果见表3。由表3可知,发酵12 h时,添加植物乳杆菌种子培养液对高产酯酿酒酵母的生长有所抑制,酵母数分别下降20%、20%、30%、33%;而发酵到24 h时,即使添加了植物乳杆菌种子培养液,酵母数量与对照(植物乳杆菌种子液接种量为0时)相比也无显著差异,酵母数量在(1.90~2.10)×109 CFU/mL,说明添加植物乳杆菌种子培养液后,前12 h高产酯酿酒酵母生长缓慢,这和植物乳杆菌与酵母竞争营养物质有关,而在发酵12~24 h时,高产酯酿酒酵母逐渐成为优势菌群,进入了生长旺盛期。添加植物乳杆菌种子液对发酵结束高产酯酿酒酵母乙醇产量有略微提高,相应的发酵结束后的残糖量有所降低,在植物乳杆菌种子液接种量为0时,酿酒酵母乙醇产量为74.08 g/L;在植物乳杆菌种子液接种量为16.0%时,酿酒酵母乙醇产量为76.77 g/L。
表3 不同植物乳杆菌种子液添加量对高产酯酿酒酵母生长和酒精发酵的影响
Table 3 Effects of different seed solution addition of Lactobacillus plantarum on the growth of high-yield ester Saccharomyces cerevisiae and alcoholic fermentation

植物乳杆菌种子液对高产酯酿酒酵母MY-15主要风味物质的影响结果见图2。
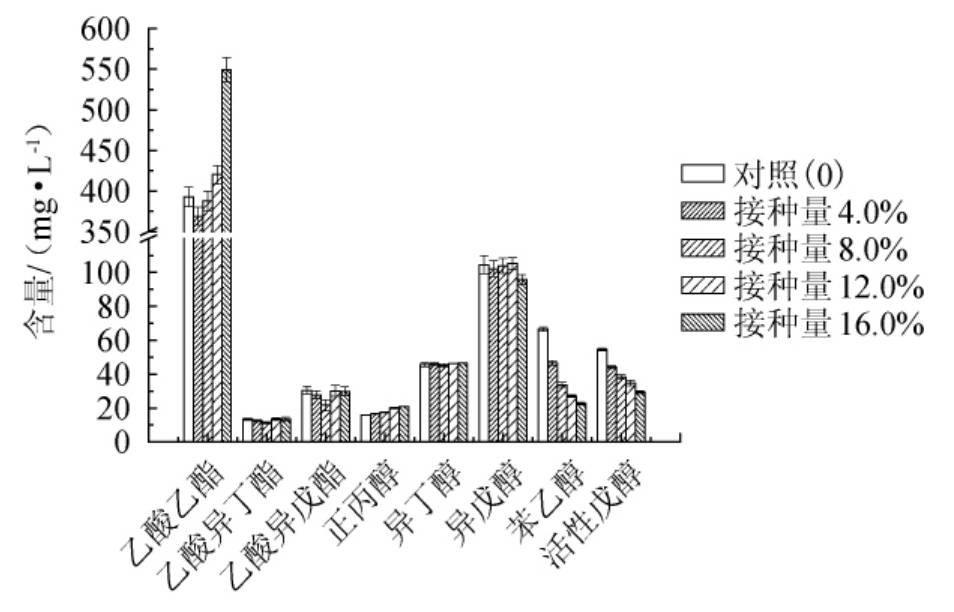
图2 不同植物乳杆菌种子液添加量对高产酯酿酒酵母主要风味物质的影响
Fig.2 Effects of different seed solution addition of Lactobacillus plantarum on major flavor substances of high-yield ester Saccharomyces cerevisiae
由图2可知,植物乳杆菌种子液对高产酯酿酒酵母MY-15酯代谢有一定影响,当植物乳杆菌种子液添加量为16.0%时,乙酸乙酯含量变化最大,增加了39.82%。在植物乳杆菌种子液各添加量下对高产酯酿酒酵母乙酸异丁酯和乙酸异戊酯的产量影响不大。植物乳杆菌种子培养液对高产酯酿酒酵母MY-15高级醇代谢的影响各有不同,正丙醇随着植物乳杆菌种子培养液添加量的增加而增加,在植物乳杆菌种子液添加量为16.0%时,正丙醇含量增加31.67%;异丁醇和异戊醇含量在植物乳杆菌种子液接种量为16.0%时稍有下降,下降了8.4%;活性戊醇和苯乙醇含量都是随着植物乳杆菌种子培养液添加量的增加而减少,在植物乳杆菌种子培养液添加量为4.0%、8.0%、12.0%、16.0%时,与对照(植物乳杆菌种子液接种量为0)相比,苯乙醇含量分别下降了30.34%、49.3%、59.24%、65.92%;活性戊醇含量分别下降了18.85%、29.96%、36.26%、46.03%。
2.3 不同乳酸含量对高产酯酿酒酵母酒精发酵及酯醇代谢的影响
培养基内不同乳酸含量对高产酯酿酒酵母MY-15生长及酒精发酵的影响结果见表4。由表4可知,发酵12 h和24 h时,培养基内乳酸质量浓度为5.3 g/L和7.1 g/L时,酿酒酵母数量下降明显,酵母数量下降明显,与对照相比,发酵12 h时,酵母数分别下降19.21%和27.81%;发酵24 h时,酵母数分别下降9.47%和13.61%,说明在培养基内乳酸质量浓度为5.3 g/L和7.1 g/L时对高产酯酿酒酵母前24 h的生长有所抑制。与对照相比,培养基内乳酸质量浓度为5.3 g/L和7.1 g/L时酿酒酵母乙醇产量有所提高,分别提高了1.56%和5.64%。
表4 不同乳酸含量对高产酯酿酒酵母生长和酒精发酵的影响
Table 4 Effects of different lactic acid contents on the growth of high-yield ester Saccharomyces cerevisiae and alcoholic fermentation

培养基内不同初始乳酸含量对高产酯酿酒酵母主要风味物质代谢的影响见图3。由图3可知,培养基内不同初始乳酸含量对高产酯酿酒酵母MY-15酯代谢有一定影响,与对照相比,当培养基内乳酸质量浓度为5.3 g/L和7.1 g/L时,酿酒酵母乙酸乙酯含量增加了39.51%和39.49%。乙酸异戊酯随着培养基内乳酸含量的增加而减少,与对照相比,培养基内初始乳酸含量为1.8 g/L、3.5 g/L、5.3 g/L、7.1 g/L时酿酒酵母乙酸异戊酯分别减少了21.27%、25.89%、30.65%、39.97%。培养基内不同初始乳酸含量对酿酒酵母MY-15高级醇代谢的影响各有不同,正丙醇随着培养基内植物乳杆菌发酵液的增多而增多,在培养基内初始乳酸质量浓度为1.8 g/L、3.5 g/L、5.3 g/L、7.1 g/L时,与对照相比,正丙醇含量增加了20.28%、40.11%、50.21%、70.33%。酿酒酵母异丁醇含量在培养基内初始乳酸浓度为1.8 g/L、3.5g/L时,与对照相比有所增加,分别增加了11.23%和8.79%,而当培养基内初始乳酸质量浓度为5.3 g/L、7.1 g/L时,酿酒酵母异丁醇含量与对照相比分别降低了14.23%和19.5%。酿酒酵母异戊醇和苯乙醇含量随着培养基内乳酸质量浓度的增加而逐渐降低,与对照相比,异戊醇含量分别下降了16.67%、33.33%、41.67%、75.01%;苯乙醇含量分别下降了25.05%、48.65%、62.35%、75.64%,这可能与培养基内酸浓度的增高及培养基中各氨基酸的含量不同有关系。

图3 不同乳酸含量对高产酯酿酒酵母主要风味物质的影响
Fig.3 Effects of different lactic acid contents on major flavor substances of high-yield ester Saccharomyces cerevisiae
3 结论
该研究在高粱汁培养基内同时接种植物乳杆菌(Lac tobacillusplantarum)和高产酯酿酒酵母(Saccharomycescerevisiae),探究植物乳杆菌及其代谢产物对高产酯酿酒酵母酒精发酵及酯醇代谢的影响。结果表明,植物乳杆菌菌悬液及种子液各接种量下对高产酯酿酒酵母生长及酒精发酵的影响不大,发酵72 h后残糖量都在5 g/L以内,乙醇产量为74~78 g/L,但植物乳杆菌菌悬液及种子液使高产酯酿酒酵母乙酸酯和高级醇产量降低。培养基内含有少量乳酸(质量浓度1.8~7.1 g/L)能够使高产酯酿酒酵母乙酸酯产量提高,并且降低高级醇的产量,尤其是苯乙醇的产量下降明显。
白酒生产是多菌群混合发酵,发酵过程中参与的微生物种类繁多,而且不同的微生物对酿酒酵母的影响各有不同,本实验研究了植物乳杆菌对高产酯酿酒酵母酒精发酵、乙酸酯及高级醇代谢的影响,为高产酯酿酒酵母的实际应用提供了理论依据,但想要透彻了解相互作用机理,还需从转录组学及分子生物学进行更深层次的研究。
[1]ZHENG X W,HAN B Z.Baijiu,Chinese liquor:History,classification and manufacture[J].J Ethn Food,2016,3(1):19-25.
[2]ZHENG X W,TABRIZI M R,NOUT M J R,et al.Daqu-a traditional Chinese liquor fermentation starter[J].J Inst Brew,2012,117(1):82-90.
[3]郭敏.基于高通量测序对酱香大曲制曲微生态多样性的研究[D].贵阳:贵州大学,2018.
[4]刘彩霞,郭学武,李玲玲,等.高产酯酿酒酵母与乳酸菌共发酵过程中的相互作用研究[J].现代食品科技,2017,33(7):36,85-90.
[5]张艳.酱香型白酒发酵中两株主要乳酸菌对酿造微生物群体的影响[J].微生物学通报,2015,42(11):2087-2097.
[6]ABE A,FURUKAWA S,WATANABE S,et al.Yeasts and lactic acid bacteria mixed-specie biofilm formation is a promising cell immobilization technology for ethanol fermentation[J].Appl Biochem Biotechnol,2013,171(1):72-79.
[7]WELTHAGEN J.Yeast profile in Gouda cheese during processing and ripening[J].Int J Food Microbiol,1998,41(3):94-185.
[8]熊君燕,李小东,谢圣凯,等.清香型白酒中乳酸菌和酵母菌的相互作用[J].微生物学通报,2017,44(8):1767-1776.
[9]谢玉球,钟雨,谢旭,等.乳酸菌在固态法白酒生产中的地位与作用[J].酿酒科技,2008(11):83-86.
[10]肖冬光.白酒生产技术[M].北京:化学工业出版社,2011:31-38.
[11]LI X R,MA E B,YAN L Z,et al.Bacterial and fungal diversity in the traditional Chinese liquor fermentation process[J].Int J Food Microbiol,2011,146(1):31-37.
[12]李斌,闫志鹏,李慧星,等.基于高通量测序技术的浓香型和芝麻香型白酒酒曲细菌群落结构分析[J].中国酿造,2018,37(8):148-152.
[13]陈申习,唐洁,张龙,等.清香型小曲白酒机械化生产中微生物动态变化研究[J].中国酿造,2018,37(6):68-72.
[14]邢敏钰.芝麻香型白酒发酵过程中乳酸菌群结构及功能[D].无锡:江南大学,2017.
[15]陈美竹,邱数毅,胡宝东,等.酱香型白酒酿造体系中酵母菌的研究进展[J].中国酿造,2015,34(6):5-10.
[16]唐洁,王海燕,徐岩.酿酒酵母和异常毕赤酵母混菌发酵对白酒液态发酵效率和风味物质的影响[J].微生物学通报,2012,39(7):921-930.
[17]秦伟帅.葡萄酒酵母遗传操作构建高级醇低产菌株的研究[D].泰安:山东农业大学,2013.
[18]邱并生.混菌发酵对白酒液态发酵效率和风味物质的影响[J].微生物学通报,2014,41(7):1477-1478.
[19]马立娟,王超,杜丽平,等.植物乳杆菌和酿酒酵母发酵菠萝汁的性能比较及产物分析[J].中国酿造,2018,37(3):72-77.
[20]杨林娥,彭晓光,杨庆文,等.斐林试剂法测定还原糖方法的改进[J].中国酿造,2010,29(5):160-161.
[21]朱明光,史媛英.血球计数板法测定酵母数和出芽率时应注意的问题[J].啤酒科技,2001(9):38-38.
[22]周德庆.微生物学实验教程(第2 版)[M].北京:高等教育出版社,2006:91-95.