海藻寡糖(algal oligosaccharides,AOS)是由聚合度较低的β-D-甘露糖醛酸(β-D-mannuronic acid,M)与α-L-古罗糖醛酸(α-L-guluronic acid,G)连接而成的低聚糖,是海藻多糖经过酸、氧化剂或裂合酶降解而获得的小分子质量片段。海藻寡糖具有许多重要的生物学功能,如具有抗氧化活性[1-2]、抗凝血活性[3]、降血压活性[4]、免疫调节活性[5]、植物生长调节活性[6-8]、诱导植物抗病活性[9]、促进逆境中食用菌的生长[10]等作用。
海藻多糖钠盐即海藻酸钠(sodium alginate,AGS),是生产海藻寡糖的主要原料,主要也是由β-D-甘露糖醛酸与α-L-古罗糖醛酸以3种方式(MM段、GG段和MG段)通过α-1,4糖苷键连接而成,是一种高聚合度的多糖类物质。海藻酸钠由于具有水溶性差、凝胶性强、黏度大等性质,限制了其在生物医药等领域的应用,但其降解产物——海藻寡糖,聚合度低、分子质量小,易溶于水,容易被吸收,且具有多种生理活性,使其逐渐成为研究热点。
海藻寡糖的制备方法主要有酸降解法[11]、物理降解法[12]、氧化降解法[13]和酶解法[14]等,其中传统的生产就是通过酸水解海藻酸钠,但是高浓度酸溶液和复杂的分离纯化步骤,不仅对环境造成污染,而且提取效率低,产物的聚合度难以控制[15]。而酶解法制备海藻寡糖不仅反应条件温和、节能环保,而且产物聚合度可控性强,产物容易分离纯化,提取效率高,因此酶法制备海藻寡糖逐渐成为近年来研究的热点[16]。黄菊等[17]使用商业的褐藻胶裂解酶酶解海藻酸钠制备海藻胶低聚糖,产率高达75%。包华芳等[18]利用褐藻胶裂解酶酶解海藻酸钠制备海藻寡糖并对其抗氧化活性进行研究。许雷等[19]用酶解法制备海藻寡糖并研究其吸湿及保湿性能。陈淑琼等[20]优化了酶解制备褐藻寡糖的工艺条件,并研究了褐藻寡糖的抗氧化活性和抑菌活性。本研究采用单因素试验和响应面试验设计优化酶解海藻酸钠生产海藻寡糖工艺,得到制备海藻寡糖的最佳酶解条件,同时也为酶法制备海藻寡糖的研究提供实验基础和理论参考。
1 材料与方法
1.1 材料与试剂
海藻酸钠(化学纯):青岛聚大洋藻业集团有限公司;海藻胶裂解酶(1×104 U/mL):青岛百成海洋生物资源有限公司;盐酸、氢氧化钠、磷酸氢二钠、磷酸二氢钠、亚硫酸钠、无水乙醇、酒石酸钾钠、3,5-二硝基水杨酸(dinitrosalicylic acid,DNS)、苯酚(均为分析纯):国药化学试剂有限公司。
1.2 仪器与设备
PHS-3EpH计:上海仪电科学仪器股份有限公司;TZL-98型恒温振荡器:浙江省宁波市医疗器械厂;全自动新型ZRD-A7080P鼓风干燥箱:杭州汇尔仪器设备有限公司。
1.3 方法
1.3.1 酶解条件优化单因素试验设计
以海藻寡糖平均聚合度(average degree of polymerization,DP)为评价指标,分别考察酶解时底物质量浓度(0.6 g/100 mL、0.8 g/100 mL、1.0 g/100 mL、1.2 g/100 mL、1.4 g/100 mL、1.6 g/100 mL)、酶解温度(25 ℃、30 ℃、35 ℃、40 ℃、45 ℃、50 ℃)及酶解pH值(6.5、7.0、7.5、8.0、8.5、9.0)对海藻酸钠酶解效果的影响[2,19]。
1.3.2 响应面试验优化酶法提取海藻寡糖的工艺
利用响应面分析法中Box-Behnken 试验设计原理,采用单因素试验确定的中心值(用“0”表示)、低水平(用“-1”表示)和高水平(用“+1”表示),以海藻寡糖的平均聚合度(Y)为响应值,对酶解反应体系中底物质量浓度(A)、酶解温度(B)及酶解pH值(C)进行优化,得到最佳酶解条件,响应面试验因素与水平见表1。
表1 Box-Behnken试验因素与水平
Table 1 Factors and levels of Box-Behnken experiments

1.3.3 分析检测
体系中总糖含量与还原糖含量的比值,即为体系的平均聚合度[21],其中还原糖含量采用DNS法[22]测定,总糖含量用苯酚-硫酸法[14]测定。
2 结果与分析
2.1 酶解条件优化单因素试验结果
2.1.1 底物质量浓度对酶法提取海藻寡糖的影响
海藻酸钠水解越彻底,酶解体系中还原性糖含量越高,海藻寡糖平均聚合度就越低。不同底物质量浓度对海藻酸钠酶解效果的影响见图1。由图1可知,随着海藻酸钠质量浓度的增加,海藻寡糖的平均聚合度呈现先降后升的趋势,当海藻酸钠质量浓度为1.0 g/100 mL时,海藻寡糖的平均聚合度最小,为4.08,即此时海藻酸钠水解效果最佳,故将1.0g/100mL作为响应面设计中海藻酸钠质量浓度的中心点。
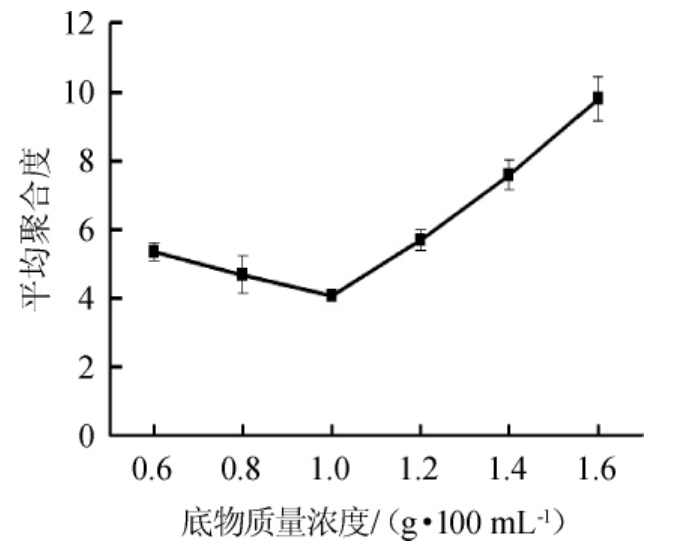
图1 底物质量浓度对海藻酸钠酶解效果的影响
Fig.1 Effect of substrate concentration on sodium alginate hydrolysis
2.1.2 酶解温度对酶法提取海藻寡糖的影响
酶解温度对海藻酸钠酶解效果的影响见图2。由图2可知,随着酶解温度升高,海藻寡糖平均聚合度呈现先下降后上升的趋势,当酶解温度为40 ℃时,海藻寡糖平均聚合度达到最小,达到3.85,故将40 ℃作为响应面设计中酶解温度的中心点。
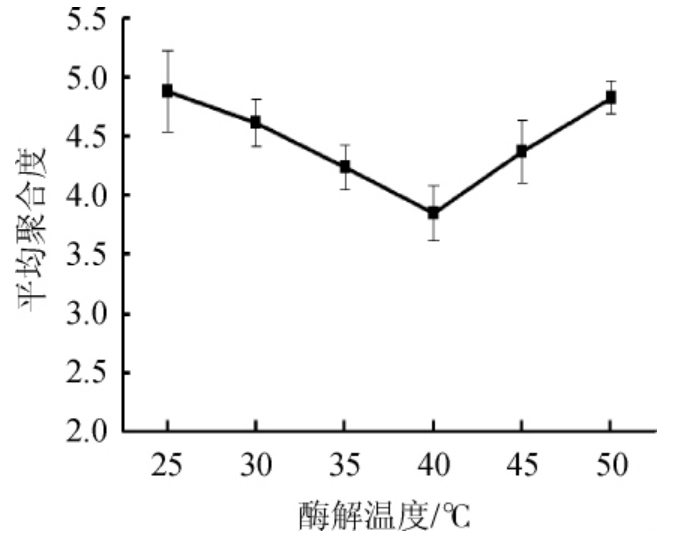
图2 酶解温度对海藻酸钠酶解效果的影响
Fig.2 Effect of enzymatic hydrolysis temperature on sodium alginate hydrolysis
2.1.3 酶解pH值对酶法提取海藻寡糖的影响
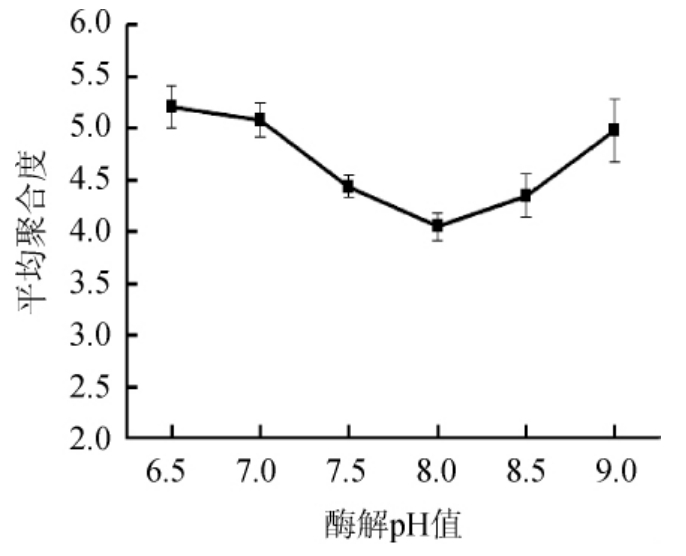
图3 酶解pH值对海藻酸钠酶解效果的影响
Fig.3 Effect of enzymatic hydrolysis pH on sodium alginate hydrolysis
不同酶解pH值对海藻酸钠酶解效果的影响结果见图3。由图3可知,随着酶解pH值的增加,海藻寡糖平均聚合度呈现先下降后上升的趋势,当酶解pH值为8.0时,海藻寡糖平均聚合度为4.05,达到最低值;酶解pH值>8.0时,海藻寡糖平均聚合度显著上升,故将pH值为8.0作为响应面设计中酶解pH值的中心点。
2.2 响应面优化酶法提取海藻寡糖的工艺
2.2.1 回归方程建立与方差分析
根据单因素试验结果,以底物质量浓度(A)、酶解温度(B)及酶解pH值(C)为自变量,海藻寡糖平均聚合度(Y)为因变量进行响应面试验,Box-Benhken试验设计及结果见表2,方差分析结果见表3。
表2 Box-Behnken试验设计及结果
Table 2 Design and results of Box-Behnken experiments
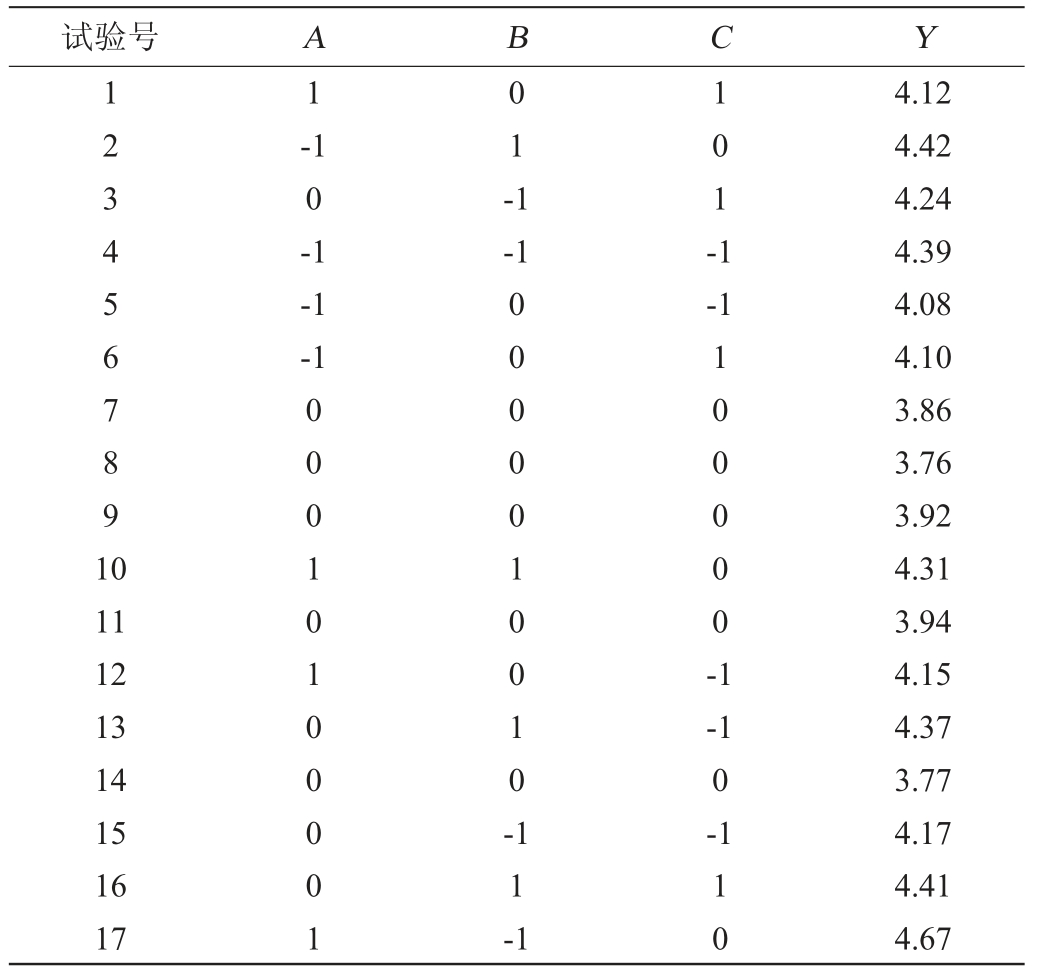
采用Design Expert 8.0.5软件对表2数据进行二次回归方程拟合,得到海藻寡糖平均聚合度(Y)对底物质量浓度(A)、酶解温度(B)及pH值(C)的多元二次回归方程:
表3 响应面试验回归模型方差分析
Table 3 Variance analysis of regression mode for response surface experiments

由表3可知,该模型显著(P=0.004 2<0.05),失拟项不显著(P=0.177 8>0.05),决定系数R2=0.920 7,说明有92.07%的变差能够由该模型解释;变异系数(coefficient of variation,CV)为2.6%,说明变异(偏离)程度较小。因此,该模型具有良好的拟合度,能真实地描述各因素与响应值之间的关系,可对海藻胶裂解酶水解海藻酸钠生产海藻寡糖的酶解条件进行预测和分析。
2.2.2 各因素响应面交互作用分析
采用Design Expert8.0.5软件对影响海藻胶裂解酶水解海藻酸钠生产海藻寡糖的3个因素进行交互分析,结果见图4。由图4可知,回归模型存在稳定点A=0.98,B=39.82,C=7.99,对应的实际取值为A=1.0,B=40,C=8.0。根据实际操作条件优化,得最佳酶解条件为底物质量浓度1.0 g/100 mL,酶解温度40 ℃,酶解pH值8.0,预测海藻寡糖平均聚合度为3.84,实际值为4.08。实际值与预测值基本接近,说明所建模型拟合良好且可靠。

图4 底物质量浓度、酶解温度和酶解pH值交互作用对海藻寡糖平均聚合度影响的响应曲面及等高线
Fig.4 Response surface plots and contour lines of effects of interaction between substrate concentration,enzymatic hydrolysis temperature and pH on average degree of polymerisation of algal oligosaccharides
2.3 最优酶解条件的确定及验证
为检验模型的可靠性和有效性,分别用模型预测的最优酶解条件和原始酶解条件进行海藻寡糖酶解试验,检测不同取样时间海藻寡糖平均聚合度,结果见图5。

图5 酶解条件优化前后海藻寡糖平均聚合度的变化
Fig.5 Changes of average degree of polymerisation of algal oligosaccharide before and after optimization of enzymatic hydrolysis conditions
由图5可知,在酶解1.5 h后,优化后海藻寡糖平均聚合度为4.08,比优化前的海藻寡糖平均聚合度5.62降低了27.35%。模型的预测值与实际酶解结果接近,说明模型能较好的反映底物质量浓度、酶解温度和酶解pH值对海藻胶裂解酶水解海藻酸钠制备海藻寡糖的影响,预测性良好。聚合度(degree of polymerization,DP)优于大部分已报道的酶解产海藻寡糖的结果[2,19-20],达到优化目的。
3 结论
本试验通过单因素试验和响应面分析法中Box-Behnken试验设计方法进行酶解条件的优化,得到最佳酶解条件为底物质量浓度1.0 g/100 mL、酶解温度为40 ℃和酶解pH值8.0。在最佳酶解条件下,海藻寡糖的平均聚合度为4.08。本试验也获得了一个能较好反映底物浓度、酶解温度和酶解pH对海藻胶裂解酶水解海藻胶制备海藻寡糖的模型,为酶解提取海藻寡糖的条件优化提供了技术参考。
[1]XU X,BI D C,LI C,et al.Morphological and proteomic analyses reveal that unsaturated guluronate oligosaccharide modulates multiple functional pathways in murine macrophage RAW264.7 cells[J].Mar Drugs,2015,13(4):1798-1818.
[2]张明杰,李恒,蒋敏,等.低分子质量褐藻寡糖的高效酶法制备及其抗氧化活性评价[J].海洋科学,2016,40(12):62-70.
[3]LIN C Z,GUAN H S,LI H H,et al.The influence of molecular mass of sulfated propylene glycol ester of low-molecular-weight alginate on anticoagulant activities[J].Eur Polym J,2007,43(7):3009-3015.
[4]UENO M,TAMURA Y,TODA N,et al.Sodium alginate oligosaccharides attenuate hypertension in spontaneously hypertensive rats fed a low-salt diet[J].Clin Exp Hypertens,2012,34(5):305-310.
[5]IWAMOTO M,KURACHI M,NAKASHIMA T,et al.Structure-activity relationship of alginate oligosaccharides in the induction of cytokine production from RAW264.7 cells[J].FEBS Lett,2005,579(20):4423-4429.
[6]张运红,和爱玲,杨占平,等.海藻酸钠寡糖灌根处理对小麦光合特性、干物质积累和产量的影响[J].江西农业学报,2018,30(11):1-5.
[7]IWASAKI K,MATSUBARA Y.Purification of alginate oligosaccharides with root growth-promoting activity toward lettuce[J].Biosci Biotech Bioch,2000,64(5):1067-1070.
[8]LUAN L Q,NAGASAWA N,HA V T T,et al.Enhancement of plant growth stimulation activity of irradiated alginate by fractionation[J].Radiat Phys Chem,2009,78(9):796-799.
[9]王松.褐藻寡糖的制备及诱导烟草抗性研究[D].青岛:中国海洋大学,2003.
[10]周林,郭尚,杨臻,等.外源海藻糖对高温胁迫下双孢蘑菇菌株生长的促进效应与耐高温株系筛选[J].西南农业学报,2019,32(1):154-160.
[11]DONATI I,GAMINI A,SKJK-BRAEK G,et al.Determination of the diadic composition of alginate by means of circular dichroism:a fast and accurate improved method[J].Carbohyd Res,2003,338(10):1139-1142.
[12]YANAKI T,NISHII K,TABATA K,et al.Ultrasonic degradation of Schizophyllum commune polysaccharide in dilute aqueous solution[J].J Appl Polym Sci,1983,28(2):873-878.
[13]杨钊,李金平,管华诗,等.一种新的褐藻胶寡糖制备方法-氧化降解法[J].海洋科学,2004,28(7):19-21.
[14]WONG T Y,PRESTON L A,SCHILLER N L.Alginate lyase:review of major sources and enzyme characteristics,structure-function analysis,biological roles,and applications[J].Annu Rev Microbiol,2000,54(1):289-340.
[15]SUN Y J,HOU ST,SONG S,et al.Impact of acidic,water and alkaline extraction on structural features,antioxidant activities of Laminaria japonica polysaccharides[J].Int J Biol Macromol,2018,112:985-995.
[16]SHARMA S,HORN S J.Enzymatic saccharification of brown seaweed for production of fermentable sugars[J].Bioresource Technol,2016,213:155-161.
[17]黄菊,丁晨,谢超,等.海藻胶低聚寡糖的酶法制备纯化技术及保水理化性质分析[J].海洋与湖沼,2015,46(3):595-602.
[18]包华芳,刘璘,丁玉庭.酶解制备褐藻胶寡糖及其抗氧化活性研究[J].中国酿造,2010,217(4):82-84.
[19]许雷,李湛,周火兰,等.酶解褐藻胶寡糖的吸湿及保湿性能研究[J].日用化学工业,2011,41(1):42-45.
[20]陈淑琼,李晓月,吴晨烁,等.酶解制备褐藻寡糖工艺优化及活性研究[J].食品研究与开发,2019,40(13):51-56.
[21]陶银凤.海藻酸钠裂解酶的分离与纯化[D].青岛:青岛科技大学,2014.
[22]张惟杰.糖复合物生化研究技术[M].杭州:浙江大学出版社,1999:133.