果醋是以水果或果品加工的下脚料为主要原料,经酒精发酵、醋酸发酵酿制而成的一种集营养食疗为一体的新一代酸性调味品或饮料[1]。果醋的营养丰富,富含多种有机酸,人体所需的多种氨基酸、维生素及生物活性物质,起到促进血液循环、降血压、调节体液酸碱平衡、抑制血糖升高、抗菌消炎和催眠镇静的作用[2-4]。
醋酸菌是能够将酒精氧化为醋酸的一类微生物的总称。醋酸菌对人及动物均无致病性,且大部分醋酸菌性状优良,营养要求较简单,环境适应能力强,可造成果实的细菌性腐败,造成酒的酸化,产生气味较温和的有机酸,引起酒的变色与风味改变[5-6]。优良的醋酸菌菌种是影响果醋品质的重要因素。国内外果醋酿造专用醋酸菌大都为食醋菌种AS1.41(Acetobacter rancens var.tubidans)和沪酿1.01(A.pasteurianus subsp.pasteurianus)等[7]。选育方法常用的有自然选育法或诱变育种法,但总体来看选育后的菌株产酸能力、耐酒精能力有限,而且发酵果醋形成的风味也不佳[8],转酸率高的菌株可以充分利用原料资源,节约成本,因此急需选育综合性能优良,特别是转酸率高的菌种。
冬枣也叫水果枣、冰糖枣,是目前枣中最高档的鲜食品种。其营养丰富,含19种人体必需氨基酸,维生素A、维生素E,钾、铁、铜、硒等多种微量元素;同时,枣多酚、黄酮含量高,具有较强的抗氧化活性、调节血脂和防治脑血管疾病的功效,是天然的滋补佳品[9-11]。我国有悠久的果醋制作历史,冬枣醋作为一种冬枣深加工产品,既具有冬枣特有的风味和营养价值,又兼有果醋的营养成分和保健功能,是一种新型的天然营养保健醋,具有广阔前景[12]。柿子醋醅中含有多种优良醋酸菌菌种,产酸迅速,其生产的柿子果醋富含多种香气、口感浓醇、回味深长,深受消费者喜爱[13]。本研究从传统自然发酵柿子醋醅中分离鉴定一株产酸性能优异的菌株,并利用其进行冬枣醋的发酵,通过单因素和正交试验对发酵条件进行优化,制得一款酸甜爽口的冬枣醋,为发掘利用醋酸菌资源,解决冬枣贮藏难的问题,开发营养、美味和具有保健功能的新型冬枣醋提供了依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料和菌种
柿子醋醅:山西运城盐湖区市场;奥尔兰醋杆菌(Acetobacter orleanense):国家菌种保藏中心CICC7001;大肠杆菌(Escherichia coli)DH5α:本实验室保藏;活性干酵母粉:中法王朝葡萄酒厂。
1.1.2 化学试剂
FlukaTM果胶酶(20 U/mg):德国霍尼韦尔公司;pUCm-T载体、脱氧核糖核酸(deoxyribonucleic acid,DNA)片断凝胶回收试剂盒、Taq DNA聚合酶(5 U/μL)、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)、DNA片段回收纯化试剂盒:上海生物工程技术服务有限公司;标准分子质量核酸![]() DNA Marker:北京全式金生物技术有限公司。
DNA Marker:北京全式金生物技术有限公司。
1.1.3 培养基
醋酸菌分离培养基:葡萄糖1%,酵母膏1%,体积分数95%的乙醇3%,0.5%琼脂,2%CaCO3,pH 4.5。121 ℃高压蒸汽灭菌20 min。
Hoyer-Frateur培养基:乙醇3%,(NH4)2SO40.1%,KH2PO40.01%,MgSO4·7H2O 0.025%,FeCl30.000 5%。115 ℃高压蒸汽灭菌20 min。
葡萄糖酸试验培养基:酵母膏3%,葡萄糖10%,K2HPO40.1%,MgSO40.035%,NaNO30.1%,KCl 0.025%,蛋白胨0.05%,琼脂2%,CaCO32%。115 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
ABI 2720聚合酶链式反应(polymerase chain reaction,PCR)仪:美国Thermo 公司;GIS-2009紫外凝胶成像仪:上海Tanon公司;HZQ-X100恒温振荡培养箱:北京东联哈尔仪器制造有限公司;DHP-420电热恒温培养箱:天津中环实验电炉有限公司;A-103多功能榨汁搅拌机:浙江顺敬工贸有限公司。
1.3 方法
1.3.1 柿子醋醅中高产酸醋酸菌的筛选
采用稀释涂布平板法[14]对柿子醋醅中的醋酸菌进行分离,稀释至10-1、10-2和10-3浓度,将稀释液涂布在醋酸菌分离培养基中,30 ℃、倒置培养3 d,钙溶解圈直径大的菌落相应产酸性能优良,从培养基中挑选菌落形态一致,透明圈直径H与菌落直径C的比值较大,具有生长优势的单个菌落,在平板上多次划线分离、培养,对菌株进行纯化。将纯化后的各菌株分别取一环接种于斜面分离培养基上,编号,并30 ℃条件下静置培养3 d。按照文献[15]中的FeCl3溶液法进行产酸定性实验,筛选出产醋酸的单菌落菌株。
1.3.2 醋酸菌形态特征观察
取一环筛选的菌株分别接种于分离培养基平皿上,30 ℃倒置培养3 d,观察菌落特征,并将各菌株进行革兰氏染色观察其细胞形态,其运动性利用直针穿刺法进行观察。
1.3.3 醋酸菌的生理生化特征的测定
接触酶、氧化酶、吲哚、V-P、明胶液化、乙醇过氧化、甘油生酮、产5-酮葡萄糖酸盐参考文献[16,17]进行;以铵盐为唯一氮源生长试验:在Hoyer-Frateur培养基上接种斜面菌株并观察生长情况;产葡萄糖酸试验:取一环菌接种到葡萄糖酸试验培养基,观察是否有透明圈。按照参考文献[15]中的中和滴定法进行菌株产醋酸能力的测定,取产酸能力最高的菌株进行后续实验。对照菌株为醋化醋杆菌奥尔兰亚种(A.orleanense)。
1.3.4 醋酸菌的分子生物学鉴定
(1)16S rDNA基因片断的扩增
取分离得到醋酸菌菌株一接种环悬浮于50 μL ddH2O中混匀15 s,5 000 r/min离心1 min,取上清做模板。
上游引物:5'-GCT GGC GGC ATG CTT AAC ACA T-3';
下游引物:5'-AACCACATGCTCCACCGCTTG-3'[18]。
PCR扩增反应体系(50μL):上下游引物各1μL(10pmol/μL),模板DNA(100 ng/μL)5 μL,10×PCR Buffer 5 μL,dNTP Mix 2 μL,超纯水35 μL,Taq酶1 μL。
PCR扩增反应程序为:94 ℃预变性4 min;94 ℃变性30 s,58 ℃退火1 min,72 ℃延伸2 min,循环30次;72 ℃延伸10 min;4 ℃保存。
(2)醋酸菌16S rDNA基因序列分析
按片断凝胶回收试剂盒和DNA片段回收纯化试剂盒说明书进行PCR产物的回收及纯化。按pUCm-T载体说明书进行PCR产物与pUCm-T Vector连接,16 ℃条件下下反应过夜。将连接产物送上海生工生物工程公司测序。
测序结果去除引物序列后在美国国立生物技术信息中心(national center for biotechnology information,NCBI)的GenBank数据库中进行Blast比对,选取同源性高的模式菌株的16S rDNA序列,采用MEGA 5 软件中的邻接(neighbor joining,NJ)法构建系统发育树。
1.3.5 冬枣醋发酵工艺流程及操作要点
冬枣选果、清洗→去核打浆→酶解→离心分离→澄清冬枣汁→成分调整→杀菌→冷却→酒精发酵→醋酸发酵→过滤→杀菌→冬枣醋
操作要点:
选果、清洗、去核打浆:选择新鲜、成熟的果实,剔除烂果,用清水清洗2~3次。去除枣核,将冬枣用榨汁机破碎打浆。立即将果汁用真空抽滤机过滤,并在95 ℃下灭酶30 s。
果胶酶酶解:果胶酶用量0.08%,酶解温度50 ℃,柠檬酸调pH 3.5,酶解时间3 h。
离心分离:在5 000 r/min的条件下离心10 min,除去沉淀得到澄清冬枣汁。
成分调整:添加蔗糖调节初始糖度为16%,柠檬酸调pH 4.5。
杀菌、冷却:105 ℃条件下杀菌20 s,冷却至50~55 ℃。
酵母菌活化:试管装入0.5 g蔗糖于10 mL蒸馏水中,高压灭菌后冷却至37 ℃左右,加入0.5 g活性干酵母粉,37 ℃水浴活化30 min。将3接种环酵母菌活化液接入灭菌的5 mL冬枣汁中,30 ℃静置培养24 h。将培养的酵母菌液按3%的接种量接入灭菌的100 mL冬枣汁,30 ℃静置培养24 h,备用。
醋酸菌活化:将2接种环选定的产醋酸菌株接入灭菌的5 mL冬枣汁中于30 ℃、120 r/min摇床中培养24 h。将培养的菌株按3%的接种量接入灭菌的100 mL冬枣汁,于30 ℃、120 r/min摇床中培养24 h,备用。
酒精发酵:初始糖度16%,酵母菌接种量5%,发酵温度30 ℃,密闭静置发酵至酒精度上升缓慢时停止。
醋酸发酵:调整初始酒精度为8%vol,醋酸菌接种量10%,装液量为50 mL/150 mL,发酵温度30 ℃,在50 r/min转速下振荡发酵14 d,以发酵液酸度上升缓慢时发酵停止。
过滤、杀菌:用硅藻土抽滤,95 ℃杀菌10 min,冷却后得到冬枣醋。
1.3.6 酒精发酵条件优化单因素试验
将冬枣汁的初始糖度分别调至8%、10%、12%、14%、16%、18%,分别接入0.5%、1.0%、3.0%、5.0%、7.0%、9.0%二级扩培酵母液,将酒精发酵温度分别调至10 ℃、24 ℃、26 ℃、28 ℃、30 ℃、32 ℃,发酵时间为4 d,以考察不同酵母菌接种量、发酵温度及初始糖度对冬枣汁酒精度的影响。
1.3.7 醋酸发酵条件优化单因素试验
将冬枣汁的初始酒精度分别调至6%vol、8%vol、10%vol、12%vol、14%vol、16%vol,分别接入6%、8%、10%、12%、14%、16%二级扩培醋酸菌液,将发酵温度分别调至26 ℃、28 ℃、30 ℃、32 ℃、34 ℃、36 ℃条件下发酵14 d,以考察不同醋酸菌接种量、初始酒精度及发酵温度对冬枣醋酸度的影响。
1.3.8 冬枣醋醋酸发酵条件优化正交试验
在单因素试验的基础上,对醋酸发酵温度(A)、初始酒精度(B)、醋酸菌接种量(C),进行3因素3水平的正交试验,以总酸含量为评价指标,采用L9(34)正交设计,确定醋酸发酵的最佳工艺条件。正交试验因素与水平见表1。
表1 醋酸发酵条件优化正交试验因素与水平
Table 1 Factors and levels of orthogonal tests for acetic acid fermentation conditions optimization

1.3.9 冬枣醋品质分析
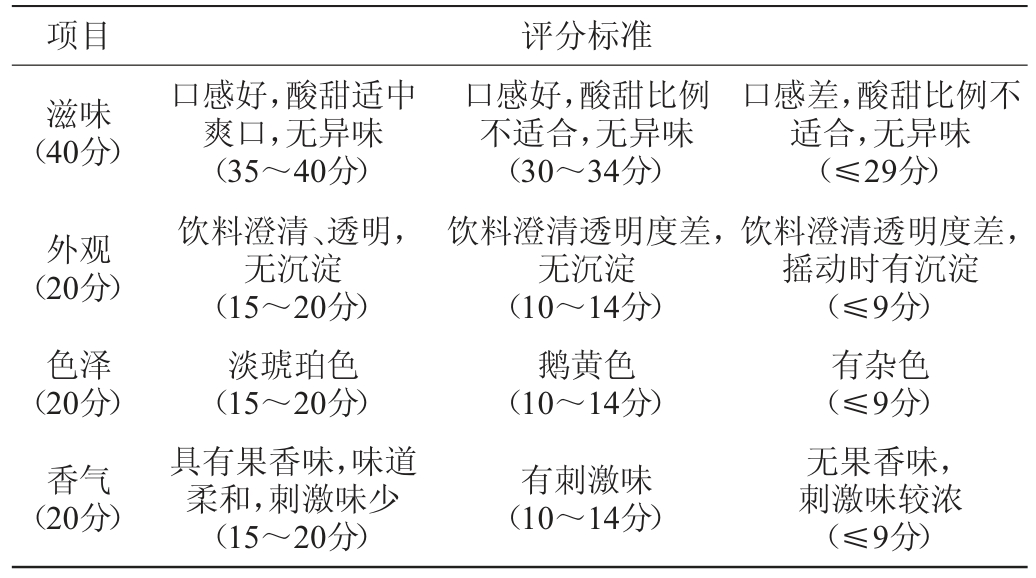
(1)感官评价:根据国标GB/T 30884—2014《苹果醋饮料》[19],对冬枣醋色泽(20分)、香气(20分)、滋味(40分)、外观(20分)方面进行感官评分,满分100分,由10人品评取平均分,冬枣醋感官评分标准[20]见表2。
表2 冬枣醋感官评分标准
Table 2 Sensory evaluation standard of winter jujube vinegar
(2)理化指标的测定:根据国标GB/T 12456—2008《食品中总酸的测定国家标准》对冬枣醋中总酸含量(以醋酸计)进行测定;采用重铬酸钾比色法测定酒精度;采用糖度计测定糖度;采用酸度计测定pH值。
(3)微生物指标的测定:根据国标GB 7101—2015《食品安全国家标准饮料》,对冬枣醋的菌落总数、大肠菌群及致病菌(指肠道致病菌)进行检验和测定。
2 结果与分析
2.1 醋酸菌的分离鉴定
从醋酸菌分离纯化固体培养基中挑选透明圈大,细胞形态类同,且占生长优势的单菌落80个,保留革兰氏阴性产酸菌株12 株,按照A1~A12进行编号。各菌株的菌落形态为白色半透明状,圆形,隆起,表面光滑,直径2~3 mm,均有运动性,在穿刺培养基中穿刺线向四周呈云雾状扩散。菌株A1革兰氏染色呈阴性,细胞呈杆状,大小(0.5~0.8)μm×(1.0~4.2)μm,成对或成链。
将筛选出的菌株A1~A12进行生理生化试验鉴定,结果见表3。由表3可知,对照第九版《伯杰细菌鉴定手册》及《常见细菌系统鉴定手册》,菌株A1、A2、A6、A8、A9不产2,5-二酮基葡萄糖酸、产5-酮基葡萄糖酸且不铵盐为唯一氮源,初步判定为木醋杆菌(Acetobacter xylinum),菌株A3、A5、A10无甘油生酮表现且不产5-酮基葡萄糖酸,初步判定为巴氏醋杆菌(Acetobacter pasteurianus),菌株A4、A11以铵盐为唯一氮源,初步判定为醋化醋杆菌(Acetobacter aceti),菌株A7、A12产2,5-二酮基葡萄糖酸且无乙醇过氧化表现,初步判定为氧化葡糖杆菌(Gluconobacter oxydans)。
表3 分离醋酸菌的生理生化试验结果
Table 3 Results of physiological and biochemical tests of isolated acetic acid bacteria
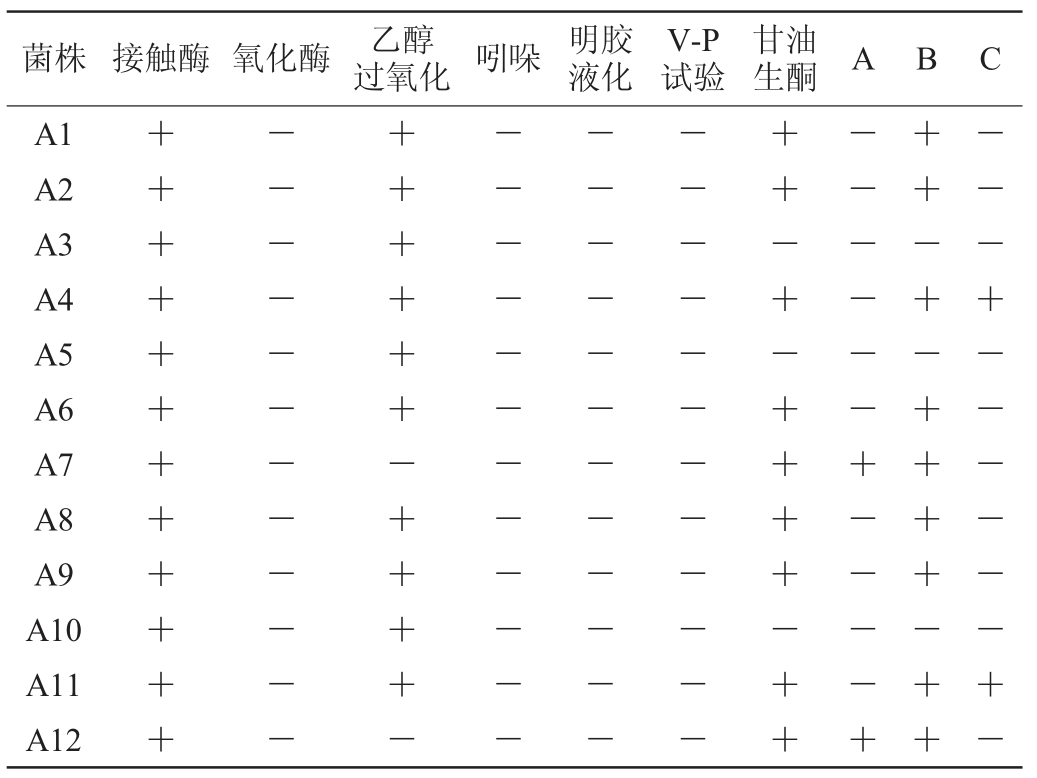
注:“+”表示阳性反应,“-”表示阴性反应。A代表产2,5-二酮基葡萄糖酸结果,B代表产5-酮基葡萄糖酸结果,C代表以铵盐为唯一氮源是否生长。
从不同种属的菌株中选择菌株A1、A3、A4、A7进行产酸量试验,结果见表4。由表4可知,菌株A3产酸能力低于对照菌株,A7与对照菌株产酸能力相当,均为9 d产酸量5.62 g/mL,菌株A1、A4的产酸能力高于对照菌株,A1产酸能力最高,为9 d产酸量5.89 g/mL。因此,选择菌株A1进行分子生物学鉴定。
表4 分离醋酸菌的产酸量比较
Table 4 Comparison of acid yield of isolated acetic acid bacteria

注:A0为对照菌株:奥尔兰醋酸杆菌。
2.2 16S rDNA测序鉴定分离菌株的结果
2.2.1 16S rDNA基因片断提取和PCR扩增
选取醋酸产量高的菌株A1进一步用分子生物学方法进行鉴定。菌株A1 16S rDNA 扩增产物连接T载体后PCR,经琼脂糖凝胶电泳检测结果见图1。
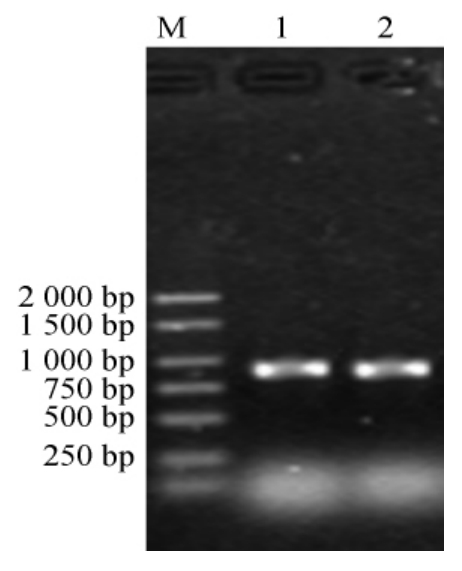
图1 重组质粒的PCR鉴定结果
Fig.1 Identification results of recombinant plasmid by PCR
M:DGL2000 DNA Marker;1,2:重组质粒。
由图1可知,观察到出现0.8 kbp左右的一条纯的DNA条带,表明已获得了纯的菌株A1的16S rDNA基因片断。
2.2.3 序列分析结果
将所测核苷酸序列用NCBI的基本局部比对搜索工具(basic local alignment search tool,BLAST)软件进行序列同源性分析。采用MegaX软件的NJ法构建系统发育树,结果如图2所示。

图2 基于16S rDNA序列菌株A1的系统发育树
Fig.2 Phylogenetic tree of strain A1 based on 16S rDNA sequences
由图2可知,在核酸水平上,菌株A1的16S rDNA部分序列与A.xylinum(登记号为X75619.1)的16S rDNA在同一分支且有98%的一致性。综合细胞形态、菌落形态及生理生化特征、16S rDNA序列同源性比较,鉴定菌株A1为木醋杆菌(Acetobacter xylinum)。
2.3 冬枣醋发酵条件优化
2.3.1 冬枣醋酒精发酵条件优化单因素试验
酒精作为醋酸发酵的重要原料,直接影响冬枣醋的酸度,进而影响其品质,使用酵母菌可以将糖代谢为酒精,以酒精度为评价指标,考察酒精发酵中酵母菌接种量、温度和初始糖度对冬枣醋品质的影响,结果见图3。
由图3a可知,酵母接种量在1%~5%范围内,酒精度随接种量增加而增加;酵母接种量为5%时,酒精度最大,为8.2%vol;酵母接种量>5%之后,酒精度基本稳定不变。因此,最佳接种量为5%。
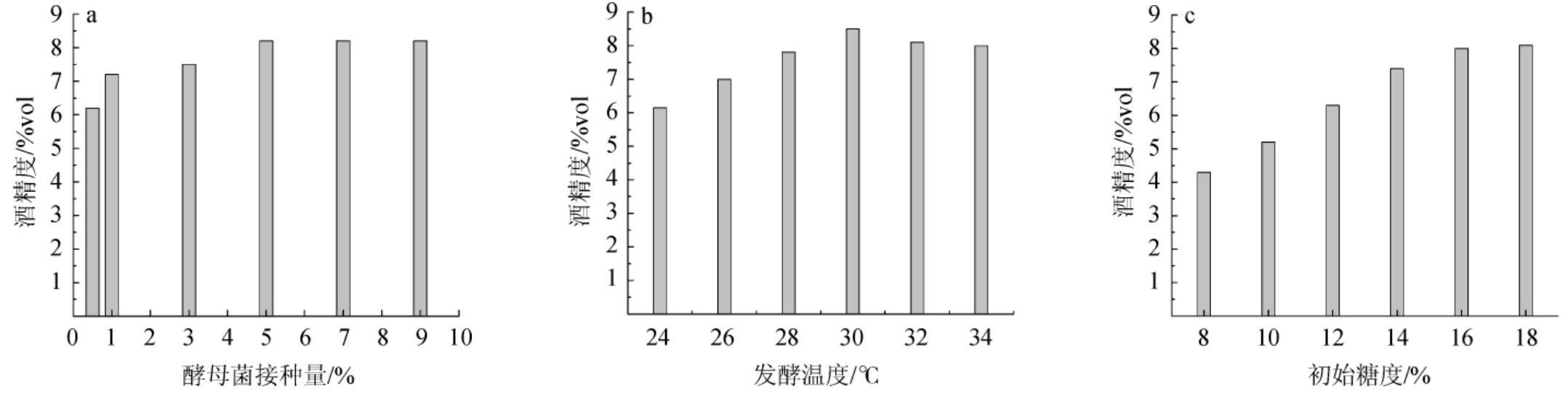
图3 酵母菌接种量(a)、发酵温度(b)和初始糖度(c)对冬枣醋酒精发酵的影响
Fig.3 Effect of yeast inoculum (a),fermentation temperature (b) and initial sugar content (c) on alcoholic fermentation of winter jujube vinegar
细胞内温度升高,酶反应加速,促进代谢和生长,但生物活性物质可能发生变性使细胞功能下降。由图3b可知,发酵温度在24~30 ℃时,随发酵温度的升高,酒精度也随之上升;发酵温度为30 ℃时,酒精度最大,为8.5%vol;发酵温度>30℃时,随温度的升高,酒精度反而下降。因为细胞内温度升高,酶反应加速,促进代谢和生长,但生物活性物质可能发生变性使细胞功能下降。因此,选择最佳发酵温度为30℃。
糖是酒精发酵的重要基质原料,直接影响到酒精转化情况,糖度高时产生的酒精度也相对较高,但过高反而抑制微生物的发酵。由图3c可知。随初始糖度在8%~16%范围内的增大,酒精度随之增加;初始糖度为16%时,酒精度为8%vol;初始糖度>16%之后,酒精度基本稳定。因此,初步确定最适初始糖度为16%。
2.3.2 冬枣醋醋酸发酵条件优化单因素试验
以酸度为评价指标,考察醋酸发酵中醋酸菌接种量、酒精度及发酵温度对冬枣醋品质的影响,结果见图4。

图4 醋酸菌接种量(a)、初始酒精度(b)及发酵温度(c)对冬枣醋醋酸发酵的影响
Fig.4 Effect of acetic acid bacteria inoculum (a),initial alcohol content (b) and fermentation temperature (c) on acetic fermentation of winter jujube vinegar
由图4a可知,酸度随醋酸菌接种量在4%~10%范围内增加而升高,接种量在10%以上酸度变化不大,这是由于发酵液内的营养物质不能高效利用。因此,选择10%为醋酸菌最佳接种量。由图4b可知,酸度随初始酒精度在4%vol~8%vol范围内提高而升高,酒精度在8%vol以上酸度变化不明显,选择最适初始酒精度为8%vol。由图4c可知,发酵温度在26~30 ℃范围内增加,酸度随发酵温度升高而增加;发酵温度在30 ℃时,酸度最大,为3.42 g/100 mL;发酵温度>30 ℃之后,酸度随发酵温度升高而降低。因此,选择30 ℃为最佳发酵温度。
2.3.3 冬枣醋醋酸发酵条件优化正交试验
为了确定冬枣醋醋酸发酵的最优条件,对醋酸菌接种量(A)、发酵温度(B)、初始酒精度(C)进行3因素3水平的L9(34)正交试验,发酵时间为14 d,以酸度为考察指标,正交试验优化醋酸发酵条件结果与分析见表5。
表5 醋酸发酵条件优化正交试验结果与分析
Table 5 Results and analysis of orthogonal tests for acetic acid fermentation conditions optimization

续表
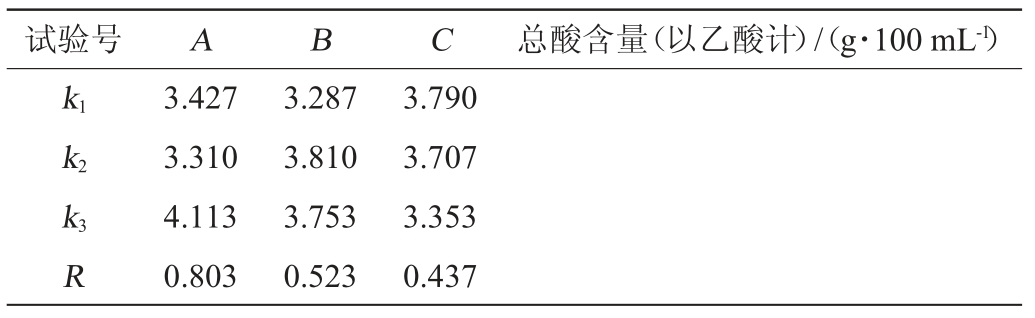
由表5可知,3个影响因素的主次关系是:A(发酵温度)>B(初始酒精度)>C(接种量)。最佳发酵条件组合为A3B2C1,即冬枣醋醋酸发酵条件为发酵温度为32 ℃,初始酒精度为9%vol,接种量为8%,发酵时间为14 d。在此最佳醋酸发酵条件下进行3次验证试验,冬枣醋总酸含量(以乙酸计)为4.76 g/100 mL。
2.4 冬枣醋醋饮料品质评价
在最佳发酵条件下制备冬枣醋,成品冬枣醋的感官指标、理化指标及微生物指标测定结果见表6。由表6可知,冬枣醋饮各项品质指标均满足相关国标要求。
表6 冬枣醋品质指标测定结果
Table 6 Determination results of quality indexes of winter jujube vinegar

3 结论
本研究从民间传统柿子醋醅中筛选出菌株A1,经菌落细胞形态观察、生理生化试验及分子生物学鉴定其为木醋杆菌(Acetobacter xylinum)。将该木醋杆菌菌株用于冬枣醋发酵饮料的研制,采用单因素及正交试验优化冬枣醋最佳醋酸发酵条件为木醋杆菌接种量8%,发酵温度32 ℃,初始酒精度为9%vol。在此优化醋酸发酵条件下酿造得到的冬枣醋感官评分91分,总酸含量(以醋酸计)4.76 g/100 mL,固形物含量1.5%,淡琥珀色,口味酸甜爽口,具有冬枣特有的果香,理化及微生物指标均符合国家相关标准。
[1]OZTURK I,CALISKAN O,TORNUK F,et al.Antioxidant,antimicrobial,mineral,volatile,physicochemical and microbiological characteristics of traditional home-made Turkish vinegars[J].LWT-Food Sci Technol,2015,63(1):144-151.
[2]王敏.发酵型果醋饮料的研究现状与发展趋势[J].饮料工业,2016,19(3):76-78.
[3]高佳琪,于泽鹏,刘聪,等.大枣果醋的镇静、催眠及抗焦虑作用[J].中国老年学杂志,2018,38(22):156-158.
[4]向进乐,罗磊,郭香凤,等.果醋功能性研究进展[J].食品科学,2013,34(13):356-360.
[5]SAICHANA N,MATSUSHITA K,ADACHI O,et al.Acetic acid bacteria:A group of bacteria with versatile biotechnological applications[J].Biotechnol Adv,2014,33(6):1260-1271.
[6]ROOS D J,VUYST D L.Acetic acid bacteria in fermented foods and beverages[J].Curr Opin Biotech,2018,49:115-119.
[7]魏长庆,王海庆,张凌,等.葡萄果醋发酵用醋酸菌的分离及鉴定[J].中国酿造,2010,29(4):42-44.
[8]张蕾,郭龙,傅力.紫外线诱变选育高产醋酸的醋酸菌研究[J].新疆农业科学,2012,49(6):1120-1126.
[9]郭雪飞,周晓凤,冯一峰,等.不同枣品种果实矿质元素含量分析及综合评价[J].食品工业科技,2018,39(22):268-275.
[10]张平平,邓杰,袁亚娜,等.冬枣总黄酮对高脂小鼠的降脂作用[J].营养学报,2015,37(6):596-599.
[11]张泽炎,张海生.干燥时间对枣多酚得率和抗氧化活性的影响[J].食品与发酵工业,2017,43(8):151-156.
[12]李忠,董成虎,高元惠,等.不同处理方法对冬枣贮藏效果的影响[J].保鲜与加工,2018,18(3):57-61.
[13]刘滔,朱维,李春美.我国柿子加工产业的现状与对策[J].食品工业科技,2016,37(24):369-375.
[14]朱艺恒,潘红菊,汪涯.南丰蜜橘中产醋酸菌的分离及其生长特性[J].生物化工,2019,5(1):52-55.
[15]苏龙,庄明川,梁广波,等.醋酸高产菌株的筛选及百香果果醋发酵条件的优化[J].食品科技,2017,43(4):33-37.
[16]东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学出版社,2001:69-100.
[17]布坎南R E,吉本斯N E.《伯杰氏细菌鉴定手册》(第九版)[M].北京:科学出版社,1989:67-89.
[18]POBLET M,ROWS N,GUILLAMON J M,et al.Identification of acetic acid bacteria by restriction fragment length polymorphism analysis of a PCR-amplified fragment of the gene coding for 16S rDNA[J].Lett Appl Microbiol,2000,31(1):63-67.
[19]国家质量监督检验检疫总局,国家标准化管理委员会.GB/T 30884—2014 苹果醋饮料[S].北京:中国标准出版社,2014.
[20]靳桂敏,贺银凤,钟震雄.柚子果醋及其饮料生产工艺研究[J].中国酿造,2007,26(2):64-66.