硒代半胱氨酸(selenocysteine,Sec)是蛋白质中硒的主要存在形式,也是唯一含有准金属元素的氨基酸[1]。Sec被称为第21种氨基酸[2],作为活性中心存在于谷胱甘肽过氧化酶、硫氧还蛋白还原酶、甘氨酸还原酶、甲酸脱氢酶等含硒酶中。其在合成高活性硒化物,生产富硒食品,医药保健方面有着巨大潜力。如硒代半胱氨酸的甲基化衍生物硒甲基半胱氨酸(methyl selenocysteine,SeMcys)是一种有着良好抗癌前景的物质。硒甲基半胱氨酸具有补硒、防治癌症、抗氧化、抗衰老、治疗心脑血管疾病、解重金属毒等作用[3]。硒代半胱氨酸是多种低分子硒代多肽类物质的组分[4]。包含硒代半胱氨酸残基的蛋白称为硒蛋白[5]。含有硒代半胱氨酸的硒蛋白有多种重要作用[6],是人和动物体内是不可缺少的关键物质,大规模生产硒代半胱氨酸有着良好的市场效益。目前可利用化学法和生物法合成硒代半胱氨酸。
1 化学法合成硒代半胱氨酸
化学法合成硒代半胱氨酸先用氯丙氨酸(C3H6ClNO2)与二硒化钠(Na2Se2)反应生成硒代胱氨酸(SeC),然后用金属钠/液氨在-70 ℃的条件下将硒代胱氨酸还原裂解成硒代半胱氨酸[7]。该方法中的化学反应需在-70 ℃的条件下进行,且需用到性质活泼的金属钠,反应条件苛刻,工艺设备要求高,氯丙氨酸原料价格高,生产成本高,很难投入大规模的生产中。
2 生物法合成硒代半胱氨酸
植物、动物、微生物均能合成硒代半胱氨酸。硒代半胱氨酸在生物体内合成需要依赖复杂的转移核糖核酸(transfer ribonucleic acid,tRNA)合成机制[8],其tRNA起初由丝氨酸-tRNA连接酶加载丝氨酸(serine,Ser),但其无法被普通的翻译因子识别。该丝氨酰可被含有磷酸吡哆醛的硒代半胱氨酸合成酶替换为硒半胱胺酰。然后Sec-tRNA与硒特异延伸因子(SelB或mSelB)结合,通过核糖体翻译该mRNA。无机硒通过硫的合成途径,传递到核糖体,并插入到新生的硒蛋白[9]。生物法合成硒代半胱氨酸相较于化学法,反应相对温和,材料成本低廉,大规模生产方面更具前景。
2.1 植物合成硒代半胱氨酸及检测提取方法
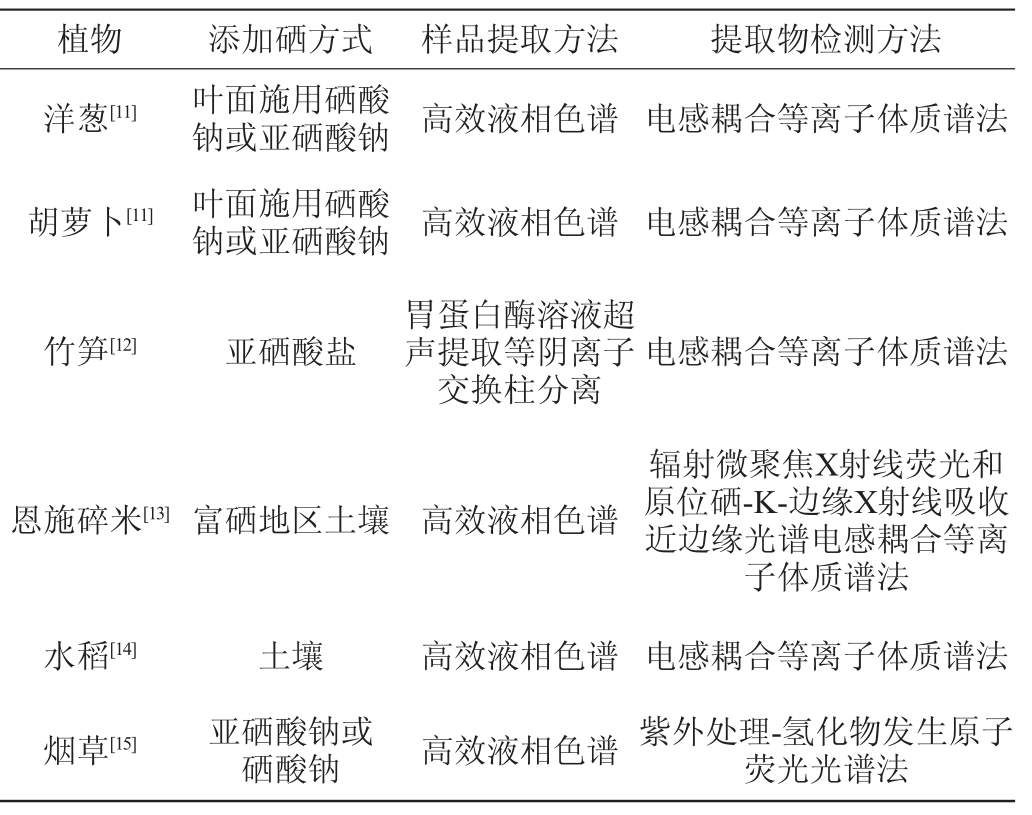
植物硒的主要来源是土壤中的硒。六价硒被吸收进入植物叶绿体细胞后在谷胱甘肽和5-磷硫酸腺苷(adenosine 5-phosphosulfate,APS)的作用下转化为四价硒,然后在植物叶绿体内经过半胱氨酸合成酶(cysteine synthase,CSase)的作用转化成硒代半胱氨酸[10]。植物中硒代半胱氨酸合成效率较低,应用于实际生产较为困难。不同植物来源的硒代半胱氨酸提取及检测方法见表1。
表1 不同植物来源的硒代半胱氨酸提取及检测方法
Table 1 Extraction and detection methods of selenocysteine from different plants
2.2 动物合成硒代半胱氨酸及检测提取方法
动物合成硒代半胱氨酸的途径与微生物合成硒代半胱氨酸途径相同,但动物体内硒的转化效率和硒代半胱氨酸合成效率较低,提取手段较为复杂。在哺乳动物中,比较基因组学和实验分析表明哺乳动物的硒代半胱氨酸合成酶(selenocysteine synthetase,Secs)是含吡咯磷酸盐(pyrrole phosphate)的蛋白质[16],被称为可溶性肝抗原。硒代半胱氨酸合成酶需要磷酸硒和膦酰-tRNA[Ser]Sec作为底物产硒代半胱氨酸-tRNA[Ser]Sec[17]。此外,在由硒化物、三磷酸腺苷(adenosine triphosphate,ATP)和丝氨酸组成的tRNA支架上,用tRNA[ser]sec、seryl-tRNA合成酶(seryl-tRNA synthetase)、膦酰-tRNA[Ser]SEC激酶(phosphonoy-tRNA[Ser]Sec kinase)、激酶磷酸硒合成酶、硒代半胱氨酸合成酶在tRNA支架上合成了硒代半胱氨酸[18]。不同动物来源的硒代半胱氨酸提取及检测方法见表2。
表2 不同动物来源的硒代半胱氨酸提取及检测方法
Table 2 Extraction and detection methods of selenocysteine from different animals

2.3 微生物合成硒代半胱氨酸

图1 酿酒酵母硫硒氨基酸生物合成途径
Fig.1 Biosynthesis of sulfur amino acid in Saccharomyces cerevisiae
CH2-THF:5,10-亚甲基四氢叶酸;CH3-THF:5-甲基四氢叶酸;SeMCys:硒甲基半胱氨酸;γ-glu-SeMCys:γ-谷氨酰-硒甲基-半胱氨酸;SAM:腺苷甲硫氨酸;SAHSeCys,同型腺苷半胱氨酸;GSH1,谷氨酰半胱氨酸合成酶,GSH2,谷胱甘肽合成酶。
硒酸盐在还原酶的作用下与氨基酸结合成硒代氨基酸再参与生物体代谢,主要生成硒蛋白和含硒酶类。硒与硫在微生物中的代谢途径和是相似的,均使用同一个丝氨酸代谢途径[25]。图1显示了硒进入微生物体内后的代谢和硒代蛋氨酸(selenomethionine,SeMet)转化为硒代半胱氨酸途径,以及硒代半胱氨酸合成硒代甲基半胱氨酸和谷胱甘肽途径。硒化氢(H2Se)与O-乙酰丝氨酸(O-acetyl serine,OAS)在同型半胱氨酸合成酶作用下合成同型硒半胱氨酸,在蛋氨酸合成酶作用下合成硒代蛋氨酸。同型硒半胱氨酸与丝氨酸在半胱氨酸-β-合成酶作用下生成硒代胱硫醚,然后在胱硫醚-γ-裂解酶(cystathionine-γ-lyase)的作用下生成硒代半胱氨酸(SeCys)。
硒代半胱氨酸的合成与selA、selB、selC、selD四个基因的产物相关[26]。SelC是一个特异性的硒代半胱氨酸-tRNASec,在进行翻译时,SelC会被氨酰化,在Seryl-tRNA合成酶催化完成反应,同动物硒代半胱氨酸合成途径相似,形成SertRNASec提供了基本的碳骨架来生成硒代半胱氨酸[27]。
2.4 常用硒代半胱氨酸检测方法优缺点比较
比色法、荧光分光光度法、氢化物-原子荧光法、火焰原子吸收法、氢化物-原子吸收法、石墨炉-原子吸收法、催化动力学光度法、高效液相色谱法和电感耦合等离子体质谱法[28]是常用测定总硒含量的方法。但上述方法并不能完全有效的检测硒代半胱氨酸,需对硒代半胱氨酸进行高效的分离提取,并与检测方法联用对硒代半胱氨酸进行测定。硒代半胱氨酸检测提取方法及优缺点见表3。
表3 硒代半胱氨酸检测方法优缺点
Table 3 Advantages and disadvantages of detection methods for selennocysteine

3 微生物发酵生产硒代半胱氨酸进展
动、植物生产硒代半胱氨酸成本高,且受季节、地域、气候的限制。而微生物生长速度快,原料经济廉价,便于培养,产出效率高,可通过控制培养条件提高产量,故利用微生物生产硒代半胱氨酸。
3.1 富硒菌种选育
硒代半胱氨酸的发酵生产需先选育出高耐硒性菌株。硒酸盐或亚硒酸盐作为添硒剂,均对菌种产生毒性并对菌体生长有抑制作用[29],要想得到具有高硒积累能力的菌株,其在生长过程中需表现出较高的抗硒盐能力[30],故选育菌种需有一定的耐硒性。筛选过程前需对菌种的富硒能力进行评估,选用富硒能力强的菌株作为实验菌株。菌种选育阶段首先需考虑抗性筛选过程,对样本菌种进行不同浓度硒的梯度培养,以达到初筛目的。微生物主要利用透性酶对硒吸收,已发现的细菌硫透性酶基因有cysA,cysU,cysW,以上基因发生突变将会提高硒的耐受性[31]。在此基础上对具有耐硒能力的菌种继续采用诱变育种的方式筛选。
富硒诱变育种通常采用紫外线照射或亚硝酸等诱变剂进行单因素诱变,王小波等[32]以富硒酵母Y2为出发菌株,通过60Coγ射线照射诱变育种,筛选获得一株生物量和富硒能力都较高的突变菌株YR166,进行富硒培养后硒含量达到2 531.4 μg/g,较原菌株提高74.2%,酵母生物量达到14.9 g/L,较原菌株提高36.7%。复合诱变相对于单因素诱变过程更为复杂,但可以更有针对性的培育菌种,达到更好的诱变效果。曾礼华等[33]以热带假丝酵母菌(Candida tropicalis)1254为出发菌株进行了亚硝基胍诱变和亚硒酸钠抗性筛选,紫外线诱变和乙硫氨酸抗性筛选等两轮突变和筛选,获得突变菌株1254-6-1,其生物量、总硒含量、有机硒的含量及转化率分别达到7.60 g/L、5 626.00 μg/g、4 879.99 μg/g、86.74%,分别为原始出发菌株的1.85倍、7.90倍、9.35倍、1.18倍。富硒复合诱变流程如下:硒盐抗性初筛→选出硒耐受性及富硒能力强的菌株→亚硝基胍诱变及硒盐抗性复筛→进一步筛选富硒能力强的菌株→紫外诱变及乙硫氨酸抗性筛选→富硒菌株。以上步骤筛选出的菌株一般具有良好的抗硒性。从中继续筛选硒代半胱氨酸产量高的菌株进行发酵优化。
3.2 硒代半胱氨酸发酵条件优化
通常有两种硒源在实验中被广泛使用,亚硒酸钠(Na2SeO3)和硒酸钠(Na2SeO4),对于两种不同价态的硒,硒代半胱氨酸产率也不同。两种硒盐对菌体的生长均有抑制作用,发酵培养过程中添加硒酸钠能提高有机硒的产量。因为亚硒酸钠不同于硒酸钠,可与还原糖(如葡萄糖)反应生成单质Se[34],而生物几乎无法利用单质Se。
发酵过程中,由于硒与硫在菌体吸收过程中的竞争关系,富硒过程中需控制硫与硒的比值发酵。MAPELLI V等[34]在高硫硒比和低硫硒比的情况下对酿酒酵母进行发酵,发现只有在缺硫的情况下硒才会被完全消耗,但由于硒盐对菌体的毒性,在缺硫条件下细胞会生长不良;在高硫硒比时,硒难以被菌体所吸收。合适的硫硒比在硒代半胱氨酸的发酵生产中尤为关键。酵母细胞在添加硒盐后会导致细胞尺寸减小[35],具体原因还有待研究。DHANJAL S等[36]发现随着硒盐浓度的增加,细菌细胞大小随之减小。细胞大小和数量的减少在细胞形态上可归因于高浓度有毒离子对生长细胞施加的胁迫。换而言之,单个细胞体积减小,它们的相对表面积更大,能更好地吸收环境胁迫条件下的营养物质。
发酵方式的选用对细胞营养吸收至关重要。补料分批发酵比其他发酵方式在调整营养物质浓度方面有更大的优势。将常用碳源葡萄糖的浓度维持在适当的水平,应用于补料分批培养,以控制葡萄糖效应,提高细胞密度[37]。发酵过程中对发酵参数如酵母细胞产率、发酵效率、有机硒生产率、产量和消耗率、生物量、底物和硒代半胱氨酸的浓度等进行测定。其他因素包括蒸发气体损失,pH值测定,消泡手段,生物量体积,样品的提取,这些都是影响酵母生长的因素[38]。
4 展望
本文探讨了硒代半胱氨酸的生物合成以及检测提取方法。植物、动物、微生物中均能合成硒代半胱氨酸,但植物、动物中产硒代半胱氨酸效率较低,微生物较二者更适合生产硒代半胱氨酸。介绍了硒代半胱氨酸多种检测提取方法。从菌种选育和发酵条件优化两方面概述微生物发酵生产硒代半胱氨酸方法。需注意以下几点:高耐硒性菌株的选育和诱变筛选方式选用,硒源、发酵方法的选取以及适当硫硒比对微生物产硒代半胱氨酸的影响。
微生物合成硒代半胱氨酸可以从以下几个方面拓展:(1)Sec常与其二聚体(Seenocystine,Sec2)混淆,易导致硒代半胱氨酸无法被准确的定性和定量,该问题是Sec检测方面值得深入研究内容。(2)在诱变育种基础上能够通过原生质体融合或基因工程的方法进一步提高菌种的耐硒性或是提高菌种产硒代半胱氨酸能力。(3)微生物利用硒代半胱氨酸产出相应高活性硒化物。硒代半胱氨酸可在γ-谷氨酰半胱氨酸合成酶酶的催化下,与谷氨酸可能发生反应生成谷氨酰硒半胱氨酸,然后在谷胱甘肽合成酶催化下该产物进一步与甘氨酸反应可能生成硒代谷胱甘肽。硒代谷胱甘肽(GSeH)是谷胱甘肽(glutathione,GSH)的硒类似物,氧化型硒代谷胱甘肽(selenoglutathione)是一种具有类似谷胱甘肽过氧化物酶(glutathione peroxidase,GPX)抗氧化能力的物质[39],其还原物硒代谷胱甘肽的抗氧化能力更强。
坚信随着社会发展和研究深入,人们将会科学认识和了解硒代半胱氨酸以及其衍生物,基于微生物发酵生产相应高活性抗癌硒化物将越来越受人们青睐,在食品、医疗等方面具有良好的经济效益和和社会效益。
[1]VARLAMOVA E G.The role of selenium and selenocysteine-containing proteins in the mammalian male reproductive system[J].Biophysics,2016,61(4):580-584.
[2]JOHANSSON L,GAFVELIN G,ARNER E.Selenocysteine in proteinsproperties and biotechnological use[J].Biochim Biophys Acta,2005,1726(1):1-13.
[3]刘建群,刘芳,张小平,等.硒-甲基硒代半胱氨酸的合成与拆分研究[J].化学研究与应用,2008,20(11):1498-1501.
[4]LEONARD J L,LEONARD D M,SHEN Q,et al.Selenium-regulated translation control of heterologous gene expression:normal function of selenocysteine-substituted gene products[J].J Cellu Biochem,1996,61(3):410-419.
[5]BECK A,FORCHHAMMER K,HEIDER J,et al.Selenocysteine:the 21st amino acid[J].Mol Microbiol,2010,5(3):515-520.
[6]HOLBEN D H,SMITH A M.The diverse role of selenium within selenoproteins:a review[J].J Am Diet Associat,1999,99(7):836-843.
[7]姚昭,张小平,邓泽元,等.L-硒甲基硒代半胱氨酸的化学合成方法代谢途径及其生物活性的研究进展[J].农产品加工(学刊),2012(11):122-125.
[8]AUGUST B.Selenium proteins containing selenocysteine[M]//Encyclopedia of inorganic and bioinorganic chemistry.John Wiley&Sons,Ltd,2012.
[9]SUPPMANN S,PERSSON B C,BECK A.Dynamics and efficiency in vivo of UGA-directed selenocysteine insertion at the ribosome[J].Embo J,2014,18(8):2284-2293.
[10]SOUZA M P,DE,LYTLE C M,MULHOLLAND M M,et al.Selenium assimilation and volatilization from dimethylselenoniopropionate by Indian mustard[J].Plant Physiol,2000,122(4):1281-1288.
[11]K POLNA E,LAURSEN K H,HUSTED S,et al.Bio-fortification and isotopic labelling of Se metabolites in onions and carrots following foliar application of Se and Se[J].Food Chem,2012,133(3):650-657.
[12]NI Z,LIU Y,QU M.Determination of 5 natural selenium species in selenium-enriched bamboo shoots using LC-ICP-MS[J].Food Sci Biotechnol,2014,23(4):1049-1053.
[13]CUI L,ZHAO J,CHEN J,et al.Translocation and transformation of selenium in hyperaccumulator plant Cardamine enshiensis from Enshi,Hubei,China[J].Plant Soil,2018,1:1-12.
[14]SUN G X,LIU X,WILLIAMS P N,et al.Distribution and translocation of selenium from soil to grain and its speciation in paddy rice(Oryza sativa L.)[J].Environ Sci Technol,2010,44(17):6706-6011.
[15]HAN D,LI X,XIONG S,et al.Selenium uptake,speciation and stressed response of Nicotiana tabacum L[J].Environ Exp Botany,2013,95:6-14.
[16]LOBANOV A V,HATFIELD D L,GLADYSHEV V N.Reduced reliance on the trace element selenium during evolution of mammals[J].Genome Biol,2008,9(3):R62.
[17]程天德,吴永尧.硒蛋白的生物合成与调控[J].生命的化学,2004,24(5):394-396.
[18]XU X M,CARLSON B A,MIX H,et al.Biosynthesis of selenocysteine on its tRNA in eukaryotes[J].PLoS Biol,2006,5(1):e4.
[19]SELE V,ØRNSRUD R,SLOTH J J,et al.Selenium and selenium species in feeds and muscle tissue of Atlantic salmon[J].J Trace Element Med Biol,2018,47:124-133.
[20]GODIN S,FONTAGN-DICHARRY S,BUENO M,et al.Influence of dietary selenium species on selenoamino acid levels in rainbow trout[J].J Agr Food Chem,2017,63(28):6484-6492.
[21]BRIENS M,MERCIER Y,ROUFFINEAU F,Comparative study of a new organic selenium source v.seleno-yeast and mineral selenium sources on muscle selenium enrichment and selenium digestibility in broiler chickens[J].Brit J Nutr,2013,110(4):617-624.
[22]CALAMARI L,PETRERA F,BERTIN G.Effects of either sodium selenite or Se yeast(Sc CNCM I-3060)supplementation on selenium status and milk characteristics in dairy cows[J].Livest Sci,2010,128(1-3):154-165.
[23]JEONG J S,LEE J,PAK Y N.Quantitative speciation of selenium in human blood serum and urine with AE-RP-and AF-HPLC-ICP/MS[J].Bull Korean Chem Soc,2013,34(12):3817-3124.
[24]JUNIPER D T,PHIPPS R H,RAMOS-MORALES E,et al.Effect of high dose selenium enriched yeast diets on the distribution of total selenium and selenium species within lamb tissues[J].Livest Sci,2009,122(1):63-67.
[25]CHEN D M,NIGAM S N,MCCONNELL W B.Biosynthesis of Se-methylselenocysteine and S-methylcysteine in Astragalus bisulcatus[J].Canad J Biochem,1970,48(11):1278-1283.
[26]STOLZ J F,BASU P,SANTINI J M,et al.Arsenic and selenium in microbial metabolism[J].Ann Rev Microbiol,2006,60(1):107-130.
[27]LIONEL R,CLAIRE P C,SYLVIE N,et al.Methylation of inorganic and organic selenium by the bacterial thiopurine methyltransferase[J].J Bacteriol,2002,184(11):3146-3149.
[28]王复龙,彭增起,王蓉蓉,等.动物可食用组织中硒的形态研究进展[J].肉类研究,2011,25(4):57-60.
[29]LETAVAYOV L,VLAS KOV D,SPALLHOLZ J E,et al.Toxicity and mutagenicity of selenium compounds in Saccharomyces cerevisiae[J].Mutat Res,2008,638(1):1-10.
[30]YOSHINAGA M,HOW S,BLANCO D,et al.Directed evolution of Saccharomyces cerevisiae for increased selenium accumulation[J].Microorganisms,2018,6(3):81.
[31]杜玉潇,李亚男,陈大清.植物硒代谢积累及相关酶的研究进展[J].热带亚热带植物学报,2007,15(3):269-276.
[32]王小波,柳乐,李学如.高富硒酵母菌种选育研究[J].食品与发酵科技,2011,47(5):6-9.
[33]曾礼华,马平美,李维,等.高富硒酵母菌诱变选育研究[J].食品与生物技术学报,2013,32(10):1085-1090.
[34]MAPELLI V,HILLESTR M P R,K POLNA E,et al.Metabolic and bioprocess engineering for production of selenized yeast with increased content of seleno-methylselenocysteine[J].Metab Eng,2011,13(3):282-293.
[35]RAJASHREE K,MUTHUKUMAR T.Preparation of organic selenium yeast by fed-batch fermentation[J].Int J Food Ferment Technol,2013,3(2):135.
[36]DHANJAL S,CAMEOTRA S S.Aerobic biogenesis of selenium nanospheres by Bacillus cereus isolated from coalmine soil[J].Microbial Cell Factories,2010,9(1):52-60.
[37]GHAHREMANI H,PISHVAIE M R,VOSSOUGHI M,et al.Optimization of a fed-batch fermenter producing baker's yeast using simulated annealing method[J].Ira J Biotechnol,2009,7(3):157-165,191.
[38]WALTER B.Calculation of fermentation parameters from the results of a fed-batch test taking account of the volume of biomass in the fermenting medium[J].Brazil Arch Biol Technol,2008,51(3):441-446.
[39]SHIMODAIRA S,ASANO Y,ARAI K,et al.Selenoglutathione diselenide:unique redox reactions in the GPx-like catalytic cycle and repairing of disulfide bonds in scrambled protein[J].Biochemistry,2017,56(42):5644-5653.