Fe和Zn都是人体必需的微量元素[1],众所周知,长期缺Fe或Zn对人体健康具有较大的危害[2]。猪肝系列产品中含有丰富的Fe和Zn,之前的研究以测定Fe和Zn总量为主,对其形态分析较少[3]。相关研究报告表明[4-7],人体对微量元素的吸收与其形态密切相关,与无机态相比,有机态的金属元素更易被人体吸收。近年来,随着对微量元素研究的深入,已有一些形态分析研究报道,MEI T等[8]利用高效液相色谱-电感耦合等离子体质谱联用技术发现,金针菇水溶性蛋白中至少含有6种含硒蛋白,约占总可溶性硒的7.0%;李红卫等[9]利用4-氯-3,5-二硝基三氟甲苯柱前衍生,建立高效液相色谱法测定富硒米曲霉中有机硒形态的分析方法,取得了良好的效果。
实验动物模型可以较好的模拟人体消化和吸收的过程,但其成本高、耗时、耗力。本实验以实验室研制的猪肝酱为研究对象,采用体外全仿生消化(含消化酶)技术[10-13]模拟猪肝酱在胃、肠中消化,依据化学仿生(人工胃、肠)与医学仿生(酶的作用)原理,模拟猪肝酱经胃肠环境的转运机制,研究胃、肠所含的无机物、有机物及消化酶对猪肝酱中Fe、Zn形态和生物可给性的影响。利用0.45 μm微孔滤膜分离悬浮态和可溶态,通过D101大孔树脂实现无机态和有机态的分离。微波消解后使用高分辨-连续光源原子吸收光谱(high resolution-continuum source atomic absorption spectrometry,HR-CS AAS)仪[14-18]测定各形态Fe和Zn的含量,为科学补充Fe和Zn提供基础数据。
1 材料与方法
1.1 材料与试剂
猪肝酱:实验室研制产品。
粘液素、牛血清白蛋白、黏蛋白、胰液素、淀粉酶、脂肪酶(均为生化试剂):上海源叶生物科技有限公司;KCl、KSCN、NaH2PO4、Na3PO4、NaCl、NaOH、CaCl2、NH4Cl、NaHCO3、KH2PO4、MgCl2(均为分析纯):国药集团化学试剂有限公司。
1.2 仪器与设备
ContrAA 700高分辨-连续光源原子吸收光谱仪(简称HR-CS AAS):德国Analytik Jena公司;XT-9900型智能微波消解仪、XT-9800多用预处理加热仪:上海新拓微波溶样测试技术有限公司;CascadaTM实验室超纯水系统:美国Pall公司;3-30K台式高速冷冻离心机:德国Sigma公司;L550台式低速离心机:湖南湘仪实验室仪器开发有限公司。
1.3 方法
1.3.1 猪肝酱制作工艺流程[19-21]

腌制:将沥水后的猪肝和五花肉加入香料,滚揉腌制30 min。腌制配比:猪肝100 g,五花肉10 g,料酒3 g,葱1 g,姜3 g,蒜3 g,白砂糖2 g。
炒制:将20 g植物油和5 g猪油加入锅中,加热后加入蒜末和姜末,出味后依次加入五香粉、盐、味精、淀粉、糊精等进行炒制,炒制时间为3 min。
炒制配方:猪肝100 g,五花肉10 g,蒜3.75 g,姜3.75 g,五香粉1 g,盐3.75 g,味精0.5 g,淀粉3.5 g,糊精7 g,亚硝酸钠1.2 g,复合磷酸盐1 g。
脱气:将斩拌好的样品真空滚揉10 min。
杀菌:将灌装好的猪肝酱121 ℃杀菌60 min。
1.3.2 仪器工作参数
HR-CS AAS(火焰法)测定Fe和Zn的工作参数见表1。同时进行乙炔流量和燃烧器高度的优化。
表1 HR-CS AAS工作参数
Table 1 Working parameters of HR-CS FAAS

1.3.3 样品前处理及其Fe和Zn的测定
参考文献[1],采用微波消解处理猪肝酱及其胃、肠消化后的样品,根据Fe和Zn的实际浓度,进行适当稀释,最后再使用HR-CS AAS按表1的工作参数测定Fe和Zn。
1.3.4 消化液的制备
参考文献[22],分别加入唾液、胃液、十二指肠液和胆汁中所含的有机物和无机物,利用HCl和NaHCO3调节pH值,再用超纯水定容至500 mL,置于4 ℃冷藏保存备用,使用前在此基础上分别加入相应的消化酶。
1.3.5 模拟猪肝酱在胃中消化
在50.0 g猪肝酱中添加5.00 mL唾液,混匀后在37 ℃、60 r/min条件下恒温振荡5 min后;再添加75.0 mL胃液,混匀后在37 ℃、60 r/min条件下恒温振荡2 h[22];结束后将样品转移至适当离心管中,通过离心实现固液分离,称量上清液(猪肝酱胃全仿生消化液)质量。
1.3.6 模拟猪肝酱在肠中消化
在50.0 g猪肝酱中添加5.00 mL唾液,混匀后在37 ℃、60 r/min条件下恒温振荡5 min后;添加75.0 mL胃液,混匀后在37 ℃、60 r/min条件下恒温振荡2 h;再添加100.0 mL十二指肠液和40.0 mL胆汁,混匀后在37 ℃、60 r/min条件下恒温振荡7 h;结束后将样品转移至适当离心管中,通过离心实现固液分离,称量上清液(猪肝酱肠全仿生消化液)质量。
1.3.7 悬浮态与可溶态的分离和测定
将一定质量的猪肝酱胃全仿生消化液转移至适当离心管中,通过高速离心实现固液分离,再将上清液通过0.45 μm滤膜,悬浮态将被滤膜截留下来,通过的为可溶态[1],并称其质量。再按1.3.3方法对可溶态样品进行处理和测定。按同样的方法处理猪肝酱肠全仿生消化液。
悬浮态Fe(或Zn)=Fe(或Zn)总量-可溶态Fe(或Zn)
1.3.8 无机态与有机态的分离和测定
参考文献[22],处理D101大孔吸附树脂,将一定质量的可溶态溶液通过树脂,用体积分数1%的HNO3按一定流速洗涤树脂,再按1.3.3方法对洗脱液样品进行处理和测定,洗脱液样品中Fe和Zn为无机态。
有机态Fe(或Zn)=可溶态Fe(或Zn)-无机态Fe(或Zn)
1.3.9 Fe(或Zn)生物可给性的计算
模拟猪肝酱在胃、肠中消化,Fe(或Zn)生物可给性的计算公式如下:
式中:BA为Fe(或Zn)的生物可给性,%;TK为胃、肠消化液中可溶态Fe(或Zn)含量,μg/g;TZ为猪肝酱中Fe(或Zn)总量,μg/g。
2 结果与分析
2.1 测定参数的优化
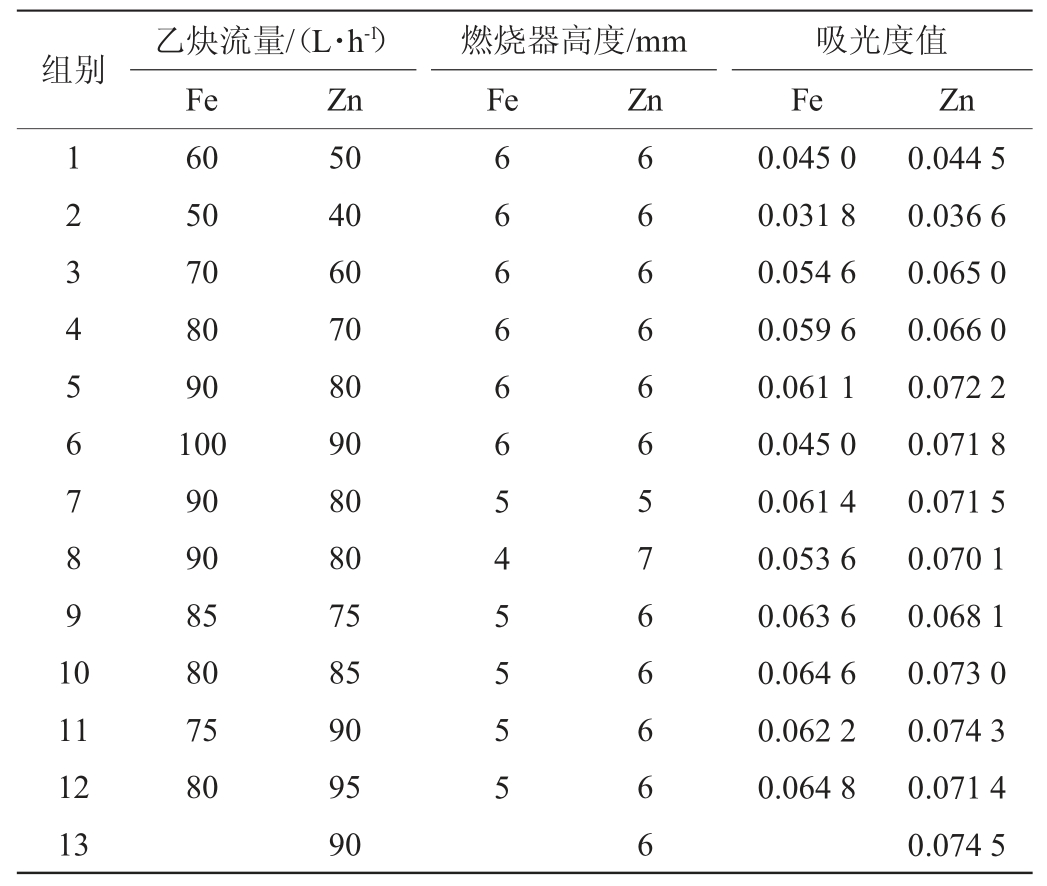
使用HR-CS AAS测定Fe和Zn时,利用仪器自带优化功能对不同测定参数进行优化,优化结果见表2。
由表2可知,HR-CS AAS测定Fe的最佳参数为乙炔流量80 L/h,燃烧器高度5 mm;测定Zn的最佳参数为乙炔流量90 L/h,燃烧器高度6 mm。
表2 测定参数的优化
Table 2 Optimization of determination parameters
2.2 标准工作曲线的绘制
使用HR-CS AAS测定不同浓度的Fe标准溶液,吸光度值以A表示,Fe标准溶液浓度以c表示,经仪器自带软件绘制,得Fe回归方程为A1=(-0.001 375 2+0.025 587 4×c1)/(1+0.019 396 3×c1),相关系数R2为0.999 5;同理,得Zn回归方程为A2=(-0.018 503+0.131 201 5×c2)/(1+0.128 793 8×c2),相关系数R2为0.999 1;Fe和Zn标准工作曲线的相关系数R2均≥0.999,这表明浓度与吸光度值有良好的关系。
2.3 加标回收率
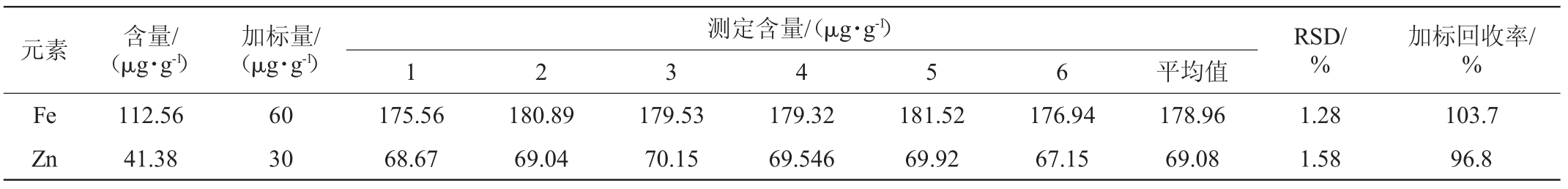
将一定量Fe、Zn标准溶液和猪肝酱样品一起置于微波消解罐中进行微波消解,按1.3.3方法进行处理和测定,重复6次,计算加标回收率[23],结果见表3。
由表3可知,Fe平均加标回收率为103.7%,相对标准偏差(relative standard deviation,RSD)=1.28%;Zn平均加标回收率为96.8%,RSD=1.58%。这表明按1.3.3方法进行处理和测定,结果准确可靠。
表3 加标回收率测定结果
Table 3 Results of adding standard recoveries
2.4 消化液中Fe的形态分析
胃、肠消化后猪肝酱中Fe的形态分析,结果见表4。
由表4可知,猪肝酱含有丰富的Fe,达(112.56±3.13)μg/g;消化前猪肝酱中可溶态Fe为(9.21±0.40)μg/g,占总量的8.18%,其中有机态Fe占总量的1.75%,Fe的生物可给性为8.18%;猪肝酱在模拟胃中消化后可溶态Fe为(21.24±0.52)μg/g,占总量的18.87%,其中有机态Fe占总量的8.02%,Fe的生物可给性为18.87%;猪肝酱在模拟肠中消化后可溶态Fe为(29.22±0.76)μg/g,占总量的25.96%,其中有机态Fe占总量的13.42%,Fe的生物可给性为25.96%。
表4 消化液中Fe的形态分析
Table 4 Speciation analysis of Fe in digestive juice
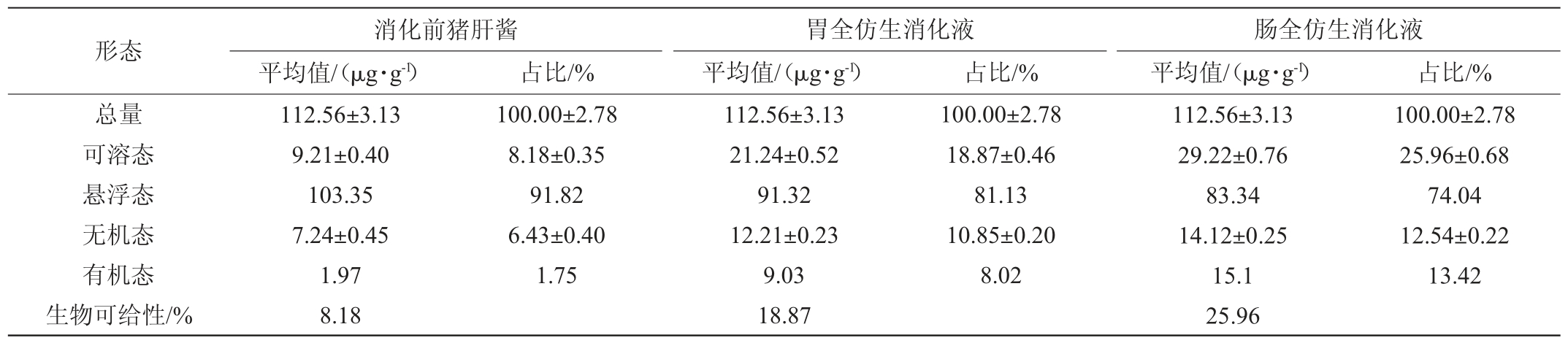
相比消化前,胃消化后除悬浮态Fe,其他各形态Fe的含量都所有增加,生物可给性变大;相比胃消化,肠消化后除悬浮态Fe,其他各形态Fe的含量都所有增加,生物可给性变大;这表明胃、肠消化都是将一部分悬浮态Fe消化成可溶态Fe,其中以有机态Fe为主,有利于人体吸收。
2.5 消化液中Zn的形态分析
胃、肠消化后猪肝酱中Zn的形态分析,结果见表5。
由表5可知,猪肝酱含有丰富的Zn,达(41.38±1.14)μg/g;消化前猪肝酱中可溶态Zn为(8.13±0.36)μg/g,占总量的19.65%,其中有机态Zn占总量的1.81%,Zn的生物可给性为19.65%;猪肝酱在模拟胃中消化后可溶态Zn为(12.48±0.32)μg/g,占总量的30.16%,其中有机态Zn占总量的7.85%,Zn的生物可给性为30.16%;猪肝酱在模拟肠中消化后可溶态Zn为(18.48±0.49)μg/g,占总量的44.66%,其中有机态Zn占总量的16.09%,Zn的生物可给性为44.66%。
相比消化前,胃消化后除悬浮态Zn,其他各形态Zn的含量都所有增加,生物可给性变大;相比胃消化,肠消化后除悬浮态Zn,其他各形态Zn的含量都所有增加,生物可给性变大;这表明胃、肠消化都是将一部分悬浮态Zn消化成可溶态Zn,其中以有机态Zn为主,有利于人体吸收。
表5 消化液中Zn的形态分析
Table 5 Speciation analysis of Zn in digestive juice

3 结论
通过单因素试验,确定Fe最佳测定条件:乙炔流量为80 L/h,燃烧器高度为5 mm;Zn最佳测定条件:乙炔流量为90 L/h,燃烧器高度为6 mm。在此条件下,测定猪肝酱中Fe含量为112.56 μg/g,Zn含量为41.38 μg/g。胃、肠消化后除悬浮态Fe和Zn,其他各形态Fe和Zn的含量都有所增加,生物可给性变大,这表明胃、肠消化都是将一部分悬浮态Fe和Zn消化成可溶态Fe和Zn,其中以有机态Fe和Zn为主。
[1]陈安徽,陈尚龙,巫永华,等.黄精酵素口服液中钙、铁和锌的形态分析[J].现代食品科技,2016,32(1):272-277.
[2]张滨,马美湖.金属螯合亲合层析(MCAC)分离血红素肽-铁及功能活性研究[J].中国食品学报,2010,10(2):60-66.
[3]GÓMEZNIETO B,GISMERA M J,SEVILLA M T,et al.Determination of essential elements in beverages,herbal infusions and dietary supplements using a new straightforward sequential approach based on flame atomic absorption spectrometry[J].Food Chem,2017,219:69-75.
[4]POHL P,STELMACH E,SZYMCZYCHA-MADEJA A.Simplified sample treatment for the determination of total concentrations and chemical fractionation forms of Ca,Fe,Mg and Mn in soluble coffees[J].Food Chem,2014,163(20):31-36.
[5]MAO G H,REN Y,LI Q,et al.Anti-tumor and immunomodulatory activity of selenium(Se)-polysaccharide from Se-enriched Grifola frondosa[J].Int J Biol Macromol,2016,82:607-613.
[6]BARBOSA U A,PEÑA-VAZQUEZ E,BARCIELA-ALONSO M C,et al.Simultaneousdetermination and speciation analysisofarsenic and chromium in iron supplements used for iron-deficiency anemia treatment by HPLCICP-MS[J].Talanta,2017,170:523-529.
[7]高淑云.火焰原子吸收法测定牛蒡中元素含量[J].徐州工程学院学报(社会科学版),2007,22(6):32-35.
[8]MEI T,LI B,SUN T,et al.HPLC-ICP-MS speciation of selenium in Se-cultivated Flammulina velutipes[J].Arab J Chem,2017,219:69-75.
[9]李红卫,王开萍,吴娱,等.柱前衍生-反相高效液相色谱法检测富硒米曲霉中有机硒形态[J].食品科学,2015,36(22):137-141.
[10]WU P,BHATTARAI R R,DHITAL S,et al.In vitro,digestion of pectinand mango-enriched diets using a dynamic rat stomach-duodenum model[J].J Food Eng,2017,202:65-78.
[11]SUN L,LIU G,YANG M,et al.Bioaccessibility of cadmium in fresh and cooked Agaricus blazei Murill assessed by in vitro,biomimetic digestion system[J].Food Chem Toxicol,2012,50(5):1729-1733.
[12]LI S X,LIN L X,ZHENG F Y,et al.Metal bioavailability and risk assessment from edible brown alga Laminaria japonica,using biomimetic digestion and absorption system and determination by ICP-MS[J].J Agr Food Chem,2011,59(3):822-828.
[13]WAGH P,PARUNGAO G,VIOLA R E,et al.A new technique to fabricate high-performance biologically inspired membranes for water treatment[J].Sep Purif Technol,2015,156(2):754-765.
[14]PERONICO V C D,RAPOSO J L.Ultrasound-assisted extraction for the determination of Cu,Mn,Ca,and Mg in alternative oilseed crops using flame atomic absorption spectrometry[J].Food Chem,2016,196:1287-1292.
[15]OZBEK N,BAYSAL A.A new approach for the determination of sulphur in food samples by high-resolution continuum source flame atomic absorption spectrometer[J].Food Chem,2015,168:460-463.
[16]PAZ-RODRÍGUEZ B,ABOAL-SOMOZA M,BERMEJO-BARRERA P.Application of high resolution-continuum source flame atomic absorption spectrometry(HR-CS FAAS):determination of trace elements in tea and tisanes[J].Food Chem,2015,170:492-500.
[17]BAYSAL A,AKMAN S.A practical method for the determination of sulphur in coal samples by high-resolution continuum source flame atomic absorption spectrometry[J].Talanta,2011,85(5):2662-2665.
[18]宋慧,陈尚龙,李超,等.火焰原子吸收光谱法测定牛奶中不同化学形态的钙[J].食品科学,2012,33(22):278-281.
[19]崔瑞颖,张志胜,任慧,等.猪肝酱加工工艺的优化[J].食品工业,2013,34(6):11-13.
[20]余静,王卫,张佳敏.猪肝调味酱加工工艺优化[J].成都大学学报(自然科学版),2017,36(3):247-251.
[21]李银塔,陈英乡,位正鹏,等.猪肝酱的加工工艺研究[J].肉类工业,2010(12):26-28.
[22]陈尚龙,刘恩岐,陈安徽,等.应用体外全仿生模型初步分析2 种富硒产品中硒形态及生物可给性[J].食品科学,2018,39(4):225-232.
[23]赵欣,杨庆文,韩建欣,等.微波消解-原子吸收光谱法测定山西老陈醋中微量元素[J].中国酿造,2017,36(3):165-169.