牛肝菌(Boletus)是一种药、食兼用的野生珍稀食用菌。它富含多糖、多酚、多种维生素、氨基酸、蛋白质等人体需要的营养物质,具有降血脂、抗肿瘤、改善免疫系统、抗氧化等功效[1-5]。
当前牛肝菌为我国菌类产品出口创汇作出了重要贡献,并且牛肝菌作为一种未被完全开发的高营养的美味食用菌类,对其药用及营养价值的研究将对更深一步开发牛肝菌资源有着十分重要的理论意义。近年来,牛肝菌的研究主要集中在其的营养成分含量[6-8]、多糖的提取工艺[9-10]及抗氧化作用[11]。常用的提取多糖方法有热水浸提法、微波提取法、泡沫分离法等[12-14]。目前报道较多的是热水浸提法,微波提取牛肝菌多糖的相关研究鲜见报道。
本试验通过单因素和正交试验优化云南牛肝菌多糖提取工艺,并利用1,1二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)法和羟基自由基(·OH)清除能力测定法对其抗氧化性进行了测定[15-16]。以期为牛肝菌食物资源的开发和综合利用提供参考依据。
1 材料与试剂
1.1 材料与试剂
牛肝菌粉末:云南;无水氯化钙、乙醇、葡萄糖、苯酚(重蒸馏)、硫酸、3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)、DPPH(均为分析纯):国药集团化学试剂有限公司。
1.2 仪器与设备
KQ-250E超声波清洗器:昆山市超声仪有限公司;TDL-4低速离心机:福州精仪仪器有限公司;GZX-GF101-3-BS-Ⅱ电热恒温鼓风干燥机:上海跃进医疗器械有限公司;T22SP分光光度计:上海棱光仪器有限公司;BSA224S电子天平:赛多利斯科学仪器(北京)有限公司。
1.3 试验方法
1.3.1 牛肝菌粗多糖的提取方法
称取一定量牛肝菌子实体粉末,以水为提取液,按一定的料液比,在一定温度条件下超声一定时间后,4 000 r/min离心10 min,收集上清液;上清液用氯化钙法去除蛋白[17-18],4 000 r/min离心10 min,收集上清液;上清液进行旋转蒸发浓缩至原来体积的1/3,加入4倍体积体积分数95%的乙醇过夜沉淀;4 000 r/min离心10 min,收集沉淀,沉淀于60 ℃干燥得牛肝菌粗多糖。
1.3.2 牛肝菌粗多糖提取工艺优化单因素试验
料液比对牛肝菌粗多糖提取的影响:称取2 g牛肝菌粉末,控制超声时间为1 h、超声温度为60 ℃、超声波功率为400 W,分别在不同料液比(1∶15、1∶20、1∶25、1∶30、1∶35(g∶mL))条件下进行超声波浸提试验,考察牛肝菌多糖在不同料液比条件的提取效果。
超声时间对牛肝菌粗多糖提取的影响:称取牛肝菌粉末2 g,料液比为1∶20(g∶mL),在超声温度为60 ℃、超声功率为400 W的条件下,超声不同时间(0.5 h、1.0 h、1.5 h、2.0 h、2.5 h),考察牛肝菌多糖在不同超声时间下的提取效果。
超声温度对牛肝菌粗多糖提取的影响:称取牛肝菌粉末2 g,料液比为1∶20(g∶mL),超声时间为0.5 h,超声功率为400 W的条件下,在不同超声温度(40 ℃、50 ℃、60 ℃、70 ℃、80 ℃)条件下进行超声,考察牛肝菌多糖在不同超声温度条件下的提取效果。
1.3.3 牛肝菌粗多糖提取工艺优化正交试验
在单因素试验的基础上,选取料液比、超声时间和超声温度3个因素,每个因素3个水平进行L9(33)正交试验,优化超声浸提过程的工艺条件。正交试验因素与水平设计见表1。
表1 牛肝菌粗多糖提取条件优化正交试验因素与水平
Table 1 Factors and levels of orthogonal tests for crude polysaccharide extraction conditions optimization from Boletus

1.3.4 测定方法
牛肝菌多糖含量:采用苯酚-硫酸法[19-20]进行测定。多糖得率计算公式如下:
1.3.5 牛肝菌粗多糖抗氧化性的测定
(1)DPPH自由基(DPPH·)清除能力:参照参考文献[21-22]的方法进行测定。
取不同质量浓度(0.2 mg/mL、0.4 mg/mL、0.6 mg/mL、0.8 mg/mL、1.0 mg/mL、1.2 mg/mL)的牛肝菌多糖溶液2 mL;添加2 mL DPPH溶液(0.2 mmol/L),振荡摇匀后,暗处、室温条件下静置30 min,在波长517 nm处测其吸光度值(A1),同时以2 mL不同浓度的多糖与2 mL无水乙醇混匀后,在波长517 nm处测得吸光度值(A2);以无水乙醇为空白,测得吸光度值(A0);以不同质量浓度(0.02 mg/mL、0.04 mg/mL、0.06 mg/mL、0.08 mg/mL、0.1 mg/mL、0.15 mg/mL、0.2 mg/mL)的抗坏血酸(vitamin C,VC)水溶液为对照。每个样品溶液进行3个平行。清除率按公式(1)计算。
(2)·OH清除率:参照参考文献[23-24]的方法进行测定。
取不同质量浓度(2mg/mL、4mg/mL、6mg/mL、8mg/mL、10 mg/mL)的牛肝菌多糖溶液1 mL于试管中,加入1 mL硫酸亚铁溶液(9 mmol/L)和1 mL水杨酸乙醇溶液(9 mmol/L),再加入1 mL的H2O2溶液(8.8 mmol/L),37 ℃水浴中反应30 min后,6 000 r/min离心10 min,在波长510 nm处测定吸光度值(A1),同时以蒸馏水代替H2O2溶液,其他条件不变,测定吸光度值(A2);以不加多糖的蒸馏水为空白组,测定吸光度值(A0);以不同质量浓度(0.05 mg/mL、0.10 mg/mL、0.15mg/mL、0.20mg/mL、0.25mg/mL、0.30mg/mL、0.40mg/mL)的抗坏血酸(VC)水溶液为对照。每个样品溶液进行3个平行。清除率按公式(2)计算。
2 结果与分析
2.1 牛肝菌粗多糖提取工艺单因素试验结果
2.1.1 料液比对牛肝菌多糖提取效果的影响
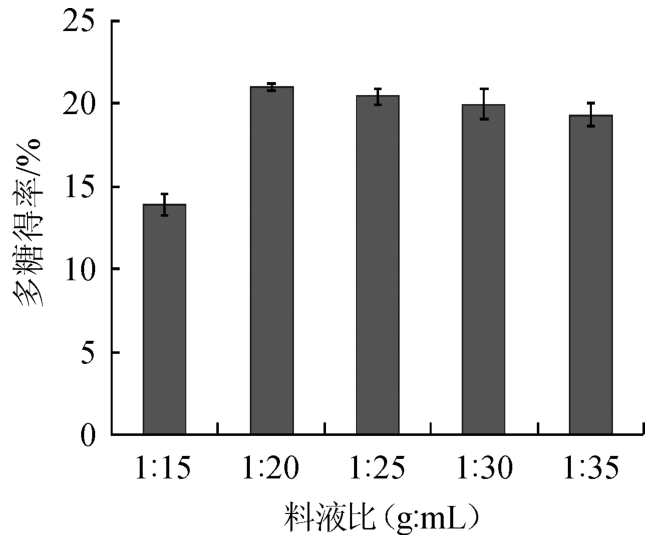
图1 料液比对牛肝菌多糖得率的影响
Fig.1 Effect of material to liquid ratio on polysaccharide yield from Boletus
由图1可见,牛肝菌多糖得率随着料液比中用水量的增大而逐渐增加,当料液比为1∶20(g∶mL)时,多糖得率最高,为21%;而料液比为1∶25~1∶35(g∶mL)时,多糖得率反而有所降低,说明适宜的料液比有利于多糖的浸出,料液比过低,多糖浸出不完全,导致多糖得率较低,料液比过高,不利于后期的蒸馏浓缩。因此,选择最适料液比为1∶20(g∶mL)。
2.1.2 超声时间对牛肝菌多糖提取效果的影响
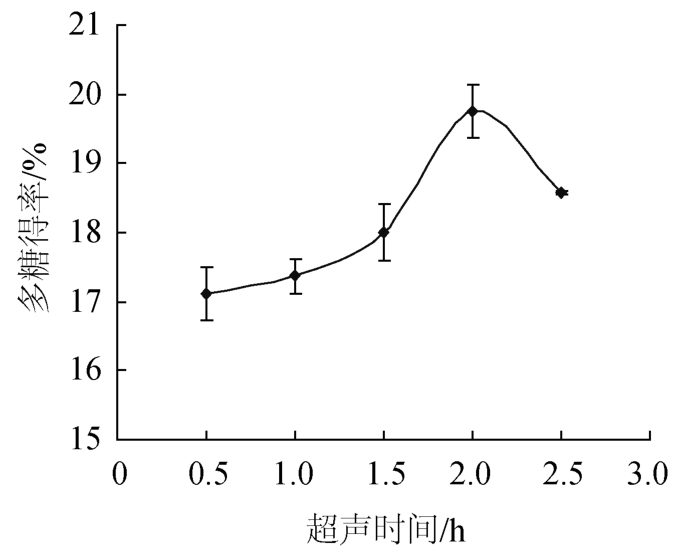
图2 超声时间对牛肝菌多糖得率的影响
Fig.2 Effect of ultrasonic time on polysaccharide yield from Boletus
由图2可见,牛肝菌多糖得率随着超声时间的延长呈先增后降的趋势。在超声时间为0.5~2.0 h时,随着超声时间的延长,多糖得率逐渐增大;当超声时间为2.0 h时,多糖得率达到最大值,为19.76%;之后,牛肝菌多糖得率随着超声时间的延长逐渐降低。这可能是由于超声波的机械剪切作用过度,导致部分多糖被降解,从而使多糖得率下降[11]。因此,选择最适超声时间为2.0 h。
2.1.3 超声温度对牛肝菌多糖提取效果的影响

图3 超声温度对多糖得率的影响
Fig.3 Effect of ultrasonic temperature on polysaccharide yield from Boletus
由图3可见,多糖的提取率随着超声温度的升高呈先增后降的趋势。当超声温度为40~60 ℃时,多糖得率随温度的升高急速上升;当超声温度达到60 ℃,牛肝菌的多糖得率最高,可达21.17%;之后,多糖得率逐渐下降。这是因为随着浸提温度的升高,液体介质的表面张力和黏度降低,使细胞内破坏程度增大,这促进了细胞内部物质溶出,从而使得多糖得率增加[12];但是太高的超声温度会使蛋白质发生变性,反而不利于细胞内糖蛋白的溶出。因此,选择最适超声温度为60℃。
2.2 牛肝菌多糖提取的正交设计试验
表2 牛肝菌粗多糖提取条件优化正交试验结果与分析
Table 2 Results and analysis of orthogonal tests for extraction conditions optimization of polysaccharide from Boletus
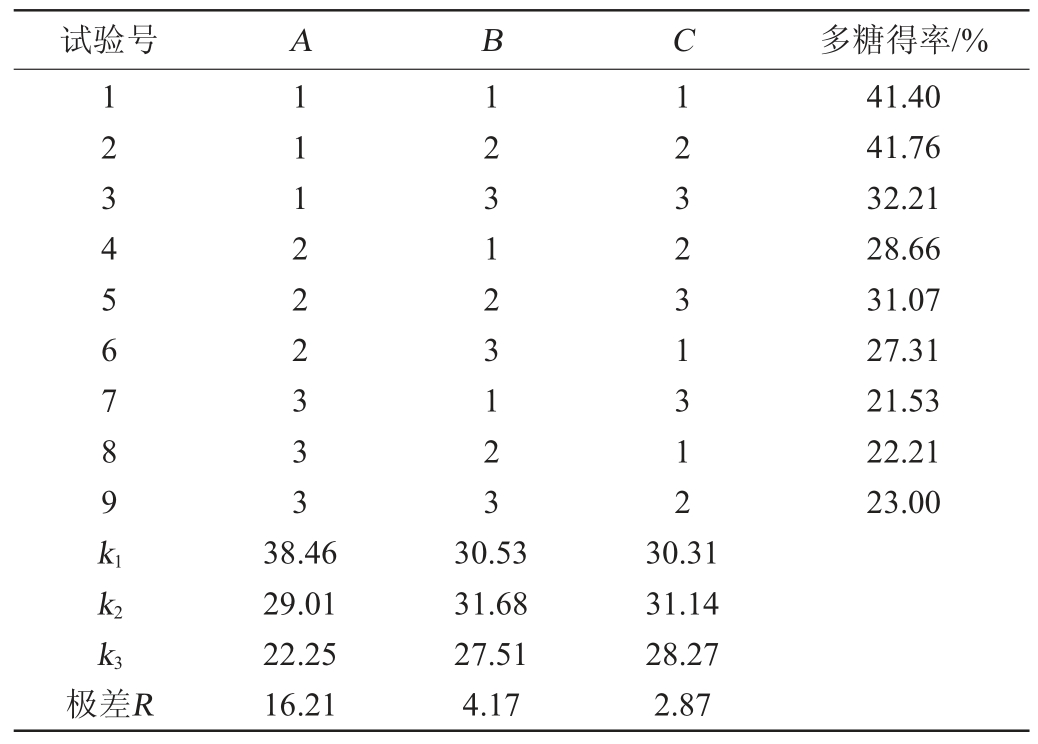
由表2可知,牛肝菌粗多糖得率受各因素影响的次序为A>B>C,即料液比对粗多糖得率的影响最大,超声温度次之,超声时间最小。最佳工艺组合为A1B2C2,即料液比为1∶15(g∶mL),超声时间为2 h,超声温度为60 ℃,在此条件下,牛肝菌的多糖得率为41.76%。
2.3 牛肝菌粗多糖对DPPH·和·OH的清除作用

图4 牛肝菌粗多糖对DPPH·(a)和·OH(b)的清除效果
Fig.4 Scavenging effect of crude polysaccharides of Boletus on DPPH·(a) and·OH (b)
由图4(a)可见,VC和牛肝菌多糖的浓度对DPPH·清除率具有显著影响。当VC质量浓度为0.2 mg/mL时,其DPPH·清除率已达100%;与VC相比,牛肝菌多糖质量浓度为0.752 mg/mL时,DPPH·清除率为50%;当多糖质量浓度为1.0 mg/mL时,多糖对DPPH·的清除率可达71.19%。多糖对DPPH·的半抑制浓度(half maximal inhibition concentration,IC50)为0.75mg/mL。
由图4(b)可见,VC对·OH具有很强的清除能力。当VC质量浓度为2.0 mg/mL时,清除效果已经达到100%。与VC相比,牛肝菌多糖对·OH清除作用较差。当牛肝菌多糖质量浓度为5.12 mg/mL时,多糖对·OH的清除率为50%;当多糖质量浓度为10 mg/mL时,多糖对·OH的清除率可达80.69%。多糖对·OH的IC50值为5.12mg/mL。
3 结论
在单因素试验基础上,通过正交试验,获得超声波浸提牛肝菌多糖的最佳工艺组合为A1B2C2,即料液比为1∶15(g∶mL),超声时间为2 h,超声温度为60 ℃,在此条件下,牛肝菌的多糖得率为41.76%。与VC相比,多糖对DPPH·和·OH的清除能力存在一定的差异,多糖对DPPH·和·OH的IC50值分别为0.75mg/mL和5.12mg/mL,当多糖质量浓度分别为1.00 mg/mL和10.00 mg/mL时,多糖对DPPH·和·OH的清除率分别为71.19%和80.69%。
[1]张园园,张晶,王勇,等.美味牛肝菌研究现状及开发前景[J].食用菌,2017,39(2):1-5.
[2]顾可飞,李亚莉,刘海燕,等.牛肝菌、羊肚菌营养功能特性及利用价值浅析[J].食品工业,2018,39(5):287-291.
[3]杨智,孙国太,邸迎彤,等.茶褐牛肝菌化学成分研究[J].热带亚热带植物学报,2018,26(3):309-316.
[4]肖艳红,张晓敏,郭梦南,等.牛肝菌多糖对2-型糖尿病大鼠血糖、体重及血脂水平的影响[J].中国老年学杂志,2018,39(5):1192-1194.
[5]周云波,徐怀春,刘芳,等.文山野生牛肝菌多糖的提取测定及抗氧化性研究[J].文山学院学报,2017,37(3):24-27.
[6]顾可飞,周昌艳,邵毅,等.云南省野生牛肝菌与羊肚菌营养成分分析[J].2017,38(17):129-133.
[7]苏久艳,张霁,李杰庆,等.野生牛肝菌元素含量特征分析及其种类鉴别研究[J].现代食品科技,2019,35(2):1-10.
[8]王林,马青云,黄圣卓,等.牛肝菌化学成分及其生物活性的研究进展[J].热带生物学报,2017,8(1):127-132.
[9]余丽,晏爱芬,陈瑶.野生美味牛肝菌多糖提取条件优化[J].天津农业科学,2018,24(12):14-15,19.
[10]矫丽曼.美味牛肝菌菌丝多糖提取工艺的优化[J].辽宁林业科技,2016,37(3):5-8.
[11]黄俊丽,张憨.松茸、黑牛肝菌、双孢白蘑菇提取物体外抗氧化性试验研究[J].食品与生物技术学报,2011,30(1):342-347.
[12]肖艳红,周晓慧,徐倩,等.正交法优化野生牛肝菌多糖的提取工艺[J].承德医学院学报,2018,35(2):147-149.
[13]朱静,张甜.牛肝菌多糖提取工艺及抗肿瘤作用研究进展[J].安徽农业科学,2016,44(31):120-121.
[14]李志洲.泡沫分离法优化美味牛肝菌多糖分离工艺[J].食品与机械,2012,28(3):130-134.
[15]谢美华,宋信信,贾丹,等.平菇粗多糖提取方法及抗氧化活力的研究[J].楚雄师范学院学报,2015,30(6):18-21.
[16]孙丽平,李笑,苏雪娇.中华牛肝菌多糖的性质及抗氧化性[J].食品工业科技,2016,37(24):173-175.
[17]王珊,黄胜阳.植物多糖提取液脱蛋白方法的研究进展[J].食品科技,2012,37(9):188-191.
[18]莫重文,马宇翔,杨国龙,等.蛋白质化学与工艺[M].北京:化学工业出版社,2007:81.
[19]姜琼,谢妤.苯酚-硫酸法测定多糖方法的改进[J].江苏农业科学,2013,41(12):316-318.
[20]张媛媛,张彬.苯酚-硫酸法与蒽酮-硫酸法测定绿茶茶多糖的比较研究[J].食品科学,2016,37(4):158-163.
[21]胡仲秋,王利,王保玲,等.枸杞多糖提取及消除羟自由基活性研究[J].食品科学,2009,30(24):93-98.
[22]朱显峰,余晨晨,范书军,等.蜜环菌水溶性多糖的抗氧化活性研究[J].食品工业科技,2012,33(3):89-91.
[23]李鹏霄,茆广华,赵婷,等.火棘果红色素的提取及抗氧化活性[J].食品科学,2013,34(17):116-119.
[24]董银萍,李拖平.山楂果胶的抗氧化活性[J].食品科学,2014,35(3):29-32.