解淀粉芽孢杆菌(Bacillus amyloliquefaciens)属于兼性厌氧型革兰氏染色呈阳性的芽孢杆菌,与枯草芽孢杆菌(Bacillus subtilis)亲缘性相近,大部分分离来自土壤和植物,也有少部分从畜禽体内分离获得[1]。由于芽孢杆菌在热杀菌下等不利条件下易形成芽孢,而芽孢对热、干燥、辐射、化学消毒剂和其他理化因素有较强的抵抗力,且大部分芽孢杆菌能产生毒素,对食品安全产生威胁。而解淀粉芽孢杆菌作为少数无毒的芽孢杆菌之一,研究杀菌方式对其芽孢的影响可为控制其他芽孢杆菌提供借鉴。
乳酸链球菌素(Nisin)、山梨酸钾、脱氢乙酸钠均是食品中常见的防腐剂,但抑菌机理和应用范围有所不同,对于一般微生物防腐剂的复配更能起到协同杀菌效应[2]。研究表明,乳酸链球菌素对枯草芽孢杆菌(Bacillus subtilis)和巨大芽孢杆菌(Bacillus megaterium)有抑制作用,而山梨酸钾对它们无抑制作用[1,3]。王征征等[4]研究表明,脱氢乙酸钠对蜡样芽孢杆菌(Bacillus cereus)、枯草芽孢杆菌、巨大芽孢杆菌、产硫芽孢杆菌(Bacillus sulfordii)、球形赖氨酸芽孢杆菌(Lysinibacillus sphaericus)有明显抑制作用。由于解淀粉芽孢杆菌非致腐、非致病性微生物,因此,很少见关于防腐剂或其他方式杀灭、抑制解淀粉芽孢杆菌芽孢作用效果研究。
20世纪60年代,开始了等离子体(plasma)被用于灭菌的研究[5]。随后,有关低温等离子体(low-temperature plasma)对微生物的杀灭作用的研究报道迅速增加。等离子体是指气体在加热或者强电磁场作用下产生的高度电离的气体云,其所含的活性自由基及射线对微生物有较好的杀灭作用[6-7],由于产生等离子体的方式不同,所以对微生物的杀灭机制也不同。传统的产生等离子体的方式有两种:一是大气压下的高电压气体击穿电离(几千伏到上万伏),如相对低温的介质阻挡放电(dielectric barrier discharge,DBD)技术,二是真空室中的低温大面积放电[8]。目前,国内外众多研究证明,低温等离子体对细菌繁殖体[9-10]、真菌[11-12]、病毒[13]等都具有良好的杀灭效果。然而不同方法(激发源、基础气体、放电方法等因素)产生的低温等离子体成分不同,同种成分的浓度也可能不同,杀菌效果就会有差别[14-15]。
鉴于解淀粉芽孢杆菌芽孢对食品安全的威胁,本实验选用乳酸链球菌素、山梨酸钾、脱氢乙酸钠防腐剂,考察其对解淀粉芽孢杆菌芽孢的抑菌效果,并对防腐剂的最佳配比进行优化;以高压电源为激发源,以空气为基础气体,以介质阻挡放电技术产生大气压低温等离子体[16],研究其对解淀粉芽孢杆菌芽孢的灭活效果。从而为控制解淀粉芽孢杆菌及其芽孢在杀菌食品中的残留提供理论及应用指导,为进一步确保食品微生物安全提供技术保障。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
解淀粉芽孢杆菌(Bacillus amyloliquefaciens):某食品公司技术研究中心提供。
1.1.2 化学试剂
番红花红T:天津市致远化学试剂有限公司;孔雀石绿:天津市永大化学试剂有限公司;磷酸盐缓冲液(phosphate buffer solution,PBS)(pH7.2~7.4):北京索莱宝科技有限公司;酵母浸粉、蛋白胨(均为生化试剂)、氯化钠(分析纯):北京奥博星生物技术有限责任公司;山梨酸钾、脱氢乙酸钠(均为分析纯)、乳酸链球菌素(效价940 IU/mg):双汇食品有限公司技术研究中心。
1.1.3 培养基
LB液体培养基、营养琼脂(nutrient agar,NA)培养基、平板计数琼脂(plate count agar,PCA)培养基:北京奥博星生物技术有限责任公司。
1.2 仪器与设备
FA224电子分析天平:上海舜宇恒平科学仪器有限公司;1379Ⅱ级A2型生物安全柜:赛默飞世尔(苏州)仪器有限公司;XH-T涡旋混合器:江苏金怡仪器有限公司;FXB303-2电热恒温培养箱:上海树立仪器仪表有限公司;THZ-C台式恒温振荡器:太仓市华美生化仪器厂;SX-500全自动蒸汽灭菌器:北京五洲东方科技发展有限公司;SY-DT02低温等离子体处理仪:苏州市奥普斯等离子体科技有限公司;DHG-9143BS电热恒温鼓风干燥箱:上海新苗医疗器械制造有限公司;BM1000生物显微镜:南京江南永新光学有限公司。
1.3 实验方法
1.3.1 解淀粉芽孢杆菌芽孢菌悬液的制备
将活化的解淀粉芽孢杆菌接入含LB液体培养基的锥形瓶,摇匀,放进台式恒温振荡培养箱里,37 ℃、150 r/min条件下振荡培养过夜至对数生长期。移取上述菌液200 μL接种到含有0.001%氯化锰的营养琼脂平板上,37 ℃培养5 d后室温放置1~3 d,然后挑取培养基上单个典型菌落,涂片固定,并以5%孔雀石绿溶液和0.5%番红花红T法染色,并在显微镜下进行镜检,当芽孢形成率>95%时为合格,镜检合格后用无菌0.03 mol/L磷酸盐缓冲液(pH=7.2)洗下,转入含有无菌玻璃珠锥形瓶内振摇5 min,接着将锥形瓶放入90 ℃水浴30 min使菌自溶断链,形成均匀的芽孢悬液后离心(5 000 r/min、15 min)取沉淀物,用无菌磷酸盐缓冲液(pH=7.2)重悬3次,采用平板记数法测得芽孢悬液的浓度约为2.34×105 CFU/mL,制得的芽孢菌悬液置4 ℃冰箱备用,使用前(90 ℃、30 min)灭活繁殖体并进行适度稀释[17]。
1.3.2 单一防腐剂对解淀粉芽孢杆菌芽孢灭活效果
脱氢乙酸钠:制备含脱氢乙酸钠质量浓度为1~10 mg/mL(浓度梯度为1 mg/mL)的平板计数琼脂培养基,吸取100 μL的芽孢菌悬液到计数培养基表面,并涂布,于37 ℃静置培养24 h,考察不同浓度脱氢乙酸钠对解淀粉芽孢杆菌芽孢致死率的影响。
山梨酸钾:制备含山梨酸钾质量浓度为1~10 mg/mL(浓度梯度为1 mg/mL)的平板计数琼脂培养基,吸取100 μL的芽孢菌悬液到计数培养基表面,并涂布,于37 ℃静置培养24 h,考察不同浓度山梨酸钾对解淀粉芽孢杆菌芽孢致死率的影响。
乳酸链球菌素:制备含乳酸链球菌素质量浓度为1~10 mg/mL(浓度梯度为1 mg/mL)的平板计数琼脂培养基,吸取100 μL的芽孢菌悬液到计数培养基表面,并涂布,于37 ℃静置培养24 h,考察不同浓度乳酸链球菌素对解淀粉芽孢杆菌芽孢致死率的影响。
1.3.3 复合防腐剂对解淀粉芽孢杆菌芽孢灭活效果
分别制备含脱氢乙酸钠∶乳酸链球菌素=1∶1、山梨酸钾∶乳酸链球菌素=2∶1、山梨酸钾∶脱氢乙酸钠=2∶1、脱氢乙酸钠∶山梨酸钾∶乳酸链球菌素=1∶2∶1的菌落计数平板,移取100 μL芽孢悬液,然后用无菌涂布棒涂布均匀,同时向空白计数平板只涂100 μL稀释浓度相同的芽孢悬液作为空白对照,最后在37 ℃条件下恒温培养24 h后计数。
1.3.4 低温等离子体对解淀粉芽孢杆菌芽孢致死率的影响
用无菌生理盐水将芽孢悬液稀释为300 CFU/mL,振荡均匀,并标记好处理的电源功率(300~500 W)与时间(50~500 s)。经低温等离子体处理后,取100 μL菌悬液涂布平板计数,依次用同样的方法进行其他处理,同时做好空白对照组,然后将平板于37 ℃条件下恒温培养24 h后计数。
1.3.5 分析检测
把培养24 h的平板计数琼脂培养基从培养箱中取出,对平板计数琼脂培养基上长出的菌落数进行计数,并标记出平板上菌落个数,记录实验数据[18]。解淀粉芽孢杆菌芽孢致死率计算公式如下[19]:
1.3.6 数据分析
利用SPSS13.0软件对数据作单因素方差分析。
2 结果与分析
2.1 解淀粉芽孢杆菌菌落及芽孢形态观察
把培养好的解淀粉芽孢杆菌单个菌落培养挑起,在显微镜下镜检,结果见图1。由图1A可知,解淀粉芽孢杆菌菌落呈淡黄色不透明菌落,表面粗糙,有隆起,边缘不规则;由图1B可知,解淀粉芽孢杆菌芽孢呈椭圆形,两端钝圆,芽孢囊不膨大,中生到次端生,可以看到菌落中芽孢率达到95%以上。

图1 解淀粉芽孢杆菌的菌体(A)及芽孢(B)形态
Fig.1 Cell (A) and spore (B) morphology of Bacillus amyloliquefaciens
2.2 单一防腐剂对解淀粉芽孢杆菌芽孢致死率的影响
3种防腐剂在不同浓度的条件下对解淀粉芽孢杆菌芽孢致死率的影响结果见表1。
表1 单一防腐剂对解淀粉芽孢杆菌芽孢致死率的影响
Table 1 Effects of single preservative on the lethallty rate of Bacillus amylopolyticus spores %
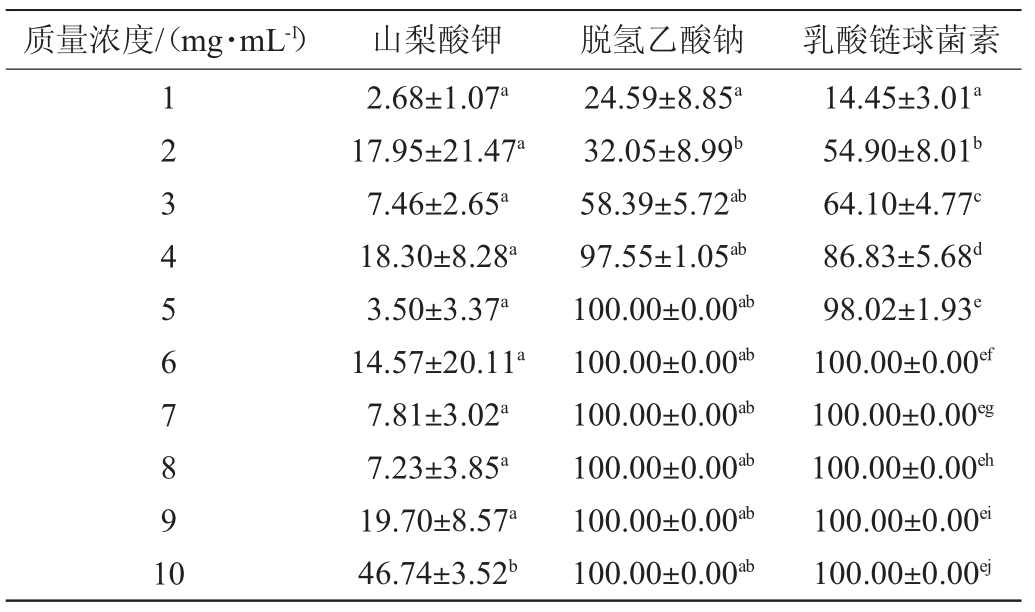
注:同一列相同字母表示不具有显著性差异(P>0.05),不同字母表示具有显著性差异(P<0.05)。下同。
由表1可知,山梨酸钾对解淀粉芽孢杆菌芽孢致死率的变化差异较大,波动性较为明显,在最大质量浓度为10 mg/mL时,对解淀粉芽孢杆菌芽孢致死率仅为46%。而脱氢乙酸钠、乳酸链球菌素浓度分别为4 mg/mL、5 mg/mL时,其对解淀粉芽孢杆菌芽孢致死率已达95%以上。结果表明,3种防腐剂中,抑制效果由大到小顺序为脱氢乙酸钠>乳酸链球菌素>山梨酸钾。
2.3 复合防腐剂对解淀粉芽孢杆菌芽孢致死率的影响
按照不同配比,分析三种防腐剂复配对解淀粉芽孢杆菌芽孢致死率的影响,结果见表2。由表2可知,脱氢乙酸钠与Nisin(1∶1)、Nisin∶山梨酸钾(1∶2)及脱氢乙酸钠∶山梨酸钾(1∶2)复配防腐剂对解淀粉芽孢杆菌芽孢抑制效果较好,二者质量浓度分别为0.5 mg/mL、0.8 mg/mL、0.8 mg/mL时,芽孢抑制率可达90%以上;脱氢乙酸钠∶山梨酸钾∶Nisin配比为1∶2∶1、质量浓度为0.5 mg/mL时,芽孢抑制率可达90%以上。
表2 复合防腐剂对解淀粉芽孢杆菌芽孢致死率的影响
Table 2 Effects of compound preservatives on lethallty rate of Bacillus amylopolyticus spores %

2.4 低温等离子体对解淀粉芽孢杆菌芽孢致死率的影响
低温等离子体对解淀粉芽孢杆菌芽孢致死率的影响结果见表3。
表3 低温等离子体对解淀粉芽孢杆菌芽孢的致死率的影响
Table 3 Effects of low temperature plasma on lethallty rate of Bacillus amylolyticus spores %
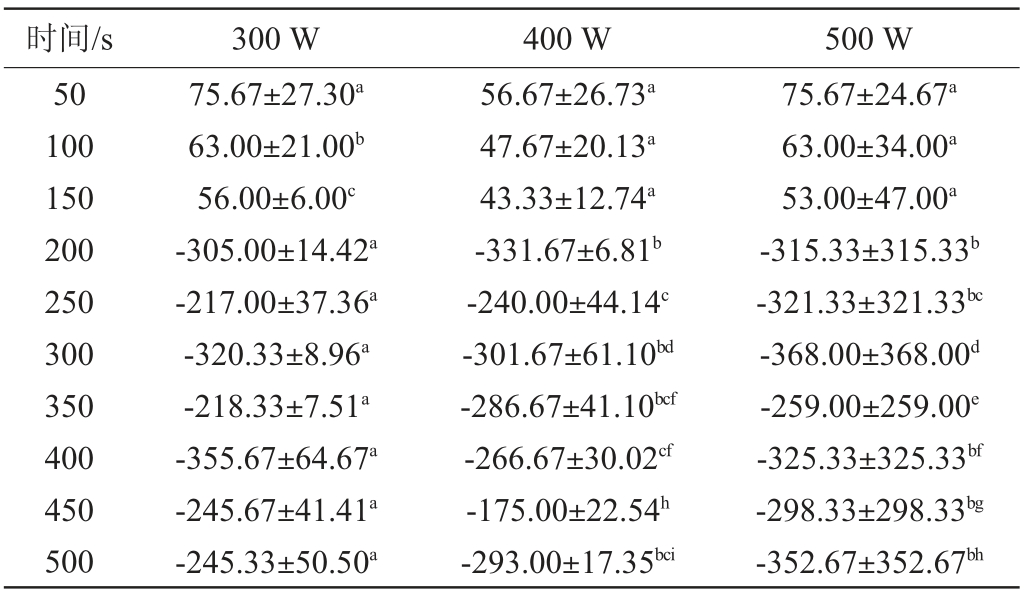
由表3可知,处理时间为50 s,功率为300 W时,解淀粉芽孢杆菌芽孢致死率为75%,随着处理时间的延长到150 s,其作用效果逐渐变差,进一步延长处理时间达200 s以上后,甚至显示对芽孢的萌发及存活具有较好的促进效应,明显和对营养体的作用效果不同[6-7,13],关于其原因尚待进一步研究解释。而400 W、500 W条件下不同处理时间对解淀粉芽孢杆菌芽孢的致死率的影响和300 W具有一定的相似性。结果表明,低温等离子体在低强度处理时,不宜处理较长时间。
3 结论
本实验以解淀粉芽孢杆菌芽孢为研究对象,通过山梨酸钾、脱氢乙酸钠、乳酸链球菌素3种防腐剂的单一与复配,以及低温等离子体对芽孢的处理,研究其对解淀粉芽孢杆菌芽孢抑制的影响。结果表明,单一添加防腐剂时,3种防腐剂中脱氢乙酸钠对该芽孢抑制效果最佳,在4 mg/mL时抑制效果可达97%;乳酸链球菌素次之,山梨酸钾抑制效果最差。防腐剂复配时,脱氢乙酸钠∶乳酸链球菌素(1∶1)、脱氢乙酸钠∶山梨酸钾∶Nisin(1∶2∶1)复合防腐剂抑制效果较好,质量浓度为0.5 mg/mL时可达90%以上。使用低温等离子体处理芽孢时,参数设置为50 s、300 W或500 W时效果最佳,芽孢抑制率达到75%。
[1]MARAT A,NATALIA G T,MARTA H,et al.Inhibitory activity of reuterin,nisin,lysozyme and nitrite against vegetative cells and spores of dairy-related Clostridium species[J].Int J Food Microbiol,2014,172:70-75.
[2]黄现青,王玉芬,赵改名,等.一株玉米肠致腐菌的16S rDNA 鉴定及其防腐剂复配优化[J].中国农业科学,2010,43(24):5112-5120.
[3]AOUADHI C,MEJRI S,MAAROUFI A.Inhibitory effects of nisin and potassium sorbate alone or in combination on vegetative cells growth and spore germination of Bacillus sporothermodurans in milk[J].Food Microbiol,2015,46:40-45.
[4]王征征,李玉峰,李明元,等.防腐剂对腌制大头菜中腐败微生物的抑制效果研究[J].中国食品添加剂,2016(1):119-126.
[5]SHI X M,YUAN Y K,SUN Y Z,et al.Experimental research of inactivation effect of low-temperature plasma on bacteria[J].Plasma Sci Technol,2006,8(5):569-572.
[6]朱亮,张梅,杨雪霞,等.常压低温等离子体灭菌实验研究[J].东华大学学报(自然科学版),2009,35(5):609-614.
[7]张梅.低温等离子体灭菌实验研究[D].上海:东华大学,2006.
[8]刘慧,李海蓉.常压下低温等离子体射频流灭杀大肠杆菌的机理分析[C]//全国等离子体医学研讨会会议,2013.
[9]孙艳,张志伟,王世清.常压低温等离子体对黄瓜表面大肠杆菌杀菌效果及品质的影响[J].粮油食品科技,2018,26(1):61-67.
[10]崔海英,柏梅,戴锦铭,等.冷等离子体技术对黄瓜表面大肠杆菌O157:H7 生物膜的清除作用研究[J].食品工业科技,2017,38(2):161-165.
[11]GUO J,HUANG K,WANG X,et al.Inactivation of yeast on grapes by plasma-activated water and its effects on quality attributes[J].J Food Protect,2017,80(2):225-230.
[12]DASAN B G,BOYACI I H,MUTLU M.Nonthermal plasma treatment of Aspergillus spp.spores on hazelnuts in an atmospheric pressure fluidized bed plasma system:Impact of process parameters and surveillance of the residual viability of spores[J].J Food Eng,2017,196:139-149.
[13]项良剑.低温常压等离子体对不同亚型乳腺癌细胞的影响及机理研究[D].无锡:江南大学,2018.
[14]李喜,李杰,谢宇彤,等.大气压介质阻挡放电综述[J].高能量密度物理,2013,2:86-92.
[15]章程,邵涛,龙凯华,等.大气压空气中纳秒脉冲介质阻挡放电特性分析[J].中国电机工程学报,2010,30(7):111-117.
[16]王新新.介质阻挡放电及其应用[J].高电压技术,2009,35(1):1-11.
[17]黄现青.Bacillus subtilis fmbJ 产生的脂肽抗微生物效果及安全性评价[D].南京:南京农业大学,2006.
[18]中华人民共和国国家卫生和计划生育委员会,国家食品药品监督管理总局.GB 4789.2—2016 食品安全国家标准食品微生物学检验菌落总数测定[S].北京:中国标准出版社,2016.
[19]黄现青,董飒爽,李传令,等.冷却鸡胸肉脉冲强光杀菌参数试验优化[J].农业机械学报,2019,50(2):333-339.