发酵豆制品是发酵食品中的一大类,在亚洲国家人民饮食中占重要地位,其中豆豉、豆酱、酱油和腐乳又被称为中国四大传统发酵豆制品,在我国有深厚的消费基础[1-2]。随着发酵豆制品具有抗氧化、降血压、降血糖、溶血栓等保健功效被揭示[1,3],以及人们对食品安全和食品营养的关注度越来越高,保障发酵豆制品的安全性显得越发重要。
脱氢乙酸是继苯甲酸钠、尼泊金和山梨酸钾后的新一代广谱型食品防腐剂,对霉菌、酵母菌和细菌的抑制能力极强[4-5]。但已有毒理学研究表明,脱氢乙酸会对人体的肾脏、肝脏以及中枢神经系统产生慢性影响,并可能引发癌症[6]。目前,国标GB 2760—2014《食品添加剂使用标准》[7]中明确规定了发酵豆制品中脱氢乙酸的最大使用量为0.3 g/kg。由于发酵豆制品成分复杂,运用国标方法[8-9]检测时,前处理方法除杂效果差,色谱分离效果十分不理想,且分析时间长,不利于大批量发酵豆制品中脱氢乙酸的准确测定。因此,建立适应性更强的检测方法成为了亟待解决的问题。本实验从前处理方法(包括蛋白沉淀剂种类、除油脂方法、除盐方法、提取方法、提取时间、固相萃取小柱种类)和色谱条件(流动相体系)两方面优化了发酵豆制品中脱氢乙酸的检测方法,为食品中脱氢乙酸的测定的食品安全国家标准的制修订和日常监督检测提供科学依据。
1 材料与方法
1.1 材料与试剂
豆酱:某公司;脱氢乙酸(1 000μg/m L):农业部环境保护科研监测所;甲醇、乙腈(均为色谱纯):德国默克公司;乙酸铵(分析纯):天津市大茂化学试剂厂;磷酸二氢钾、氢氧化钠、硫酸锌、亚铁氰化钾、乙酸锌、硫酸铜、甲酸、乙酸、氨水(均为分析纯):国药集团化学试剂有限公司。实验用水为GB/T 6682—2008规定的一级水。CleanertSC18固相萃取小柱(500mg/6m L):天津博纳艾杰尔科技有限公司;Bond ElutC18固相萃取小柱(500mg/6mL):美国Agilent公司。
1.2 仪器与设备
1260型高效液相色谱仪:美国Agilent公司;ST16台式离心机:德国Thermo FisherScientific公司;LC-250型超声波清洗器:山东济宁鲁超超声设备有限公司;VM 24固相萃取仪:天津博纳艾杰尔科技有限公司;M illi-Q纯水机:德国默克公司。
1.3 方法
1.3.1 标准溶液配制
脱氢乙酸标准工作溶液:量取适量脱氢乙酸标准储备溶液,加水定容至刻度,依次配制成质量浓度分别为1.0μg/m L、5.0μg/m L、10.0μg/m L、20.0μg/m L、50.0μg/m L的标准工作溶液。
1.3.2 样品前处理方法
提取:称取约5.0 g均匀样品于50m L塑料离心管中,加入约10m L水,加入0.2m L亚铁氰化钾,摇匀,再加入0.2m L乙酸锌,摇匀,用氢氧化钠溶液(20 g/L)调pH至7.5,加水稀释至50m L,摇匀。超声提取20m in(超声功率250W),8 000 r/min离心10min,上清液待净化。
净化富集:取20m L上清液,用10%的甲酸水溶液调pH至5.0,定容至25m L,取5m L过已活化的C18固相萃取小柱(依次用5m L甲醇,10m L水活化小柱),用5m L水淋洗,2m L体积分数为70%的甲醇水溶液洗脱,收集洗脱液2m L,涡旋混匀,过0.45μm有机滤膜,供高效液相色谱测定。
1.3.3 色谱条件
色谱柱:Welch Ultimate AQ-C18色谱柱(5μm,4.6mm×250mm);流动相为甲醇:0.02mol/L乙酸铵(用氨水调节pH至9.0)=2∶98(V/V),流速1.0m L/min;柱温30 ℃;进样量10μL;检测波长为293 nm。
2 结果与分析
2.1 前处理方法的优化
2.1.1 蛋白沉淀剂及用量的选择
根据国家标准[8-9]、地方标准[10-11]及相关研究[12-19]中所使用的蛋白沉淀剂,选择了有机沉淀剂(丙酮)、亚铁氰化钾和乙酸锌、硫酸铜和氢氧化钠与硫酸锌共4种蛋白沉淀剂进行对比试验。称取12份均匀的空白豆酱样品(每份约5.0 g),分为4组(每组3个平行样),加标量均为10.0mg/kg,加入蛋白沉淀剂的量分别为丙酮2m L、亚铁氰化钾溶液(106 g/L)和乙酸锌溶液(220 g/L)各2 mL、硫酸铜溶液(100 g/L)和氢氧化钠溶液(40 g/L)各2m L、硫酸锌溶液(120 g/L)5mL,其他步骤按1.3.2(1)处理样品,取上清液过0.45μm有机滤膜,高效液相色谱法测定。结合4种不同沉淀剂的提取效率及沉淀效果,亚铁氰化钾溶液(106 g/L)和乙酸锌溶液(220 g/L)的提取率最高,样品平均回收率为92.7%,相对标准偏差(relative standard deviation,RSD)为1.1%,沉淀蛋白质效果最佳。因此,选择亚铁氰化钾和乙酸锌作为蛋白沉淀剂。
对亚铁氰化钾和乙酸锌的加入量进行优化,称取33份均匀的空白豆酱样品(每份约5.0 g),分为11组(每组3个平行样),加标量均为10.0mg/kg,分别加入亚铁氰化钾溶液(106g/L)和乙酸锌溶液(220 g/L)各0.1mL、0.2m L、0.3m L、0.4m L、0.5m L、1.0m L、1.5m l、2.0m L、3.0m L、4.0m L、5.0m L,其他步骤按1.3.2(1)处理样品,取上清液过0.45μm有机滤膜,高效液相色谱法测定。亚铁氰化钾溶液(106g/L)和乙酸锌溶液(220 g/L)的添加量对脱氢乙酸的加标回收率试验结果的影响如表1所示。由表1可知,亚铁氰化钾溶液(106g/L)和乙酸锌溶液(220 g/L)各加入0.2mL时提取率最高,相对标准偏差(relative standard deviation,RSD)为0.6%。因此,选择亚铁氰化钾溶液(106 g/L)和乙酸锌溶液(220 g/L)的加入量均为0.2m L进行后续试验。
表1 亚铁氰化钾溶液和乙酸锌溶液的添加量对脱氢乙酸测定的影响
Table 1 Effect of potassium ferrocyanide solution and zinc acetate solution addition on the determ ination of dehydroacetic acid

亚铁氰化钾溶液和乙酸锌溶液加入量/m L本底值/(mg·kg-1)加标量/(mg·kg-1)平均回收率/%RSD/%0.1 0.2 0.3 0.4 0.5 1.0 1.5 2.0 3.0 4.0 5.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 10.0 10.0 10.0 10.0 10.0 10.0 10.0 10.0 10.0 10.0 10.0 93.4 95.5 94.7 95.5 92.1 92.3 90.9 93.5 81.6 72.2 45.9 93.4 96.4 94.8 95.6 92.5 93.3 89.7 92.4 81.2 74.0 45.5 92.2 96.5 94.6 93.9 92.4 90.2 91.9 90.5 82.5 74.8 44.5 93.0 96.1 94.7 95.0 92.3 91.9 90.8 92.1 81.8 73.7 45.3 0.7 0.6 0.1 1.0 0.2 1.7 1.2 1.6 0.8 1.8 1.6测定回收率/%1 2 3
2.1.2 除油脂方法的选择
称取12份均匀的空白豆酱样品(每份约5.0g),分为4组(每组3个平行样),加标量均为10.0mg/kg,将1.3.2(1)中经过超声提取后的样液分别采用8 000 r/min离心10min后用注射器吸取上层油脂[20]、依照国标方法[8-9]用正己烷萃取油脂除油、8 000 r/min离心10min和4 000 r/min离心10min共4种不同方法进行除油脂,其他步骤按1.3.2(1)处理样品,取清液过0.45μm有机滤膜,高效液相色谱法测定。结果表明,8000 r/min离心10min相较于其他3种除油脂方法不仅无需使用有机试剂、且有较好的除油脂效果,操作简便、省时省力。因此,选择8000 r/min离心10min作为最适除油脂方法。
2.1.3 提取方法的选择
称取9份均匀的空白豆酱样品(每份约5.0 g),分为3组(每组3个平行样),加标量均为10.0mg/kg,分别采用涡旋、超声、70℃恒温水浴加热提取30m in[21]3种不同的提取方式进行提取,其他步骤按1.3.2(1)处理样品,取上清液过0.45μm有机滤膜,高效液相色谱法测定。结果表明,3种提取方式的提取效率无显著性差异,超声提取的样品回收率较高且省时省力。因此,选择超声提取作为最适提取方法。
2.1.4 提取时间的选择
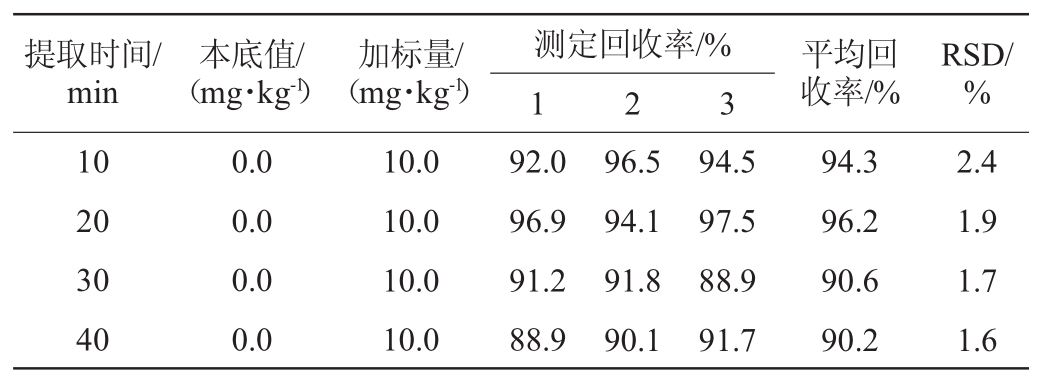
称取12份均匀的空白豆酱样品(每份约5.0g),分为4组(每组3个平行样),加标量均为10.0mg/kg,设定超声提取时间分别为10min、20min、30min、40min,其他步骤按1.3.2(1)处理样品,取上清液过0.45μm有机滤膜,高效液相色谱法测定。不同提取时间对脱氢乙酸的加标回收率试验结果的影响如表2所示。结果表明,20min的提取效果最佳(平均回收率96.2%,RSD为1.9%)。因此,确定最适超声提取时间为20min。
表2 提取时间对脱氢乙酸测定的影响
Table2Effectofextractiontimeondehydroaceticacid determination
提取时间/min本底值/(mg·kg-1)加标量/(mg·kg-1)平均回收率/%RSD/%10 20 30 40 0.0 0.0 0.0 0.0 10.0 10.0 10.0 10.0 92.0 96.9 91.2 88.9 96.5 94.1 91.8 90.1 94.5 97.5 88.9 91.7 94.3 96.2 90.6 90.2 2.4 1.9 1.7 1.6测定回收率/%1 2 3
2.1.5 固相萃取小柱的选择
由于发酵豆制品含盐量高[3],本实验选择了2种固相萃取小柱(分别为BondElutC18柱和CleanertSC18柱)进行除盐效果对比试验。BondElutC18柱是强疏水性的键合硅胶吸附剂,可用于在离子交换之前去除水相基质中的盐分,盐能毫无保留地通过吸附剂。CleanertSC18柱是以高纯球型硅胶为基质的反相C18萃取柱。球型材料均匀度更高,流速更稳定,高纯的硅胶表面,避免了对碱性与极性物质的过度吸附,更适合用于萃取低浓度分析物。可应用于样品的脱盐、环境水样中的有机物的富集等。
对2种固相萃取小柱分别进行低、中、高浓度(加标量分别为2.0mg/kg、5.0mg/kg和10.0mg/kg)的加标回收试验(每组6个平行样),按1.3.2处理样品,脱氢乙酸的加标回收率试验结果见表3。由表3可知,使用BondElutC18柱进行净化,当加标量为2.0mg/kg时,脱氢乙酸的平均回收率仅为74.1%,难以对低浓度的脱氢乙酸进行准确定量。而使用CleanertSC18柱进行净化,加标量为2.0mg/kg、5.0mg/kg和10.0mg/kg时,平均回收率均高于BondElutC18柱,RSD为1.3%~2.9%。当样品加标量均为5.0mg/kg时,将用国标方法GB5009.121—2016《食品中脱氢乙酸的测定》进行前处理、样品经BondElutC18柱净化、及样品经CleanertSC18柱净化后的样品色谱图进行对比,结果见图1。如图1所示,样品经CleanertSC18柱净化后杂质更少。因此,试验选择CleanertSC18柱。
表3 2种固相萃取小柱的加标回收率试验结果(n=6)
Table3Resultsofaddingstandardrecoverytestof2typesofsolidphaseextractioncolumn(n=6)

固相萃取小柱 本底值/(mg·kg-1)加标量/(mg·kg-1)平均回收率/%RSD/%BondElutC18 CleanertSC18 0.0 0.0 0.0 0.0 0.0 0.0 2.0 5.0 10.0 2.0 5.0 10.0 75.2 84.9 85.9 90.9 94.9 96.3 75.6 86.9 87.7 89.4 92.5 94.1 72.7 85.9 86.9 89.1 92.7 89.6 70.1 88.3 88.3 89.9 91.2 96.6 75.8 88.0 87.6 92.9 92.8 96.8 75.4 83.5 90.1 85.9 92.1 95.9 74.1 86.3 87.8 89.7 92.7 94.9 3.1 2.2 1.6 2.6 1.3 2.9 2 3 4 5 6测定回收率/%1

图1 加标样品高效液相色谱图
Fig.1HPLCchromatogramsofaddingstandardsamples
A:按GB5009.121—2016进行前处理的样品图谱;B:经BondElutC18柱净化的样品图谱;C:经CleanertSC18柱净化的样品图谱
2.2 流动相的选择
国标方法[8-9]中采用甲醇-0.02mol/L乙酸铵体系作为流动相进行发酵豆制品中脱氢乙酸的检测时,使用甲醇-0.02mol/L乙酸铵(10∶90,V/V)洗脱样品溶液,目标峰(脱氢乙酸)拖尾,杂质峰与目标峰之间常常无法实现分离,甚至在40m in附近还有杂质峰被洗出,造成分析时间长、效率低下。因此,本研究根据文献报道对比了乙腈-0.02mol/L磷酸二氢钾体系[19-20]、甲醇-0.02mol/L乙酸铵(用乙酸调节pH至5.5)体系[16]、甲醇-0.02mol/L乙酸铵(用氨水调节pH至9.0)体系[22]共3种体系作为流动相进行等度洗脱,进行发酵豆制品中脱氢乙酸的检测,脱氢乙酸标准HPLC色谱图见图2。由图2可知,流动相为甲醇∶0.02mol/L乙酸铵(用氨水调节pH至9.0)=2∶98(V/V)时,相较于乙腈∶0.02mol/L磷酸二氢钾=35∶65(V/V)、甲醇∶0.02mol/L乙酸铵(用乙酸调节pH至5.5)=40∶60(V/V)两种流动相体系,目标峰对称性好,与杂质峰分离效果好。因此,选择甲醇∶0.02mol/L乙酸铵(用氨水调节pH至9.0)=2∶98(V/V)进行洗脱。

图2 脱氢乙酸标准品高效液相色谱图
Fig.2 HPLC chromatogram of dehydroacetic acid standard
A:流动相为乙腈∶0.02mol/L磷酸二氢钾=35∶65(V/V);B:流动相为甲醇∶0.02mol/L乙酸铵(用乙酸调节pH至5.5)=40∶60(V/V);C:流动相为甲醇∶0.02mol/L乙酸铵(用氨水调节pH至9.0)=2∶98(V/V)。
2.3 线性范围及检出限
脱氢乙酸标准工作溶液的质量浓度分别为1.0μg/m L、5.0μg/m L、10.0μg/m L、20.0μg/m L、50.0μg/m L,按1.3.3色谱条件进样分析,以峰面积(y)和脱氢乙酸标准溶液质量浓度(x)绘制标准曲线,结果见图3。

图3 脱氢乙酸标准曲线
Fig.3 Standard curve of dehydroacetic acid
由图3可知,该方法在1~50μg/m L质量浓度范围内线性关系良好,标准曲线线性回归方程为y=25.084x-0.640,相关系数R2为1.000 0,以3倍信噪比计算检出限,方法检出限为1.0mg/kg。
2.4 精密度试验
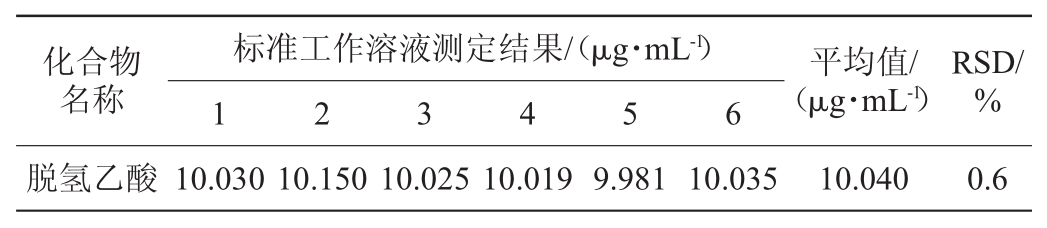
以质量浓度10.0μg/m L的脱氢乙酸标准工作溶液连续重复进样6次进行精密度试验,分别计算脱氢乙酸的含量并计算相对标准偏差(RSD),结果见表4。由表4可知,脱氢乙酸的测定结果的RSD为0.6%,表示该方法精密度良好。
表4 精密度试验结果
Table 4 Results of precision tests
化合物名称平均值/(μg·m L-1)RSD/%脱氢乙酸 10.030 10.150 10.025 10.019 9.981 10.035 10.040 0.6标准工作溶液测定结果/(μg·m L-1)1 2 3 4 5 6
2.5 加标回收率试验
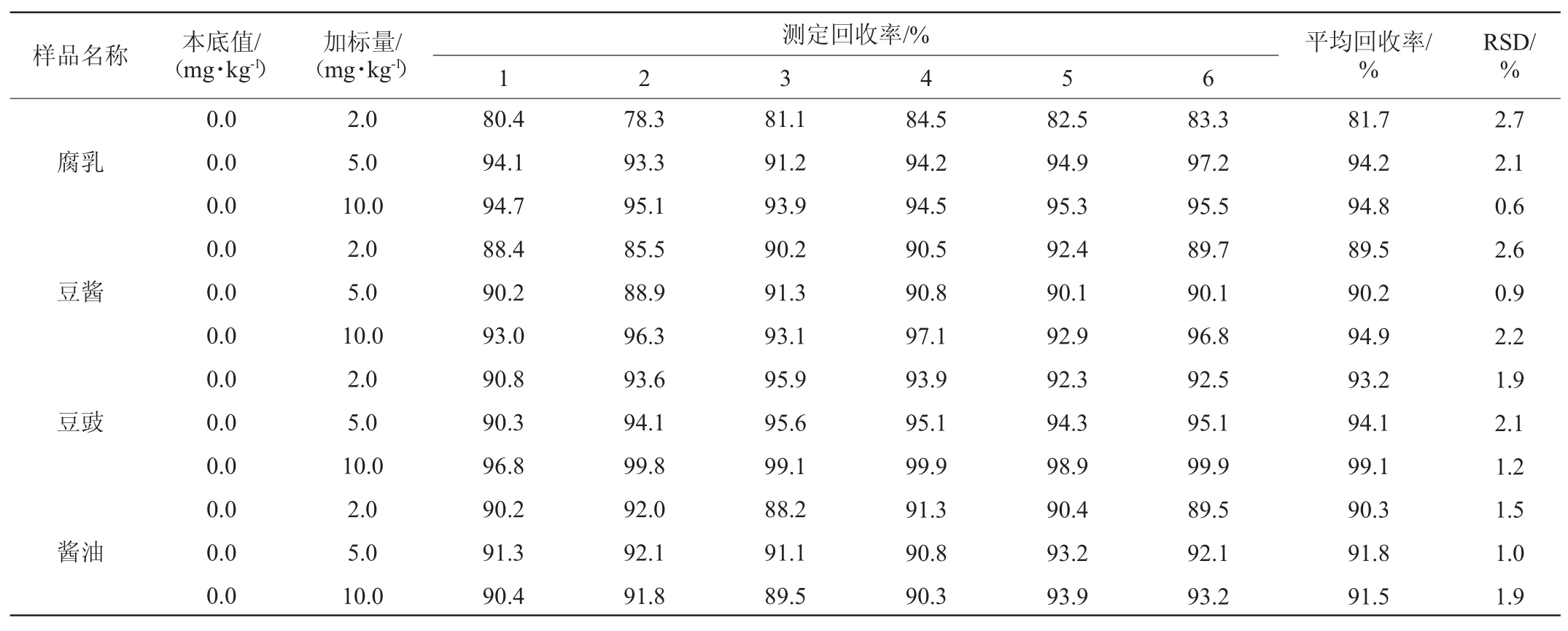
称取空白腐乳、豆酱、豆豉、酱油样品各18份(每份约5.0 g),将每个品种的发酵豆制品各分为3组(每组6个平行样),分别添加适量标准溶液,使3组样品中脱氢乙酸的加标量分别为2.0mg/kg(低)、5.0mg/kg(中)和10.0mg/kg(高)三个水平,按1.3.2处理样品进行回收实验,样品加标回收率试验结果见表5。由表5可知,该方法平均回收率为81.7%~99.1%,RSD为0.6%~2.7%。结果表明,该方法准确度良好,结果准确可靠。
表5 加标回收率试验结果
Table 5 Results of adding standard recovery tests
样品名称 本底值/(mg·kg-1)加标量/(mg·kg-1)平均回收率/%RSD/%腐乳豆酱豆豉酱油0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 2.0 5.0 10.0 2.0 5.0 10.0 2.0 5.0 10.0 2.0 5.0 10.0 80.4 94.1 94.7 88.4 90.2 93.0 90.8 90.3 96.8 90.2 91.3 90.4 78.3 93.3 95.1 85.5 88.9 96.3 93.6 94.1 99.8 92.0 92.1 91.8 81.1 91.2 93.9 90.2 91.3 93.1 95.9 95.6 99.1 88.2 91.1 89.5 84.5 94.2 94.5 90.5 90.8 97.1 93.9 95.1 99.9 91.3 90.8 90.3 82.5 94.9 95.3 92.4 90.1 92.9 92.3 94.3 98.9 90.4 93.2 93.9 83.3 97.2 95.5 89.7 90.1 96.8 92.5 95.1 99.9 89.5 92.1 93.2 81.7 94.2 94.8 89.5 90.2 94.9 93.2 94.1 99.1 90.3 91.8 91.5 2.7 2.1 0.6 2.6 0.9 2.2 1.9 2.1 1.2 1.5 1.0 1.9 2 3 4 5 6测定回收率/%1
3 结论
本试验对发酵豆制品中脱氢乙酸的检测方法的前处理条件及色谱条件进行了优化,建立了一种固相萃取-高效液相色谱测定发酵豆制品中脱氢乙酸的方法,有效的解决了发酵豆制品中脱氢乙酸的高效净化富集、液相色谱条件的优化、准确定性定量的三大关键问题。该方法在1~50μg/m L范围内线性关系良好,相关系数R2>0.999,方法检出限为1.0mg/kg,精密度试验结果RSD为0.6%,加标回收率为81.7%~99.1%,相对标准偏差(RSD)为0.6%~2.7%。该方法相较于现行国标方法,灵敏度更高、除杂效果明显,且回收率和重现性良好。不仅有利于延长色谱柱及高效液相色谱仪的使用寿命,还可以为食品中脱氢乙酸测定的食品安全国家标准的制修订和日常监督检测提供科学依据。
[1]马艳莉,李里特.发酵豆制品酿造过程中组分和营养功能因子的变化及调控[J].食品科学,2012,33(3):292-299.
[2]李幼筠,周逦.中国独具特色的发酵豆制品[J].中国酿造,2010,29(4):12-16.
[3]杨杨,曾剑华,王冰,等.中国传统发酵豆制品风味物质的研究进展[J].大豆科学,2018,37(6):969-974.
[4]付丽莎,胡侠.糕点中纳他霉素和脱氢乙酸实验方法的改进[J].食品安全导刊,2017(21):73.
[5]于喆源,张婕.对食品中脱氢乙酸HPLC检验方法的研究[J].化工管理,2017(29):207.
[6]ZHANG Y M,DU Y F,YIN J,et al.Determ ination and depletion of dehydroacetic acid residue in chicken tissues[J].Food Add Contam in,2012,29(6):918-924.
[7]中华人民共和国国家卫生和计划生育委员会.GB 2760—2014食品安全国家标准食品添加剂使用标准[S].北京:中国标准出版社,2014.
[8]中华人民共和国国家卫生和计划生育委员会.GB 5009.121—2016食品安全国家标准食品中脱氢乙酸的测定[S].北京:中国标准出版社,2016.
[9]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 23377—2009食品中脱氢乙酸的测定高效液相色谱法[S].北京:中国标准出版社,2009.
[10]河北省卫生和计划生育委员会.DBS13/006—2016食品安全地方标准食品中苯甲酸、山梨酸、脱氢乙酸、糖精钠和乙酰磺胺酸钾(安赛蜜)的测定高效液相色谱法[S].北京:中国标准出版社,2016.
[11]湖南省质量技术监督局.DB43/T 445—2009食品中脱氢乙酸的测定高效液相色谱法[S].北京:中国标准出版社,2009.
[12]李玉强,晏晓清,张艳芳,等.高效液相色谱同时检测蛋白饮料中安赛蜜、糖精钠、苯甲酸、山梨酸、脱氢乙酸的前处理方法研究[J].科技与企业,2014(4):249-251.
[13]杨帛,刘锐萍,刘浩,等.食品中多种防腐剂同时检测方法的优化研究[J].饮料工业,2014,17(11):27-30.
[14]杨海昕,曹云,肖君,等.高效液相色谱法测定食品中脱氢乙酸前处理方法探讨[J].江苏预防医学,2015,26(5):100-102.
[15]金悦敏,胡国华.HPLC法测定糕点类食品中的8种常用防腐剂[J].食品工业,2018,39(6):270-273.
[16]于喆源,张婕.对食品中脱氢乙酸HPLC检验方法的改进[J].食品安全导刊,2017(24):55-56.
[17]肖树秀.食品中脱氢乙酸的检测方法[J].煤炭与化工,2017,40(1):149-151.
[18]雷德卿.双波长高效液相色谱法测定米豆腐中4种防腐剂[J].食品安全质量检测学报,2017,8(10):4057-4060.
[19]殷晶晶.非发酵性豆制品中脱氢乙酸的高效液相色谱测定法[J].职业与健康,2018,34(16):2200-2202.
[20]蒋孟圆,张瑞雨,刘晓松,等.二极管阵列-超高效液相色谱法同时测定食品中5种添加剂的含量[J].食品安全质量检测学报,2017,8(10):3819-3825.
[21]高功敏,邹强,杨希,等.食品中安赛蜜、苯甲酸、山梨酸、糖精钠、脱氢乙酸同时检测方法[J].广东化工,2017,44(18):176,184.
[22]刘云波,李海涛,朱旭东,等.高效液相色谱法分离食品防腐剂和甜味剂中五种化合物[J].广东化工,2017,44(21):145-149.