我国作为猕猴桃的原产国,野生资源丰富,拥有62个种,已有2 000多年的文字记载历史[1]。野生猕猴桃具有较高的营养价值和功能作用,是酿造果酒的优质资源,但因其含有较高的有机酸,造成酒体粗糙,酸味过重,通常还会伴随着酒体失光、浑浊等不良现象[2]。
苹果酸-乳酸发酵(malolactic fermentation,MLF)是乳酸菌以L-苹果酸为底物,在苹果酸乳酸酶(malolactic enzyme,MLE)的催化作用下,转变成L-乳酸和CO2的过程[3-4]。其被认为是一个二次发酵过程,在大多数果酒的生产中发挥着不可或缺的作用。MLF可适当地降低酒体中的有机酸含量[5-6],改善葡萄酒的稳定性[7],降低果酒中某些有害成分[8],是提高果酒柔和度和稳定性的重要工序,已在葡萄酒或苹果酒中广泛应用。
在传统的果酒发酵过程中,MLF是在酒精发酵刚刚完成之后进行的,可以是自然发酵,也可以是接种发酵剂发酵。然而,在复杂的酒体中,并非所有的细菌都容易生长,如低pH值(<3.5)、高SO2(>50mg/L)、高酒精度(>4%vol)以及中链脂肪酸、酚类化合物(如酚酸、单宁)和酵母发酵副产物抑制蛋白质等均可以抑制乳酸菌的生长[9]。因此,筛选苹果酸-乳酸发酵的优良菌株,最基本的要求是具有良好的适应性和酿酒特性,并具有较强的苹果酸降解能力。目前,国内外猕猴桃酒优良MLF乳酸菌相关研究较少。以果酒为原料分离筛选优良MLF乳酸菌是MLF乳酸菌选育的主要手段之一[10]。
因此,本研究通过形态观察、生理生化试验从自然发酵的野生猕猴桃酒中分离筛选出能够进行MLF的乳酸菌,以商业用菌为对照菌株,对分离菌株的SO2、酒精、pH耐受能力进行研究,从而获得综合耐受能力较强的优良菌株。旨在为猕猴桃酒的工业生产提供MLF高耐受性优良菌株,同时为提高猕猴桃酒的质量和稳定性提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 原料
野生猕猴桃果实:于2017年9月采摘自豫南大别山区,成熟度为八成。
1.1.2 菌株
果酒专用酵母:安琪酵母股份有限公司;商业乳酸菌(SY)(Leuconostoconos.b.V.D):法国LALLEMANDS.A.公司。
1.1.3 化学试剂
过氧化氢、D-L苹果酸、乳酸、溴酚蓝、体积分数50%冰乙酸、正丁醇:国药集团化学试剂有限公司。所用试剂均为分析纯。
1.1.4 培养基
改良MRS培养基、改良番茄汁琼脂(tomato juice agar,TJA)培养基:北京奥博星生物技术有限责任公司;酸性番茄(acid tomato juice,ATB)培养基:招远拓普生物工程有限公司;糖发酵培养基:杭州微生物试剂有限公司;石蕊牛奶培养基:北青岛高科园海博生物技术有限公司。
1.2 仪器与设备
JC303型生化培养箱:南通嘉程仪器有限公司;SW-CJ-2F型双人双面净化工作台:杭州博大净化设备有限公司;JC101型电热鼓风干燥箱:西安安森智能仪器股份有限公司;WYT-J型手持糖度计:上海沪粤明科学仪器有限公司;LDZX-50FA型立式压力蒸汽灭菌器:上海申安医疗器械厂;TP310型pH计:北京时代新维测控设备有限公司。
1.3 方法
1.3.1 猕猴桃酒的发酵
选取新鲜、成熟的猕猴桃果实,破碎,打浆后加入0.2g/L活化果酒专用酵母启动酒精发酵。调节总SO2质量浓度为60mg/L,分装至2 L发酵罐中,在25℃条件下进行酒精发酵,待酒精发酵结束后去渣倒罐,利用猕猴桃酒体中的乳酸菌自然启动MLF。
1.3.2 苹果酸-乳酸发酵的监测
以1.5%乳酸标准液为对照,采用纸层析法[11]测定乳酸含量,进而对苹果酸-乳酸发酵进行监测。
1.3.3 苹果酸-乳酸发酵乳酸菌的分离
参照何志刚等[12]的方法,略作改动。在无菌条件下,取自然启动MLF的酒样,适当稀释后,吸取0.1m L酒样均匀涂布于ATB培养基,在28℃条件下培养5~6 d,挑取圆形且稍扁平的单菌落在MRS培养基上进行分离纯化,获得纯菌株进行编号。
1.3.4 形态观察
参照周安玲[13]的方法,略作改动。将适当稀释度的分离菌悬液分别涂布于TJA培养基,于25℃条件下恒温培养2~3 d,逐一观察菌落的形状、大小、边缘、表面、隆起形状、透明度、颜色等特点,并分别进行革兰氏染色,在油镜下观察细胞形态。
1.3.5 生理生化试验
对分离菌株进行乳糖发酵试验、触酶试验和石蕊牛奶试验,参照《伯杰细菌鉴定手册》[14]、《葡萄酒酿造微生物学-实验技术与规程》[15]及《乳酸细菌基础、技术和应用》[16]对试验结果进行分析,筛选出具有MLF能力的乳酸菌。
1.3.6 耐受性试验
一般情况下,乳酸菌代谢糖类的适宜温度为22~25℃,且MLF速度较快,挥发酸较多;在15~20℃条件下,MLF速度稍慢,酒体成分也会发生相应变化;10℃以下,乳酸菌的生长会受到抑制。因此,本试验选择在25℃条件下,参照段浩云等[17]的方法(略作改动)研究筛选菌株的耐受性。具体方法:挑取适量保存于TJA斜面的菌株分别接种于10mLATB液体培养基中,25℃条件下活化24~48h。取1m L种子液(107 CFU/m L)分别接种于9m L不同SO2质量浓度(40mg/L、60mg/L、80mg/L、100mg/L、120mg/L)、酒精度(8%vol、10%vol、12%vol、14%vol、16%vol)、pH值(2.8、3.0、3.2、3.4、3.6)的MRS液体培养基中,25 ℃条件下静置培养2 d,在显微镜下用血细胞计数板对活菌进行计数,筛选出综合耐受性能较好的乳酸菌。
2 结果与分析
2.1 乳酸菌的分离筛选
对自然启动MLF的野生猕猴桃酒样中的乳酸菌进行分离、纯化,得到6株疑似乳酸菌,均呈革兰氏阳性,分别编号为R6、R7、R11、R14、R15、R18,6株疑似乳酸菌的菌落形态及细胞形态详细描述见表1。
表1 分离菌株的菌落和细胞形态结果
Table 1 Colonialand cellmorphology of isolated strains
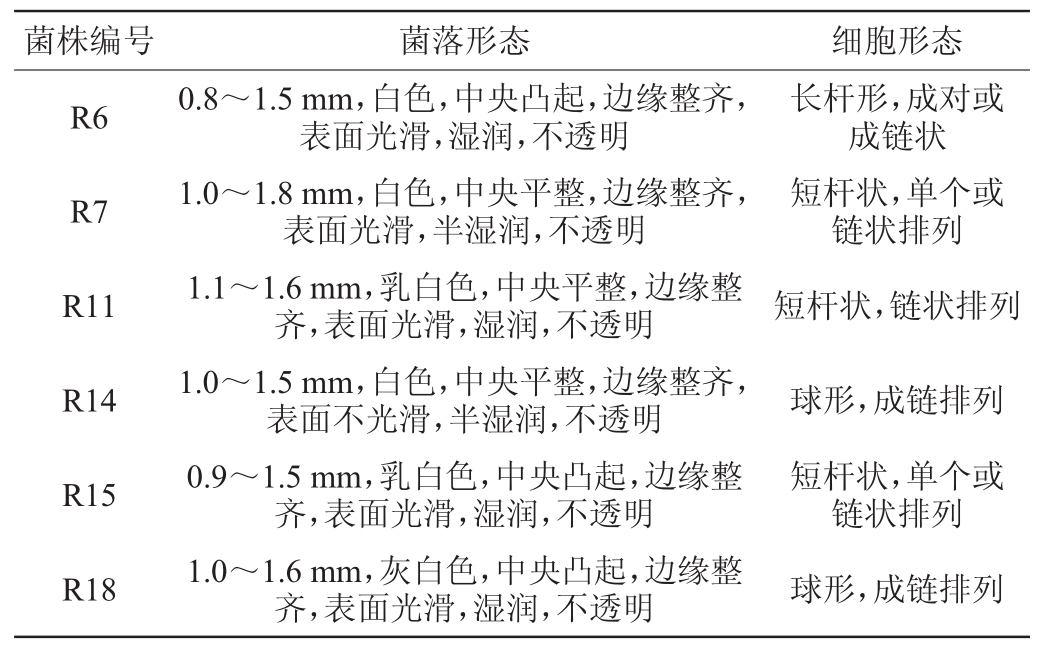
菌株编号 菌落形态 细胞形态R6 R7 R11 R14 R15 R18 0.8~1.5mm,白色,中央凸起,边缘整齐,表面光滑,湿润,不透明1.0~1.8mm,白色,中央平整,边缘整齐,表面光滑,半湿润,不透明1.1~1.6mm,乳白色,中央平整,边缘整齐,表面光滑,湿润,不透明1.0~1.5mm,白色,中央平整,边缘整齐,表面不光滑,半湿润,不透明0.9~1.5mm,乳白色,中央凸起,边缘整齐,表面光滑,湿润,不透明1.0~1.6mm,灰白色,中央凸起,边缘整齐,表面光滑,湿润,不透明长杆形,成对或成链状短杆状,单个或链状排列短杆状,链状排列球形,成链排列短杆状,单个或链状排列球形,成链排列
由表1可知,分离得到的6株疑似乳酸菌菌落较小,菌落直径在0.8~1.8mm,圆形,白色、乳白色或灰白色,均不透明。其中菌株R6、R11、R15、R18菌落表面光滑、湿润;菌株R7和R14菌落表面半湿润;菌株R14菌落表面不光滑;菌株R6、R15、R18菌落中央凸起,菌株R7、R11、R14菌落中央平整。菌株R14和R18细胞呈球形,成链排列;其他菌株细胞形态为短杆状或长杆状,单个或成对或链状排列。
对6株分离菌株分别进行乳糖发酵试验、触酶试验、石蕊牛奶试验,结果表明,6株分离菌株触酶试验均为阴性,牛奶石蕊试验和乳糖发酵试验均为阳性。结合菌落形态和细胞形态初步鉴定6株菌均为乳酸菌。
2.2 分离菌株耐受性研究
2.2.1 SO2耐受能力
SO2是果酒酿造中广为使用的添加剂,其主要作用是防止酒体褐变和避免杂菌的污染。但是乳酸菌的生长对SO2较为敏感,在已报道的菌株中,大多菌株的SO2耐受能力<60mg/L[18],为防止酒体氧化褐变和杂菌大量繁殖而导致挥发酸含量升高,寻找具有耐受高SO2能力的乳酸菌株成为MLF进程中的关键。因此,以商业乳酸菌SY为对照,对分离得到的6株乳酸菌的SO2耐受性进行测定,结果见表2。
表2 分离菌株的SO2耐受性
Table 2 SO2 tolerance of isolated strains
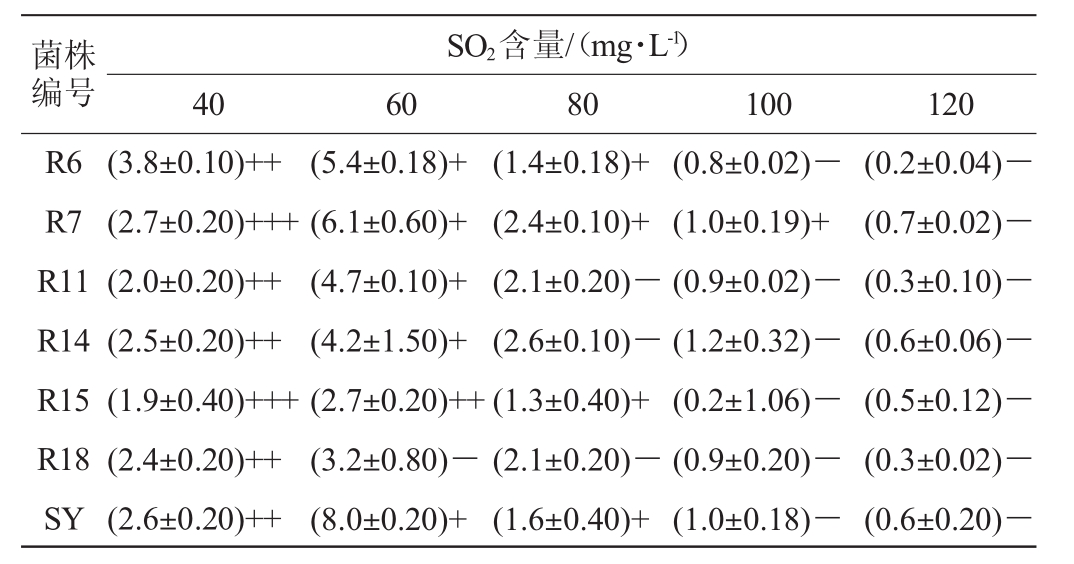
注:以(A)b形式表示乳酸菌对SO2的耐受能力,其中,A表示活菌数增长倍数,A>1表示活菌数呈正增长;A<1表示活菌数呈负增长。b表示活菌数级别,“+++”、“++”、“+”、“-”分别表示平板记数法培养液中的菌体密度达108 CFU/m L、107 CFU/m L、106 CFU/m L、<105 CFU/m L或不生长。下同。
菌株编号R6 R7 R11 R14 R15 R18 SY(3.8±0.10)++(2.7±0.20)+++(2.0±0.20)++(2.5±0.20)++(1.9±0.40)+++(2.4±0.20)++(2.6±0.20)++(5.4±0.18)+(6.1±0.60)+(4.7±0.10)+(4.2±1.50)+(2.7±0.20)++(3.2±0.80)-(8.0±0.20)+(1.4±0.18)+(2.4±0.10)+(2.1±0.20)-(2.6±0.10)-(1.3±0.40)+(2.1±0.20)-(1.6±0.40)+(0.8±0.02)-(1.0±0.19)+(0.9±0.02)-(1.2±0.32)-(0.2±1.06)-(0.9±0.20)-(1.0±0.18)-(0.2±0.04)-(0.7±0.02)-(0.3±0.10)-(0.6±0.06)-(0.5±0.12)-(0.3±0.02)-(0.6±0.20)-SO2含量/(mg·L-1)40 60 80 100 120
由表2可知,当SO2含量为40mg/L时,所有菌株活菌数>107 CFU/m L,最高可达108 CFU/m L;当SO2含量为60mg/L时,除菌株R18外,其他菌株均表现出较强的SO2耐受能力,活菌数均>106 CFU/m L;当SO2含量为80mg/L时,菌株R6、R7、R15表现出较强的SO2耐受能力,活菌数均>106 CFU/m L;当SO2含量为100mg/L时,菌株R6、R11、R15、R18均呈现负增长趋势,且处于不生长状态,菌株R7仍表现出较好的耐受能力,菌株R14未出现负增长,但处于不生长状态;当SO2含量为120mg/L时,6株分离菌均呈现负增长趋势,且处于不生长状态。从杆菌与球菌之间来看,整体上杆菌对SO2的耐受能力高于球菌。以SO2质量浓度为80mg/L时,商业乳酸菌SY的增殖量为标准,可筛选确定SO2耐受能力较强的菌株为R6、R7和R15,其中,菌株R7的SO2耐受能力最强。
2.2.2 酒精耐受能力
在猕猴桃酒发酵过程中,酵母菌代谢的主要产物是乙醇,随着发酵的进行,猕猴桃酒中酒精度越来越高,一般可达10%vol~14%vol。酒精度是抑制乳酸菌生长的重要因素,过高的酒精度可影响乳酸菌的新陈代谢活动,抑制其生长。因此,以商业乳酸菌SY为对照,对分离得到的6株乳酸菌的酒精耐受性进行测定,结果见表3。
表3 分离菌株的酒精耐受性
Table 3 Alcohol tolerance of isolated strains

菌株编号R6 R7 R11 R14 R15 R18 SY(5.3±0.40)+++(6.7±0.60)+++(5.0±0.30)+++(3.9±0.20)++(4.6±0.20)+++(5.4±0.60)++(6.6±0.40)+++(1.4±0.10)+++(2.1±0.24)+++(1.8±0.17)++(8.2±1.50)++(1.7±0.60)++(6.9±0.28)+(8.0±0.20)++(6.7±0.20)+(4.4±0.80)++(2.1±0.20)+(5.2±0.10)+(7.3±0.26)+(3.8±0.20)-(5.6±0.10)++(1.8±0.12)+(2.0±0.60)+(4.9±0.60)-(2.2±0.40)-(1.8±1.24)-(3.3±0.20)-(4.0±0.30)++(1.1±0.09)-(1.3±0.60)-(3.4±0.02)-(1.6±0.06)-(2.5±0.12)-(6.3±0.11)-(1.2±0.02)+酒精度/%vol 8 10 12 14 16
由表3可知,酒精度对分离乳酸菌的生长均表现出一定程度的抑制作用,随着培养基中酒精度由8%vol逐渐增大,对乳酸菌的抑制作用逐渐增强,两者呈显著正相关(P<0.05)。当酒精度为8%vol时,6株菌株的活菌数均>107 CFU/mL,生长状况良好;当酒精度为10%vol时,菌株R11、R15、R18的活菌数下降一个级别,而菌株R6、R7的活菌数依然为108 CFU/m L;当酒精度增至12%vol时,所有分离菌株的活菌数均下降一个级别,其中菌株R18降至105 CFU/m L以下或不生长;当酒精度为14%vol时,6株分离菌株酒精耐受能力继续下降,大部分菌株不生长,而筛选菌株R6和R7的活菌数仍为106 CFU/m L,表现出较强的酒精度耐受力,但均低于商业乳酸菌SY;当酒精度增至16%vol时,分离菌的活菌数均降至105 CFU/m L以下或不生长。参照菌株SY在酒精度12%vol的活菌数,确定酒精度耐受性较强的菌株为R7,整体上杆菌对酒精的耐受能力高于球菌。
2.2.3 pH值耐受能力
不同乳酸菌对pH值的适应能力不同,大部分的乳酸菌最适生长pH接近中性[19],也有一些种属如酒球菌属(Oenococcus)和乳杆菌(Lactobacillus)是嗜酸的[20]。猕猴桃酒体的pH值一般在2.8~3.6范围内变化,因此,以商业乳酸菌SY为对照,对分离得到的6株乳酸菌的pH值耐受性进行测定,结果见表4。
由表4可知,pH值对分离乳酸菌的生长均表现出一定程度的抑制作用,随着培养基中pH由3.6逐渐降低,对乳酸菌的抑制作用逐渐增强,两者呈显著负相关(P<0.05)。当pH值为3.6时,6株乳酸菌活菌数均>107 CFU/m L,总体生长较好,其中菌株R6、R15和R18的活菌数达到108 CFU/m L;当pH值下降到3.4时,除菌株R11、R18外,其他菌株活菌数均下降一个级别,活菌数开始显著下降;当pH值下降到3.2时,活菌数继续显著下降,其中,菌株R14下降到105 CFU/m L以下或不生长;当pH值下降到3.0时,活菌数继续显著下降,但菌株R15仍表现出较好的pH值耐受能力;当pH值下降到2.8时,分离菌株及商业乳酸菌SY的活菌数均不增长。整体上杆菌对pH的耐受能力高于球菌。参照商业乳酸菌SY,菌株R15的pH耐受性较好。
表4 分离菌株的pH值耐受性
Table 4 pH tolerance of isolated strains
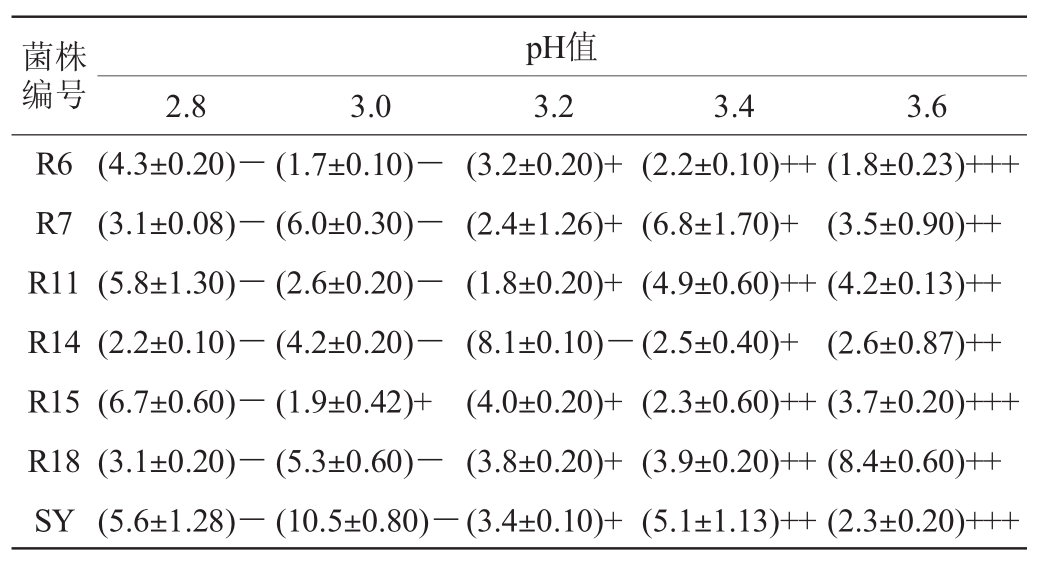
菌株编号R6 R7 R11 R14 R15 R18 SY(4.3±0.20)-(3.1±0.08)-(5.8±1.30)-(2.2±0.10)-(6.7±0.60)-(3.1±0.20)-(5.6±1.28)-(1.7±0.10)-(6.0±0.30)-(2.6±0.20)-(4.2±0.20)-(1.9±0.42)+(5.3±0.60)-(10.5±0.80)-(3.2±0.20)+(2.4±1.26)+(1.8±0.20)+(8.1±0.10)-(4.0±0.20)+(3.8±0.20)+(3.4±0.10)+(2.2±0.10)++(6.8±1.70)+(4.9±0.60)++(2.5±0.40)+(2.3±0.60)++(3.9±0.20)++(5.1±1.13)++(1.8±0.23)+++(3.5±0.90)++(4.2±0.13)++(2.6±0.87)++(3.7±0.20)+++(8.4±0.60)++(2.3±0.20)+++pH值2.8 3.0 3.2 3.4 3.6
综上,可以初步认为在从自然启动MLF的野生猕猴桃酒中分离得到的6株乳酸菌中,菌株R6、R7和R15的SO2、酒精及pH耐受性较好,可以作为猕猴桃酒的生物降酸优良菌株,对果酒生物降酸技术的提升及果酒质量的提高有着重要意义。
3 结论
采用ATB培养基,通过形态观察及生理生化试验从自然启动MLF野生猕猴桃酒中初筛得到6株乳酸菌,分别为R6、R7、R11、R14、R15、R18。通过对6株乳酸菌的SO2、酒精及pH耐受性的研究发现,分离菌株中乳酸杆菌的耐受能力高于球菌。其中,3株乳酸菌(R6、R7、R15)具有较强的SO2、酒精及pH耐受能力,菌株R6、R15在SO2 80mg/L及菌株R7在SO2 100mg/L可维持生长;菌株R6、R7在酒精度14%vol及菌株R15在酒精度12%vol可维持生长;菌株R6、R7在pH值3.2及菌株R15在pH 3.0时可维持生长。结果表明,菌株R6、R7、R15可以作为MLF优良乳酸菌进一步开发与应用的研究对象。
[1]邹游.猕猴桃品种间的遗传多样性分析[D].成都:四川大学,2007.
[2]张占洋.酒酒球菌在野生猕猴桃酒中降酸作用的初步研究[D].郑州:河南科技大学,2013.
[3]李华.现代葡萄酒工艺学[M].陕西:陕西人民出版社,2000:109-118.
[4]DAVISC R,WIBOWO D,ESCHENBRUCH R,et al.Practical implicationsofmalolactic fermentation:a review[J].Am J Enol Viticulut,1985,36(4):290-301.
[5]朱宝镛.葡萄酒科学与工艺[M].北京:中国轻工业出版社,1992:17-18.
[6]王华,张春辉,李华.苹果酸-乳酸发酵对葡萄酒品质的影响[J].西北农业大学学报,1999(6):74-78.
[7]GONZALEZ-ARENZANA L,LÓPEZ-ALFARO I,GARDE-CERDÁN T,et al.M icrobial inactivation and MLF performances of Tempranillo Rioja wines treated with PEFafter alcoholic fermentation[J].Int J Food M icrobiol,2018,269:19-26.
[8]TOIT M D,ENGELBRECHT L,LERM E,et al.Lactobacillus:the next generation ofmalolactic fermentation starter cultures-an overview[J].Food Bioproc Technol,2011,4(6):876-906.
[9]ALEXANDREA H.Saccharomyces cerevisiae-Oenococcusoeni interactions in wine:Currentknow ledgeand perspectives[J].Int J Food M icrobiol,2004,93(2):141-154.
[10]李维新.优良MLF乳酸菌选育及其产酶特性研究与应用[D].福州:福建农林大学,2012.
[11]李华.葡萄酒酿造与质量控制[M].西安:天则出版社,1990:57-63.
[12]何志刚,任香云,李维新,等.枇杷酒中苹果酸乳酸发酵优良乳酸菌的分离与鉴定[J].中国食品学报,2011,12(1):165-170.
[13]周安玲.葡萄酒苹果酸-乳酸发酵优良乳酸菌的筛选及其发酵特性分析[D].兰州:甘肃农业大学,2015.
[14]BUKANNAN R E,JIBUSIN E,等.伯杰细菌鉴定手册[M].北京:科学出版社,1984:797-822.
[15]福杰桑(美)著,徐岩,康文怀(译).葡萄酒酿造微生物学-实验技术与规程(第二版)[M].北京:中国轻工业出版社,2010:192-205.
[16]张刚.乳酸细菌基础、技术和应用[M].北京:化学工业出版社,2007:52-78.
[17]段浩云,田洪涛,檀建新,等.葡萄酒MLF高耐受性优良乳酸菌的筛选与鉴定[J].中国食品学报,2015,15(5):200-203.
[18]秦伟帅,王玉峰,赵新节,等.葡萄酒苹果酸-乳酸发酵工艺控制研究进展[J].中外葡萄与葡萄酒,2008(5):64-67.
[19]GUZZON R,POZNANSKIE,CONTERNO L,etal.Selection of a new highly resistant strain formalolactic fermentation under difficult conditions[J].SAfr J Enol Viticult,2009,30(2):133-141.
[20]HUTKINSRW,NANNEN N.pH homeostasis in lactic acid bacteria[J].JDairy Sci,1993,76(8):2354-2365.