中药材狗尾草(Setaria viridis)为禾本科植物狗尾草属多种植物的总称又名绿狗尾草、谷莠子[1]。狗尾草中富含多糖和酚类物质,并含有钙、磷、镁、钾、钠、硫、氯等元素,其种子粒中含有48%~50%的淀粉[2-5]。狗尾草性平、味淡、无毒,具有清热利湿、祛风明目、解毒、杀虫等功效,可治疗痈肿、疮癣、赤眼等[6-8]。多酚类物质是植物的主要次生代谢产物之一,多酚通过提供氢原子或螯合剂来抑制氧化作用,使其具有较强的抗氧化能力和清除自由基能力[9-11],且研究证实多酚类化合物具有抗氧化、抗肿瘤、抗炎、抗病毒、抗血栓形成和抗动脉硬化等重要作用。
目前国内对狗尾草属的研究主要集中于狗尾草种子活力及其萌发特性,国外狗尾草中活性物质提取的研究较少。杨楠等[12]利用正交试验对狗尾草中总黄酮类物质进行提取,得到狗尾草中总黄酮类物质最大提取率为2.20%。
本研究以成熟狗尾草为原料,乙醇为提取溶剂,采用超声波辅助提取狗尾草中的多酚,并通过响应面法优化提取工艺,确定狗尾草中提取多酚的最佳提取条件,并对狗尾草多酚的体外抗氧化性进行探讨,旨为狗尾草的开发利用提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 试验材料
狗尾草:于2018年10月采摘于沈阳工学院,新鲜,无病虫害,烘干磨粉后备用。
1.1.2 药品试剂
没食子酸:武汉鼎国生物技术有限公司;乙醇、无水碳酸钠、福林酚(folin phenol,FC)试剂、2,6-二叔丁基-4-甲基苯酚(butylatedhydroxytoluene,BHT)、1,1-二苯基-2-三硝基苯肼(diphenyl-2-picrylhydrazyl,DPPH):国药集团化学试剂有限公司。实验所用试剂均为分析纯。
1.2 仪器与设备
KQ-250E医用超声波清洗器:昆山市超声仪器有限公司;TU-1800紫外可见分光光度计:北京普析通用仪器有限责任公司;XS-255A精密电子天平:普利赛斯国际贸易(上海)有限公司;HC-500T2高速多功能粉碎机:永康市天祺盛世工贸有限公司;TGL-18B离心机:上海安亭科学仪器厂;GM0.33A隔膜真空泵:天津市津腾实验设备有限公司;DGG-9076A电热恒温鼓风干燥箱:上海一恒科技有限公司。
1.3 试验方法
1.3.1 狗尾草中多酚的提取工艺流程
狗尾草种子烘干→去除杂质→粉碎过60目筛→加入乙醇→超声辅助提取(功率250 W)→真空抽滤→蒸发浓缩→多酚
1.3.2 没食子酸标准曲线的绘制[13]
准确称取没食子酸标准品0.011 g用蒸馏水溶解并定容至100 mL,配制成质量浓度0.11 mg/mL;精确移取0、0.4 mL、0.6 mL、0.8 mL、1.0 mL、1.2 mL于25 mL棕色容量瓶中,分别添加蒸馏水至6.0 mL,然后分别加入福林酚试剂0.5 mL,混匀后加入1.5 mL 20%Na2CO3溶液,充分混匀后定容至刻度,30℃避光放置0.5 h,在波长760 nm处测定其吸光度值,同时用试剂空白为参比液。以没食子酸质量浓度为横坐标,吸光度值为纵坐标,绘制标准曲线。
1.3.3 狗尾草提取液中的多酚含量测定
取1.0mL狗尾草提取液按照1.3.2中的方法于波长760nm处测其吸光度值,通过标准曲线回归方程计算出1.0 mL中样品的多酚含量,按下式计算得到多酚提取率。
式中:X为多酚提取率,%;m1为1.0 mL提取液中的多酚含量,mg/mL;V1为提取液的总体积,mL;M1为称取的狗尾草粉末质量,g。
1.3.4 狗尾草提取液工艺优化单因素试验
采用超声波辅助乙醇法,考察料液比、乙醇体积分数、提取温度、提取时间对狗尾草中多酚提取率的影响。
精确称取5.0 g狗尾草干粉末,置于100 mL烧杯中。分别在不同料液比(1∶15、1∶20、1∶25、1∶30、1∶35、1∶40(g∶mL)),乙醇体积分数(55%、60%、65%、70%、75%、80%),提取温度(55℃、60℃、65℃、70℃、75℃、80℃),提取时间(70 min、75 min、80 min、85 min、90 min、95 min)条件下进行提取,取1 mL提取液,在波长760 nm处测其吸光度值,根据标准曲线回归方程计算其多酚含量。
1.3.5 狗尾草多酚提取工艺优化响应面试验分析
在单因素试验结果基础上,以多酚提取率(Y)为考察指标,以料液比(A)、乙醇体积分数(B)、提取温度(C)、提取时间(D)为4个因素,每个因素选取3个水平,进行Box-Benhnken试验设计[14-17],优化狗尾草中多酚类物质的提取工艺。响应面试验因素与水平见表1。
表1 狗尾草多酚提取条件优化响应面试验因素与水平
Table 1 Factors and levels of response surface methodology for extraction conditions optimization of polyphenols from Setaria viridis
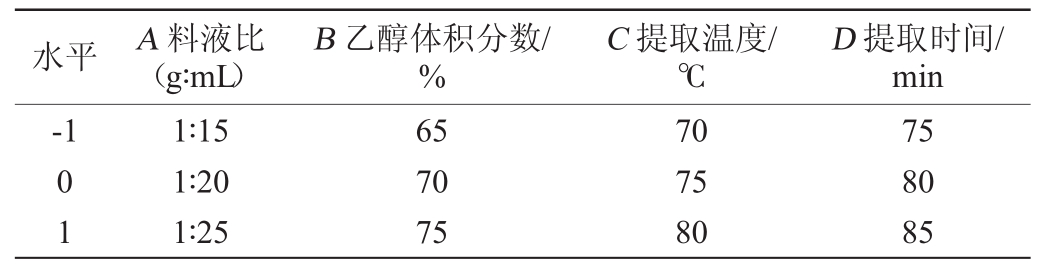
水平 A料液比(g∶mL)D提取时间/min-1 B乙醇体积分数/%C提取温度/℃0 1 1∶15 1∶20 1∶25 65 70 75 70 75 80 75 80 85
1.3.6 抗氧化活性测定
(1)羟基自由基(OH·)清除率
按照参考文献[18]的方法进行测定。以BHT作阳性对照,重复测定3次取平均值。OH·清除率计算公式如下:
式中:A1为空白对照组吸光度值;A2为样品组吸光度值;A3为蒸馏水代替水杨酸的溶液的吸光度值。
(2)超氧阴离子自由基(O2-·)清除测定
按照参考文献[19]的方法进行测定。以BHT作阳性对照,重复测定3次取平均值。O2-·清除率计算公式如下:
超氧阴离子自由基清除率=A0-A1+A2
A0×100%
式中:A0为空白对照组吸光度值;A1为样品组吸光度值;A2为蒸馏水代替邻苯三酚的溶液的吸光度值。
(3)DPPH自由基(DPPH·)清除能力测定
按照参考文献[20]的方法进行测定。以BHT作阳性对照,重复测量3次取平均值。DPPH·清除率计算公式如下:
式中:A1为样品组吸光度值;A2为无水乙醇代替DPPH的溶液的吸光度值;A3为空白对照组吸光度值。
2 结果与分析
2.1 没食子酸标准曲线
以焦性没食子酸质量浓度(x)为横坐标,吸光度值(y)为纵坐标,得到标准曲线,结果见图1。由图1可知,标准曲线回归方程为:y=0.443 9x+0.021 2,相关系数R2=0.990 6。

图1 没食子酸标准曲线
Fig.1 Standard curve of gallic acid
2.2 单因素试验
2.2.1 料液比对多酚提取率的影响

图2 料液比对狗尾草多酚提取率的影响
Fig.2 Effect of solid to liquid ratio on extraction rate of polyphenols fromSetaria viridis
由图2可知,随着料液比在1∶15~1∶25(g∶mL)的范围内增大,多酚提取率提高;当料液比达到1∶25(g∶mL)时,多酚提取率达到2.66%;继续增大料液比时,多酚提取率提高不显著;原因可能是开始时溶剂用量增加促进多酚的提取,当溶剂用量达到某一数值,增加溶剂用量相同的提取时间内提取效果提高不显著。因此,选取最佳料液比为1∶25(g∶mL)。
2.2.2 乙醇体积分数对多酚提取率的影响
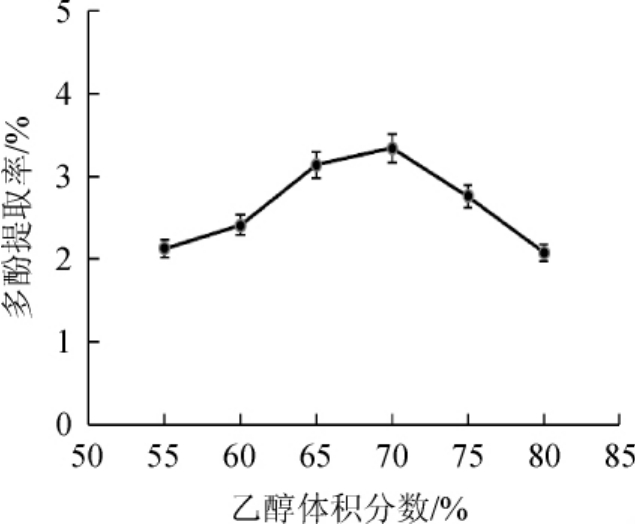
图3 乙醇体积分数对狗尾草多酚提取率的影响
Fig.3 Effect of ethanol volume fraction on extraction rate of polyphenols fromSetaria viridis
由图3可知,随着乙醇体积分数在55%~70%范围内的增加,多酚提取率提高;当乙醇体积分数为70%时,多酚提取率达到3.34%;再增加乙醇体积分数,多酚提取率降低;原因可能是不同乙醇体积分数极性不同,且多酚化合物极性较高,根据相似相溶原理,多酚在乙醇体积分数为70%时溶出效率最高。因此,选取最佳乙醇体积分数为70%。
2.2.3 提取温度对多酚提取率的影响
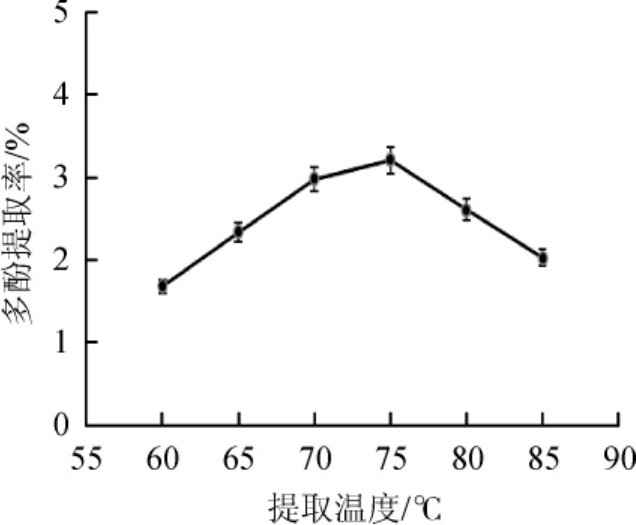
图4 提取温度对狗尾草多酚提取率的影响
Fig.4 Effect of extraction temperature on extraction rate of polyphenols fromSetaria viridis
由图4可知,随着提取温度在60~75℃范围内的升高,多酚提取率提高;当提取温度达到75℃时,多酚提取率达到3.21%;随着提取温度继续升高,多酚提取率降低;原因可能是多酚提取率随着温度升高而增加,但是温度过高,多酚结构遭到破坏,提取率降低。因此选取最佳提取温度为75℃。
2.2.4 提取时间对多酚提取率的影响
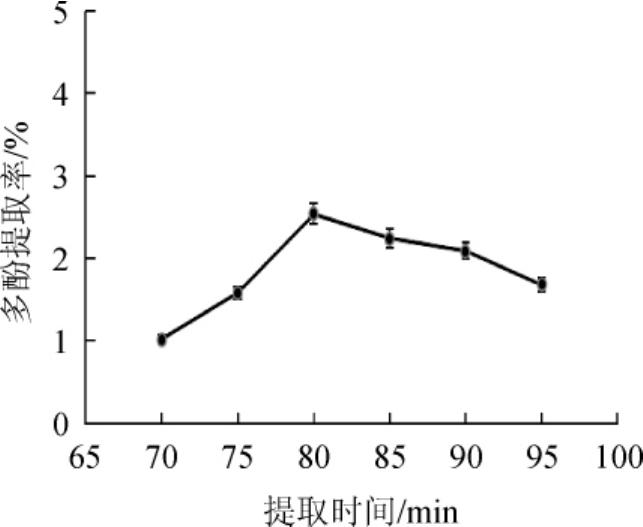
图5 提取时间对狗尾草多酚提取率的影响
Fig.5 Effect of extraction time on extraction rate of polyphenols fromSetaria viridis
由图5可知,随着提取时间在70~80min范围内的增加,多酚提取率提高;当提取时间为80 min时,多酚提取率达到2.54%;提取时间继续增加,多酚提取率降低;原因可能是当提取时间过短时,多酚提取不完全,提取时间过长时,多酚的稳定性降低,导致多酚提取率降低。因此选取最佳提取时间为80 min。
2.3 响应面法优化提取试验结果及分析
2.3.1 回归模型的建立及方差分析
响应面试验设计方案与结果见表2,回归方程方差分析的结果见表3。
根据Design Expert 8.0.6.1对表2试验数据进行的多元回归拟合,得到以多酚提取率为响应值的回归方程:
Y=3.51-0.049A+0.077B+0.035C+0.038D+0.25AB+0.023AC-0.033AD+0.15BC+0.13BD-0.15CD-0.38A2-0.27B2-0.38C2-0.26D2
表2 狗尾草多酚提取条件优化响应面试验设计与结果
Table 2 Design and results of response surface methodology for extraction conditions optimization of polyphenols from Setaria viridis
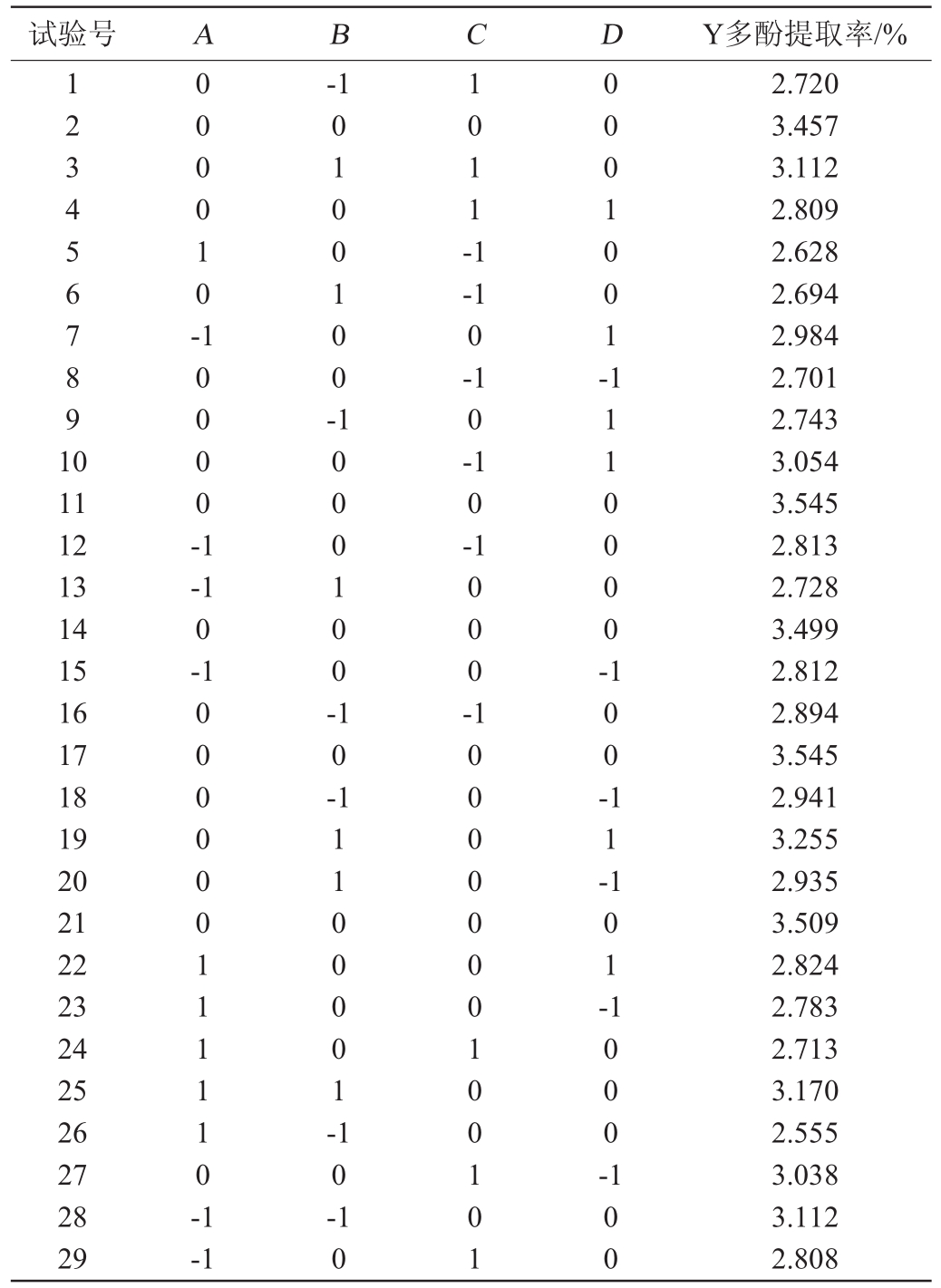
试验号 A B C D Y多酚提取率/%1 2 3 4 5 6 7 8 9 1 0 0 0 0 0 1 0--1 0 1 0 0 1 0 0-1 0 1 1-1 0 0 0 1 0 0 1-11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 1 0 0 0 0-1-1 0-1 0-1 0-1-1 0-1 1 1 1 0 0 0 0-0 0 0 0 0 0 1 1 1 1 1 0-1 1 0 0 0 1 0 0-1 0-0 0 0-1 1 1 0 0 0 0 1-1 0 0-1 1-1 0 1-1 0-1 0 0 0--1 1 0 1 0 0 0 0 0 0 0 1 0 0 1 0 1 1 0 0 2.720 3.457 3.112 2.809 2.628 2.694 2.984 2.701 2.743 3.054 3.545 2.813 2.728 3.499 2.812 2.894 3.545 2.941 3.255 2.935 3.509 2.824 2.783 2.713 3.170 2.555 3.038 3.112 2.808
由表3可以看出,回归模型极显著(P<0.001),失拟项不显著(P>0.05);回归方程调整决定系数R2adj=0.969 0,决定系数R2=0.919 8,表明该模型拟合程度较好。在所取的各因素水平范围内,影响狗尾草多酚提取率因素主次顺序为:乙醇体积分数>料液比>提取时间>提取温度,交互项AB、BC、BD、CD 极显著(P<0.001);二次项A2、B2、C2、D2对狗尾草多酚提取率均有极显著影响(P<0.001)。
2.3.2 响应面分析及最佳提取工艺研究
表3 回归方程方差分析
Table 3 Variance analysis of regression equation
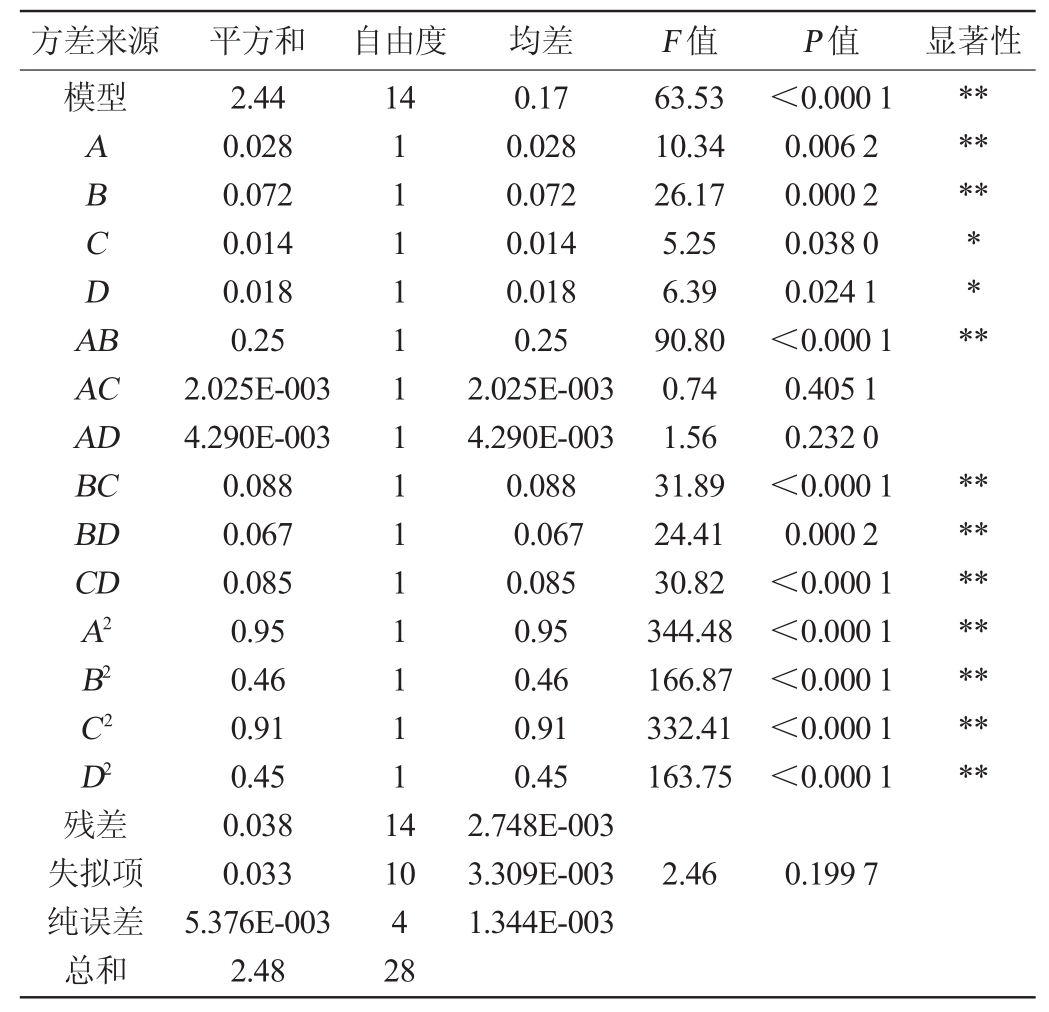
注:“*”表示差异显著(P<0.05);“**”表示差异极显著(P<0.01)。
方差来源 平方和 自由度 均差 F值 P值 显著性模型14 A B C D A B**********AC AD BC BD CD A2 B2 C2 D2 63.53 10.34 26.17 5.25 6.39 90.80 0.74 1.56 31.89 24.41 30.82 344.48 166.87 332.41 163.75<0.0001 0.0062 0.0002 0.0380 0.0241<0.0001 0.4051 0.2320<0.0001 0.0002<0.0001<0.0001<0.0001<0.0001<0.0001残差失拟项纯误差总和2.44 0.028 0.072 0.014 0.018 0.25 2.025E-003 4.290E-003 0.088 0.067 0.085 0.95 0.46 0.91 0.45 0.038 0.033 5.376E-003 2.48 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 4 10 4 28 0.17 0.028 0.072 0.014 0.018 0.25 2.025E-003 4.290E-003 0.088 0.067 0.085 0.95 0.46 0.91 0.45 2.748E-003 3.309E-003 1.344E-003 2.460.1997**************

图6 料液比、乙醇体积分数、提取温度、提取时间交互作用对狗尾草多酚提取率影响的响应曲面与等高线
Fig.6 Response surface plots and contour lines of effects of interaction between solid to liquid ratio,ethanol volume fraction,extraction temperature and time on extraction rate of polyphenols fromSetaria viridis
响应面可直观反映出各因素对响应值的影响,曲面越陡说明相关因素之间的交互作用越强[21]。从图6可以看出,各因素大小从四周逐渐趋向中心点时,曲面图呈凸起趋势,即多酚提取率趋向最大化,说明存在最大响应值。运用Design Expert 8.0.6.1软件对其结果进行分析,当理论响应值最大时,4个因素所对应的最佳值为料液比1∶20.11(g∶mL)、乙醇体积分数69.73%、提取温度79.90℃、提取时间75.21min时,在此条件下多酚提取率可达3.499%。
为方便操作,修改最佳条件为料液比1∶20(g∶mL)、乙醇体积分数70%、提取温度80℃、提取时间75 min,对狗尾草多酚提取率进行3次平行试验,结果显示多酚提取率平均值为3.234%。该实际值与理论值相近,因此利用响应面优化得到的工艺条件具有可行性。
2.4 狗尾草多酚的体外抗氧化活性
2.4.1 对羟基自由基的清除作用
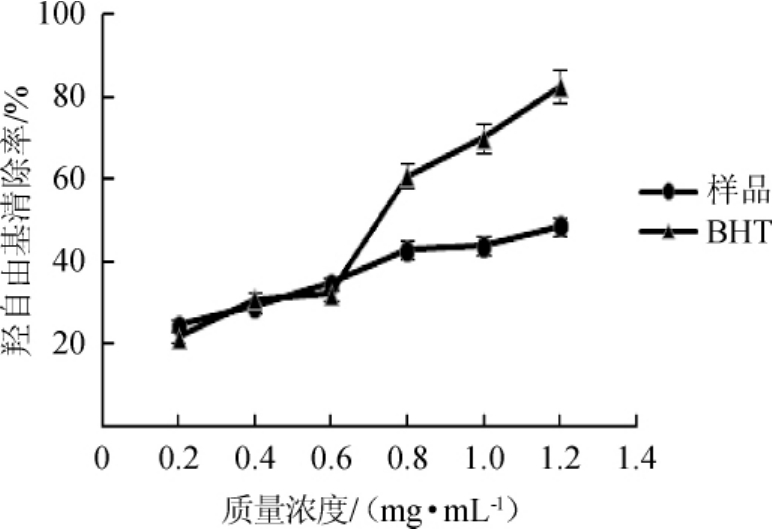
图7 狗尾草多酚对羟基自由基的清除效果
Fig.7 Scavenging effect of polyphenols fromSetaria viridison hydroxyl free radicals
由图7可知,随着狗尾草多酚和BHT质量浓度的增加,对羟基自由基的清除率均逐渐增大,当质量浓度为1.2 mg/mL时,BHT、狗尾草多酚对羟基自由基的清除率分别为(82.70±4.526)%、(48.56±3.457)%。
2.4.2 对DPPH自由基的清除作用

图8 狗尾草多酚对DPPH自由基的清除效果
Fig.8 Scavenging effect of polyphenols fromSetaria viridison DPPH radicals
由图8可知,随着狗尾草多酚和BHT质量浓度的增加,对DPPH自由基的清除率均逐渐增大,当质量浓度为0.4mg/mL时,其清除率分别为(65.34±4.190)%和(64.20±4.778)%。
2.4.2 对超氧阴离子自由基的清除作用
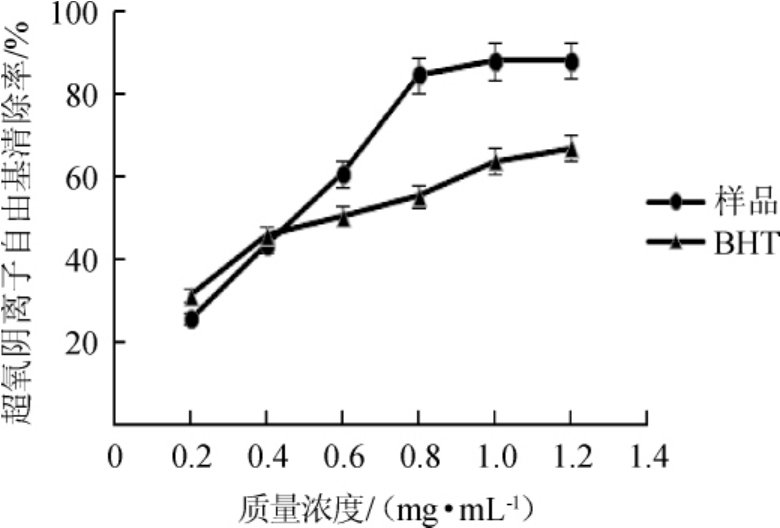
图9 狗尾草多酚对超氧阴离子自由基的清除效果
Fig.9 Scavenging effect of polyphenols fromSetaria viridison superoxide anion radical
由图9可知,低浓度时(<0.4 mg/mL),BHT清除超氧阴离子自由基能力高于狗尾草多酚的清除能力。当质量浓度>0.8 mg/mL以后,狗尾草多酚清除率趋于稳定,清除率最大值为(88.05±2.954)%;BHT对超氧阴离子的清除率逐渐增大,最大值为(66.93±4.229)%。
3 结论
本研究以狗尾草为原料提取多酚,以料液比、乙醇体积分数、提取温度、提取时间为考察因素,以提取率为响应值,在单因素试验基础上进行响应面回归方程确定狗尾草多酚提取工艺的最优条件为:料液比1∶20(g∶mL)、乙醇体积分数70%、提取温度80℃、提取时间75 min,在此条件下,狗尾草多酚提取率为3.234%,与理论值3.499%基本一致。影响狗尾草多酚提取率大小的因素顺序为乙醇体积分数>料液比>提取时间>提取温度。
抗氧化试验结果表明,狗尾草多酚可以有效的清除羟基自由基、超氧阴离子自由基和DPPH自由基,当样品质量浓度达到试验最大浓度时,清除率分别为(48.56±3.457)%、(88.05±2.954)%、(65.34±4.190)%,表现出较好的体外抗氧化活性。
[1]赵辉,郭静远,孔华,等.金刚砂辅助农杆菌转化狗尾草种子高效遗传转化体系的建立[J].分子植物育种,2017,15(12):4955-4960.
[2]成亮,刘宝玲,刘盼,等.青狗尾草Dof基因家族的全基因组鉴定及组织特异性表达分析[J].分子植物育种,2018,16(13):4226-4234.
[3]秦源源,张桓溥,罗富成,等.自然储藏过程中纳罗克非洲狗尾草种子活力及其营养含量动态[J].江苏农业科学,2018,46(15):139-141.
[4]张爱武,罗素琴,刘乐乐,等.狗尾草果实中总鞣质的提取和含量测定[J].内蒙古医学院学报,2012,34(1):26-29.
[5]张勇,周丽明,张超,等.苹果原花色素提取分离及其抗氧化作用[J].上饶师范学院学报,2018,38(6):56-60.
[6]张玉曼,王月,李乔,等.AM真菌影响入侵植物黄顶菊与本土物种狗尾草竞争生长的机理研究[J].西北植物学报,2015,35(6):1215-1221.
[7]赵辉,张丽丽,郭静远,等.氯化钠胁迫下模式植物狗尾草种子萌发期抗盐性鉴定与评价指标研究[J].热带作物学报,2017,38(12):2273-2279.
[8]李玉环.高湿对破除休眠农田狗尾草种子萌发及幼苗胚芽鞘生长的影响[J].种子,2017,36(5):101-104.
[9]潘文洁,郭雯.超声波辅助提取竹叶茶多酚工艺研究[J].中国林副特产,2011(4):16-18.
[10]张宇思,王成章,舒阿庆,等.响应面法优化超声波辅助提取豹皮樟多酚工艺[J].生物质化学工程,2014,48(5):19-23.
[11]赵梓燕.柑橘果实多甲氧基黄酮的提取、富集与分离纯化方法研究[D].重庆:西南大学,2018.
[12]杨楠,韩国庆,高建萍.正交试验法优选狗尾草中总黄酮提取工艺研究[J].内蒙古医科大学学报,2017,39(3):207-210,214.
[13]袁旭,伍小宇,李伟丽,等.郫县豆瓣的营养、多酚含量与抗氧化活性评价[J].食品与发酵工业,2018,44(9):270-274.
[14]欧阳玉祝,李雪峰,毛山山.响应面优化田基黄总多酚提取工艺[J].天然产物研究与开发,2013,25(12):1715-1721.
[15]陈亮,张炜,陈元涛,等.响应曲面法优化黑果枸杞多糖的超声提取工艺[J].食品科技,2015,40(1):220-227.
[16]赵旭,苏伟,文飞,等.糖化酶协同微生物酿造黑糯米酒工艺探究[J].食品科技,2016,41(2):287-291.
[17]张崇军,唐贤华,赵龙,等.响应面法优化大曲中黄曲霉毒素B1提取工艺[J].中国酿造,2018,37(12):132-136.
[18]李哲,李芬芳,袁德保,等.超声波辅助提取低褐变程度香蕉皮中总酚的研究[J].现代食品科技,2012,28(9):1166-1169,1172.
[19]郭庆启,张娜,姜元松,等.榛子仁蛋白酶解工艺的优化及酶解物抗氧化能力的研究[J].食品科学,2013,34(9):189-193.
[20]叶广彬,陈源红,王长丽,等.柠檬明串珠菌TD1产胞外多糖条件的响应面法优化及其抗氧化性研究[J].中国酿造,2018,37(11):70-75.
[21]何弥尔,王伟,吴立生,等.星点设计-效应面法优选灯盏花乙素超声提取工艺[J].中药材,2010,33(6):984-988.