Viili发酵乳是芬兰传统的乳制品,通常采用常温(28℃左右)发酵,具有良好的口感和令人愉快的风味,含有大量的多糖成分[1]。Viili发酵乳是由在乳酸菌、酵母菌和丝状真菌白地霉(Geotrichum candidum)等多种微生物共同发酵而成,因此Viili发酵乳不仅具有传统发酵乳的双乙酰风味和乙醛风味,同时还具有特殊的白地霉香味[2]。相较于保加利亚乳杆菌(Lactobacillus bulgaricus)和嗜热链球菌(Streptococcus thermophilus)发酵的发酵乳,具有独特的风味和品质。
Viili发酵乳不仅具有优良的风味品质,还具有抗疲劳[3]、调节免疫[4]、降低胆固醇[5]、抗氧化[6]等多种功能活性。近些年对Viili发酵乳的研究主要集中于对其胞外多糖以及菌种组成方面的研究[7-10],缺乏对Viili发酵性能及理化性质等方面的深入了解及产品的研发。由于Viili发酵乳菌相较为复杂,产酒精产气微生物的存在使Viili发酵乳酒精控制以及品质控制等问题越发突出,制约了其发酵产品的多元化发展。直投式酸奶发酵剂(direct-vat-set,DVS)具有菌相明确、高菌量、高菌活的菌种特点,并且能够方便快捷、安全有效的生产乳制品[11],已经成为商业乳制品发酵生产的主要方式。开发Viili直投式发酵剂能够解决Viili发酵过程菌相不明确的问题,可以通过控制发酵菌种得到优良稳定的Viili发酵产品,具有广泛的应用前景。
目前,我国发酵乳产品同质化现象较为严重,发酵菌种较为单一,因此,Viili直投式发酵剂及Viili发酵乳的研究与开发对发酵乳品的多元化具有十分重要的意义。针对上述问题,本研究以最优发酵条件下的Viili发酵乳为比较标准,通过对不同菌相的优化复配,开发发酵性能优良,并能够产生Viili特色风味和品质的直投式发酵剂,为后续Viili产品的开发提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 试验菌种
保加利亚乳杆菌(Lactobacillus bulgaricus)LB-DR、嗜热链球菌(Streptococcus thermophilus)St-G、乳酸乳球菌乳脂亚种(Lactococcus lactissubsp.cremoris)BY3、克鲁维毕赤酵母(Pichia kluyveri)NEER:本实验室保藏;假肠膜明串珠菌(Leuconostoc pseudomesenteroides)Lp-S、白地霉(Galactomyces candidum)Gc-S:筛选自Viili发酵乳。
1.1.2 化学试剂
Viili发酵乳:芬兰乳品Valio集团;三氯乙酸(trichloroacetic acid,TCA):天津市福晨化学试剂有限公司;邻苯二胺、双乙酰标准品:国药集团化学试剂有限公司;可溶性淀粉、亚硫酸氢钠、碳酸氢钠:天津市天利化学试剂有限公司。实验所用试剂均为分析纯或生化试剂。
1.1.3 培养基
脱脂乳培养基:将脱脂奶粉溶于水,配制成质量分数为12%的复原乳,100℃灭菌15 min;MRS培养基:北京奥博星生物技术有限公司。
1.2 仪器与设备
721可见分光光度计:上海菁华科技仪器有限公司;7al-16a高速冷冻离心机:德国海蒂诗有限公司;FE20KpH计:梅特勒-托利多仪器(上海)有限公司;SKP-02.300恒温培养箱:黄石市恒丰医疗器械有限公司;NDJ-5S数字式黏度计:上海佑科仪器仪表有限公司。
1.3 方法
1.3.1 Viili发酵乳制备及前处理
将Viili发酵乳以3%接种量接入灭菌脱脂乳培养基中28℃进行培养[5-6],每隔2 h进行取样分成两组。一组不进行处理,直接进行pH值、酸度、持水力(water holding capacity,WHC)以及表观黏度的测定;另一组取适量不同发酵时间的Viili发酵乳,加入等体积的16%三氯乙酸(TCA)溶液,充分混匀后静置10 min,在4℃的离心机中以4 500 r/min离心10min,将上清液再用滤纸进行过滤,取澄清上清液用于双乙酰含量及乙醛含量测定[12]。
1.3.2 菌株复配分组及样品处理
根据对Viili菌种组成的相关文献[13-15]及实验室前期利用Illumina测序和聚合酶链式反应-变性梯度凝胶电泳(polymerase chain reaction-denaturing gradient gel electrophoresis,PCR-DGGE)技术对Viili发酵乳研究结果选取5株乳酸菌、1株酵母菌、1株霉菌作为复配菌种,乳酸菌和酵母菌分别经过两次活化后进行不同组合复配发酵,以3%接种到灭菌脱脂乳培养基中28℃进行培养发酵,每间隔1 h进行pH值测定,同时对7组的凝乳时间进行观察。发酵乳处理方法如1.3.1,分组方式如下:
V1组:St-G+LB-DR(162∶16);V2组:St-G+LB-DR+BY3(162∶16∶8);V3组:St-G+LB-DR+Lp-S(162∶16∶14);V4组:St-G+LB-DR+BY3+Lp-S(162∶16∶8∶14);V5组:St-G+LB-DR+BY3+Lp-S+Gc-S(162∶16∶8∶14∶74);V6组:St-G+LB-DR+BY3+Lp-S+NEER(162∶16∶8∶14∶1);V7组:St-G+LB-DR+BY3+Lp-S+Gc-S+NEER(162∶16∶8∶14∶74∶1)。
1.3.3 分析检测
(1)pH值的测定
使用pH计直接测定不同发酵时间Viili发酵乳的pH值。(2)酸度的测定
参照国标GB5009.239—2016《食品安全国家标准食品酸度的测定》中的方法进行测定。
(3)持水力的测定[16]
在10 mL离心管中加入5 mL不同发酵时间的发酵乳样品,以3 000 r/min离心10 min后,静置10 min后弃去上清液,测定剩余的质量,样品的持水力计算公式如下:式中:WHC为样品持水力,%;W0为空10 mL离心管质量,g;W1为样品与离心管的总质量,g;W2为剩余样品与离心管总质量,g。
(4)表观黏度的测定[17]
用黏度计三号转子以30 r/min常温条件下测定其表观黏度。
(5)双乙酰含量的测定[12]
乙酰酰标准曲线绘制:取20 μL双乙酰(2,3-丁二酮)标准品,蒸馏水定容至500 mL,分别取0、2.0 mL、4.0 mL、6.0mL、8.0mL、10.0mL于空试管中用水补足到10mL。每个试管中再加入10 mL的16%三氯乙酸。取12支编号的试管分别加入上述不同浓度的样品10 mL分两排摆放,每排6支试管。第一排试管中加入0.5 mL的1%的邻苯二胺溶液,第二排试管不加作为空白对照,将试管摇匀后置于黑暗处。反应30 min后加入4.0 mol/L盐酸终止反应,第一排试管加2.0 mL盐酸,第二排试管加2.5 mL盐酸,振荡混匀后以第二排试管空白作为参比液,在波长335 nm条件下测定吸光度值。以双乙酰质量浓度(x)为横坐标,吸光度值(y)为纵坐标绘制双乙酰标准曲线。
样品中双乙酰浓度的测定:取1.3.1节中处理好的各个样品澄清液,用16%的三氯乙酸溶液稀释适当的倍数,按照双乙酰标准曲线的方法测定样品吸光度值,使其范围在0.2~1.0之间,再根据双乙酰标准曲线回归方程计算Viili样品中双乙酰质量浓度(mg/L),如果样品稀释则再需要乘以稀释倍数得到样品中双乙酰含量。
(6)乙醛含量的测定[12]
取1.3.1节中处理好的各个样品的上清液10 mL,加入1%的NaHSO3溶液2.0 mL于250 mL具塞三角瓶中,摇匀后在室温状态下静置1 h,加入1 mL1%淀粉溶液,先用浓度为0.10 mol/L的碘标准溶液滴定至临近终点,再用浓度为0.01mol/L碘标准溶液滴定至终点(溶液呈淡蓝紫色,且30s内不褪色),不计数。再加入20 mL的1 mol/L的NaHCO3溶液,混匀至溶液蓝紫色消失,用0.01 mol/L碘标准溶液滴定至终点,此时记录消耗的标准碘液的体积,同时做空白试验。乙醛含量计算公式如下:式中:V1为样品滴定消耗I2标准溶液的体积,mL;V2为空白滴定消耗I2标准溶液的体积,mL;C为1/2 I2标准溶液的浓度,mol/L;0.022为乙醛化学反应基本单位,g;10为乙醛样品体积,mL。
2 结果与分析
2.1 双乙酰标准曲线的建立
以双乙酰质量浓度(x)为横坐标,吸光度值(y)为纵坐标绘制双乙酰标准曲线,结果见图1。
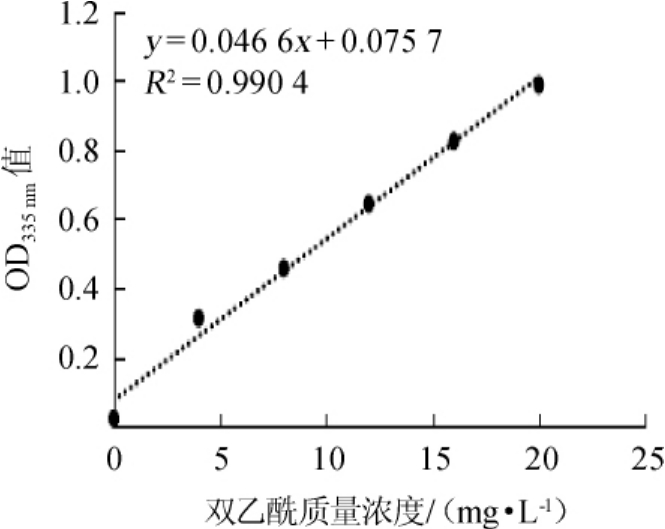
图1 双乙酰标准曲线
Fig.1 Standard curve of diacetyl
由图1可知,双乙酰质量浓度范围为0~20 mg/L,标准曲线线性回归方程为y=0.046 6x+0.075 7,相关系数为R2=0.990 4>0.99,表明双乙酰标准液质量浓度与吸光度值之间呈良好的线性关系,可以用于双乙酰含量测定。
2.2 Viili发酵乳不同发酵时间理化性质
不同发酵时间的Viili发酵乳基本理化指标见图2。由图2A可知,在Viili发酵乳发酵前12 h的pH值从6.34迅速下降到4.69,而12~24 h内的pH值变化较小基本维持在4.4左右。而酸度的变化在前12 h酸度由13.2°T显著上升至91.85°T,12h后变化较小,维持在100.65°T左右。由图2B可知,发酵前12 h的Viili发酵乳持水力呈现逐渐增加的趋势,而后12~24 h持水力有小幅度增加,最终到24 h增加至66.5%。由图2C可知,由于胞外多糖的累积导致Viili发酵乳的表观黏度持续增加,在24 h达到最高值为10 440 mPa·s。由图2D和2E可知,发酵乳中双乙酰含量以及乙醛含量在0~12 h均呈现递增趋势且在12 h含量达到顶峰,即双乙酰含量达到15.672mg/L,乙醛含量达到10.63mg/L。而后12~24 h双乙酰含量以及乙醛含量均呈现下降的趋势。
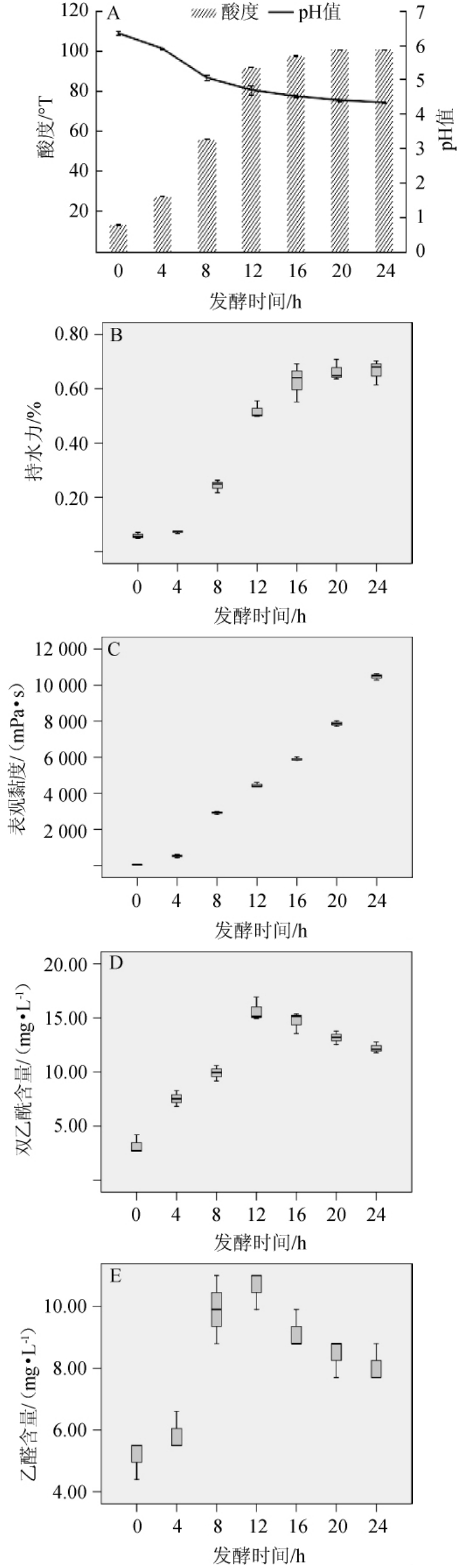
图2 不同发酵时间的Viili发酵乳基本理化指标
Fig.2 Basic physical and chemical indexes of Viili fermented milk
with different fermentation time
综上所述,Viili发酵乳最适发酵时间为12 h,此时pH值为4.69,酸度为91.85°T,持水力为51.78%,表观黏度为4457mPa·s,双乙酰含量为15.67mg/L,乙醛含量为10.63mg/L。
2.3 菌株复配发酵酸奶pH值及凝乳时间的测定
将活化后的5株菌及白地霉孢子悬浊液按比例分组接入12%脱脂奶中,28℃条件下恒温发酵,不同分组的菌株复配发酵酸奶的pH变化曲线见图3,同时观察凝乳时间,结果见表1。
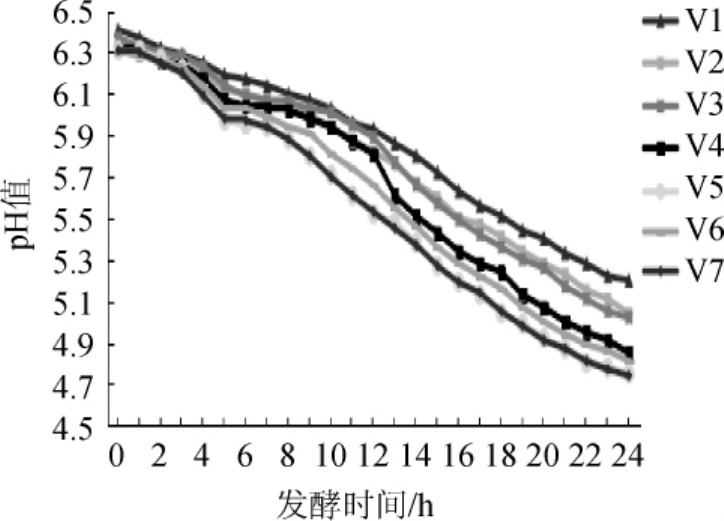
图3 不同组别酸奶发酵过程中的pH值变化
Fig.3 Change of pH of yoghurt during fermentation process with different groups
表1 不同组别酸奶发酵过程中的凝乳时间
Table 1 Curding time of yoghurt during fermentation process with different groups

组别 凝乳时间/h 组别 凝乳时间/h V1 V2 V3 V4 30 24 23 21 V5 V6 V7 19 20 19
由图3可知,随着发酵时间延长,7组发酵酸奶pH均呈下降趋势,7组都是在0~3 h内pH值变化不明显,因为此时菌株基本处于延滞期,菌株生长缓慢,在3 h后产酸加快7组产酸量逐渐拉开差距。由表1可知,添加真菌组(V5、V6、V7)产酸速度明显高于纯乳酸菌发酵组(V1、V2、V3、V4),且添加真菌组较纯乳酸菌发酵组凝乳时间明显缩短。纯乳酸菌发酵组中V4组产酸速度明显高于其余三组。由此可以得出,V5组和V7组发酵乳产酸能力较好,具有较短的凝乳时间(19 h)。
2.4 菌株复配发酵酸奶的理化性质
7组不同菌株复配酸奶发酵完成后,对7组酸奶进行基础理化指标测定,结果见图4。
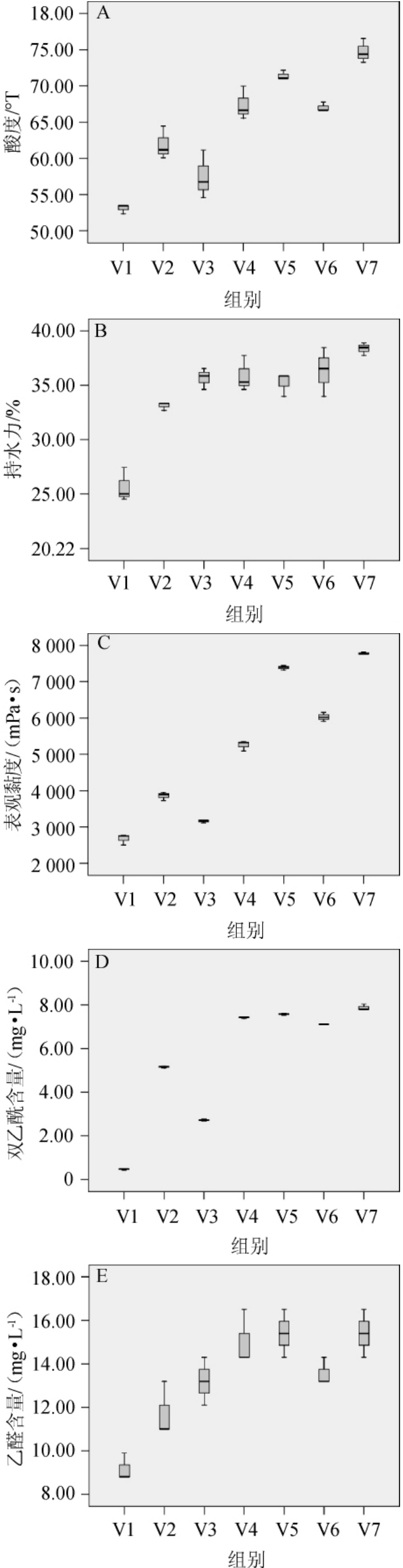
图4 不同组别发酵酸奶的基本理化指标
Fig.4 Basic physical and chemical indexes of fermented yoghurt in different groups
由图4可知,V7组呈现出较优异的理化性质。只添加乳酸菌的四组中,V4组的各项理化指标较优于其他三组,证明本试验所用四组乳酸菌:嗜热链球菌St-G、保加利亚乳杆菌LB-DR、乳酸乳球菌乳脂亚种BY3、假肠膜明串珠菌Lp-S可在牛乳中协同发酵,且V1、V2、V3、V4的各个理化指标含量除乙醛含量外,均是呈现V4>V2>V3>V1。添加真菌的三组V5、V6、V7各项指标均高于纯乳酸菌发酵的组别,白地霉Gc-S和克鲁维毕赤酵母NEER共同存在的V7组的酸度为74.73°T,持水力为38.10%,表观黏度为7780mPa·s,双乙酰含量为7.87 mg/L,乙醛含量为15.4 mg/L。
2.5 Viili发酵乳与菌株复配酸奶理化性质比较
将与Viili发酵乳类似菌株进行复配,且选择复配菌株酸奶理化性质最优异的V7组与Viili发酵乳理化性质进行对比,结果见表2。
表2 复配发酵酸奶与Viili发酵乳理化性质比较
Table 2 Comparison of physical and chemical properties of compound fermented yoghurt and Viili fermented milk
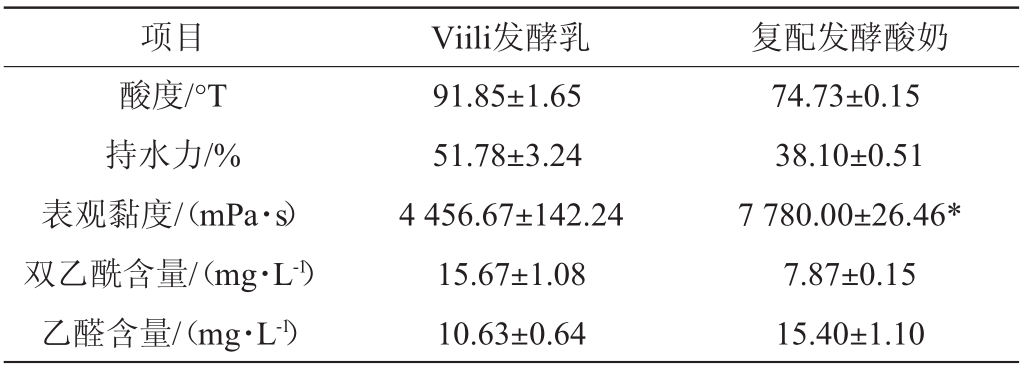
注:“*”表示差异显著(P<0.05)。
项目 Viili发酵乳 复配发酵酸奶酸度/°T持水力/%表观黏度/(mPa·s)双乙酰含量/(mg·L-1)乙醛含量/(mg·L-1)91.85±1.65 51.78±3.24 4 456.67±142.24 15.67±1.08 10.63±0.64 74.73±0.15 38.10±0.51 7 780.00±26.46*7.87±0.15 15.40±1.10
由表2可知,复配菌株发酵V7组与Viili发酵乳12 h的理化性质相对比,复配菌株组与Viili发酵乳的表观黏度有显著差异(P<0.05),复配菌株组呈现更好的表观黏度;复配菌株发酵酸奶V7组在酸度、持水力、双乙酰含量均略低于Viili发酵乳,但二者差异不显著(P>0.05);复配菌株发酵酸奶最适发酵时间为19 h,与Viili发酵乳发酵时间(12 h)相比时间较长。结果表明,本试验所选的复配菌株以及菌株间比例较为合适,可用于后续Viili发酵乳直投式发酵剂的开发。
3 讨论
pH值、酸度、持水力和表观黏度是衡量发酵乳产品重要的理化指标。发酵乳凝乳的主要原因是发酵乳中的乳酸菌发酵牛乳中乳糖产生乳酸,乳酸的增加使发酵乳的整体pH值下降,当pH值降至4.6~4.7时达到酪蛋白的等电点[18],使奶中形成的酪蛋白胶粒开始聚集沉降,蛋白质网络立体结构随着酪蛋白胶粒的聚集逐渐形成[19],使流动的奶变成半固体的凝胶体—凝乳[20-21]。这个过程会伴随持水力以及表观黏度值的变化。
发酵乳的酸度主要是乳酸菌通过发酵脱脂奶中的乳糖产生乳酸引起的,pH值和酸度的高低不仅关系到发酵乳的风味[22],还影响发酵乳的凝胶特性。凝固型发酵乳持有全部或者部分自身水的能力被定义为发酵乳的持水力。持水力和表观黏度反映出酸奶的质构及流变特性。持水力和表观黏度的增加体现了发酵乳中凝胶交联增加、无乳清析出,即发酵乳肉眼可见的黏稠、易贴壁,且口感浓醇[23]。Viili发酵乳中含有丰富的微生物种类,微生物的生长代谢过程会在Viili发酵乳中形成一层较厚的黏液样的胞外多糖[24],有文献报道胞外多糖能够增强酸的的持水能力,可以有效防止乳清的析出,能够较长时间的维持发酵乳的品质[25]。因此在Viili发酵乳发酵12~24 h表观粘度持续增加,持水力有小幅增加。
除品质以外,风味气味也是衡量酸奶品质的重要标准。双乙酰和乙醛是发酵乳中主要的香气成分。双乙酰一般由嗜温乳酸球菌生产,包括乳酸乳球菌丁二酮亚种(Lactococcus lactissubsp.biovar diacety lactis)、肠膜明串珠菌肠膜亚种(Leuconostoc mesenteroidessubsp.mesenteroides)、链球菌和热链球菌等[26]。有文献证明[27]发酵乳制品发酵时间过长会导致双乙酰和乙醛含量降低,根据双乙酰的发酵代谢途径,双乙酰在发酵后期能在3-羟基丁酮脱氢酶的作用下可逆地生成3-羟基丁酮,并进一步转化为2,3-丁二醇,导致双乙酰含量下降。而乙醛则是因为发酵过程乙醛还原酶的存在使发酵乳中乙醛的含量出现降低的现象[28]。Viili的风味品质与其菌种组成有密切关系,其中乳酸菌、酵母菌和白地霉共同形成了Viili的独特风味。国外工厂为方便Viili发酵乳的市场销售,将其中传统酵母菌替换成无醇酵母,虽降低了Viili特有酒香[3],但保留了Viili发酵乳多菌发酵的奶香。因此,在本研究的直投式发酵剂中,进行了三类菌相的不同复配组合,选取发酵乳主要香气成分乙醛和双乙酰作为香气衡量指标。
嗜热链球菌St-G、保加利亚乳杆菌LB-DR、假肠膜明串珠菌Lp-S、乳酸乳球菌乳脂亚属BY3这四株菌可以在牛乳中协同发酵加速产酸,从而达到缩短发酵时间的效果。乳酸乳球菌乳脂亚属BY3可将牛奶中的乳糖发酵形成乳酸,降低牛乳中pH值,进而产生风味物质双乙酰和乙醛,因此V2、V3、V4组各项指标均高于V1组。复配发酵酸奶在乙醛含量中V3>V2,主要原因推测在本试验中所用的乳酸乳球菌乳脂亚属BY3和假肠膜明串珠菌Lp-S均具有良好的产乙醛特性,但是由于最初接种量假肠膜明串珠菌Lp-S相对较多,因此在复配发酵酸奶中V3组含量较V2组多。由V6组可以看出,虽然克鲁维毕赤酵母NEER添加量较少,但是对酸奶pH值起到积极影响。主要原因是克鲁维毕赤酵母NEER属于非酿酒酵母,在发酵过程中可以产生甘油、挥发酸、琥珀酸和乳酸等代谢产物,可以增加酸奶中酸度,降低pH值促使蛋白质达到等电点产生凝胶现象,以此缩短凝乳时间,同时促进香味产生[29]。白地霉可以产生脂肪酶和蛋白酶,白地霉通过其在蛋白质代谢和脂肪代谢途径增加了奶制品的香气和口感滋味。部分白地霉可以产生氨肽酶,这种酶可以降解奶制品中低分子质量肽,在奶制品的风味中起到降低肽产生的苦味增加独特香味的作用。V5、V7组pH值变化曲线基本重叠且凝乳时间相同,说明在混菌发酵中白地霉Gc-S会增加产酸能力,并且白地霉Gc-S对产酸的影响远远大于克鲁维毕赤酵母NEER的影响。同时有文献报道酵母菌和白地霉混合培养对奶酪香气化合物形成具有一定的积极影响[30]。
本研究得到V7组具有优良稳定的发酵性能,综合理化性质良好,且品质更接近于Viili发酵乳。嗜热链球菌(Streptococcus thermophilus)St-G、保加利亚乳杆菌(Lactobacillus bulgaricus)LB-DR、乳酸乳球菌乳脂亚种(Lactococcus lactissubsp.cremoris)BY3、假肠膜明串珠菌(Leuconostoc pseudomesenteroides)Lp-S、白地霉(Galactomyces candidum)Gc-S和克鲁维毕赤酵母(Pichia kluyveri)NEER明确的菌种组合解决了Viili发酵过程中菌相复杂,难以控制的问题,并保留了Viili发酵乳的黏稠、表面具有丝状绒毛的特征属性及独特的风味。
4 结论
本研究结果表明V7组为最优菌相复配组合发酵剂,为嗜热链球菌St-G、保加利亚乳杆菌LB-DR、乳酸乳球菌乳脂亚种BY3、假肠膜明串珠菌Lp-S、白地霉Gc-S和克鲁维毕赤酵母NEER以162∶16∶8∶14∶74∶1比例进行复合,其在28 ℃发酵条件下发酵19 h后所产发酵乳与Viili发酵乳理化性质最为接近,可作为Viili直投式发酵剂用于多元化Viili发酵乳产品的研发。
[1]HEFA C.Volatile flavor compounds in yogurt:A review[J].Crit Rev Food Sci Nutr,2010,50(10):938-950.
[2]王豪,刘振民,章慧.酸马奶和维利的研究进展[J].食品科学,2016,37(3):247-252.
[3]CHENG L.Viili as fermented food in health and disease prevention:a review study[J].J Agr Sci Food Technol,2016,2(7):105-113.
[4]WU J,LI M,LIU L,et al.Nitric oxide and interleukins are involved in cell proliferation of RAW264.7 macrophages activated by Viili exopolysaccharides[J].Inflammation,2013,36(4):954-961.
[5]刘晶.Viili中乳酸菌的分离及其胞外多糖的研究[D].保定:河北农业大学,2015.
[6]陈杨扬.副干酪乳杆菌VL8胞外多糖(VL8-EPS)的结构与免疫活性研究[D].保定:河北农业大学,2017.
[7]李萌,王昌禄,王玉荣,等.Viili中乳酸菌的分离及对秀丽线虫寿命的影响[J].中国酿造,2010,29(5):124-126.
[8]王勇,刘勇,罗成,等.Viili中乳酸菌的初步分离和鉴定[J].安徽农业科学,2010,38(6):2831-2832,2853.
[9]陈廷涛,Viili中益生菌的分离及其发酵性质研究[J].中国微生态学杂志,2009,21(12):1064-1069.
[10]刘旭川,王勇,罗成,等.Viili中霉菌的分离纯化与鉴定[J].食品科学,2010,31(3):207-208.
[11]陈旭峰,史改玲,樊伟鑫,等.开菲尔直投式发酵剂在益生菌干酪生产中的应用研究[J].中国酿造,2018,37(7):35-41.
[12]胡凯丽,唐俊妮,龙虎,等.牦牛、牛酸乳发酵过程中品质特性的变化规律[J].食品工业科技,2018,39(3):17-21
[13]MACORI G,COTTER P D.Novel insights into the microbiology of fermented dairy foods[J].Curr Opin Biotechnol,2018,49:172-178.
[14]WANG S Y,CHEN H C,DAI T Y,et al.Identification of lactic acid bacteria in Taiwanese ropy fermented milk and evaluation of their microbial ecology in bovine and caprine milk[J].J Dairy Sci,2011,94(2):630-635.
[15]SUBROTA H,SUJIT D,SURAJIT M.Engineering tools in the beverage industry[M].London:Woodhead Publishing,2019:101-136.
[16]ILYAS A.Functional kefir production from high pressure homogenized hazelnut milk[J].LWT-Food Sci Technol,2019,107:256-263.
[17]PANG Z,XU R,LUO T,et al.Physiochemical properties of modified starch under yogurt manufacturing conditions and its relation to the properties of yogurt[J].J Food Eng,2019,245:11-17.
[18]张兰威,梁金钟.发酵食品工艺学[M].北京:中国轻工业出版社,2011:75-77.
[19]BEZERRA M F,SOUZA D F S,CORREIA R T P.Acidification kinetics,physicochemical properties and sensory attributes of yoghurts prepared from mixtures of goat and buffalo milks[J].Int J Dairy Technol,2012,65(3):437-443.
[20]MCCANN T H,FABRE F,DAY L.Microstructure,rheology and storage stability of low-fat yoghurt structured by carrot cell wall particles[J].Food Res Int,2011,44(4):884-892.
[21]ZARE F,BOYE J I,ORSAT V,et al.Microbial,physical and sensory properties of yogurt supplemented with lentil flour[J].Food Res Int,2011,44(8):2482-2488.
[22]MITALI M,SUBROTA H.Fermented beverages and their health benefits[M].London:Woodhead Publishing,2019:1-29.
[23]KOK C R,HUTKINS R.Yogurt and other fermented foods as sources of health-promoting bacteria[J].Nutr Rev,2018,76(1):4-15.
[24]陈岑,韩艳丽,曹正,等.不同直投式酸奶发酵剂发酵性能的比较研究[J].中国酿造,2017,36(1):126-130.
[25]ADESULU-DAHUNSI A T,SANNI A I,JEYARAM K,et al.Extracellular polysaccharide fromWeissella confusaOF126:Production,optimization,and characterization[J].Int J Biol Macromol,2018,111:514-525.
[26]MARSILI R.Flavors and off-flavors in dairy foods[M]//Encyclopedia Dairy Sciences.New York:Academic Press,2011:533-551.
[27]MAURICE G A.Handbook for sensory and consumer-driven new product development[M].London:Woodhead Publishing,2017:259-280.
[28]SHERIDAN M K,ELIAS R J.Reaction of acetaldehyde with wine flavonoidsin the presence ofsulfur dioxide[J].J Agr Food Chem,2016,64(45):8615-8624.
[29]FIORDA F A,VINICIUS D M P G,THOMAZ-SOCCOL V,et al.Microbiological,biochemical,and functional aspects of sugary kefir fermentation-A review[J].Food Microbiol,2017,66:86-95.
[30]MARTIN N,BERGER C,SPINNLER H E.Sensory and instrumental flavor analysesofcheese curd cocultured with selected yeast and bacteria[J].J Sens Stud,2002,17(1):1-17.