白酒中98%是乙醇和水,2%是一些微量物质,而白酒的独特风味主要来源于这些微量物质[1]。在白酒微量物质中,含量最多且对白酒影响最大的就是酯类,酯类是组成白酒香味的主要物质,主要的酯类有四种,分别是己酸乙酯、乳酸乙酯、乙酸乙酯、丁酸乙酯[2]。酱香型白酒中酯类化合物成分种类很多,乙酸乙酯和乳酸乙酯在酱香型白酒中含量均很高,它们是形成白酒香味的重要物质,其中酱香型酒代表茅台酒中乙酸乙酯和乳酸乙酯的比率为1∶1左右[3-5]。国标GB/T 26760—2011《酱香型白酒国家标准》[6]中规定优级酒总酯含量(以乙酸乙酯计)≥2.2 g/L,一级酒总酯含量(以乙酸乙酯计)≥2.0 g/L。
目前,对中国白酒酿造大曲产酯菌种的研究主要集中在酵母菌和霉菌[7-10],而对细菌的研究报道目前还比较少,因此,加强对产酯细菌的研究显得很有必要。本研究旨在从酱香型窑醅中筛选出产酯能力较强的菌株,并从形态观察、生理生化试验和16S rRNA分子生物学等方面鉴定该菌种,并运用顶空固相微萃取技术(headspace solid phase microextraction technology,HS-SPME)和气质联用(gas chromatography massspectrometry,GC-MS)对分离菌株的产酯能力及代谢产物进行测定,为后期进一步的研究和白酒中的应用奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
酱香型白酒窖醅样品:四川郎酒股份有限公司;麸皮:四川省自贡市某饲料加工厂。
1.1.2 化学试剂
葡萄糖(分析纯)、蛋白胨、牛肉膏、琼脂(均为生化试剂):北京奥博星生物技术有限责任公司;其他试剂均为分析纯。
1.1.3 培养基
筛选培养基[11]:蛋白胨10 g,牛肉膏3 g,NaCl 5 g,琼脂20 g,三丁酸甘油酯4 mL,蒸馏水1 L,pH 7.4~7.6。
基本培养基:蛋白胨10 g,牛肉膏3 g,NaCl5 g,琼脂20 g,蒸馏水1 L,pH 7.4~7.6。
发酵培养基:蛋白胨10 g,牛肉膏3 g,NaCl 5 g,蒸馏水1 L,pH 7.4~7.6。
麸皮固体培养基:麸皮700 g,花生米粉300 g,蒸馏水1 L。以上培养基灭菌条件为121℃、15 min。
1.2 仪器与设备
6890N-5975B气质联用仪:安捷伦科技(中国)有限公司;TG-16离心机:四川蜀科仪器有限公司;SHP-80生化培养箱:常州普天仪器制造有限公司金坛市晶玻实验仪器厂;SW-CJ-IF净化工作台:苏净集团苏州安泰空气技术有限公司;V-1000可见分光光度计:翱艺仪器(上海)有限公司。SKY-2102C恒温培养振荡器:上海苏坤实业有限公司。
1.3 试验方法
1.3.1 产酯菌株的筛选
(1)产酯菌株的初筛:将酱香型窖醅研磨成粉,称取25 g于装有225 mL无菌生理盐水的三角瓶中,振荡30 min得到菌悬液。取菌悬液,按10倍梯度稀释到10-7,取各稀释度菌悬液0.2 mL均匀涂布于筛选培养基上,置于37℃恒温培养箱中培养24 h。产酯细菌产生的一种酯酶能够分解或者合成甘油三酯的酯类,并且在适当的条件下还可以合成其他酯类[12-14]。若筛选培养基上出现透明圈则表明该菌种能产酯酶,并利用了三丁酸甘油酯,将具有明显透明圈的菌落挑出,并纯化至由单菌落,再于4℃冰箱斜面保存。
(2)产酯菌株的复筛:将初筛获得的菌种活化,重复透明圈实验,使用游标卡尺测定透明圈直径(D)和菌落直径(d),并计算出透明圈直径和菌落直径的比值(D/d),D/d值越大分解或者合成酯类的能力越强[11],筛选出D/d值较大的菌株进行后续试验。
(3)产酯优良菌株的选择:将复筛获得的菌种活化后,制作成菌浓度为106 CFU/mL种子液,并以5%的接种量接种于液体发酵培养基中,在37℃、150 r/min摇床培养24 h。用指示剂法[15-16]测定复筛菌种的产酯量,最后选择1株产酯量最高的菌株作进一步研究。
1.3.2 产酯优良菌株的鉴定
(1)形态观察及生理生化试验:将筛选出的一株产酯优良菌株在基本培养基上进行划线分离纯化,37℃培养24 h,对单菌落进行革兰氏染色[17],观察其显微镜下个体形态,并通过各项生理生化试验[18-19],包括芽孢染色试验、淀粉水解试验、蛋白水解试验和接触酶试验。
(2)分子生物学鉴定:提取筛选菌株的脱氧核糖核酸(deoxyribonucleoside,DNA)基因组,通过聚合酶链式反应(polymerase chain reaction,PCR)扩增技术获取目的基因DNA片段,并测序,PCR扩增条件:94℃预变性5 min;94℃变性30 s,50℃退火30 s,72℃延伸1 min,35次循环;最后72℃延伸10 min。从Genebank中选择同源性亲近的几株菌株的16S rDNA基因序列,采用Clustalx 1.83软件进行序列多重比较,用Mega 5.0软件进行统计和聚类分析,构建系统发育树,并对所构建的系统发育树进行评估[20-21]。
1.3.3 产酯香气物质的测定
将产酯优良菌株接种于麸皮固体培养基,37℃发酵4 d,采用顶空固相微萃取-气质联用(HS-SPME-GC-MS)技术对其产生的香气物质进行分析。
(1)顶空固相微萃取条件:50/30μmDVB/CAR/PDMS固相微萃取,为了使固定相更好的附在柱子的内壁上,第一次使用时需于气相色谱进样口230℃老化2 h,高温可以去除一些杂质和溶剂,看到气相上的基线平稳后就可以进行下一步操作。称取5 g发酵产物,水10 mL于15 mL顶空瓶中,为了减少被分析物(有机物)在水溶液中的可溶性,使更多的挥发性物质挥发至溶液的顶空,吸附到纤维头上,在顶空瓶中加入1.5 g NaCl,混匀后置于60℃水浴顶空吸附30 min,解吸3 min,用于GC-MS分析。
(2)气相色谱条件:DB-WAX毛细管色谱柱(60 m×250μm,0.25μm),手动无分流进样,进样口温度250℃,程序升温:初始温度40℃,保留1 min,以3℃/min的速率升至180℃,再以2.5℃/min的速率升至230℃,保留10 min,汽化室温度250 ℃,载气氦气(He),流速2.5 mL/min[22-23]。
质谱条件:电子电离(electronic ionization,EI)源,电子能量70 eV,扫描范围10~500 m/z,离子源温度250℃,接口温度230℃。
(3)定性定量方法
定性:化合物经计算机检索,同时与美国国家标准技术研究所(national institute of standards and technology,NIST)和Wiley 6.0相匹配。本研究只报道匹配度和纯度>850的鉴定结果。
定量:按照峰面积归一化计算相对百分含量。
1.3.4 数据处理
实验操作重复3次,每个样品设3个平行,采用Origin 8.5和SPSS 20.0软件进行数据分析,测定结果以平均值±标准差表示。
2 结果与分析
2.1 产酯菌株的初筛
通过筛选培养基,从酱香型窖醅中分离出7株(编号为1#、2#、3#、4#、5#、6#、7#)具有明显透明圈的菌株,其结果见图1。由图1可知,7株菌的菌落形态及透明圈大小各有差异。

图1 筛选菌株的菌落形态及透明圈
Fig.1 Colony morphology and transparent zone of screened strains
2.2 产酯菌株的复筛
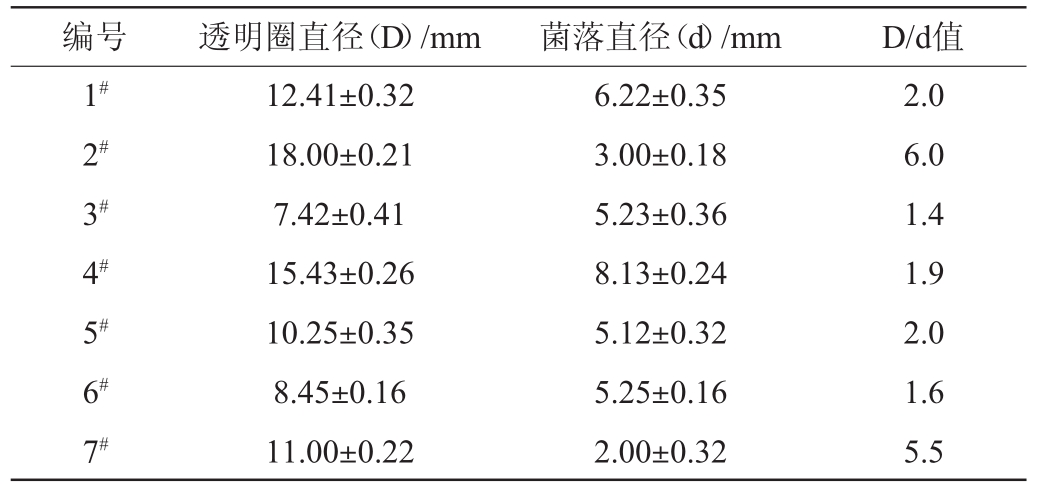
将初筛过程筛选出的7株菌株再次进行透明圈试验,结果见表1。由表1可知,1#、2#、5#、7#菌株D/d值较大,在2.0~6.0之间。因此,选择1#、2#、5#、7#菌株作进一步试验。
表1 筛选菌株的透明圈直径与菌落直径比值
Table 1 Diameter ratio of transparent zone to colony of screened strains
编号 透明圈直径(D)/mm 菌落直径(d)/mm D/d值1# 2# 3# 4# 5# 6# 7#12.41±0.32 18.00±0.21 7.42±0.41 15.43±0.26 10.25±0.35 8.45±0.16 11.00±0.22 6.22±0.35 3.00±0.18 5.23±0.36 8.13±0.24 5.12±0.32 5.25±0.16 2.00±0.32 2.0 6.0 1.4 1.9 2.0 1.6 5.5
2.3 产酯优良菌株的选择
对复筛挑选出来的4株菌株进行产酯发酵实验,结果见表2。由表2可知,2#菌株的产酯能力最强,达到了1.837 g/L。因此,选择2#菌株作为优良菌株进行下一步鉴定试验,并将其编号为LH2。
表2 菌株发酵液的总酯含量
Table 2 Total ester content in fermentation broth of strain

编号总酯含量/(g·L-1)1# 2# 5# 7#1.531±0.261 1.837±0.125 1.449±0.316 1.743±0.218
2.4 菌株LH2的鉴定
2.4.1 形态观察
菌株LH2在基本培养基上37℃培养12 h,平板具有明显单菌落后进行形态观察,结果见图2。由图2可知,菌株LH2菌落为圆形,边缘整齐,菌落白色,湿润状。对细菌进行革兰染色,显微镜下观察结果为菌体呈紫色,杆状,两端钝圆,单个或少量链状存在,有芽孢,芽孢端生或中生,为革兰阳性菌。
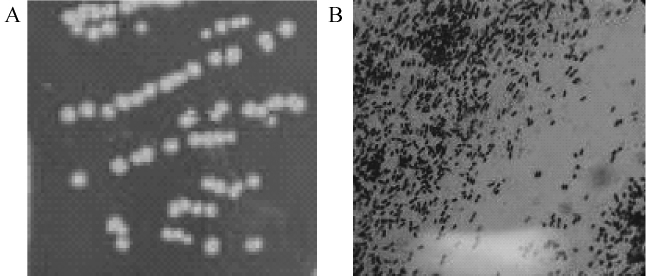
图2 菌株LH2的菌落形态(A)和细胞形态(B)
Fig.2 Colony morphology(A)and cell morphology(B)of strain LH2
2.4.2 生理生化试验
对菌株LH2进行芽孢染色、淀粉水解试验、蛋白水解实验和接触酶试验,结果见表3。由表3可知,菌株LH2产蛋白酶、淀粉酶,产芽孢,可初步判断为革兰氏阳性芽孢杆菌。
表3 菌株LH2的生理生化试验结果
Table 3 Results of physiological and biochemical tests of strain LH2
注:“+ ”为阳性反应;“-”为阴性反应。
项目 芽孢革兰氏染色 淀粉水解 蛋白水解 接触酶实验结果 + + + +
2.4.3 分子生物学鉴定
将菌株LH2的16SrDNA序列输入美国国立生物技术信息中心(national center for biotechnology information,NCBI)进行对比,利用MEGA6软件构建系统发育树,结果见图3。由图3可知,菌株LH2与枯草芽孢杆菌(Bacillus subtilis)的亲缘关系相近,相似度达到了99%,结合形态观察和生理生化试验特征将菌株LH2鉴定为枯草芽孢杆菌(Bacillus subtilis)。

图3 基于16S rRNA菌株LH2的系统发育树
Fig.3 Phylogenetic tree of strain LH2 based on 16S rRNA sequences
2.5 菌株LH2生长曲线和产酯曲线
为了确定菌株LH2最佳培养时间和产酯时间。将菌株LH2接种于发酵培养基,37℃持续培养,每隔2 h,测定发酵液OD600nm值和总酯含量。菌株LH2生长曲线和产酯曲线结果见图4。由图4可知,菌株LH2培养4 h后进入对数期,在34 h左右达到稳定期,在36 h左右总酯含量最高,达到2.2 g/L,继续发酵,OD600nm值和产酯量都趋于平稳,变化不大。因此,菌株LH2的最佳培养时间为36 h,此时其产酯量达到最大。
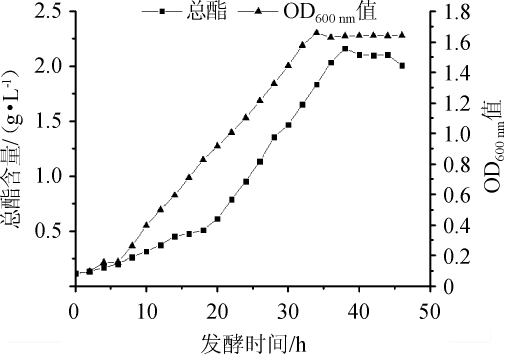
图4 菌株LH2的生长曲线及产酯曲线
Fig.4 Growth curve and ester-producing curve of strain LH2
2.6 菌株LH2发酵产物香气成分分析
将菌株LH2接种于麸皮固体培养基,37℃发酵4 d后,采用HS-SPME-GC-MS检测其发酵产物中的香气成分,其GC-MS分析总离子流色谱图见图5,各香气成分相对含量检测结果见表4。

图5 菌株LH2发酵产物香气成分GC-MS分析总离子流色谱图
Fig.5 Total ion chromatogram of aroma components in fermentation products of strain LH2 analyzed by GC-MS
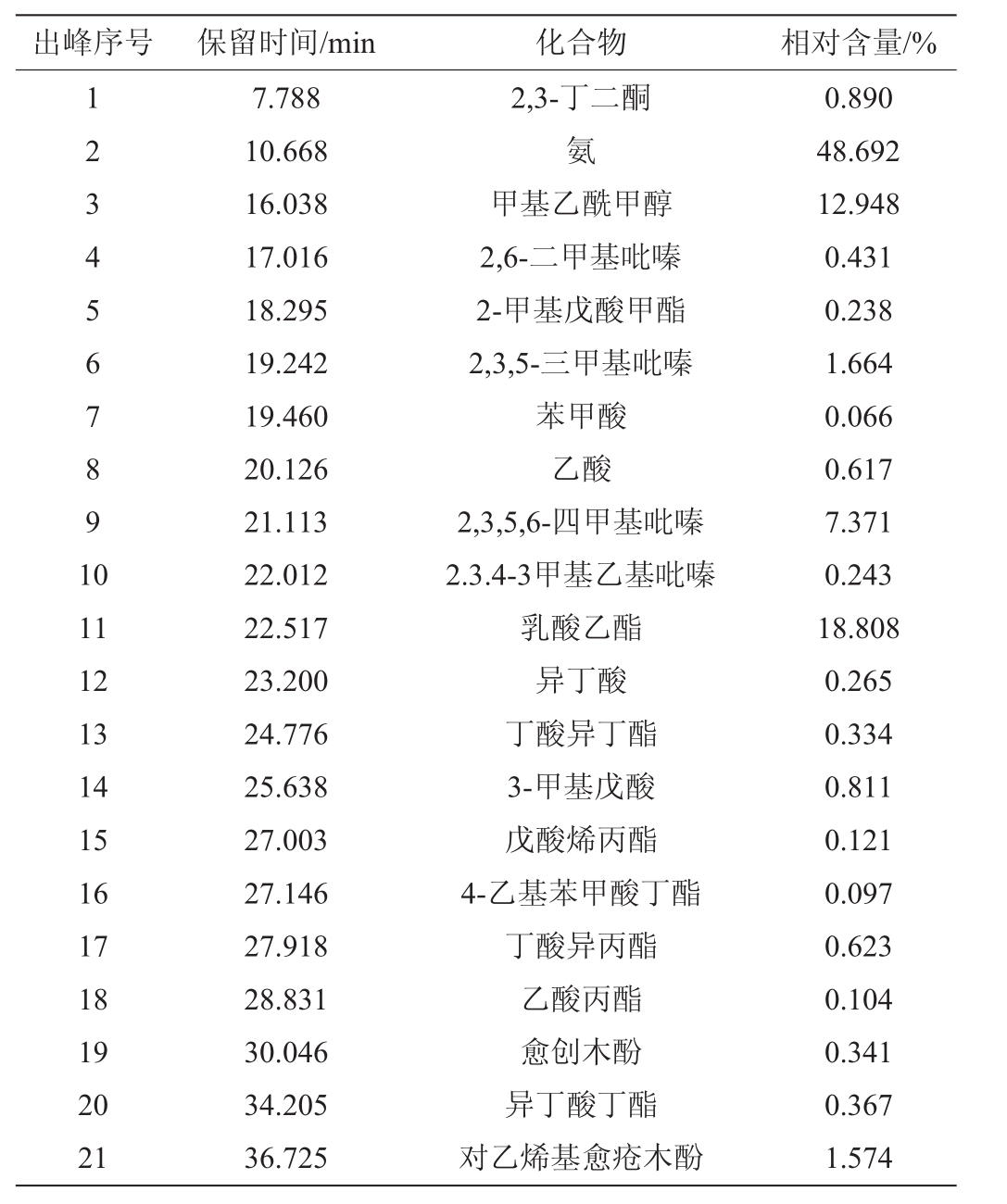
由图5和表4可知,菌株LH2发酵产物中共鉴定出21种香气成分,主要是酯类、酸类、吡嗪类和醇类,其中酯类的含量占18.692%。在酯类中主要的酯为乳酸乙酯,其含量为18.808%;酸类物质占2.755%,主要为苯甲酸,含量为0.066%;醇类主要为甲基乙酰甲醇,含量为12.948%。结果表明,菌株LH2具有较强的产酯能力,与此同时,吡嗪类物质的含量也比较多,占总挥发性物质含量的9.709%,特别是对人体非常有益的四甲基吡嗪占比达到7.371%。
表4 菌株LH2发酵产物香气成分GC-MS检测结果
Table 4 Determination results of aroma components in fermentation products of strain LH2 analyzed by GC-MS
出峰序号 保留时间/min 化合物 相对含量/%1234567891 0 11 12 13 14 15 16 17 18 19 20 21 7.788 10.668 16.038 17.016 18.295 19.242 19.460 20.126 21.113 22.012 22.517 23.200 24.776 25.638 27.003 27.146 27.918 28.831 30.046 34.205 36.725 2,3-丁二酮氨甲基乙酰甲醇2,6-二甲基吡嗪2-甲基戊酸甲酯2,3,5-三甲基吡嗪苯甲酸乙酸2,3,5,6-四甲基吡嗪2.3.4-3甲基乙基吡嗪乳酸乙酯异丁酸丁酸异丁酯3-甲基戊酸戊酸烯丙酯4-乙基苯甲酸丁酯丁酸异丙酯乙酸丙酯愈创木酚异丁酸丁酯对乙烯基愈疮木酚0.890 48.692 12.948 0.431 0.238 1.664 0.066 0.617 7.371 0.243 18.808 0.265 0.334 0.811 0.121 0.097 0.623 0.104 0.341 0.367 1.574
3 结论
利用透明圈法从酱香型窖醅中分离得到产酯最高的菌株LH2,其透明圈直径与菌落直径之比(D/d)为6.0。通过形态观察、生理生化试验和16S rDNA等方法鉴定菌株LH2为枯草芽孢杆菌(Bacillus subtilis)。参考国标GB/T26760—2011《酱香型白酒国家标准》优级酒总酯含量(以乙酸乙酯计)为2.2 g/L;一级酒总酯含量(以乙酸乙酯计)为2.0 g/L,筛选出的菌株LH2产酯总量为2.2 g/L,虽然发酵条件和发酵环境与酱香型白酒差别很大,但从酯含量来说,该菌株具有较高的产酯能力。
运用顶空固相微萃取气质联用(HS-SPME-GC-MS)技术对菌株LH2发酵产物的香气物质进行分析,共鉴定出21种香气成分,主要是酯类(18.692%)、酸类(2.755%)、吡嗪类(9.709%)和醇类(12.948%),并在产酯能力较强的同时也产生四甲基吡嗪等有益身体健康的物质增加了菌株LH2在健康白酒方向进一步研究的价值。
[1]李莉,王秋叶,盛夏,等.白酒中酯类对酒质的影响[J].食品安全导刊,2016(36):130.
[2]沈怡方.白酒生产技术全书[M].北京:中国轻工业出版社,2007:180-200.
[3]FAN W,QIAN M C.Identification of aroma compounds in Chinese'Yanghe Daqu'liquor by normal phase chromatography fractionation followed by gas chromatography olfactometry[J].Flavour Frag J,2010,21(2):333-342.
[4]于勇.酱香型酒中的乳酸及乳酸乙酯[J].酿酒,2004,31(4):21-22.
[5]谭超,吴同,李惟一,等.近红外光谱组合区间偏最小二乘法定量白酒中的乙酸乙酯[J].计算机与应用化学,2014,31(4):510-512.
[6]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 26760—2011酱香型白酒[S].北京:中国标准出版社,2011.
[7]ZHOU S S,XIONG J C.Isolation and identification of ester-producing yeast in wine starter and its application in ester production[J].Mod Food Sci Technol,2010,26(1):98-108.
[8]LUO H B,WANG D D,WANG Y,et al.Screening of mold producing aroma in Chinese kojiand optimization of culture conditions[J].Adv Mater Res,2014,1033:744-747.
[9]牛广杰.优良产酯酵母菌的筛选及发酵性能研究[J].酿酒,2013,40(6):56-59.
[10]杨恩超,程世春,刘光烨.己酸乙酯酯化菌分离筛选及鉴定[J].食品与发酵科技,2010,46(3):33-36.
[11]黄丹,方春玉,储玉龙,等.一株酯化酶细菌的分离、鉴定及代谢产物特征[J].四川理工学院学报(自然科学版),2010,29(3):321-323.
[12]王耀,范文来,徐岩,等.浓香型大曲中酯化酶测定方法的研究[J].酿酒,2003,30(2):18-21.
[13]李河,张宿义,敖宗华,等.浓香型白酒酯化液的研究进展[J].中国酿造,2016,35(8):5-8.
[14]NIELSEN T.Industrial application possibilities for lipase[J].Fette Seifen Anstr,1985,87(1):15-19.
[15]刘阳.中高温大曲中产酯化酶细菌的选育[D].芜湖:安徽工程大学,2013.
[16]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 10345—2007白酒分析方法[J].北京:中国标准出版社,2007.
[17]BAEILE M F.Gram staining technique[M].New York:Methods Mycoplasmolo,1983:39-42.
[18]LIX.Studies on bacteria producing Bouquet in Lang Wine Daqu[J].J Chongqing Teacher College(Natural Science Edition),1997,14(4):20-23.
[19]东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学出版社,2001:59-63.
[20]廖永红,任文雅,孙宝国,等.米醋中蜡状芽孢杆菌DNA提取及其ERIC-PCR 体系建立[J].中国食品学报,2011,11(4):7-13.
[21]XIU L,GUO K,ZHANG H.Determination of microbial diversity in Daqu,a fermentation starter culture of Maotailiquor,using nested PCR-denaturing gradient gel electrophoresis[J].World J Microb Biot,2012,28(6):2375-2381.
[22]赵兴秀,何义国,赵长青,等.产酱香功能菌的筛选及其风味物质研究[J].食品工业科技,2016,37(6):196-200.
[23]LI W,HU G,LEI L,et al.Identification and aroma impact of volatile terpenes in Moutailiquor[J].Int J Food Prop,2016,19(6):1335-1352.