作为中国“四大名醋”之一的山西老陈醋,其采用传统自然固体发酵并结合独特熏、淋、晒等工艺,形成老陈醋独特的酸、绵、香、甜风味与口感[1]。老陈醋的独特风味得益于微生物菌群的生长和代谢以及复杂的协同作用,芽孢杆菌(Bacillus)也是山西老陈醋发酵生产过程中的重要微生物种群,其在老陈醋风味和功能成分的形成中起到重要作用。王进龙[2]从山西老陈醋中分离出解淀粉芽孢杆菌(Bacillus amyloliquefaciens)、地衣芽孢杆菌(Bacillus licheniformis)、枯草芽孢杆菌(Bacillussubtilis)、短小芽孢杆菌(Bacillus pumilus)、萎缩芽孢杆菌(Bacillus atrophaeus)、巨大芽孢杆菌(Bacillus megaterium)。
芽孢杆菌具有很强的分泌蛋白的能力,能产生大量的淀粉酶、纤维素酶、蛋白酶等,提高原料的利用率[3]。史改玲[4]从山西老陈醋成熟醋醅中分离筛选出的甲基营养型芽孢杆菌(Bacillus methylotrophicus)CP-1576淀粉酶活力最高(61.40 U/mL),球形赖氨酸芽孢杆菌(Lysinibacillus sphaericus)CP-2436的纤维素酶活力最高(54.99 U/mL),地衣芽孢杆菌CP-1853的蛋白酶活力最高(22.80 U/mL);王进龙[2]从山西老陈醋大曲中分离出的芽孢杆菌BA8的糖化酶活力为41.01 U/mL,BP6的蛋白酶活力为28.29 U/mL。
乙偶姻是山西老陈醋重要功能成分川芎嗪的前体物质[5],而芽孢杆菌产乙偶姻的能力比乳酸菌、醋酸菌更强、更稳定[6]。在国内外,乙偶姻生产菌种的筛选、育种、发酵主要集中于芽孢杆菌。高文睿等[7]从凉州熏醋中筛选出高产乙偶姻(2.376 mg/mL)的芽孢杆菌Y4;张显[8]采用传统诱变方法对枯草芽孢杆菌JNA 3-10进行复合诱变,获得一株2,3-丁二醇脱氢酶(2,3-butanediol dehydrogenase,BDH)缺失型乙偶姻高产突变株JNA-UD-6,乙偶姻产量为53.9 g/L。芽孢杆菌在陈醋中除产乙偶姻外,还产多酚类物质,从而赋予山西老陈醋抗氧化的功能,郇阿梅等[9]从四川传统麸醋醋醅中筛选出一株芽孢杆菌YB-32,培养24h后总酚产量为263.6 μg/mL。另外,芽孢杆菌的代谢产物与发酵体系中的其他物质发生反应,生成一些风味物质,可以很好地改善食醋风味。
随机扩增多态性脱氧核糖核酸(randomamplifiedpoly morphicdeoxyribonucleicacid,RAPD)技术是一种基于基因组聚合酶链式反应(polymerase chain reaction,PCR)的多态性分析的分子分型技术[10]。近年来,RAPD用于保加利亚乳杆菌(Lactobacillusbulgaricus)和嗜热链球菌(Streptococcus thermophilus)分型的研究较多[11],但关于芽孢杆菌菌种间基因分型的研究鲜有报道。本研究从山西老陈醋酿造过程的醋醅中分离芽孢杆菌,采用分子生物学技术对其进行鉴定,并采用RAPD技术对其进行菌株分型,明确山西老陈醋芽孢杆菌的主要种类;在此基础上,对芽孢杆菌的酶、乙偶姻、多酚、总酯的生产能力进行测定,进一步探讨了型别与菌株特性之间的关系,从中筛选出优良菌株,以期丰富山西老陈醋生产强化菌株,对食醋的营养、功能、风味、生产效率的提高等都具有重要意义。
1 材料与方法
1.1 材料与试剂
1.1.1 样品
醋醅:取自山西东湖醋厂老陈醋醋酸发酵第0天、1天、3天、5天、7天、9天、11天醋醅缸中表层至底层20cm处的醋醅。
1.1.2 培养基与试剂
MRS培养基:青岛高科园海博生物科技有限公司。
细菌DNA提取试剂盒:北京博迈德基因科技有限公司;PCR引物:由深圳华大基因公司合成;DNA Maker、MIX:上海生工生物工程有限公司;福林试剂、肌酸、没食子酸(均为分析纯):北京索莱宝科技有限公司。
1.2 仪器与设备
T100型PCR仪、Universial HoodⅡ型凝胶成像系统:美国Bio-Rad公司;DYY-6C型琼脂糖凝胶电泳仪:北京六一仪器厂;5417R型高速冷冻离心机:德国Eppendorf公司;722型可见分光光度计:上海精密科学仪器有限公司。
1.3 实验方法
1.3.1 山西老陈醋中芽孢杆菌的分离
无菌条件下,称取25 g样品于内置玻璃珠的225 mL无菌生理盐水中,室温、140 r/min条件下振荡培养20 min,使其混匀。对样品进行梯度稀释,选取梯度为10-5、10-6、10-7的稀释液涂布于MRS固体培养基平板中,37℃静置培养1~2 d。选择具有30~300个菌落的平板,并挑取平板上表面粗糙、菌落形态较大的单个菌落进行分离纯化。
1.3.2 山西老陈醋中芽孢杆菌的鉴定
对分离纯化的菌株进行革兰氏染色,并观察菌株的菌落和细胞形态,选取革兰氏阳性、有芽孢的杆状菌株进行分子生物学鉴定。
采用细菌DNA提取试剂盒提取分离菌株的基因组,以其为模板,采用引物27F(5′-AGAGTITGATCCTGGCTCAG-3′)和1492R(5′-ACGGYTACCTI'GTI'ACGACTY-3′)对细菌的16S rDNA进行PCR扩增[12]。PCR扩增产物经1%琼脂糖凝胶检测后进行测序,测序结果提交至美国国立生物技术信息中心(nationalcenterforbiotechnologyinformation,NCBI)的Genebank数据库中进行BLAST比对,选取同源性较高的菌株,利用MEGA5.1软件中的邻接(neighbor-joining,NJ)法构建系统发育树。
1.3.3 山西老陈醋中芽孢杆菌的基因分型
将分离纯化的芽孢杆菌菌株分别接种于MRS液体培养基,37℃、140 r/min条件下培养24 h,以基因组DNA为模板,采用引物(GTG)5(5′-GTGGTGGTGGTGGTG-3′)[13]进行PCR扩增;PCR扩增体系:引物3 μL,模板3.5 μL,2×MIX 15 μL,双蒸水(ddH2O)10.5 μL;PCR扩增程序:94 ℃预变性4 min;94℃变性30 s,58℃退火1 min,72℃延伸2 min,30个循环;72℃再延伸10 min。PCR扩增产物经1.0%琼脂糖凝胶电泳分离,进行RAPD分型分析。
1.3.4 山西老陈醋中优良芽孢杆菌的筛选
将分离的30株芽孢杆菌接种于MRS液体培养基中,37℃、140 r/min条件下培养24 h,发酵液经8 000 r/min离心10 min,取上清,采用3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)比色法[14]测定芽孢杆菌发酵液的糖化酶酶活、纤维素酶酶活;采用福林-酚比色法测定蛋白酶酶活[15]、多酚含量[16];采用O'Meara-比色法[17]测定乙偶姻含量;采用氢氧化钠皂化法[18]测定总酯含量。
2 结果与分析
2.1 山西老陈醋中芽孢杆菌的分离与鉴定
从山西老陈醋醋酸发酵过程的醋醅中共分离得到30株芽孢杆菌,分别为菌株10、18、19、28、33、38、59、61、140、146、250、253、277、285、290、510、665、670、804、936、1145、1146、1463、1576、1882、1918、1959、1986、2035、2372,其中6株典型芽孢杆菌的菌落和细胞形态见图1和表1。
由图1和表1可知,菌株665的菌落呈圆形,边缘齿状,中间凹陷,乳白色;菌株1882的菌落边缘褶皱,中间凸起成雪花状,淡黄色;菌株2035的菌落近似圆形,扁平,边缘平整,干燥;菌株1576的菌落呈圆形,边缘齿状,中间凸起成圈,乳白色;菌株936的菌落边缘褶皱,中间凹陷,扁平,淡黄色;菌株670菌落呈圆形,边缘褶皱,中间凹陷,扁平,乳白色。菌落形态多不透明,细胞均呈杆状,革兰氏阳性(G+)。经菌落和细胞形态观察,初步鉴定30株分离菌株均为芽孢杆菌属(Bacillus)。

图1 山西老陈醋中典型芽孢杆菌的菌落(A)和细胞形态(1 000×)(B)
Fig.1 Colony morphology(A)and cell morphology(1 000×)(B)of typicalBacillusfrom Shanxi aged vinegar
表1 山西老陈醋中典型芽孢杆菌的菌落和细胞形态结果
Table 1 Results of colony and the cell morphology of typicalBacillus from Shanxi aged vinegar

菌株 菌落形态 细胞形态665 1882 2035 1576 G+,中长粗杆状G+,细长杆状G+,细长杆状G+,粗杆状936 670菌落呈圆形,边缘齿状,中间凹陷,乳白色,不透明边缘褶皱,中间凸起成雪花状,淡黄色,不透明菌落近似圆形,扁平,边缘平整,半透明,干燥菌落呈圆形,边缘齿状,中间凸起成圈,乳白色,不透明边缘褶皱,中间凹陷,扁平,淡黄色,不透明菌落呈圆形,边缘褶皱,中间凹陷,扁平,乳白色,不透明G+,短杆状G+,细长杆状
30株芽孢杆菌经16S rDNA测序比对并构建系统进化树,结果见图2。
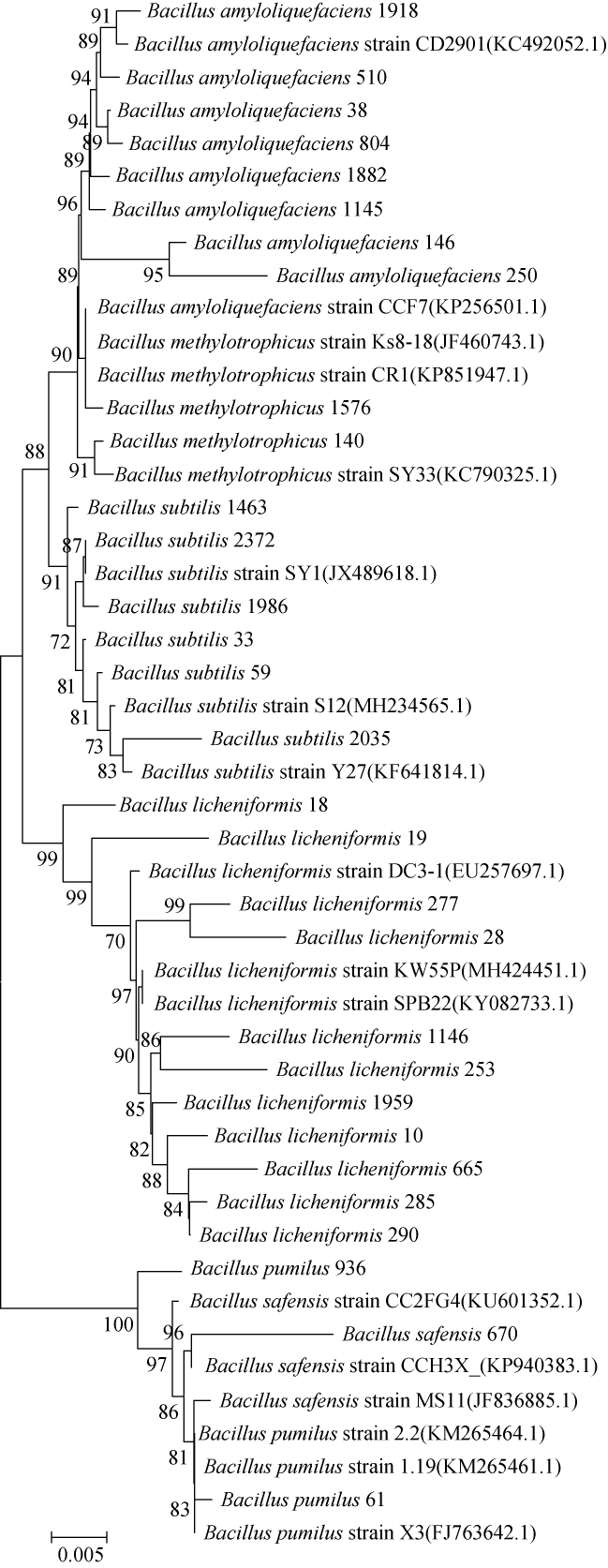
图2 山西老陈醋中芽孢杆菌的16S rDNA序列系统发育树
Fig.2 Phylogenetic tree ofBacillusfrom Shanxi aged vinegar based on the 16S rDNA sequences
由图2可知,菌株10、18、19、28、1146、1959、253、277、285、290、665与模式菌株BacilluslicheniformisstrainKW55P(MH424451.1)、BacilluslicheniformisstrainDC3-1(EU257697.1)、BacilluslicheniformisstrainSPB22(KY082733.1)聚于一支,亲缘关系最近,可达99%,因此,鉴定这些菌株为地衣芽孢杆菌(Bacillus licheniformis);菌株33、59、1463、1986、2035、2372与模式菌株Bacillus subtilisstrain SY1(JX489618.1)、BacillussubtilisstrainS12(MH234565.1)、Bacillussubtilisstrain Y27(KF641814.1)聚于一支,亲缘关系最近,因此,鉴定这些菌株为枯草芽孢杆菌(Bacillussubtilis);菌株38、146、250、510、804、1145、1882、1918与模式菌株Bacillus amyloliquefaciensstrain CD2901(KC492052.1)聚于一支,亲缘关系也较近,鉴定为解淀粉芽孢杆菌(Bacillus amyloliquefaciens);同理,鉴定菌株140、1576为甲基营养型芽孢杆菌(Bacillus methylotrophicus);菌株61、936为短小芽孢杆菌(Bacillus pumilus);菌株670为沙福芽孢杆菌(Bacillus safensis)。
综上,30株芽孢杆菌中11株为地衣芽孢杆菌,8株为解淀粉芽孢杆菌,6株为枯草芽孢杆菌,2株为甲基营养型芽孢杆菌,2株为短小芽孢杆菌及1株为沙福芽孢杆菌,分别占芽孢杆菌的36.67%、26.67%、20.00%、6.67%、6.67%、3.33%。
2.2 山西老陈醋中芽孢杆菌的基因分型
为了解山西老陈醋中芽孢杆菌种内菌株的基因多样性,采用RAPD技术对30株芽孢菌菌株进行基因分型,结果见图3。
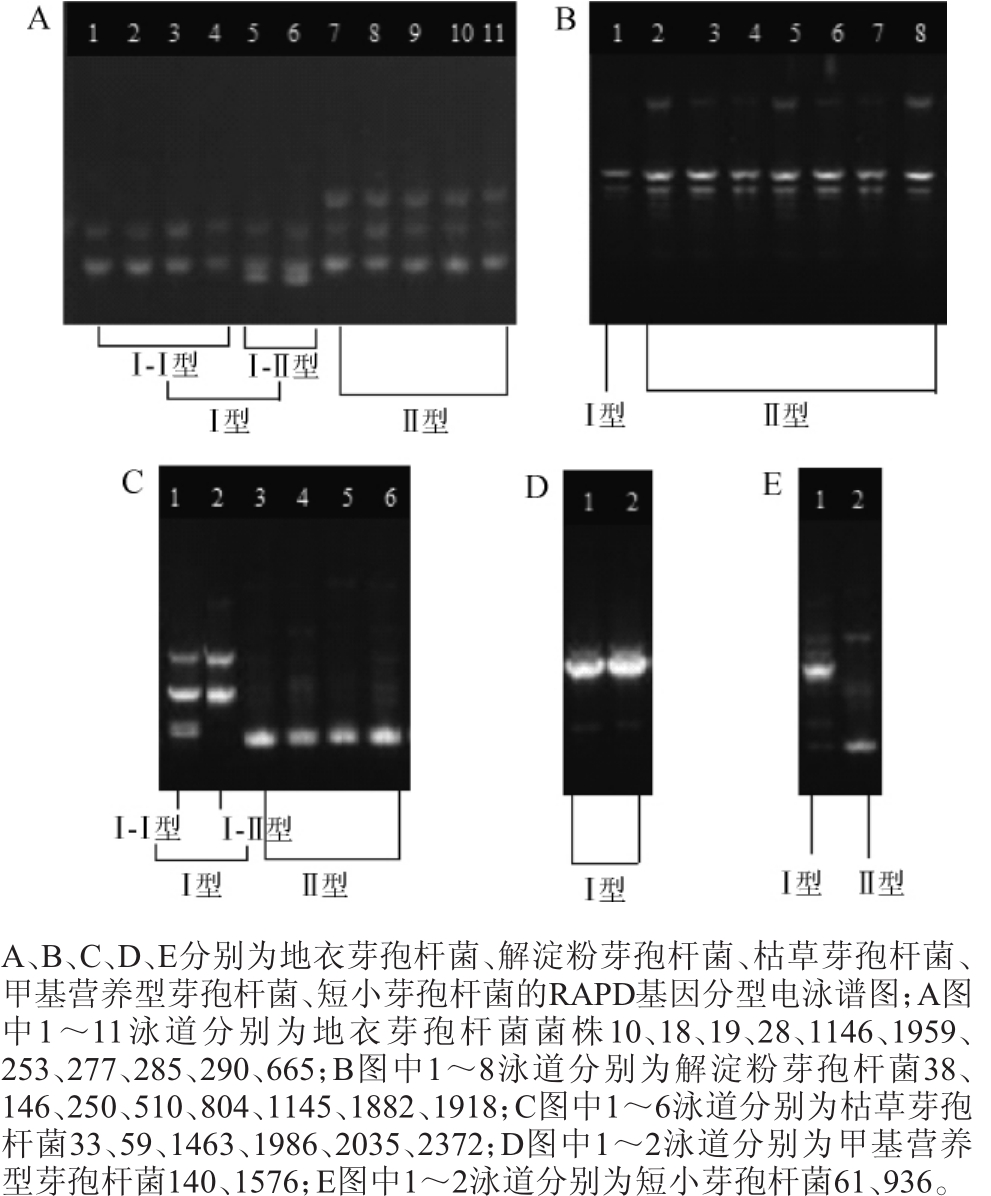
图3 山西老陈醋中芽孢杆菌的RAPD基因分型结果
Fig.3 RAPD genotyping results ofBacillusfrom Shanxi aged vinegar
由图3A可知,11株地衣芽孢杆菌主要呈现Ⅰ、Ⅱ2个型别,Ⅰ型又分为Ⅰ-Ⅰ、Ⅰ-Ⅱ2个亚型,其中菌株10、18、19、28为Ⅰ-Ⅰ型,菌株1146、1959为Ⅰ-Ⅱ型,其余菌株253、277、285、290、665均为Ⅱ型。由图3B可知,8株解淀粉芽孢杆菌也被分成Ⅰ、Ⅱ2个型别,菌株38为Ⅰ型,而菌株146、250、510、804、1145、1882、1918被归属为Ⅱ型。由图3C可知,6株枯草芽孢杆菌被分成Ⅰ、Ⅱ2个型别,Ⅰ型又分为Ⅰ-Ⅰ、Ⅰ-Ⅱ2个亚型,其中菌株33为Ⅰ-Ⅰ型,菌株59为Ⅰ-Ⅱ型,菌株1463、1986、2035、2372均为Ⅱ型。由图3D可知,2株甲基营养型芽孢杆菌菌株为同一基因型。由图3E可知,2株短小芽孢杆菌属于不同的型别。综上所述,来源于老陈醋醋酸发酵过程中的30株芽孢杆菌具有菌株基因多样性,为菌株的特性筛选提供了遗传基础。
2.3 山西老陈醋中优良芽孢杆菌的筛选
2.3.1 芽孢杆菌产糖化酶能力的测定
淀粉酶可以催化淀粉及糖原水解,生成葡萄糖和麦芽糖。用淀粉酶做糖化剂来酿造食醋,可以提高食醋原料利用率,提高产量,降低生产成本,缩短食醋生产周期[19]。淀粉酶主要有α-淀粉酶和糖化酶,α-淀粉酶是将大分子淀粉水解成中等和低分子物质,产生大量新的非还原性末端,糖化酶则将α-淀粉酶水解出的一些中、低分子产物水解为可直接利用的葡萄糖。芽孢杆菌能够分泌产生糖化酶,研究较多的芽孢杆菌有解淀粉芽孢杆菌、凝结芽孢杆菌、纳豆芽孢杆菌、枯草芽孢杆菌、地衣芽孢杆菌等[20]。30株芽孢杆菌糖化酶活力测定结果见图4。
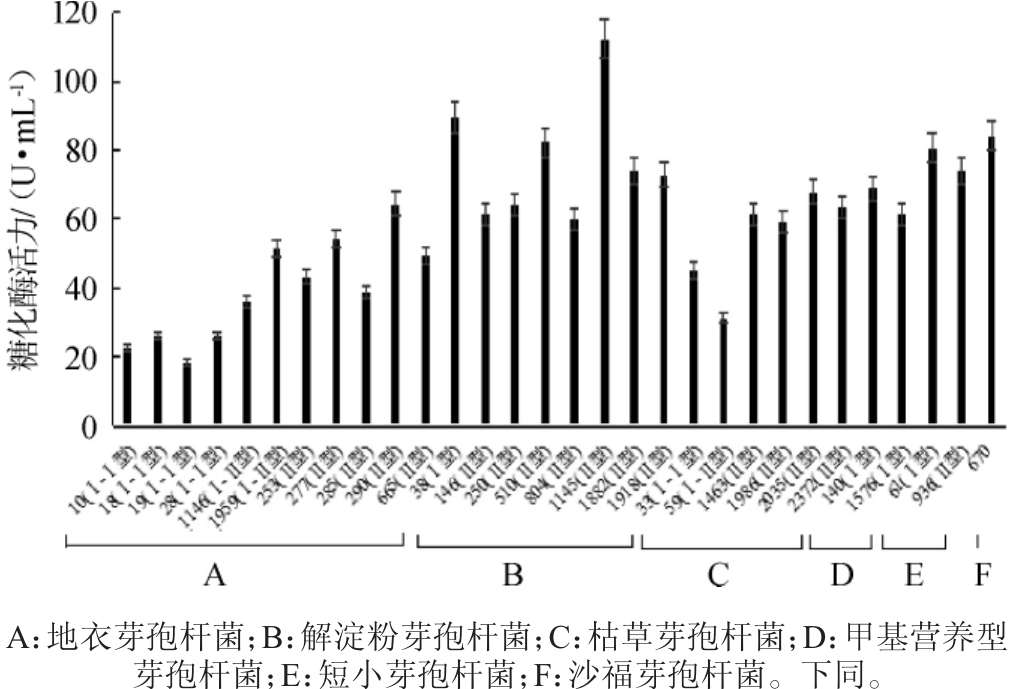
图4 山西老陈醋中芽孢杆菌糖化酶活力的测定结果
Fig.4 Determination results of glucoamylase activity ofBacillusfrom Shanxi aged vinegar
由图4可知,30株芽孢杆菌的糖化酶酶活在20~120U/mL范围内,其中解淀粉芽孢杆菌1145(112.45 U/mL)、解淀粉芽孢杆菌38(89.68 U/mL)、沙福芽孢杆菌670(84.24 U/mL)的糖化酶活较高,但低于徐颖[21]从土壤中筛选的枯草芽孢杆菌的糖化酶酶活(784 U/mL),不同来源的芽孢菌菌株产糖化酶的能力显著不同,这与菌株的生境直接相关,但醋醅中分离、筛选的土著优良高产糖化酶芽孢杆菌对陈醋酿造环境的适应性,具有其他来源菌株无可比拟的优势。另外,Ⅱ型地衣芽孢杆菌的糖化酶酶活性(38~64U/mL)显著高于Ⅰ型(18~36 U/mL);相似地,Ⅱ型枯草芽孢杆菌的糖化酶酶活(59~68 U/mL)也显著高于Ⅰ型(31~45 U/mL),表明同种同型别芽孢杆菌产糖化酶的能力具有相似性,同种不同型别芽孢杆菌产糖化酶的能力具有差异性。
2.3.2 芽孢杆菌产蛋白酶能力的测定
在食醋制作过程中,蛋白酶分解原料中的蛋白成分,提高陈醋中氨基氮的含量,同时提高了老陈醋的澄清度和稳定性[22]。蛋白酶主要来源于微生物,其中芽孢杆菌是蛋白酶的重要生产菌株。30株芽孢杆菌的蛋白酶活力测定结果见图5。

图5 山西老陈醋中芽孢杆菌蛋白酶活力的测定结果
Fig.5 Determination results of protease activity ofBacillusfrom Shanxi aged vinegar
由图5可知,30株芽孢杆菌发酵液的蛋白酶酶活在3~35 U/mL范围内,其中解淀粉芽孢杆菌38(34.53 U/mL)、甲基营养型芽孢杆菌1576(27.75 U/mL)、甲基营养型芽孢杆菌140(21.62U/mL)发酵液的蛋白酶酶活较高,但低于黄家驷等[23]从酒曲中筛选出的地衣芽孢杆菌的酶活(180U/mL)。这可能与芽孢菌的来源不同有关。Ⅰ型地衣芽孢杆菌的蛋白酶酶活(6~16 U/mL)显著高于Ⅱ型(4~9 U/mL);同理,Ⅰ型解淀粉芽孢杆菌的蛋白酶酶活(34.53 U/mL)高于Ⅱ型(13~19 U/mL),结果表明,不同型别芽孢杆菌的特性差异性较大,而同型别菌株特性相似。
2.3.3 芽孢杆菌产纤维素酶能力的测定
纤维素酶是一种具有催化纤维素分解成葡萄糖的生物活性蛋白质,纤维素酶能破坏植物细胞壁,便于淀粉、蛋白质、脂肪类物质的释放,高粱作为陈醋生产原料,其纤维素含量高达4%~10%,纤维素酶可以加快发酵速度,提高食醋的产量和原料利用率。本研究中30株芽孢杆菌的纤维素酶活力测定结果见图6。
由图6可知,30株芽孢杆菌的纤维素酶酶活在9~35 U/mL范围内,其中沙福芽孢杆菌670、解淀粉芽孢杆菌510、枯草芽孢杆菌2372的纤维素酶活较高,分别为35.38 U/mL、33.61 U/mL、33.02 U/mL,纤维素酶酶活均高于董丹等[24]从酒醅中筛选出的枯草芽孢杆菌XWS-1(26.4U/mL)。从菌株基因分型来看,Ⅱ型枯草芽孢杆菌产纤维素酶(22~33U/mL)的能力明显高于Ⅰ型(20~21U/mL),其余同种不同型别的芽孢杆菌、同种同型别的芽孢杆菌产纤维素酶能力相似。
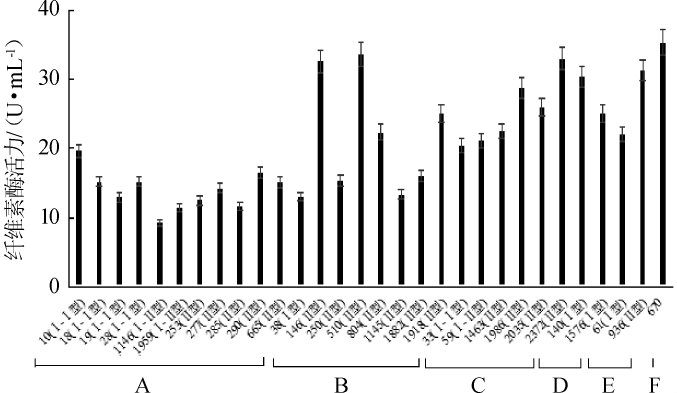
图6 山西老陈醋中芽孢杆菌纤维素酶活力的测定结果
Fig.6 Determination results of cellulase activity ofBacillusfrom Shanxi aged vinegar
2.3.4 芽孢杆菌产乙偶姻能力的测定
乙偶姻是山西老陈醋中重要功能成分川芎嗪的前体物质,国内外产乙偶姻菌株的筛选、育种、发酵集中于芽孢杆菌。30株芽孢杆菌乙偶姻生产能力的测定结果见图7。
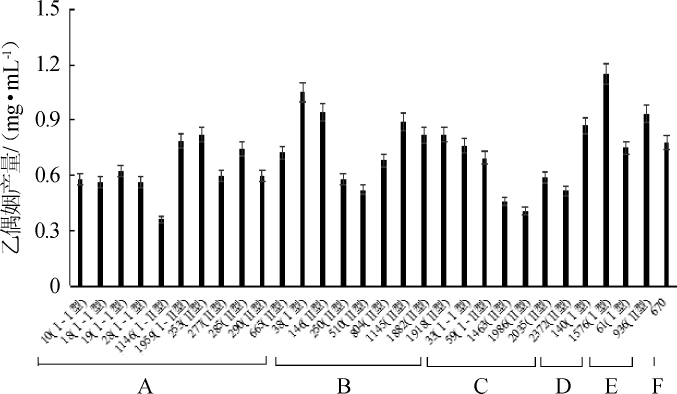
图7 山西老陈醋中芽孢杆菌产乙偶姻能力的测定结果
Fig.7 Determination results of acetoin production ability of Bacillusfrom Shanxi aged vinegar
由图7可知,30株芽孢杆菌的乙偶姻产量在0.3~1.2 mg/mL范围内,其中甲基营养型芽孢杆菌1576的乙偶姻产量最高,为1.15 mg/mL,其次是高产糖化酶和蛋白酶的解淀粉芽孢杆菌38(1.05 mg/mL),显著高于王霜等[25]从兼香型白酒酒醅中筛选到的地衣芽孢杆菌LS9的乙偶姻生产能力(0.065mg/mL)。Ⅰ型解淀粉芽孢杆菌的乙偶姻产量(1.05 mg/mL)显著高于Ⅱ型(0.52~0.94 mg/mL),而且Ⅰ型枯草芽孢杆菌的乙偶姻产量(0.69~0.76 mg/mL)也同样高于Ⅱ型(0.52~0.58 mg/mL),进一步表明,同种同型别的芽孢杆菌的优良特性具有相似性,不同型别的芽孢菌其特性具有差异性。
2.3.5 芽孢杆菌产多酚能力的测定
多酚类物质具有抗氧化、强化血管壁、促进肠胃消化、降低血脂肪、抑制细菌与癌细胞生长等多种生理活性功能[16]。30株芽孢杆菌的多酚产量测定结果见图8。

图8 山西老陈醋中芽孢杆菌产多酚能力的测定结果
Fig.8 Determination results of polyphenols production ability of Bacillusfrom Shanxi aged vinegar
由图8可知,30株芽孢杆菌的多酚产量在120~430μg/mL范围内,其中解淀粉芽孢杆菌804(428.35μg/mL)、解淀粉芽孢杆菌1145(407.07μg/mL)、地衣芽孢杆菌1146(403.71μg/mL)的多酚产量较高,而高产糖化酶、纤维素酶和乙偶姻的解淀粉芽孢杆菌38产多酚能力次之,产量为401.36μg/mL。Ⅰ-Ⅱ型地衣芽孢杆菌的多酚产量在320~400 μg/mL范围内,而Ⅱ型地衣芽孢杆菌在260~325 μg/mL范围内。
2.3.6 芽孢杆菌产总酯能力的测定
芽孢菌代谢产生的乳酸、苹果酸、酒石酸、丙酮酸等有机酸,可以与醇类物质酯化生成酯类物质,丰富老陈醋味感与口感。30株芽孢杆菌的总酯生产能力测定结果见图9。
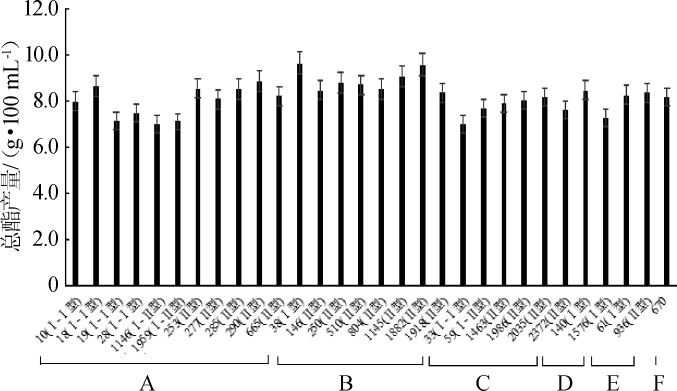
图9 山西老陈醋中芽孢杆菌产总酯能力的测定结果
Fig.9 Determination results of total esters production ability of Bacillusfrom Shanxi aged vinegar
由图9可知,30株芽孢杆菌的总酯产量在6.98~9.62 g/100 mL范围内,其中解淀粉芽孢杆菌38产总酯能力(9.62 g/100 mL)最强;其次为解淀粉芽孢杆菌1882、解淀粉芽孢杆菌1145,分别为9.54 g/100 mL、9.05 g/100 mL。
综上,30株芽孢杆菌中解淀粉芽孢杆菌38产糖化酶、蛋白酶、乙偶姻、多酚和总酯的能力均较高,为优良菌株。
3 结论
从山西老陈醋醋酸发酵过程的醋醅中共分离出30株芽孢杆菌,经分子生物学鉴定,其中11株为地衣芽孢杆菌(Bacillus licheniformis),8株为解淀粉芽孢杆菌(Bacillus amyloliquefaciens),6株为枯草芽孢杆菌(Bacillus subtilis),2株为甲基营养型芽孢杆菌(Bacillusmethylotrophicus),2株为短小芽孢杆菌(Bacillus pumilus),1株为沙福芽孢杆菌(Bacillus safensis)。采用RAPD技术对其进行基因分型,发现芽孢杆菌种内具有基因多样性。另外对30株芽孢杆菌产酶、乙偶姻、多酚、总酯的能力进行筛选,发现同种同型别的芽孢杆菌产酶、乙偶姻、多酚、总酯的能力具有相似性;但同种不同型别的芽孢杆菌的特性具有差异性,并且筛选出1株产糖化酶(89.68U/mL)、蛋白酶(34.53U/mL)、乙偶姻(1.05 mg/mL)、多酚(401.36 μg/mL)、总酯(9.62 g/100 mL)能力均较高的解淀粉芽孢杆菌38,证明了芽孢杆菌作为山西老陈醋强化直投式发酵剂具有巨大的开发潜力。
[1]NIE Z,YU Z,DU H,et al.Dynamics and diversity of microbial community succession in 5 traditional fermentation of Shanxi aged vinegar[J].Food Microbiol,2015,47(12):62-68.
[2]王进龙.山西老陈醋大曲中芽孢杆菌的分离鉴定及特性研究[D].晋中:山西农业大学,2016.
[3]VIDAL A,MARIN S,SANCHIS V,et al.Hydrolysers of modified mycotoxins in maize:α-amylase and cellulase induce an underestimation of the total aflatoxin content[J].Food Chem,2018,248(6):86-92.
[4]史改玲.山西老陈醋源优良芽孢杆菌菌株的鉴定及筛选[J].中国酿造,2018,37(5):22-27.
[5]AKASAKA,NAOKI,SAKODA,et al.An efficient method using gluconacetobacter europaeus to reduce an unfavorable flavor compound,acetoin,in rice vinegar production[J].Appl Environ Microbiol,2013,79(23):7334-7342.
[6]LU L,WEI X,YU W,et al.Enhancement of acetoin production from Bacillus licheniformisby 2,3-butanediol conversion strategy:Metabolic engineering and fermentation control[J].Process Biochem,2017,57(10):35-42.
[7]高文睿,贠建民.凉州熏醋中高产乙偶姻菌株的分离筛选及发酵特性初探[J].农业科技与信息,2015(16):26-29.
[8]张显.高产乙偶姻枯草芽孢杆菌的代谢工程改造[D].无锡:江南大学,2013.
[9]郇阿梅,刘军,王洋,等.一株分离至传统麸醋醋醅芽孢杆菌发酵特性研究[J].中国调味品,2014,39(8):23-28.
[10]ENANMR.Applicationofrandomamplified polymorphic DNA(RAPD)to detect the genotoxic effect of heavy metals[J].Biotechnol Appl Bioc,2011,43(3):147-154.
[11]李艳莉.酸奶及发酵剂中分离乳酸菌药物敏感性研究[D].广州:华南理工大学,2015.
[12]TAKUYA Y,TATSUJI S,TAKENORI N,et al.Lactic acid bacteria from kefir increase cytotoxicity of natural killer cells to tumor cells[J].Foods,2018,7(4):48-56.
[13]KHOWAL S,SIDDIQUI M Z,ALI S,et al.A report on extensive lateral genetic reciprocation between arsenic resistantBacillus subtilisand Bacillus pumilusstrains analyzed using RAPD-PCR[J].Mol Phylogenet Evol,2017,107:443-454.
[14]RAMALINGAM V,RAJARAM R,ANANTH S,et al.Development of thermostable amylase enzyme fromBacillus cereusfor potential antibiofilm activity[J].Bioorg Chem,2018,77:494-506.
[15]MIKHAIL M.VOROB'EV,BUTRE C I,SFORZA S,et al.Demasking kinetics of peptide bond cleavage for whey protein isolate hydrolysed by Bacillus licheniformisprotease[J].J Mol Catal B-Enzym,2017,133(1):26-31.
[16]ALVAREZJUBETE L,WIJNGAARD H,ARENDT E K,et al.Polyphenol composition andin vitroantioxidant activity of amaranth,quinoa buckwheat and wheat as affected by sprouting and baking[J].Food Chem,2010,119(2):770-778.
[17]SENTER S D,CHAPMAN G W,WRJR F,et al.Sugar and nonvolatile acid composition of persimmons during maturation[J].J Food Sci,2010,56(4):989-991.
[18]CIANI M,COMITINI F,MANNAZZU I,et al.Controlled mixed culture fermentation:a new perspective on the use of non-Saccharomyces yeasts in winemaking[J].Fems Yeast Res,2010,10(2):123-133.
[19]CIHAN A C,YILDIZ E D,SAHIN E,et al.Introduction of novel thermostable α-amylases from genus anoxybacillus and proposing to group the Bacillaceae related α-amylases under five individual GH13 subfamilies[J].World J Microb Biot,2018,34(7):95.
[20]乔羽,于迪,邢晓莹.山西老陈醋发酵阶段高产淀粉酶芽孢杆菌的筛选与鉴定[J].中国酿造,2018,37(1):30-34.
[21]徐颖.高产α-淀粉酶生产菌的筛选鉴定及其酶学性质研究[D].成都:四川大学,2007.
[22]贾莉,郝林,金越.产酸性蛋白酶菌株在老陈醋澄清上的应用[J].食品工程,2003(2):22-23.
[23]黄家驷,刘盾,陈玄阳,等.浓香型高温酒曲中蛋白酶产生菌的筛选与鉴定[J].安徽农学通报,2017(21):35-37.
[24]董丹,车振明,关统伟.白酒酒糟中产纤维素酶菌株的筛选及其酶活力特性检测[J].中国酿造,2015,34(8):44-48.
[25]王霜,缪礼鸿,张明春,等.浓酱兼香型酒醅中产酱香芽孢杆菌的筛选及发酵风味成分分析[J].中国酿造,2017,36(10):61-65.