枸杞(Lycium barbarum L.)为茄科植物枸杞的成熟果实,枸杞籽油因其具有良好的保健作用而受到市场的广泛亲睐[1-2]。由于枸杞在生长过程中,频繁的使用农药,其残留的危害也可能影响到枸杞籽油的安全性[3]。目前为止,尚未有关于枸杞籽油中农药残留的检测的相关研究。食用植物油中的农药残留进行检测时,必须尽可能的除去基质中脂肪、有机酸、色素及其他高分子质量的干扰物,否则基质干扰很大,容易污染检测仪器,降低仪器使用寿命。目前,农药残留的前处理方法主要有固相萃取、液液萃取冷脱脂法、基质固相分散法、凝胶渗透色谱等[4-13]。这些方法中有些操作繁琐,有些只针对特定种类的农药,当测定多组分农药残留时,需要采用不同的前处理方法,大大加大了检测难度及成本。
本研究将样品经乙腈提取,以QuEChERS(quick,easy,cheap,effective,rugged,and safe)方法为前处理技术,采用丙基乙二胺(primary secondary amine,PSA)、C18、硫酸镁(MgSO4)吸附剂,优化最佳配比,可较好去除油脂和色素等杂质,大大地减小了样品基质干扰。提取溶液经过滤后气相色谱串联质谱(gas chromatography-tandem mass spectrometry,GC-MS/MS)检测,在质谱多反应监测(multiple reaction monitoring,MRM)模式下,进行基质外标法定量,可同时快速地检测枸杞籽油中28种农药残留量。该方法具有净化效果好,快速、简便、实用等优点,对枸杞籽油中多组分农药残留有普遍适用性,对于完善枸杞籽油卫生标准体系起到重要的推动作用。
1 材料与方法
1.1 材料与试剂
枸杞籽油:市售;PSA、C18、硫酸镁(适用于QuEChERS方法的填料):美国安捷伦公司;乙腈(色谱纯):赛默飞世尔科技有限公司;甲苯(色谱纯):天津市科密欧化学试剂有限公司;氯化钠(色谱纯):国药集团化学试剂有限公司。
氧化乐果、克百威、甲霜灵、三唑酮、氟虫腈、稻丰散、克菌丹、硫丹、杀扑磷、丙溴磷、氟硅唑、醚菌酯、三唑磷、丙环唑、异菌脲、联苯菊酯、溴螨酯、乙螨唑、甲氰菊酯、氯氟氰菊酯、双甲脒、咪鲜胺、哒螨灵、氯氰菊酯、氰戊菊酯、苯醚甲环唑、烯酰吗啉、嘧菌酯(纯度均>98%):德国Dr.Ehrenstorfer公司。
1.2 仪器与设备
7890B/7000C安捷伦三重四级杆气相色谱-质谱联用仪:美国安捷伦科技有限公司;3K15离心机:德国Sigma公司;IKAT25数显型分散机:德国IKA公司;Vortex-Genie2漩涡混合器:美国SI仪器公司。
1.3 方法
1.3.1 标准溶液的配制
准确称取28种农药标准品,用乙腈配制成1.0 mg/mL的标准储备液。用乙腈逐级稀释成1.0 μg/mL的混合标准中间溶液;准确移取混合标准中间溶液用空白基质提取液稀释成质量浓度为5.0 μg/L、10.0 μg/L、20.0 μg/L、50.0 μg/L、100.0 μg/L、200.0 μg/L系列标准工作溶液,供气相色谱-质谱联用仪测定。
1.3.2 原始样品的前处理
称取2 g枸杞籽油于50 mL离心管中,加入10 mL乙腈,于13 000 r/min条件下均质1 min,加入2 g氯化钠,继续均质1 min,4 ℃条件下,以9 000 r/min离心5 min,取上清液2 mL,加入100 mg C18、100 mg PSA及100 mg MgSO4吸附剂净化,涡旋离心,取上清液过0.22 μm的滤膜,供气相色谱-质谱联用仪测定。
1.3.3 仪器条件
气相色谱条件:DB-5MSUI毛细管色谱柱(30m×0.25mm×0.25 μm);进样口温度280 ℃;不分流进样;载气为氦气(纯度99.999%),流速1.0 mL/min;程序升温:60 ℃下保持1 min,以40 ℃/min升至170 ℃,不保持,再以10 ℃/min升至310 ℃,不保持,全部程序时间21 min,自动进样,进样量1 μL。
质谱条件:接口温度290 ℃;电子电离(electronic ionization,EI)源;溶剂延迟4.0 min;四级杆温度150 ℃;增益10;多反应监测。枸杞籽油中28种农药的定量和定性离子、碰撞能量等参数详见表1。
表1 28种农药的质谱分析参数
Table 1 Mass spectrum analysis parameters of 28 pesticides

化合物 保留时间/min前级离子 产物离子 驻留时间/min碰撞能量/eV氧化乐果克百威甲霜灵三唑酮6.67 7.74 9.19 9.96 155.9 164.2 234 208 109.9/79 149.1/121.1 174.1/146.1 181.1/111 60 50 60 25 5/20 10/5 10/20 5/20
续表
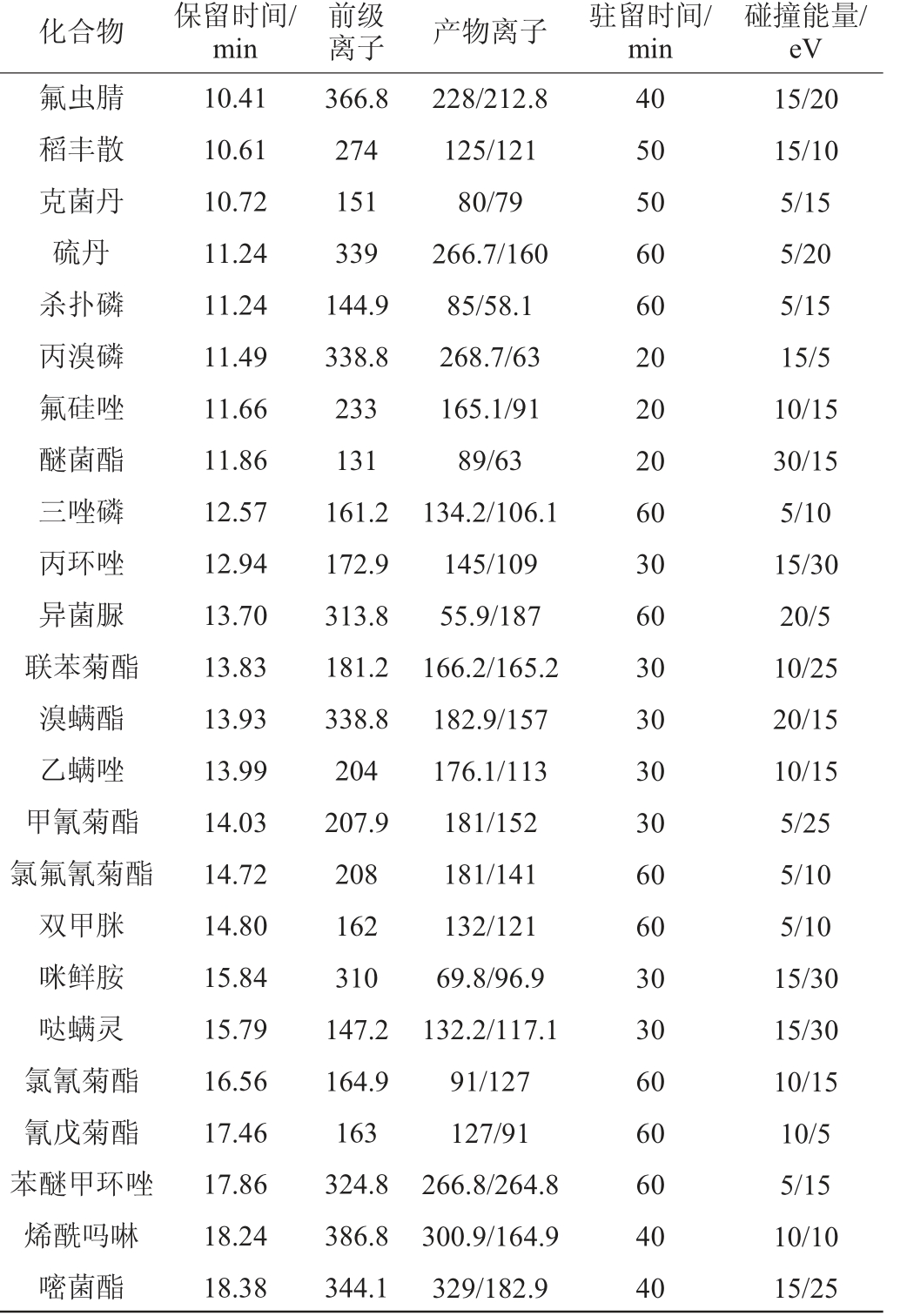
化合物 保留时间/min前级离子 产物离子 驻留时间/min碰撞能量/eV氟虫腈稻丰散克菌丹硫丹杀扑磷丙溴磷氟硅唑醚菌酯三唑磷丙环唑异菌脲苯菊酯溴螨酯乙螨唑氰菊酯氟氰菊酯双甲脒咪鲜胺哒螨灵氰菊酯戊菊酯醚甲环唑酰吗啉嘧菌酯10.41 10.61 10.72 11.24 11.24 11.49 11.66 11.86 12.57 12.94 13.70 13.83 13.93 13.99 14.03 14.72 14.80 15.84 15.79 16.56 17.46 17.86 18.24 18.38 366.8 274 151 339 144.9 338.8 233 131 161.2 172.9 313.8 181.2 338.8 204 207.9 208 162 310 147.2 164.9 163 324.8 386.8 344.1 228/212.8 125/121 80/79 266.7/160 85/58.1 268.7/63 165.1/91 89/63 134.2/106.1 145/109 55.9/187 166.2/165.2 182.9/157 176.1/113 181/152 181/141 132/121 69.8/96.9 132.2/117.1 91/127 127/91 266.8/264.8 300.9/164.9 329/182.9 40 50 50 60 60 20 20 20 60 30 60 30 30 30 30 60 60 30 30 60 60 60 40 40 15/20 15/10 5/15 5/20 5/15 15/5 10/15 30/15 5/10 15/30 20/5 10/25 20/15 10/15 5/25 5/10 5/10 15/30 15/30 10/15 10/5 5/15 10/10 15/25联甲氯氯氰苯烯
2 结果与分析
2.1 检测农药的选择
鉴于枸杞籽油是以枸杞籽为主要原材料的加工产品,前期对目前市场中枸杞常用农药的品种进行调查,并对120批次枸杞中农药残留量进行评估[14],针对枸杞中阳性农药对枸杞籽油进行分析检测。
2.2 质谱条件优化
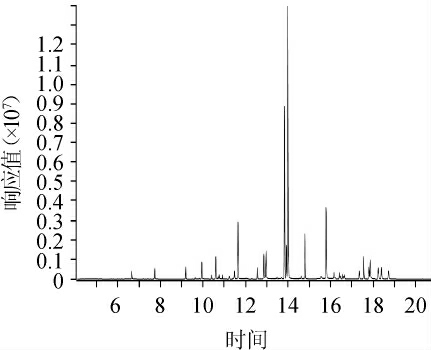
图1 28种农药混合标准溶液在MRM模式下总离子流色谱图
Fig. 1 Total ion chromatograms of mixed standard solutions of 28 pesticides under MRS mode conditions
分别采用单离子监测(single ion monitor,SIM)模式与MRM模式进行28种农药含量的测定。在SIM模式下,由于部分目标物响应较低、干扰大,难以准确定性;采用MRM模式,其针对性强,灵敏度高,对于较低含量的样品能准确的定性定量。因此,本研究选用MRM模式进行检测。在MRM模式下,质量浓度为100 μg/L的28种农药标准溶液总离子流图见图1。
2.3 基质效应
基质效应是在提取基质中的目标物时,基质中的干扰物影响目标化合物的离子化,使得目标化合物在仪器上的响应发生了增强或者抑制的现象[15]。基质效应的存在一方面可能导致样品产生假阳性或者假阴性的问题,另一方面会对待测物的准确定量产生严重干扰。本研究在采用纯溶剂配制的标准曲线进行定量时,28种农药在枸杞籽油中均为不同程度的基质增强效应。为提高目标化合物测定的准确度,本研究使用不含农药的空白基质提取液配制标准曲线,降低基质干扰的影响。
2.4 标准曲线、线性范围及检出限
在优化的条件下,以质量浓度为横坐标,定量离子峰面积为纵坐标,将配制的5.0 ng/mL、10.0 ng/mL、20.0 ng/mL、50.0 ng/mL、100.0 ng/mL、200.0 ng/mL系列浓度绘制标准曲线。28种农药的线性回归方程、相关系数、线性范围及检出限(limit of detection,LOD)(信噪比S/N≥10)见表2。结果表明,28种农药在基质中的线性范围良好,相关系数R2均≥0.996,检出限在10~50 μg/kg。
表2 28种农药的线性回归方程、相关系数、线性范围及定量限
Table 2 Linear equation, coefficient correlation, linear range,LOQ of the 28 pesticide

化合物 线性回归方程 相关系数R2线性范围/(ng·mL-1)检出限/(μg·kg-1)氧化乐果克百威甲霜灵三唑酮氟虫腈稻丰散克菌丹硫丹杀扑磷丙溴磷氟硅唑醚菌酯三唑磷丙环唑异菌脲联苯菊酯Y=3 490.17X-15 992.80 Y=3 548.98X-26 853.01 Y=2 548.74X-7 003.12 Y=1 202.80X-1 816.85 Y=2 350.79X-10 322.81 Y=5 054.42X-18 726.14 Y=206.00X+6 730.61 Y=661.81X-1 321.37 Y=104.44X-177.26 Y=2 740.03X-6 054.16 Y=4 282.53X-9 162.72 Y=11 581.09X-26 018.02 Y=4 142.16X-12 867.66 Y=9 272.24X-19 913.20 Y=201.74X+924.76 Y=40 095.15X-64 021.14 0.996 0.997 0.998 0.999 0.998 0.998 0.998 0.999 0.999 0.999 0.999 0.999 0.999 0.999 0.996 0.999 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 30 30 30 20 30 30 10 10 50 20 10 30 30 10 10 20
续表
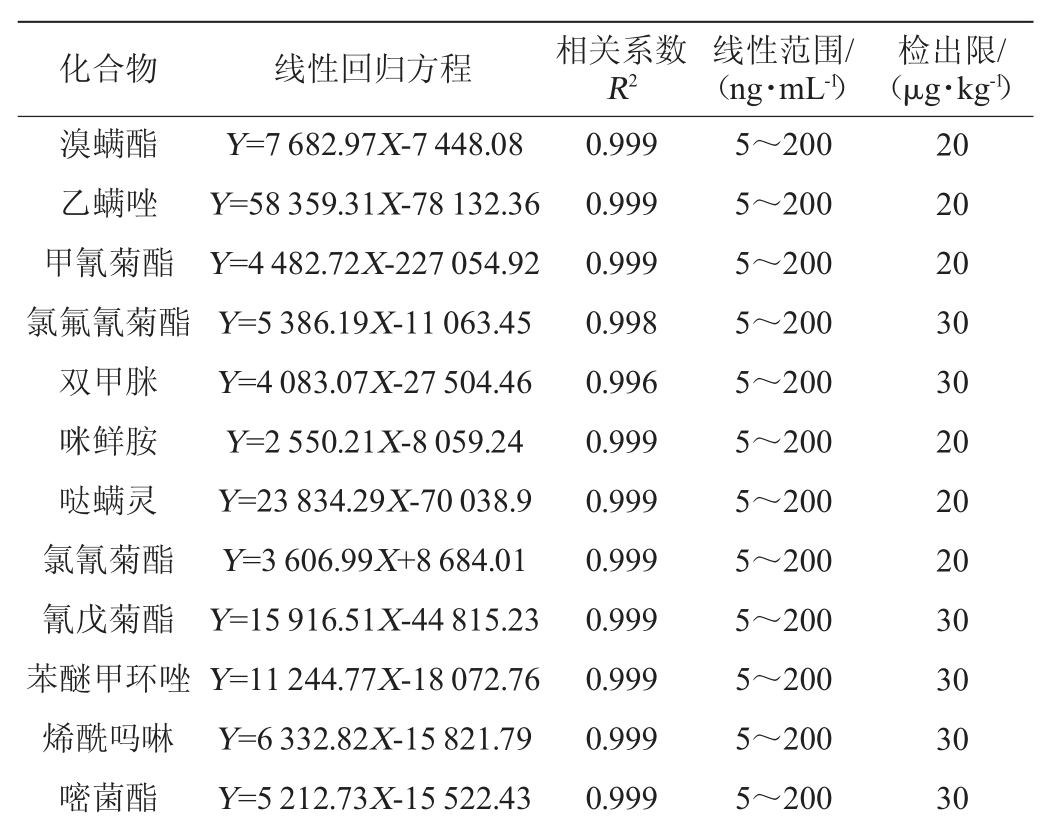
化合物 线性回归方程 相关系数R2线性范围/(ng·mL-1)检出限/(μg·kg-1)溴螨酯乙螨唑甲氰菊酯氯氟氰菊酯双甲脒咪鲜胺哒螨灵氯氰菊酯氰戊菊酯苯醚甲环唑烯酰吗啉嘧菌酯Y=7 682.97X-7 448.08 Y=58 359.31X-78 132.36 Y=4 482.72X-227 054.92 Y=5 386.19X-11 063.45 Y=4 083.07X-27 504.46 Y=2 550.21X-8 059.24 Y=23 834.29X-70 038.9 Y=3 606.99X+8 684.01 Y=15 916.51X-44 815.23 Y=11 244.77X-18 072.76 Y=6 332.82X-15 821.79 Y=5 212.73X-15 522.43 0.999 0.999 0.999 0.998 0.996 0.999 0.999 0.999 0.999 0.999 0.999 0.999 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 5~200 20 20 20 30 30 20 20 20 30 30 30 30
2.5 不同比例的净化填料对回收率的影响
不同比例的三种常用吸附剂PSA、C18、MgSO4对农药残留的影响,结果见图2。
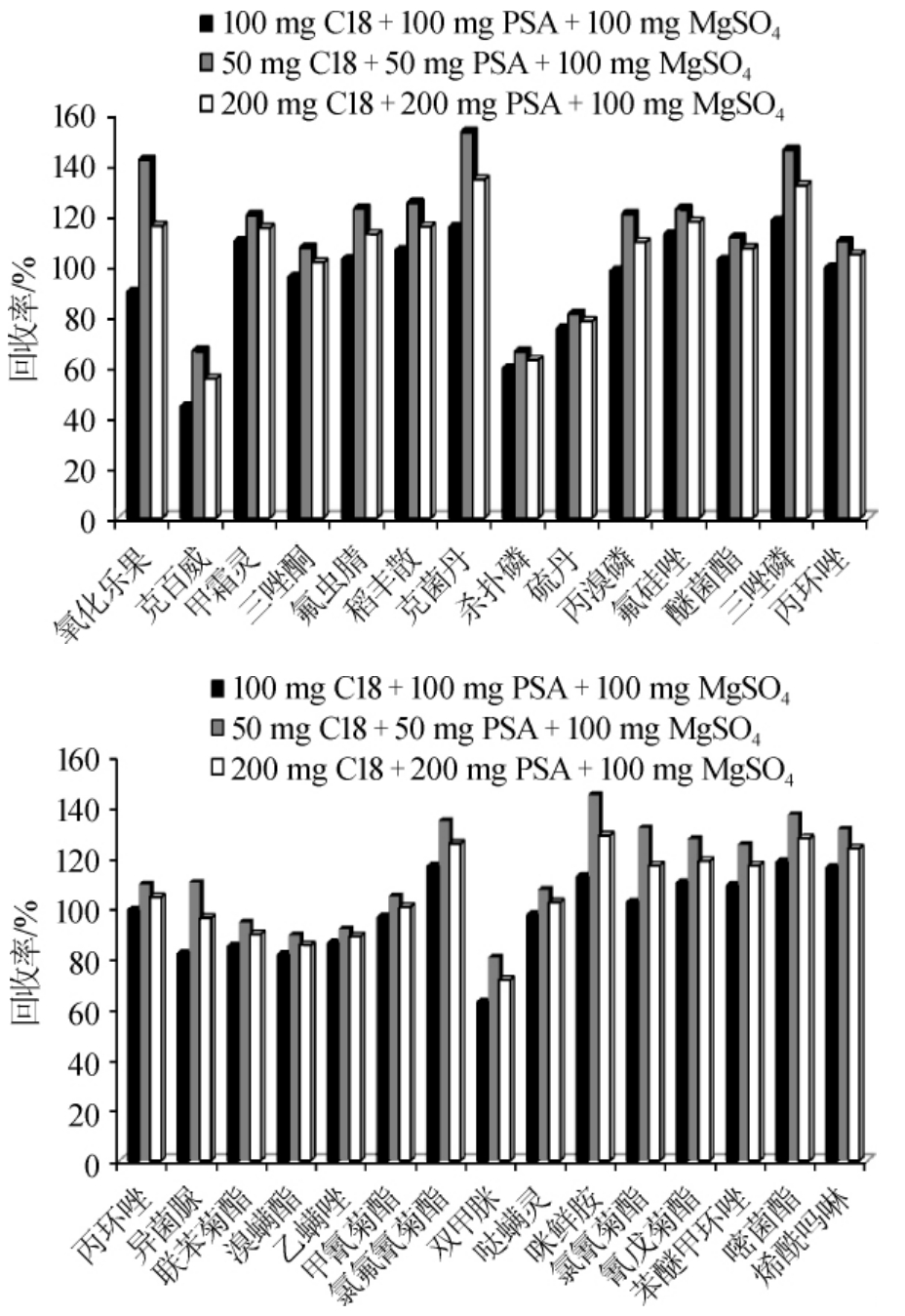
图2 不同吸附剂组合对28种农药回收率的影响
Fig. 2 Effect of different sorbent combinations on recovery rate of the 28 pesticide
由图2可知,当添加50 mg C18、50 mg PSA、100 mg MgSO4时,由于净化效果不明显,仍存在明显的基质增强效应,使得所有化合物的回收率均偏高,只有44.4%以上的农药回收率在70%~120%,氧化乐果、克菌丹、三唑磷、氯氟氰菊酯、咪鲜胺、氯氰菊酯、嘧菌酯等的回收率偏高明显,均>120%。当采用200 mg C18、200 mgPSA、100 mg MgSO4吸附剂组合时,有70.4%以上的农药回收率在70%~120%。而当采用100 mg C18、100 mg PSA、100 mg MgSO4吸附剂组合时,有88.9%以上的农药回收率在70%~120%。因此,选择PSA、C18和硫酸镁用量各为100 mg,可以取得较好的净化效果。
2.6 回收率试验
加标量分别为0.025 mg/kg和0.10 mg/kg,用枸杞籽油空白基质样品进行加标回收试验,结果见表3。由表3可知,低浓度加标回收率范围为60.10%~128.03%,相对标准偏差(relative standard deviation,RSD)为2.02%~17.9%;高浓度加标回收率范围为63.20%~105.10%,RSD为1.53%~9.82%。结果表明,该检测方法准确度较好。
表3 28种农药加标回收率试验结果
Table 3 Results of adding standard recovery rates of 28 pesticides

化合物氧化乐果克百威甲霜灵三唑酮氟虫腈稻丰散克菌丹硫丹杀扑磷丙溴磷氟硅唑醚菌酯三唑磷丙环唑异菌脲联苯菊酯溴螨酯乙螨唑甲氰菊酯氯氟氰菊酯双甲脒咪鲜胺哒螨灵氯氰菊酯氰戊菊酯苯醚甲环唑嘧菌酯烯酰吗啉添加质量浓度0.025 mg/kg回收率/%RSD/%添加质量浓度0.100 mg/kg回收率/% RSD/%62.89 69.53 84.85 78.51 99.57 91.48 89.49 120.09 85.30 72.25 93.23 95.33 111.65 81.80 75.32 71.94 68.66 73.48 74.09 128.03 60.1 93.42 112.12 80.89 99.08 96.71 98.88 85.66 8.42 9.02 6.93 7.36 4.76 3.03 16.3 17.9 15.3 5.33 2.02 3.76 5.00 2.36 14.0 8.55 4.69 3.01 11.0 5.71 12.7 4.44 6.46 16.6 5.05 4.70 6.74 5.70 79.30 79.10 86.30 84.30 88.30 86.10 80.70 81.10 81.80 77.80 90.70 94.70 105.10 82.60 78.10 69.50 70.10 75.90 81.10 98.70 63.20 79.30 98.20 87.20 87.10 88.20 95.80 89.60 5.49 8.48 3.20 2.14 9.63 2.70 3.14 5.01 1.53 5.33 2.00 1.58 4.47 1.70 6.21 4.10 1.67 1.91 2.82 9.82 7.56 3.26 4.15 4.80 2.74 3.50 2.32 3.50
2.7 样品检测
由于枸杞生长过程易交替发生病虫害,且种类颇多,因此防治难度非常大。根据前期对枸杞干果中农药残留量的检测发现,枸杞籽油中检出的农药在枸杞干果中均被检出。因此,枸杞籽油中的农药残留是来自于枸杞果中。同时可以看出菊酯类在枸杞籽油中的检出率较高,可能是由于菊酯类农药广泛使用于枸杞蚜虫防治,枸杞蚜虫对拟除虫菊酯药剂氰戊菊酯、氯氟氰菊酯、氰菊酯已产生低至中等水平抗性[19]。由于不能有效的控制枸杞蚜虫病,缺乏管理技术,农户的不规范用药,因此在正常水平上加大剂量使用,导致大量的枸杞果干中存在较高残留,而枸杞籽油中的部分菊酯农残可能是枸杞干果中引入的[20]。对市售23个枸杞籽油样品中的农药残留量进行检测,结果见表4。
表4 枸杞籽油及枸杞干果阳性样品农药残留水平
Table 4 Levels of pesticide residues in goji seed oil and positive samples of goji dried fruit

化合物 枸杞籽油阳性样品农药残留量/(mg·kg-1)枸杞干果阳性样品农药残留量/(mg·kg-1)氯氟氰菊酯氯氰菊酯氰戊菊酯0.033~0.321 0.022~0.346 0.034~0.369 0.009~2.450 0.011~0.470 0.003~0.740
由表4可知,氯氟氰菊酯、氯氰菊酯、氰戊菊酯均有不同程度检出,其余农药均未检出。
与枸杞果中阳性样品农药残留量相比较,枸杞籽油阳性样品农药残留量明显降低,其中氯氟氰菊酯残留量下降7.6倍,氯氰菊酯残留量由0.470 mg/kg下降至0.346 mg/kg,氰戊菊酯残留量下降了2倍,可能是由于枸杞籽油一般都是经过枸杞鲜果打浆后清洗出枸杞籽作为油料种子,在这个过程中可能使残留在油料种子中的农药分解、吸附。但从枸杞到枸杞籽,从枸杞籽油料到成品油加工过程中农药种类和残留量的变化情况仍不清楚,值得进一步研究。
3 结论
本研究建立了气相色谱三重四级杆串联质谱法(GCMS/MS)同时测定枸杞籽油中28种农药残留的方法。枸杞籽油经乙腈提取,以QuEChERS法为前处理技术,优化PSA、C18、MgSO4用量各为100 mg,在质谱多反应监测(MRM)模式下,进行基质外标法定量。结果表明,28种农药在5~200 μg/L的范围内线性关系良好,回归方程相关系数(R2)均>0.996,样品在添加水平为0.100 mg/kg下的平均回收率为63.20%~105.10%,相对标准偏差(RSD)为1.53%~9.82%。该方法前处理操作简便,有机溶剂用量很少,对环境和人体友好;准确度、精密度高,能够满足枸杞籽油中28种农药残留的定性和定量分析。本方法的建立为枸杞及枸杞籽油中农药残留的监控、风险评估等的研究提供了一种快速、高效、可靠的分析手段。
[1]高琳,马桂娟,张瑶.气相色谱法测定枸杞籽油中α-亚麻酸的含量及其不确定度评定[J].食品研究与开发,2017,38(2):174-177.
[2]陈妙瑞.食品检测中的农药残留检测技术探讨[J].山东工业技术,2018(21):231-245.
[3]罗淑年,刘丹怡,孙立斌,等.食用油脂的安全性[J].农业机械,2013(29):37-40.
[4]李欣.分散固相萃取-气相色谱-质谱法测定土壤中8 种菊酯类农药的残留量[J].干旱环境监测,2018,32(3):97-101.
[5]马昕.农药残留检测研究进展[J].青海农林科技,2018(3):56-59.
[6]王润.食品中农药残留检测的样品前处理技术[J].中国食品安全,2018(9):71.
[7]CUNHA S C,LEHOTAY S J,MASTOVSKA K,et al.Evaluation of the QuEChERS sample preparation approach for the analysis of pesticide residues in olives[J].J Separat Sci,2007,30:620-632.
[8] HERRMANN S S, POULSEN M E. Clean-up of cereal extracts for gas chromatography-tandem quadrupole mass spectrometry pesticide residues analysis using primary secondary amine and C18[J]. J Chromatogr A,2015,1423:47-53.
[9]KOESUKWIWAT U,LEHOTAY S J,MASTOVSKA K,et al.Extension of the QuEChERS method for pesticide residues in cereals to flaxseeds,peanuts,and doughs[J].J Agr Food Chem,2010,58:5950-5958.
[10]史晓梅,陈士恒,章晴,等.分散固相萃取-气相色谱法快速测定食用植物油中66 种农药残留[J].中国粮油学报,2016,31(7):132-137.
[11]王贵双,高丽华,赵俊平,等.固相萃取-气相色谱-质谱法测定粮谷中17 种有机氯和拟除虫菊酯农药残留[J]. 中国酿造,2010,29(11):165-168.
[12]周建科,唐翠苓,韩朝家,等.分散液液微萃取-液相色谱法测定白葡萄酒中拟除虫菊酯类农药[J].中国酿造,2012,31(7):164-166.
[13]阮华,荣维广,宋宁慧,等.QuEChERS-在线凝胶色谱-气相色谱-质谱法测定植物油中34 种农药残留[J]. 分析化学,2014,42(8):1110-1116.
[14]汤丽华,马桂娟,朱捷,等.高效液相色谱-串联质谱法同时测定枸杞中31 种农药残留[J].食品工业科技,2017,38(14):26-30.
[15]黄宝勇,肖志勇,陈丹,等.农药残留检测方法中关于基质效应补偿的相关问题探讨[J].农药科学与管理,2010,31(3):39-43.
[16]高尧华,滕爽,宋卫得,等.大豆、花生及粮油中56 种农药残留量的检测方法[J].大豆科学,2018,37(2):284-294.
[17]张云青,孟祥龙,唐秀,等.进口植物油脂中农药残留检测的前处理方法研究[J].食品研究与开发,2017,38(24):165-169.
[18]吴凤琪,靳保辉,吴卫东,等.分散固相萃取-气相色谱串联质谱法同时测定食用植物油中的8 种农药[J].中国油脂,2014,39(6):95-97.
[19]洪波,王坚,钱永德,等.宁夏枸杞蚜虫抗药性测定及防治试验[J].宁夏农学院学报,2000,21(4):30-34.
[20]张艳,苟春林,姜瑞,等.宁夏枸杞中拟除虫菊酯类农药残留风险评估[J].新疆农业科学,2015,52(12):2273-2278.