微生物采油(microbial enhanced oil recovery,MEOR)是通过向油藏注入微生物及营养源,或单独注入营养物质激活内源微生物,使微生物快速生长繁殖和合成代谢产物来提高石油采收率[1]。期间,微生物及其代谢产物能改变原油组成及其黏度和流动性,增大油层压力和扫油面积[2]。
碳源对MEOR有重要影响[3]。研究表明,补加糖类碳源可以促进采油微生物生长繁殖,降低原油利用率[4]。李清心等[5]以芽孢杆菌L-32利用原油产生的酸性代谢产物,降低原油黏度,补加葡萄糖会加快菌体生长,提高原油采收率。包木太等[6]利用5%淀粉水解液可以对油藏内源有益采油菌烃类氧化菌(hydrocarbon-oxidizing bacteria,HOB)有较好的激活效果,菌体能维持较长的平稳期并同时产酸和产表面活性物质,从而增加油层压力,降低原油黏度以及原油/岩石体系界面张力,提高残油采收率。于海威等[7]在45℃厌氧筛选的驱油菌株SF67可以利用原油快速生长,降解饱和烷烃,降低含蜡量及界面张力,促进原油采收。
深层油藏温度较高,筛选耐高温菌种及适宜营养尤为重要[8]。利用微生物产生的表面活性剂提高原油采收率有很好的应用前景[9]。前期研究发现芽孢杆菌属耐高温采油菌株ZY-1能产糖脂类阴离子表面活性剂[10]。本实验主要研究该菌株利用不同碳源生长、产表面活性物质以及对不同碳源的利用进行比较分析,为深入研究和应用提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 实验菌株
节杆菌属(Arthrobacter sp.)菌株ZY-1:分离自辽河油田原油,在200 g/L甘油中于-80℃冰箱中保存。
1.1.2 化学试剂
木糖、葡萄糖、石油醚、环己烷(均为分析纯):天津科密欧化学试剂有限公司;液体石蜡、淀粉(化学纯):天津市博迪化工有限公司。
1.1.3 培养基
斜面培养基:牛肉膏5 g/L,NaCl 5 g/L,蛋白胨10 g/L,琼脂20 g/L,蒸馏水1 L,pH值为7.0。
种子培养基:牛肉膏5 g/L,NaCl 5 g/L,蛋白胨10 g/L,蒸馏水1 L,pH值为7.0。
发酵培养基:Na2HPO4 1.5 g/L,KH2PO4 3.4 g/L,NaNO3 4 g/L,MgSO4·7H2O 0.2 g/L,酵母粉0.2 g/L,石蜡2 g/L,蒸馏水1 L,pH值为7.0。
培养基均在121℃条件下灭菌20 min。
1.2 仪器与设备
CR21G高速冰冻离心机:日本日立公司;WFJ 7200型可见光分光光度计:上海尤尼柯仪器有限公司;Jzhy1-180界面张力仪:承德大华试验机有限公司;GC-8900气相色谱仪:山东滕州经纬分析仪器有限责任公司。
1.3 方法
1.3.1 菌种活化及种子液的制备
将-80℃储存的菌种接于斜面培养基,于60℃活化24 h,得活化菌种。在种子培养基中接入2环/100 mL活化菌种,在60℃培养24 h,得液体种子。
1.3.2 菌株对不同碳源的利用效果
分别在不同碳源(石蜡2 g/L、木糖2 g/L+石蜡2 g/L、葡萄糖2 g/L+石蜡2 g/L、淀粉2 g/L+石蜡2 g/L)的发酵培养基接入5%液体种子,60℃静置培养7 d。每天定时取样测定发酵液的菌体密度(OD600 nm值),上清液的表面张力、乳化活性及石蜡的含量。
1.3.3 测定方法
菌体密度:根据浊度法测定[11]。
表面张力:以表面张力仪测定[12]。将弃油相发酵液3 000×g离心20 min,用表面张力仪测上清液表面张力。
乳化活性:在1.5 mL弃油相发酵液中加入1 mL石蜡,振荡5 min后静置24 h,测定乳化层和总液层高度[13-14]。乳化活性=乳化层高度/总液层高度×100%。
石蜡含量:采用气相色谱法测定[15]。进样室:280℃,火焰离子化检测器(flame ionization,FID):300℃,初始柱温:80℃,升温速度:5℃/min升温至200℃维持2 min;再以8℃/min升温至280℃维持30 min。进样量:0.2μL。
2 结果与分析
2.1 不同碳源对菌株生长的影响
由图1可知,以石蜡为碳源时,菌株ZY-1在发酵0~3 d时生长速度快,发酵3 d时菌体密度OD600 nm值为0.60,随后急降至OD600 nm值为0.41,发酵7 d后菌体密度升至OD600 nm值为0.62;以木糖+石蜡为碳源时,菌株ZY-1在发酵1 d时菌体生长速度较快,随后减慢,3 d后平稳上升,发酵7 d时菌体密度升至OD600nm值为0.77;以葡萄糖+石蜡、淀粉+石蜡为碳源时,菌株ZY-1在发酵1 d时菌体生长速度较快,随后生长缓慢,发酵7 d后菌体密度分别为OD600nm值0.29、OD600 nm值0.31,且菌体生长量始终低于以石蜡为碳源时。因此,以木糖+石蜡为碳源时有利于菌体生长。
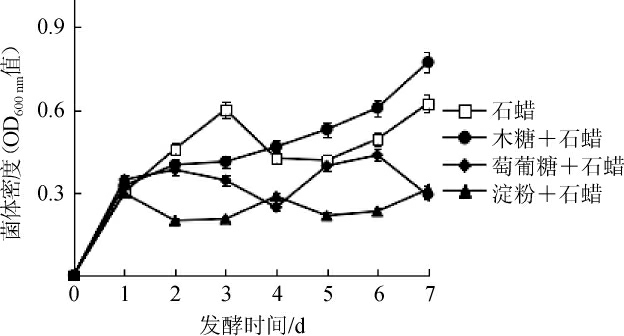
图1 碳源对菌株生长的影响
Fig.1 Effect of carbon sources on the strain growth
2.2 不同碳源对发酵液表面张力的影响
由图2可知,以石蜡为碳源时,发酵液表面张力在发酵2 d时降55.45 mN/m,发酵2~3 d时上升至62.6 mN/m,发酵7 d时发酵液表面张力降至52.3 mN/m;以木糖+石蜡为培养基碳源时,发酵液在发酵2 d时表面张力快速下降,且整个发酵过程表面张力较低,在发酵7 d时发酵液表面张力降至50.45 mN/m;以葡萄糖+石蜡、淀粉+石蜡为碳源时,发酵液表面张力均在发酵3 d时降至最低,分别为45.9 mN/m、43.8 mN/m,发酵7 d时,表面张力分别降至49.5 mN/m、47.9 mN/m。因此,淀粉+石蜡为碳源时最利于发酵液表面张力的降低,效果最好。
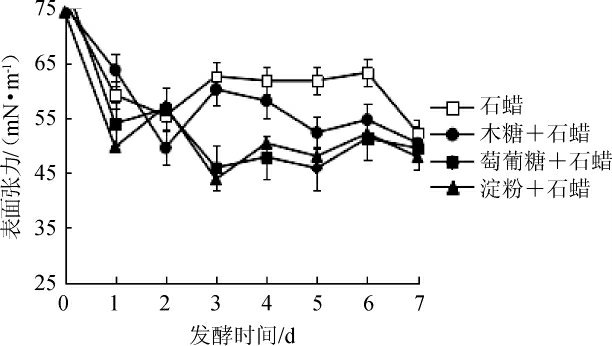
图2 碳源对发酵液表面张力的影响
Fig.2 Effect of carbon sources on surface tension of fermentation broth
2.3 不同碳源对发酵液乳化活性的影响
由图3可知,以石蜡为碳源时,发酵液乳化活性在发酵2 d时升至41.6%,发酵2~4 d时下降至14%,发酵7 d时发酵液乳化活性升至55.7%;以木糖+石蜡、淀粉+石蜡为培养基碳源时,发酵液乳化活性均在发酵2 d时快速上升,分别达到61.3%、63.3%,且整个发酵过程乳化活性较高,在发酵7 d时发酵液乳化活性分别达到50%和60%。以葡萄糖+石蜡为碳源时,发酵液乳化活性在发酵3 d时升至最高为63.3%,发酵7 d时乳化活性为46.6%。因此,以木糖+石蜡、淀粉+石蜡为碳源时更有利于发酵液乳化活性的升高。
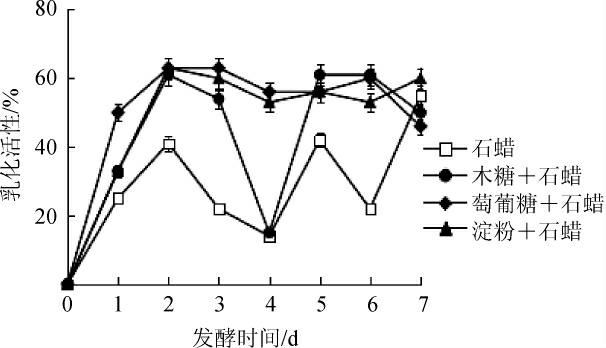
图3 碳源对发酵液乳化活性的影响
Fig.3 Effect of carbon sources on emulsification of fermentation broth
2.4 不同碳源对发酵过程中石蜡消耗的影响
由图4可知,菌株ZY-1以石蜡为碳源时,发酵0~3 d石蜡快速大量消耗,消耗了55%,发酵3~7 d消耗减慢,发酵7 d消耗石蜡72%,与菌体生长密切相关。在石蜡碳源培养基中外加糖类碳源,可以在发酵0~3 d明显减慢对石蜡的消耗,其中木糖+石蜡碳源消耗石蜡41%,淀粉+石蜡消耗石蜡43%,葡萄糖+石蜡碳源消耗石蜡54%,发酵7 d分别消耗石蜡61%、77%、79%。因此,与葡萄糖和淀粉相比,木糖更有利于减慢石蜡的消耗。
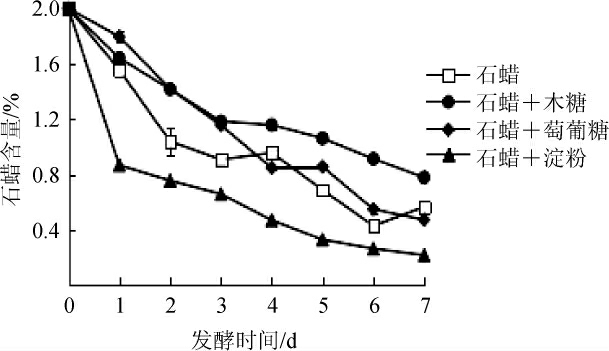
图4 碳源对发酵过程中石蜡含量的影响
Fig.4 Effect of carbon sources on paraffin content during the fermentation
3 讨论
耐高温采油菌株ZY-1以石蜡为唯一碳源进行生长繁殖,产生的表面活性剂很少,加入糖类碳源可以促进产物生成,表现在发酵液表面张力更低,乳化活性更高。同菌属菌株23-1产脂肽类阴离子表面活性剂,也有相同的实验结果[17]。菌株ZY-1以木糖-石蜡为混合碳源在整个发酵过程比单独石蜡碳源的石蜡消耗慢且少,木糖的存在可以降低石蜡的利用速度和利用量,说明与石蜡相比该菌株更易利用木糖生长。这与菌株Acinetobacter BHSN以木糖为碳源更有利于细胞生长与合成生物表面活性剂的结果相似,而与同菌株以葡萄糖为碳源加快细胞生长速度,但对促进生物表面活性剂合成效果不明显的结果相反[18]。葡萄糖对提高伊朗油藏采收率作用显著[19]。本研究石蜡分别与木糖、葡萄糖以及淀粉的混合碳源可不同程度的减慢菌株对石蜡的利用率,促进生物表面活性剂合成效果明显,使发酵上清液表面张力降至更低,乳化活性更高。在菌株Geobacillus toebii R-32639的采油模型中添加淀粉等营养源,可使原油表面张力降低25.3%,改善原油的流动能力,提高采收率[20]。本研究混合碳源发酵液的表面张力较之降低幅度更大,减慢发酵过程对原油的消耗,故有利于石油采收。
4 结论
补加碳源与单一石蜡作为培养基碳源相比更有利于促进菌株代谢环境的表面张力降低以及乳化活性升高,其中木糖-石蜡碳源有利于促进细胞生长OD600 nm值为0.77,减少了11%的石蜡消耗,并且表面张力降至最低49.5 mN/m,乳化活性高达61.3%。葡萄糖-石蜡以及淀粉-石蜡碳源不能明显促进细胞生长,但在发酵前期能减慢对石蜡的利用,明显促进生物表面活性剂的合成。在菌株ZY-1采油应用中,宜利用木糖促进合成生物表面活性剂,并减少短链烷烃的消耗,从而提高原油的采收率。添加葡萄糖和淀粉虽然不能明显促进细胞生长,但由于其可以减慢对石蜡的消耗,并在一定程度上促进生物表面活性剂的产生,对微生物采油也具有一定的应用价值。
[1]柏璐璐.微生物采油技术现状及发展探讨[J].化学工程与装备,2018(8):285-287.
[2]王鑫.微生物采油技术提高采收率机理及影响因素分析[J].云南化工,2018(6):87-88.
[3]冯云,段传慧,林军章,等.中高温油藏内源微生物厌氧激活[J].生物加工过程,2016(3):12-16.
[4]ROLING WF,HEAD IM,LAMER S R.The microbiology of hydrocarbon degradation in subsurface petroleum reservoirs and prospects[J].Res Microbiol,2003,154(5):321-328.
[5]李清心,康从宝,林建强,等.芽孢杆菌L-32发酵条件优化及提高原油采收率实验研究[J].石油大学学报:自然科学版,2004(3):52-55,140.
[6]包木太,袁书文,宋智勇,等.不同碳源激活剂对胜利油田中一区油藏内源菌激活效果评价[J].化工学报,2011,62(3):786-791.
[7]于海威.驱油菌SF67的室内性能评价实验研究[J].中国石油和化工标准与质量,2012,32(4):50.
[8]ZHANG G Y,MA F,LIANG Y B,et al.Domain and theory-technology progress of global deep oil&gas exploration[J].Acta Petrolei Sinica,2015,36(9):1161-1163.
[9]BANAT I M,MAKKAR R S,CAMEETRAS.Potential commercial applications of microbial biosurfactants[J].Appl Microbiol Biot,2000,53(5):495-508.
[10]王佳新.外加碳源对微生物采油特性的影响[D].大连:大连工业大学,2011.
[11]MARGARITIS A,ZAJIC JE,GERSON D F,et al.Production and surface-active properties of microbial surfactants[J].Biotechnol Bioeng,1979,21(7):1151-1162.
[12]柴玲玲,樊国栋,葛君.无溶剂法合成食品添加剂菜籽油蔗糖酯的研究[J].中国酿造,2011,30(7):39-42.
[13]NITSCHKE M,PASTORE G M.Production and properties of a surfactant obtained from Bacillus subtilis grown on cassava waste water[J].Bioresouce Technol,2016,97(2):336-341.
[14]杨宁,王伟明,姚琳,等.3,5-二硝基水杨酸法测定发酵型果露酒中总糖含量[J].中国酿造,2018,37(1):181-184.
[15]BARATHI S,VASUDEAN N.Utilization of petroleum hydrocarbons by Pseudomonas fluorescens isolated from a petroleum contaminated soil[J].Environ Int,2001,26(55):413-416.
[16]刘廷丹,杨秀娟,邓君明,等.苯酚-硫酸法测定蛤蚧酒中多糖含量[J].食品工业,2018(8):298-301.
[17]李牧,杨红,刘思贤.微生物表面活性剂在稠油乳化降粘中的实验研究[J].特种油气藏,1999(4):53-58,67.
[18]曹娟,徐志辉,李凌之.生物表面活性剂的石油降解菌Acinetobacter BHSN 的研究[J].生态与农村环境学报,2009,25(1):73-78.
[19]金佩强,王琪,杨克远.在MEOR过程中产生生物表面活性剂提高伊朗油藏采收率的试验方法[J].国外油油田工程,2005(10):10-14,20.
[20]MOHAMAD FULAZZAKY,DEA INDRIANI ASTUTI.Laboratory simulation of microbial enhanced oil recovery using Geobacillus toebii R-32639 isolated from the Handil reservoir[J].RSC Adv,2015,5:3908-3916.