中国白酒是世界著名的六大蒸馏酒之一,是一种以谷物为原料、酒曲为糖化发酵剂、采用双边或固态糖化发酵生产的酯香浓郁的蒸馏酒[1]。大曲作为白酒酿造过程中的糖化、发酵和生香剂,具有丰富的微生物和酶系,对白酒的风味和口感起关键性的作用[2]。因此,在我国传统酿酒行业一直流传着“曲乃酒之骨”[3-4]的说法。由于多种微生物富集在大曲里且在制曲过程中自然生长起来,因此整个大曲微生物复杂而多样[5]。
散囊菌属(Eurotium)真菌大量存在于传统发酵食品生产过程中,具有产多种生物酶以及吲哚衍生物、二酮哌嗪等活性次级代谢产物的性能[6-7],可催化发酵食品中各种相关物质发生氧化、聚合、降解、转化,是一种重要的功能微生物类群。如茯砖茶中的“金花菌”-“冠突散囊菌(Eurotium cristatum)”,可产生多酚氧化酶、阿魏酸酯酶、酯化酶、纤维素酶、蛋白酶等多种生物酶,并具有降脂、降压、调节糖代谢、抗氧化、抑菌等功能[8-9]。目前,在传统白酒生产领域有关散囊菌的研究主要集中在分离鉴定水平,已有文献显示[10-12],冠突散囊菌(E.cristatum)、谢瓦散囊菌(E.cheva lieri)、阿姆斯特丹散囊菌(E.amstelidami)均可分离自白酒大曲,其中谢瓦散囊菌在清香型、浓香型及浓香型大曲中均可分离到,且为浓香型和酱香型大曲中的优势真菌[12-13],但对这些菌种在白酒大曲中的相关功能研究较少。
本研究通过多相鉴定和响应面方法[14]对该菌种进行分类学研究及培养条件优化,旨在提高其生物量,后期该菌种将主要以菌粉或菌剂形式强化于白酒大曲生产中,以达到提高大曲阿魏酸酯酶活性及改善大曲风味特征的效果,从而进一步提高酒体品质。
1 材料与方法
1.1 材料与试剂
1.1.1 试验菌株
散囊菌(Eurotium)CICC 41584:分离于山东扳倒井股份有限公司中高温大曲,保藏于中国工业微生物菌种保藏管理中心(China Center of Industrial Culture Collection,CICC)。
1.1.2 化学试剂
蔗糖、葡萄糖、乳糖、麦芽糖、果糖、麦芽糖、纤维二糖、可溶性淀粉:广东汕头西陇化工有限公司;酵母浸粉、牛肉浸粉、蛋白胨、大豆蛋白胨、胰蛋白胨:北京奥博星生物技术有限责任公司;硫酸铵、硝酸铵、MgSO4、FeSO4、CaCl2、KCl、NaCl、K 2HPO4(均为分析纯):北京化学试剂公司;真菌脱氧核糖核酸(deoxyribonucleic acid,DNA)基因组提取试剂盒:生工生物工程股份有限公司。试验所用试剂均为分析纯或生化试剂。
1.1.3 培养基
察氏琼脂培养基(Czapek dox agar,CDA)、麦芽浸粉肉汤培养基(malt extract broth,MEB):北京陆桥技术股份有限公司;API20C AUX试剂盒:生物梅里埃(中国)公司。
CDA培养基:蔗糖30 g/L,KCl 0.5 g/L,FeSO4·7H2O 0.01 g/L,K2HPO4 1.0 g/L,NaNO3 3.0 g/L,MgSO4·7H2O 0.5 g/L,琼脂15.0 g/L,自然pH,121℃灭菌15 min。
MEB培养基:麦芽浸粉20g/L,自然pH,121℃灭菌15min。
基础生长培养基:在MEB培养基中添加蔗糖40 g/L,自然pH,121℃灭菌15 min。
1.2 仪器与设备
Olympus BH-2光学显微镜:奥林巴斯有限公司;Hitachi SU8010扫描电镜:日本HITACHI公司;Tprofessional standard 96 Gradient聚合酶链式反应(polymerase chain reaction,PCR)仪:德国Biometra公司;FE20型pH计:梅特勒-托利多仪器(上海)有限公司;BHG-8082型恒温培养箱、THZ-98C恒温振荡培养箱:上海一恒科学仪器有限公司;SHB-III循环水式多用真空泵:郑州长城科工贸有限公司;CS101-3D电热鼓风干燥箱:重庆四达试验设备有限公司。
1.3 试验方法
1.3.1 菌株CICC 41584多相分类学鉴定
采用多相分类学鉴定技术对菌株CICC 41584的形态特征观察、生理生化试验以及分子生物学进行研究。
形态学观察:将菌株CICC 41584接种到察氏琼脂培养基上,25℃恒温培养7 d,观察菌落形态特征,并使用光学显微镜观察菌体特征。收集新鲜菌体,加入质量分数为2.5%的戊二醛,在4℃条件下固定过夜,离心收集菌体,使用pH 7.2、浓度100 mmol/L的磷酸盐缓冲液漂洗3次。分别使用体积分数50%、70%、85%、95%的乙醇溶液梯度脱水,无水乙醇脱水3次后使用临界冷冻干燥仪进行二氧化碳临界点干燥,再通过喷金-离子溅射仪进行喷金后,使用Hitachi SU8010扫描电镜观察菌丝及其孢子的形态特征[15]。
生理生化试验:采用API 20 C AUX试剂盒测定菌株CICC 41584对碳源底物的利用能力[16]。具体操作过程:首先将新鲜菌体加到0.85%NaCl缓冲液中,制备成2 McFarland菌悬液,准确吸取100μL菌悬液加到试剂盒培养基中,混匀后,滴加到API 20 C AUX试剂条中,25℃培养5 d,观察试验结果。
分子生物学鉴定:使用真菌DNA基因组试剂盒提取DNA,具体操作步骤见试剂盒说明书。利用引物Bt2a(5'GGTAACCAAATCGGTGCTGCTTTC3')和Bt2b(5'ACCCTCAGTGTAGTGACCCTTGGC')扩增β-tubulin基因[17]。PCR反应体系:10×PCR Buffer 5μL,脱氧核糖核苷三磷酸(deoxyribonucleoside triphosphate,dNTPs)(2.5 mmol/L)4 μL,模板2μL,Taq DNA聚合酶1μL,引物各1μL,补充去离子水至50μL。PCR反应条件:94℃预变性5 min;94℃变性50 s,55℃退火50 s,72 ℃延伸50 s,33个循环;72 ℃再延伸7 min[18]。PCR扩增产物使用1.0%的琼脂糖进行验证后,送于北京诺赛基因组研究中心有限公司进行测序。将测序结果在美国国家生物技术信息中心(national center of biotechnology information,NCBI)数据库中进行相似性比对,采用Blast程序进行同源性序列分析,使用MEGA 5.0构建系统发育树[19]。
1.3.2 种子液制备
菌种活化:将甘油保藏的菌株CICC 41584接种于CYA察式平板培养基中,待培养物产生大量黄色孢子后连续转接3次,备用。
种子液制备:挑取一环活化好的菌株接入装有200 mL液体的MEB培养基中,于28℃、120 r/min条件下恒温振荡培养7 d,制备成种子液。
1.3.3 培养条件优化单因素试验设计
碳源确定:在MEB培养基中分别添加葡萄糖、蔗糖、果糖、麦芽糖、乳糖、纤维二糖、可溶性淀粉(添加量为40 g/L)。接种量2%,装液量50 mL/250 mL,28℃、120 r/min恒温振荡培养7 d,培养结束之后用定性滤纸过滤,在80℃干燥箱中烘干至恒质量,测定菌丝干质量,毎组3个平行试验,考察不同碳源对菌丝干质量的影响。
氮源确定:在碳源优化的培养基基础上,分别添加酵母浸粉、NH4NO3、胰蛋白胨、蛋白胨、大豆蛋白胨、硫酸铵、牛肉浸粉(添加量为10 g/L),其他成分不变。接种量2%,装液量50 mL/250 mL,28℃、120 r/min振荡培养7 d,测定菌丝干质量,考察不同氮源对菌丝干质量的影响。
无机盐确定:在碳源、氮源优化的培养基基础上,分别添加K 2HPO4、MgSO4、FeSO4、CaCl2、KCl、NaCl(添加量为5 g/L),其他成分不变。接种量2%,装液量50 mL/250 mL,28℃、120 r/min培养7 d,测定菌丝干质量,考察不同无机盐对菌丝干质量的影响。
1.3.4 培养条件优化Plackett-Burman试验设计
在确定碳源、氮源以及无机盐种类的基础上,选取影响菌丝干质量的发酵时间、pH值、接种量、装液量、转速及温度共9个因素进行Plackett-Burman试验设计,设计2个空项以估计试验误差,每个因素选高低2个水平,以(-1,+1)编码各值[20],利用Design Expert 10.0软件对其进行N=12的Plackett-Burman试验设计,以菌丝干质量(Y)作为响应值,每组试验设置3个平行[21]。Plackett-Burman试验设计的因子与水平如表1所示。
表1 Plackett-Burman试验设计因素与水平
Table 1 Factors and levels of Plackett-Burman experimental design
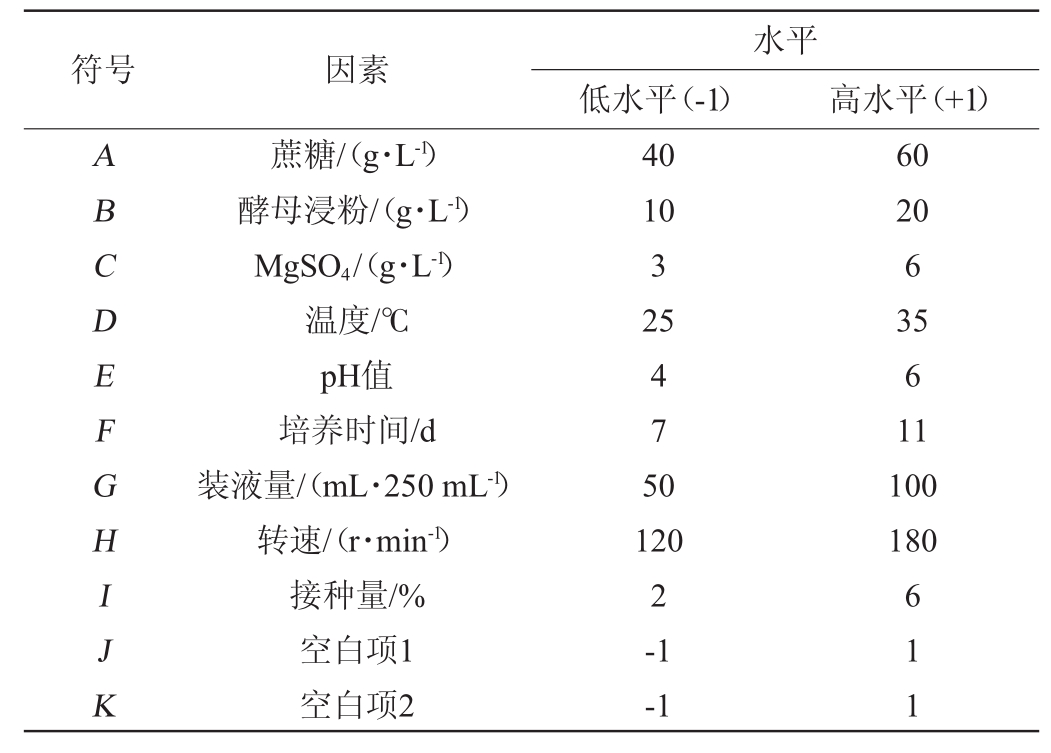
符号 因素 水平低水平(-1) 高水平(+1)A B C D E F G H I J K蔗糖/(g·L-1)酵母浸粉/(g·L-1)MgSO4/(g·L-1)温度/℃pH值培养时间/d装液量/(mL·250 mL-1)转速/(r·min-1)接种量/%空白项1空白项2 40 10 3 25 4 7 5 0 120 2-1-1 60 20 6 35 6 11 100 180 6 1 1
1.3.5 培养条件优化最陡爬坡试验
根据表1试验数据的分析结果,从众多因素中筛选出对菌丝干质量影响较大的3个显著因素,以此来确定各因素的水平,爬坡方向和步长,能快速、经济地逼近最佳值区域,来确定响应面分析的中心点[22-23],进而对选出的3个显著因素进行Box-Behnken试验设计[24]。
1.3.6 培养条件优化Box-Behnken试验设计
采用Box-Behnken试验设计对酵母浸粉、硫酸镁以及发酵时间进行优化,以菌丝干质量(g/100 mL)为响应值,每个因素的3个水平以(-1,0,+1)编码,每个试验点进行3次平行试验[25]。Box-Behnken试验设计的因子与水平见表2。
表2 Box-Behnken试验设计因素与水平
Table 2 Factors and levels of Box-Behnken experimental design
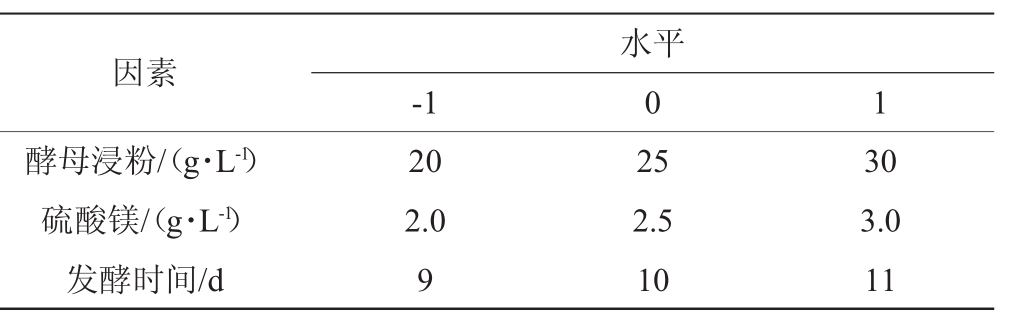
因素酵母浸粉/(g·L-1)硫酸镁/(g·L-1)发酵时间/d-1水平0 1 20 2.0 9 25 2.5 10 30 3.0 11
2 结果与分析
2.1 菌株CICC 41584多相分类学鉴定
2.1.1 形态学鉴定
菌株CICC 41584在察氏琼脂培养基上25℃培养7 d,菌落形态鉴定及镜检测定结果如图1所示。由图1a可知,菌落直径30~31 mm,中央黄褐色,周围蛋黄色;中心凸起;质地丝绒状;反面浅橙黄色;无渗出液产生,无可溶性色素产生;由图1b和1c可知,菌丝黄色具饰,缠绕、较细;闭囊壳大量,黄褐色,存在于具饰菌丝网中,直径150~200μm,成熟后破裂释放出大量子囊;子囊近球形或椭圆形,长轴直径10~20μm,内含8个子囊孢子;由图1d可知,子囊孢子双凸镜形,中部具鸡冠状凸起,长轴直径为5.0~7.5μm;未见分生孢子结构。
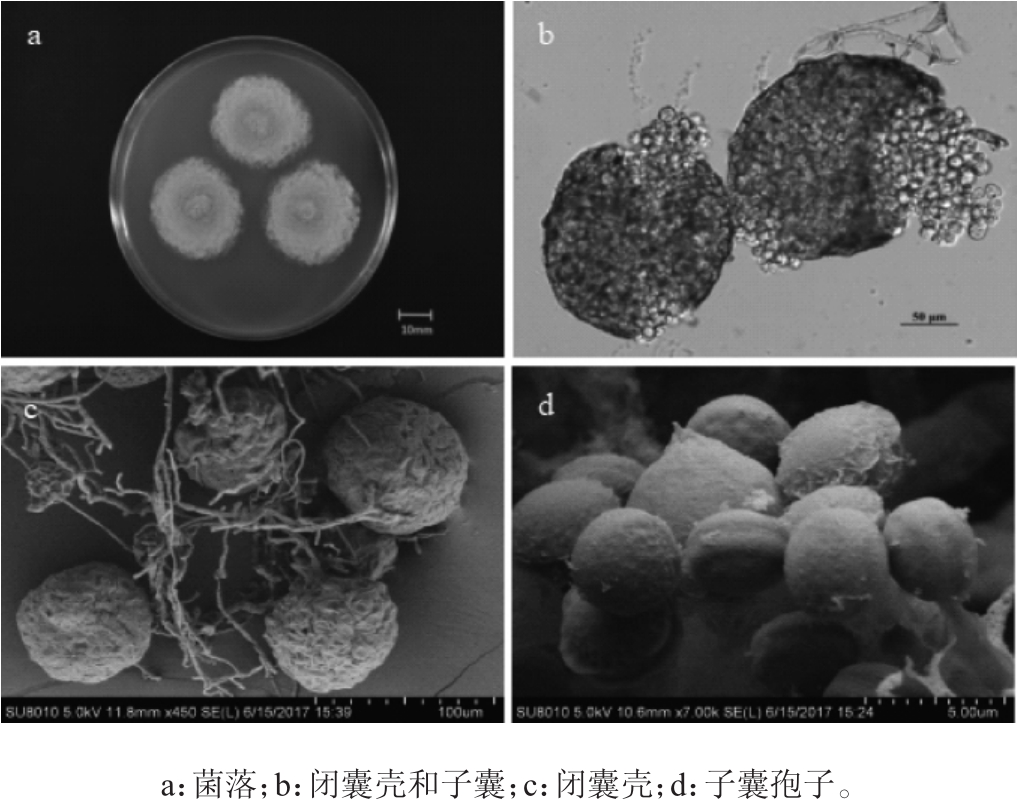
图1 菌株CICC 41584的形态学观察结果
Fig.1 Morphological observation results of strain CICC 41584
2.1.2 生理生化特征分析
表3 菌株CICC 41584的碳源利用结果
Table 3 Carbon source utilization results of strain CICC 41584
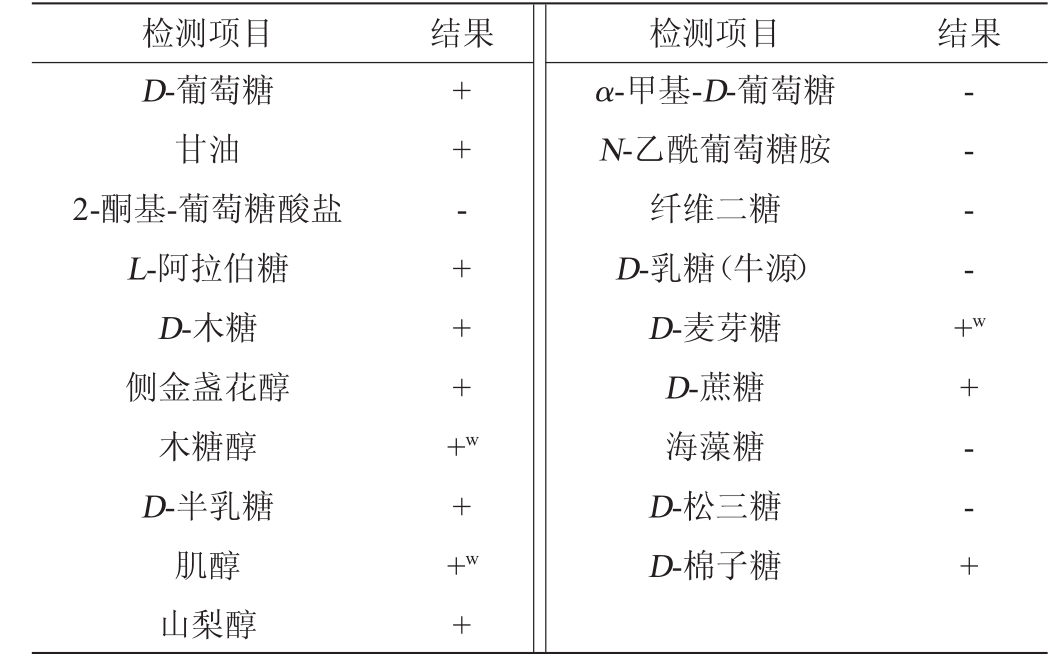
注:“+”表示结果呈阳性;“+w”表示呈弱阳性;“-”表示结果呈阴性。
检测项目 结果 检测项目 结果D-葡萄糖甘油2-酮基-葡萄糖酸盐L-阿拉伯糖D-木糖侧金盏花醇木糖醇D-半乳糖肌醇山梨醇+ + - + + + +w + +w +α-甲基-D-葡萄糖N-乙酰葡萄糖胺纤维二糖D-乳糖(牛源)D-麦芽糖D-蔗糖海藻糖D-松三糖D-棉子糖- - - - +w + - - +
由表3可知,菌株CICC 41584能够很好地利用D-葡萄糖、甘油、L-阿拉伯糖、D-木糖、侧金盏花醇、D-半乳糖、山梨醇、D-蔗糖、D-棉子糖;菌株对木糖醇、肌醇、D-麦芽糖表示弱生长;不能利用2-酮基-葡萄糖酸盐、α-甲基-D-葡萄糖、N-乙酰葡萄糖胺、纤维二糖、D-乳糖、海藻糖、D-松叁糖。
2.1.3 分子生物学鉴定
将菌株CICC 41584测序结果在NCBI数据库中进行Nucleotide blast比对,并构建系统发育树。菌株的系统发育树如图2所示。
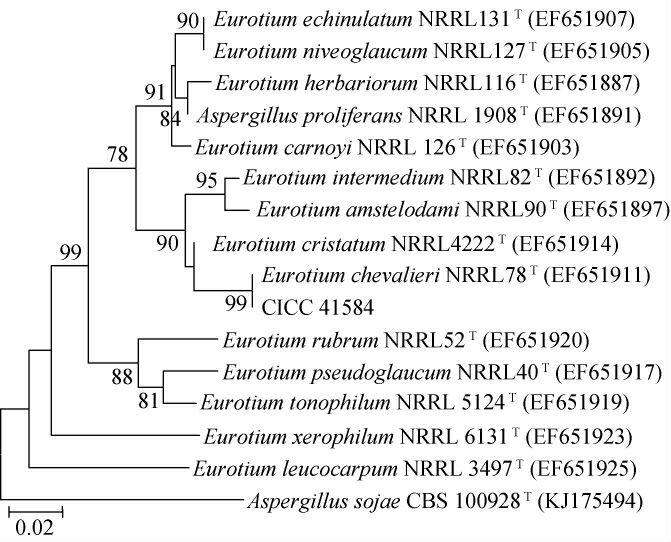
图2 基于β-tubulin基因菌株CICC 41584的系统发育树
Fig.2 Phylogenetic tree of strain CICC 41584 based onβ-tubulin gene
由图2可知,菌株CICC 41584与谢瓦散囊菌(Eurotium chevalieri)NRRL78 T处于同一系统发育支,序列的相似性为100%,结合形态学特征和生理生化试验结果,鉴定菌株CICC 41584为谢瓦散囊菌(Eurotium chevalieri),其无性型名称为谢瓦曲霉(Aspergillus chevalieri)。
2.2 单因素试验
2.2.1 碳源对菌丝干质量的影响
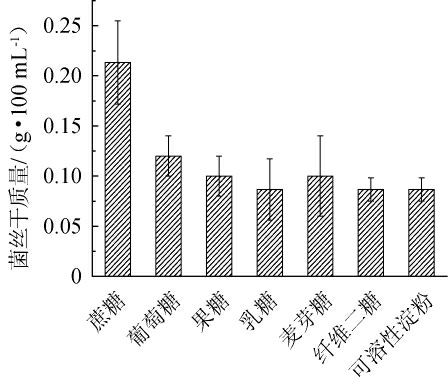
图3 不同碳源对菌丝干质量的影响
Fig.3 Effect of different carbon sources on dry mass of mycelium
不同碳源对菌丝干质量的影响结果见图3。由图3可知,菌株CICC 41584以蔗糖为碳源时,菌丝干质量最高,能达到0.21 g/100 mL。因此,选择蔗糖为后续试验的碳源。
2.2.2 氮源对菌丝干质量的影响
不同氮源对菌丝干质量的影响结果见图4。由图4可知,不同的氮源对菌丝产生量的影响较大,酵母浸粉作为氮源时菌丝干质量最高,能达到0.97 g/100 mL。因此,选择酵母浸粉为最佳氮源。
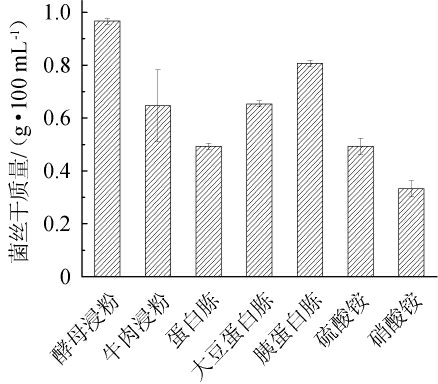
图4 不同氮源对菌丝干质量的影响
Fig.4 Effect of different nitrogen sources on dry mass of mycelium
2.2.3 无机盐对菌丝干质量的影响
不同无机盐对菌丝干质量影响结果见图5。由图5可知,不同无机盐对菌丝干质量影响较大,硫酸镁作为无机盐时菌丝干质量最高,能达到1.01 g/100 mL。因此,选择硫酸镁为最佳无机盐。
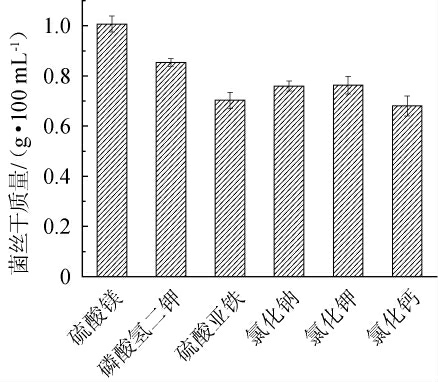
图5 不同无机盐对菌丝干质量的影响
Fig.5 Effect of different inorganic salts on dry mass of mycelium
2.3 Plackett-Burman试验结果
通过Design Expert10.0软件进行N=12的Plackett-Burman试验设计,每组试验设置3个平行,取平均值,结果见表4,方差分析结果见表5。
由表5可知,9个因素中的对响应值影响的显著顺序为酵母浸粉>发酵时间>硫酸镁>装液量>蔗糖>转速>接种量>温度>pH值,其中酵母浸粉的影响最为显著,硫酸镁、发酵时间有显著影响。另外,该试验模型的P=0.038 4<0.05,表明该模型是显著的。决定系数R2=0.991 3,表明这个方程能解释变量响应值的99.13%。调整决定系数R2Adj=0.952 4,表明该方程的拟合度较好。此外,还可以看出其中酵母浸粉、发酵时间对菌丝量的影响呈正效应,硫酸镁对菌丝量的影响呈负效应。
经分析获得的一次回归方程为:Y=0.66+0.028A+0.14B-0.073C-5.833E-003D+6.667E-003E+0.076F-0.078G-0.017H+1.000E-002I
表4 Plackett-Burman试验设计及结果
Table 4 Design and results of Plackett-Burman experiments
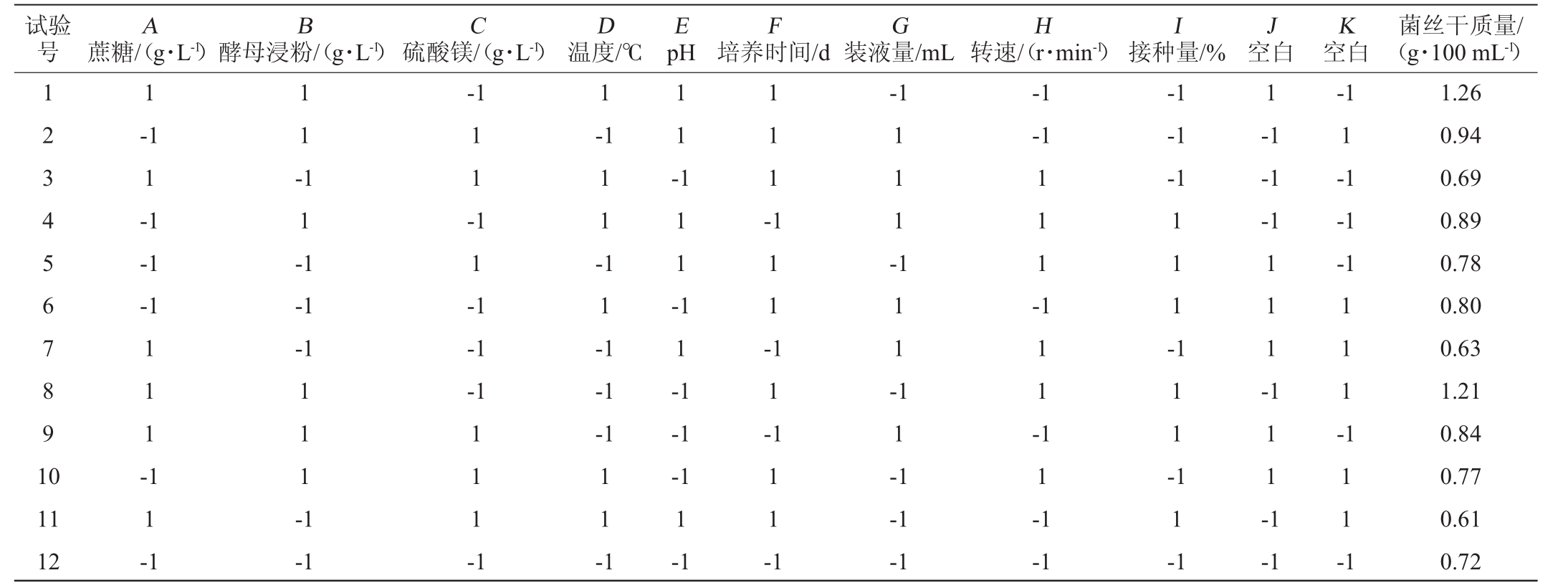
试验号A B C D E F G H I蔗糖/(g·L-1)酵母浸粉/(g·L-1)硫酸镁/(g·L-1)温度/℃pH 培养时间/d 装液量/mL 转速/(r·min-1)接种量/%1 2 3 4 5 6 7 8 9 1 0 1-11-1-1 1-1-1-1 1 1 --1-1-1 1 1 -1 1 1 -1 1 -1 1 -1 1 1 --1-1-1 1 1 1 -1 1 1 -1 1 -1 1 1 1 -1 1 1 --1-1-1-1 1 1 -1 1 1 1 -1 1 1 -1 1 -1 1 1 1 -1 1 -1 1 1 -1 1 -1 1 1 1 -1 1 -1 11 12 1 1 1 -1 1 1 -1-1-1-1 1 1 1 -1 1 1 -1-1-1 1-1 1 1 1 -1-1-1-1 1 1 -1 J空白1-1-1-1 1 1 1 -1 1 1 -1-1 K空白-1 1-1-1-1 1 1 1 -1 1 1 -1菌丝干质量/(g·100 mL-1)1.26 0.94 0.69 0.89 0.78 0.80 0.63 1.21 0.84 0.77 0.61 0.72
表5 Plackett-Burman试验结果方差分析
Table 5 Variance analysis of Plackett-Burman experiments results
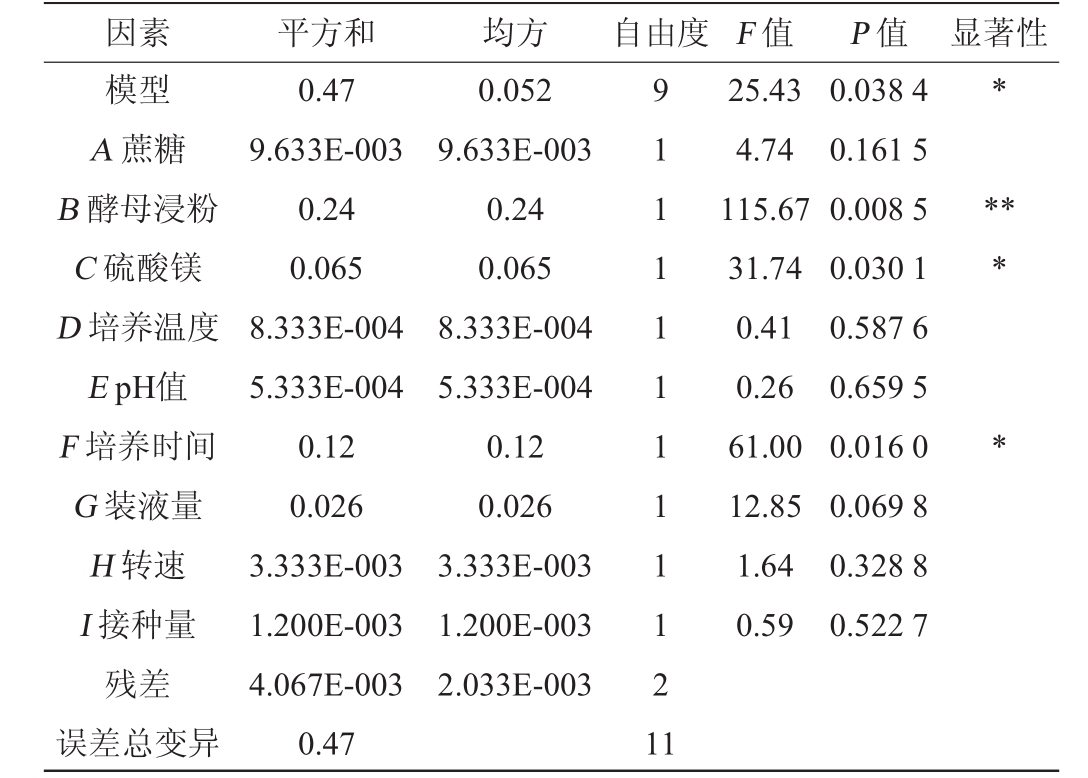
注:“*”表示差异显著(P<0.05);“**”表示差异极显著(P<0.01)。下同。
因素 平方和 均方 自由度 F值 P值 显著性模型A蔗糖B酵母浸粉C硫酸镁D培养温度E pH值F培养时间G装液量H转速I接种量残差误差总变异0.47 9.633E-003 0.24 0.065 8.333E-004 5.333E-004 0.12 0.026 3.333E-003 1.200E-003 4.067E-003 0.47 0.052 9.633E-003 0.24 0.065 8.333E-004 5.333E-004 0.12 0.026 3.333E-003 1.200E-003 2.033E-003 9 1 1 1 1 1 1 1 1 1 2 1 1 25.43 4.74 115.67 31.74 0.41 0.26 61.00 12.85 1.64 0.59 0.038 4 0.161 5 0.008 5 0.030 1 0.587 6 0.659 5 0.016 0 0.069 8 0.328 8 0.522 7*****
2.4 最陡爬坡试验
根据Plackett-Burman试验结果选取酵母浸粉、硫酸镁、发酵时间3个显著因素进行最陡爬坡试验。试验设计及结果见表6。由表6可知,随着酵母浸粉、硫酸镁以及发酵时间的变化,菌丝干质量呈现先上升后下降的趋势。当酵母浸粉25 g/L、硫酸镁2.5 g/L、发酵时间10 d时,菌丝干质量最大,能达到1.88 g/100 mL,因此选为中心点,进行Box-Behnken响应面设计。
表6 最陡爬坡试验设计及结果
Table 6 Design and results of the steepest ascent experiments
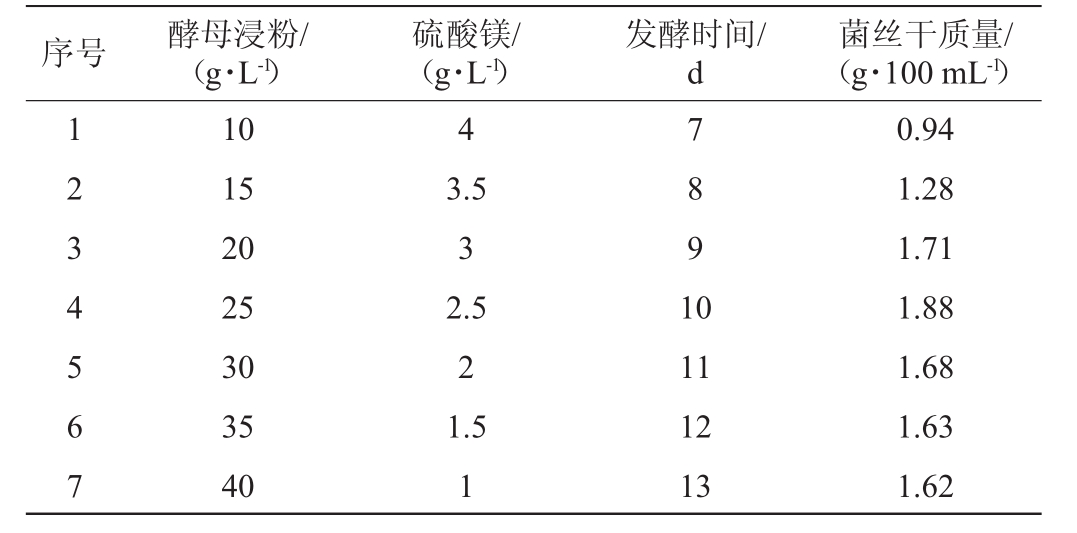
序号 酵母浸粉/(g·L-1)硫酸镁/(g·L-1)发酵时间/d菌丝干质量/(g·100 mL-1)1 2 3 4 5 6 7 10 15 20 25 30 35 40 4 3.5 3 2.5 2 1.5 1 7 8 9 1 0 11 12 13 0.94 1.28 1.71 1.88 1.68 1.63 1.62
2.5 Box-Behnken试验结果
采用Box-Behnken试验设计,利用Design Expert 10.0软件进行3因素3水平的响应面试验结果分析。以酵母浸粉(A)、硫酸镁(B)、发酵时间(C)为自变量,菌丝干质量(R)为响应值,试验结果见表7,方差分析见表8。
应用Design Expert 10.0软件对表7中的数据进行回归分析,得到的二次回归方程为:
由表7和表8可知,回归模型的决定系数R2=0.954 5,F值=16.63,P值=0.000 7<0.01,达到极显著水平,失拟项的F值=0.085 1>0.05,说明失拟项不显著,方程的拟合程度较好。另外,一次项A的P<0.01,说明酵母浸粉的影响极显著。交互项AC、BC的P<0.05,说明酵母浸粉和发酵时间及硫酸镁和发酵时间之间的交互作用显著。根据二次回归方程得到的响应面图如图6所示。
表7 Box-Behnken试验设计与结果
Table 7 Design and results of Box-Behnken experiments
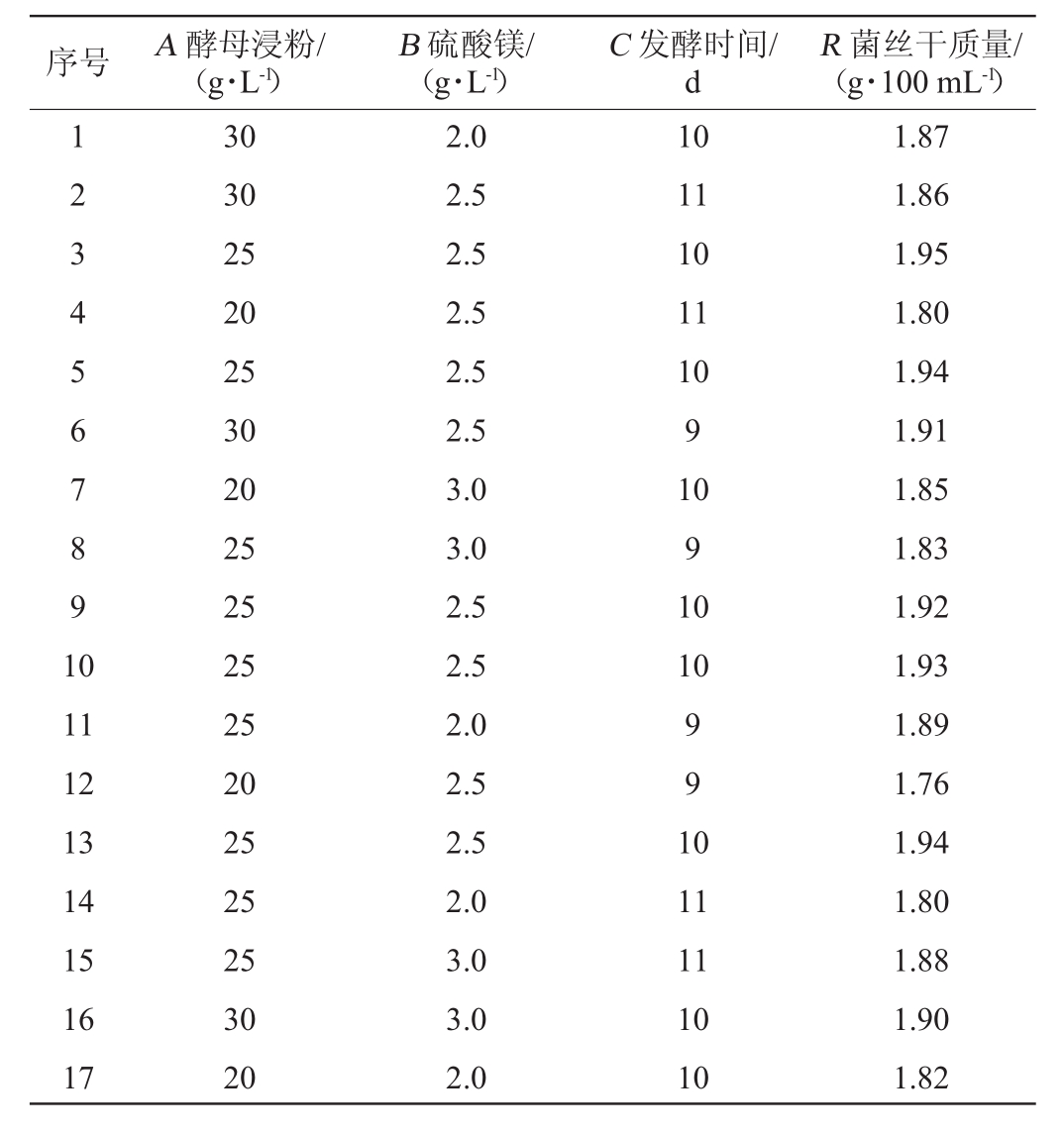
序号 A酵母浸粉/(g·L-1)B硫酸镁/(g·L-1)C发酵时间/d R菌丝干质量/(g·100 mL-1)1 2 3 4 5 6 7 8 9 1 0 10 11 10 11 10 9 10 9 10 10 11 12 13 14 15 16 17 30 30 25 20 25 30 20 25 25 25 25 20 25 25 25 30 20 2.0 2.5 2.5 2.5 2.5 2.5 3.0 3.0 2.5 2.5 2.0 2.5 2.5 2.0 3.0 3.0 2.0 9 9 1 0 11 11 10 10 1.87 1.86 1.95 1.80 1.94 1.91 1.85 1.83 1.92 1.93 1.89 1.76 1.94 1.80 1.88 1.90 1.82
表8 回归模型方差分析
Table 8 Variance analysis of regression model
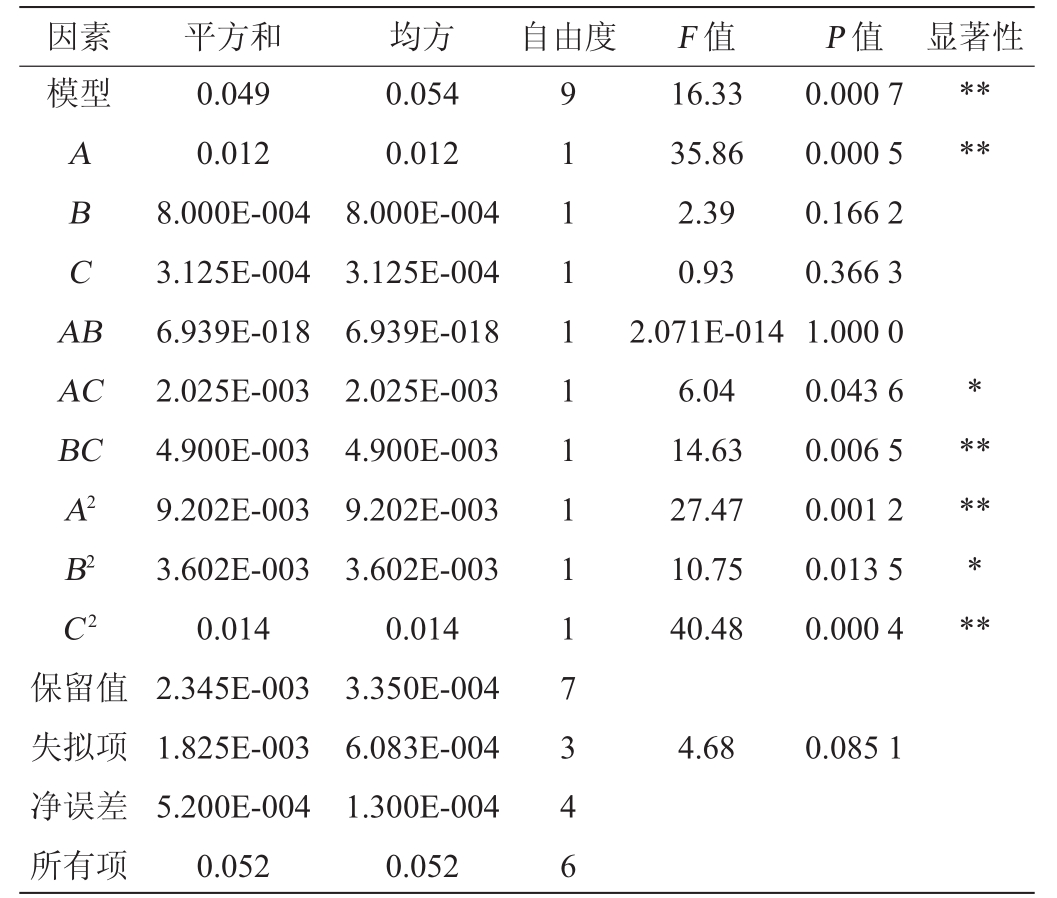
因素 平方和 均方 自由度 F值 P值 显著性模型A B C A B****AC BC A 2 B2 C 2保留值失拟项净误差所有项0.049 0.012 8.000E-004 3.125E-004 6.939E-018 2.025E-003 4.900E-003 9.202E-003 3.602E-003 0.014 2.345E-003 1.825E-003 5.200E-004 0.052 0.054 0.012 8.000E-004 3.125E-004 6.939E-018 2.025E-003 4.900E-003 9.202E-003 3.602E-003 0.014 3.350E-004 6.083E-004 1.300E-004 0.052 9 1 1 1 1 1 1 1 1 1 7 3 4 6 16.33 35.86 2.39 0.93 2.071E-014 6.04 14.63 27.47 10.75 40.48 0.000 7 0.000 5 0.166 2 0.366 3 1.000 0 0.043 6 0.006 5 0.001 2 0.013 5 0.000 4********4.680.085 1
由图6可知,硫酸镁与发酵时间对菌丝干质量的交互作用极显著(P<0.01),酵母浸粉与发酵时间对菌丝干质量的交互作用显著(P<0.05),酵母浸粉与硫酸镁对菌丝干质量的交互作用不显著(P>0.05)。
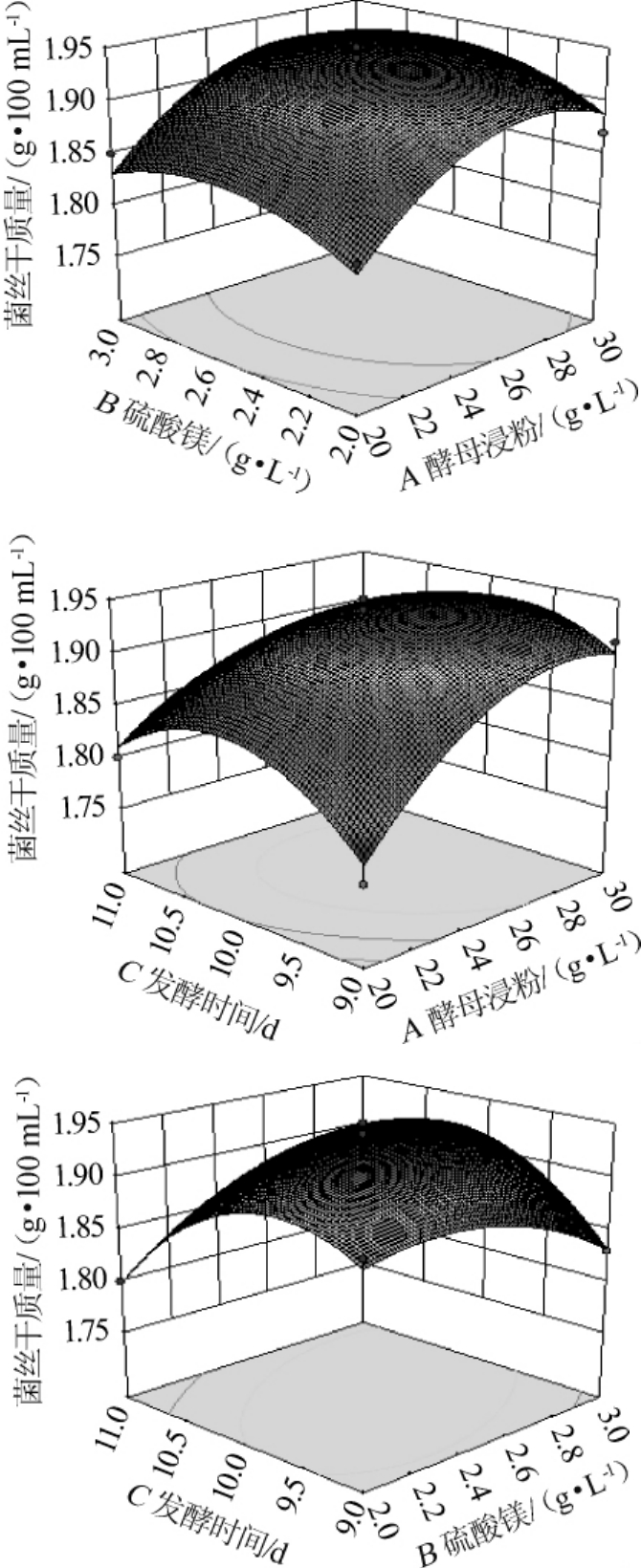
图6 酵母浸粉、硫酸镁、发酵时间交互作用对菌丝干质量影响的响应面及等高线
Fig.6 Response surface plots and contour line of effects of interaction between yeast powder,MgSO 4,fermentation time on dry mass of mycelium
根据上述模型,通过软件分析得到的最佳培养条件为酵母浸粉27.201 g/L、硫酸镁2.553 g/L、发酵时间10 d,预测得到的菌丝干质量为1.945 g/100 mL。为方便实际操作,修改培养条件为酵母浸粉27.2 g/L、硫酸镁2.6 g/L、发酵时间10 d,在最佳培养条件下进行3次平行试验,获得的菌丝干质量的平均值为1.950 g/100 mL,与理论预测值接近,说明该模型可行。
3 结论
本研究采用多相鉴定方法确定了分离自白酒大曲中菌株CICC 41584的分类学地位,并采用单因素试验及响应面法对其培养条件进行了优化。鉴定结果表明,该菌株为谢瓦散囊菌(Eurotium chevalieri)。采用单因素试验确定了最佳碳源、氮源、无机盐分别为蔗糖、酵母浸粉、硫酸镁;通过Plackett-Burman试验筛选出显著影响菌丝干质量的因素为酵母浸粉、硫酸镁和发酵时间,并通过Box-Behnken试验确定了最优培养条件为蔗糖添加量40 g/L、酵母浸粉添加量27.2 g/L、硫酸镁添加量为2.6 g/L、温度28℃、培养时间10 d、转速120 r/min、接种量2%、装液量50 mL/250 mL。在此优化培养条件下,菌丝干质量能达到1.950 g/100 mL,较优化之前提高了8.29倍,将为该菌株的进一步生物学功能研究、及其白酒大曲中的产业化应用奠定了基础。
[1]申孟林,王娟,蔡馨,等.白酒大曲微生物酶系研究进展[J].中国酿造,2018,37(4):7-11.
[2]廖昶,严伟,吴生文,等.不同尺寸大曲对特香型白酒质量和产量影响的研究[J].酿酒,2014,43(3):32-36.
[3]崔海灏,孟姣姣.大曲质量与原料粉碎度、水分的关系研究[J].酿酒,2016,43(2):86-88.
[4]董瑞丽,罗恵波,叶光斌.浓香型大曲中的嗜热真菌[J].中国酿造,2011,30(4):75-77.
[5]王晓丹,罗小叶,邱树毅.茅台大曲中一株嗜热放线菌的分离筛选及特性研究[J].中国酿造,2018,37(4):51-56.
[6]HAMASAKI T,NAGAYAMA K,HATSUDA Y.Structure of a new metabolite from Aspergillus chevalieri[J].J Agr Chem Soc Jpn,1976,40(1):203-205.
[7]KANOKMEDHAKUL K,KANOKMEDHAKUL S,SUWANNATRAI R,etal.Bioactive meroterpenoids and alkaloids from the fungus Eurotium chevalieri[J].Tetrahedron,2011,67(30):5461-5468.
[8]黄彦,石瑞,苏二正.冠突散囊菌的研究与应用进展[J].生物加工过程,2017,15(1):49-56.
[9]王冰,张凯,方热军.冠突散囊菌的营养作用研究进展[J].饲料博览,2012(12):26-28.
[10]班世栋,王晓丹,陈孟强,等.酱香型大曲中具产酶功能霉菌的分离筛选[J].酿酒,2014,41(4):31-36.
[11]徐佳,邱树毅,周鸿翔,等.酱香大曲中可培养的冠突散囊菌的初步研究[J].中国酿造,2016,35(6):55-59.
[12]黄晓宁,黄晶晶,李兆杰,等.浓香型和酱香型大曲微生物多样性分析[J].中国酿造,2016,35(9):33-37.
[13]朱文优,聂尧,徐岩.不同季节大曲生产过程中真菌群落结构的演变[J].食品与机械,2017,33(10):16-22.
[14]刘志祥,曾超珍.响应面法在发酵培养基优化中的应用[J].北方园艺,2009(2):127-129.
[15]孙思佳,翟磊,白飞荣,等.菌株CICC 33077的鉴定及培养基组分的响应面优化[J].中国酿造,2018,37(4):44-50.
[16]BEGANOVIC′J,KOS B,LEBOŠ P A,et al.Traditionally produced sauerkraut as source of autochthonous functional starter cultures[J].Microbiol Res,2014,169(7-8):623-632.
[17]白飞荣,姚粟,凌空,等.黄曲霉和米曲霉的多相鉴定方法[J].微生物学通报,2018,45(1):215-226.
[18]白飞荣,刘洋,李辉,等.香山黄栌枯萎病叶片真菌的分离与鉴定[J].生物学通报,2014,49(5):51-53.
[19]TAMURA K,DUDLEY J,NEIM,et al.MEGA4:molecular evolutionary genetics analysis(MEGA)software version 4.0[J].Mol Biol Evol,2007,24(8):1596.
[20]吴志军,王艳红,韩俊芬,等.Plackett-Burman试验评价Bacillus subtilis-1101产生物表面活性剂条件[J].黑龙江八一农垦大学学报,2012,24(3):38-40.
[21]XU C P,KIM S W,HWANG H J,et al.Application of statistically based experimental designs for the optimization of exo-polysaccharide production by Cordyceps militaris NG3[J].Biotechnol Appl Bioc,2011,36(2):127-131.
[22]MONTGOMERY D C.Design and analysis of experiments[J].Technometrics,1991,48(1):158.
[23]XIAO Z J,LIU P H,QIN J Y,et al.Statistical optimization of medium components for enhanced acetoin production from molasses and soybean meal hydrolysate[J].Appl Microbiol Biotechnol,2007,74(1):61-68.
[24]FERREIRA S L C,BRUNS R E,FERREIRA H S,et al.Box-Behnken design:An alternative for the optimization of analytical methods[J].Anal Chim Acta,2007,597(2):179-186.
[25]CHENG X,WANG Q,ZHANG S,et al.Determination of four kinds of carbamate pesticides by capillary zone electrophoresis with amperometric detection at a polyamide-modified carbon paste electrode[J].Talanta,2007,71(3):1083-1087.