氧气在酿酒过程中至关重要,在葡萄酒生产过程中使用适宜的氧可以提高葡萄酒的品质[1]。众所周知,温和的氧化可以改善红葡萄酒的颜色,由于氧气与花青素的反应,颜色更加稳定,与单宁反应而产生的涩味和苦味软化,然而氧气也会产生不良和不可预测的影响[2-3]。在这种情况下,需要研究氧气消耗对葡萄酒成分的不同影响,以及更好地了解葡萄酒氧化中SO2作用的机制。由于多种原因,如多酚含量较低,以及许多葡萄酒品种香气的氧敏感性质,葡萄酒抗氧化性和SO2的使用和其他抗氧化剂仍然存在一个重要问题。
许多学者认为SO2不直接与O2反应。当氧气溶解在葡萄酒中时,由铜和铁等金属催化的一系列氧化反应会氧化酚类化合物[4-5]。在此过程中,形成高活性物质如醌和过氧化氢,SO2是与两种中间体反应的关键组分。如果存在SO2,则与H2O2反应,将其还原成H2O并将其自身氧化成硫酸盐[6-7]。此外,SO2可以与醌反应,将其还原成儿茶酚或通过亲核反应生成儿茶酚磺酸盐。如果没有SO2,H2O2会引发芬顿(Fenton)反应,其中Fe2+在羟基自由基(·OH)中转化H2O2,羟基自由基是最活泼的氧自由基之一,能够从有机化合物中提取氢原子成为H2O[8-9]。这是乙醇氧化成乙醛的主要原因,乙醛如果积累,将赋予葡萄酒特有的氧化气味。这些反应是葡萄酒中影响酚类和芳香类化合物的重要途径。GABRIELE M等[10]通过研究多酚与氧气的氧化进程发现,其进程可以被SO2缓解,在微氧处理下的葡萄酒中SO2添加量越大,葡萄酒的微氧效应越缓慢,达到预期效果越久。
本实验通过研究在5次空气饱和循环过程中溶解氧的消耗规律、SO2的消耗规律、葡萄酒酚类物质的变化,以期建立SO2与O2消耗的偏最小二乘(partial least squares,PLS)回归模型,通过饱和循环中检测SO2与O2的变化快捷的分析葡萄酒中的酚类物质含量,深入了解与葡萄酒消耗O2直接或间接相关的不同过程,进而更便捷的分析葡萄酒质量。
1 材料与方法
1.1 材料与试剂
2019年赤霞珠干红葡萄酒(A1)、2020年赤霞珠干红葡萄酒(A2):新疆吐鲁番新葡王葡萄酒有限公司,橡木桶存放于公司地下酒窖。
模拟酒(A3、A4)(酒石酸5 g/L,pH3.2):挑选成熟度好的葡萄,破碎收集葡萄皮,提取色素,辅以色素浸提液、乙醛、单宁酸、Fe2+、Cu2+[11]。贮存于5 L不锈钢罐中。
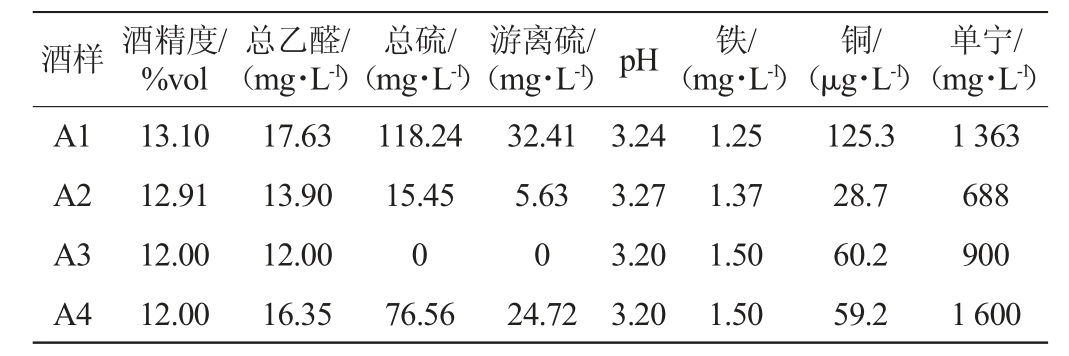
4种酒样的部分理化指标见表1。
表1 不同酒样的理化指标
Table 1 Physicochemical indexes of different wine samples
二氯甲烷、甲醇、己烷(均为色谱纯):北京迪科马科技有限公司;乙醚、丙酮(均为色谱纯):宝鸡市国康生物科技有限公司;甲酸、乙醇、乙腈、硫酸(均为色谱纯):上海诺泰化工有限公司。
1.2 仪器与设备
YRE-2000B旋转蒸发仪:巩义市予华仪器有限责任公司;AA-3300F原子吸收分光光度仪:上海元析仪器有限公司;TANK PRO微波消解仪:上海新仪微波化学科技有限公司;APUS PLUS高效液相色谱仪:成都珂睿科技有限公司;便携式溶解氧测定仪:上海梅特勒-托利多仪器有限公司;JA1003电子天平:上海精密仪器仪表有限公司;SDSCY10微型充氧仪:济南金君电子科技有限公司;722G可见分光光度计:上海仪电分析仪器有限公司。
1.3 方法
1.3.1 空气饱和葡萄酒制备
每个样品取500 mL,在1 L密闭烧瓶中轻轻摇动10 s,之后打开盖子让空气进入,并且摇动2次,然后将空气饱和的葡萄酒分配在螺旋盖的60 mL小瓶中,严格避免任何顶部空间。当葡萄酒消耗90%的初始氧气或7 d后,将剩余的葡萄酒从室中取出以进行新的饱和。按照前述方法进行操作,一共累计5次饱和。
1.3.2 空气饱和循环中葡萄酒溶解氧的测定
使用便携式溶解氧分析仪,每天至少监测两次所有小瓶溶解氧(dissolved oxygen,DO)含量。
1.3.3 单体酚含量的测定
单体酚含量的检测参考文献[12]的方法;洗脱程序参照韩国民等[13]的方法。
1.3.4 铜、铁离子含量的测定
葡萄酒中的铜、铁离子参考黄河柳[14]的方法。
1.3.5 总乙醛的测定
采用气相色谱法测定总乙醛[15],通过注射1 L用2-丁醇作为内标的葡萄酒样品。DB-WAX(30 m×0.53 mm×2 μm)毛细管柱,喷射器保持在250 ℃,分流比为1∶4。氢气(H2)用作载气,压力保持在27.5 kPa。升温程序为初始温度50 ℃、保持5 min,然后在10 min内升至220 ℃。火焰离子化检测器(flame ionization detector,FID)温度为250 ℃,补充气体的检测器气体流量为95 kPa,氢气为35 kPa,空气为60 kPa。分析一式两份进行。在含有已知量乙醛的模型酒(5 g/L酒石酸,12%乙醇,1.5%丙烷-1,2-二醇,10 g/L甘油,pH 3.2)中进行外部校准。
1.3.6 葡萄酒基础理化指标分析
SO2含量根据GB/T 15038—2006《葡萄酒、果酒通用分析方法》[16]规定的方法检测,酒精度、总酸、pH、挥发酸利用葡萄酒全自动分析检测仪进行检测。
1.3.7 数据处理和统计分析
使用Unscrambler 9.7进行偏最小二乘(PLS)回归。相关性研究在Excel 2013中进行,使用Origin 8.5进行作图。
2 结果与分析
2.1 空气饱和循环中葡萄酒溶解氧的变化情况
不同酒的耗氧情况见表2。
表2 空气饱和循环中葡萄酒溶解氧的变化
Table 2 Changes of dissolved oxygen in wine during air saturated cycle
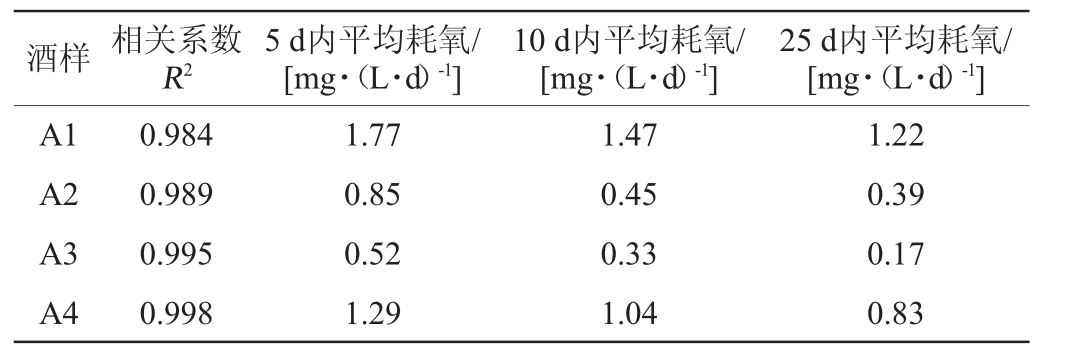
由表2可知,A1葡萄酒的初始耗氧量高于其他组,在25 d内耗氧率逐渐下降,其他组与A1耗氧情况相似,分析原因可能是单宁、SO2以及葡萄酒本身具有大量的耗氧物质,在第一次氧饱和阶段内参与氧化反应消耗了大量的氧,随着反应底物的减少,反应的速率逐渐下降。
以A2葡萄酒为例,消耗的氧气总量与时间的关系(图1)可知,氧气在饱和后的第一天内消耗得非常快,而在最后一次饱和中,溶解氧含量先快速下降再缓慢增加。分析原因是产生了芬顿反应,其中乙醇通过自由基作用机理氧化成乙醛。并且最后一次饱和中的游离SO2水平非常低,在这种情况下,当没有可用于清除H2O2的SO2发生反应时。羟基自由基将与O2反应,产生作为反应子产物的过氧化氢和氧气[17]。通过这一现象并应用线性回归分析,可以估算其耗氧率,即初始速率和平均速率。
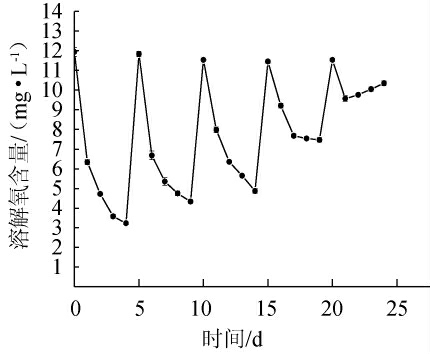
图1 空气饱和循环中A2葡萄酒溶解氧的变化
Fig.1 Changes of dissolved oxygen in wine A2 during air saturated cycle
2.2 空气饱和循环中葡萄酒总SO2的变化情况
葡萄酒在空气饱和循环中总SO2含量的变化见图2。由图2可知,SO2在几个饱和循环期间沿着线性趋势降低,图中每个处理组末端斜率较前面几次饱和变得陡峭,这意味着在最后的饱和中消耗更多的SO2,但A2的总SO2含量在10 d之后变化不明显。结合耗氧率分析,其中最后两次饱和中O2的消耗非常低,但SO2消耗量很大。这表明在所有葡萄酒中SO2以恒定的时间速率消耗,而O2在试验中以逐渐降低的速率消耗,这表明前期在饱和中氧化的一些化学物质在两周后被SO2还原回来。
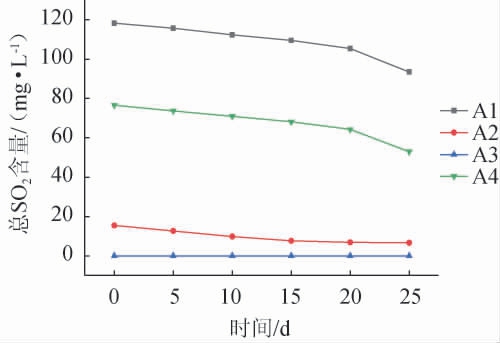
图2 每次空气饱和循环结束时总SO2含量的变化
Fig.2 Changes of total SO2 content at the end of each air saturation cycle
2.3 耗氧率对葡萄酒成分的影响
表3总结了在氧饱和循环时葡萄酒所进行的化学变化,以及它们与OCR的相关性。正相关系数属于在氧化过程中水平降低的物种,表明在较为快速消耗氧气的葡萄酒中消耗较大。这部分可能与目前用于表征葡萄酒中酚类聚合物部分的分析的局限性有关。由表3可知,具有高初始OCR的葡萄酒具有不同的氧化模式,其特征在于通过解聚释放的一些亚基而降低,例如表儿茶素和表儿茶素-3-O-没食子酸酯以及儿茶素。葡萄酒中酚类成分氧化引起的主要变化是酚酸含量的相关增加以及黄烷醇和黄酮醇含量的降低。苯甲酸含量平均增加5.2 mg/L和羟基肉桂酸增加3.713 mg/L,表明当SO2消耗量低时,这些物质会优先与氧发生反应。相反,在SO2<10 mg/L时,山奈酚的减少与O2负相关。初始OCR与表没食子儿茶素和铜显著正相关(P<0.05)。10 d的OCR与铜呈正相关。
表3 氧化期间氧、二氧化硫消耗与各参数的平均增量之间的相关系数
Table 3 Correlation coefficient between the average increment of each parameter and O2,SO2 consumption
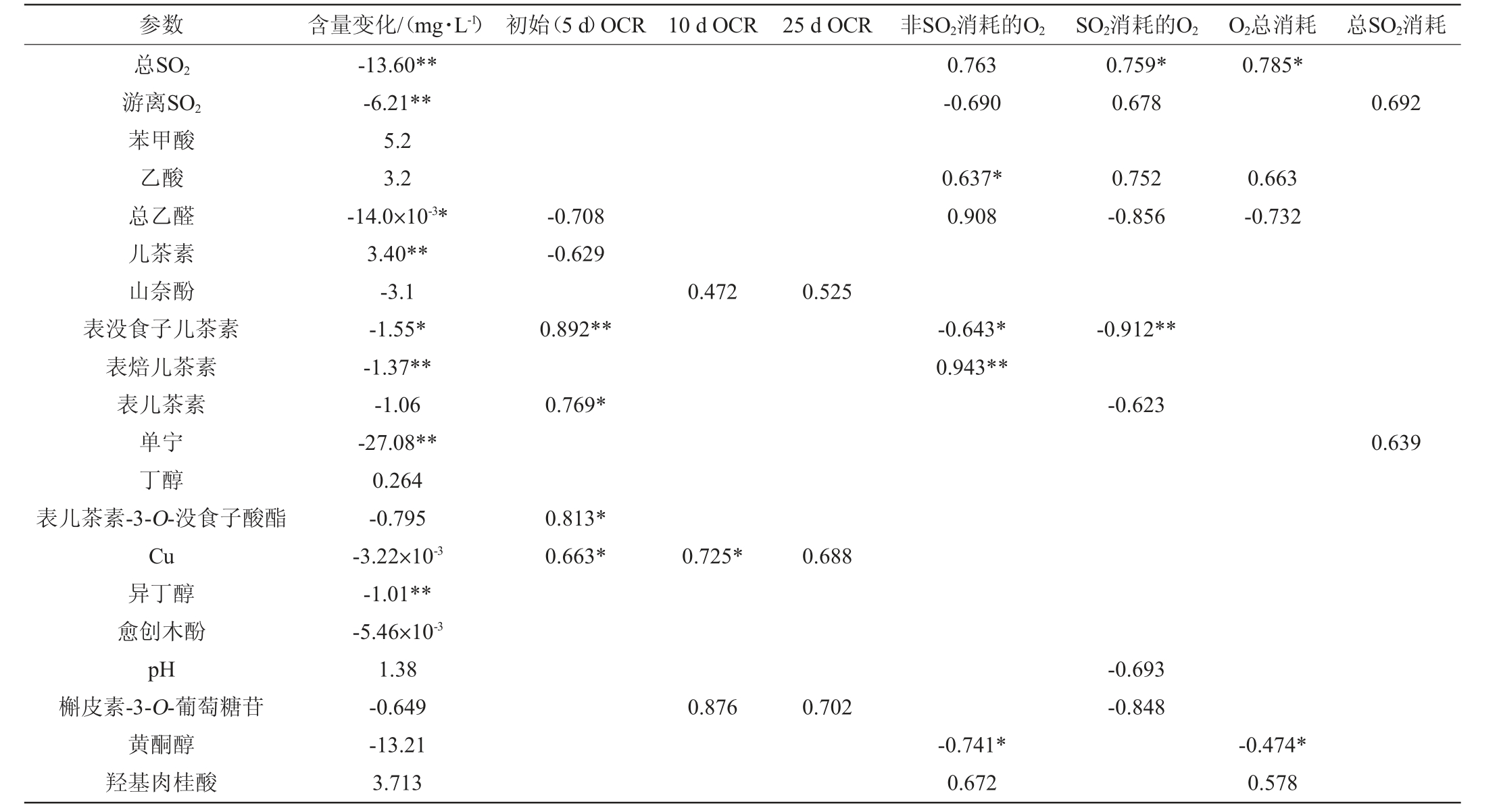
注:*:P<0.05;**:P<0.01。
2.4 葡萄酒溶解氧饱和循环中O2和SO2消耗相关的PLS模型建立
PLS模型解释了与葡萄酒的O2和SO2消耗相关的不同动力学参数,葡萄酒成分主要变化的函数。
建立具有预测能力的PLS模型,PLS模型解释了与葡萄酒的O2和SO2消耗相关的不同动力学参数,葡萄酒成分主要变化的函数,结果见表4。所有模型在结构上都非常相似,通过交叉验证解释了原始方差的89.7%~95.9%。
表4 O2和SO2消耗相关的偏最小二乘法回归模型
Table 4 Partial least squares regression model for O2 and SO2 consumption
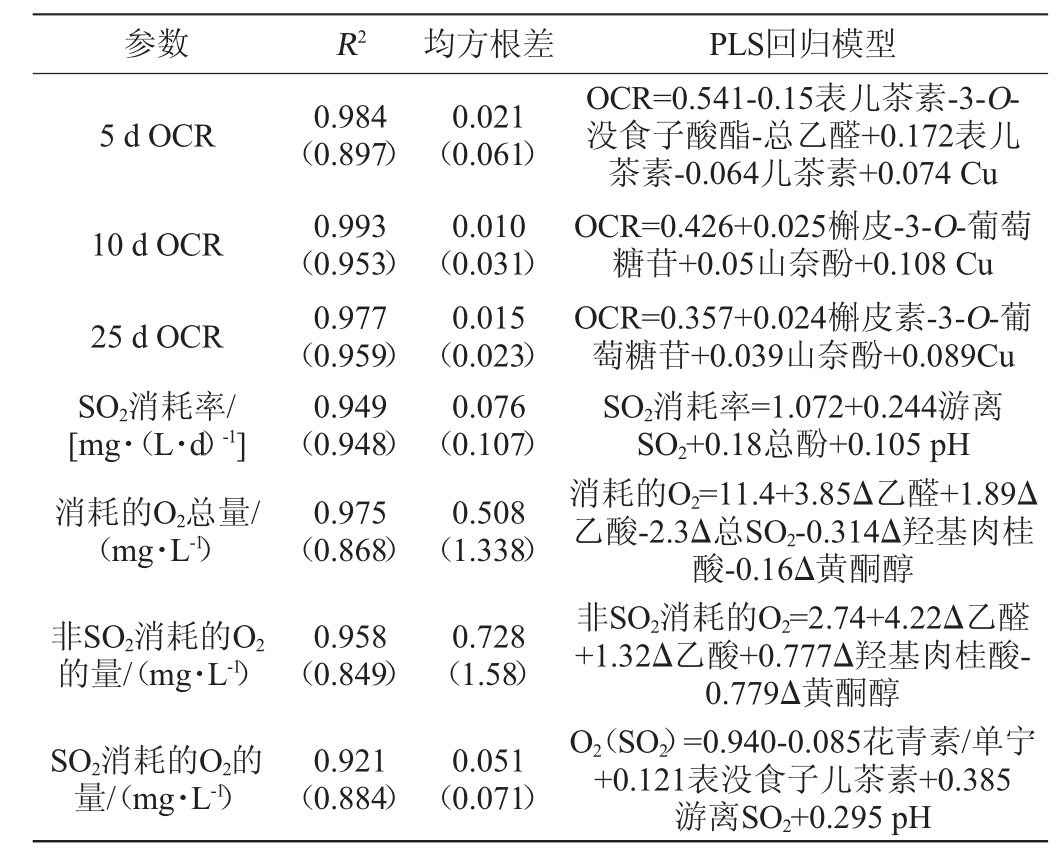
注:括号内的值是通过交叉验证获得的模型质量参数。
铜和黄酮醇以及羟基肉桂酸是决定初始OCR的关键化合物,初始OCR与葡萄酒初始含量的总乙醛、没食子酸以及单宁中儿茶素的含量呈负相关,较高R2说明在葡萄酒中这些化合物以较慢的速率消耗氧气。相反,葡萄酒中的表儿茶素-3-O-没食子酸酯和铜可以更快地消耗氧气。此模型与SANTOS M C等[19]所建立的模型非常相似,保持负相关的化合物是总乙醛,通过间苯三酚解离的黄烷醇单体(表儿茶素-3-O-没食子酸)以及单宁的一些衍生物组成亚基。
利用PLS建模将初始OCR与第二次饱和期间观察到的化学变化联系起来。该模型表明,具有高初始OCR的葡萄酒产生较少量的总乙醛,这可能是由于这些葡萄酒含有大量乙醛反应性多酚,因此乙醛将通过反应迅速除去。该模型还表明,含有表儿茶素-3-O-没食子酸酯的单宁在具有高初始OCR的葡萄酒中被消耗,而在具有低初始OCR的葡萄酒中略微产生。在低OCR的葡萄酒中,儿茶素、没食子酸和单宁在快速的降低,这表明它们可能是氧化中消耗的底物,可能是通过与SO2反应,并且这种消耗在低浓度的溶解氧下更强烈。可以从PLS模型中提取的最后一点是,红葡萄酒中的不同OCR涉及单宁解聚释放不同,在较低的OCR中,O2的缓慢消耗与儿茶素减少和表儿茶素-3-O-没食子酸酯的增加有关,但较高的OCR与表儿茶素-3-O-没食子酸酯的变化量显著性相关(P<0.01)。
2.5 SO2的消耗量及其与初始化学成分的关系
通过PLS建模进行评估(交叉验证为94%),该模型的最大系数是游离SO2,这意味着葡萄酒消耗SO2的第一个明显必要条件是游离形式。其中总SO2的含量对SO2消耗有影响。可能是与花青素形成络合物,而红葡萄酒中游离SO2的活性较小,并且还归因于它们通过促进结合SO2解离的缩合反应除去游离乙醛的较高能力。该模型还表明,葡萄酒在氧化过程中消耗SO2的能力与其pH,总酚含量呈正相关。
3 讨论
低浓度的SO2不再起任何还原作用,但氧气仍在快速的被消耗,这表明葡萄酒中仍有其他物质可以利用氧,结合A3初始耗氧率以及初始消耗SO2的由此可推测在并非所有的SO2都作用于溶解氧上,既存在非SO2消耗的氧,在前期的氧化过程中,葡萄酒里面的抗氧化的成分通过氧化还原消耗氧气,这一部分是在第一饱和期被其他亲核性物质消耗的[20]。
第一次饱和期间的低SO2消耗表明葡萄酒应含有能够与SO2竞争主要在O2吸收时形成的Fe(III),醌或氧化过程中产生的H2O2的其他成分[21]。这些成分将在第一次饱和时耗尽,这解释了为什么在第二次饱和时SO2的消耗增加。由表3可知,SO2消耗量与葡萄酒中游离或总SO2含量之间的相关性比较差,这表明可能还有以下两种影响SO2消耗量的因素:在消耗SO2之前存在能够与醌反应的亲核物质[22];在消耗SO2之前存在能够与Fe(III)或H2O2反应的抗氧化剂[23]。
基于表中所示的相关系数,表没食子儿茶素在第二次饱和过程中所涉及的反应性多酚,含有较高水平这些化合物的葡萄酒在氧化过程中将消耗较高水平的SO2[24]。相反,富含儿茶素的单宁属于第四类,因此,这些单宁中最丰富的葡萄酒在氧化过程中几乎不会消耗SO2。
乙醛所起的明显作用导致乙醛反应性多酚可能是决定O2消耗动力学的关键因素。不同的初始OCR还涉及能够进行解聚的单宁不同变化:低初始OCR与儿茶素的快速减少和表儿茶素-3-O-没食子酸酯的增加有关;较高的OCR与表儿茶素-3-O-没食子酸酯的降低以及儿茶素增加有关。
A1中葡萄酒黄烷-3-醇单体的含量高于表儿茶素。磺化黄烷醇的来源来自原花青素的裂解,通过裂解黄烷键和SO2对C4阳离子的破坏。由于陈酿葡萄酒中黄烷-3-醇磺酸盐的含量随着SO2含量的增加而增加,在陈酿过程中损失的SO2大部分被氧消耗。此外,由于具有较高SO2含量的葡萄酒单宁水平较低,这表明SO2在陈酿过程中改变了单宁特征,这一过程可能影响陈年酒的涩味感,单宁磺化可能导致老化红葡萄酒中涩味下降[25]。
4 结论
建立氧化过程中与消耗的O2总量、非SO2消耗的O2参数相联的葡萄酒成分的PLS模型。消耗的总O2模型表明,O2主要投入氧化SO2和生产乙醛和乙酸,这是葡萄酒的主要氧化产物。在没有伴随的SO2消耗O2的模型表明,除了氧化乙醇之外,O2还用于黄酮醇的降解和羟基肉桂酸的产生。
建立与初始OCR相关联的葡萄酒成分的PLS模型。根据该模型,初始OCR与总乙醛、没食子酸中的葡萄酒初始含量以及单宁中儿茶素的含量呈负相关,较高R2说明在葡萄酒中这些化合物的以较慢的速率消耗氧气。
建立了解释SO2消耗率的PLS模型。该模型通过交叉验证解释了92%的方差,主要变量是游离SO2和总酚含量。既葡萄酒中一般抗氧化剂与氧化底物。因此,该模型表明,虽然大多数葡萄酒多酚被氧化伴随着SO2的消耗,但具有清除活性的化合物可能与SO2竞争一些自由基。
通过检测饱和循环中SO2与O2的变化而建立相关模型,对预测以及分析葡萄酒中的酚类物质含量变化有显著的作用。
[1]李维新,苏昊,何志刚,等.南方山葡萄酒的氧化褐变动力学研究[J].中国食品学报,2020,20(1):190-195.
[2]ORTEGA C,LÓPEZ R,CACHO J,et al.Fast analysis of important wine volatile compounds development and validation of a new method based on gas chromatographic-flame ionisation detection analysis of dichloromethane microextracts[J].J Chromatogr A,2001,923(1-2):205-214.
[3]李华,康文怀,陶永胜,等.微氧处理对赤霞珠葡萄酒多酚及其品质的影响[J].江苏大学学报(自然科学版),2006(5):401-404.
[4]BEKKER M Z,SMITH M E,SMITH P A,et al.Formation of hydrogen sulfide in wine:interactions between copper and sulfur dioxide[J].Molecules,2016,21(9):1214.
[5]OBERHOLSTER A,ELMENDORF B L,LERNO L A,et al.Barrel maturation,oak alternatives and micro-oxygenation: Influence on red wine aging and quality[J].Food Chem,2015,173(6):1250-1258.
[6]MANOLE V,GHEORGHIT,Ǎ M,PAUN V P.Wine ageing chemistry.An economic fundamentation of wine storage period[J].Revista de Chimie,2006,57(8):902-904.
[7]荆红彭,刘明,陈晓明,等.二氧化硫对蓝莓酒发酵动力学及品质变化的影响[J].食品与发酵工业,2021,47(21):73-78.
[8]史红梅,王恒振,孙玉霞,等.高效液相色谱法测定葡萄皮、籽中的15种单体酚[J].食品工业科技,2016,37(11):318-322,337.
[9] GALUSKA S,MAKRIS D P,KEFALAS P.Browning development in wine-like liquid model matrices:dependence on phenolic,Fe(III)and SO2 concentrations[J].J Food Process Eng,2010,33(5):934-945.
[10]GABRIELE M,GERARDI C,JEANNETTE J,et al.Effects of low sulfur dioxide concentrations on bioactive compounds and antioxidant properties of Aglianico red wine[J].Food Chem,2018,245:1105-1112.
[11]ROUSSEY C,COLIN J,DU CROS R T,et al.In-situ monitoring of wine volume,barrel mass,ullage pressure and dissolved oxygen for a better understanding of wine-barrel-cellar interactions[J].J Food Eng,2021,291:110233.
[12]PETERSON A,CHOLET C,GENY L,et al.Identification and analysis of new α-and β-hydroxy ketones related to the formation of 3-methyl-2,4-nonanedione in musts and red wines[J].Food Chem,2020,305:125486.
[13]韩国民,陈锋,侯敏,等.葡萄酒中14种单体酚的高效液相色谱测定[J].食品科学,2011,32(2):180-183.
[14]黄河柳.微波辅助消解-原子吸收分光光度法测定催化剂中铜、铁、镍含量[J].广州化工,2003(1):44-47.
[15]王光冲.葡萄酒中生物胺、乙醛及矿质元素检测方法研究[D].保定:河北大学,2014.
[16]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 15038—2006葡萄酒、果酒通用分析方法[S].北京:中国标准出版社,2006.
[17]ZHANG Q A,SHEN Y,FAN X H,et al.Online monitoring of electrical conductivity of wine induced by ultrasound[J].CyTA-J Food,2016,14(3):496-501.
[18]王宏.宁夏干红葡萄酒陈酿过程中酚类物质及颜色的变化规律研究[D].银川:宁夏大学,2015.
[19]SANTOS M C,NUNES C,FERREIRA A S,et al.Comparison of high pressure treatment with conventional red wine aging processes: impact on phenolic composition[J].Food Res Int,2019,116:223-231.
[20] GUERRERO R F,CANTOS-VILLAR E.Demonstrating the efficiency of sulphur dioxide replacements in wine:A parameter review[J].Trends Food Sci Tech,2015,42(1):27-43.
[21]SACKS G L,HOWE P A,STANDING M,et al.Free,bound,and total sulfur dioxide(SO2)during oxidation of wines[J].Am J Enol Viticult,2020,71(4):266-277.
[22] GALUSKA S,MAKRIS D P.The effect of chlorogenic acid,catechin and SO2 on browning development in white wine model solutions[J].J I Brewing,2013,119(4):309-313.
[23]张文皓,张帅,李宗芮,等.葡萄酒中铜、铁含量检测的能力验证研究[J].食品安全质量检测学报,2016,7(4):1452-1455
[24]SAA P A,PÉREZ-CORREA J R,CELENTANO D,et al.Impact of carbon dioxide injection on oxygen dissolution rate during oxygen additions in a bubble column[J].Chem Eng J,2013,232:157-166.
[25]MA L J,WATRELOT A A,ADDISON B,et al.Condensed tannin reacts with SO2 during wine aging,yielding flavan-3-ol sulfonates[J].J Agr Food Chem,2018,66(35):9259-9268.