γ-氨基丁酸(γ-aminobutyricacid,GABA)是一种天然存在的四碳非蛋白质氨基酸,具有降血压[1]、促进睡眠[2]、保护肝脏[3]、改善肠道功能[4]、抗焦虑[5]、预防癫痫[6]等多种生理活性,广泛分布于自然界,在食品、医药及化工领域受到广泛的关注。
目前,GABA的生产方法主要包括化学合成法、植物提取法以及微生物发酵法[7]。其中,微生物发酵法因其发酵周期短、条件温和、提取工艺相对简单等突出优势,更适用于规模化工业生产,因而在GABA制备领域展现出广阔的应用前景[8]。迄今,文献报道的产GABA菌种已涵盖多种微生物类群,如大肠杆菌(Escherichia coli)[9]、短乳杆菌(Lactobacillus brevis)[10]、植物乳植杆菌(Lactiplantibacillus plantarum)[11]、发酵乳杆菌(Lactobacillus fermentum)[12]、戊糖片球菌(Pediococcus pentosaceus)[13]、酿酒酵母(Saccharomyces cerevisiae)[14]、紫色红曲霉(Monascus purpureus)[15]、马克斯克鲁维酵母(Kluyveromyces marxianus)[16]等。这些研究为从丰富多样的微生物资源中筛选高产GABA菌株提供了重要的理论基础和菌种参考。
酒的酿造本质上是一个复杂的微生物群落发酵过程。伴随消费升级,未来酿造酒的发展方向是风味与健康双导向[17],因此,深入挖掘并利用能够产生诸如GABA等活性功能成分的微生物菌株,并将其应用于酿造过程中,已成为提升酿造行业产品品质与健康附加值的关键策略之一。然而,目前针对酒的酿造体系进行高产GABA功能菌株筛选的研究相对匮乏。已有零星研究提供了初步探索,如曾林等[18]从四川泡菜中分离筛选出3株产GABA酵母菌,将其中一株应用于桑葚果汁发酵,经发酵条件优化后,在发酵144 h时GABA含量提升至1.15 g/L;李炫辰等[15]从酱香型白酒大曲中筛选出一株紫色红曲霉(M.purpureus),该菌株在高粱基质中发酵可产生0.57 g/kg的GABA。这些成果虽然具有启发性,但直接针对白酒酿造核心环节进行系统化菌种资源挖掘与性能优化的研究尚显不足。
本研究聚焦于白酒酿造过程产生的酒醅作为来源,创新性地采用培养组学技术策略和耐受性分析,高效分离筛选其中具有高产GABA能力的本土微生物。在此基础上,进一步通过培养条件优化,明确关键发酵参数,以期提高GABA产量,并将其应用于清香型白酒酿造中。本研究不仅有助于丰富酿造功能微生物菌种资源库,更将为通过微生物调控提升酒的健康内涵与整体品质提供重要的理论依据和技术支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
酒醅:劲牌有限公司酿造车间;糯高粱:黑龙江大庆;桂花曲、酒糟:劲牌有限公司制曲车间。
1.1.2 化学试剂
TIANGENR土壤基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:天根生化科技有限公司;DNA凝胶回收试剂盒:美国Axygen公司;Q5高保真DNA聚合酶(1 U/μL):美国New England公司;聚合酶链式反应(polymerase chain reaction,PCR)缓冲液、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphates,dNTPs)混合液、引物27F和1492R:宝日医生物技术(北京)有限公司;青霉素G钠(1 650 U/mg):上海阿拉丁生化科技股份有限公司;乙醛、甲醇、正丙醇、乙酸乙酯等标准品(均为色谱纯),葡萄糖、牛肉粉、蛋白胨、酵母粉、磷酸氢二钾、乙酸钠、柠檬酸二铵、硫酸镁、硫酸锰、L-谷氨酸钠、氯化钙(均为分析纯或生化试剂):中国医药集团有限公司。
1.1.3 培养基
MRS肉汤培养基:广东环凯生物科技有限公司。MRS固体培养基[19]:MRS肉汤培养基中添加琼脂20 g/L,121 ℃高压蒸汽灭菌30 min。
MRS改良培养基:在MRS肉汤培养基基础上再添加L-谷氨酸钠15 g/L,115 ℃高压蒸汽灭菌15 min。
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD)培养基[20]:酵母膏10 g/L,葡萄糖20 g/L,蛋白胨20 g/L,琼脂20 g/L,115 ℃高压蒸汽灭菌15 min。
YPD改良培养基:酵母膏10 g/L,葡萄糖20 g/L,蛋白胨20 g/L,15 g/L L-谷氨酸钠,115 ℃高压蒸汽灭菌15 min。
大米改良培养基[21]:取一定量籼稻米,浸泡3 h沥干后,添加15 g/kg L-谷氨酸钠,121 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
AL204电子分析天平:梅特勒-托利多仪器(上海)有限公司;JJ1000电子天平:常熟双杰测试仪器厂;QYC-200全温空气摇床:上海福玛实验设备有限公司;YXQ-LS-75S蒸汽灭菌锅、SPX-100B-Z生化培养箱:上海博讯实业有限公司;5424R艾本德小型离心机:艾本德(中国)仪器有限公司;BCM-1600A洁净工作台:苏州安泰空气技术有限公司;Nikon ECLIPSE E200显微镜:日本Nikon公司;E2695高效液相色谱-三重四级杆质谱(high performance liquid chromatography-triple quadrupole mass spectrometry,HPLC-MS/MS)仪:美国Waters公司;2720型PCR仪:美国赛默飞世尔科技公司;DYY-6C型电泳仪:北京六一仪器厂;BG-gdsAUTO(130)凝胶成像系统:北京百晶生物科技有限公司;WFJ 2000紫外可见分光光度计:尤尼柯(上海)仪器有限公司。
1.3 方法
1.3.1 高产GABA菌株的分离筛选
分离纯化[22]:取5 g GABA含量高的酒醅样品加入95 mL的无菌蒸馏水中,于20 ℃、150 r/min条件下富集培养30 min。取富集液按10倍梯度稀释至10-4,取200 μL稀释度为10-3和10-4的菌悬液分别涂布于MRS固体培养基和YPD培养基上,分别于37 ℃和30 ℃条件下培养3~5 d,挑取单菌落进行多次分离纯化。
筛选:将分离纯化后的细菌菌株单菌落接种于MRS液体培养基中,于37 ℃条件下静置培养24 h作为种子液;随后将种子液按2%(V/V)的接种量接种于MRS改良培养基,30 ℃条件下静置培养2 d,测定GABA含量。将分离纯化后的酵母菌株单菌落接种于YPD液体培养基,于30 ℃、140 r/min振荡条件下培养24 h作为种子液;将种子液按2%(V/V)的接种量接种于YPD改良培养基中,于30 ℃条件下培养3 d,测定GABA含量。将分离纯化后的红曲霉菌株单菌落接种于YPD固体培养基,30 ℃条件下培养5 d,用无菌水洗下孢子作为种子液,将种子液(1×106 CFU/L)按10%(V/W)的接种量接种于大米改良培养基,30 ℃条件下静置培养7 d,测定GABA含量。通过上述方法筛选高产GABA的菌株。
1.3.2 筛选菌株的鉴定
形态学观察:观察MRS固体培养基上菌株的菌落形态;用接种针挑取少量菌体放于载玻片中,使用革兰氏染色法进行染色后,于显微镜(10×100)下进行菌体显微观察。
分子生物学鉴定:收集菌体,采用TIANGEN 土壤基因组DNA提取试剂盒进行DNA提取,具体方法参照其说明书。以提取的基因组DNA为模板,采用16S rRNA通用引物27F(5'-AGAGTTTGATCCTGGCTCAG-3')和1492R(5'-GGTTACCTTGTTACGACTT-3')对筛选菌株的16S rRNA基因序列进行PCR扩增。PCR扩增体系:PremixTaqTM15 μL,引物27F(10 μmol/L)和1492R(10 μmol/L)各为0.5 μL,DNA模板1 μL,双蒸水(ddH2O)13 μL。PCR扩增条件:94 ℃预变性5 min;94 ℃变性30s,55 ℃退火50 s,72 ℃延伸30 s,共32个循环;72 ℃再延伸10 mim,4 ℃保存。PCR扩增产物经2%琼脂糖凝胶电泳检测合格后,委托广州华大基因科技股份有限公司进行测序。将测序结果提交至美国国立生物技术信息中心(National Center for Biotechnology Information,NCBI)的GenBank数据库中与已知序列进行基本局部比对搜索工具(basic local alignment search tool,BLAST)同源性搜索,选取同源性较高的模式菌株的16S rRNA基因序列,采用MEGA 11.0中的邻接(neighbor-joining,NJ)法构建系统发育树。
土壤基因组DNA提取试剂盒进行DNA提取,具体方法参照其说明书。以提取的基因组DNA为模板,采用16S rRNA通用引物27F(5'-AGAGTTTGATCCTGGCTCAG-3')和1492R(5'-GGTTACCTTGTTACGACTT-3')对筛选菌株的16S rRNA基因序列进行PCR扩增。PCR扩增体系:PremixTaqTM15 μL,引物27F(10 μmol/L)和1492R(10 μmol/L)各为0.5 μL,DNA模板1 μL,双蒸水(ddH2O)13 μL。PCR扩增条件:94 ℃预变性5 min;94 ℃变性30s,55 ℃退火50 s,72 ℃延伸30 s,共32个循环;72 ℃再延伸10 mim,4 ℃保存。PCR扩增产物经2%琼脂糖凝胶电泳检测合格后,委托广州华大基因科技股份有限公司进行测序。将测序结果提交至美国国立生物技术信息中心(National Center for Biotechnology Information,NCBI)的GenBank数据库中与已知序列进行基本局部比对搜索工具(basic local alignment search tool,BLAST)同源性搜索,选取同源性较高的模式菌株的16S rRNA基因序列,采用MEGA 11.0中的邻接(neighbor-joining,NJ)法构建系统发育树。
1.3.3 筛选菌株耐受性分析
温度耐受性:按2%(V/V)的接种量将筛选菌株种子液接种到MRS液体培养基中,分别置于30 ℃、37 ℃、42 ℃、47 ℃、52 ℃的恒温摇床中,160 r/min振荡培养24 h,采用紫外可见分光光度计于波长600 nm处测定培养液的吸光度值(OD600nm值)。
pH耐受性:按2%(V/V)的接种量将筛选菌株种子液分别接种至初始pH值为2.5、3、3.5、4.0、4.5的MRS液体培养基中,于37 ℃、160 r/min条件下培养24 h,采用紫外可见分光光度计于波长600 nm处测定培养液的吸光度值。
乙醇耐受性:按2%(V/V)的接种量将筛选菌株种子液分别接种于乙醇体积分数为0、3%、6%、9%、12%、15%、18%的MRS液体培养基中,于37 ℃、160 r/min条件下培养24 h,采用紫外可见分光光度计于波长600 nm处测定培养液的吸光度值。
1.3.4 筛选菌株产GABA发酵工艺的优化
发酵条件的优化:按2%(V/V)的接种量将筛选菌株种子液分别接种于MRS改良培养基中,发酵培养条件设置4个实验组,分别为实验组1:30 ℃静置培养;实验组2:30 ℃、140 r/min条件下培养;实验组3:37 ℃静置培养;实验组4:37 ℃、140 r/min条件下培养,培养过程中,每天连续取样至培养第4天,测定样品中GABA含量。
发酵培养基的优化:按2%(V/V)的接种量将筛选菌株种子液分别接种于MRS改良培养基中,采用单因素轮换法分别考察L-谷氨酸钠不同质量浓度(0、20 g/L、35 g/L、50g/L、65g/L、80g/L)、葡萄糖不同质量浓度(0、10g/L、20g/L、30 g/L、40 g/L、50 g/L)对筛选菌株产GABA的影响。
1.3.5 高产GABA优良菌株在清香型白酒生产中的应用
称取500 g高粱,加入60 ℃的温水(水面过粮面一指高),放入60 ℃烘箱中泡粮24 h。将泡好的粮食放入灭菌蒸锅中121 ℃初蒸10 min。初蒸完毕后,加入100 ℃水闷粮10 min,过滤完水之后再放入灭菌蒸锅115 ℃复蒸10 min。将复蒸好的粮食冷却至30 ℃后装至自封袋中,加入1%桂花曲,将混合好的粮曲放入30 ℃的培养箱中糖化24 h,糖化过程中将自封袋封口打开,并用湿毛巾封住开口,确保糖化过程中所需氧气和水分的供应。将糖化好的粮食与灭菌酒糟按照质量比1∶1进行混合,放入气体采样袋中,进行密封,并抽成真空,放入30 ℃的培养箱中发酵7 d。分别在糖化和发酵阶段添加不同比例(0、0.5‰、1.0‰、1.5‰、2.0‰)的X920发酵液(菌体浓度为1×109 CFU/L),发酵结束后,测定GABA含量。
1.3.6 GABA含量的测定
发酵液前处理:精密量取0.5 mL发酵液,加入25 mL 50%甲醇-水溶液,振摇10 min,以8 000 r/min条件下离心5 min,上清液以0.22 μm滤膜过滤,精密量取滤液1 mL,加入20 μL 10 mg/L的L-缬氨酸-d8内标使用液混匀,备用。
酒醅前处理:精密称取酒醅2.0 g,加入25 mL 50%甲醇-水溶液,振摇10 min,53 kHz超声10 min,以8 000 r/min离心5 min,上清液以0.22 μm滤膜过滤后稀释5倍,为酒醅稀释液。精密量取稀释液1 mL,加入20 μL 10 mg/L的L-缬氨酸-d8内标使用液混匀,备用。
色谱条件:进样体积5μL;XselectHSST3色谱柱(3.5μm,2.1 mm×100 mm),柱温40 ℃,采用0.01%甲酸水(A)与乙腈(B)作为流动相进行梯度洗脱,流速0.30 mL/min,梯度洗脱条件为0~1 min,95%A;1~3 min,70%A;3~8 min,20%A;8~15 min,95%A。
质谱条件:电喷雾离子源(electrospray ionization,ESI);雾化器温度400 ℃;离子源温度150 ℃;雾化气流速800 L/h;锥孔气体流速100 L/h;碰撞气流速0.17 mL/min。γ-氨基丁酸、L-缬氨酸-d8的质谱多反应监测采集条件见表1。
表1 质谱多反应监测采集条件
Table 1 Multiple reaction monitoring acquisition conditions for mass spectrometry
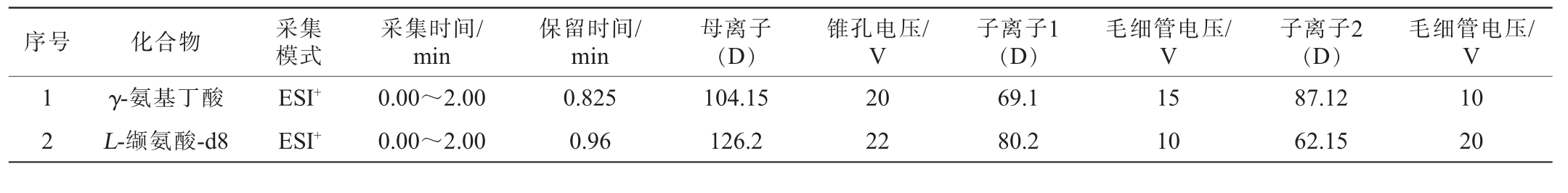
定性、定量方法:根据保留时间进行定性;采用内标法进行定量。
1.3.7 数据处理
每个试验重复3次,结果用“平均值±标准差”表示。采用Origin Pro2018分析软件对数据进行绘图分析。
2 结果与分析
2.1 高产GABA菌株的分离及筛选
从酒醅样品中共分离筛选得到产GABA的4株酵母菌(SY1~SY4)、5株红曲霉菌(SM1~SM5)以及3株乳酸菌(X920、X925、X952),其GABA产量见图1。
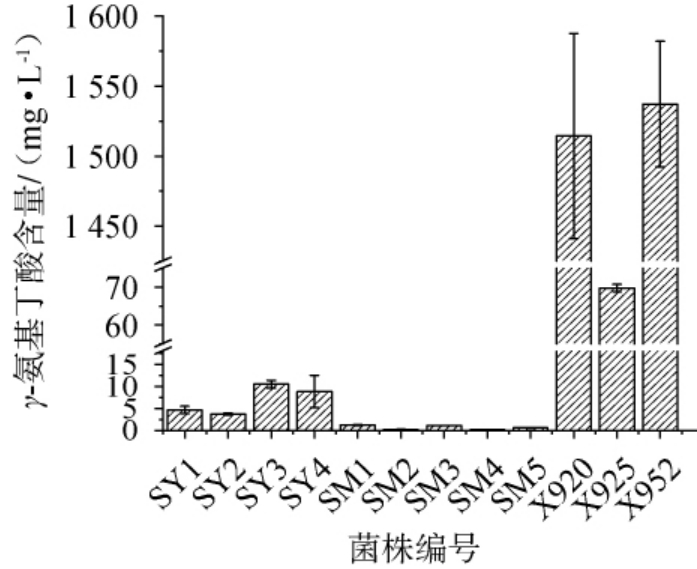
图1 不同分离菌株产γ-氨基丁酸能力分析
Fig.1 Analysis of γ-aminobutyric acid production ability of different isolated strains
由图1可知,各菌株的GABA产量呈现明显差异。4株酵母菌(SY1~SY4)在改良PDA培养基中的GABA产量分别为4.64 mg/L、3.74 mg/L、10.53 mg/L和8.84 mg/L;5株红曲霉菌(SM1~SM5)的产量相对较低,在0.12~1.24 mg/L之间;3株乳酸菌(X920、X925、X952)表现出优异的GABA合成能力,GABA产量分别为1 514.45 mg/L、69.77 mg/L和1 537.26 mg/L,结果表明,细菌产GABA的能力远高于酵母和红曲霉,与参考文献[23-25]报道一致。基于此,筛选出细菌X920和X952为高产GABA的菌株。
2.2 高产GABA菌株的鉴定
2.2.1 形态学观察
菌株X920和X952在MRS固体培养基上的菌落及细胞形态特征见图2。
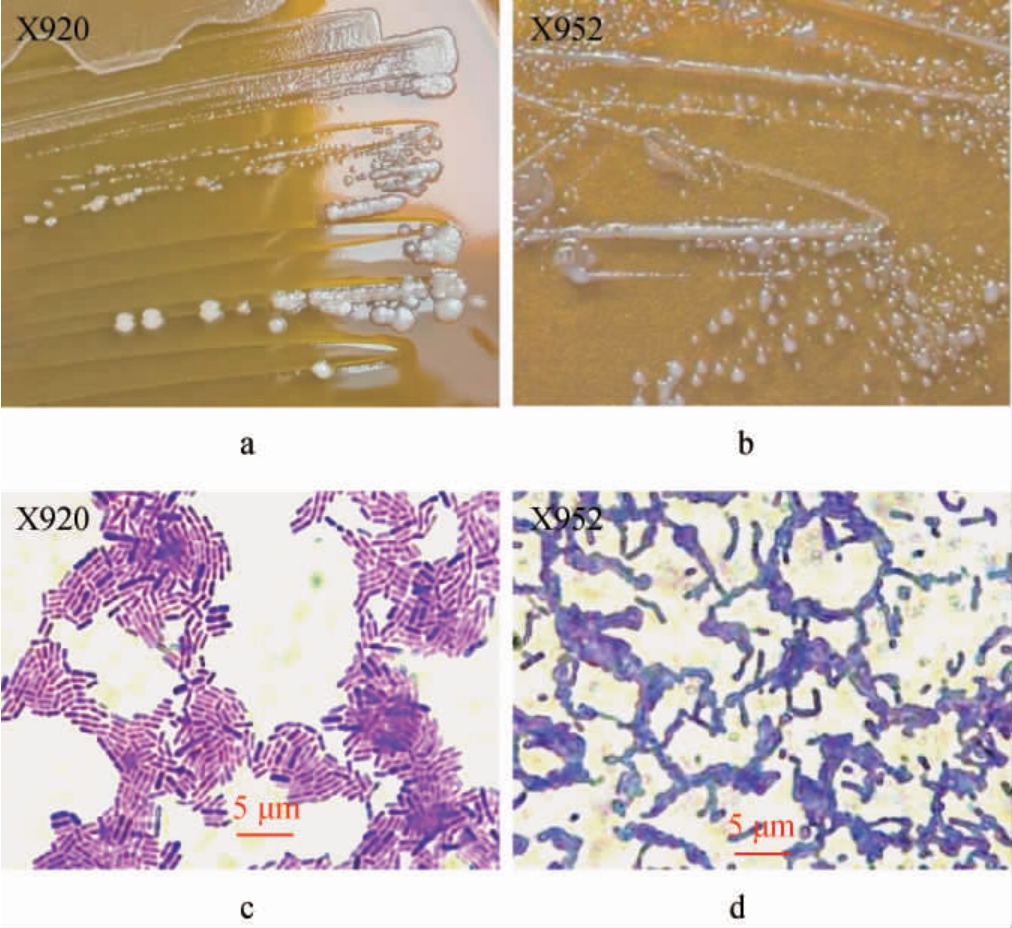
图2 菌株X920和X952的菌落(a、b)及细胞(c、d)形态
Fig.2 Colonies (a,b) and cells (c,d) morphology of strains X920 and X952
由图2可知,两株菌株均呈现典型的杆状形态,菌株X920的菌体长度为1.5~4μm,宽度为0.5~1.0μm,无荚膜,无芽孢,为革兰氏阳性菌;菌落呈白色、不透明,表面光滑,菌落边缘扩散,呈花瓣状。菌株X952菌体长度为2~6 μm,宽度为0.5~1.0 μm,无荚膜,无芽孢,为革兰氏阳性菌;菌落呈白色、不透明,表面光滑,边缘形态规则,呈典型的圆形轮廓。
2.2.2 分子生物学鉴定
基于16S rRNA基因序列构建菌株X920和X952的系统发育树,结果见图3。
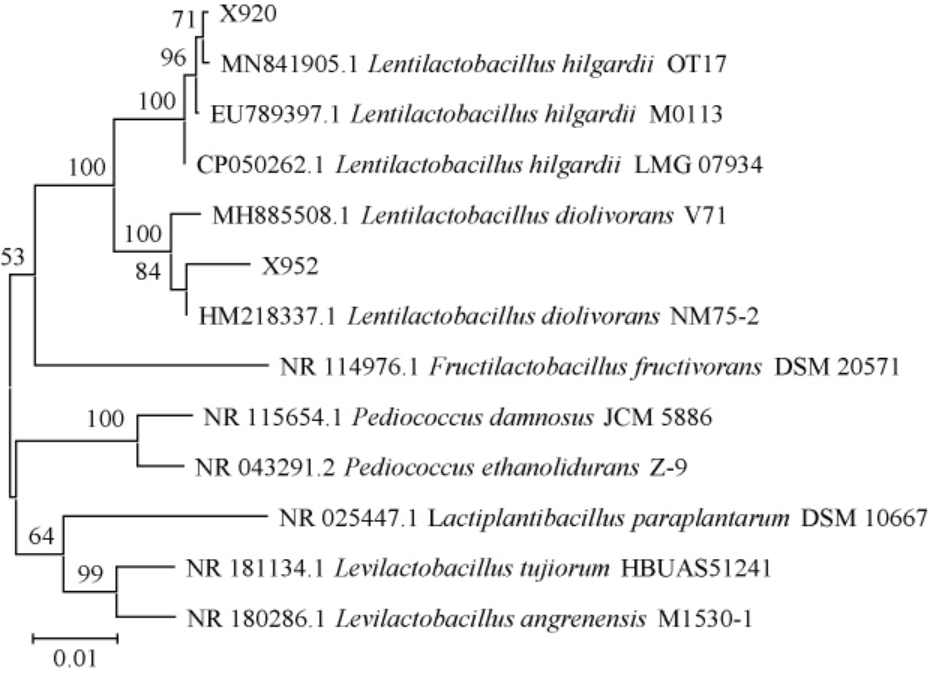
图3 基于16S rDNA基因序列菌株X920与X952的系统发育树
Fig.3 Phylogenetic tree of strains X920 and X952 based on 16S rDNA gene sequences
由图3可知,菌株X920和X952分别与希氏乳杆菌(Lentilactobacillus hilgardii)EU789397.1和食糖扁豆乳杆菌(Lentilactobacillus diolivorans)MN841905.1聚于一个分支,序列相似性均达99.7%。结合形态学特征,最终鉴定菌株X920和X952分别为希氏乳杆菌(Lentilactobacillus hilgardii)、食糖扁豆乳杆菌(Lentilactobacillus diolivorans)。
2.3 高产GABA菌株的耐受性分析
鉴于菌株X920和X952具有较好的GABA合成能力,为评估其在酿酒实际生产中的应用潜力,进一步考察这两株菌对酿造关键环境因素的耐受性,结果见图4。
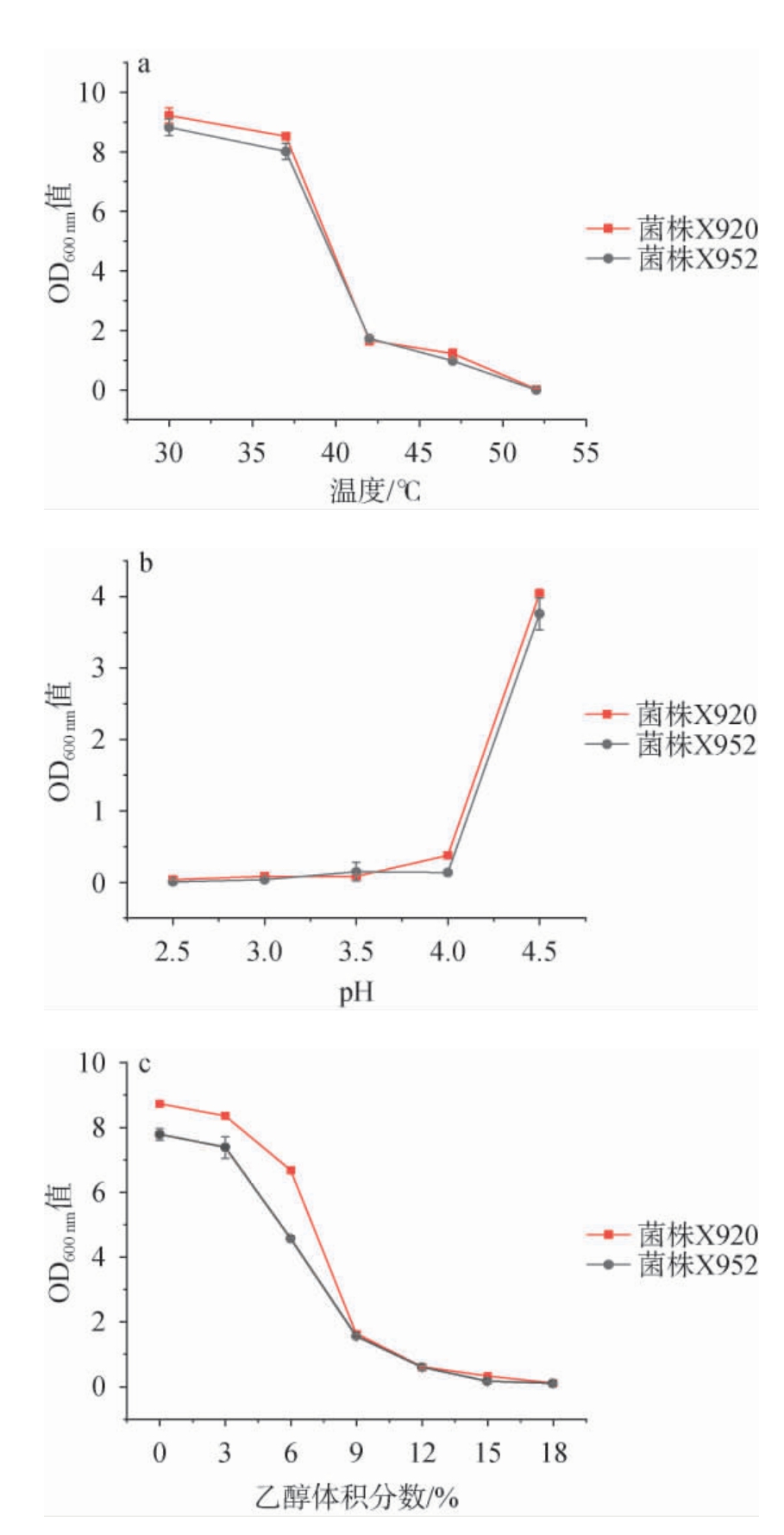
图4 菌株X920和X952对温度(a)、pH(b)及乙醇(c)的耐受性分析
Fig.4 Tolerance analysis of strains X920 and X952 to temperature (a),pH (b),and ethanol(c)
由图4可知,两株菌株均表现出良好的酿造环境适应性。在温度耐受性方面,菌株X920和X952的最适生长温度范围为30~37 ℃,其中菌株X920表现出更优的生长性能,当培养温度>37 ℃之后,两株菌的生长均受到严重抑制,且当培养温度为52 ℃时,两株菌株的生长完全受到抑制。pH耐受性分析显示,当pH为4.5时,两株菌株均能正常生长,且菌株X920表现出更优的生长性能,但当pH<4.5时,两菌株的生长均受到严重抑制,菌株X920和X952分别在pH 3.5和4.0时生长完全受到抑制。在乙醇耐受性方面,两株菌株在乙醇体积分数0%~9%范围内均能良好生长,且菌株X920的生长优势明显。当乙醇体积分数提升至15%时,两株菌株的生长均完全受到抑制。综上,菌株X920和X952均能适应典型的酿酒环境条件,其中菌株X920展现出更优的环境适应性,具有更大的工业化应用潜力,因此,选择希氏乳杆菌X920为高产GABA的优良菌株。
2.4 希氏乳杆菌X920产GABA发酵工艺优化
2.4.1 发酵条件优化
不同发酵条件对希氏乳杆菌X920产GABA的影响见图5。
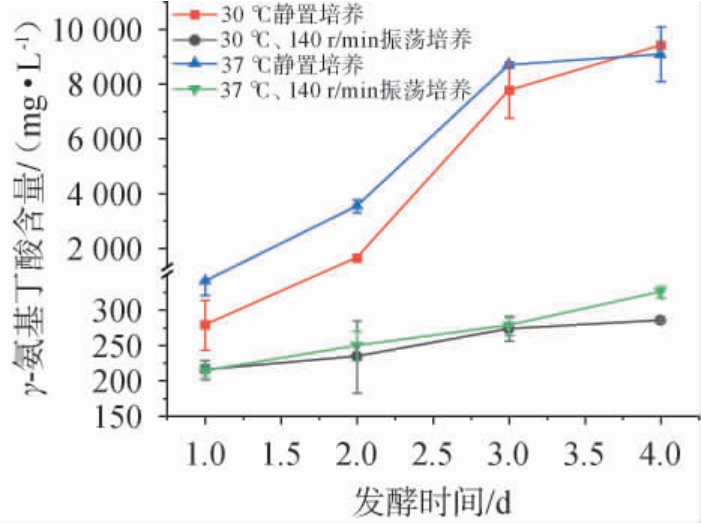
图5 不同发酵条件对希氏乳杆菌X920产γ-氨基丁酸的影响
Fig.5 Effect of different fermentation conditions on γ-aminobutyric acid production by Lentilactobacillus hilgardii X920
由图5可知,GABA含量随发酵时间的增加随之增加,呈现典型的阶段性特征,发酵前3天GABA含量大幅增加,第4天含量增加幅度降低,基于生产效率与成本的综合考量,确定最佳发酵周期为3d,与参考文献[26]报道一致。静置培养状态下GABA含量大幅高于振荡培养状态,结果证实GABA合成主要依赖无氧发酵途径。在37 ℃静置条件下GABA含量略高于30 ℃静置条件,表明适度升温有利于GABA生物合成。当37 ℃静置培养3 d时,GABA含量为8 700.47 mg/L。因此,确定最佳发酵条件为37 ℃静置培养。
2.4.2 发酵培养基优化
L-谷氨酸钠为GABA生物合成的直接前体物质[26],葡萄糖能促进菌株产GABA[27],因此,考察L-谷氨酸钠及葡萄糖添加量对希氏乳杆菌X920产GABA的影响,结果见图6。
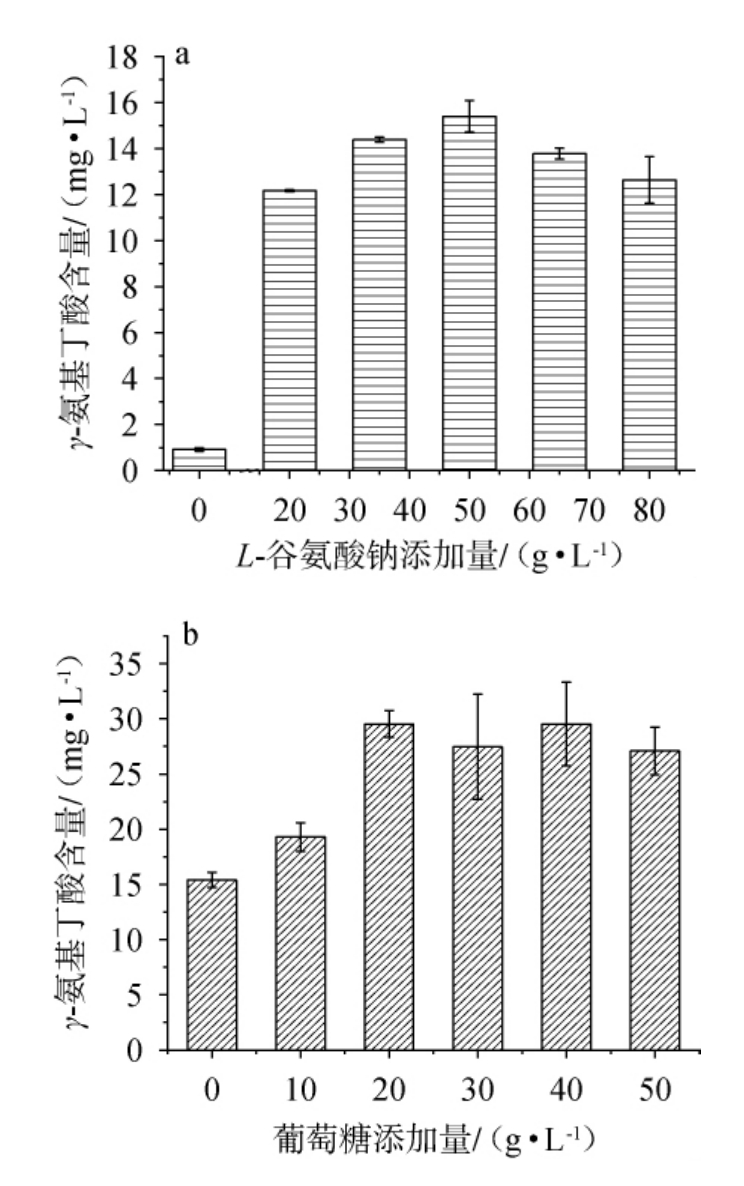
图6 L-谷氨酸钠(a)及葡萄糖(b)添加量对希氏乳杆菌X920产γ-氨基丁酸的影响
Fig.6 Effect of monosodium glutamate (a) and glucose (b) addition on γ-aminobutyric acid production by Lentilactobacillus hilgardii X920
由图6a可知,相较于不添加L-谷氨酸钠,添加L-谷氨酸钠明显提高GABA含量,且随着L-谷氨酸钠质量浓度的升高,GABA含量呈先升高后下降的趋势,当L-谷氨酸钠含量为50 g/L时,GABA含量达到最高为15.4 g/L。因此,确定最佳L-谷氨酸钠添加量为50 g/L。由图6b可知,添加葡萄糖能明显提高GABA含量,且随着葡萄糖质量浓度的升高,GABA含量整体呈先升高后下降的趋势,当葡萄糖质量浓度为20 g/L时,GABA含量最高,为29.54 g/L,较初始条件(1 514.45 mg/L)提升19.5倍。因此,确定最优葡萄糖添加量为20 g/L。
2.5 希氏乳杆菌X920在清香型白酒生产中的应用
将希氏乳杆菌X920应用于清香型白酒小试酿造试验,测定酒醅中的GABA含量,结果见图7。
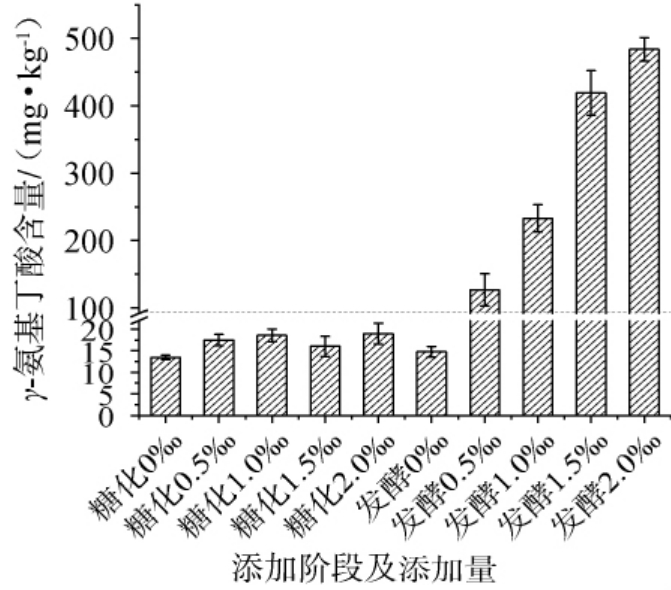
图7 不同阶段添加希氏乳杆菌X920发酵液对酒醅中γ-氨基丁酸含量的影响
Fig.7 Effect of adding X920 fermentation liquid at different stages on the γ-aminobutyric acid content in fermented grains
由图7可知,发酵阶段添加希氏乳杆菌X920发酵液对酒醅GABA含量的提升效果明显优于糖化阶段。在发酵阶段添加时,GABA产量与希氏乳杆菌X920发酵液添加量呈正相关,在不影响发酵的水分含量情况下,添加量达到2‰时,酒醅GABA含量达到最高,为483.82 mg/kg,是对照组(14.76 mg/kg)的32倍。这一现象可能源于以下机制:功能菌液本身含有高质量浓度GABA;添加的活菌在酒醅中持续代谢产生GABA;菌株代谢活动促进原料中谷氨酸向GABA的转化。该结果证实了发酵阶段添加功能菌液是实现酒醅GABA富集的最有效策略。
3 结论
本研究从传统酿造酒醅样品中成功分离筛选出两株具有高产γ-氨基丁酸能力的细菌。结合形态学观察及分子生物学鉴定,确定菌株X920为希氏乳杆菌(Lentilactobacillus hilgardii),菌株X952为食糖扁豆乳杆菌(Lentilactobacillus diolivorans)。进一步的环境适应性研究表明,菌株X920在模拟酿酒环境的胁迫条件下展现出显著优势,可耐受温度47 ℃、pH 4.0、乙醇体积分数12%的环境条件。通过系统的发酵条件优化试验,确定菌株X920高效合成GABA的最佳工艺参数:以添加50 g/L L-谷氨酸钠、20 g/L葡萄糖的MRS液体培养基为发酵基质,于37 ℃静置培养3 d,在此条件下,GABA含量达到29.53 g/L,较优化前提升了19.5倍。为验证其实际应用价值,进一步将菌株X920应用于清香型白酒小试规模酿造试验,结果显示,在发酵阶段添加2‰优化菌株X920发酵液(菌体浓度为1×109 CFU/L)的处理组,其酒醅中GABA含量最高,达到483.82 mg/kg,为对照组(14.76 mg/kg)的32倍。本研究创新性地建立了一套从菌株筛选、鉴定到发酵工艺优化的完整技术体系,所获得的工艺参数为传统酿造食品中GABA的定向富集提供了可靠的技术方案,对开发功能性酿造食品具有重要的产业化应用价值。
[1] 张瑞姣,杨鹏,宫安东,等.微生物发酵生产γ-氨基丁酸的研究进展[J].信阳师范学院学报,2023,36(1):162-172.
[2] 王淑豪,赵京涛,王彬.γ-氨基丁酸的生物学功能[J].廊坊师范学院学报,2023,23(3):32-36,53.
[3] WANG S L,XIANG Y Y,ZHU J C,et al.Protective roles of hepatic GABA signaling in acute liver injury of rats[J].Am J Physiol Gastrointest Liver Physiol,2017,312(3):G208-G218.
[4] 吕旦,陈冰,曹俊明,等.γ-氨基丁酸的生物学功能及其在动物生产中的应用[J].动物营养学报,2024,36(11):6903-6916.
[5] 李瑶,王雷,孙鑫,等.γ-氨基丁酸生物学功能研究进展[J].农业与技术,2024,44(10):12-14.
[6]李海峰,李冰冰,石硕硕,等.γ-氨基丁酸在食品中的应用研究进展[J].河南工业大学学报,2023,44(1):117-125.
[7] WU M,DING J J,ZHANG Z F,et al.Kinetic modeling of gamma-aminobutyric acid production by Lactobacillus brevis based on pH-dependent model and rolling correction[J].Chin J Chem Eng,2022,50:352-360.
[8] 蒋艾廷,李宝坤,金丹,等.PB试验优化德氏乳杆菌增殖培养基的研究[J].中国酿造,2017,36(7):32-36.
[9] YU P,REN Q,WANG X X,et al.Enhanced biosynthesis of γ-aminobutyric acid(GABA)in Escherichia coli by pathway engineering[J]. Biochem Eng J,2019,141:252-258.
[10] LIM H S,CHA I T,ROH S W,et al.Enhanced production of γ-aminobutyric acid by optimizing culture conditions of Lactobacillus brevis HYEl isolated from kimchi,a Korean fermented food[J].J Microbiol Biotechnol,2017,27(3):450-459.
[11] 曾林,谭霄,张庆,等.四川泡菜中产γ-氨基丁酸植物乳杆菌BC114发酵条件优化[J].食品与发酵工业,2017,43(3):116-122.
[12] LIN Q,LI D N,QIN H Z.Molecular coning,expression,immobilization of glutamate decarboxylase from and Lactobacillus fermentum YS2[J].Electron J Biotechnol,2017,27:8-13.
[13] 周燕,杨慧群,崔晓睿,等.一株产γ-氨基丁酸的戊糖片球菌分离鉴定及药敏分析[J].中国微生态学杂志,2023,35(4):410-413.
[14] ZHANG Q,SUN Q,TAN X,et al.Characterization of γ-aminobutyric acid (GABA)-producing Saccharomyces cerevisiae and coculture with Lactobacillus plantarum for mulberry beverage brewing[J].J Biosci Bioeng,2020,129(4):447-453.
[15] 李炫辰,杨欣,程迈,等.红曲霉菌株的分离鉴定及其对酱香型白酒副产物窖底水的降解处理[J].中国酿造,2025,44(5):104-112.
[16] PERPETUINI G,TITTARELLI F,BATTISTELLI N,et al.γ-aminobutyric acid production by Kluyveromyces marzianus strains[J]. J Appl Microbiol,2020,129(6):1609-1619.
[17] 李锐,江威,吕义俊,等.高产酚酸菌株筛选及其在清香型白酒生产中的应用[J].酿酒科技,2024(7):50-55.
[18] 曾林,谭霄,张庆,等.生物转化γ-氨基丁酸酿酒酵母的筛选及其在桑葚酒酿造中的应用[J].食品与发酵工业,2017,43(6):122-128.
[19] 李晶晶,郭万春,胡瑞峰,等.发酵肉制品中潜在改善高脂血症乳酸菌的筛选及鉴定[J].中国酿造,2023,42(7):73-80.
[20] 朱丽萍,李群,张帆,等.马克斯克鲁维酵母筛选及其在白酒酿造中降低正丙醇的研究[J].酿酒,2024,51(2):75-80.
[21] 朱丽萍,杨强,刘源才,等.清香型小曲白酒生产中红曲霉的分离及发酵特性研究[J].酿酒科技,2021(10):133-139.
[22] 陈申习,唐洁,张龙,等.清香型小曲白酒机械化生产中微生物动态变化研究[J].中国酿造,2018,37(6):68-72.
[23] ZHU L P,LI L Q,YANG Q,et al.Study on microbial community of''Greencovering'' Tuqu and the effect of fortified autochthonous Monascus purpureus on the flavor components light-aroma-type Baijiu[J].Front Microb,2022,13:973616.
[24] 冯志彬,吴思颖,张玉香,等.短乳杆菌产γ-氨基丁酸发酵条件的优化[J].鲁东大学学报(自然科学版),2012,28(3):248-251.
[25] 赵国群,关军锋.高产γ氨基丁酸酿酒酵母的筛选及其在梨酒酿制中的应用[J].食品工业科技,2015,36(23):173-176,181.
[26] 邢宏博,许赣荣,倪冬姣,等.响应面法优化红曲菌固态发酵产γ-氨基丁酸的研究[J].饲料研究,2021,44(20):64-69.
[27] HUSSIN F S,CHAY S Y,ZARE I,et al.Potentiality of self-cloned Lactobacillus plantarum Taj-Apis362 for enhancing GABA production in yogurt under glucose induction: Optimization and its cardiovascular effect on spontaneous hypertensive rats[J].Foods,9(12):9121826.