酱香型白酒是中国最早确立的四大香型白酒之一,酿造工艺复杂,包括高温大曲制作与贮存、高温堆积发酵和窖内发酵3个重要的微生物演替节点。高温堆积发酵又称为“二次制曲”,是酱香型白酒生产的核心工艺之一,将蒸熟的高粱与大曲混合物以圆锥形堆放于地面2~7 d,直至酒堆内部温度≥50 ℃时结束,可抑制杂菌的生长,大量富集耐高温酿酒微生物,为入池发酵提供基础[1],在此过程中,各种发酵微生物积累并在酒精发酵和风味形成中发挥关键作用[2]。针对酱香型白酒产区堆积发酵过程酒醅微生物群落结构的变化与演替已进行了大量研究,胡小霞等[3]研究发现,1轮次堆积发酵过程中含有13个优势细菌属,其中乳酸杆菌属(Lactobacillus)、大肠埃希氏菌属-志贺氏菌属(Escherichia-Shigella)、芽孢杆菌属(Bacillus)占主导地位;张红霞等[4]研究发现,造沙轮次优势真菌属为毕赤酵母属(Pichia)、酵母属(Saccharomyces)、嗜热子囊菌属(Thermoascus)、曲霉属(Aspergillus)、红曲霉属(Monascus)。
第6轮次酒又名“小回酒”,具有酱香突出、醇和、糊香好和味长的酒体特征,但基酒品质总体不如大回酒[5],有研究表明,第6轮次堆积发酵阶段酒醅淀粉和还原糖含量降低,受酸度和水分影响较大,导致微生物群落结构与第4、5轮次具有差异。如WANG H等[6]对贵州地区酒醅堆积发酵过程菌群结构进行研究,发现代尔夫特菌属(Delftia)、鞘氨醇单胞菌属(Sphingomonas)是第4、5轮次优势菌属,第6轮次优势菌属为根瘤菌属(Rhizobium)、寡养单胞菌属(Stenotrophomonas);王源等[7]利用MiSeq高通量测序技术对北京地区第6轮次堆积发酵酒醅细菌群落进行研究,发现共有14个优势菌属,相较于其他产区,北京地区酱香型白酒第6轮次堆积发酵过程中不动杆菌属(Acinetobacter)相对丰度较低且堆积发酵结束时细菌菌群种类数量较少;王玉荣等[5]研究发现,湖北地区第6轮次酒醅堆积过程中Lactobacillus、高温放线菌属(Thermoactinomyces)、克罗彭斯特菌属(Kroppenstedtia)、Saccharomyces、Thermoascus和嗜热真菌属(Thermomyces)在不同位置相对含量差异显著,酒醅微生物间存在共生或竞争的演替作用。
目前,关于酱香型白酒堆积发酵过程微生物群落变化的研究较多聚焦于川贵、北方地区,而湖南地区相关研究鲜有报道,湖南湘北武陵区位于世界黄金酿酒地带,气候温和湿润、水质纯净、土质纯良、富含有益微量元素,空气和土壤中含有丰富参与酿酒发酵所需微生物,此外,独特的湿地环境土壤有机质含量丰富,适宜芽孢杆菌等多种微生物生长、发育、繁殖和富集,赋予武陵酱香型白酒特有的味感和爽净感。本研究以武陵酱香型白酒第6轮次堆积发酵酒醅为研究对象,采用高通量测序技术及传统可培养方法对其微生物多样性进行解析,采用常规检测方法对其理化指标进行检测分析,并采用典型相关分析(canonical correlation analysis,CCA)法构建微生物群落与理化因子间相互作用关系,同时解析优势微生物群落间的作用关系,为深入研究武陵酱香型白酒酿造菌群来源、定向提升酿造品质提供基础数据。
1 材料与方法
1.1 材料与试剂
1.1.1 样品来源
堆积酒醅样品:湖南武陵酒有限公司。为全面分析堆积过程总体发酵情况,每次取样共采集10个实验窖池的堆积酒醅样品40份,混匀后获得1份综合样,酒醅拌曲、收堆结束开始取样(取样方法为围绕堆醅一周,选取四个对称点,采集距地面高0.9 m,距堆醅表面40 cm深的酒醅),每间隔24 h取样1次,直至破堆,共取得3份综合样(DJ-0 h、DJ-24 h、DJ-48 h)。取样后立即装入无菌自封袋中,置于-80 ℃保存备用。
1.1.2 培养基与试剂
营养琼脂培养基、MRS培养基、孟加拉红培养基、麦芽汁培养基:杭州微生物试剂有限公司;脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:美国Omega BioTek公司;DL2000 DNA Marker:日本Takara公司;琼脂糖凝胶试剂、P7589 Quant-iT PicoGreen dsDNA Assay Kit荧光染料:美国Invitrogen公司;M0491L Q5 High-Fidelity DNA Poly merase(2 000 U/mL):美国New England Biolabs公司。
High-Fidelity DNA Poly merase(2 000 U/mL):美国New England Biolabs公司。
1.2 仪器与设备
HH-8水浴锅:力辰仪器科技有限公司;SW-CJ-2FD超净操作台:苏州净化设备有限公司;MJ-250I生化培养箱:上海一恒科学仪器有限公司;NB-DGL-75G灭菌锅:南北仪器有限公司;101-2AB鼓风干燥箱:天津泰斯特仪器有限公司;Nanodrop2000超微量紫外分光光度计:美国Thermo Scientific公司;DYY-6C电泳仪:北京六一生物科技有限公司;BG-gdsAUTO(130)凝胶成像系统:北京百晶生物技术有限公司;Tissuelyser-48研磨仪:上海净信实业发展有限公司;2720聚合酶链式反应(polymerase chain reaction,PCR)扩增仪:美国Applied Biosystems公司;FLX800T酶标仪:美国BioTek公司。
1.3 方法
1.3.1 理化指标检测
根据沈怡方[8]所述方法测定酒醅水分、酸度、淀粉含量。
1.3.2 可培养微生物的分离计数
参考朱安然等[9]的方法对微生物进行培养,营养琼脂培养基、MRS培养基放置于36 ℃培养2 d,孟加拉红培养基、麦芽汁培养基放置于28 ℃培养2 d,选择合适稀释梯度培养基进行菌落数量记录。
1.3.3 微生物菌群多样性分析
采用基因组DNA提取试剂盒提取堆积酒醅样品的微生物宏基因组DNA,采用0.8%琼脂糖凝胶电泳检测其碱基长度,利用超微量紫外分光光度计对DNA进行定量,以其为模板,采用引物F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和R(5'-GCTGCGTTCTTCATCGATGC-3')对真菌菌群的ITS1区基因序列进行PCR扩增;采用引物338F(5'-ACTC CTACGGGAGGCAGCA-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')对细菌菌群16S rDNA的V3~V4区基因序列进行PCR扩增。
PCR扩增条件[10]:98 ℃预变性2 min;98 ℃变性15 s,55 ℃退火30 s,72 ℃延伸30 s,共循环25次;72 ℃再延伸5 min。PCR扩增体系:5×reaction buffer 5 μL,5×GC buffer 5 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)(2.5 mmol/L)2 μL,正向引物(10 μmol/L)1 μL,反向引物(10 μmol/L)1 μL,模板DNA 2 μL,双蒸水(ddH2O)8.75 μL,Q5 DNA聚合酶0.25 μL。委托上海派森诺生物科技有限公司基于Illumina Miseq平台进行高通量测序。
1.3.4 数据处理
每个实验进行3个生物学重复。使用QIIME2 2022.11平台对微生物组生物学信息进行分析。原始序列数据使用demux插件进行解码处理,cutadapt插件进行引物切除,使用去噪分析分辨率更高、准确性更强的DADA2插件对序列进行质量过滤、去噪、拼接和嵌合体去除处理,对上述获得的序列按100%的序列相似度进行归并,生成特征性序列扩增序列变体(amplified sequence variants,ASVs)以及丰度数据表格[11]。利用Silva、Unite数据库进行基因序列比对和注释。采用Origin 2024绘制折线图、堆积柱形图,采用SPSS 26.0进行Spearman相关性分析,为降低网络复杂性,仅选择具有显著相关性(P<0.05)的菌属于Cytoscape软件绘制相关性网络图,采用派森诺云平台进行典型相关分析(CCA)和线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析。
2 结果与分析
2.1 第6轮次堆积发酵过程中酒醅理化指标的变化
酸度、水分、淀粉是指导白酒生产及改进工艺的关键指标,决定白酒出酒率和酒体质量,淀粉和其他多糖经酶促水解成葡萄糖和其他可发酵糖,为微生物的生长和新陈代谢提供物质基础和能量来源[12],微生物代谢过程中的各种生理和生化反应可调节水分和酸度,比较两者含量可评估酒醅的发酵状态。第6轮次堆积发酵过程中酒醅的水分含量、酸度、淀粉含量动态变化规律见图1。由图1可知,在第6轮次堆积发酵过程中,淀粉含量基本维持恒定,为(12.90±0.46)%~(12.74±0.39)%,与吴成等[13]的研究报道一致;酸度、水分含量均略有降低,破堆时(48 h)分别为(3.30±0.26)mmol/10 g、(52.93±0.35)%,分析原因可能是由于酵母和霉菌富集活动较为活跃,抑制了产酸细菌代谢,导致酸度降低,微生物生长繁殖产生大量热量使水分含量降低[14]。
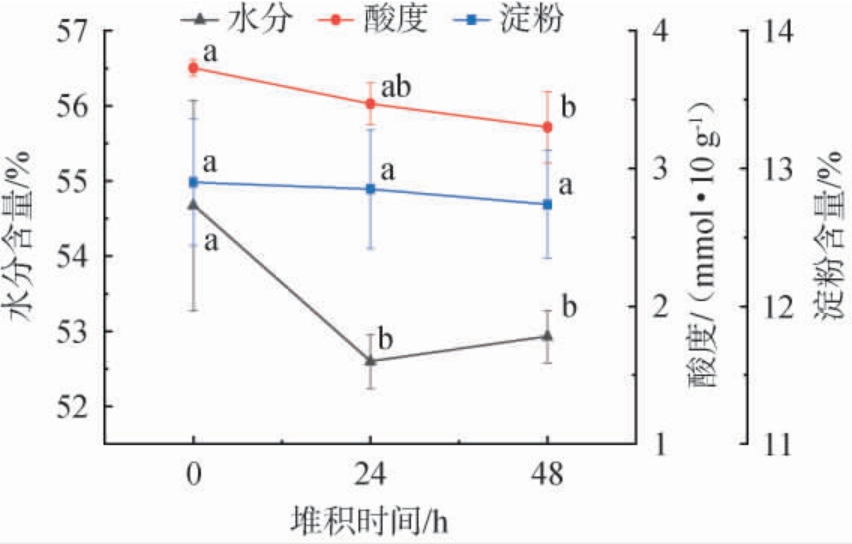
图1 武陵酱香型白酒第6轮次堆积发酵过程中酒醅理化指标的变化
Fig.1 Changes of physicochemical indexes of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu
小写字母不同表示同一指标不同发酵时间之间差异显著(P<0.05)。
2.2 第6轮次堆积发酵过程中酒醅可培养微生物活菌数的变化
酒醅堆积发酵过程可培养微生物活菌数的变化见表1。由表1可知,细菌菌落总数在105、106数量级浮动,堆积发酵过程中有明显增加趋势,破堆时达到1.51×106 CFU/g;耐高温芽孢杆菌活菌数略有降低,稳定在104数量级;霉菌和乳酸菌活菌数较少,菌落数量在103数量级;破堆时酵母菌活菌数由105升至106数量级,活菌数达到8.25×106 CFU/g,成品大曲制作过程经过两次高温发酵导致酵母菌活菌数变少使其发酵力不足,堆积发酵过程酵母菌迅速富集可有效弥补此缺陷[15]。
表1 武陵酱香型白酒第6轮次堆积发酵过程中酒醅微生物活菌数的变化
Table 1 Changes of viable microbial colonies of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu

注:同一指标不同小写字母表示差异显著(P<0.05)。
2.3 第六轮次堆积发酵过程中酒醅微生物多样性分析
2.3.1 高通量测序结果
基于Illumina Miseq平台从第6轮次堆积发酵过程中的酒醅样品中共检测到1 088 341条细菌有效序列,序列碱基长度集中于236~450 bp,平均碱基长度为416.04 bp;真菌有效序列数为772 052条,序列碱基长度集中于229~448 bp,平均碱基长度为258.11 bp。以100%序列相似度聚类生成ASVs,细菌菌群共得到689个ASVs,真菌菌群共得到104个ASVs,细菌菌群ASVs总数远高于真菌菌群。为了直观对比样品微生物群落的共性和差异,绘制第六轮次堆积发酵过程中酒醅样品细菌(a)和真菌(b)菌群ASVs的韦恩图,结果见图2。由图2可知,第6轮次堆积发酵过程中酒醅样品的共有细菌ASVs为36个,真菌ASVs为17个,堆积发酵0 h时,细菌和真菌菌群的ASV数量均最多,说明起堆微生物丰富度较高。
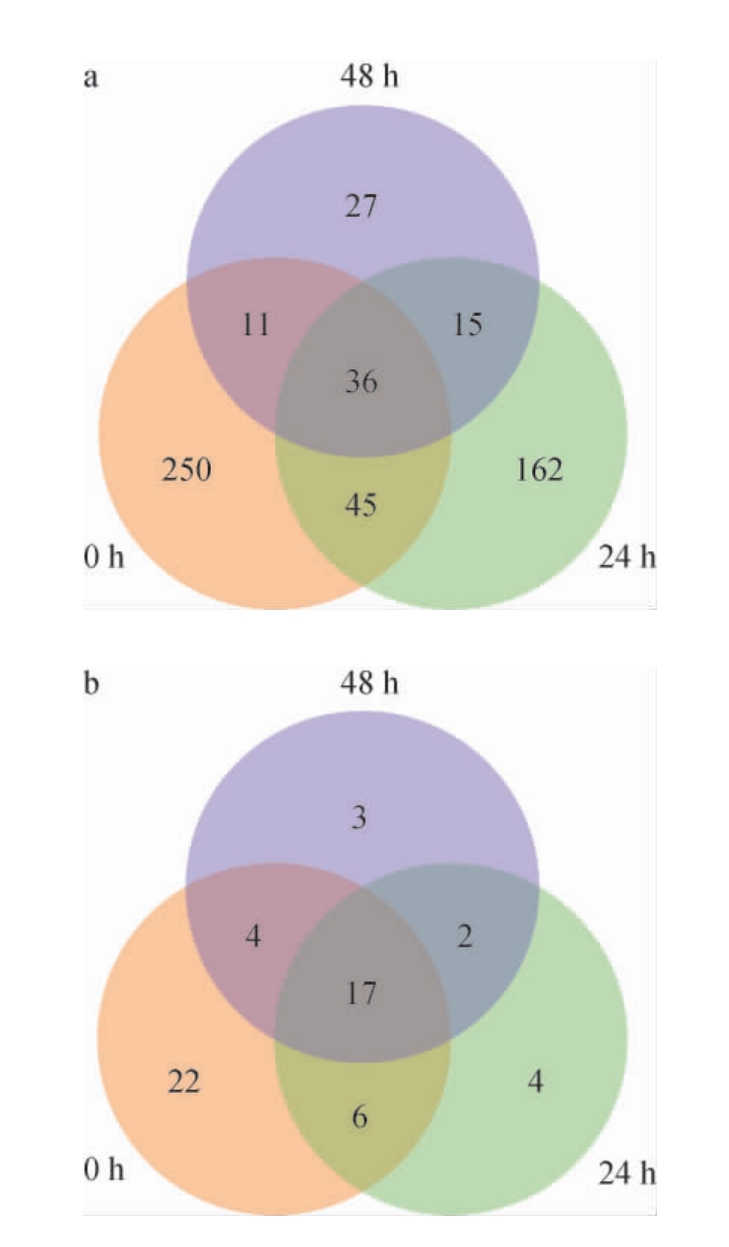
图2 武陵酱香型白酒第6轮次堆积发酵过程中酒醅细菌(a)和真菌(b)菌群扩增子序列变体的韦恩图
Fig.2 Venn diagram of amplified sequence variants of bacterial (a)and fungal (b) communities of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu
2.3.2 Alpha多样性分析
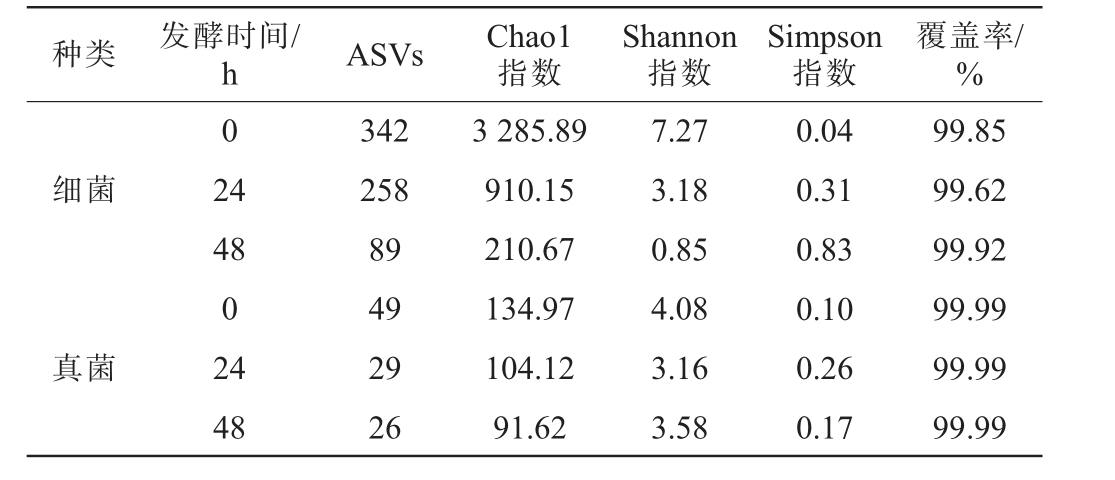
对ASVs表进行抽平处理,最小抽平深度为10,在这一深度与最小深度之间均匀选取10个深度值,每个深度值抽平10次,计算所选的Alpha多样性指数,第6轮次堆积发酵过程中酒醅样品微生物菌群的Alpha多样性分析结果见表2。由表2可知,细菌和真菌菌群测序覆盖率均>99%,表明测序深度足够[16],测序结果能代表本次样品微生物群落的真实情况。Chao1指数表征丰富度,值越大代表样品物种数量越多,Shannon指数和Simpson指数则表征微生物群落的多样性,Shannon指数值越高、Simpson指数越低代表样品群落多样性越高[17]。第6轮次堆积发酵阶段酒醅样品中的细菌菌群多样性指数普遍高于真菌菌群,说明此阶段细菌菌群的多样性和丰富度优于真菌菌群,REN T T等[11]研究了贵州地区下沙阶段酒醅菌群结构,也论证了堆积发酵时细菌菌群的丰富度高于真菌菌群,而入池发酵阶段则相反。堆积发酵0 h时,细菌和真菌菌群的Chao1指数、Shannon指数值最大、Simpson指数值最小,说明此时细菌和真菌菌群的丰富度和多样性更高,相比堆积发酵0 h时,堆积发酵48 h时,Chao1指数、Shannon指数值下降、Simpson指数值升高,可能是堆积过程温度升高导致特征微生物的自然筛选,优势微生物群落进一步扩大生长优势,非优势微生物群落则走向消亡,群落丰度的均匀性也变差。王源等[7]对北京地区6轮次酱香型白酒堆积酒醅的细菌菌群多样性进行分析,得到了与本研究结果相似的结论,但总体而言Alpha多样性指数变化幅度较为平缓,可能是由于北京地区酒堆升温慢而堆积时间较长(84 h),而湖南常德属亚热带季风气候,气温变化小,且环境微生物丰富,堆积时间短(48 h),酒堆升温快,各指数变化较明显。
表2 武陵酱香型白酒第6轮次堆积发酵过程中酒醅细菌和真菌菌群的Alpha多样性指数
Table 2 Alpha diversity indexes of bacterial and fungal communities of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu
2.3.3 微生物群落组成分析
样品经高通量测序后,细菌共鉴定出12个门、19个纲、51个目、86个科、156个属、144个种,真菌共鉴定出4个门、9个纲、13个目、19个科、25个属、40个种。为探寻第6轮次堆积发酵过程中酒醅样品微生物群落结构的变化情况,在门和属水平上对细菌和真菌群落结构进行分析,结果分别见图3和图4。将相对丰度>1%的菌门或菌属定义为优势菌门或优势菌属,由图3a可知,从第6轮次堆积发酵过程共注释到3个优势细菌门,分别为变形菌门(Proteobacteri)、厚壁菌门(Firmicutes)、放线菌门(Actinobacteriota)。其中,Proteobacteri相对丰度随堆积发酵时间的延长呈快速上升趋势,破堆(48 h)时达到最高,为88.97%,Firmicutes与之相反,相对丰度由起堆(0 h)时68.58%急剧降低至破堆时的10.72%,Actinobacteriota小幅降低,破堆时相对丰度降至0.11%。Proteobacteri是细菌中最大的一类门,为革兰氏阴性菌,Firmicutes可以产芽孢[16],两者不仅是酱香型白酒酿造中的优势微生物,也是其他香型白酒酿造中的优势微生物[18]。王源等[7]对北京地区第6轮次堆积发酵酒醅进行研究,发现优势细菌门种类与本研究结果一致,但Firmicutes始终属于绝对优势细菌门,整个发酵阶段相对丰度均>85%,而本研究中的Firmicutes相对丰度呈下降趋势,因此随着堆积发酵的进行,第6轮次酒醅不产芽孢的细菌门逐渐占据较大比例。
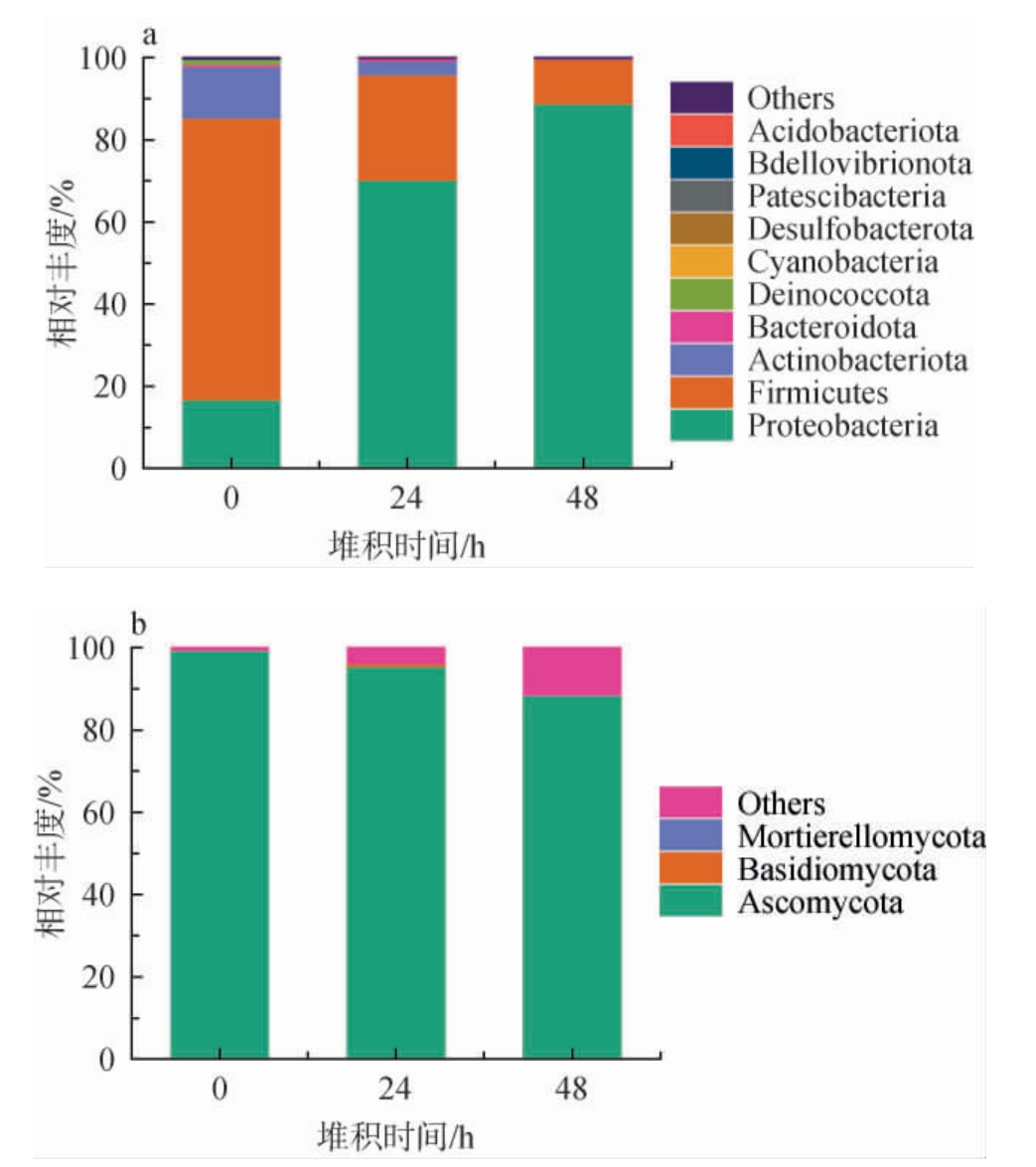
图3 基于门水平武陵酱香型白酒第6轮次堆积发酵过程中酒醅细菌(a)和真菌(b)群落组成
Fig.3 Bacterial (a) and fungal (b) community composition of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu based on phylum level
Others表示未分类真菌门或细菌门。
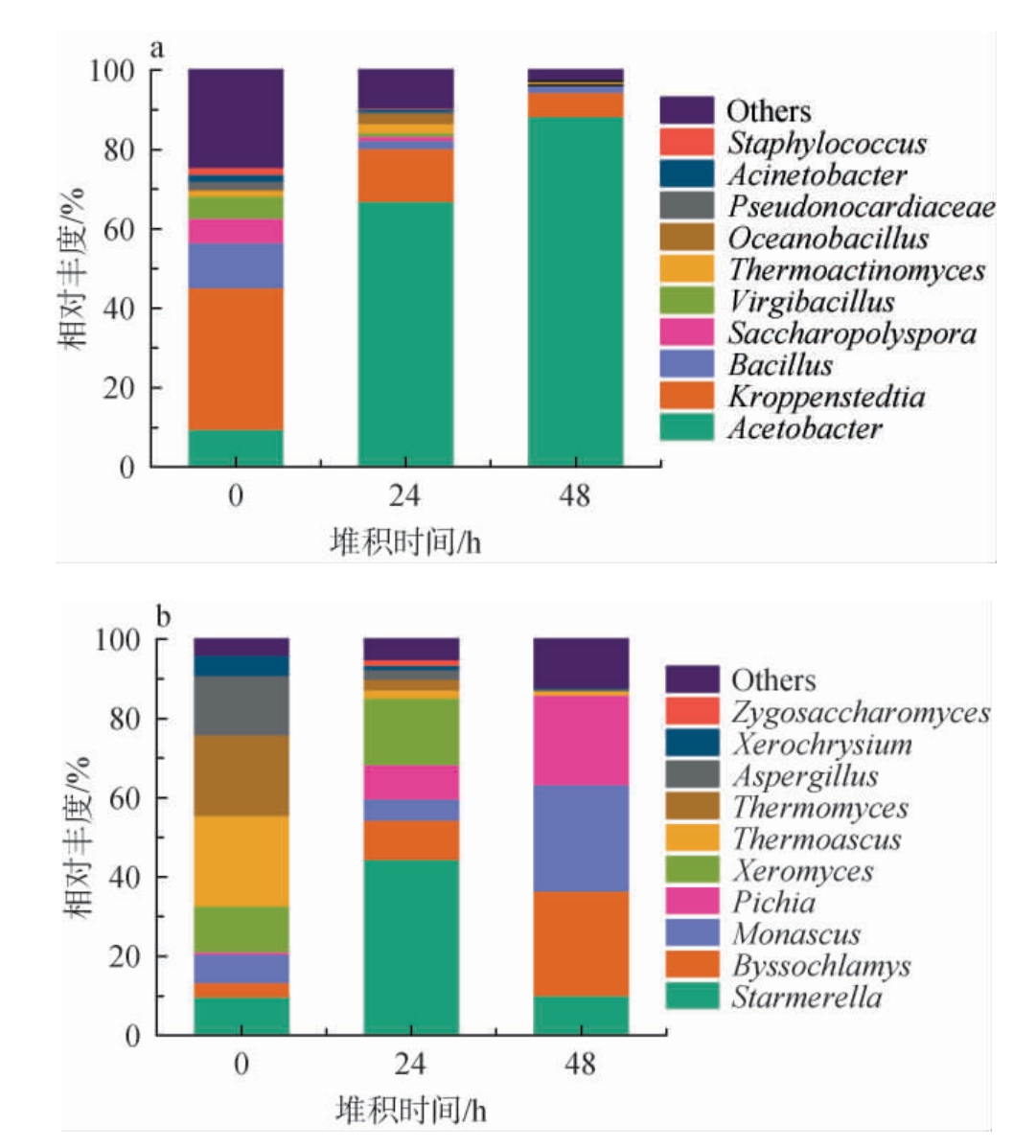
图4 基于属水平武陵酱香型白酒第6轮次堆积发酵过程中酒醅细菌(a)和真菌(b)群落组成
Fig.4 Bacterial (a) and fungal (b) community composition of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu based on genus level
Others表示未分类细菌属或真菌属。
由图3b可知,从第6轮次堆积发酵过程共注释到1个优势真菌门,为子囊菌门(Ascomycota)。Ascomycota为绝对优势真菌门,主要是酵母菌和霉菌[19],整个堆积发酵过程中其相对丰度略有下降,但均>88%,与吴成等[12]的研究结果一致,各大白酒产区窖泥中均有检出[20],Ascomycota是传统发酵食品的优势真菌门,在发酵酸鱼、腊肉、泡菜、乳制品中均有检出,且相对丰度均占据主导优势[21-22]。Basidiomycota发酵中期(24 h)相对丰度增至0.65%。堆积发酵48 h时优势真菌门为Ascomycota(88.54%),未分类真菌门(Others)明显高于未分类细菌门(Others),说明堆积发酵过程中酒醅真菌群落结构复杂,包含多种在现有数据库中无法识别或未被识别的物种。
由图4a可知,从第6轮次堆积发酵过程中的酒醅样品中共注释到10个优势细菌属,分别为醋酸杆菌属(Acetobacter)、克罗彭斯特菌属(Kroppenstedtia)、芽孢杆菌属(Bacillus)、糖多孢菌属(Saccharopolyspora)、枝芽孢杆菌属(Virgibacillus)、高温放线菌属(Thermoactinomyces)、海洋芽孢杆菌属(Oceanobacillus)、假诺卡氏菌属(Pseudonocardiaceae)、不动杆菌属(Acinetobacter)、葡萄球菌属(Staphylococcus)。与真菌属相比,堆积发酵阶段细菌属多样性减少,群落结构快速演替,这与ZHANG H X等[23]的结果相似,而真菌属菌群结构变化较为均匀。Acetobacter与Kroppenstedtia为整个堆积发酵阶段的主体细菌属,两者呈此消彼涨的趋势,破堆时Acetobacter的相对丰度高达88.37%,Kroppenstedtia的相对丰度降至6.13%,Bacillus、Saccharopolyspora、Virgibacillus在堆积发酵过程中呈下降趋势,其他优势细菌属的相对丰度也明显低于0 h和24 h。YANG L等[24]在贵州地区酱香型白酒6轮次堆面酒醅中检测出与本研究相似的优势细菌属,Acetobacter相对丰度亦较高,而此菌属在其研究中鲜有发现,Acetobacter主要存在于酒堆外侧,通过参与半胱氨酸和蛋氨酸代谢、牛磺酸和次牛磺酸代谢,促进硫化合物转化为挥发性较低的含硫氨基酸,降低堆积发酵谷物中挥发性硫化合物的含量,从而有效减少盐菜味缺陷酒的产出[25]。Kroppenstedtia是参与有机酸生物合成的关键细菌属,Bacillus可以合成多种酶(如淀粉酶和蛋白酶)和乙酸乙酯、香兰素等物质,这些成分间接或直接影响白酒风味形成[26],此外还被证实具有产吡嗪类风味物质能力,特别是甲基类吡嗪化合物,是酱香型白酒中的关键风味物质之一[27]。
由图4b可知,从第6轮次堆积发酵过程中的酒醅样品中共注释到10个优势真菌属,分别为Starmerella、丝衣霉菌属(Byssochlamys)、红曲霉属(Monascus)、毕赤酵母属(Pichia)、耐干霉菌属(Xeromyces)、嗜热子囊菌属(Thermoascus)、嗜热真菌属(Thermomyces)、曲霉属(Aspergillus)、Xerochrysium、接合酵母属(Zygosaccharomyces)。相比细菌属,真菌属相对丰度的变异性较细菌属小。Starmerella在堆积发酵24 h时相对丰度明显增加(44.48%),后又急剧降低(10.15%),此前鲜有学者在酱香型白酒堆积酒醅中发现此真菌属,Starmerellas分离自过熟葡萄、发酵葡萄汁[28],目前包含48种酵母物种,具有耐糖、耐硫化物和耐低温特性,可进行氨基酸代谢,赋予葡萄酒果香、花香、焦糖味[29]。堆积发酵0 h时,Xeromyces、Thermoascus、Thermomyces、Aspergillus、Starmerella为主要优势真菌属,相对丰度分别为11.66%、22.89%、20.29%、14.90%、9.85%,而堆积发酵48 h时,Byssochlamys、Monascus、Pichia为主要优势真菌属,且三者相对丰度较为均衡,分别为26.45%、26.81%、22.52%,总体看来,发酵初期真菌菌群以霉菌属为主,发酵中期和后期霉菌属和酵母属共同作用于堆积酒醅,具有耐热、嗜热特性[24],霉菌分泌的水解酶通过降解淀粉、蛋白质等大分子物质为酵母菌的生长和发酵提供底物,而酵母菌将底物转化为醇和风味物质[9,30]。YANG L等[24]研究发现,Candida是贵州地区关键真菌属之一,其他优势真菌属与本研究基本相似;DUAN Z F等[2]研究发现,北京地区6轮次堆积酒醅发酵开始时,Thermoascus是酒醅中含量最丰富的真菌属(45.0%),随着时间的推移,优势真菌属首先转变为Thermomyces(46.7%),最后是Issatchenkia(79.7%),可见不同产区优势真菌属种类既有相似性,又有差异性,独特菌属、各菌属丰度组成比例是导致各产区酱香型白酒风格差异的原因。
2.4 武陵酱香型白酒第6轮次堆积发酵过程中差异微生物分析
为进一步分析第6轮次堆积发酵过程中酒醅中微生物群落差异性,利用LEfSe分析不同堆积发酵时间样品之间的差异细菌和真菌(LDA得分>4),结果见图5。由图5a可知,在属水平上,共检测到5种差异细菌属,其中堆积发酵0 h时差异细菌属为Kroppenstedtia、Saccharopolyspora、Limosilactobacillus、Staphylococcus,堆积发酵48 h时差异细菌属为Acetobacter。由图5b可知,在属水平上,共检测到6种差异真菌属,其中堆积发酵0 h时差异真菌属为Thermomyces、Thermoascus、Aspergillus、Saccharomyces,堆积发酵24 h时差异真菌属为Hyphopichia,堆积发酵48 h时差异真菌属为Pichia,这些差异菌属LDA分数均>4,说明对堆积酒醅差异贡献最大。与细菌相比,真菌的差异分类群落总数较低,NIU J L等[26]在不同高温大曲中也有同样的发现。酒醅堆积过程微生物群落发生了显著变化,这些差异菌落的演变对白酒酿造有重要意义。
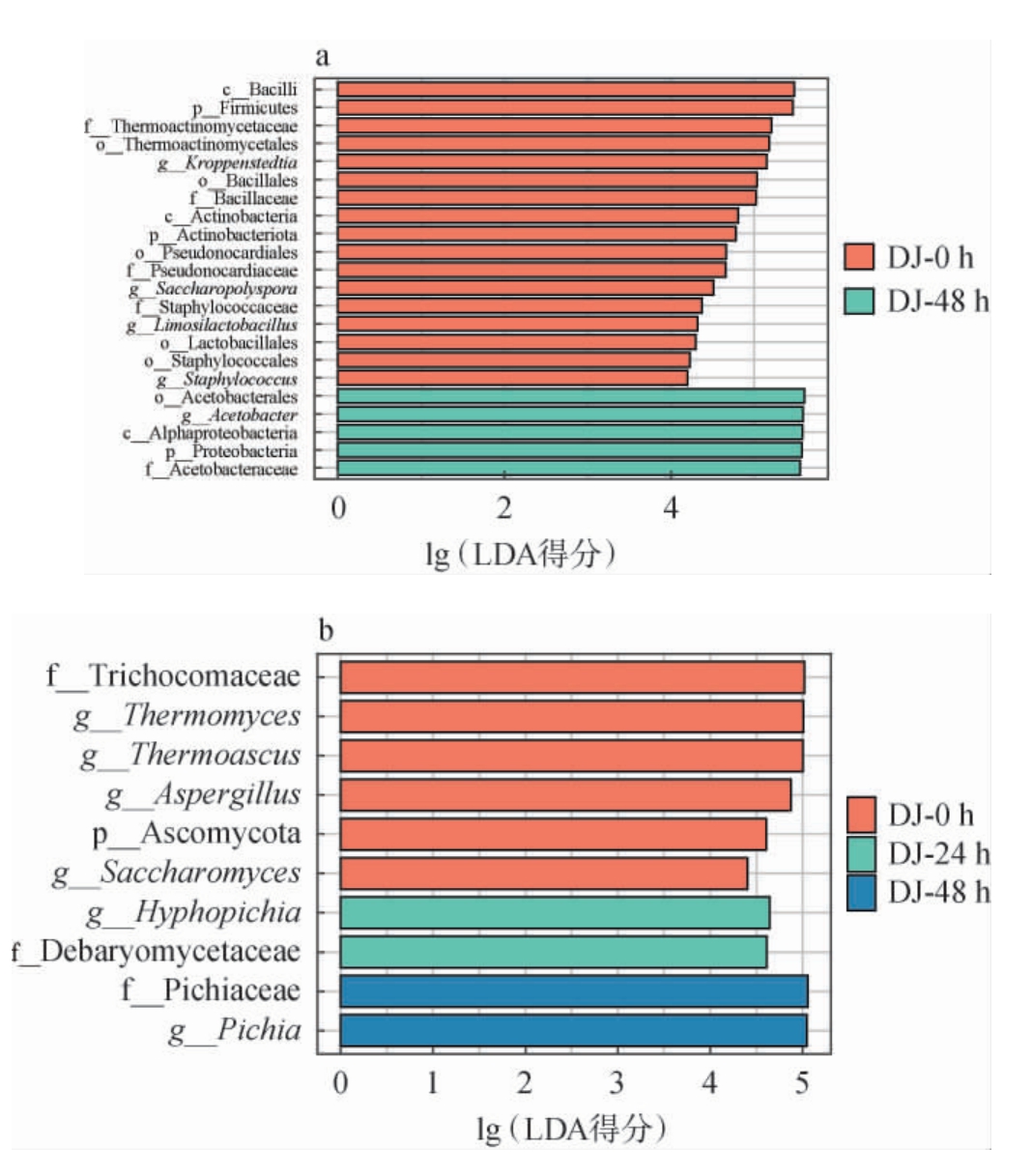
图5 基于线性判别分析效应大小分析武陵酱香型白酒第6轮次堆积发酵过程中酒醅差异细菌(a)及真菌(b)线性判别分析值
Fig.5 Linear discriminate analysis value of differential bacteria (a)and fungi (b) of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu based on linear discriminant analysis effect size analysis
c_代表纲,p_代表门,o_代表目,f_代表科,g_代表属。
2.5 相关性分析
2.5.1 优势菌属间的相关性分析
为进一步探究武陵酱香型白酒第6轮次堆积发酵过程微生物群落间的相互作用,对堆积发酵过程中的优势菌属进行Spearman相关性分析,选择相关性显著(P<0.05)的多对优势菌属绘制相关性网络图,结果见图6。由图6可知,共产生18个高相关性节点(hubs),与其他多种菌属存在正相关或负相关关系[3]。相关性网络图包含41对正相关关系,31对负相关关系,说明多数优势菌属间呈正相关调节机制。Acetobacter、Kroppenstedtia、Saccharopolyspora、Pichia、Aspergillus 5个菌属与其他菌属的相关性最为丰富,均有10个以上的相关性连线,说明这些菌属容易受到环境条件和其他菌属的影响,在堆积发酵过程中极易发生演替,导致相对丰度差异较大[31]。Acetobacter、Pichia是核心负相关性hubs,分别与11个、10个菌属间存在负相关关系,对这些菌属具有显著抑制作用,Kroppenstedtia、Saccharopolyspora、Aspergillus是核心正相关性hubs,分别与9个、9个、8个菌属间存在正相关关系。陈博超[31]对北京地区酱香型白酒进行研究,发现Oceanobacillus、厌氧杆菌属(Anaerosalibacter)、假纤细芽孢杆菌属(Pseudogracilibacillus)、Thermoactinomyces是核心hubs;不同产区核心hubs不尽相同,相互关系错综复杂,连接线纵横密集分布,这些相互生物学关系构成了发酵过程的基本生物学调控机制,也是发酵过程发酵动力、风味动力形成和调控机制的基本组成[32]。
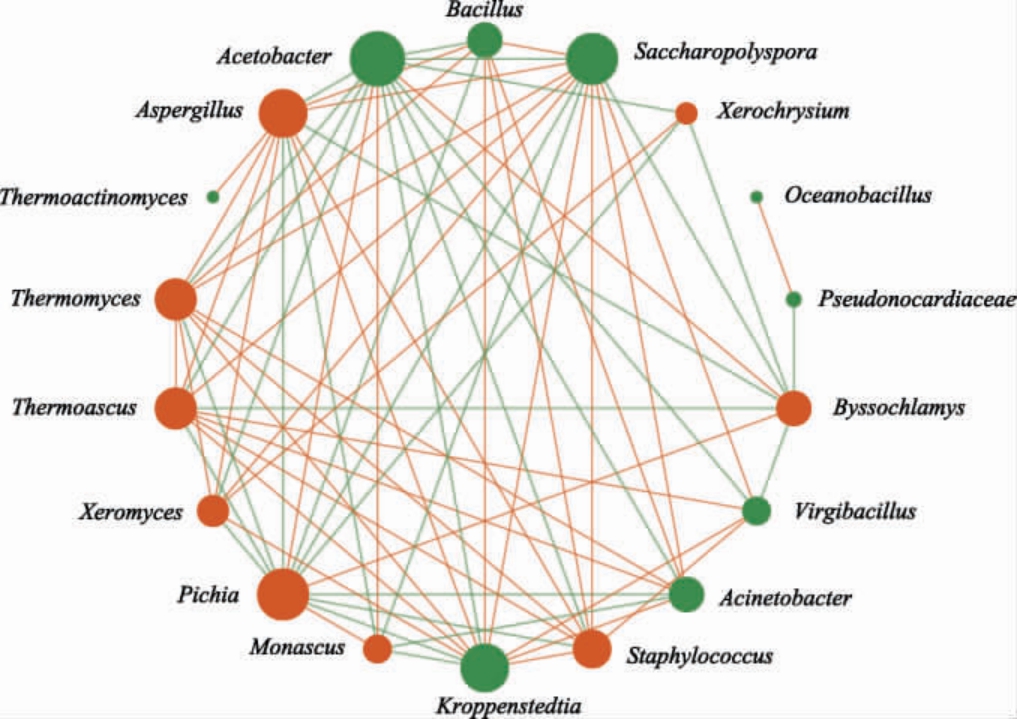
图6 武陵酱香型白酒第6轮次堆积发酵过程中酒醅微生物群落相关性网络
Fig.6 Correlation network of microbial communities of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu
橙色圆代表真菌属,绿色圆代表细菌属,实心圆圈越大代表与之相互作用的菌属越多,红色连线代表两者呈正相关,绿色连线代表两者呈负相关。
2.5.2 优势菌属与理化因子典型相关性分析
为研究堆积发酵过程理化因子对微生物群落的影响,选取优势菌属与理化因子进行CCA,结果见图7。由图7a可知,CCA1和CCA2共解释了优势细菌属78.38%的变异率,优势细菌群落与理化指标存在较强的相关性。Acetobacter与酸度、水分、淀粉呈负相关,Bacillus、Virgibacillus、Pseudonocardiaceae、Acinetobacter、Staphylococcus均与酸度、水分、淀粉呈正相关,Oceanobacillus、Kroppenstedtia、Thermoactinomyces与酸度、水分呈正相关,与淀粉呈负相关,Saccharopolyspora与淀粉、水分呈正相关。有研究表明,芽孢杆菌可以在高温下生长,具有产生多种有机酸和脂肪酸酯的能力[33],以及高产淀粉酶、蛋白质水解能力,朱安然等[9]对酱香型白酒1轮次糟醅微生物群落结构与理化因子的相关分析中也得出了同样的结论。
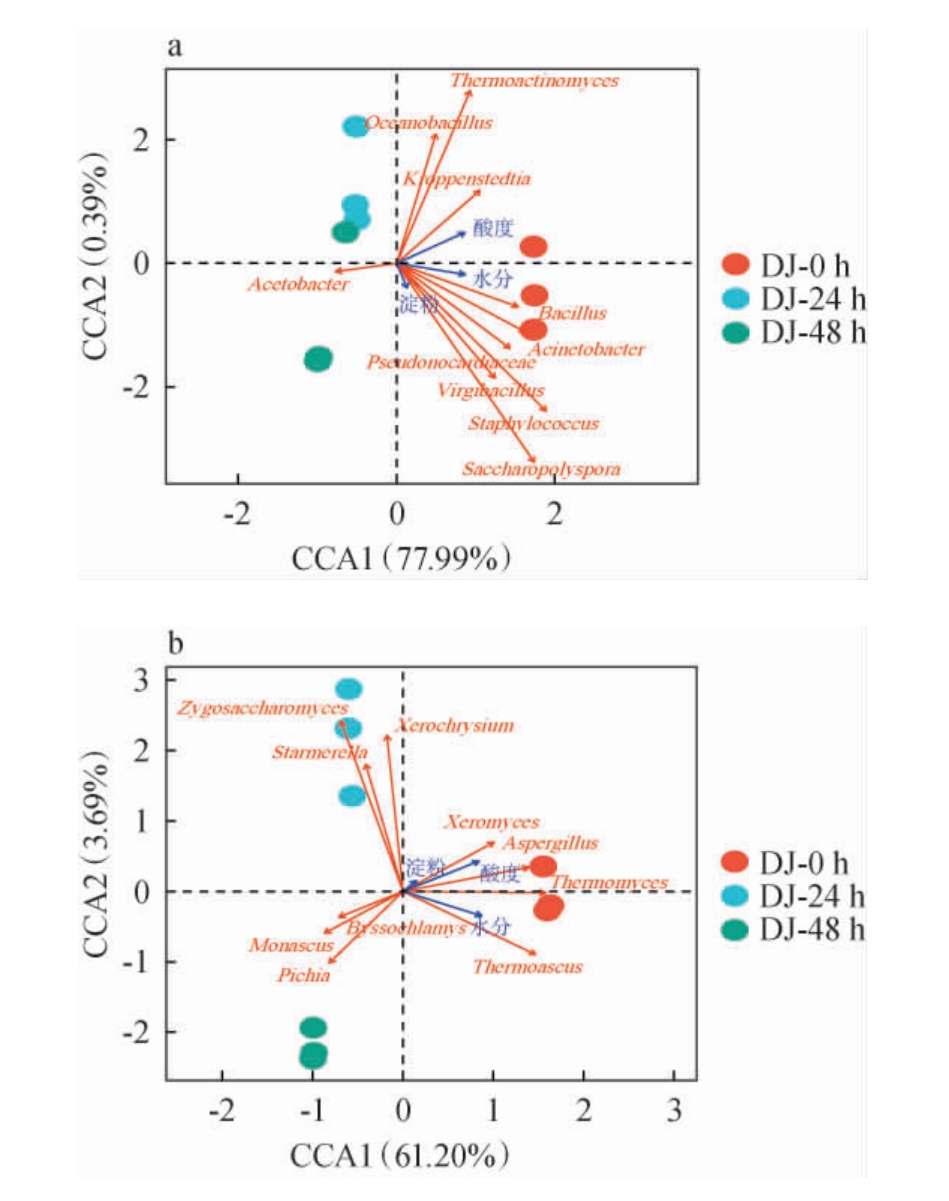
图7 武陵酱香型白酒第6轮次堆积发酵过程中酒醅优势细菌(a)、真菌(b)与理化指标的典型相关性分析结果
Fig.7 Canonical correlation analysis among dominant bacteria (a),fungi (b) and physicochemical indexes of fermented grains during the sixth round stacking fermentation of Wuling sauce-flavor Baijiu
由图7b可知,CCA1和CCA2共解释了优势真菌属64.89%的变异率。Zygosaccharomyces、Starmerella、Xerochrysium与淀粉和酸度呈正相关,与水分呈负相关,Byssochlamys、Monascus、Pichia与淀粉、水分、酸度呈负相关,Aspergillus、Thermomyces、Xeromyces与酸度、水分、淀粉呈正相关,Thermoascus与酸度、水分呈正相关。Aspergillus在发酵过程中可产生大量的酸性蛋白酶、纤维素酶和糖基酸盐,生成挥发性酸,增加发酵环境中的酸度[33];Pichia具有很强的乳酸耐受性,发酵过程通过代谢降低乳酸含量,为其他酵母生长和乙醇生成提供相对适宜的环境[33]。综上,理化指标与微生物群落的演替相关,进而影响白酒的发酵过程。
3 讨论
采用传统可培养方法和高通量测序技术对武陵酱香型白酒第6轮次堆积发酵过程微生物组成情况进行解析,两种方法对优势细菌和真菌的检测存在差异:传统可培养法显示乳酸菌是堆积发酵过程的主要细菌之一,且变化较为平缓,而高通量测序未检测出乳酸菌属。吴成等[13]同时采用Unite和RDP数据库进行比对,结果发现Unite相较于RDP数据库而言,更适用于酒醅真菌群落组成的鉴定,因此,数据库的选择会影响高通量测序技术结果的准确性;引物的选择对测序结果也有影响,朱安然等[9]对一轮次堆积酒醅进行高通量测序时,细菌扩增采用通用引物341F和805R,其结果显示Lactobacillus是6个优势细菌属之一。此外,传统可培养法显示酵母菌和霉菌是主要真菌,堆积过程中酵母菌的数量级由105升至106,霉菌菌落数量级在103,显著低于酵母菌;而高通量测序结果显示,霉菌Byssochlamys、Monascus、Aspergillus、Xeromyces在堆积过程的总相对丰度在堆积0 h、24 h、48 h时依次为37.32%、34.51%、56.53%,酵母菌Starmerella、Pichia、Zygosaccharomyces的总相对丰度依次为10.41%、54.5%、32.68%,酵母菌和霉菌相对丰度与菌落计数相比结果存在差异,可能是由于传统可培养法测得的是活菌数,堆积过程酒堆不断升温导致可培养活菌数减少、培养基的选择性和培养条件的局限性也是导致结果差异的原因。因此,两种方法各有优劣,具有互补性,高通量测序技术可以快速而广泛地分析鉴定样本微生物菌落组成,传统培养方法可以填补由于高通量测序数据库信息不全造成的结果偏差。
本研究基于相关性分析得到关键菌属,并探究了优势菌属与各理化因子间的相关性,利用LEfSe分析不同堆积阶段差异菌属的动态变化,为武陵酱香型白酒堆积酿造过程群落演替提供数据支撑。近年,基于Source tracker软件对酒醅微生物进行溯源分析开始成为趋势,朱安然[9]等结合堆积地面、生产器具表面、窗台墙壁、厂房内外空气、窖池壁等环境对堆积和窖池酒醅发酵微生物群落结构进行溯源分析,采用该软件解析了优势微生物来源和比例,为阐明酱香型白酒酿造机理提供理论基础;XU S[34]研究发现,在20年和70年车间中,室内空气、工具、环境是窖内酒醅细菌微生物的主要来源;张红霞等[4]研究发酵过程中真菌来源,发现大曲为堆积发酵提供橙色嗜热子囊菌(Thermoascus aurantiacus)、阿姆斯特丹曲霉(Aspergillus amstelodami)等霉菌类微生物,是白酒发酵糖化力的重要来源,而堆积地面则提供较多的库德里阿兹威毕赤酵母(Pichia kudriavzevii)等酵母类微生物,是白酒发酵力的重要来源。环境微生物被人为或自然地迁移,形成酱香型白酒丰富的微生物群落结构,溯源分析优势微生物来源和比例可为定向调控酱香型白酒微生态、优化酱香型白酒品质提供理论条件。后续本研究将进一步分析环境微生物的群落结构,对堆积和窖内发酵酒醅进行溯源,结合酒醅风味特性进行综合分析,深入揭示酒醅发酵过程中微生物的演替作用与基酒品质的内在联系,提升轮次基酒品质。
4 结论
在理化指标方面,堆积发酵过程中,酒醅淀粉含量基本维持恒定,酸度、水分含量略有降低。在微生物方面,堆积发酵过程中,酵母菌和细菌迅速富集,霉菌活菌数减少;细菌菌群的多样性和丰富度高于真菌菌群,但均呈下降趋势。从堆积发酵过程酒醅样品中共注释到醋酸杆菌属(Acetobacter)、克罗彭斯特菌属(Kroppenstedtia)等10种优势细菌属(相对丰度>1%),Starmerella、丝衣霉菌属(Byssochlamys)等9种优势真菌属。基于LDA得分>4共筛选得到5种差异细菌属和6种差异真菌属。通过相关性分析发现,克罗彭斯特菌属、嗜热菌属(Thermomyces)等为关键相关性节点,与多个菌属间存在相关关系;芽孢杆菌属(Bacillus)演替过程与酸度、水分、淀粉呈正相关,曲霉属(Aspergillus)与毕赤酵母属(Pichia)分别与酸度呈正、负相关。本研究初步分析了武陵酱香型白酒堆积发过程酒醅微生物群落演替,为企业深入研究酱香型白酒发酵机理提供理论支撑。
[1] 王云胜,辛健康,陈银翠,等.酱香白酒第七轮次堆积发酵过程中细菌群落的动态变化[J].基因组学与应用生物学,2022,41(6):1244-1253.
[2] DUAN Z F,WU Y F,ZHANG C N,et al.Comparison of fungal communities and flavour substances in surface and inner layers of fermented grains during stacking fermentation of sauce-flavour Baijiu[J].J Biosci Bioeng,2023,136(4):295-303.
[3] 胡小霞,黄永光,涂华彬,等.酱香型白酒1轮次酿造细菌的菌群结构[J].食品科学,2020,41(14):175-182.
[4] 张红霞,徐岩,杜海.酱香型白酒堆积发酵过程中真菌的结构及其来源分析[J].食品与发酵工业,2024,50(20):42-49.
[5] 王玉荣,马佳佳,田龙新,等.酱香型白酒第六轮次堆积发酵醅堆微生物类群与感官品质的相关性分析[J].现代食品科技,2024,40(9):107-117.
[6] WANG H,HUANG Y G,HUANG Y L,et al.Microbiome diversity and evolution in stacking fermentation during different rounds of Jiang-flavoured Baijiu brewing[J].LWT-Food Sci Technol,2021,143:111119.
[7] 王源,李微微,李秀婷,等.北京地区酱香型白酒第六轮次堆积发酵中细菌群落多样性分析[J].食品科学技术学报,2022,40(3):68-76.
[8] 沈怡方.白酒生产全书[M].北京:中国轻工业出版社,1998:651-654.
[9] 朱安然,汪地强,胡建锋,等.酱香型白酒一轮次糟醅微生物群落结构及溯源分析[J].食品科学,2025,46(4):117-125.
[10] 王依文,田瑶瑶,张克粉,等.不同季节及层级浓香型白酒窖泥微生物群落多样性与风味物质的比较及相关性分析[J].食品科学,2025,46(4):100-109.
[11] REN T T,SU W,MU Y C,et al.Study on the correlation between microbial communities with physicochemical properties and flavor substances in the Xiasha round of cave-brewed sauce-flavor Baijiu[J].Front Microbiol,2023,14:1124817.
[12] TIAN L,XU P,CHEN J Y,et al.Comprehensive analysis of spatial heterogeneity reveals the important role of the upper-layer fermented grains in the fermentation and flavor formation of Qingxiangxing Baijiu[J].Food Chem,2024,22:101508.
[13] 吴成,程平言,谢丹,等.酱香型白酒4轮次堆积发酵理化因子、风味物质与微生物群落相关性分析[J].食品科学,2023,44(2):240-247.
[14] 李喆,冯海燕,吴德光,等.酱香型白酒堆积发酵过程中不同空间位置酒醅差异性比较[J].中国酿造,2023,42(3):58-64.
[15] 李潮云,卢君,冯海燕,等.酱香型白酒二轮次堆积酒醅酵母菌数量与理化指标变化分析[J].中国酿造,2024,43(2):48-52.
[16] 兰林,段树华,汪晟羽,等.基于高通量测序技术分析豆腐乳中微生物多样性[J].中国酿造,2023,42(1):31-36.
[17]段姿睿,杨絮,陈小娥,等.酒糟草鱼发酵过程中微生物菌群组成与挥发性风味物质及其相关性分析[J].食品科学,2025,46(14):111-123.
[18] 任爱容,黄永光.茅台镇不同主酿区域酱香型白酒酿造大曲中细菌菌群结构分析[J].食品科学,2021,42(4):167-174.
[19] 王佳丽,胥强,路程顺,等.芦台春酱香型白酒酿造过程中真菌菌群多样性及代谢分析[J].中国酿造,2024,43(4):45-52.
[20] 任海伟,李志娟,刘美琪,等.基于高通量测序技术分析不同窖龄窖泥真菌群落多样性与空间异质性[J].食品科学,2024,45(2):178-187.
[21] 唐丽,魏雯丽,赵雅娇,等.工业萝卜泡菜发酵过程中理化特性及真菌群落多样性分析[J].食品与发酵工业,2022,48(6):25-31.
[22] 文开勇,汪月,文鹏程,等.四川传统腊肉中微生物群落结构研究[J].食品与发酵工业,2020,46(3):36-42.
[23] ZHANG H X,WANG L,TAN Y W,et al.Effect of Pichia on shaping the fermentation microbial community of sauce-flavor Baijiu[J].Int J Food Microbiol,2021,336:108898.
[24] YANG L,XIAN C,LI P,et al.The spatio-temporal diversity and succession of microbial community and its environment driving factors during stacking fermentation of Maotai-flavor Baijiu[J]. Food Res Int,2023,169:112892.
[25] YANG L,CHEN R Y,LIU C,et al.Spatiotemporal accumulation differences of volatile compounds and bacteria metabolizing pickle like odor compounds during stacking fermentation of Maotai-flavor Baijiu[J].Food Chem,2023,426:136668.
[26] NIU J L,LI W W,DU B H,et al.Temporal heterogeneity of microbial communities and flavor metabolism during storage of high-temperatureDaqu[J].Food Chem,2024,464(1):141577.
[27] 唐佳代,刘力萍,龙亚飞,等.不同感官特性酱香大曲细菌群落结构与理化特性研究[J].中国酿造,2022,41(1):138-142.
[28] PERPETUINI G,ROSSETTI A P,BATTISTELLI N,et al.Contribution of Starmerella bacillaris and oak chips to Trebbiano d'Abruzzo wine volatile and sensory diversity[J].Foods,2023,12(5):1102.
[29] CSOMA H,KÁLLAI Z,CZENTYE K,et al.A yeast that has adapted to the conditions in the oenological environment[J]. Int J Food Microbiol,2023,401:110282.
[30] CAI W C,XUE Y A,WANG Y R,et al.The fungal communities and flavor profiles in different types of high-temperature daqu as revealed by high-throughput sequencing and electronic senses[J].Front Microbiol,2021,12:784651.
[31] 陈博超.北方酱酒第五轮次细菌群落解析与功能研究[D].天津:天津科技大学,2023.
[32] 黎瑶依,胡小霞,黄永光.茅台镇酱香型白酒酿造环境中真菌菌群多样性分析[J].食品科学,2021,42(18):164-170.
[33] GUAN T,WU X,HOU R,et al.Application of Clostridium butyricum,Rummeliibacillus suwonensis,and Issatchenkia orientalis for nongxiangxing Baijiu fermentation: improves the microbial communities and flavor of upper fermented grain[J].Food Res Int,2023,169:112885.
[34] XU S S,ZHOU H,XU B Y,et al.Environmental microbiota and its influence on microbial succession and metabolic profiles in Baijiu fermentation across three distinct-age workshops[J].LWT-Food Sci Technol,2024,201:116262.