红酸汤是贵州独有的民族调味品,以番茄与辣椒为主要原料,经清洗、破碎后配以食盐、生姜、大蒜等辅料,经30~90 d自然发酵制成[1]。成品色泽红亮,酸辣协调,富含类胡萝卜素、有机酸等活性成分,具有抗氧化、增强免疫力等功效,广受消费者欢迎[2]。红酸汤品质与独特的微生物菌群密切相关,其中乳酸杆菌属(Lactobacillus)与毕赤酵母属(Pichia)为发酵体系中的核心菌群。在发酵初期乳酸菌占比达94.81%,后期酵母菌逐渐成为主导菌群[3-4]。陆敏等[1]研究表明,乳杆菌科(Lactobacillaceae)、酵母科(Saccharomycodaceae)、链球菌科(Streptococcaceae)与红酸汤中可溶性固形物、总酸、氨基酸态氮等理化指标呈显著正相关(P<0.05);且植物乳植杆菌(Lactiplantibacillus plantarum)、耐酸乳杆菌(Lactobacillus acetotolerans)、膜醭毕赤酵母(Pichia membranaefaciens)等特定菌株可通过代谢合成有机酸、酯类、醇类等代谢产物,共同塑造红酸汤的特征风味轮廓[5]。
鉴于微生物对红酸汤品质形成的关键作用,可以品质优良的红酸汤作为菌株来源。目前,主成分分析(principal component analysis,PCA)、熵值法(entropy weight method,EWM)、层次分析法(analytic hierarchy process,AHP)等为主要的食品品质综合评价方法。主成分分析通过降维提取主要信息,但其结果高度依赖数据分布,且难以获得具体分析指标的权重;熵值法基于数据离散程度客观赋权,却忽略了指标的实际专业意义[6]。相比之下,AHP通过构建层次模型和两两比较,能够有效整合专业知识与客观数据,已成功应用于灰枣、胡柚等多种传统食品的评价,其一致性检验机制能确保权重分配的科学性,适用于红酸汤多属性、多层次的品质评价需求[7-8]。然而,AHP法在红酸汤领域的应用报道较少,且现有菌株筛选研究多基于自制样品,存在菌源单一、未与样品综合品质系统关联等问题[9-10]。
基于此,本研究以9个贵州不同地区红酸汤样品(编号为QB、QX1、QX2、QZ、QDN1~QDN5)为研究对象,通过分析其感官品质、理化指标及活性成分,结合AHP构建综合评价体系,筛选优质红酸汤样品。结合传统分离法,发酵性能、耐受性及安全性试验,从中分离筛选性能优良乳酸菌,结合形态学观察与分子生物学技术鉴定菌种,并将其应用于红酸汤进行发酵验证实验,考察菌株对产品品质风味的影响。旨在完善红酸汤品质评价体系,并为红酸汤直投式菌剂的开发提供优良菌种资源。
1 材料与方法
1.1 材料与试剂
9个贵州不同地区红酸汤样品,分别为黔北(QB)、黔西(QX1、QX2)、黔中(QZ)、黔东南(QDN1~QDN5):市售。
MRS肉汤培养基、MRS固体培养基:上海博微生物科技有限公司;苹果酸、琥珀酸、柠檬酸、乙酸、乳酸、酒石酸、草酸标准品(纯度均>98%):北京索莱宝科技有限公司;番茄红素、α-胡萝卜素、β-胡萝卜素、叶黄素标准品(纯度均>98%):上海希格玛高技术有限公司;抗生素药敏纸片:杭州微生物试剂有限公司;甲醇、磷酸二氢钾、甲基叔丁基醚(均为色谱纯)、3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)(分析纯):上海麦克林生化科技有限公司;其他试剂均为国产分析纯。
1.2 仪器与设备
SHP-250智能生化培养箱:上海光都仪器设备有限公司;PHS-3C雷磁pH计:上海仪电科学仪器股份有限公司;HP-TD32数字折光仪:深圳市测友科技有限公司;UV-5200PC紫外可见分光光度计:上海仪电分析仪器有限公司;1260Infinty高效液相色谱(high performance liquid chromatography,HPLC)仪、ZORBAX SB-AQ色谱柱(4.6 mm×250 mm,5 μm):安捷伦科技(中国)有限公司;U3000超高效液相色谱仪、Thermal Cycler2720聚合酶链式反应(polymerase chain reaction,PCR)仪:赛默飞世尔科技公司;Carotenoid S色谱柱(150 mm×4.6 mm,3 μm):日本YMC株式会社;RJ-TGL-1850R台式高速冷冻离心机:无锡市瑞江分析仪器有限公司;PEN3电子鼻:德国Airsense公司。
1.3 方法
1.3.1 感官评价
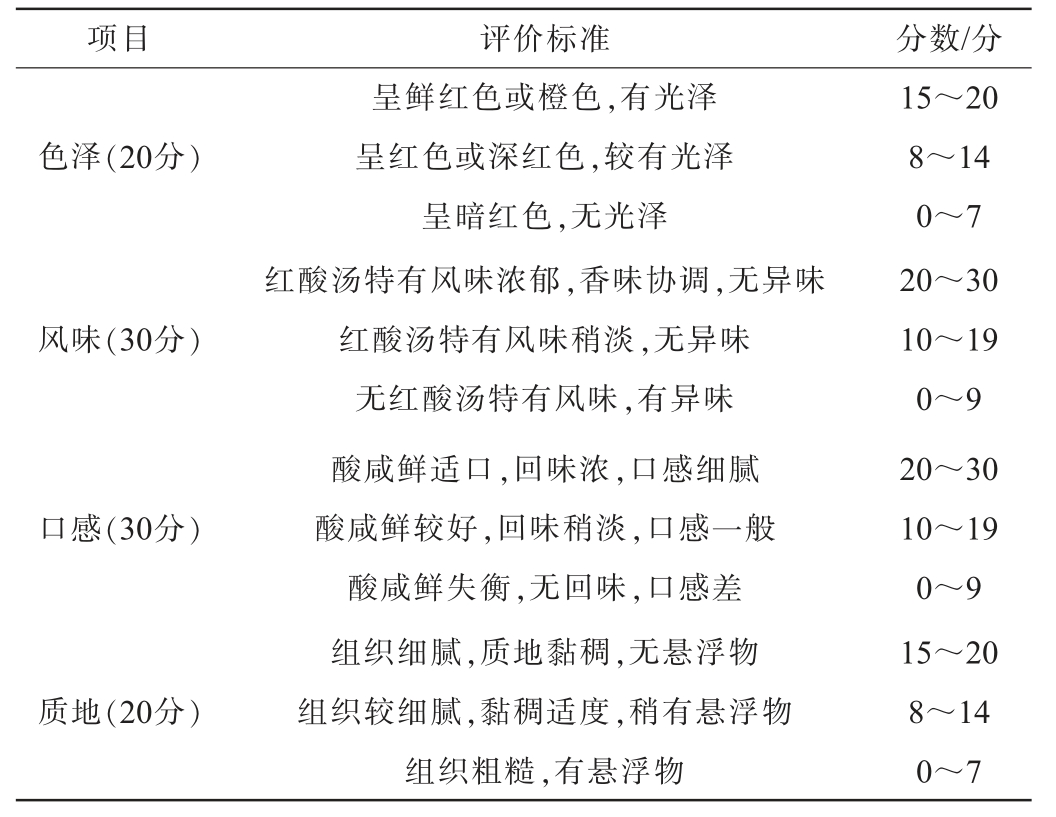
由10名经过感官培训的评价人员,参考红酸汤地方标准DB52/T 986—2015《地理标志产品凯里红酸汤》对红酸汤进行感官评价,分别从色泽、风味、口感及质地4个方面进行感官评价,满分100分,红酸汤感官评分标准见表1。
表1 红酸汤感官评分标准
Table 1 Sensory score standards of red sour soup
1.3.2 理化指标检测
pH值测定:采用pH计;可溶性固形物含量测定:采用手持折光仪;总酸含量测定:参照GB/T12456—2021《食品安全国家标准 食品中总酸的测定》;氨基酸态氮含量测定:参照GB 5009.235—2016《食品中氨基酸态氮测定》;还原糖含量测定:采用DNS比色法[11]。
1.3.3 活性成分测定
有机酸:采用高效液相色谱法测定有机酸含量。取样品2.5 g,加入0.1 g的活性炭,定容至25 mL,4 ℃、8 000 r/min离心10 min,上清液经0.22 μm水系滤膜过滤,待测。色谱条件:ZORBAX SB-AQ色谱柱(4.6 mm×250 mm,5 μm);流动相为甲醇:0.02 mol/L磷酸二氢钾溶液(5∶95,V/V);流速0.8 mL/min;柱温35 ℃;检测波长210 nm;进样量10 μL。以保留时间定性,外标法定量。
类胡萝卜素:采用超高效液相色谱法测定类胡萝卜素含量。将0.5 g样品与2 mL无水乙醇(含0.1%2,6-二叔丁基对甲酚)涡旋混匀,80 ℃水浴5 min后加入100 μL 80%氢氧化钾溶液,再80 ℃水浴15 min,之后加入1 mL纯化水和1 mL正己烷涡旋混匀,3 000 r/min离心5 min取上清液,残渣再用1 mL正己烷重复提取一次。合并2次上清液,30 ℃氮吹至干后0.2 mL甲醇复溶。色谱条件:Carotenoid S色谱柱(150 mm×4.6 mm,3 μm);流动相A相为甲醇,流动相B为甲醇∶甲基叔丁基醚∶水(20∶75∶5,V/V);梯度洗脱程序为0 min,100%A;15 min,39%A;25 min,0%A;25.1~30.0 min,100%A;柱温40 ℃;检测波长450 nm;流速1.0 mL/min;进样量2 μL;二极管阵列检测器(diode array detector,DAD)。以保留时间定性,外标法定量。
1.3.4 基于AHP的红酸汤品质评价
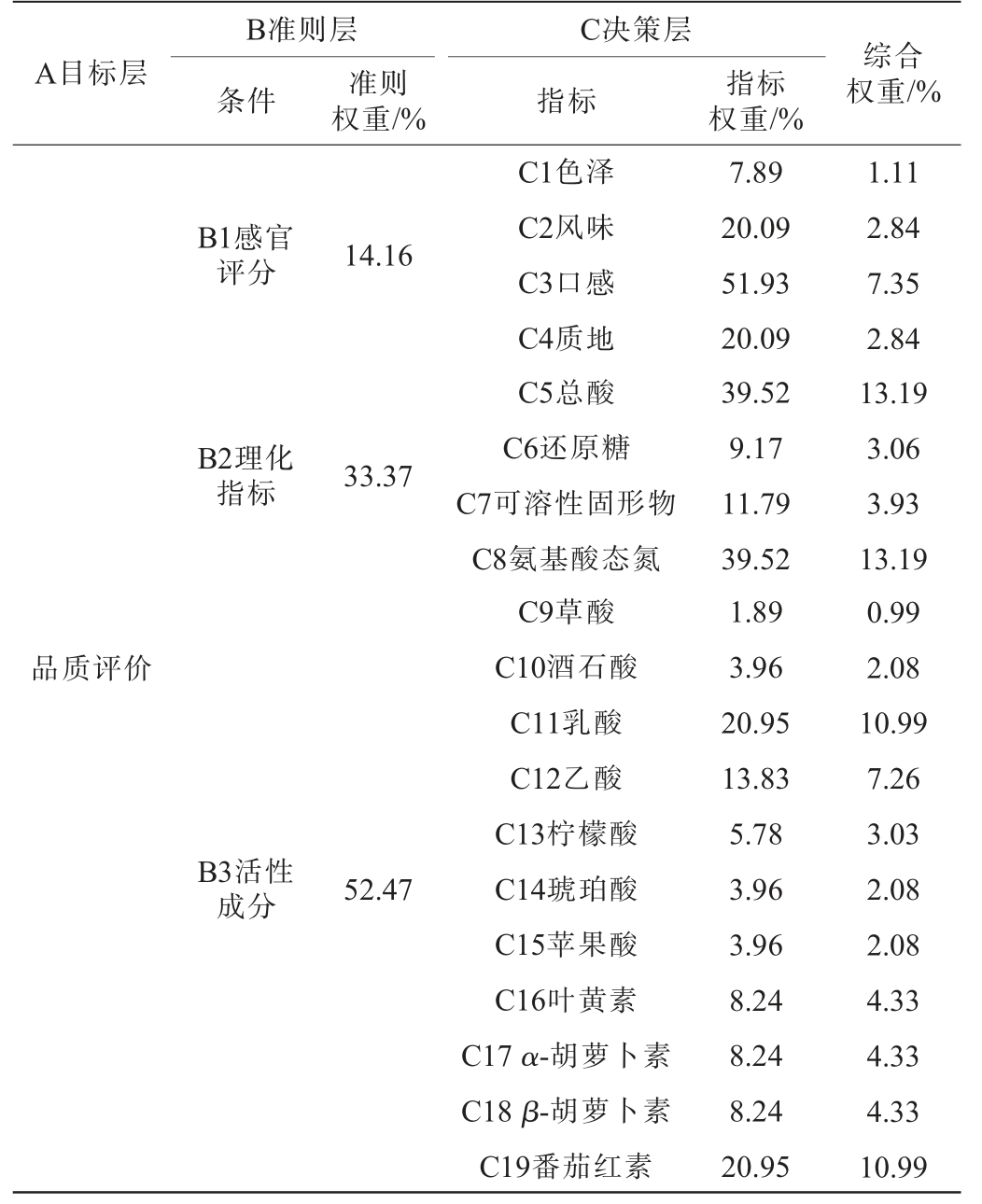
采用AHP构建红酸汤品质多维度评价体系[12],将所测的19个指标分为目标层(拟解决的问题),准则层(解决该问题需要考虑的指标),决策层(准则层的具体评价指标),即红酸汤品质评价为目标层A;将感官评分、理化指标与活性成分作为准则层B;将色泽、风味、口感、质地、总酸、还原糖、可溶性固形物、氨基酸态氮、草酸、酒石酸、乳酸、乙酸、柠檬酸、琥珀酸、苹果酸、叶黄素、α-胡萝卜素、β-胡萝卜素及番茄红素共19个指标,列为决策层C。基于DB52/T 986—2015《地理标志产品 凯里红酸汤》和T/KLST 001—2021《凯里酸汤 红酸汤》,采用1~9标度法(即指标间相对重要性以1~9的整数表示)对各层级指标进行两两比较,构建判断矩阵,对原始数据进行标准化处理后,结合综合权重(表2)计算得出红酸汤综合品质得分。
表2 基于层次分析法的红酸汤样品品质评价指标权重
Table 2 Weighting of quality evaluation indicators for red sour soup samples based on analytic hierarchy process
利用方根法计算各判断矩阵的权重W,其计算公式如下:

式(1)中:Wi 为第i个指标的权重;n为指标个数(即判断矩阵阶数);aij为指标i相对于指标j的重要性标度;k为行内连乘变量,用于区分求和下标j。
之后,进行一致性检验,一致性比率(consistency ratio,CR)<0.1表明判断逻辑一致,权重结果可信。其计算公式如下:

式(2)中:CR为一致性比率;A为判断矩阵;(AW)i为判断矩阵A与权重W乘积的第i个分量;RI为同阶平均随机一致性指标。
各指标的综合权重为其准则层权重与决策层权重的乘积[13],其计算公式如下:
式(3)中:W综为任一指标的综合权重;WB为该指标所属准则层的权重,WC为该指标在其所属决策层内的权重。
1.3.5 乳酸菌菌株分离、纯化
将红酸汤样品用无菌生理盐水按10倍梯度稀释至10-7,取各梯度稀释液100 μL,涂布于MRS固体培养基上,37 ℃培养24 h。挑取圆形、表面光滑、呈乳白色的菌落分离纯化3次,对其进行革兰氏染色和接触酶试验,挑选革兰氏阳性和接触酶阴性菌株。
1.3.6 优良乳酸菌菌株的筛选
发酵性能测定:挑取分离纯化后的乳酸菌单菌落,接种至装液量为30mL/100mLMRS液体培养基,于37℃、150r/min摇床振荡培养24 h,制得乳酸菌种子液备用。将菌株种子液按5%(V/V)接种量接种至MRS肉汤培养基中,37 ℃摇瓶发酵36 h后测定发酵液pH值与乳酸含量。
耐受性能测定:将菌株种子液以5%(V/V)接种量接种到不同pH(2.0、2.5、3.0、3.5、4.0)、不 同NaCl含 量(6%、8%、10%、12%、14%)的MRS肉汤培养基中,37 ℃培养48 h,测定菌株培养前后的OD480nm值,计算ΔOD480nm值(ΔOD480nm值=培养后OD480nm值-培养前OD480nm值),判定菌株的耐酸与耐盐性能。
安全性能测定:参考徐兆娜[14]的方法进行硫化氢、吲哚、硝酸盐还原与明胶液化试验。采用纸片扩散法[15]检测菌株对8种常见抗生素(红霉素、诺氟沙星、环丙沙星、庆大霉素、丁胺卡那、氯霉素、氨苄西林、头孢唑啉)的敏感性,根据美国临床和实验室标准协会(Clinical Laboratory Standards Institute,CLSI)标准[16]与试剂盒推荐标准进行判定。
1.3.7 优良乳酸菌菌株鉴定
形态学观察:将筛选的菌株划线接种于MRS固体培养基,37 ℃培养24 h,观察菌落的外观、大小、颜色、边缘形状及表面干湿状态等菌落形态特征。革兰氏染色液将其染色后采用显微镜观察其细胞形态。
分子生物学鉴定:用细菌基因组提取试剂盒提取基因组脱氧核糖核酸(deoxyribonucleic acid,DNA),以此为模板,采用细菌通用上游引物27F(5'-AGTTTGATCMTGGCTCAG-3')、下游引物1492R(5'-GGTTACCTTGTTACGACTT-3')进行菌株16S rDNA基因片段扩增。PCR扩增体系(25 μL):5 μL DNA模板(50 ng/μL);0.75 μL上游引物(10μmol/L);0.75μL下游引物(10 μmol/L);12.5 μL2×ASFast Direct PCR Mix;6 μL双蒸水(ddH2O)。PCR扩增程序:95 ℃预变性5 min;98 ℃变性10 s,56 ℃退火30 s,68 ℃延伸90 s,共38个循环;68 ℃再延伸10 min。PCR产物送往青岛睿博兴科生物技术有限公司进行测序,测序结果提交至美国国家生物技术信息中心(national center for biotechnology information,NCBI)的GenBank数据库中进行基本局部比对搜索工具(basic local alignment search tool,BLAST)比对,选择同源性较高的相关序列使用MEGA X软件来构建菌株的系统发育树。
1.3.8 优良乳酸菌菌株制备红酸汤验证实验
(1)红酸汤的制备
按辣椒与番茄质量比为1∶2称量,洗净沥干后破碎,加入5%食盐、2%生姜、1%大蒜及1%白酒,充分混合均匀。强化发酵组按总接种量3%(V/V)接入菌株L1与L9菌液,其中菌株L1、L9菌液接种量各为1.5%(V/V);自然发酵组不接种外源菌株。2个组别均于35 ℃恒温发酵15 d。发酵结束后,测定其感官评分、理化指标及活性成分,并按照1.3.4构建的AHP综合评价模型进行品质综合评分。
(2)电子鼻检测
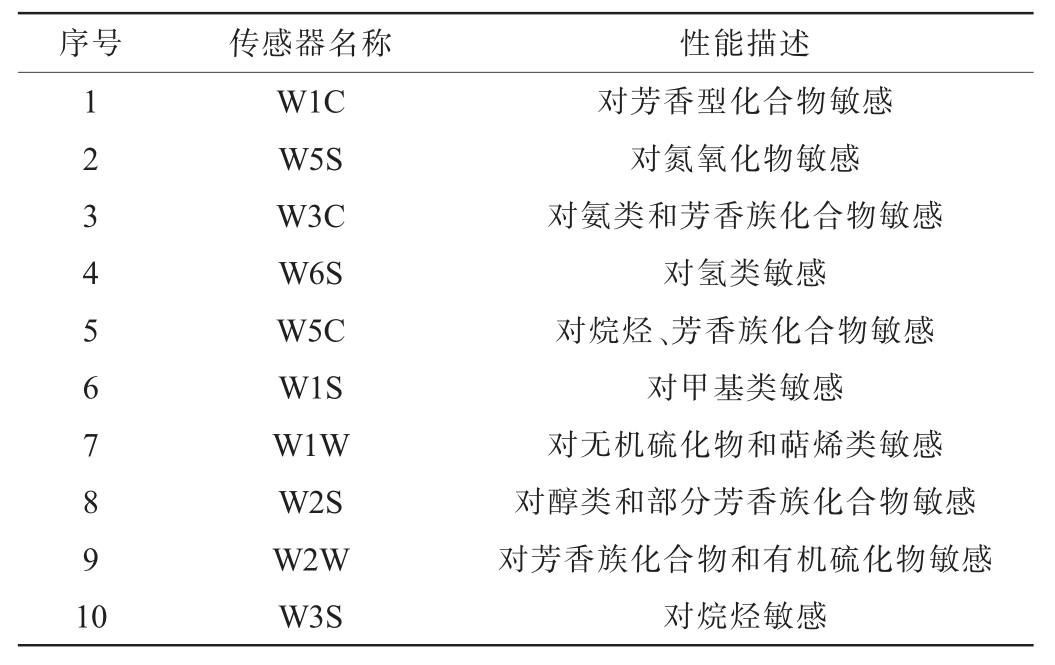
采用电子鼻分析红酸汤的挥发性风味物质,准确量取10 mL红酸汤样品置于20 mL顶空瓶中,密封室温平衡15 min后插入电子鼻探头测定红酸汤挥发性风味物质。电子鼻检测条件:检测时间60 s;清洗时间5 s;预进样时间60 s;进样流量300 mL/min;载气流速300 mL/min。电子鼻传感器性能描述见表3。
表3 电子鼻传感器名称与性能描述
Table 3 Name and performance descriptions of electronic nose sensor
1.3.9 数据处理及分析
采用软件IBM SPSS Statistics 26、Origin 2024和Excel 2019进行数据统计分析及综合评价计算,每个指标均平行测量3次,结果以“平均值±标准偏差”表示。
2 结果与分析
2.1 红酸汤品质分析
2.1.1 感官评价
红酸汤样品的感官评分见图1。由图1可知,样品QDN4与QX1色泽得分较高(分别为18.9分、17.9分),呈鲜亮红色,有光泽。样品QB风味与口感得分(分别为28.7分、27.6分)高于其他样品,酸香浓郁、回味悠长。样品QB、QX1与QDN2质地得分均>18分,组织均一致密,质地黏稠,而样品QX2、QDN4与QDN5质地评分较低。综上,样品QB在风味、口感与质地方面表现最优,感官评分最高(89.6分);样品QDN2与QX1感官评分次之(分别为89.1分、85.8分)。
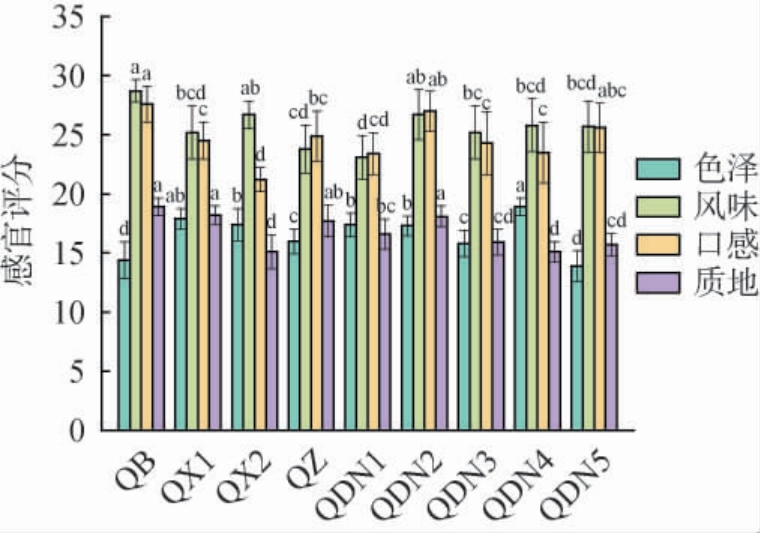
图1 红酸汤样品的感官评分
Fig.1 Sensory score of red sour soup samples
不同小写字母表示差异显著(P<0.05)。下同。
2.1.2 理化指标检测结果
红酸汤样品理化指标检测结果见图2。总酸是评价红酸汤酸度与风味的重要指标,其积累过程与微生物介导的淀粉、纤维分解及有机酸代谢过程密切相关[17]。由图2a可知,9个样品总酸含量为0.77%~3.65%。其中,样品QDN3的总酸含量最高(3.65%),样品QZ、QB与QX1的总酸含量为2.51%~2.85%,而样品QDN1的总酸含量(0.77%)最低。这种差异可能源于不同样品间微生物群落结构及代谢功能的特异性。氨基酸态氮作为红酸汤鲜味的主要呈味物质,其生成依赖于微生物对原料蛋白质的水解作用[18]。样品QDN2与QDN5的氨基酸态氮含量较高,分别为0.29 g/100 g、0.28 g/100 g,表明其发酵体系中的蛋白质水解与氨基酸积累过程可能更为高效;样品QB、QDN3、QDN4的氨基酸态氮含量较高(0.21~0.26 g/100 g),而QDN1的含量最低,为0.16 g/100 g。
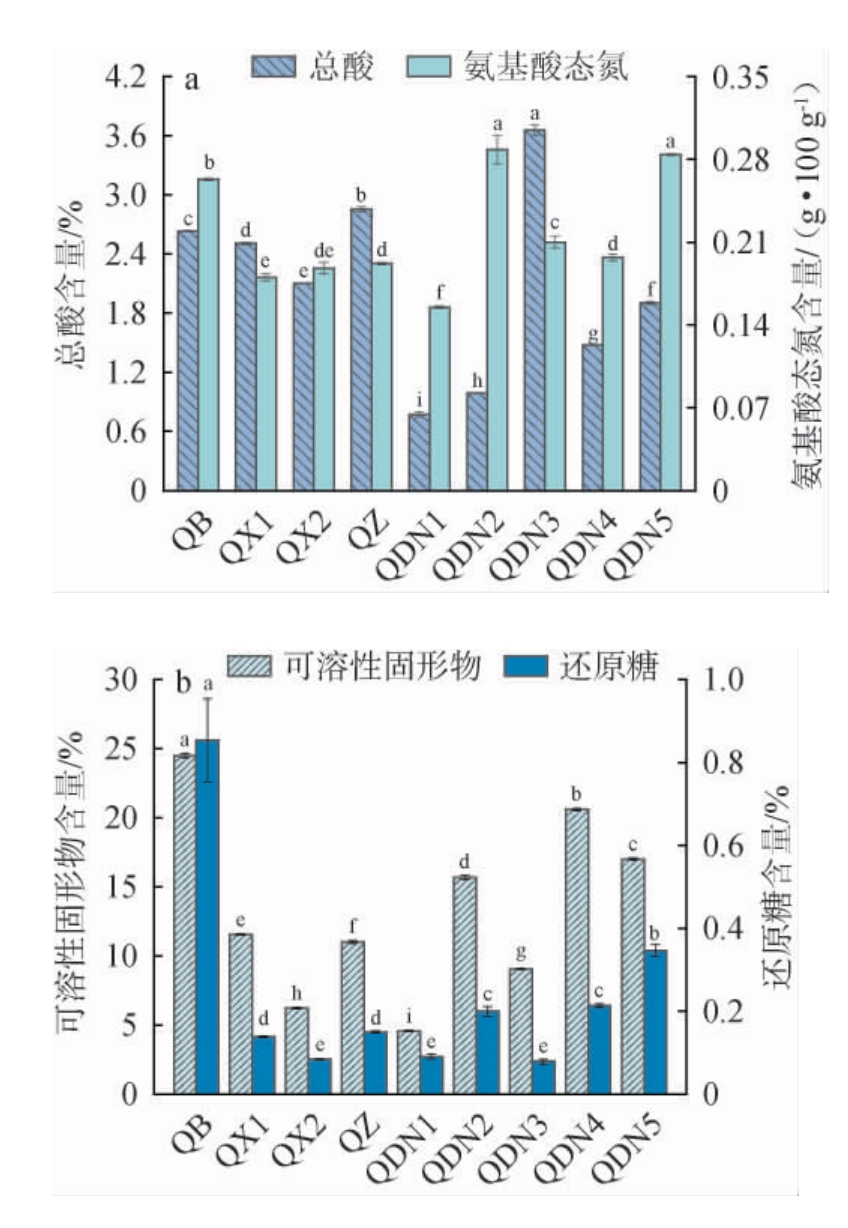
图2 红酸汤样品理化指标检测结果
Fig.2 Detection results of physicochemical indexes of red sour soup samples
由图2b可知,9个样品红酸汤的可溶性固形物含量为4.57%~24.50%,还原糖含量为0.08%~0.85%。样品QB的可溶性固形物(24.50%)、还原糖(0.85%)含量最高,这与其感官评价中质地均一、黏稠适度的结果相符,表明高固形物含量有助于形成饱满协调的质地结构。样品QDN4(20.60%)、QDN5(17.00%)、QDN2(15.67%)的可溶性固形物含量较高,而剩余样品含量均<12%,且样品QDN1的可溶性固形物含量最低(4.57%)。还原糖含量则由原料初始糖分与发酵过程中的微生物消耗动态平衡所决定[19]。样品QDN2、QDN4与QDN5的还原糖含量为0.20%~0.35%,而样品QX2的还原糖含量最低(0.08%)。较高还原糖含量通常与原料含糖量丰富或发酵过程中糖消耗程度较低有关,其在体系中可为红酸汤提供适度的甜味基调,有助于形成更协调的风味轮廓。
2.1.3 有机酸含量检测结果
红酸汤样品的有机酸含量检测结果见图3。由图3可知,所有样品均检出草酸、乳酸、乙酸与苹果酸;酒石酸仅于样品QDN2、QDN4与QDN5中检出,而样品QDN3未检出琥珀酸。不同样品总有机酸含量为16.97~93.24 g/kg,其在样品QB中含量最高,其在样品QDN1中含量最低。乳酸、琥珀酸与乙酸在红酸汤样品中含量较高。乳酸含量(5.46~28.16g/kg)整体高于潘季红等[20]报道的结果5.07~11.50 g/kg,且在样品QX2、QZ、QDN1等多个样品中含量最高,表明乳酸是红酸汤酸味体系的核心成分之一。乙酸作为重要的挥发性酸,其含量为1.87~18.26 g/kg,在样品QDN2(18.26 g/kg)和QDN3(7.81 g/kg)中含量较高,贡献了特征的刺激性酸香[11]。琥珀酸在样品QB中含量高达63.26 g/kg,显著高于其他样品(P<0.05)及文献报道的泡菜、盐酸菜等常见发酵食品[21],其在样品QX2、QDN2和QX1中含量亦较高(12.15~15.06 g/kg)。因此,乳酸、乙酸与琥珀酸是构成红酸汤特征酸味与功能性质的关键有机酸,其含量与组成差异直接影响样品的整体风味。
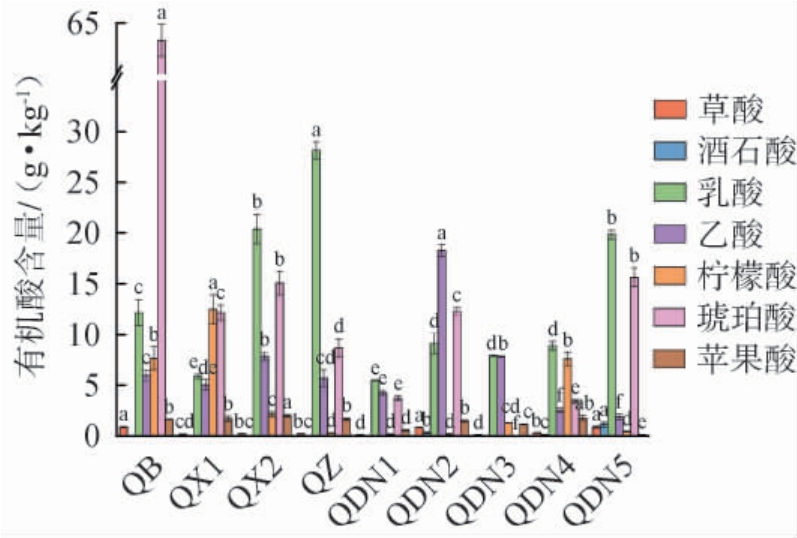
图3 红酸汤样品的有机酸含量检测结果
Fig.3 Detection results of organic acid contents in red sour soup samples
2.1.4 类胡萝卜素含量检测结果
类胡萝卜素作为红酸汤的关键活性物质,在色泽形成、香气与风味塑造中具有重要作用[22]。红酸汤样品的类胡萝卜素含量检测结果见图4。由图4可知,9个红酸汤样品共检出4种类胡萝卜素,包括叶黄素、α-胡萝卜素、β-胡萝卜素、番茄红素。类胡萝卜素总含量为0.17~3.86 μg/g,其中番茄红素与β-胡萝卜素含量较高。样品QX1、QX2、QZ、QDN1~QDN4中番茄红素含量丰富,其含量范围为0.13~3.56 μg/g。样品QDN4中番茄红素最高,高达3.56 μg/g,高于周艳等[23]所报道的自然发酵红酸汤中的番茄红素含量(2.96 μg/g),其在样品QX1(3.07 μg/g)与QDN2(2.75 μg/g)中含量次之;其含量差异可能与微生物代谢及番茄红素在低pH环境中降解及构型转变有关[24]。β-胡萝卜素在所有样品中均有检出(0.02~0.73 μg/g),以样品QX1含量最高,该物质作为维生素A前体与视觉健康密切相关[25]。样品QB未检出α-胡萝卜素,而叶黄素含量(0.28 μg/g)显著高于其他样品(P<0.05)。
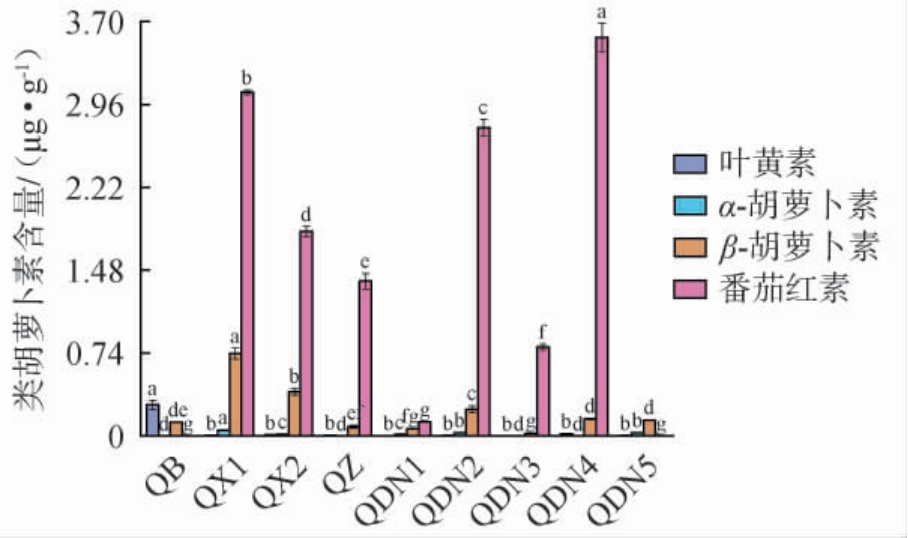
图4 红酸汤样品的类胡萝卜素含量检测结果
Fig.4 Detection results of carotenoid contents in red sour soup samples
2.1.5 基于AHP的红酸汤品质综合评价
根据以上检测结果,通过AHP法构建红酸汤品质综合评价体系,红酸汤样品的品质综合得分见表4。
表4 红酸汤样品的品质综合得分
Table 4 Overall quality score of the red sour soup samples
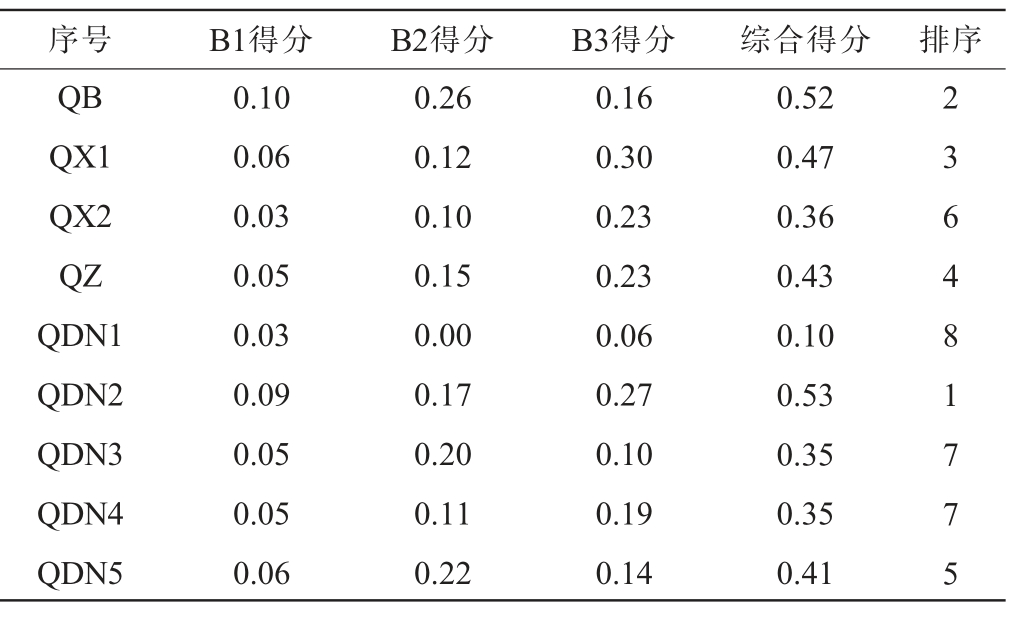
由表4可知,样品QDN2的品质综合得分排名第1(0.53分),其感官评分、氨基酸态氮、乙酸、番茄红素等含量较高。样品QB综合得分排名次之(0.52分),可溶性固形物、还原糖、有机酸含量等高于其余样品。样品QX1综合得分排名第3(0.47分),其富含类胡萝卜素。而样品QDN1的总酸、还原糖、有机酸与类胡萝卜素含量较低,导致其综合得分最低。因此,以样品QDN2、QB和QX1为菌株筛选来源。
2.2 优良乳酸菌菌株的分离及筛选
2.2.1 菌株分离及初筛
以红酸汤样品为分离源,采用梯度稀释涂布平板法进行乳酸菌的分离。经培养后,共获得23株形态符合乳酸菌典型特征(呈白色或乳白色、表面光滑、边缘整齐、圆形隆起)的菌株。进一步通过生理生化试验,初步筛选出9株革兰氏阳性与接触酶阴性的乳酸菌候选株,依次编号为L1~L9。其中,菌株L1~L4、L5~L6、L7~L9分别从QDN2、QB与QX1中筛选出来。
2.2.2 发酵性能
乳酸作为红酸汤中的特征成分,其柔和爽口的味感特征直接影响产品的风味,其与pH值是指示发酵进程中微生物代谢活动的关键参数[26]。乳酸菌的发酵性能检测结果见图5。由图5可知,初筛菌株的乳酸产量与pH具有明显差异,且两者呈负相关关系。菌株L1和L9的乳酸产量较高,分别达12.04 g/kg和11.40 g/kg,相应发酵液pH值较低(分别为4.41和4.44),其产乳酸能力优于胡悦等[27]从分料发酵红酸汤中筛选出的2株优良乳酸菌(7.41 g/kg、7.92 g/kg)。菌株L2、L3、L5与L7的乳酸产量为9.14~10.22 g/kg,对应pH值在4.59~4.65之间,而菌株L4、L6和L8的乳酸产量较低(6.31~8.95 g/kg),pH值较高(4.73~5.19)。上述差异主要源于菌株的遗传特性及其在酸胁迫下的代谢调控能力,基因与代谢通路的多样性可导致相同培养条件下产酸表现的分化[28]。综上,选择菌株L1~L3、L5、L7和L9进行后续实验。
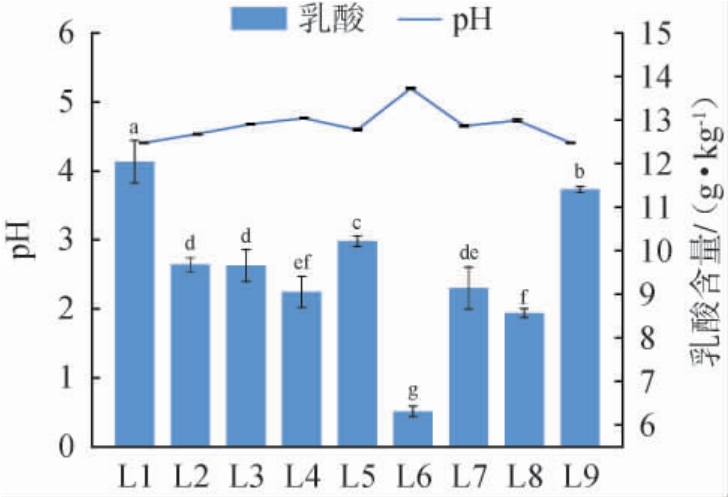
图5 乳酸菌的发酵性能检测结果
Fig.5 Detection results of fermentation performance of lactic acid bacteria
2.2.3 耐受性能
乳酸菌的pH与NaCl耐受能力检测结果见图6。由图6a可知,pH值为2~3时,菌株L1的ΔOD480nm值升高较快,由0.59升高至1.58,而其他5株菌株趋于平稳;当pH>3时,菌株L1的ΔOD480nm值升高转缓慢,菌株L3、L5、L9的ΔOD480nm值升高较快,而菌株L2、L7的ΔOD480nm值上升相对缓慢。因此,菌株L1耐酸性能较强,可耐受pH 2的酸性环境;而菌株L3、L5、L9的耐酸性能次之,可耐受pH 3.5~4.0的酸性环境。
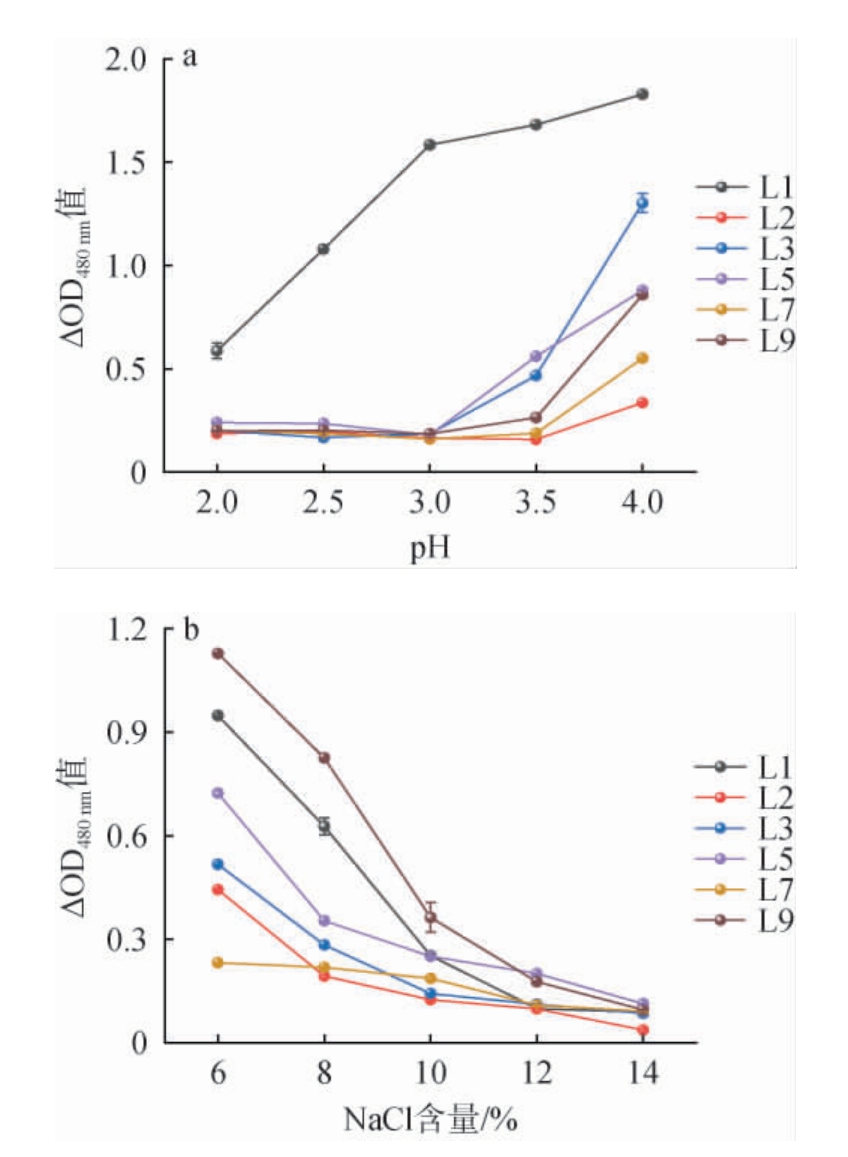
图6 乳酸菌的pH(a)与NaCl(b)耐受能力检测结果
Fig.6 Results of pH (a) and NaCl (b) tolerance capabilities of lactic acid bacteria
由图6b可知,NaCl含量为6%~10%时,菌株L1与L9的ΔOD480nm值下降最快,分别由0.95、1.13降低至0.25、0.36;菌株L2、L3、L5的ΔOD480nm值下降较快,而菌株L7的ΔOD480nm值下降相对平缓。当NaCl含量>10%时,菌株L1、L2、L5与L9的ΔOD480nm下降速度减缓,而菌株L3、L7的ΔOD480nm值逐渐趋于稳定。整体而言,菌株L1与L9的盐耐受能力较优,均可耐受10%NaCl。综上,选择菌株L1、L9进行安全性能评价。
2.2.4 安全性能评价
红酸汤在生产和储存时出现发黑、产气等现象,多因菌株发酵产硫化氢、吲哚等有害物质导致[14]。乳酸菌的安全性能检测结果见表5。由表5可知,2株乳酸菌均不产生硫化氢与吲哚,不还原硝酸盐,不水解明胶。
表5 乳酸菌的安全性能检测结果
Table 5 Safety performance detection results of lactic acid bacteria
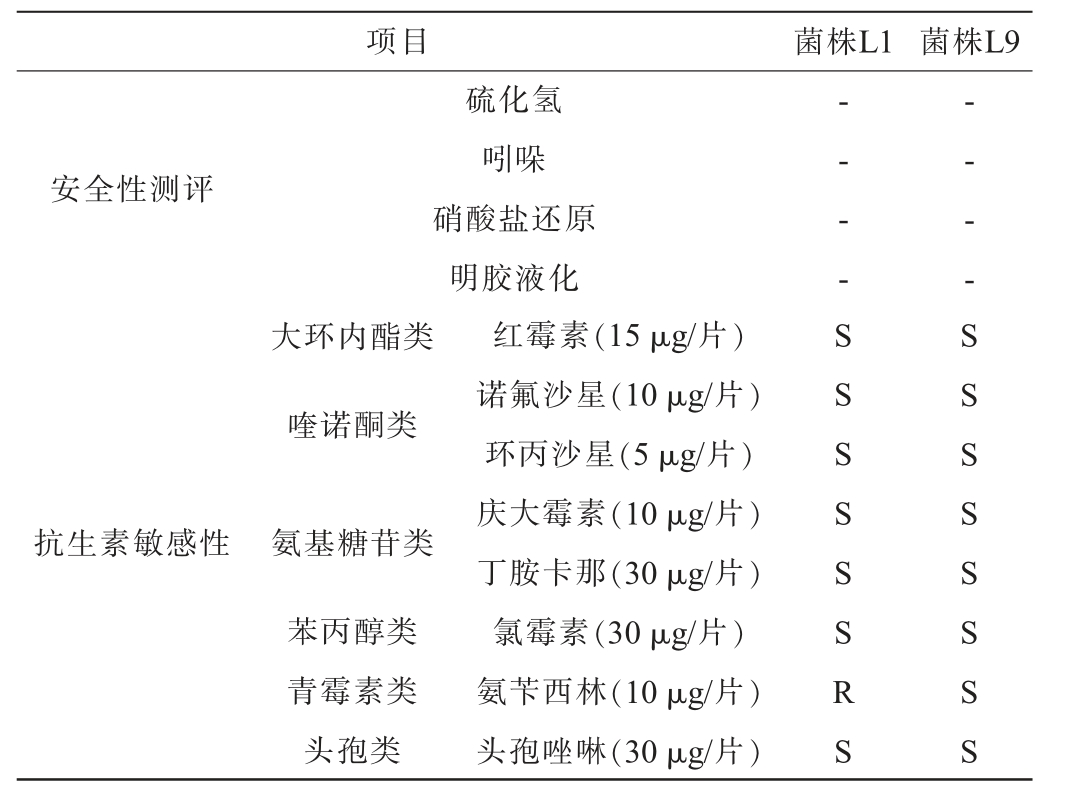
注:“+”表示90%以上菌株阳性,“-”表示90%以上菌株阴性;“R”为耐药,“S”为敏感。
乳酸菌的抗生素敏感性是关键安全评价指标,生产菌株应不携带可转移的耐药基因,以防耐药基因泛滥[29]。由表5可知,菌株L1、L9分别对7种、8种抗生素敏感,仅菌株L1表现出对青霉素类的氨苄西林耐药。菌株对青霉素的耐药性由染色体pbp基因突变介导,但pbp基因位于染色体上,故无转移风险[30]。
综上,菌株L1和L9耐受性能优良,且安全性符合要求,故用于后续生物学鉴定。
2.3 优良乳酸菌菌株的鉴定
2.3.1 形态学观察
菌株L1与L9的菌落与细胞形态见图7。由图7可知,菌株L1与L9于MRS培养基上形成乳白色,圆形光滑、质地湿润菌落,均为革兰氏阳性菌;菌株L1呈单在或成双的无芽胞无荚膜杆菌;菌株L9为成对或四联的球菌。
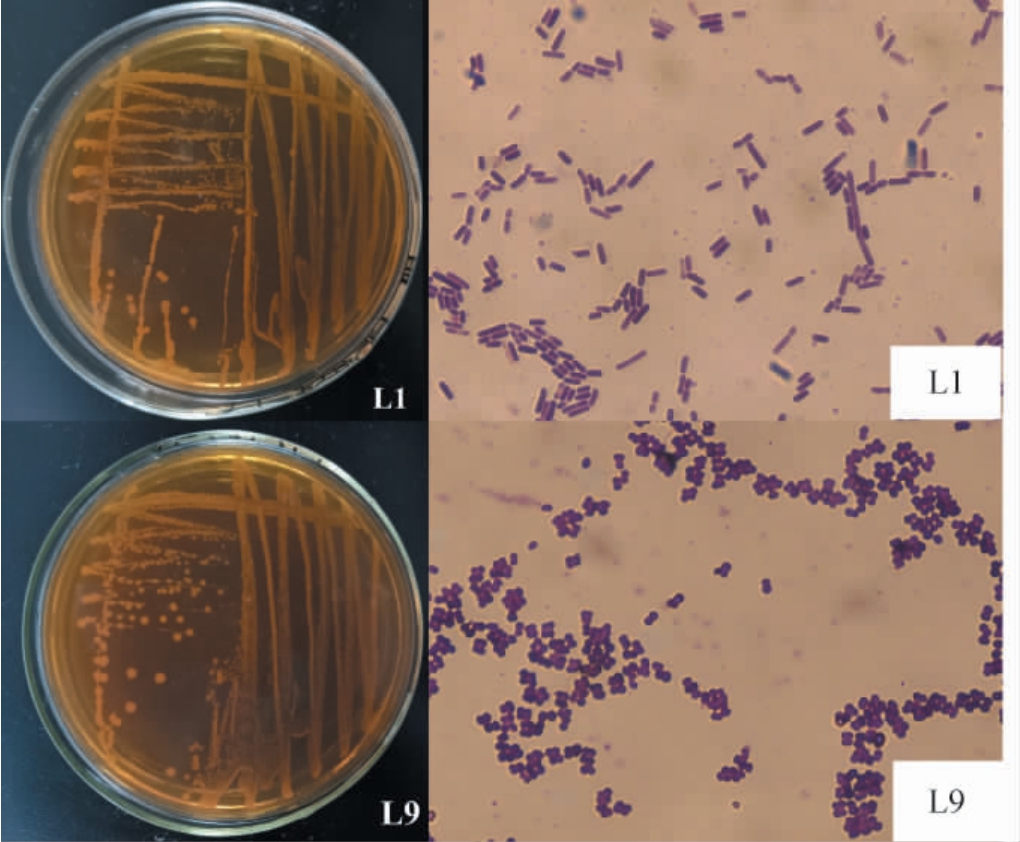
图7 优良乳酸菌菌株形态学特征
Fig.7 Morphological characteristics of excellent lactic acid bacteria strains
2.3.2 分子生物学鉴定
基于16SrDNA基因序列构建菌株L1、L9的系统发育树,结果见图8。由图8可知,菌株L1与Limosilactobacillusfermentum strain CIP 102980的同源性为100%,在系统发育树中聚于同一分枝,亲缘关系最近。菌株L9与Pediococcus ethanolidurans strain Z-9的序列同源性达到100%,聚于同一分枝,亲缘关系最近。结合形态学特征及分子生物学鉴定结果,最终将菌株L1鉴定为发酵粘液乳杆菌(Limosilactobacillus fermentum);菌株L9鉴定为耐乙醇片球菌(Pediococcus ethanolidurans)。

图8 基于16SrDNA基因序列构建菌株L1和L9的系统发育树
Fig.8 Phylogenetic tree of strains L1 and L9 based on 16S rDNA gene sequences
2.4 优良乳酸菌菌株制备红酸汤验证实验
2.4.1 品质综合评价
强化发酵使得乳酸菌快速成为体系的优势菌群,通过调控微生物群落演替直接影响产品风味与品质[19]。自然发酵与菌株L1、L9混合强化发酵红酸汤的感官评分、理化成分与活性成分检测结果见表6。
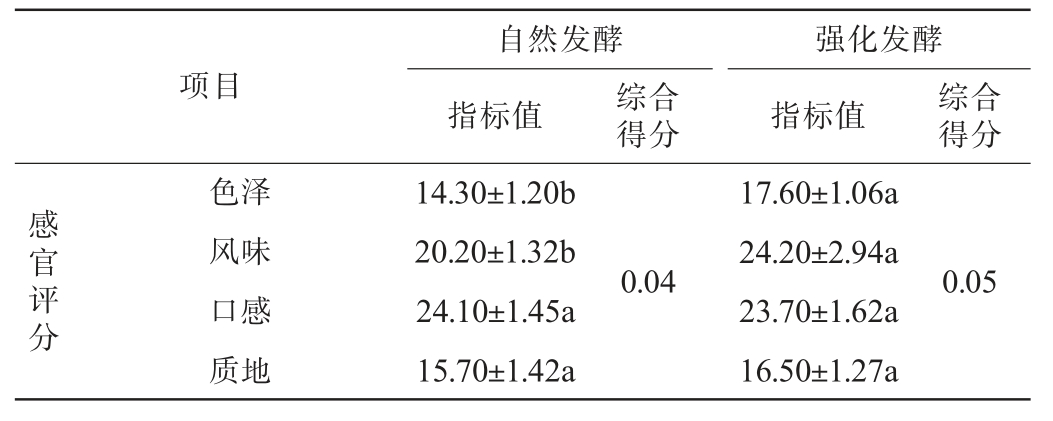
表6 自然发酵与强化发酵红酸汤的感官评分、理化指标与活性成分检测结果
Table 6 Detection results of sensory score,physicochemical indexes,and active compounds of natural fermented and fortified fermented red sour soup
续表
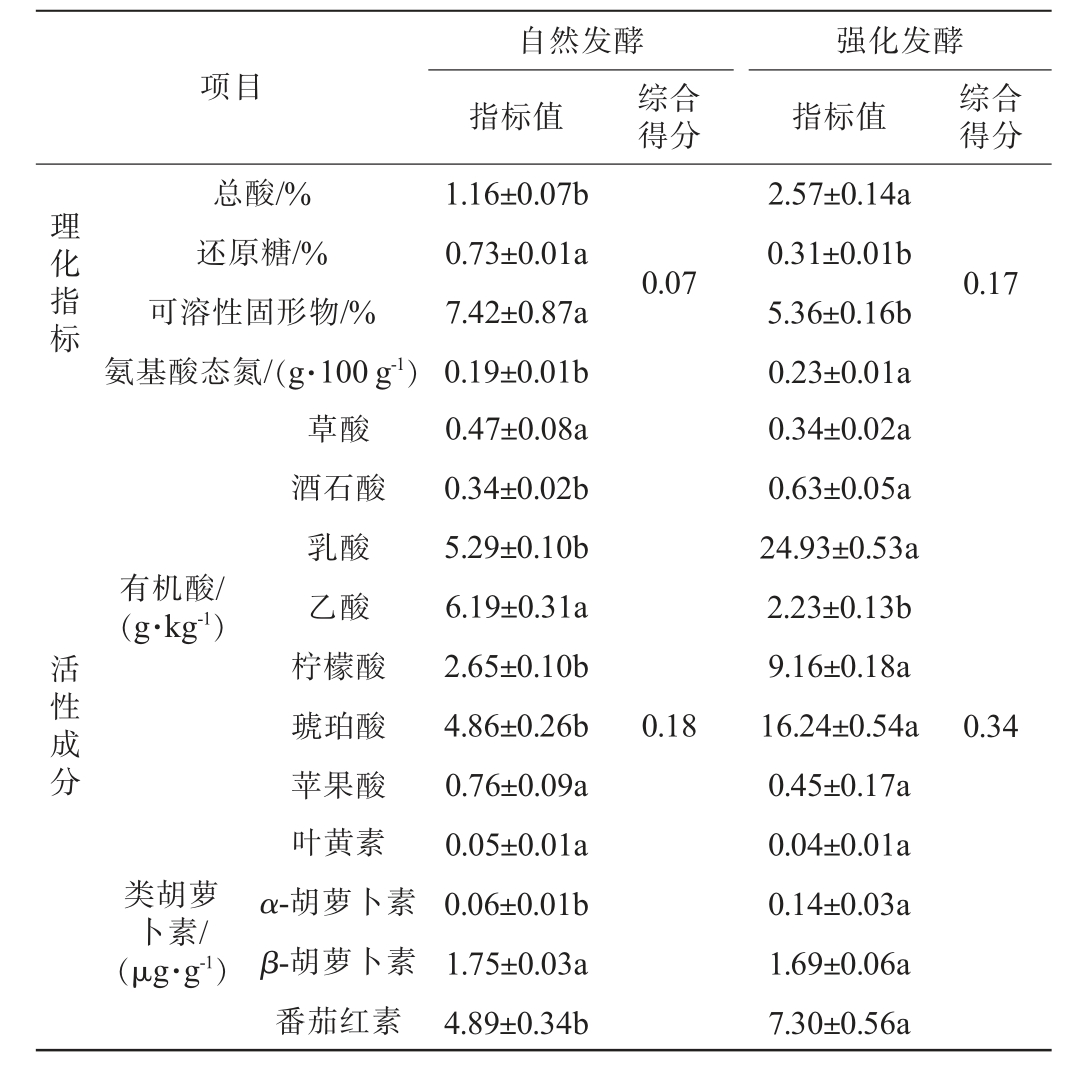
由表6可知,在感官评分方面,强化发酵组在色泽(17.6分)与风味(24.2分)方面表现更优。在理化指标方面,其总酸(2.57%)与氨基酸态氮(0.23 g/100 g)较自然发酵组分别提高了1.22倍、1.21倍。在活性成分方面,强化发酵组红酸汤的乳酸、柠檬酸与琥珀酸含量分别达到24.93 g/kg、9.16 g/kg和16.24 g/kg,为自然发酵组的4.17倍、3.46倍和3.34倍,表明筛选菌株具有优良的产酸能力。此外,番茄红素含量(7.30 μg/g)亦显著高于自然发酵组(P<0.05)。
基于前期构建的评价模型进行综合评分,强化发酵组在感官评分(0.05分)、理化指标(0.17分)与活性成分(0.34分)的得分均高于自然发酵组。因此,采用筛选菌株L1、L9进行混合强化发酵,不仅可大幅缩短生产周期,还能系统性提升红酸汤在感官、理化及活性成分方面的品质,使其整体水平达到市售优质产品品质。
2.4.2 电子鼻检测结果
为进一步揭示红酸汤的风味组成,采用电子鼻技术对其挥发性成分进行测定分析,其响应值雷达图见图9。
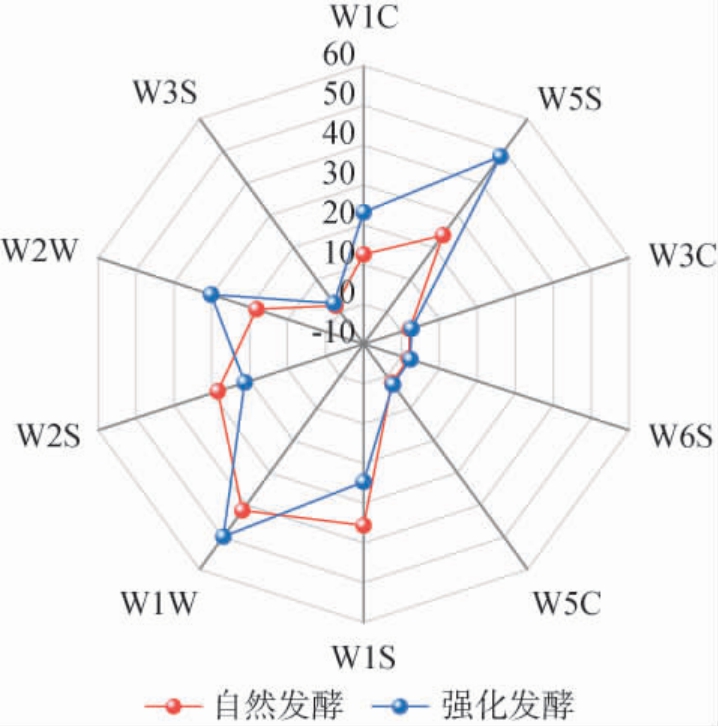
图9 自然发酵与强化发酵红酸汤电子鼻检测结果
Fig.9 Electronic nose detection results of natural fermented and fortified fermented red sour soup
由图9可知,W5S、W2W和W1W传感器在2组样品中响应较强,表明氮氧化物、硫化物及萜烯类化合物是红酸汤风味基础骨架。其中,硫化物是发酵食品中的主要挥发性风味物质,通常来源于大蒜、生姜等辅料[31]。强化发酵组W1C响应值(23.15)高于自然发酵组(12.56),表明醛类、醇类、酯类等典型香气化合物大幅增加,赋予产品更浓郁协调的香气。而W3C、W6S、W5C等传感器响应值无明显差异,表明氨类、烷烃等非主体风味成分占比稳定,该结果与杨进军等[32]研究一致。因此,乳酸菌强化发酵在维持红酸汤原有风味骨架的基础上,通过其优势代谢增强芳香型化合物的产生,定向优化产品的香气轮廓,系统改善产品综合品质。
3 结论
本研究以9个贵州不同地区红酸汤(编号为QB、QX1、QX2、QZ、QDN1~QDN5)为研究对象,通过层次分析法(AHP)筛选得到3个优质红酸汤样品QDN2、QB与QX1。其中样品QB可溶性固形物、还原糖及琥珀酸含量最高(分别为24.50%、0.85%、63.26 g/kg),样品QDN2氨基酸态氮和乙酸含量最高(分别为0.29 g/100 g、18.26 g/kg),样品QX1番茄红素含量较高(3.07 μg/g)。进一步从优质红酸汤样品中分离筛选出2株优良乳酸菌(L1与L9),经鉴定分别为发酵粘液乳杆菌(Limosilactobacillus fermentum)、耐乙醇片球菌(Pediococcus ethanolidurans),2株菌产酸含量高,乳酸产量分别达12.04 g/kg、11.40 g/kg;耐酸、耐盐性能较优;且分别对7种、8种常见抗生素敏感,安全性好。发酵验证实验结果显示,菌株L1与L9混合(1∶1)强化发酵红酸汤样品的综合得分(0.56分)高于自然发酵组(0.29分)。因此,本研究可为红酸汤品质评价体系构建提供参考,为红酸汤专用直投式菌剂的研发及工业化生产提供技术支撑。
[1] 陆敏,王雪雅,孙小静,等.贵州南部红酸汤理化指标与菌群结构的相关性分析[J].中国酿造,2023,42(9):109-114.
[2] HE Y B,LI Y F,LUO X B,et al.Effects of thermal and nonthermal processing technology on the quality of red sour soup after storage[J].Food Sci Nutr,2021,9(7):3863-3872.
[3] LI D F,DUAN F X,TIAN Q M,et al.Physiochemical,microbiological and flavor characteristics of traditional Chinese fermented food Kaili Red Sour Soup[J].LWT-Food Sci Technol,2021,142:110933.
[4] 何扬波,李国林,李咏富,等.红酸汤发酵过程中微生物区系及挥发性物质组成变化分析[J].食品工业科技,2022,43(19):177-190.
[5] LIU N,HU Y,QIN L K,et al.Flavor and quality characteristics of Guizhou red sour soup prepared by different artificially fortified fermentation methods[J].LWT-Food Sci Technol,2023,186:115247.
[6] 张霞,何南.综合评价方法分类及适用性研究[J].统计与决策,2022,38(6):31-36.
[7] 王欢欢,王晶晶,陈奇凌.3种数学方法在灰枣果实品质评价中的应用[J].中国农学通报,2025,41(7):138-144.
[8] 张慧艺,汪丽霞,吴伊静,等.18份胡柚种质果实品质分析与综合评价[J].果树学报,2024,41(6):1033-1043.
[9] 王玉婷,徐瑞屿,牛鸿艳,等.红酸汤中耐Cd2+酵母菌的筛选及其吸附特性[J].食品研究与开发,2023,44(13):183-189.
[10] 何扬波,李咏富,郑秀艳,等.60Co-γ射线辐照选育红酸汤发酵乳酸菌[J].中国酿造,2023,42(4):137-145.
[11] 许九红,王修俊,李佳敏,等.红酸汤原料番茄品种的筛选及发酵品质的综合评价[J].食品与发酵工业,2024,50(16):193-202.
[12] 穆先,涂青,陈秋慧,等.刺梨叶茶的品质分析及功能研究[J].中国酿造,2024,43(6):225-232.
[13] 沈甜,牛锐敏,黄小晶,等.基于层次-关联度和主成分分析的无核鲜食葡萄品质评价[J].食品工业科技,2021,42(3):53-60.
[14] 徐兆娜.辣椒豆瓣酱后酵期促熟增香菌株筛选及机理初探[D].贵阳:贵州大学,2023.
[15] SHU H J,HE X Q,HONG Z H,et al.Screening and genome analysis of potential probiotic lactic acid bacteria with broad-spectrum antibacterial activity from Sichuan sun-dried vinegar grains(Cupei)[J]. LWT-Food Sci Technol,2024,202:116288.
[16] ABBEY T C,DEAK E.What's new from the CLSI subcommittee on antimicrobial susceptibility testing M100,29th edition[J].Clin Microbiol Newsl,2019,41(23):203-209.
[17] LIANG H P,CHEN H Y,JI C F,et al.Dynamic and functional characteristics of predominant species in industrial Paocai as revealed by combined DGGE and metagenomic sequencing[J].Front Microbiol,2018,9:02416.
[18] 刘永飞,吴茂钊,严文俊,等.酱香型白酒对贵州糟辣椒二次发酵风味和感官品质的影响[J].中国酿造,2025,44(12):240-247.
[19] 吴姝,李金玲,龙丽丽,等.自然与乳酸菌强化发酵过程中红酸汤品质变化[J].中国酿造,2020,39(10):75-78.
[20] 潘季红,秦礼康,文安燕,等.贵州红酸汤营养品质及呈味特征分析[J].中国调味品,2020,45(6):43-48.
[21] 罗文珊,张艳,徐玉娟,等.不同芥菜品种对发酵泡菜品质的影响规律[J].现代食品科技,2022,38(5):43-55.
[22] BELTRÍN J,WURTZEL E T.Carotenoids: resources,knowledge,and emerging tools to advance apocarotenoid research[J]. Plant Sci,2025,350:112298.
[23] 周艳,李会,宋小娟.红酸汤自然发酵中番茄红素顺反异构变化及影响因素相关性分析[J].中国调味品,2023,48(6):173-177.
[24] 杨智夷.发酵番茄酸汤热加工中番茄红素量变及顺/反异构效应研究[D].贵阳:贵州大学,2024.
[25] ZHANG F Z,TAN M,HU Z E,et al.A hyaluronic acid-modified cyclodextrin self-assembly system for the delivery of β-carotene in the treatment of dry eye disease[J].Int J Biol Macromol,2025,287:138428.
[26] 李国林,何扬波,郑汝忠,等.贵州特色红酸汤发酵品质形成与改良研究进展[J].中国酿造,2025,44(7):33-37.
[27] 胡悦,刘娜,秦礼康,等.分料发酵红酸汤乳酸菌和酵母菌的分离鉴定及应用[J].食品与发酵工业,2024,50(5):116-123.
[28] LU J,MAO Y R,MA T,et al.Screening and genome analysis of lactic acid bacteria with high exopolysaccharide production and good probiotic properties[J].Food Biosci,2023,56:103211.
[29] MOHAMMED S,ÇON A H.Isolation and characterization of potential probiotic lactic acid bacteria from traditional cheese[J].LWT-Food Sci Technol,2021,152:112319.
[30] ABRIOUEL H,MUÑOZ M D C C,LERMA L L,et al.New insights in antibiotic resistance of Lactobacillus species from fermented foods[J].Food Res Int,2015,78:465-481.
[31] 陆敏,陈菊,王雪雅,等.电子鼻结合HS-SPME-GC-MS技术解析贵州主产区红酸汤香气成分[J].中国酿造,2024,43(11):231-236.
[32] 杨进军,胡金祥,王林,等.气质联用技术结合电子鼻分析红酸汤挥发性风味差异[J].食品与发酵工业,2020,46(14):234-242.