大曲作为白酒发酵剂,为白酒发酵提供了水解淀粉的糖化酶以及与乙醇、乳酸和其他风味化合物形成相关的酶和微生物,对白酒的风味有着重要贡献[1-2]。大曲本身通过发酵而成,其制作工艺亦较为复杂[3]。根据发酵过程中达到的最高温度,大曲可被分为高温大曲、中温大曲和低温大曲,其发酵顶温分别在65 ℃、55 ℃和45 ℃左右,制曲所用原料和工艺也各不相同[4-5]。低温大曲的发酵温度较低,其在发酵时无需额外添加母曲,完全依赖接种原料和环境中的微生物自发产生发酵过程[6]。在整个发酵过程中,低温大曲要经历上霉期、晾霉期、起潮火期、潮火期、大火期、后火期和养曲期7个阶段。前期的研究发现低温大曲中的微生物类群主要由芽孢杆菌属(Bacillus)、乳杆菌属(Lactobacillus)、魏斯氏菌属(Weissella)、覆膜孢酵母菌属(Saccharomycopsis)和嗜热子囊菌属(Thermoascus)等组成[7-9]。
如今,酒曲发酵过程中的微生物和品质变化被开始关注,了解这些变化规律有助于更好地控制产品品质,提高制曲和酿酒效率。已有的研究表明,发酵温度和湿度对大曲的微生物群落演替有着重要影响[10]。BAN S等[11]的研究表明,发酵温度对大曲中的根霉菌属(Rhizopus)、毕赤酵母菌属(Pichia)和威克汉姆酵母菌属(Wickerhamomyces)等的演替有显著影响;XIAO C等[12]对中温大曲发酵过程中微生物生态系统的群落演替进行了研究,结果发现,在发酵前12 d,温度动态与微生物群的快速演替密切相关,而发酵12 d后群落结构相对稳定。然而,目前关于低温大曲的细菌群落结构和类群组成在发酵过程中演替规律的研究鲜见报道。因此,解析各发酵阶段低温大曲中的微生物类群对于人们了解低温大曲发酵过程中微生物的变化规律具有积极的意义。
本研究以不同发酵阶段的低温大曲为研究对象,采用MiSeq高通量测序技术对各发酵阶段低温大曲中的细菌群落多样性和菌群组成进行解析,同时对优势细菌群间的相关性进行分析,最后使用PICRUSt软件对细菌菌群的基因功能进行预测,以期揭示低温大曲发酵过程中细菌群落结构及其功能的演替规律,这有助于人们了解制曲工艺对低温大曲微生物类群产生的影响,为低温大曲制曲工艺优化升级提供一定的理论参考依据。
1 材料与方法
1.1 材料与试剂
Omega宏基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:美国Bio-Tek公司;Taq DNA聚合酶:宝生物工程(大连)有限公司;正/反向引物338F/806R:上海桑尼生物科技有限公司;Illumina MiSeq测序试剂盒v3:美国Illumina公司。
1.2 仪器与设备
精创RCW-800无线温湿度记录仪:江苏省精创电气股份有限公司;Vetiri聚合酶链式反应(polymerase chain reaction,PCR)梯度基因扩增仪:美国AB公司;Fluor Chem FC3型化学发光凝胶成像系统:美国Protein Simple公司;MiSeq PE300高通量测序平台:美国Illumina公司;R930机架式服务器:美国DELL公司。
1.3 方法
1.3.1 低温大曲样品的采集
在曲块入房堆积排列整齐后便依次经历上霉期(第1~4天)、晾霉期(第5~8天)、起潮火期(第9~12天)、潮火期(第13~16天)、大火期(第17~19天)、后火期(第20~21天)和养曲期(第22~43天)7个发酵阶段,每个阶段结束后通过人工翻曲的方式使发酵进入下一阶段。于2023年11月22日起,从湖北省随州市某清香型白酒企业的同一间低温大曲曲房中采集入库前、上霉、晾霉、起潮火、潮火、大火、后火和养曲8个阶段的低温大曲样本,样本采集的时间点分别为大曲发酵的第0天、第4天、第8天、第12天、第16天、第19天、第21天和第43天,每个时间节点采集8份大曲样本,共计64份样本。与此同时,使用无线温湿度记录仪对发酵过程曲堆每日的温度、湿度进行监测。本研究在每个时间节点采集到的低温大曲样本均于当天运送回实验室粉碎并贮藏在-40 ℃,备用。
1.3.2 大曲样本微生物宏基因组DNA提取、PCR扩增和高通量测序
不同发酵时间低温大曲样本的微生物宏基因组DNA参照Omega宏基因组提取试剂盒说明书进行提取;以其为模板,使用添加核苷酸标签(Barcode)的引物对338F(5'-ACTCCTACGGGAGGCAGCA-3')/806R(5'-GGACTACHVGGGTWTCTAAT-3')对细菌菌群16S rRNA V3~V4区域基因序列进行PCR扩增,PCR扩增体系及程序参照窦晓等[13]的方法。采用琼脂凝胶电泳法对PCR扩增产物进行质量检测,检测合格的PCR扩增产物委托上海美吉生物医药科技有限公司在Illumina MiSeq PE300平台完成测序。
1.3.3 生物信息学分析
将测序得到的fq序列文件均上传至QIIME(v 1.9.0)平台并完成生物信息学分析[14]。使用PyNAST软件(v 1.2.2)识别核苷酸标签并根据标签信息将下机序列拆分和归并至各样品中;然后使用FLASH软件(v 1.2.7)对双端序列进行拼接,并参照CAPORASO J G等[15]提出的标准对序列进行质量控制。通过质量控制的有效序列按照97%序列相似度构建操作分类单元(operational taxonomic units,OTU)[16],然后采用UCHIME软件(v 4.1)对OTU序列进行嵌合体检查,剔除含有嵌合体的OTU[17],最后基于核糖体数据库项目(ribosomal database project,RDP)数据库(v 11.6)完成低温大曲中细菌物种信息的注释[18],同时基于测序所得OTU数据计算各样本中细菌的Chao1指数和Shannon指数等α多样性指数。
1.3.4 数据处理
使用GraphPad Prism 8.3.0软件实现不同发酵阶段低温大曲细菌菌群的α多样性指数的可视化;使用R软件(v 4.3.2)基于OTU数据对样本进行Jensen-Shannon分歧(Jensen-Shannon divergence,JSD)距离的聚类数分析和基于中心点分区(partitioning around medoids,PAM)分析及其可视化;使用R软件(v 4.3.2)对不同发酵阶段低温大曲中的优势细菌群进行可视化;使用R软件(v 4.3.2)对不同发酵阶段低温大曲中优势细菌属间的显著相关性进行计算,然后使用Gephi软件(v 0.9.2)对优势细菌属间的显著相关关系进行可视化;使用PICRUSt 1.0软件对大曲中微生物类群的功能进行预测,并使用STAMP软件(v 2.1.3)对其进行组间差异分析及可视化。
2 结果与分析
2.1 不同发酵阶段低温大曲细菌菌群α多样性解析
通过高通量测序共得到3 413 329条序列,经质量控制后得到3 398 779条有效序列,有效序列按照97%的相似度共划分到5 850个OTU,每个样本中平均含有53 106条有效序列和1 141个OTU。进一步基于测序数据在测序深度为46 010条序列时计算不同发酵阶段大曲样本中细菌菌群的Chao1指数和Shannon指数,结果见图1。
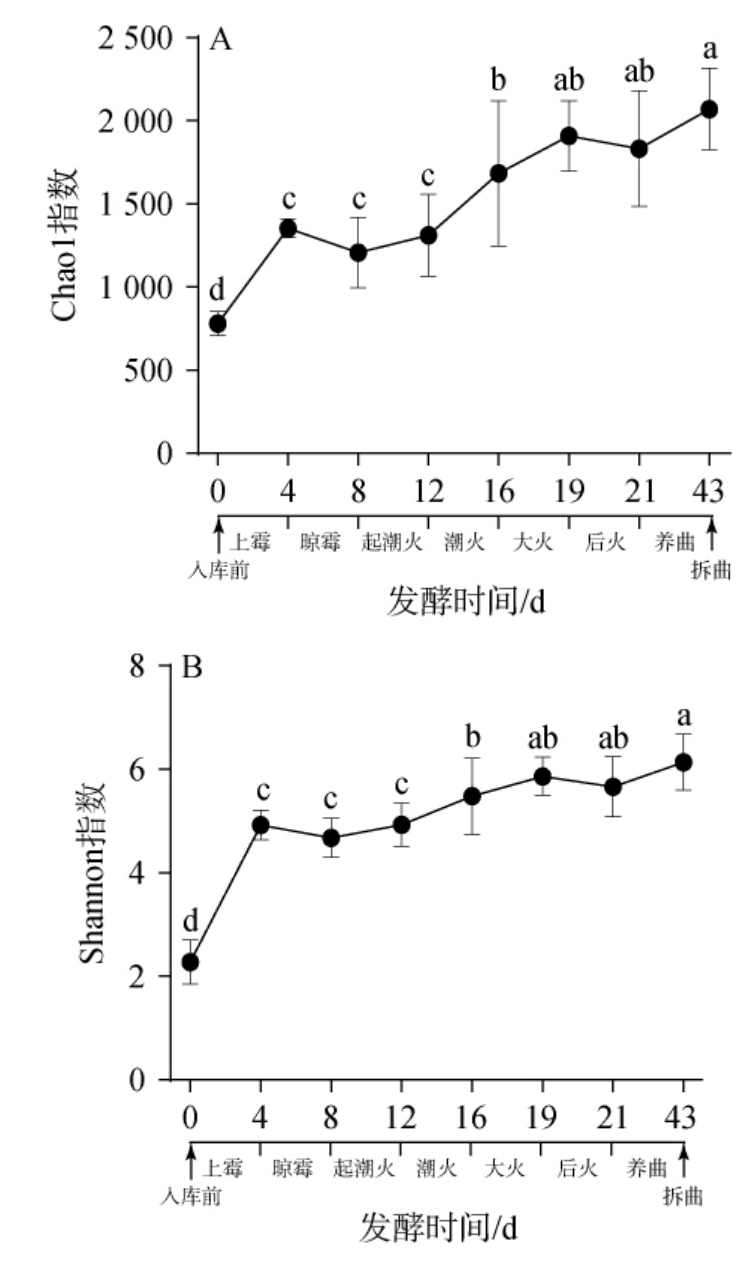
图1 不同发酵阶段低温大曲细菌菌群Chao1指数(A)和Shannon指数(B)分析结果
Fig.1 Analysis results of Chao 1 index (A) and Shannon index (B)of bacterial flora in low-temperature Daqu at different fermentation stages
不同小写字母表示差异显著(P<0.05)。
Chao1指数表征微生物丰富度,Shannon指数表征微生物多样性,由图1可知,随着发酵的进行,低温大曲中细菌菌群的α多样性指数变化趋势一致,均呈上升趋势,且均在经历上霉期后显著上升(P<0.05),然后在潮火期后再次显著上升(P<0.05),此后直到拆曲一直处于较平稳的水平。从入库前到拆曲,细菌菌群的Chao1指数和Shannon指数分别从781和2.28上升到2 071和6.14。由此可见,上霉期和潮火期对低温大曲细菌菌群丰富度和多样性的提升起到了较大的推动作用。
2.2 不同发酵阶段低温大曲细菌菌群β多样性分析
进一步对不同发酵阶段低温大曲样品细菌菌群的β多样性进行评估,结果见图2。
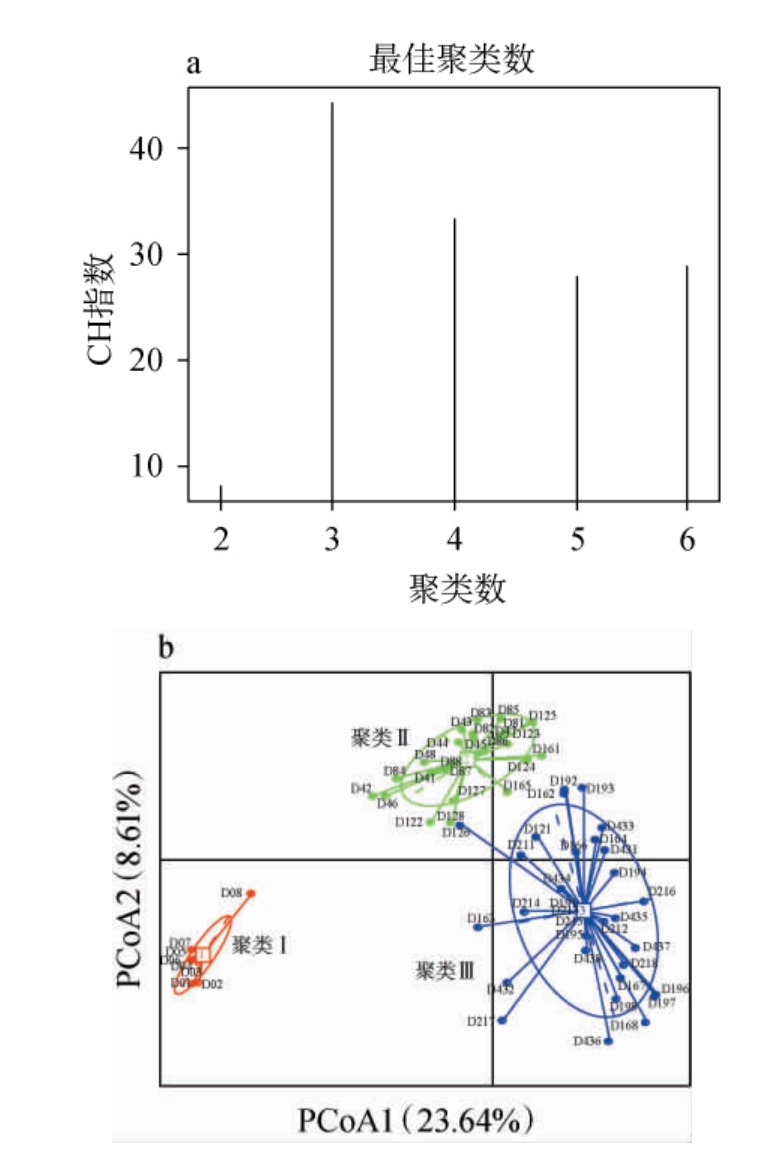
图2 不同发酵阶段低温大曲细菌菌群基于Jensen-Shannon分歧距离的聚类数分析(a)和基于中心点分区分析(b)结果
Fig.2 Results of cluster number analysis based on Jensen-Shannon divergence distance (a) and Partitioning Around Medoids analysis (b) of bacterial flora in low-temperature Daqu at different fermentation stages
由图2a可知,基于JSD距离的聚类分析发现,64份样本被分为3个聚类时卡林斯基-哈拉巴兹(Calinski-Harabasz,CH)指数最高(44.24),表明样本被分为3个聚类时最佳。由图2b可知,当样本被分为3个聚类时,入库前的样本单独构成了聚类Ⅰ;上霉期、晾霉期和起潮火期的样本构成了聚类Ⅱ;潮火期、大火期、后火期和养曲期的样本构成了聚类Ⅲ,说明低温大曲发酵过程中,上霉期、晾霉期和起潮火期细菌菌群结构较为相似,而潮火期、大火期、后火期和养曲期细菌菌群结构较为相似。由此可见,低温大曲细菌群落结构分别在上霉期后和潮火期后较前一时期发生了较大变化,这与α多样性分析结果相一致。
2.3 不同发酵阶段低温大曲细菌菌群结构解析
根据PAM分析得到的聚类,进一步基于属水平对不同发酵阶段低温大曲中的细菌菌群进行解析,结果见图3。
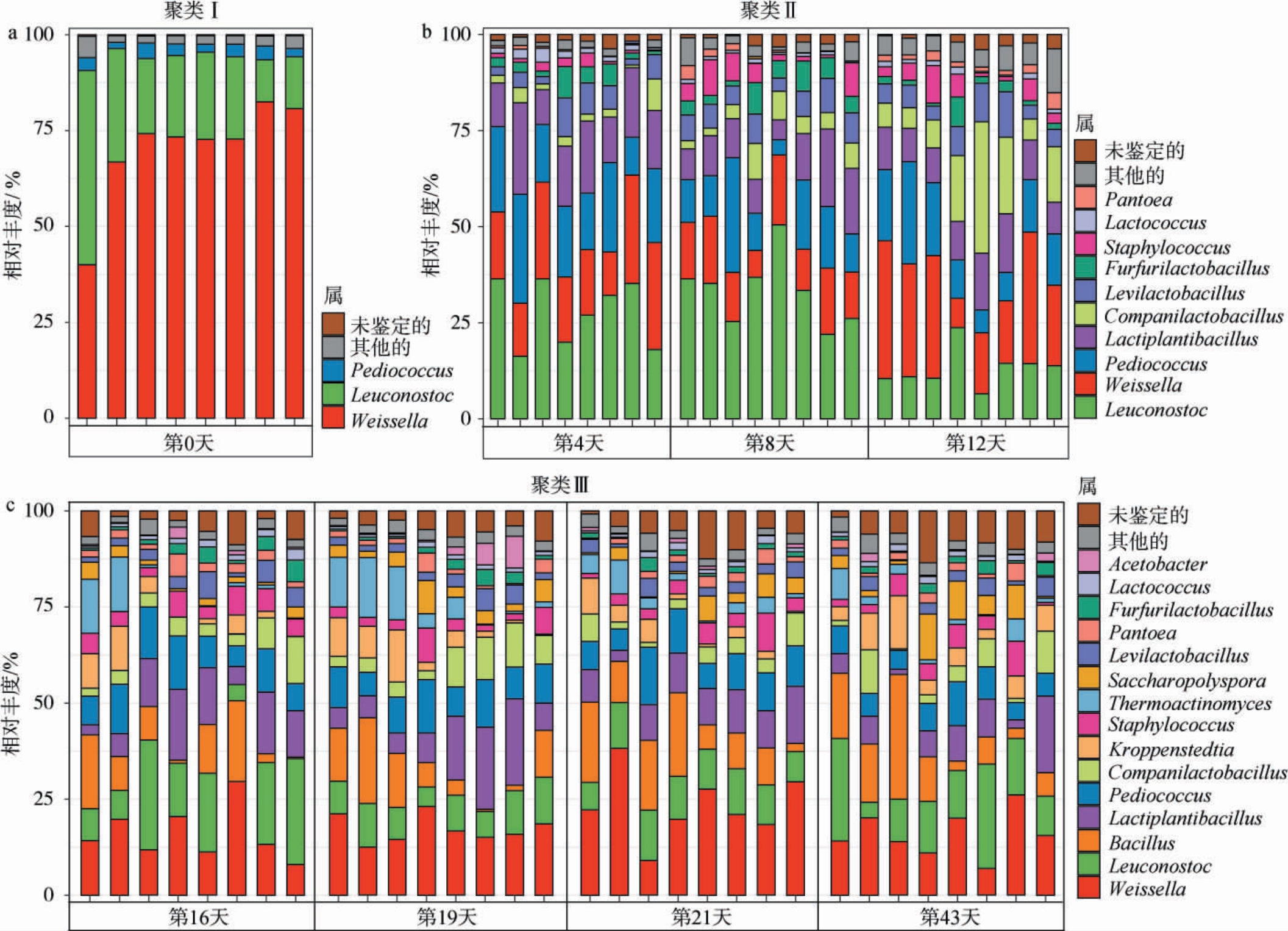
图3 不同发酵阶段低温大曲中的细菌菌群结构解析
Fig.3 Analysis of the bacterial flora structure in low-temperature Daqu at different fermentation stages
由图3a可知,入库前的样本中仅有3个优势细菌属(平均相对丰度>1%),分别为魏斯氏菌属(Weissella)(70.38%)、明串珠菌属(Leuconostoc)(23.71%)和片球菌属(Pediococcus)(2.89%),均属于乳酸菌类群,累计平均相对丰度为96.98%。由图3b可知,上霉期、晾霉期和起潮火期的样本中共有10个优势细菌属,分别为Leuconostoc(24.67%)、Weissella(19.16%)、Pediococcus(15.61%)、乳植杆菌属(Lactiplantibacillus)(12.61%)、伴生乳杆菌属(Companilactobacillus)(7.20%)、发酵剂乳杆菌属(Levilactobacillus)(6.01%)、麸皮乳杆菌属(Furfurilactobacillus)(3.49%)、葡萄球菌属(Staphylococcus)(3.45%)、乳球菌属(Lactococcus)(1.22%)和泛菌属(Pantoea)(1.14%),其中乳酸菌的累计平均相对丰度为89.97%。由图3c可知,潮火期、大火期、后火期和养曲期的样本中共有15个优势细菌属,分别为Weissella(18.09%)、Leuconostoc(13.27%)、芽孢杆菌属(Bacillus)(10.17%)、Lactiplantibacillus(9.87%)、Pediococcus(9.04%)、Companilactobacillus(5.18%)、Kroppenstedtia(4.74%)、Staphylococ cus(4.22%)、高温放线菌属(Thermoactinomyces)(4.21%)、糖多孢菌属(Saccharopolyspora)(3.53%)、Levilactobacillus(3.03%)、Pantoea(2.11%)、Furfurilactobacillus(1.84%)、Lactococcus(1.27%)和醋杆菌属(Acetobacter)(1.03%),其中乳酸菌的累计平均相对丰度为61.59%。随着发酵的进行,低温大曲中的优势细菌属数量逐渐增加,乳酸菌种类亦有增加。值得注意的是,乳酸菌在整个发酵过程中始终占比较大。在潮火期之前,乳酸菌累计平均相对丰度>85%,而在潮火期之后其累计平均相对丰度下降到60%左右,同时出现了Bacillus、Kroppenstedtia和Thermoactinomyces等耐热或嗜热菌群,它们累计平均相对丰度为19.12%。由此可见,在低温大曲的发酵过程中乳酸菌类群始终占据主导地位,但在发酵温度相对较高的潮火期开始出现部分耐热和嗜热菌群。
2.4 不同发酵阶段低温大曲细菌属间相关性和组间距离分析
进一步采用Spearman检验分析了聚类Ⅱ和聚类Ⅲ大曲样本中优势细菌属间的相关关系,并对两个聚类样本中细菌群落的组间距离进行了比较,结果见图4。
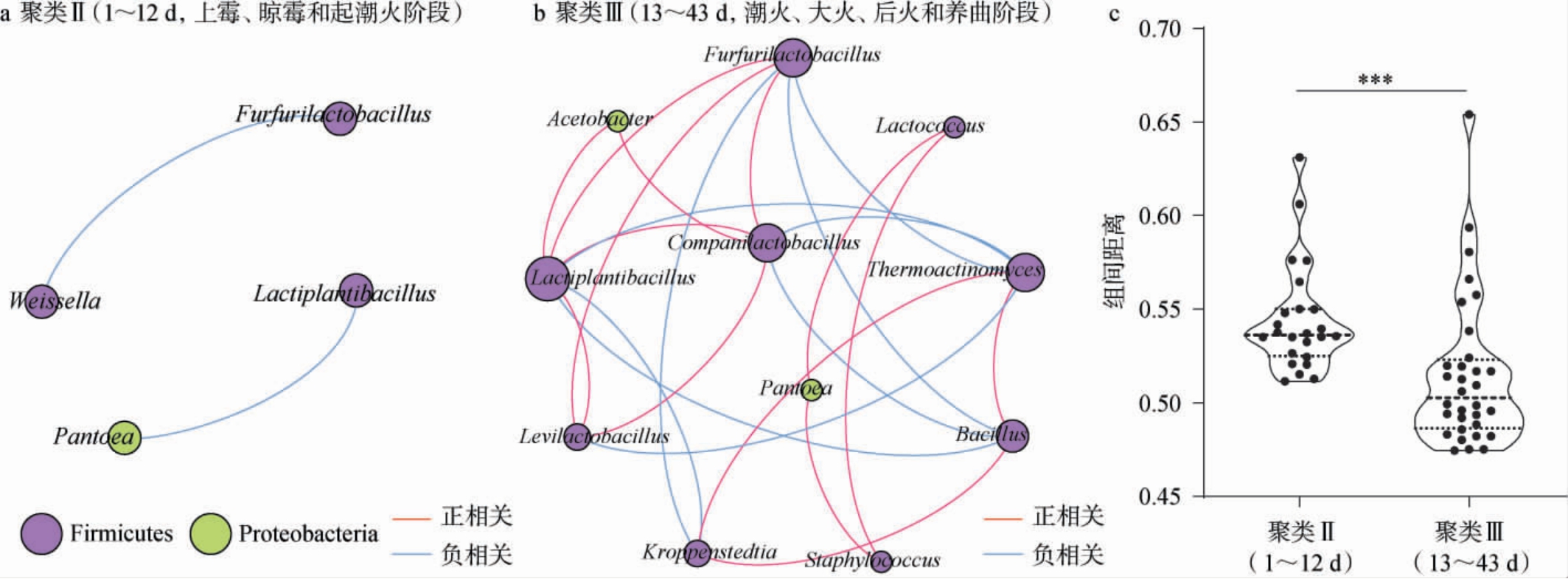
图4 不同发酵阶段低温大曲的细菌菌群间的相关性(a、b)和基于非加权UniFrac距离的组间距离(c)分析结果
Fig.4 Analysis results of the correlation (a,b) among the bacterial flora of low-temperature Daqu at different fermentation stages and the inter-group distance based on the unweighted UniFrac distance (c)
图a和b中出现的所有相关关系均显著(P<0.05);线条越粗代表相关性系数(R)越大,图c中“***”代表相关性极显著(P<0.001)。
由图4a可知,上霉期、晾霉期和起潮火期的大曲样本优势细菌属间的相关性网络较简单,仅由Weissella、Lactiplantibacillus、Furfurilactobacillus和Pantoea组成,且它们之间存在的显著相关关系较少。由图4b可知,潮火期、大火期、后火期和养曲期大曲样本优势细菌属间的相关性网络中的菌属数量较之前阶段有明显增加,且它们之间存在的显著相关关系复杂多样。由图4c可知,基于非加权UniFrac距离的组间距离分析结果显示,上霉期、晾霉期和起潮火期的样本组间距离极显著大于潮火期、大火期、后火期和养曲期的样本组间距离(P<0.001)。由此可见,经历潮火期后,低温大曲中细菌菌群间的相互作用有所增强,菌群结构变得更加稳定。
2.5 不同发酵阶段低温大曲细菌菌群基因功能预测分析
采用PICRUSt软件对不同发酵阶段低温大曲中细菌菌群的基因功能进行预测,经过与蛋白质直系同源簇数据库(clusters of orthologous groups of proteins,COG)数据库比对,共预测到了4 545个COG,隶属于23个功能大类,具体结果见图5。
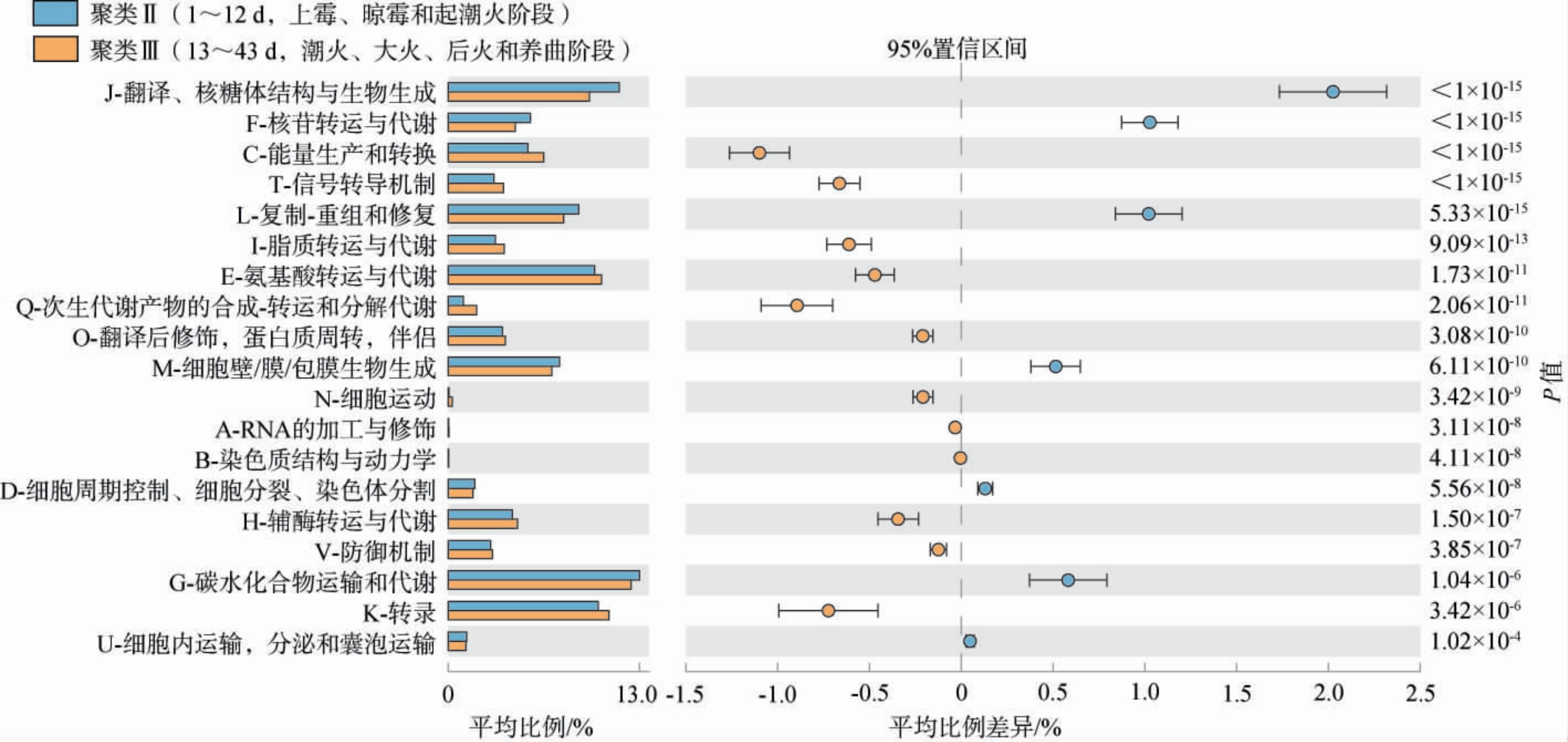
图5 基于PICRUSt预测不同发酵阶段低温大曲的细菌菌群基因功能
Fig.5 Gene function of bacterial flora in low-temperature Daqu at different fermentation stages based on PICRUSt prediction
由图5可知,Welch's t检验显示潮火期之前的样本和潮火期之后的样本细菌菌群在19个功能大类的表达量上存在显著差异(P<0.05)。两组相比较而言,潮火期之前的样本细菌菌群在D(细胞周期控制、细胞分裂、染色体分割)、G(碳水化合物运输和代谢)、F(核苷转运与代谢)、H(辅酶转运与代谢)、L(复制-重组和修复)、M(细胞壁/膜/包膜生物生成)、O(翻译后修饰,蛋白质周转,伴侣)和U(细胞内运输,分泌和囊泡运输)功能上的表达量上显著偏高(P<0.05),而潮火期之后的样本菌群在A(RNA)的加工与修饰)、B(染色质结构与动力学)、C(能量生产和转换)、E(氨基酸转运与代谢)、I(脂质转运与代谢)、J(翻译、核糖体结构与生物生成)、K(转录)、N(细胞运动)、Q(次生代谢产物的合成-转运和分解代谢)、T(信号转导机制)和V(防御机制)功能的表达量上显著偏高(P<0.05)。值得注意的是,潮火期之前的样本细菌菌群在与细胞生长繁殖等功能的表达量上普遍偏高,例如J、L、F、M和D等功能;而潮火期之后的样本细菌菌群在与能量产生和物质代谢等功能的表达量上普遍偏高,例如C、I、E、Q和H等功能。由此可见,经历潮火期后,低温大曲中的细菌基因更加偏向物质代谢等功能的表达。
3 讨论
低温大曲的发酵过程属于传统固态发酵,是原料与环境中微生物自发发生的过程[19],包含上霉期、晾霉期、起潮火期、潮火期、大火期、后火期和养曲期。在这一过程中,微生物产生的发酵热不断积累,需要通过人工翻曲的方式调节温度,进而控制微生物生长代谢的速度[12,20],因而行业内有“高温大曲制曲靠堆,低温大曲制曲靠翻”的说法。本研究发现,入库前大曲中的优势细菌属由Weissella、Leuconostoc和Pediococcus构成,而经历上霉期后,大曲中的优势菌属从最初的3个增加到10个,新出现了Lactiplantibacillus、Levilactobacillus、Furfurilactobacillus 和Companilactobacillus等细菌类群,且细菌菌群丰富度和多样性均显著提升,究其原因可能在于,上霉阶段湿度始终维持在80%以上,较高的空气湿度使草席和曲房中的微生物更容易被接种到大曲上,从而使大曲中的细菌菌群丰富度和多样性出现明显提升。较之上霉期,晾霉期和起潮火期大曲中的细菌菌群丰富度和多样性未出现明显上升或下降趋势,优势菌群组成亦与上霉期类似。究其原因可能在于,在制曲过程中,为避免持续的湿润环境导致曲块霉变腐败,操作工人会通过翻曲和打开门窗散潮(晾霉)等操作使曲房湿度下降。同时由于发酵热的积累,曲堆温度在起潮火期的最后时期已达到42 ℃左右,因而相对较高的温度和散潮会使曲块中水分挥发较快,进而抑制了菌群的生长繁殖。此外,较之晾霉期和起潮火期,处于潮火期的大曲其细菌菌群丰富度和多样性显著上升,菌群结构亦产生明显变化,优势细菌属数量从上一阶段的10个增加到了15个。为减少散热,潮火期曲块的堆积从3层增加到了4层,进而保证曲堆温度能在43 ℃左右维持4 d以上。相对较高的曲堆温度能够让曲块表层的微生物向温度相对低的曲块内部生长繁殖,尽可能充分利用原料中的营养成分,这可能是导致潮火期酒曲菌群多样性增加的主要原因。在低温大曲发酵过程中,潮火期相对较高的温度还促进了耐热和嗜热菌群的生长,因而该阶段Bacillus、Kroppenstedtia和Thermoactinomyces等耐热或嗜热菌群开始出现。本研究亦发现,乳酸菌类群在低温大曲各发酵阶段的占比均较高,且多样性会随着发酵温度的缓慢升高而增加,尽管潮火期、大火期、后火期和养曲期耐热或嗜热菌群的出现会导致乳酸菌的相对丰度有明显下降,但其仍占据主导地位,这与HU Y等[21-22]的研究结果一致。乳酸菌是自然界中广泛存在的一类细菌,亦是发酵各类酒精饮料不可缺少的菌群[23-24],它们不仅含有代谢碳水化合物的关键酶基因,还能通过代谢产生丰富的酯类,对酒的香气形成有重要贡献[25],而导致低温大曲制曲各阶段优势细菌为乳酸菌的原因可能与其发酵温度在23~43 ℃有关,该温度范围比较适合乳酸菌的生长。
基因功能预测结果显示,处于上霉期、晾霉期和起潮火期的大曲其细菌菌群在细胞周期控制、细胞分裂和染色体分割等与细胞生长发育繁殖等相关基因功能上的表达量显著偏高,而处于潮火期、大火期、后火期和养曲期的大曲其细菌菌群在氨基酸、脂质和次生代谢产物的运输和代谢以及能量生产和转换等与物质代谢相关基因功能上的表达量上显著偏高。由此可见,在经历潮火阶段后,低温大曲中的细菌群由以生长为主逐渐转变为开始产生大量的代谢物质,这可能与Bacillus、Kroppenstedtia和Thermoactinomyces等耐热或嗜热菌群在潮火阶段大量繁殖有关,越来越多的研究表明这些耐热微生物往往具有特殊的遗传背景和代谢途径,可以产生多种酶和其他具有特殊功能的活性物质[26-27]。例如,地衣芽孢杆菌(B.licheniformis)具有高产蛋白酶和淀粉酶特性[28],普通高温放线菌(Thermoactinomyces vulgaris)和糖化热放线菌(Thermoactinomyces sacchari)不仅能够分泌淀粉酶、酯酶、纤维素酶、果胶酶和磷酸酶,还能产生具有茅台风味的吡嗪类物质和其他风味物质[12,29]。较之潮火期,大火期、后火期和养曲期低温大曲中细菌类群的丰富度和多样性以及群落结构均未发生明显变化,其原因可能是在上述两个阶段发酵温度缓慢回降至30 ℃左右,加之原料中营养成分减少且大曲硬度增加,进而导致微生物生长代谢速率下降。本研究亦发现,较之上霉期、晾霉期和起潮火期,潮火期、大火期、后火期和养曲期的低温大曲中优势细菌属间的相关性网络变得更加复杂紧密,样本的组间距离亦明显变小,这说明在43 ℃经历4 d潮火期发酵后大曲中微生物类群间的共生关系和菌群稳定性均得到了增强。
4 结论
Alpha多样性分析结果显示,低温大曲发酵过程中,细菌菌群的Chao1指数和Shannon指数分别在上霉和潮火期显著上升(P<0.05)。PAM分析将不同发酵阶段低温大曲样品聚类为3类,即聚类Ⅰ(入库前样本)、聚类Ⅱ(上霉、晾霉和起潮火期样本)、聚类Ⅲ(潮火、大火、后火和养曲期样本)。聚类Ⅰ和聚类Ⅱ样本中细菌均以乳酸菌为主;聚类Ⅲ样本中乳酸菌累计平均相对丰度降低,出现了芽孢杆菌属(Bacillus)等耐热菌群。此外,经历潮火期后,细菌菌群间相关性网络变得更加紧密,组间距离显著减小(P<0.05)。基因功能预测结果显示,聚类Ⅱ样本细菌菌群基因在与细胞生长繁殖等功能上的表达量显著偏高(P<0.05),而聚类Ⅲ样本中细菌菌群基因在与物质代谢功能上的表达量显著偏高(P<0.05)。结果表明,低温大曲细菌群落结构在上霉期和潮火期发生了较大变化,在潮火期后,细菌菌群间的相互作用和结构稳定性增强,且与物质代谢相关的基因表达增加。
[1] ZHENG Y,LIANG F,WU Y,et al.Unraveling multifunction of lowtemperature Daqu in simultaneous saccharification and fermentation of Chinese light aroma type liquor[J].Int J Food Microbiol,2023,397(7):110202.
[2] WU S,DU H,XU Y.Daqu microbiota adaptability to altered temperature determines the formation of characteristic compounds[J]. Int J Food Microbiol,2023,385(1):109995.
[3] ZHENG X W,TABRIZI M R,NOUT M J R,et al.Daqu-a traditional Chinese liquor fermentation starter[J].J I Brewing,2011,117(1):82-90.
[4] KANG J,CHEN X,HAN B Z,et al.Insights into the bacterial,fungal,and phage communities and volatile profiles in different types of Daqu[J].Food Res Int,2022,158(8):111488.
[5] ZHOU Q,MA K,SONG Y,et al.Exploring the diversity of the fungal community in Chinese traditional Baijiu daqu starters made at low-,medium-and high-temperatures[J]. LWT-Food Sci Technol,2022,162(6):113408.
[6] 王军燕,甄攀,王晓勇.不同培曲工艺对清香型大曲细菌菌群结构的影响[J].酿酒,2023,50(4):72-74.
[7] YU Q,MOU F,XIAO J,et al.Correlational analysis of physicochemical indexes,microbial communities,and volatile components in light-flavor Daqu from north and south regions of China[J]. World J Microb Biot,2024,40(2):54.
[8] HOU Q,WANG Y,CAI W,et al.Metagenomic and physicochemical analyses reveal microbial community and functional differences between three types of low-temperature Daqu[J].Food Res Int,2022,156:111167.
[9] CAI W C,WANG Y R,NI H,et al.Diversity of microbiota,microbial functions,and flavor in different types of low-temperature Daqu[J].Food Res Int,2021,150:110734.
[10] ZHENG X W,YAN Z,NOUT M J R,et al.Microbiota dynamics related to environmental conditions during the fermentative production of Fen-Daqu,a Chinese industrial fermentation starter[J].Int J Food Microbiol,2014,182(7):57-62.
[11] BAN S,CHEN L,FU S,et al.Modelling and predicting population of core fungi through processing parameters in spontaneous starter(Daqu)fermentation[J].Int J Food Microbiol,2022,363(2):109493.
[12] XIAO C,LU Z M,ZHANG X J,et al.Bio-heat is a key environmental driver shaping the microbial communityof medium-temperature Daqu[J].Appl Environ Microb,2017,83(23):e01550-17.
[13] 窦晓,韩培杰,刘莉,等.泸型酒酿造期间酒醅中可培养细菌的分离鉴定及其种群演替规律研究[J].食品工业科技,2017,38(1):169-174.
[14] KUCZYNSKI J,STOMBAUGH J,WALTERS W A,et al.Using QIIME to analyze 16S rRNA gene sequences from microbial communities[J].Curr Protoc Microbiol,2012,27(1):10-20.
[15] CAPORASO J G,KUCZYNSKI J,STOMBAUGH J,et al.QIIME allows analysis of high-throughput community sequencing data[J].Nat Methods,2010,7(5):335-336.
[16] WEI Z G,ZHANG X D,CAO M,et al.Comparison of methods for picking the operational taxonomic units from amplicon sequences[J]. Front Microbiol,2021,12(3):644012-644026.
[17] EDGAR R C,HAAS B J,CLEMENTE J C,et al.UCHIME improves sensitivity and speed of chimera detection[J].Bioinformatics,2011,27(16):2194-2200.
[18] BRANDT M I,TROUCHE B,QUINTRIC L,et al.Bioinformatic pipelines combining denoising and clustering tools allow for more comprehensive prokaryotic and eukaryotic metabarcoding[J].Mol Ecol Resour,2021,21(6):1904-1921.
[19] WU Q,ZHU Y,FANG C,et al.Can we control microbiota in spontaneous food fermentation?-Chinese liquor as a case example[J]. Trends Food Sci Tech,2021,110(4):321-331.
[20] ZHANG Q,FU C,ZHAO C,et al.Monitoring microbial succession and metabolic activity during manual and mechanical solid-state fermentation of Chinese cereal vinegar[J].LWT-Food Sci Technol,2020,133(11):109868.
[21] HU Y,HUANG X,YANG B,et al.Contrasting the microbial community and metabolic profile of three types of light-flavor Daqu[J].Food Biosci,2021,44(12):101395.
[22] TANG H,LIANG H,SONG J,et al.Comparison of microbial community and metabolites in spontaneous fermentation of two types Daqu starter for traditional Chinese vinegar production[J]. J Biosci Bioeng,2019,128(3):307-315.
[23] CAPPELLO M S,ZAPPAROLI G,LOGRIECO A,et al.Linking wine lactic acid bacteria diversity with wine aroma and flavour[J].Int J Food Microbiol,2017,243(2):16-27.
[24] PANG X N,CHEN C,HUANG X N,et al.Influence of indigenous lactic acid bacteria on the volatile flavor profile of light-flavor Baijiu[J].LWTFood Sci Technol,2021,147(7):111540.
[25] PANG X N,HAN B Z,HUANG X N,et al.Effect of the environment microbiota on the flavour of light-flavour Baijiu during spontaneous fermentation[J].Sci Rep,2018,8(1):3396.
[26] ZHANG Y,XU J,DING F,et al.Multidimensional profiling indicates the shifts and functionality of wheat-origin microbiota during high-temperature Daqu incubation[J].Food Res Int,2022,156(6):111191.
[27] CAI W C,XUE Y A,WANG Y R,et al.The fungal communities and flavor profiles in different types of high-temperature Daqu as revealed by high-throughput sequencing and electronic senses[J].Front Microbiol,2021,12(12):784651.
[28] KARATA H,UYAR F,TOLAN V,et al.Optimization and enhanced production of α-amylase and protease by a newly isolated Bacillus licheniformis ZB-05 under solid-state fermentation[J]. Ann Microbiol,2013,63(3):45-52.
[29] YOON J H,PARK Y H.Phylogenetic analysis of the genus Thermoactinomyces based on 16S rDNA sequences[J]. Int J Syst Evol Microbiol,2000,50(3):1081-1086.