大曲是大曲酒类酿造的糖化发酵生香剂,其中酱香大曲是以小麦为原料、制曲过程中最高品温控制60 ℃而制成的高温大曲[1],在酿酒过程中主要起着投粮作用、接种作用和生香作用,主要用于酱香型白酒的酿造。酱香大曲的质量不仅影响酱香型白酒的出酒率,更是对其质量和风格起着决定性的作用[2],因此,常有“曲为酒之骨”的说法[3]。大曲的质量直接决定了基酒的产量与风格。在传统酿造经验中,根据贮存时间,酱香大曲可分为新曲与陈曲,新曲指完成约40 d仓内发酵后、出仓即用(贮存期0 d)的曲块;陈曲则指出仓后继续贮存180 d的曲块,并且强调新陈曲配伍使用[4-5]。经验表明,新曲因其糖化力大而能保证出酒率,陈曲则因其香醇而能提升酒体品质。大曲在贮存过程中会发生多种生化反应,使得微生物、代谢产物和酶系结构都相应发生变化[6]。研究表明[7],不同贮存期的酱香大曲在理化性质(如水分、酸度、酶活力)和微生物组成上存在显著差异,这些变化与白酒的最终风味形成密切相关[8]。贮存时间对大曲微生物群落结构及其代谢功能的影响机制仍缺乏系统性研究,尤其是微生物群落与关键酶活的关联性尚未完全阐明,不利于微生物技术在酒曲改良中的应用。
近年来,高通量测序技术因其安全性和可靠性高,能全面展现样本微生物多样性、群落结构及丰度等优势,普遍被应用于酿酒领域中不同香型大曲、酒醅、酒糟的微生物群落结构分析[9]。现有研究虽已初步揭示了酱香大曲中的微生物组成,但多集中于制曲过程的动态变化,或不同轮次酒糟的差异。对于贮存陈化这一关键工艺环节如何驱动大曲从新到陈的微生态演替,以及这种演替与理化特性、酶活功能之间的内在联系,尚缺乏系统性的阐释[10]。
本研究基于高通量测序分析新曲(贮存期0 d)和陈曲(贮存期180 d)中微生物群落结构及多样性,结合新曲和陈曲的理化指标及酿造特性检测,分析其微生物群落结构与酿造特性的关联性。从而为传统新陈曲配伍工艺提供坚实的科学理论依据,并为大曲质量的精准评价与定向调控提供新的思路与数据支撑。
1 材料与方法
1.1 材料与试剂
陈曲(贮存期180 d,编号Q1)、新曲(贮存期0 d,编号Q2):茅台镇某酒厂。
宏基因组抽提所用试剂Tris-base、乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA):德国BioFroxx公司;十二烷基硫酸钠(sodium dodecyl sulfate,SDS):美国BIOSHARP公司;脱氧核糖核酸(deoxyribonucleicacid,DNA)提取试剂盒:美国Zymo Research公司;KOD FX Neo北京百灵克生物科技有限责任公司;引物ITS1F、ITS2:苏州泓迅生物科技股份有限公司;琼脂糖(分析纯):北京博美富鑫科技有限公司。
1.2 仪器与设备
T100-ThermalCycler聚合酶链式反应(polymerase chain reaction,PCR)仪:美国BIO-RAD公司;Eppendorf-E100小型台式高速离心机:艾本德(中国)有限公司。
1.3 试验方法
1.3.1 采样
以陈曲Q1和新曲Q2为采样对象,选取曲房的5个位置,每个位置取3块曲砖,分别为上层曲砖、中层曲砖和下层曲砖,5个位置共15块曲砖,经粉碎,混匀,过筛,备用。
1.3.2 新曲和陈曲的酿造特性分析
按照轻工业行业标准QB/T 4257—2011《酿酒大曲通用分析方法》[11]对新曲和陈曲的水分、酸度、淀粉、液化力、发酵力、糖化力和酯化力进行测定。
液化力单位定义:在35 ℃、pH 4.6条件下,1 g绝干曲1 h能液化淀粉的质量为一个单位(U),以[g/(g·h)]表示。发酵力单位定义:在30 ℃,72 h内0.5 g大曲利用可发酵糖类所产生的二氧化碳质量为一个单位(U),以[g/(0.5 g·72 h)]表示。糖化力单位定义:在35 ℃、pH 4.6条件下,1 g大曲转化可溶性淀粉生成葡萄糖的质量为一个单位(U),以[mg/(g·h)]表示。酯化力单位定义:每50g大曲在35℃,经过7d催化己酸和乙醇生成己酸乙酯的质量为一个单位(U),以[g/(50g·7d)]表示。
1.3.3 酱香型大曲中DNA提取、PCR扩增和测序
采用DNA提取试剂盒分别对新曲与陈曲样品中的基因组DNA进行提取与纯化。选用细菌16S rRNA基因的V3~V4可变区及真菌ITS区作为靶标进行PCR扩增。细菌扩增所用引物为338F(5'-ACTCCTACGGGAGGCAGCA-3')与806R(5'-GGACTACHVGGGTWTCTAAT-3'),真菌扩增引物为ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2(5'-GCTGCGTTCTTCATCGATGC-3')。细菌PCR扩增体系(20 μL):5 μL KOD FX Neo Buffer、2 μL 2 mmol/L脱氧核糖核苷三磷酸(deoxyribonucleoside triphosphate,dNTPs)、正反向引物(10 μmol/L)各0.3 μL、50 ng DNA模板、0.2 μL KODFXNeo聚合酶,以超纯水补足至20μL。真菌PCR扩增体系(10 μL):5 μL 2×PCR KOD FX Neo Buffer、2 μL 2 mmol/L dNTPs、正反向引物各0.3 μL、50 ng DNA模板、0.2 μL KOD FX Neo聚合酶,以超纯水补足至10 μL。PCR扩增程序:95 ℃预变性5 min;随后进行20个循环(95 ℃变性1 min,60 ℃退火30 s,72 ℃延伸45 s);最终72 ℃延伸5 min,4 ℃保存。扩增产物经1.8%琼脂糖凝胶电泳检测并纯化,每个样本设置3次重复,取对数期PCR产物等量混合后构建测序文库。最终在Illumina NovaSeq平台上,分别对细菌16S rRNA基因V3~V4区与真菌ITS区进行双端高通量测序。
1.3.4 高通量测序数据处理与分析
原始数据预处理:测序获得的原始图像数据(Raw Data)经碱基识别(Base Calling)转换为原始序列(Raw Reads),随后进行以下两步预处理:
(1)质量过滤:使用Trimmomatic 0.33软件剔除低质量Reads,去除接头及测序噪音;进一步通过Cutadapt 1.9.1软件识别并切除引物序列,获得高质量Clean Reads。
(2)去噪与嵌合体去除:基于QIIME2 2020.6平台,采用DADA2算法对双端序列进行去噪、拼接(merge)及嵌合体过滤(chimera removal),最终生成非嵌合体有效序列(Nonchimeric Reads),用于后续分析。
数据分析:Alpha多样性分析通过QIIME2软件计算以下指标:物种丰富度指数:Chao1指数[12]和ACE指数[13],反映样本中物种总数;物种多样性指数:Shannon指数[14]和Simpson指数[15],综合评估物种多样性和均匀性。β多样性分析基于Bray-Curtis距离矩阵,通过主坐标分析(principal coordinates analysis,PCoA)和非度量多维尺度(non-metric multidimensional scaling,NMDS)分析展示样本间微生物群落差异。统计显著性检验采用相似性分析(analysis of similarities,ANOSIM)和置换多元方差分析(permutational multivariate analysis of variance,PERMANOVA)方法,使用R语言(v3.6.0)的vegan包完成[16]。采用线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)工具进行组间差异物种分析[17]。设置线性判别分析(lineardiscriminant analysis,LDA)得分阈值>4.0,P值<0.05(Kruskal-Wallis检验)的物种被认为具有显著差异。通过多级判别分析确定不同分组间具有显著差异的生物标志物。
2 结果与分析
2.1 新曲和陈曲理化指标及酿造特性分析
酱香型大曲的理化指标及酿造特性是评价其品质的关键。酱香型大曲新曲和陈曲理化指标及酿造特性分析见表1。
表1 酱香型大曲新曲和陈曲的理化指标及酿造特性
Table 1 Physicochemical indicators and brewing characteristics of new and aged sauce-flavor Daqu

注:同列不同字母表示差异显著(P<0.05)。
由表1可知,新曲与陈曲在水分、酸度、淀粉含量、发酵力、液化力、酯化力和糖化力等指标上均存在差异。新曲的水分含量(11.50%)、酸度(4.30 mmol/10 g)、淀粉含量(58.90 g/100 g)、发酵力[0.56 g/(0.5 g·72 h)]和糖化力[499.20 mg/(g·h)]均显著高于陈曲(P<0.05),表明新曲中微生物代谢活跃,具备较强的糖化发酵潜力。陈曲水分含量为10.20%,淀粉含量为57.43 g/100 g,发酵力为[0.38 g/(0.5 g·72 h)],糖化力为[241.20 mg/(g·h)],说明贮存过程中部分微生物活性减弱。值得注意的是,陈曲的液化力[0.48 g/(g·h)]和酯化力[7.00 mg/(g·h)]显著高于新曲(P<0.05),反映出贮存过程筛选并富集了具有特定代谢功能的微生物类群,其相关酶系得到积累与优化,有利于酯类风味物质的形成。该结果与已有研究[18-20]一致。新曲有较高的糖化力和发酵力,这确保了其在酿酒开始能快速启动并将淀粉高效转化为酒精,是保障出酒率的关键。而陈曲整体指标符合DB52/T 871—2014《酱香型白酒酿酒用大曲》[19]中优质大曲的要求,说明陈化有助于大曲从产酒型向生香型功能转变。
2.2 新曲和陈曲微生物多样性分析
2.2.1 Alpha多样性分析
Venn图可直观展现不同贮存期酱香型大曲样品中的共有操作分类单元(operational taxonomic unit,OTU)和特有OTU,酱香型大曲新曲和陈曲细菌和真菌OTU数Venn图见图1。由图1A可知,陈曲Q1和新曲Q2真菌中共有37个OTU,陈曲Q1中独有516个OTU,新曲Q2中独有396个OTU。由图1B可知,陈曲Q1和新曲Q2细菌中共有56个OTU,陈曲Q1中独有628个OTU,新曲Q2中独有637个OTU。陈曲样本独有的真菌和细菌可能赋予了陈曲独特的发酵特性和风味。新曲样本独有的真菌和细菌则可能是新曲表现出不同于陈曲特性的原因。
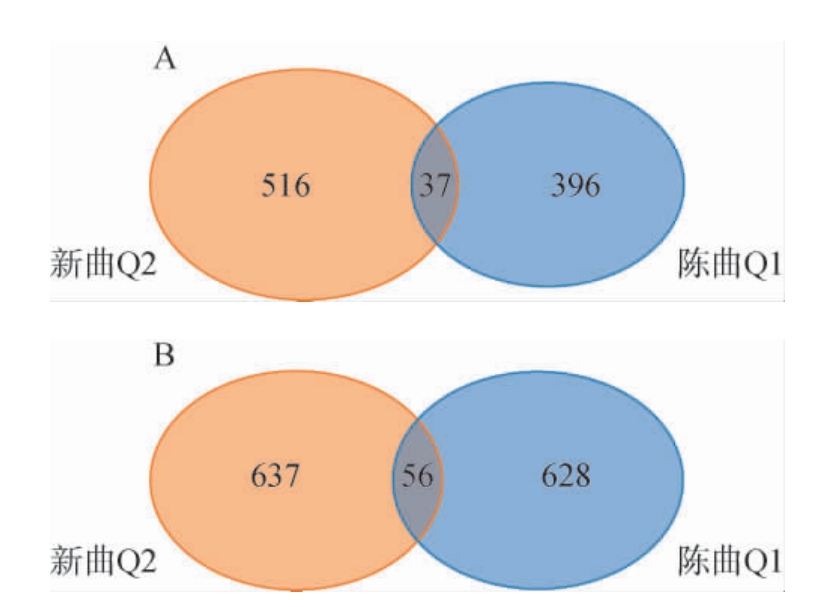
图1 酱香型大曲新曲和陈曲真菌(A)和细菌(B)操作分类单元Venn图
Fig.1 Venn diagram of operational taxonomic units of fungi (A) and bacteria (B) in new and aged sauce-flavor Daqu
OTU数稀释曲线验证测序数据量是否足以反映样品中的物种多样性,并间接反映样品中物种的丰富程度以及持续抽样下新物种出现的速率。酱香型大曲新曲和陈曲细菌和真菌OTU数稀释曲线见图2。由图2可知,新曲与陈曲6组样品的真菌和细菌OTU数随着测序条数的加大前期急剧上升,伴随抽取序列数的增加后逐渐平缓。该数据表示样品中有大量真菌物种和细菌物种被发现;当抽检数量超过40 000个序列后曲线趋于平缓,则表示此样品中的真菌物种和细菌物种并不会随测序数量的增加而显著增多,表明测序量饱和足够真实反映不同贮存时间酱香大曲的微生物多样性。
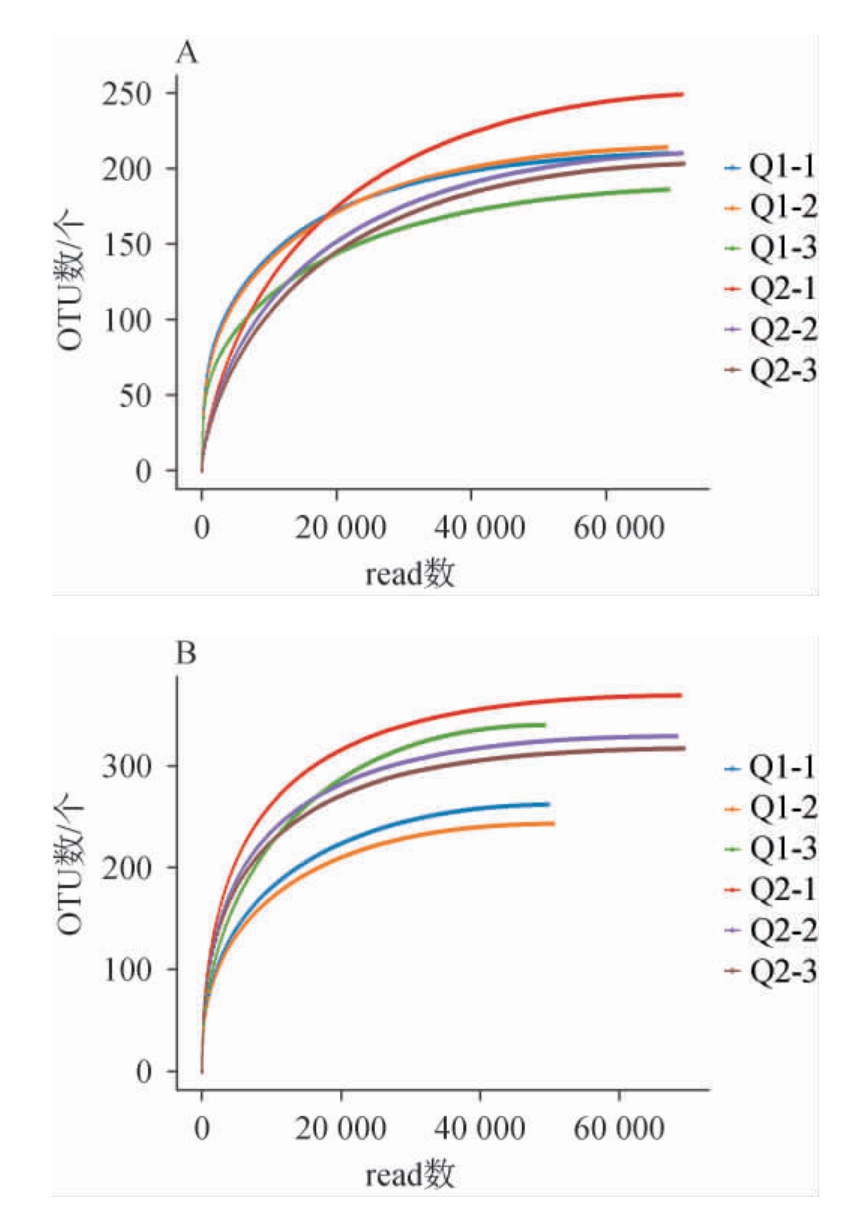
图2 酱香型大曲新曲和陈曲真菌(A)和细菌(B)操作分类单元数稀释曲线
Fig.2 Rarefaction curves of operational taxonomic units of fungi (A)and bacteria (B) in new and aged sauce-flavor Daqu
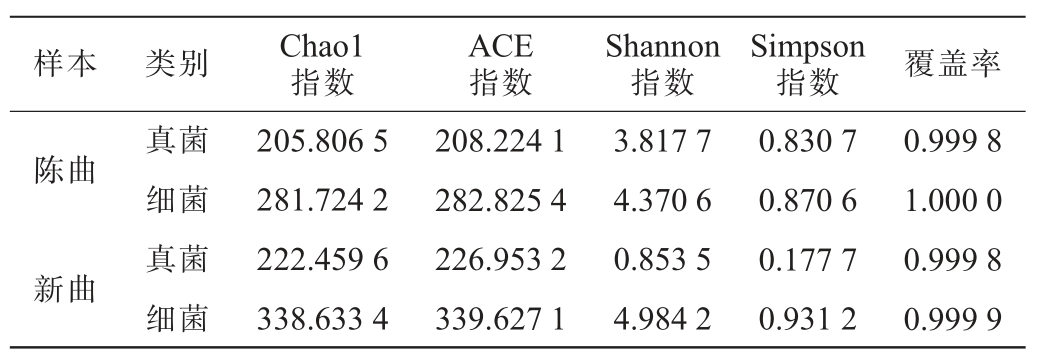
在97%一致性水平上进行酱香型大曲新曲和陈曲细菌和真菌Alpha多样性分析,结果见表2。由表2可知,覆盖率与样本中物种被测出的概率呈正比,各样本覆盖率均>0.999,认为测序结果能够真实反映样品物种丰度及物种多样性。在不同贮存期酱香型大曲中,新曲真菌的Chao1指数、ACE指数均高于陈曲,说明新曲真菌丰富度较陈曲大,陈曲真菌的Shannon指数、Simpson指数较新曲大,表明陈曲的真菌多样性高。而新曲细菌的Chao1指数、ACE指数、Shannon指数、Simpson指数均高于陈曲,表明新曲的细菌丰富度和细菌多样性均高于陈曲,该结果与徐千惠等[21]的研究结果相同。
表2 酱香型大曲新曲和陈曲真菌和细菌Alpha多样性分析结果
Table 2 Alpha diversity analysis results of fungi and bacteria in new and aged sauce-flavor Daqu
2.2.2 Beta多样性分析
主坐标分析(PCoA)通过将测序多维数据进行降维,能直观反映所获得得分及变量得分,从而实现样品真菌多样性相似性可视化[22]。酱香型大曲新曲和陈曲真菌和细菌群落主坐标分析(PCoA)结果见图3。
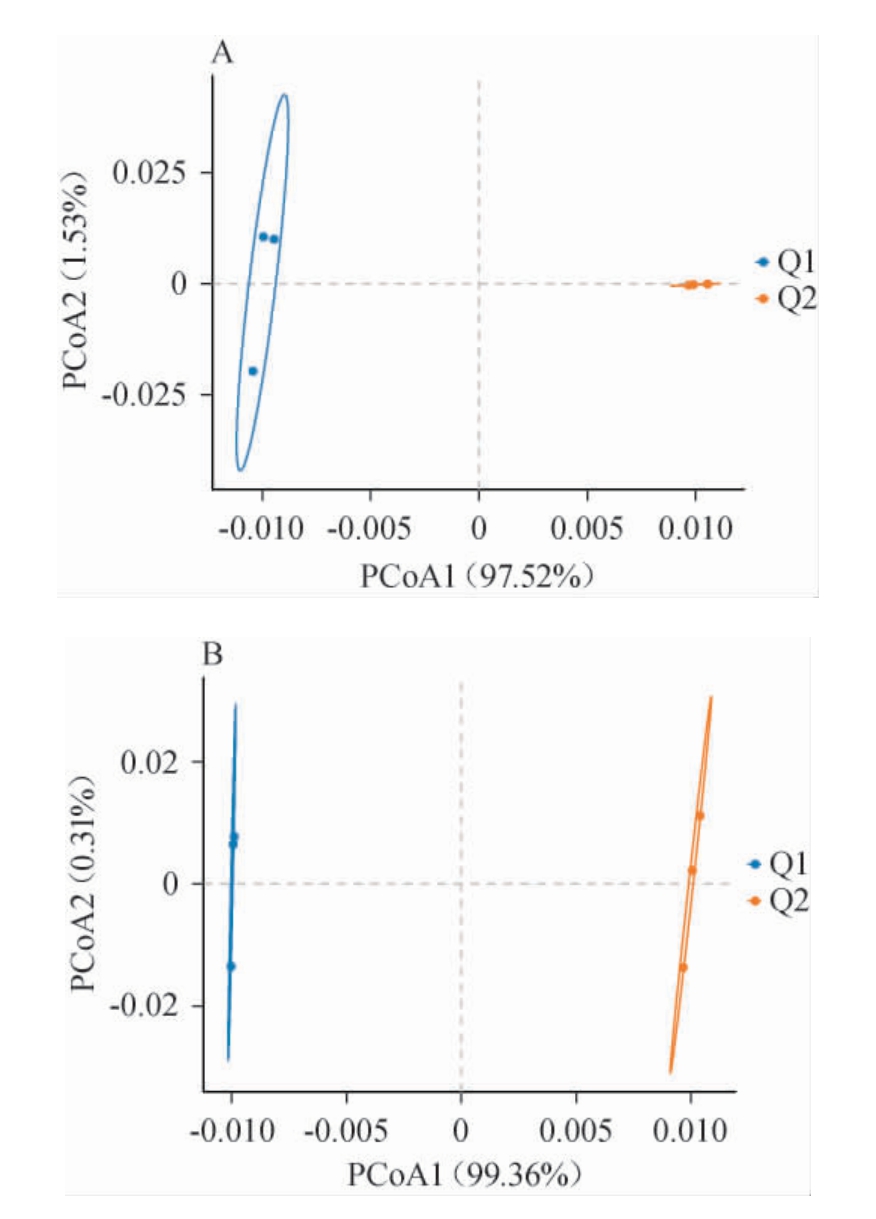
图3 酱香型大曲新曲和陈曲真菌(A)和细菌(B)群落的主坐标分析结果
Fig.3 Principal coordinates analysis results of fungal (A) and bacterial(B) communities in new and aged sauce-flavor Daqu
由图3A可知,PCoA1、PCoA2的方差贡献率分别为97.52%、1.53%,累计方差贡献率为99.05%,说明两个主成分能真实、可靠地反映样品的真菌菌群信息。酱香型大曲新曲和陈曲真菌分布在不同象限且距离较远,表明新曲和陈曲真菌差异性较大。由图3B可知,PCoA1、PCoA2的方差贡献率分别为99.36%、0.31%,累计方差贡献率为99.67%,说明两个主成分能真实、可靠地反映样品的细菌菌群信息。酱香型大曲新曲和陈曲细菌分布在不同象限且距离较远,表明新曲和陈曲细菌差异性较大。
2.2.3 基于属水平新曲和陈曲微生物群落结构分析
基于属水平酱香型大曲新曲和陈曲微生物群落结构分析结果见图4。由图4A可知,在真菌水平上,新曲样本的优势真菌属(相对丰度>1%)有嗜热子囊菌属(Thermoascus)(93.1%)、嗜热真菌属(Thermomyces)(1.93%)、曲霉属(Aspergillus)(1.15%)。陈曲样本的优势真菌属(相对丰度>1%)有嗜热子囊菌属(Thermoascus)(37.94%)、红曲霉属(Monascus)(21.07%)、毕氏酵母属(Pichia)(19.51%)、曲霉属(Aspergillus)(8.67%)、米勒酵母属(Millerozyma)(5.96%)、横梗霉属(Lichtheimia)(1.67%)。由图4B可知,在细菌属水平上,新曲样本的优势细菌属(相对丰度>1%)有斯科普利巴克属(Scopulibacillus)(19.26%)、海洋芽孢杆菌属(Oceanobacillus)(16.00%)、枝芽孢杆菌属(Virgibacillus)(15.84%)、克洛普斯泰德氏菌属(Kroppenstedtia)(11.36%)、糖多胞菌属(Saccharopolyspora)(9.73%)、葡萄球菌属(Staphylococcus)(7.91%)、芽孢杆菌属(Bacillus)(3.87%)、高温放线菌属(Thermoactinomyces)(2.67%)。陈曲样本的优势细菌属(相对丰度>1%)包括海洋芽孢杆菌属(Oceanobacillus)(47.02%)、糖多胞菌属(Saccharopolyspora)(16.81%)、芽孢杆菌属(Bacillus)(7.49%)、克洛普斯泰德氏菌属(Kroppenstedtia)(7.27%)、斯科普利巴克属(Scopulibacillus)(6.48%)、枝芽孢杆菌属(Virgibacillus)(2.46%)、魏斯氏菌属(Weissella)(2.22%)、少杆菌属(Paucibacter)(2.32%)。

图4 属水平上酱香型大曲新曲和陈曲真菌(A)和细菌(B)的群落结构
Fig.4 Structure of fungal (A) and bacterial (B) communities of new and aged sauce-flavor Daqu at the genus level
大曲的陈化过程是微生态系统在环境压力下的定向演替与功能重塑过程。真菌群落由新曲中嗜热子囊菌属(Thermoascus)(93.1%)的绝对优势,演变为陈曲中嗜热子囊菌属(Thermoascus)(37.94%)、红曲霉属(Monascus)(21.07%)与毕氏酵母属(Pichia)(19.51%)等多菌属共存的格局,功能由糖化主导转向产酯生香,从而解释陈曲酯化力增强而糖化力下降的现象。细菌群落则从新曲中多种芽孢杆菌共存的结构,经陈化筛选后趋于简化,海洋芽孢杆菌属(Oceanobacillus)相对丰度由16.00%显著上升至47.02%,成为绝对优势菌;斯科普利巴克属(Scopulibacillus)、枝芽孢杆菌属(Virgibacillus)等相对丰度下降,葡萄球菌属(Staphylococcus)等非耐受菌被淘汰,形成更稳定、耐受的群落结构。
2.2.4 基于属水平新曲和陈曲微生物群落LEfSe分析
LEfSe是一种用于发现和解释高维度生物标识的分析工具,能够快速识别出那些在特定组内显著富集且具有较高区分度的物种。LEfSe统计结果的显著差异物种线性判别分析(LDA)得分阈值衡量了某个物种在两组或多组样本间的相对丰度差异。LDA值越大,通常意味着该物种在对应组间的区分度越高,即其对于组间差异的贡献越大。酱香型大曲新曲和陈曲真菌和细菌群落线性判别分析效应大小分析得分阈值分布柱状图见图5。

图5 酱香型大曲新曲和陈曲真菌(A)和细菌(B)群落线性判别分析效应大小分析得分阈值
Fig.5 Score thresholds for linear discriminant analysis effect size analysis of fungal (A) and bacterial (B) communities in new and aged sauce-flavor Daqu
由图5A可知,在真菌群落层面,陈曲样本中属于高丰度菌属的有红曲霉属(Monascus)、毕氏酵母属(Pichia)、曲霉属(Aspergillus)、米勒罗酵母属(Millerozyma)、拉萨姆森菌属(Rasamsonia)、裸囊菌属(Gymnoascus);新曲样本中属于高丰度菌属的是嗜热子囊菌属(Thermoascus)。以上结果表明,造成真菌群落差异的主要原因是嗜热子囊菌属(Thermoascus)的衰退,以及红曲霉属(Monascus)、毕氏酵母属(Pichia)、米勒酵母属(Millerozyma)等功能性生香菌属的崛起,并辅以曲霉属、拉萨姆森菌属、裸囊菌属等构成的新的糖化/水解体系。这是一个产酒到生香的生态功能转变。
由图5B可知,在细菌群落层面,陈曲中的魏斯氏菌属(Weissella)、芽孢杆菌属(Bacillus)、糖多胞菌属(Saccharopolyspora)、海洋芽孢杆菌属(Oceanobacillus);新曲中的枝芽孢杆菌属(Virgibacillus)、斯科普利巴克属(Scopulibacillus)、葡萄球菌属(Staphylococcus)、克洛普斯泰德氏菌属(Kroppenstedtia)是造成细菌群落差异的主要原因,是陈化环境对海洋芽孢杆菌属、芽孢杆菌属、糖多胞菌属和魏斯氏菌属的正向选择,以及对枝芽孢菌属、斯科普利巴克属等菌属的负向淘汰,这个过程的本质是筛选出更耐贮存环境、且其代谢活动有利于风味成熟的菌群。
2.3 理化指标、酿造特性与微生物群落相关性分析
曼特尔检验(Mantel Test)是一种统计检验,主要用于评估两个矩阵之间的相似性或相关性。通过曼特尔检验分析酱香型大曲新曲和陈曲理化指标,酿造特性与微生物群落间的相关性,结果见图6。由图6可知,真菌群落和酸度、水分含量、糖化力、发酵力、酯化力呈显著负相关(P<0.05),这与刘敏芳等[22]对后火曲的研究结果一致;细菌和糖化力呈极显著正相关(P<0.01),与液化力和酯化力呈显著负相关(P<0.05),这与孙亮霞等[23]对中高温大曲的研究结果一致。
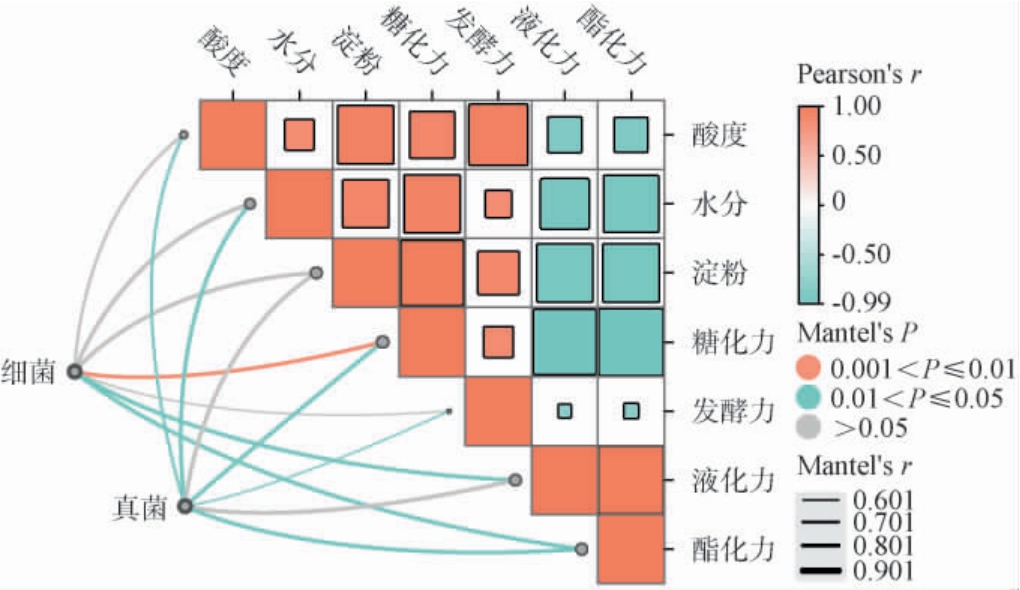
图6 酱香型大曲新曲和陈曲真菌、细菌群落与理化指标、酿造特性相关性分析
Fig.6 Correlation analysis between fungal,bacterial communities and physicochemical indexes,brewing characteristics of new and aged sauce-flavor Daqu
P<0.05表示显著相关;P<0.01表示极显著相关。
对酱香型大曲新曲和陈曲优势微生物群落与理化指标,酿造特性进行冗余分析(redundancy analysis,RDA),结果见图7。由图7A可知,优势真菌群落中,嗜热子囊菌属(Thermoascus)与糖化力、发酵力呈正相关,是新曲产酒功能的核心菌属;红曲霉属(Monascus)、毕氏酵母属(Pichia)和米勒酵母属(Millerozyma)则与酯化力和酸度紧密相关,共同构成陈曲的生香微生物群。真菌群落实现了从糖化发酵型向酯化生香型的功能重塑[24-25]。由图7B可知,优势细菌群落中,斯科普利巴克属(Scopulibacillus)等与新曲糖化力、发酵力呈正相关,而海洋芽孢杆菌属(Oceanobacillus)和芽孢杆菌属(Bacillus)则与糖化力、发酵力呈负相关。水分含量与糖化力、发酵力正相关。结果表明,糖化力与发酵力是驱动细菌群落结构的主要因子,细菌群落功能由协同产酒转向生香与适应性生存[26-27]。
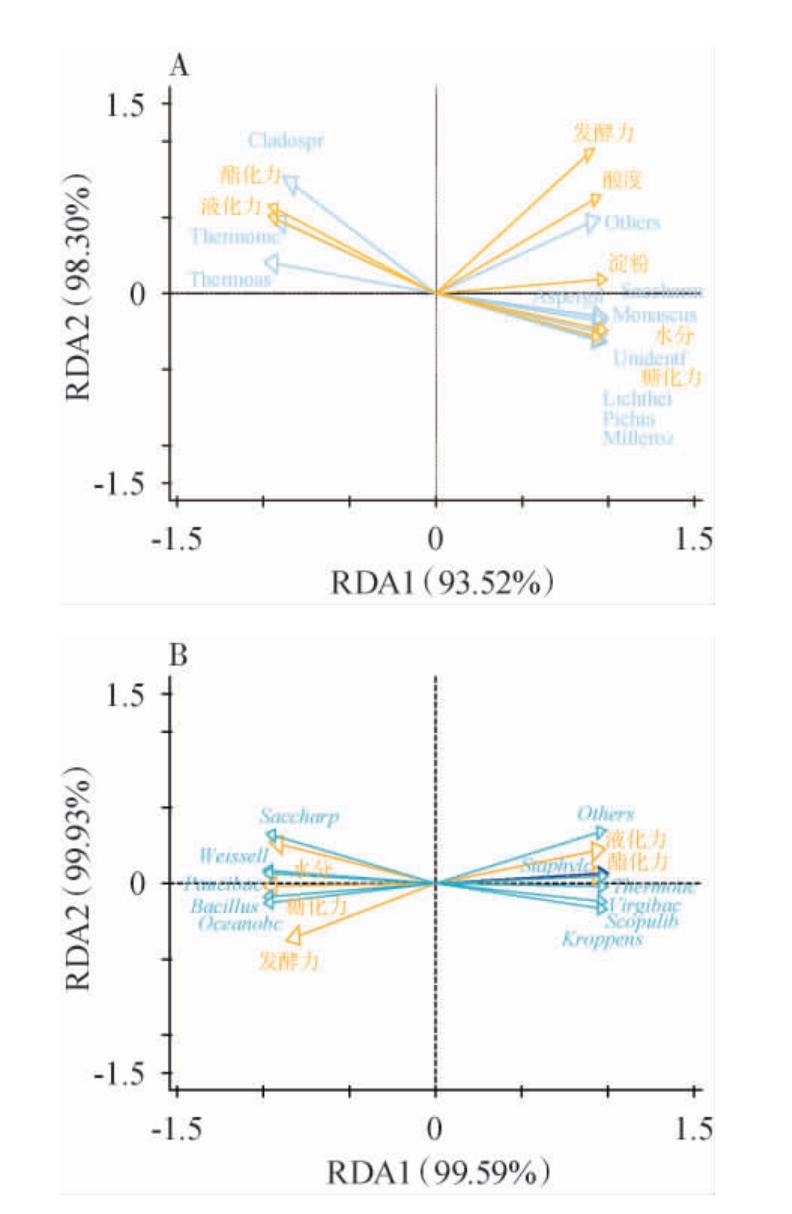
图7 酱香型大曲新曲和陈曲优势真菌(A)、优势细菌(B)群落与理化指标、酿造特性的冗余分析
Fig.7 Redundancy analysis between dominant fungal (A),dominant bacterial (B) communities and physicochemical indexes,brewing characteristics of new and aged sauce-flavor Daqu
3 结论
本研究采用高通量测序分析对比新曲和陈曲的真菌群落结构,并分析其与其理化指标、酿造特性之间的关联性。结果表明,陈化过程驱动大曲发生显著的理化与酶活功能重塑。新曲凭借其丰富的微生物区系,表现出极高的糖化力与发酵力[499.20 mg/(g·h)和0.56 g/(0.5 g·72 h)],是酿造的产酒动力;而陈曲则凭借其特异性的功能菌群,呈现出显著增强的酯化力与液化力[7.00 g/(50 g·7 d)和0.48 g/(g·h)],成为关键的生香核心。微生物多样性分析显示,新曲具有更高的真菌丰富度,而陈曲真菌群落均匀度与多样性更高。微生物群落结构分析显示,陈化过程驱动了大曲微生态系统的显著演替。在真菌群落层面,陈曲从新曲中由嗜热子囊菌属(Thermoascus)绝对主导的单一样性结构,演替为以嗜热子囊菌属(Thermoascus)、红曲霉属(Monascus)、毕氏酵母属(Pichia)和米勒酵母属(Millerozyma)等多菌属共存的、均匀度更高的多元化结构。细菌群落则经环境筛选趋于简化,海洋芽孢杆菌(Oceanobacillus)成为绝对优势菌。相关性分析结果显示,嗜热子囊菌属与糖化力、发酵力呈正相关,是产酒功能的核心执行者;而红曲霉属、毕氏酵母属等与酯化力及酸度紧密关联,构成了陈曲的生香微生物功能群。
本研究从微生态层面证实了“新陈曲配伍”这一传统经验的科学性,其为协调酿造过程中产量与质量的矛盾提供了关键工艺支撑。这一认识对于指导大曲质量标准化评价与生产工艺的精准调控具有重要的理论与实践意义。
[1] 国家市场监督管理总局,国家标准化管理委员会.GB/T 10781.4—2024白酒质量要求 第4部分:酱香型白酒[S].北京:中国标准出版社,2024.
[2] 陈蒙恩,赵聪,韩素娜,等.基于高通量测序的陶融型大曲微生物群落结构分析[J].食品科学,2021,42(8):106-113.
[3] 蒋英丽,聂宏芳,邓皖玉,等.酱香高温大曲贮存期质量变化规律的分析研究[J].酿酒科技,2022(2):61-64,68.
[4] 沈怡方.白酒生产技术全书[M].北京:中国轻工业出版社,2005:86-87.
[5] 段旭林,冯杰利,田栋伟,等.酱香型白酒品质提升技术研究进展[J].食品工业科技,2025,46(20):478-487.
[6] 任海伟,李云帆,阿丽米热·克热穆,等.不同等级金徽酒大曲贮藏过程中的细菌群落演替规律和组装机制[J].食品科学,2025,46(10):108-119.
[7] 吴成,王春晓,王晓丹,等.高通量测序技术在酿酒微生物多样性研究中的应用[J].食品科学,2019,40(3):348-355.
[8] ZHOU Y,LI Y,DONG Y,et al.Microbial community of Nongxiangxing Daqu during storage: microbial succession,assembly mechanisms and metabolic functions[J].J Sci Food Agr,2025,105(7):3665-3678.
[9] 罗方雯,黄永光,涂华彬,等.基于高通量测序技术对茅台镇酱香白酒主酿区域酵母菌群结构多样性的解析[J].食品科学,2020,41(20):127-133.
[10] HE M W,JIN Y,ZHOU R Q,et al.Dynamic succession of microbial community in Nongxiangxing Daqu and microbial roles involved in flavorformation[J].Food Res Int,2022,159(9):111559.
[11] 中华人民共和国工业和信息化部.QB/T 4257—2011酿酒大曲通用分析方法[S].北京:中国轻工业出版社,2011.
[12] MOUROUZIDOU S,VERESOGLOU D S,MONOKROUSOS N.A meta-analysis on microbial diversity responses to phytoremediation[J].Environ Monit Assess,2025,197(11):1261.
[13] XIONG S,LUO Y,ZHANG J.Constipation and oral microbiome diversity: A cross-sectional nhanes analysis[J]. Int Dent J,2025,75(S1):106053.
[14] GAO J,LIU W,LI F,et al.Investigation and analysis of microbial diversity in rice husk-based fermentation bed material[J]. Agriculture,2025,15(17):1828.
[15] ANU K,KUMARI S,CHOUDHARY G,et al.Microbial diversity analysis of Chumathang geothermal spring,Ladakh,India[J].Braz J Microbiol,2024,55(2):1545-1555.
[16] LIU Y Y,CHEN X C,LI F X,et al.Analysis of microbial diversity and metabolites in sauerkraut products with and without microorganism addition[J].Foods,2023,12(6):1164.
[17] YOGITA R,PRANAV P,MADHURA C,et al.Diversity analysis of culturable epiphytic microbial consortia of table grape berry surface[J].Food Biotechnol,2023,37(1):54-73.
[18] 唐佳代,王龙,赵益梅,等.多组学解析酱香型大曲空间异质性[J].食品科学,2025,46(16):126-134.
[19] 贵州省质量技术监督局.DB52/T 871—2014酱香型白酒酿酒用大曲[S].贵阳:贵州人民出版社,2014.
[20] 冯智伟,郭松波,孙朋朋,等.酱香型白酒高温大曲贮曲过程理化性质与微生物演替规律分析[J].中国酿造,2024,43(9):44-49.
[21] 徐千惠,饶家权,邹永芳,等.浓香型大曲贮存期微生物群落演替及代谢产物的变化机制[J].食品科学,2023,44(22):225-234.
[22] 刘敏芳,王昊乾,唐艺婧,等.后火曲制作过程中理化、生化指标和微生物菌群变化及其相关性分析[J].中国酿造,2023,42(5):70-77.
[23] 孙亮霞,王生艳,林一心,等.中高温大曲贮存期间理化指标及微生物群落动态分析[J].食品与发酵工业,2025,51(7):122-128.
[24] 吴正坤,刘蒲临,杨团元,等.不同贮存期高温大曲微生物群落演替与理化指标相关性分析[J].中国酿造,2023,42(7):160-166.
[25] 古翀羽,冉茂芳,魏阳,等.不同配料青稞大曲理化特性与微生物群落相关性研究[J].食品与发酵工业,2021,47(22):126-135.
[26] 邓阿玲.酱香大曲制曲微生态群落演替及其品质影响机制解析[D].贵阳:贵州大学,2024.
[27] 戴奕杰,敖晋滔,王英,等.贵州不同产地大曲及酱香型白酒第四轮次酒醅发酵过程中细菌群落演替规律[J].中国酿造,2025,44(10):171-177.