窖泥作为浓香型白酒发酵的基础物质,在长期的培育过程中形成复杂的微生态结构,为各种微生物生长提供了良好的生长环境[1]。窖泥中的酶对窖池环境变化异常敏感,其活性主要受窖泥养分状况和窖泥理化性质等因素共同调控,即同种酶对不同环境因子响应不同[2]。如窖泥中脲酶与蛋白酶是参与氮循环的关键酶,能够在有机氮转化为无机氮的过程中发挥重要作用[3]。β-1,4-葡萄糖苷酶(β-1,4-glucosidase,BG)和纤维二糖水解酶(cellobiohydrolase,CBH)在窖泥碳降解中参与纤维素分解过程;β-N-乙酰氨基葡萄糖苷酶(β-N-acetylglucosaminidase,NAG)可水解窖泥氮循环过程中的几丁质和肽聚糖两种重要底物;酸性磷酸酶(acid phosphatase,ACP)可参与窖泥磷循环过程中磷酸多糖和磷酸酯的水解,使之转化为可供吸收利用的无机磷[4],而多酚氧化酶(phenol oxidase,POX)和过氧化物酶(peroxidase,PER)通过微生物排泄或裂解进入环境,参与腐殖质中的丹宁和木质素降解、腐殖化、碳矿化和溶解有机碳输出等关键功能[5],它们控制着窖泥中碳、氮、磷养分的循环。韩光等[6]通过对窖泥酶活性与微生物数量之间的研究发现随窖龄增加,窖泥酶活性与微生物数量均呈上升趋势,分析表明窖泥酶活性可以作为影响窖泥中微生物活性的重要因素。有研究表明,酸性磷酸酶的活性与窖泥中部分微生物呈正相关关系,功能菌产生的功能酶也是浓香型白酒形成独特风味的关键因素[7]。长期的酿造环境使得窖池中微生物群落演化趋于稳定,窖泥渐趋老熟,不同微生物在代谢中形成浓香型白酒的独特风味物质,而这些物质在长期的发酵过程中与窖泥融为一体,从而赋予成品酒独特的香气和口感[8],因此窖泥中微生物的酶活性可作为评价窖泥质量的重要指标之一。
近几年关于窖泥酶活性的研究多是围绕淀粉酶、蛋白酶以及酯化酶等,而对与氮、磷循环相关酶以及氧化酶等的研究相对较少,不同窖龄的窖泥由于不同的熟成度所产生的菌种数量和窖泥的酶活性不同,这些不同将影响所产白酒的品质[9],本研究通过窖龄与空间异质性对浓香型白酒窖泥理化性质和参与碳、氮、磷循环的酶活性的影响,明确窖龄增长驱动的有机质稳定化(全氮(total nitrogen,TN)与δ13C累积、腐殖酸(humic acid,HA)降低)与孔隙结构优化(孔隙度与连接性提升)的关联。本研究不仅深化了对浓香型白酒发酵微生态的认识,也为传统酿造技艺的标准化、智能化升级提供了理论支撑与技术突破口,对推动中国白酒产业高质量发展具有重要战略价值。
1 材料与方法
1.1 材料与试剂
1.1.1 原料
窖泥样:取自泸州老窖浓香型白酒窖池新建窖池群和百年老窖池。
1.1.2 化学试剂
氢氧化钠(分析纯):天津市鹏坤化工有限公司;焦磷酸钠(分析纯):湖北七八九化工有限公司;重铬酸钾(分析纯):湖北振华化学股份有限公司;试亚铁灵指示剂、4-甲基伞形酮α-D-吡喃葡萄糖苷、4-甲基伞形酮基β-D-纤维二糖苷(均为分析纯):上海阿拉丁生化科技股份有限公司;浓硫酸(分析纯):江苏阳恒化工有限公司;硫酸亚铁铵指示剂(分析纯):广州众泽生物科技有限公司;无水乙酸钠(分析纯):上海源叶生物科技有限公司;4-甲基伞形酮磷酸酯(分析纯):深圳赛尔玛生物技术有限公司;4-甲基伞形酮-β-D-葡糖苷(分析纯):深圳市优里生物科技有限公司;左旋多巴(分析纯):北京百灵威科技有限公司;4-甲基伞形酮(色谱纯):百盈利创生物科技(北京)有限公司。
1.2 仪器与设备
QuantumGXX射线显微CT:美国PerkinElmer公司;vario MACRO cube元素分析仪:德国Elementar公司;Varioskan LUX酶标仪:美国赛默飞公司;Xpert-TOC/TNb总有机氮分析仪:荷兰TE公司;ZQPL-200立式振荡培养箱:天津市莱玻特瑞仪器设备有限公司;DHG-9240A电热鼓风恒温干燥箱:上海楚定分析仪器有限公司;UPT-II系列落地式超纯水机:西安优普仪器设备有限公司。
1.3 方法
1.3.1 窖泥样品采集与预处理
窖泥分为3年、40年和百年3个窖龄(标记为H、A、B),除3年窖龄采集5口窖池,其余每个窖龄采集3口窖池,共计11口窖池。分别采集窖壁上层、窖壁下层和窖底3个不同空间位置的窖泥(分别标记为T、L、D),为消除窖池不同位置窖泥的异质性,每个位置取不同点的3个样品为对照,每个点取200 g窖泥,混合均匀共计600 g,作为1个代表性样品,重复上述操作依次完成取样,同时使用环刀在每口窖池采集底泥用于窖泥容重的测定。采集完样品后迅速放入样品箱中冷藏运回,将鲜样分为两份,其中一份过2 mm筛网后分别放入4 ℃、-20 ℃、-80 ℃的冰箱保存备用。另一份在室内自然风干,风干土过0.25 mm的筛网,筛后保存备用。
1.3.2 窖泥理化指标测定方法
将过筛后的新鲜窖泥样品使用X射线显微CT进行扫描,使用开源软件ImageJ(版本:1.53t)进行CT数字图像处理及窖泥孔隙定量分析,得出窖泥孔隙度、孔隙紧密度、连接性、分形维数和各向异性指标。
容重:使用100 cm3环刀采集窖泥,用烘干法得出窖泥容重(bulk density,BD);pH值:参考刘义会等[8]的方法测定;含水量(soil water content,SWC):参考HJ 613—2011《土壤干物质和水分的测定重量法》[10]进行测定;窖泥全碳(total carbon,TC)、TN以及碳同位素(δ13C):使用元素分析仪进行测定;灰分(ash content,Ash):采用热重法进行测定;HA:参照GB/T 34766—2017《矿物源腐殖酸肥料中可溶性腐殖酸含量的测定》[11]进行测定。
1.3.3 窖泥酶活性的测定
采用酶标仪测定酸性磷酸酶(ACP),β-1,4-葡萄糖苷酶(BG),纤维二糖水解酶(CBH),β-N-乙酰氨基葡萄糖糖苷酶(NAG),多酚氧化酶(POX)和过氧化物酶(PER)6种酶的活性。其中,ACP、BG、CBH和NAG为水解酶,POX和PER为氧化酶。称取2g窖泥,加入100mL乙酸钠缓冲液(50mml/L,pH=5),放入搅拌子在搅拌器上搅拌1 min,制备成窖泥悬浮液。
水解酶活性测定:将乙酸钠缓冲液作为空白对照组、乙酸钠缓冲液和标准溶液混合液作为参考对照组、乙酸钠缓冲液和底物混合液作为阴性对照组,将窖泥悬浮液和乙酸钠缓冲液混合作为酶对照组,将窖泥悬浮液和标准溶液混合作为淬火对照组,将窖泥悬浮液和底物混合作为样品组,分别对其进行培养。上机测定前在酶标板中加入一定量NaOH(1 mol/L),其反应时间不超过2 min,用酶标仪在365 nm波长激发,并测定其在450 nm处的荧光度值,计算公式如下:

式中:100 mL为窖泥悬浊液体积;0.2 mL为添加的窖泥悬浊液或缓冲液体积;1.0 g为窖泥样品质量;0.5 μmol为每个孔添加的底物量;x为反应时间,h。
氧化酶活性测定:将窖泥悬浮液和乙酸钠缓冲液混合作为对照组,将窖泥悬浮液和底物混合作为样品组,用乙酸钠缓冲液作为空白组,乙酸钠缓冲液和底物混合作为阴性对照组,过氧化物酶样品组中额外加入H2O2,分别对其进行培养,将培养好的样品抽取一定量的上清液放入新的酶标板中,用酶标仪在460 nm波长下测定其吸光度值,计算公式如下:

具体研究测定方法参考SAIYA-CORK K R等[12]的方法。
1.3.4 数据处理
使用Excel 2021进行数据的初整理。使用SPSS 27先对所有数据进行正态分布检验,对不服从正态分布的数据进行对数转换使其满足正态分布。使用单因素方差分析、最小显著性差异法和邓肯多重范围检验,检验不同窖龄和不同位置的窖泥理化性质以及酶活性的差异性。利用R4.3.3中corrplot包绘制相关系数热图。利用Canoco 5.12对窖泥酶活性与窖泥理化因子进行冗余分析(redundancy analysis,RDA),揭示窖泥理化因子对酶活性的变异的解释程度。使用Origin 2021绘制柱状图和箱型图。图表中的数据均为“平均值±标准误差”。
2 结果与分析
2.1 不同窖龄窖池间窖泥理化性质的差异
2.1.1 不同窖龄窖泥容重、孔隙紧密度、孔隙度、连接性、分形维数、各向异性差异
不同窖龄窖泥容重、孔隙紧密度、孔隙度、连接性、分形维数、各向异性的差异见图1。随窖龄增长,不同窖龄窖泥的理化性质变化较为明显。
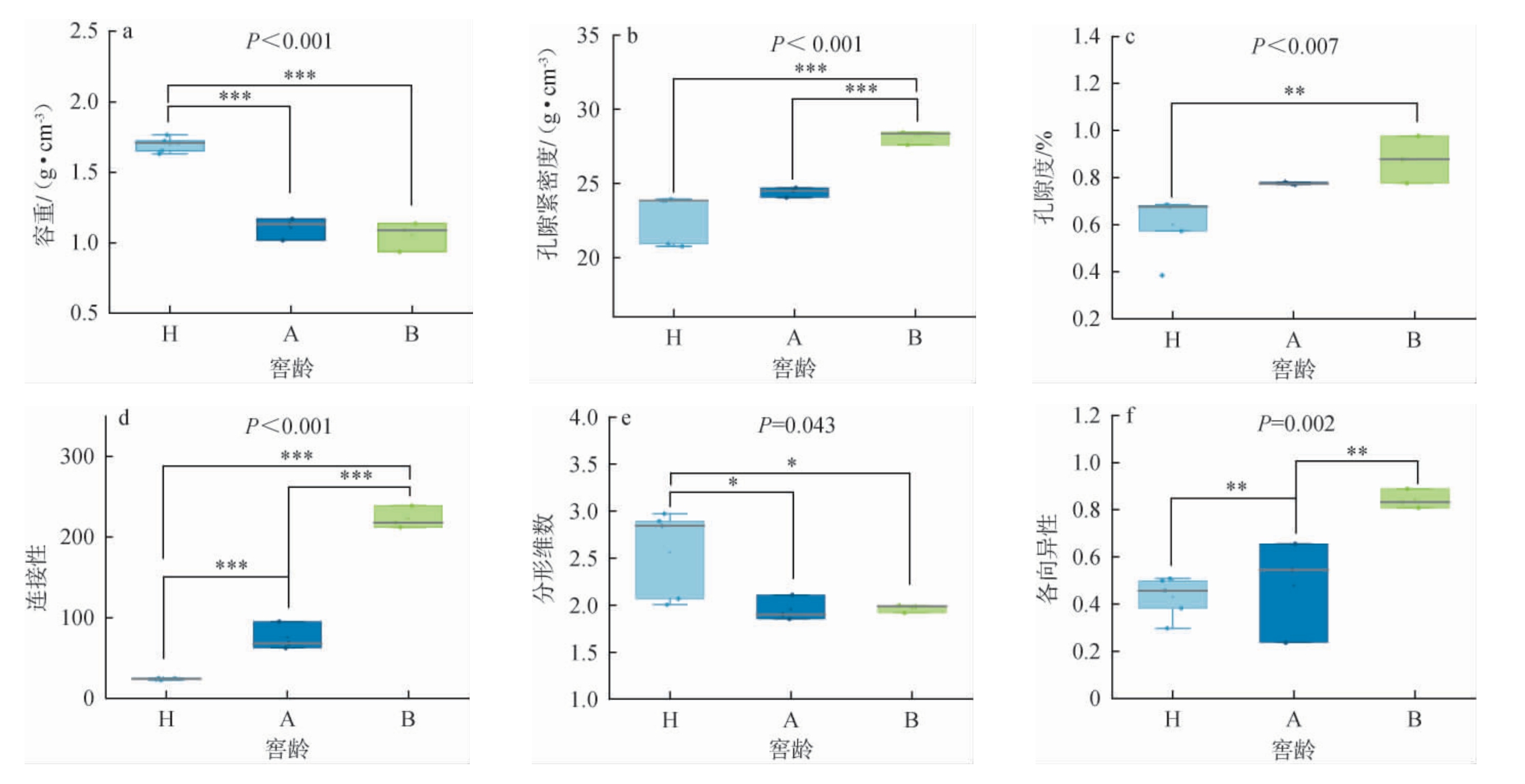
图1 不同窖龄窖泥容重、孔隙紧密度、孔隙度、连接性、分形维数、各向异性的差异
Fig.1 Differences in bulk density,pore tightness,porosity,connectivity,fractal dimension,and anisotropy of pit mud with different pit ages
H:3年窖龄;A:40年窖龄;B:百年窖龄;“*”表示差异显著(P<0.05);“**”表示差异高度显著(P<0.01);“***”表示差异极显著(P<0.001)。下同。
由图1a可知,H窖池容重与A、B两口窖池容重差异极显著(P<0.001),A和B两口窖池容重无明显差异(P>0.05)。由图1b和图1c可知,B窖池孔隙紧密度与H、A两口窖池孔隙紧密度差异极显著(P<0.001)。H窖池与B窖池的孔隙度有显著差异(P<0.01)。由图1d可知,H、A、B三口窖池之间的连接性差异极显著(P<0.001)。由图1e可知,H窖池的分形维数与A、B窖池间差异显著(P<0.05)。由图1f可知,A窖池的各向异性与H、B窖池间有极显著差异(P<0.01)。从整体来看,窖泥的容重和分形维数随窖池窖龄增加而降低,孔隙紧密度、孔隙度、连接性和各向异性随窖池窖龄增加而增加。
通过X射线计算机断层扫描技术,验证随着窖龄的增加,窖泥质地结构发生了明显的变化,随窖泥孔隙逐渐增加,质地更为疏松,具体表现为随着窖龄的增加窖泥的容重和分形维数的数值不断降低,而孔隙度、孔隙紧密度、孔隙连接性和各向异性数值不断增加并在百年窖池中达到最高值。而这一系列的变化可进一步引起不同窖龄的窖泥含水量以及其他理化指标发生变化。
2.1.2 不同窖龄窖泥理化性质差异
不同窖龄窖泥理化性质的测定结果见图2。由图2Ⅰ可知,A、B窖池的pH值与H窖池有显著差异(P<0.05),且H窖池pH值最低为3.64,而A和B窖池的窖泥pH值不显著(P>0.05),说明随着时间推移,窖泥pH值呈先上升后趋于稳定,窖泥逐渐成熟。由图2Ⅱ可知,随窖龄的增长窖泥含水量逐渐增加,B窖池的窖泥含水量最大,说明窖泥年份越长其含水量越高。由图2Ⅲ可知,窖泥中灰分含量在B窖池中含量最高为18.54,但在不同窖池间差异不显著(P>0.05),说明随着窖泥年份增长窖泥的灰分含量变化差异较小。由图2Ⅳ可知,H窖池腐殖酸含量显著高于A、B窖池(P<0.05),为2.41%,而40年窖池和百年窖池的窖泥成熟度高,腐殖酸含量较低。
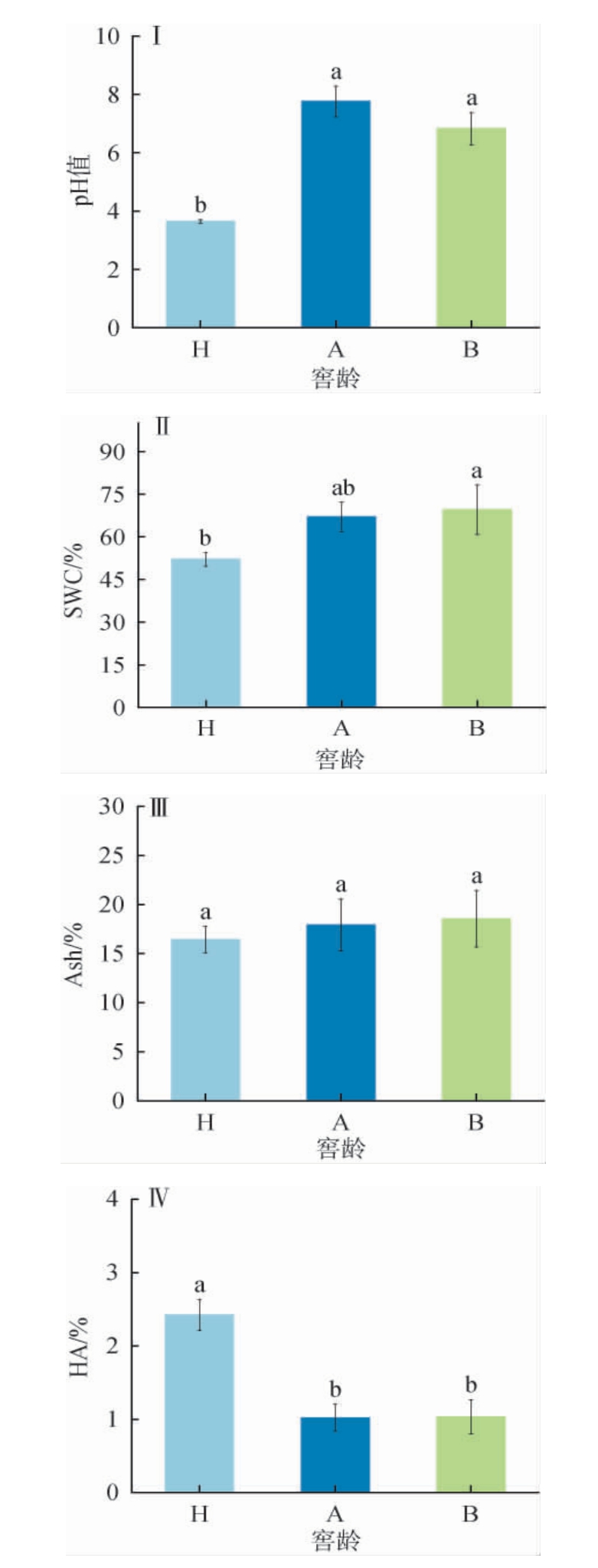
图2 不同窖龄窖泥理化性质的测定结果
Fig.2 Determination results of physicochemical properties of pit mud with different pit ages
不同小写字母表示差异显著(P<0.05)。下同。
在白酒酿造过程中产生的有机酸会影响窖泥的酸碱性[9],这不仅与窖泥中微生物的生长有重要的关系,更对酿酒品质产生重要影响。本研究中发现,窖泥的pH值和水分含量在3年窖龄的窖池中总是低于40年窖池和百年窖池,腐殖酸含量3年窖池高于40年窖池和百年窖池,原因可能为在新窖泥制作过程中,原料偏酸性,且含有大量好氧微生物,在这些微生物生长过程中,产生大量有机酸,从而降低窖泥的酸碱度,而随时间的增长,窖泥逐渐成熟,厌氧微生物增多,其生长代谢时产生的碱性物质增加了窖泥的酸碱度[13-14]。随着窖龄的增加,窖泥的含水量也不断增加,说明窖泥含水量的变化与容重及孔隙度的变化相关。优质窖泥的pH值一般在5~7左右,含水量一般高于40%[15],本研究中,3年窖池和40年窖池的含水量均高于40%,但3年窖池的pH值偏低,40年窖池的pH值偏高,百年窖池的窖泥pH值和含水量为6.82和69.5%,更符合这一标准。
2.1.3 不同窖龄窖泥碳氮相关性质差异
不同窖龄窖泥碳氮相关性质的测定结果见图3。由图3Ⅰ可知,不同窖龄的窖泥之间的TC无显著差异(P>0.05),在百年窖龄中达到最高值。由图3Ⅱ可知,全氮含量随窖池窖龄的增加而增加,百年窖龄中达到最高值,为12.11 g/kg,新窖池中最低;由图3Ⅲ可知,C/N在新窖池中比值最高,其次为百年窖池;由图3Ⅳ可知,H窖池的δ13C显著低于A、B窖池(P<0.05),且δ13C随窖池窖龄的增加而增加,窖龄越大其含量越高,百年窖池的δ13C为-14.21‰。
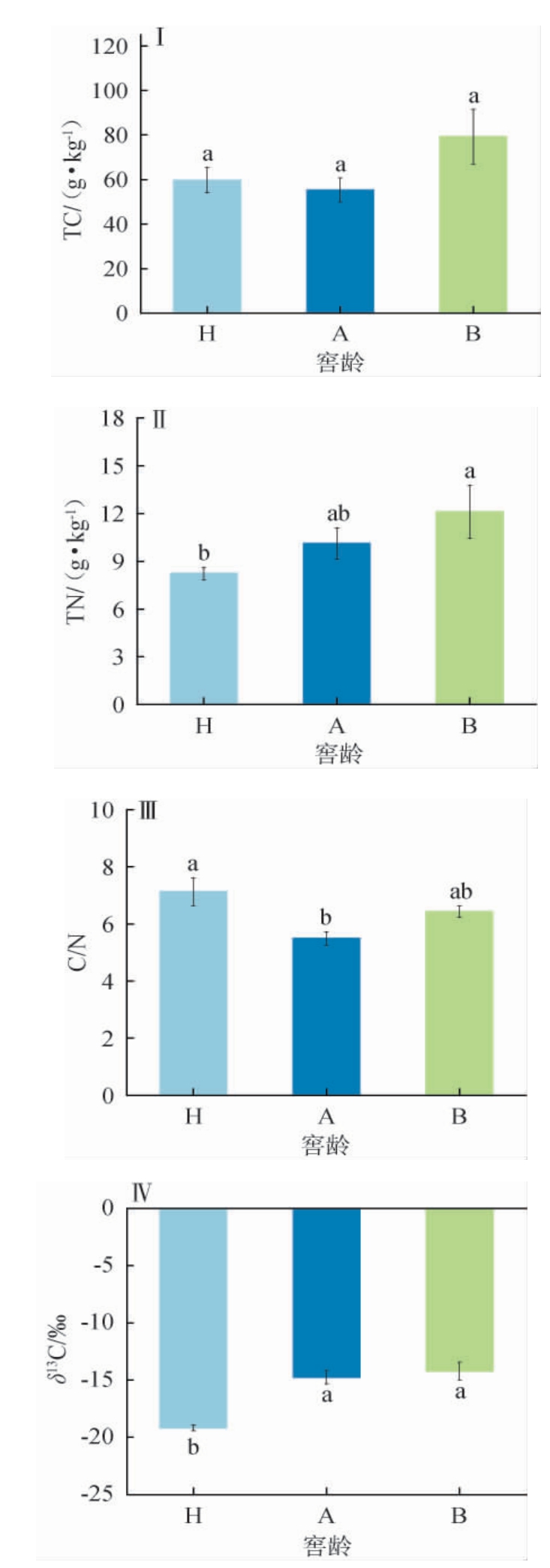
图3 不同窖龄窖泥碳氮相关性质测定结果
Fig.3 Determination results of carbon and nitrogen-related properties of pit mud with different pit ages
本研究中3年窖龄窖泥至百年窖龄窖泥的δ13C平均值为-16.04‰,变化范围为-19.17‰~-14.21‰。随窖龄的增长,窖泥的全氮也呈逐渐增长趋势,全碳和全氮之间具有正相关关系,全碳含量在不同窖龄的窖泥中变化不显著,但与全氮一样均在百年窖龄中达到最高值,而C/N从7.13下降至6.42,氮含量提高和C/N下降有利于窖泥中有机质增加,改善窖泥质地,提高窖泥质量,有利于窖泥中微生物的活动。
综上,不同窖龄间窖泥的理化性质有显著差异,容重、孔隙度、酸碱度、窖泥的含水量腐殖酸以及碳氮等营养物质在百年窖龄的窖泥中数值更为适宜,为微生物生长活动提供有利的生存空间,而新窖泥熟化程度较低,各理化性质均达不到最优水平。
2.2 不同窖龄间窖泥酶活性的差异
不同窖龄窖泥的酶活性测定结果见图4。由图4可知,在窖龄短的H窖池中ACP活性极显著高于A、B窖池(P<0.001)。A窖池中BG和CBH活性显著高于B窖池(P<0.05),但与H窖池差异不显著(P>0.05)。A窖池中NAG活性与H窖池中酶活性差异极显著(P<0.001),与B窖池中酶活性差异高度显著(P<0.01)。H窖池中POX活性与B窖池中的酶活性有显著差异(P<0.05)。PER酶活性在不同窖龄中差异均不显著(P>0.05)。
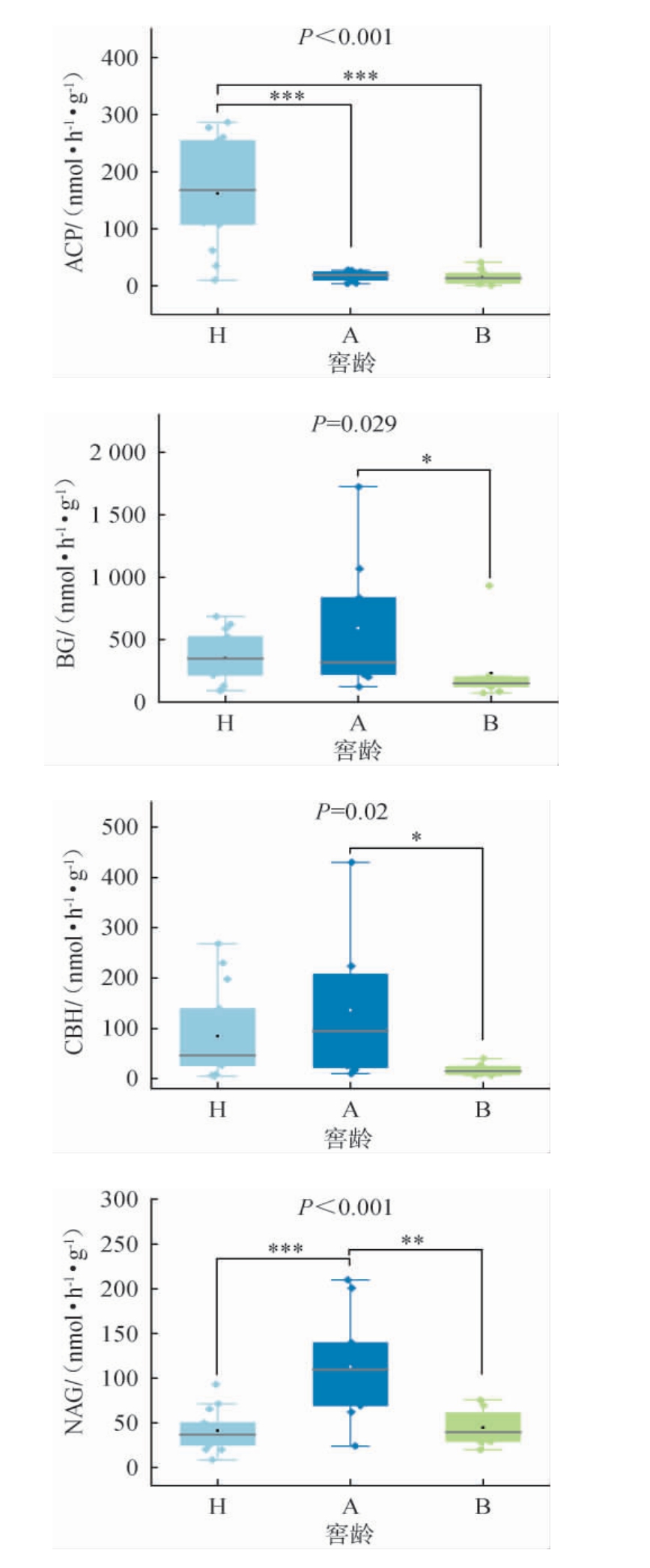
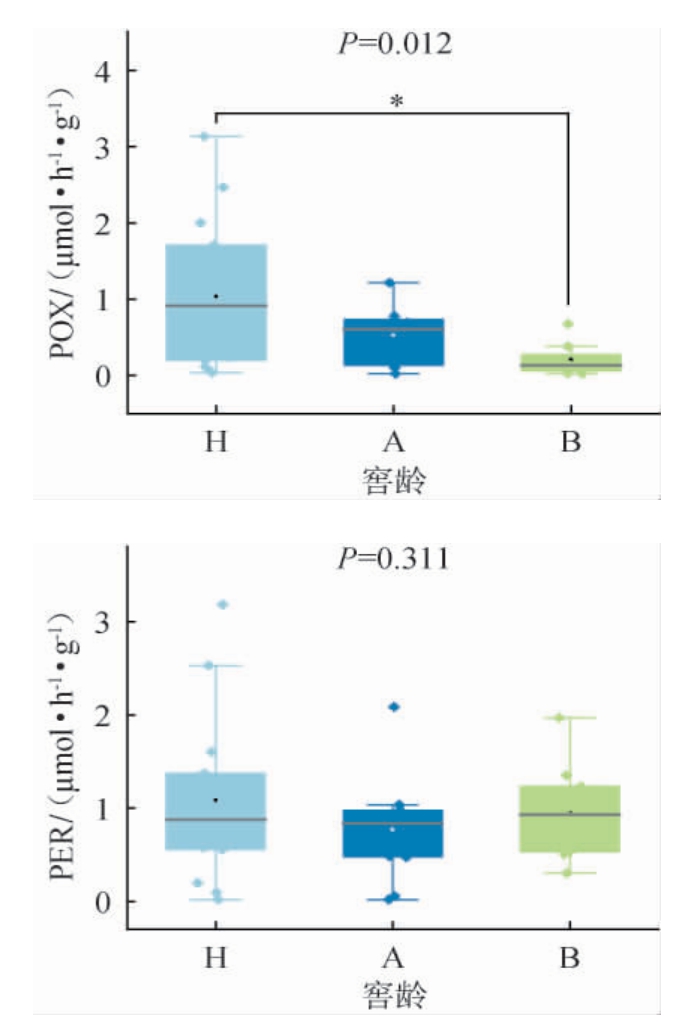
图4 不同窖龄窖泥的酶活性测定结果
Fig.4 Determination results of enzyme activity in pit mud with different pit ages
窖泥中的酶作为其重要且活跃的一部分,它对窖池中的物质和能量循环起着重要的作用,酶本质上是蛋白质,来自于微生物和动植物的活体细胞或残体[16],参与窖泥中化学生物循环,它的活性作为窖泥微生物群落活性表征指标之一[17],能够快速反应窖池中的环境变化,广泛应用于营养物质循环转化状况[18]。窖泥酶活性的变化随窖龄的变化显著,从整体来看,ACP和POX酶活性在年限较短的H窖池中明显更为活跃,而40年窖龄的BG、CBH、NAG酶活性较高,而百年窖池中各个酶活性均较低。
2.3 窖泥理化性质和酶活在不同空间位置的差异
2.3.1 窖泥理化性质在不同空间位置中的差异
窖泥理化性质在不同空间位置的差异见图5。由图5Ⅰ可知,不同窖龄的窖泥在不同空间位置的pH值都有显著差异(P<0.05),其中3年窖龄的窖泥在不同位置中的pH值均低于其他两个窖龄。由图5Ⅱ可知,窖壁上层,不同窖龄的窖泥含水量差异不显著(P>0.05),在窖壁下层和底泥中,不同窖龄的窖泥含水量有显著差异(P<0.05),窖壁下层中百年窖泥的含水量显著高于3年和40年窖龄窖泥,而在底泥中40年窖龄的窖泥含水量显著最高(P<0.05)。由图5Ⅲ可知,不同窖龄的窖泥在窖壁上下层的灰分含量具有显著差异(P<0.05),百年窖泥在窖壁上层灰分含量最低,在窖壁下层灰分含量最高,不同窖龄的窖底泥灰分含量差异不显著(P>0.05)。由图5Ⅳ可知,3年窖龄窖泥的腐殖酸含量在窖壁上层和窖底均显著高于其他两个窖龄(P<0.05),在窖壁下层与其他窖龄间差异不显著(P>0.05)。
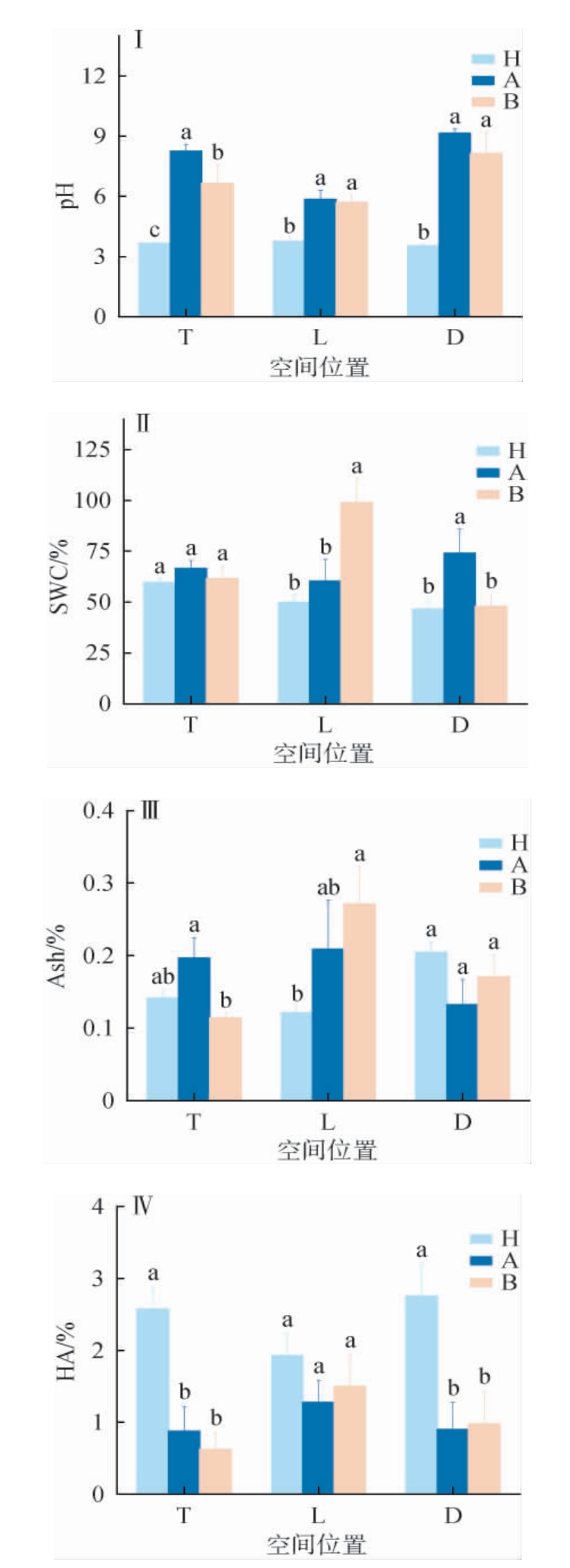
图5 不同空间位置窖泥理化性质的差异
Fig.5 Differences in physicochemical properties of pit mud at different spatial locations
窖泥碳氮相关指标在不同空间位置的差异见图6。由图6Ⅰ可知,不同窖龄窖泥的TC含量在窖壁上层和底层没有显著差异(P>0.05),百年窖泥窖壁下层的TC含量显著高于其他两个窖龄的窖泥(P<0.05);由图6Ⅱ可知,不同窖龄窖泥的TN含量在窖壁上层没有显著差异(P>0.05),百年窖泥在窖壁下层的TN含量显著高于其他两个窖龄的窖泥(P<0.05),3年窖底泥的TN含量显著低于其他两个窖龄窖泥(P<0.05)。由图6Ⅲ可知,窖壁下层中百年窖泥C/N显著高于3年和40年(P<0.05),而在底泥中3年窖泥的C/N显著高于40年和百年(P<0.05)。由图6Ⅳ可知,3年窖泥δ13C在不同空间位置均显著低于其他两个窖龄窖泥(P<0.05),百年窖泥在窖壁上层略低于40年窖泥,在其余两个位置中均为最高。
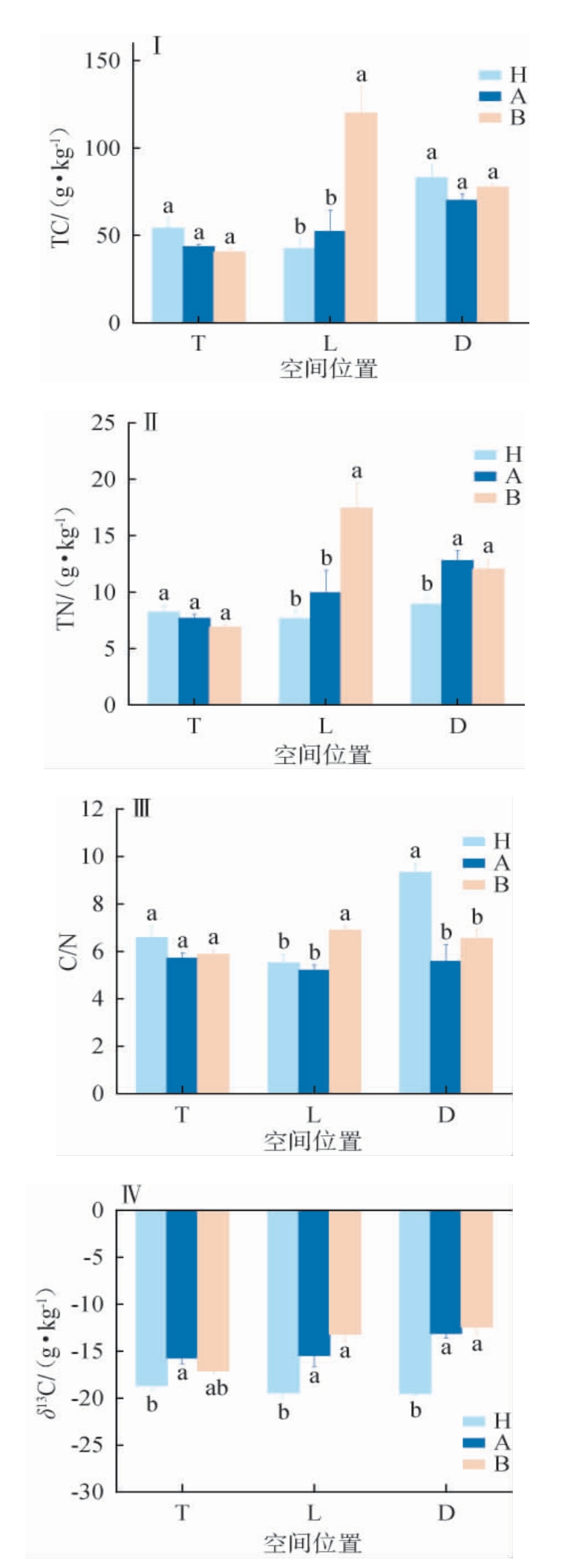
图6 不同空间位置窖泥碳氮相关性质的差异
Fig.6 Differences in carbon and nitrogen-related properties of pit mud at different spatial locations
从不同空间位置看,3年窖龄窖泥的底泥Ash、HA、TC、TN、C/N均高于窖壁。40年窖龄窖泥的pH值和SWC含量在窖壁下层最低,Ash和HA在窖壁下层中含量最高,而TC、TN和δ13C在底泥中最高。百年窖龄窖泥除pH和δ13C外,其他指标均在窖壁下层含量最高。由此可以看出,百年窖泥的熟成度高,因此它的理化因子趋于稳定,由此也影响着窖泥中酶活性在不同空间位置的变化。
2.3.2 窖泥酶活性在不同空间位置中的差异
窖泥酶活性在不同空间位置中的差异见图7。由图7Ⅰ可知,3年窖龄窖泥ACP酶活性在不同空间位置中均最高,40年和百年窖龄窖泥之间没有显著差异(P>0.05),但均显著低于3年窖龄窖泥(P<0.05);由图7Ⅱ可知,窖壁上层40年窖龄窖泥BG酶活性最高,窖壁下层则随窖龄的增加,酶活性显著降低(P<0.05),底泥中3个窖龄窖泥的酶活性差异不显著(P>0.05)。由图7Ⅲ可知,CBH酶活性在窖壁上层和底泥的变化趋势与BG酶活性变化趋势相同,但在窖壁下层中,CBH的酶活性没有显著差异(P>0.05)。由图7Ⅳ可知,40年窖龄窖泥在窖壁上层和窖壁下层NAG的酶活性最高,百年窖泥在底泥中NAG的酶活性最高。由图7Ⅴ和图7Ⅵ看出,POX和PER两个酶活性在不同空间位置中差异不显著(P>0.05)。
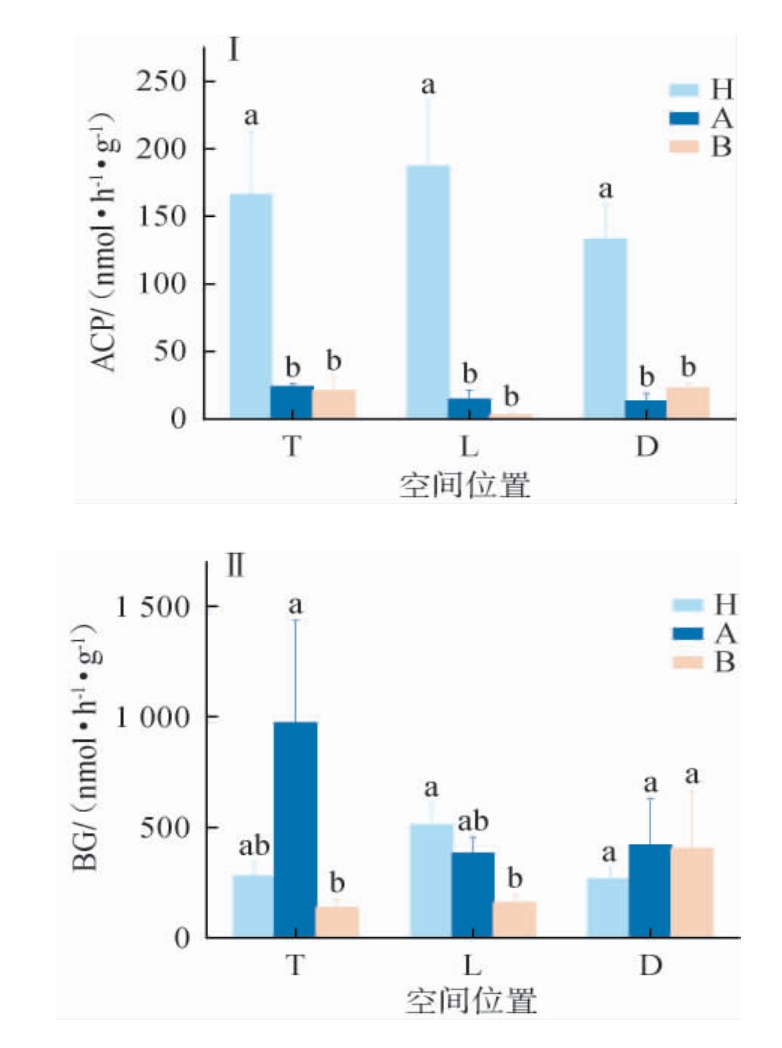
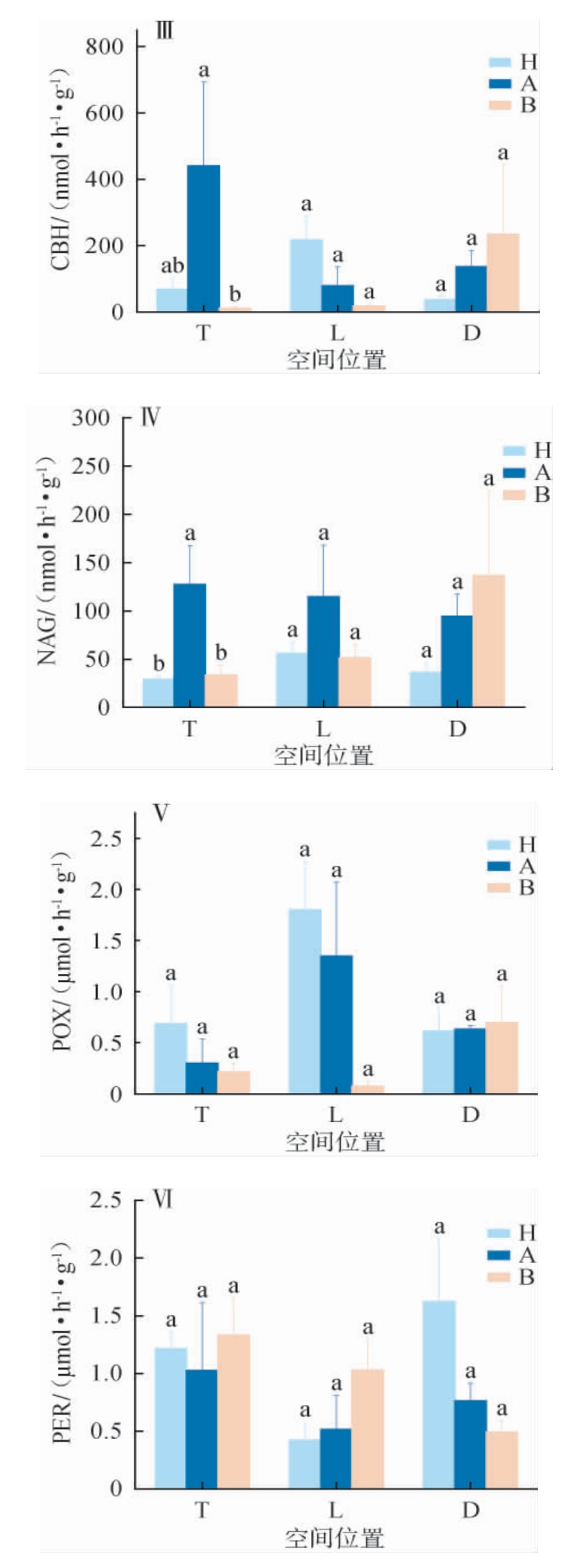
图7 不同空间位置窖泥酶活性的差异
Fig.7 Differences in enzyme activities of pit mud in different spatial locations
通过对窖泥理化性质和不同位置的窖泥酶活性分析发现,3年的窖泥不同位置理化性质和酶活性波动较大,而40年和百年的窖泥酶活性不同位置大体差异不显著,其中40年和百年窖泥的SWC除在底泥中有显著性差异,其余指标的底泥差异性均不显著。表明新窖泥可能由于成熟度不高,在窖泥的驯化过程中,对窖泥微生物进行不断地筛选,以及新窖池中偏酸性的环境和窖泥中存在较高的腐殖酸,利于微生物的生长,微生物活跃的代谢使得窖泥中酶活性较高,从而造成不同位置的酶活性差异较大的现象[3]。而随着窖池窖龄的增长,经过物质沉淀,窖泥的成熟度趋于稳定,因此在底泥中窖龄较长的窖泥没有显著差异性。
2.4 窖池窖泥的理化性质与酶活性的关系
2.4.1 窖池窖泥理化指标间相关性分析
将窖泥中理化指标进行相关性分析,结果见图8。由图8可知,窖泥的pH值与C/N呈显著负相关关系(P<0.05),与腐殖酸和容重(BD)呈极显著负相关关系(P<0.001),与含水量、TN呈显著正相关关系(P<0.05),与δ13C呈极显著正相关关系(P<0.001)。窖泥含水量与容重呈显著负相关关系(P<0.05),与δ13C呈高度显著正相关关系(P<0.01),与TN呈极显著正相关关系(P<0.001)。窖泥的TC和TN呈高度显著正相关关系(P<0.01),窖泥TN与HA和容重分别呈显著负相关关系(P<0.05)与高度显著负相关关系(P<0.01),与δ13C呈极显著正相关关系(P<0.001)。窖泥的C/N与δ13C呈显著负相关关系(P<0.05),与HA和容重呈显著正相关关系(P<.05)。窖泥中灰分的含量与其他指标之间无显著相关性(P>0.05)。窖泥的腐殖酸与δ13C呈高度显著负相关关系(P<0.01),与容重呈极显著正相关关系(P<0.001)。窖泥的δ13C与容重呈极显著负相关关系(P<0.001)。
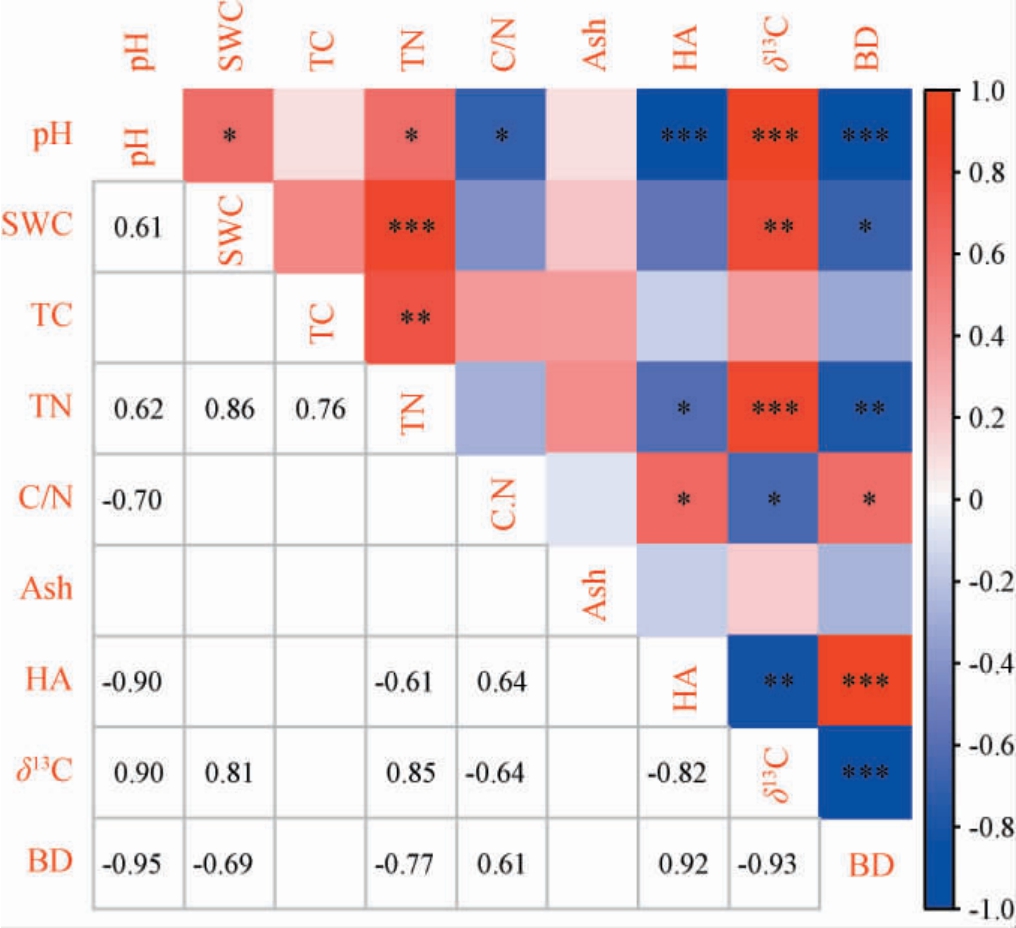
图8 窖泥理化指标间的相关性
Fig.8 Correlation between physicochemical indicators of pit mud
有统计分析均使用了原始同位素值。红色代表正相关关系,蓝色代表负相关关系。
通过相关性分析发现,窖泥的pH与SWC、TN和δ13C呈正相关,与C/N、HA和BD呈负相关,体现出pH调控碳同位素、物理结构稳定性以及碳氮代谢平衡中起到了关键作用。窖泥适宜的水分含量能够保障微生物代谢环境,又能够促进氮素在窖泥中的积累,进而影响酒体中含氮风味物质。TC和TN的正相关性,能够反映出窖泥中微生物对碳氮源的协同利用。δ13C与pH值、含水量、全氮存在正相关关系,而与腐殖酸和C/N存在负相关关系,这可能与腐殖酸中含有较多的脂类有关[19],腐殖酸含量越高,脂类物质越多,其δ13C丰度越低。
2.4.2 窖泥理化性质与酶活性的相关性分析
将窖泥的理化性质与酶活性进行相关性分析,结果见表1。由表1可知,6种酶中只有ACP酶活性和NAG酶活性与窖泥理化性质之间有显著相关性,其余四种酶活性与窖泥理化性质之间没有显著相关性(P>0.05)。其中,ACP酶活性与TN呈显著负相关关系(P<0.05)、与C/N之间呈显著正相关关系(P<0.05),与pH和δ13C呈高度显著负相关关系(P<0.01),与HA和容重之间呈高度显著正相关关系(P<0.01)。NAG酶活性与C/N呈显著负相关关系(P<0.05)。
表1 窖泥理化性质和酶活性间的相关性
Table 1 Correlation between physicochemical properties and
enzyme activity of pit mud
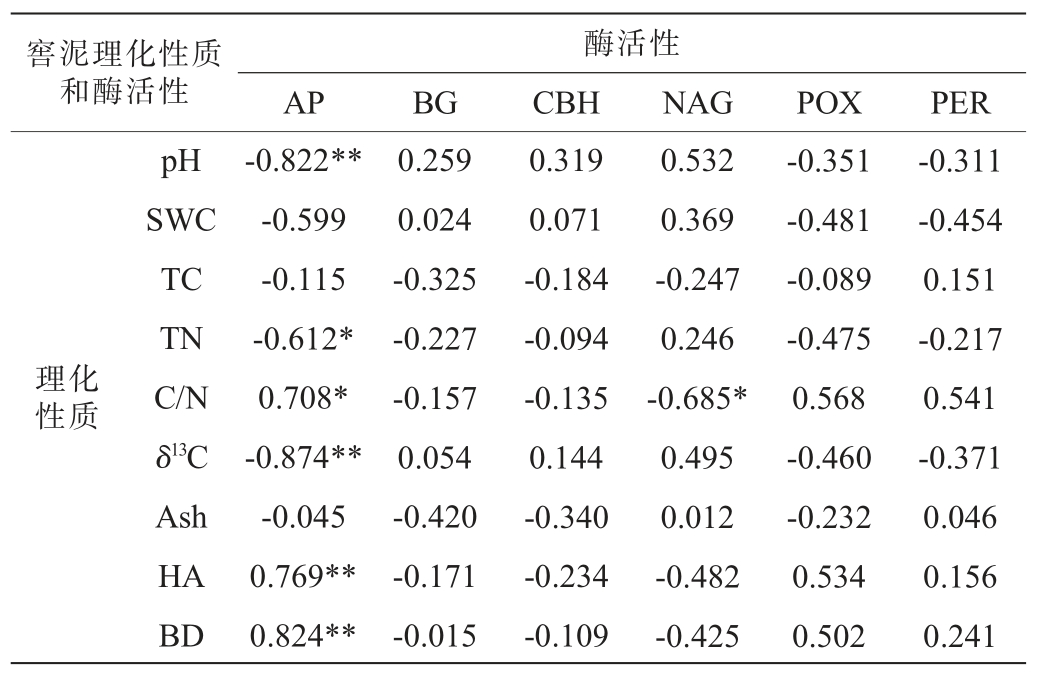
注:“*”表示显著相关(P<0.05);“**”表示极显著相关(P<0.01)。
将本研究中窖泥的六种酶活性作为响应变量,将窖泥的理化因子作为解释变量进行冗余分析(RDA),得出窖泥的理化因子对窖泥酶活性影响的大小,结果见图9。由图9可知,第1轴与第2轴的方差解释率分别为35.98%和31.34%,前两轴共解释总变异的60%以上,从而说明窖泥理化性质对于窖泥酶活性的影响较大。其中,窖泥理化因子对6种窖泥酶活性的解释变量分别为:C/N(27.1%)、pH(17.6%)、δ13C(11.3%)、Ash(7.4%)、TC(6.8%)、BD(5.5%)、TN(4.7%)、SWC(4%)、HA(3.9%),其中的C/N和pH是影响窖泥酶活性的主要因子。
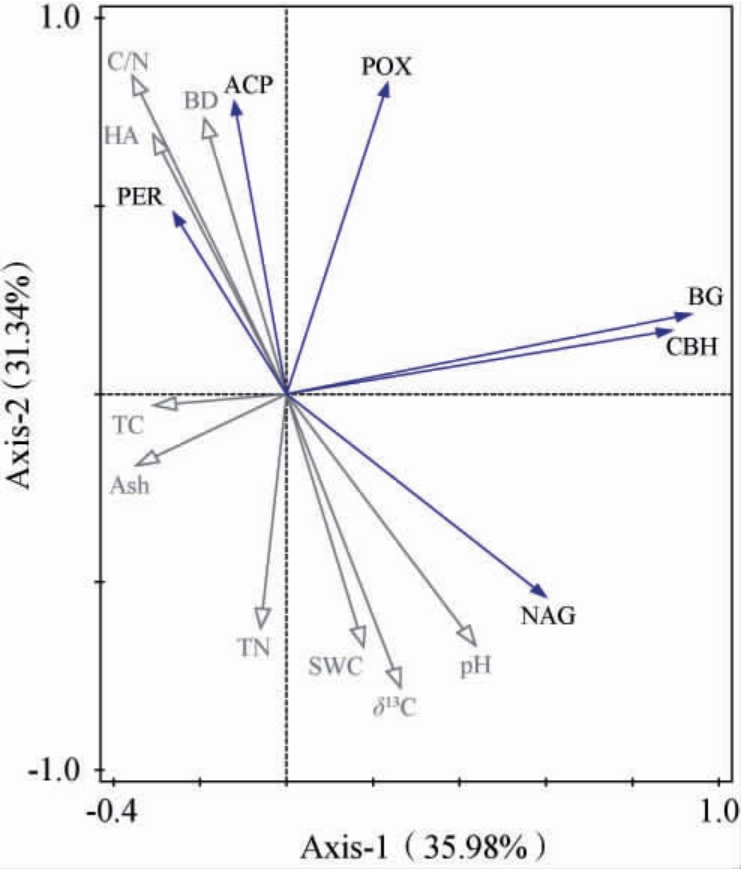
图9 窖泥理化性质和酶活性的冗余分析
Fig.9 Redundancy analysis of physicochemical properties and enzyme activities of pit mud
通过窖泥理化性质与窖泥酶活性相关性分析和RDA分析得出,C/N是影响窖泥酶活性的主要因素,其中NAG酶与C/N呈显著负相关性,ACP酶与C/N呈显著正相关关系,BG和CBH这两种酶活性之间呈显著正相关关系。ACP酶与BD、HA呈显著正相关关系,与pH呈显著负相关关系,这与万红云等[20]研究的部分结果相似,不同的土壤酶活性的最适pH不同,本研究中40年窖龄的窖泥pH值呈碱性,但BG、NAG酶活性相对其他两个来说更高,这与SINSABAUGH R L等[21]的研究结论相反,可能是由于窖池中温度、湿度和复杂的微生物环境下,窖泥中的养分通过影响微生物的生长而间接作用于窖泥酶,使得窖泥酶活性和养分之间会产生关联[22]。XU Z等[23]的研究发现,当土壤养分增加或降低时,土壤酶活性会出现相对复杂的变化。本研究中,百年窖龄的窖泥ACP、BG、CBH、NAG和POX活性相比于其他窖龄的窖泥活性较低,结合百年窖龄的窖泥TC、TN以及含水量等养分物质含量较高,有可能为百年窖龄的窖泥养分利用率高,微生物不需要分泌过多的酶类来满足对养分的需求[24]。窖泥中酶活性除受到窖泥养分、容重、pH、含水量等影响外,还与窖泥质地以及窖泥中微生物类型有关[25]。
3 结论
以四川某名酒厂不同窖龄和不同位置的窖泥为研究对象,分别对窖泥的理化指标及酶活性进行测定,并对其进行相关性分析,发现不同窖龄的窖泥理化性质和酶活性差异较大,养分物质是影响窖泥酶活性的重要因素。新窖泥培育时间短,酸性物质含量较高,含水量和养分物质含量较低,说明窖泥的品质较为普通,而窖泥处于弱酸性环境,该时期不同位置间理化指标和酶活性差异较大,窖泥的酶活性变化活跃,会影响窖泥中微生物的生长从而对生产的酒品质产生影响。老窖泥培育时间长,成熟度高,酸碱度、含水量均处于优质窖泥适宜范围及pH在7左右,含水量高于40%,且老窖泥中养分物质C、N含量较高,酶活性在不同位置中差异不显著,百年窖泥的理化性质和酶活性在窖壁下层数值较高,且在不同空间位置的变化小于新窖泥,说明该时期窖池环境稳定,有利于窖泥中微生物生长发育,窖泥品质优质。窖泥的环境因子对窖泥酶活性的影响较大,维持窖泥中适度的水分和pH有利于窖泥中碳代谢酶的提升,补充有机氮源可以促进窖泥中氮循环,而多酚氧化酶主导腐殖酸成熟,能够为窖泥功能菌构建稳定的生境,是窖泥熟度和风味持久性的关键指标。环境因子和酶的相互作用,为酿酒微生物提供可利用的养分,同时驱动风味物质前体的转化,有利于构建优质窖泥体系,并对白酒的酿造产生积极作用。
[1] CHEN L,LI Y,JIN L,et al.Analyzing bacterial community in pit mud of Yibin Baijiu in China using high throughput sequencing[J].Peer J,2020,8:e9122.
[2]马鹏宇.模拟氮沉降对东北温带典型森林和草原土壤酶活性的影响[D].哈尔滨:东北林业大学,2019.
[3] 曾波,蒲吉洲,陈秋旭,等.不同位置窖泥酶活力及其细菌群落结构相关性分析[J].食品与发酵工业,2024,50(4):102-109.
[4] SINSABAUGH R L,SHAH J F.Exoenzymatic stoichiometry and ecological theory[J].Ann Rev Ecol Evol Syst,2012,1(43):313-343.
[5] SREBOTNIK E,JENSEN K A,KAWAI S,et al.Evidence that Ceriporiopsis subvermispora degrades nonphenolic lignin structues by a one-electron-oxidation mechanism[J]. Appl Environl Microbiol,1997,11(63):4435-4440.
[6] 韩光,张宿义,卢中明.窖泥微生物、窖泥酶活性与窖泥养分相关性研究[J].酿酒科技,2011(3):48-51.
[7] 李学思,李绍亮,刘治国,等.浓香型白酒窖泥酶系与窖泥质量关联性研究[J].酿酒,2023,50(3):53-59.
[8] 刘义会,谢军,李觅,等.窖泥的酸碱缓冲容量研究[J].食品与发酵科技,2021,57(1):95-98.
[9] 吴浪涛,丁文骏,谢专,等.不同时期窖泥理化因子、风味物质和细菌组成的相关性[J].微生物学通报,2022,49(3):1030-1047.
[10] 环境保护部.HJ613—2011土壤干物质和水分的测定重量法[S].北京:中国环境科学出版社,2011.
[11] 国家质量监督检验检疫总局,国家标准化管理委员会.GB/T 35107—2017矿物源腐殖酸肥料中可溶性腐殖酸含量的测定[S].北京:中国标准出版社,2017.
[12] SAIYA-CORK K R,SINSABAUGH R L,ZAK D R.The effects of long-term nitrogen deposition on extracellular enzyme activity in an Acer saccharum forest soil[J].Soil Biol Biochem,2002,34:1309-1315.
[13] 郭杰,徐姿静,彭奎,等.不同年份窖泥理化指标的对比研究[J].酿酒科技,2021(6):134-136,142.
[14] 毛凤娇,黄均,周荣清,等.人工窖泥微生物群落对浓香型白酒发酵过程风味代谢物形成的影响[J].食品科学,2024,45(4):125-134.
[15] 杜礼泉,唐聪,古加强.活性优质窖泥的研究[J].酿酒科技,2005,129(3):49-51.
[16] ENOWASHU E,POLLA C,LAMERSDORFB N,et al.Microbial biomass and enzyme activities under reduced nitrogen deposition in an apruce forest soil[J].Appl Soil Ecol,2009,1(43):11-21.
[17] ALVAREZ S,GUERRERO M C.Enzymatic activities associated with decomposition of particulate organic matter in two shallow ponds[J].Soil Biol Biochem,2000,13(32):1941-1951.
[18] 和文祥,谭向平,王旭东,等.土壤总体酶活性指标的初步研究[J].土壤学报,2010,6(47):1232-1236.
[19] 朱书法,刘丛强,陶发祥.δ13C方法在土壤有机质研究中的应用[J].土壤学报,2005,42(3):495-503.
[20] 万红云,陈林,庞丹波,等.贺兰山不同海拔土壤酶活性及其化学计量特征[J].应用生态学报,2021,32(9):3045-3052.
[21] SINSABAUGH R L,LAUBER C L,WEINTRAUB M N,et al.Stoichiometry of soil enzyme activity at global scale[J].Ecol Lett,2008,11:1252-1264.
[22] KOCH O,TSCHERKO D,KANDELER E.Temperature sensitivity of microbial respiration,nitrogen mineralization,and potential soil enzyme activities in organic alpine soils[J]. Global Biogeochem Cycles,2007,21:4017.
[23] XU Z,YU G,ZHANG X,et al.Soil enzyme activity and stoichiometry in forest ecosystems along the North-South Transect in eastern China(NSTEC)[J].Soil Biol Biochem,2017,104:152-163.
[24] WALLENIUS K,RITA H,MIKKONEN A,et al.Effects of land use on the level,variation and spatial structure of soil enzyme activities and bacterial communities[J].Soil Biol Biochem,2011,43:1464-1473.
[25] 张鹏,王国梁.黄土高原刺槐林土壤酶化学计量沿着环境梯度变化[J].水土保持研究,2020,27(1):161-167.