 白酒发酵过程真菌群落结构差异分析
白酒发酵过程真菌群落结构差异分析 白酒发酵过程真菌群落结构差异分析
白酒发酵过程真菌群落结构差异分析中国传统白酒作为独特的发酵食品,其品质与风味的形成高度依赖于复杂的微生物群落系统。酿酒微生物的种类、数量、分布及消长变化等均对白酒发酵途径及最终产物的生成具有较大的影响[1],而微生物的生长代谢受多种生物因子和非生物因子(温度、酸度、湿度、溶解氧、总氮、总磷、速效磷等)的影响[2-4]。MA S等[3]研究发现,乳杆菌目(Lactobacillales)作为大曲优势微生物,可通过产生有机酸和细菌素促进微生物群落演替;微生物群落的改变导致酒醅挥发性风味物质如醇类风味物质含量增加,尤其是异丙醇、异戊醇和异丁醇含量显著增加。
清香型白酒作为三大基础香型之一,具有“清香纯正、醇甜柔和、自然协调、余味净爽”的风格特点[5]。独特的固态地缸发酵工艺和复杂的微生物生态系统对其风味的形成至关重要。研究发现,浓香型白酒夏季和冬季的糟醅中细菌群落结构有显著差异,夏季糟醅中乳酸菌数多,醋酸杆菌数较少[6]。夏、秋两季浓香型白酒产量虽略高于春、冬两季,但酒样感官评价较差[7],且春、夏两季基酒中总酸及四大酸(己酸、乙酸、乳酸和丁酸)含量均高于秋、冬季[8]。传统认为,冬季是酿造清香型白酒的黄金季节,该季节酿酒酒质好,产量高[9]。但是,目前对清香型白酒不同季节酒醅中微生物群落组成的比较分析研究较少,因此,本研究利用Illumina Miseq高通量测序技术对不同季节清香型大 白酒发酵过程中的真菌群落结构和多样性进行分析,解析不同季节之间白酒中真菌菌群的组成与差异,揭示冬季酿酒质量最佳的微生物学原因,并为非冬季发酵生产的调控奠定基础。
白酒发酵过程中的真菌群落结构和多样性进行分析,解析不同季节之间白酒中真菌菌群的组成与差异,揭示冬季酿酒质量最佳的微生物学原因,并为非冬季发酵生产的调控奠定基础。
酒醅样品:均取自山西某清香型酒厂。
E.Z.N.A. 土壤基因组DNA提取试剂盒:美国Omega Bio-tek公司;DNA凝胶回收纯化试剂盒:中高逾华生物技术有限公司;5×TransStart FastPfu缓冲液、TransStart FastPfu DNA聚合酶:北京全式金生物技术股份有限公司。
土壤基因组DNA提取试剂盒:美国Omega Bio-tek公司;DNA凝胶回收纯化试剂盒:中高逾华生物技术有限公司;5×TransStart FastPfu缓冲液、TransStart FastPfu DNA聚合酶:北京全式金生物技术股份有限公司。
NanoDrop2000超微量分光光度计、Qubit 4.0荧光定量仪:美国Thermo Fisher Scientific公司;ABI GeneAmp 9700型聚合酶链式反应(polymerase chain reaction,PCR)扩增仪:美国Applied Biosystems公司;JY600C通用型电泳仪:北京君意东方电泳设备有限公司;Illumina Nextseq2000高通量测序仪:美国Illumina公司。
9700型聚合酶链式反应(polymerase chain reaction,PCR)扩增仪:美国Applied Biosystems公司;JY600C通用型电泳仪:北京君意东方电泳设备有限公司;Illumina Nextseq2000高通量测序仪:美国Illumina公司。
1.3.1 样品采集
清香型白酒酿造时,同一批高粱会分两次发酵产酒:第一次发酵产酒称为“大 ”,大
”,大 馏酒后再加曲进行第二次发酵,称为“二
馏酒后再加曲进行第二次发酵,称为“二 ”,两次发酵周期均为28 d。由于夏季气温太高,难稳定控制发酵过程,所以夏季不进行大
”,两次发酵周期均为28 d。由于夏季气温太高,难稳定控制发酵过程,所以夏季不进行大 入缸。直至9月气温下降,新的生产周期启动,开始第一批次大
入缸。直至9月气温下降,新的生产周期启动,开始第一批次大 生产,这个阶段称为“立排期”。每批大
生产,这个阶段称为“立排期”。每批大 入缸发酵完成后,进行大
入缸发酵完成后,进行大 馏酒,这一批大
馏酒,这一批大 生产结束。到11月,二
生产结束。到11月,二 馏酒开始,进入“圆排期”。直至次年5月,完成最后一批大
馏酒开始,进入“圆排期”。直至次年5月,完成最后一批大 入缸,进入“挑排期”,这一批大
入缸,进入“挑排期”,这一批大 经发酵、馏酒后,整个生产周期的大
经发酵、馏酒后,整个生产周期的大 酿造环节正式结束。整个周期内可完成9批次大
酿造环节正式结束。整个周期内可完成9批次大 生产,横跨3个季节,形成了稳定有序的季节性酿造体系。
生产,横跨3个季节,形成了稳定有序的季节性酿造体系。
本研究跟踪取样同一个班组整个生产周期所有批次的大 酒醅。每批次采集发酵0 d、3 d、5 d、7 d、11 d、15 d、21 d、28 d的酒醅。采集时,取酒醅表层、中层(表层往下约50 cm处)及底层3个层次的酒醅样品,每个层次采集中心点5 cm范围内和紧贴地缸内壁的位置,然后将3个层次的酒醅混合作为一个样品以消除取样误差,混合后取500 g样品于无菌自封袋中[10],-80 ℃条件下保藏。
酒醅。每批次采集发酵0 d、3 d、5 d、7 d、11 d、15 d、21 d、28 d的酒醅。采集时,取酒醅表层、中层(表层往下约50 cm处)及底层3个层次的酒醅样品,每个层次采集中心点5 cm范围内和紧贴地缸内壁的位置,然后将3个层次的酒醅混合作为一个样品以消除取样误差,混合后取500 g样品于无菌自封袋中[10],-80 ℃条件下保藏。
1.3.2 样品微生物宏基因组DNA抽提
根据E.Z.N.A. 土壤基因组DNA提取试剂盒说明书对酒醅样品中微生物群落宏基因组DNA进行抽提,使用1%的琼脂糖凝胶电泳检测抽提的基因组DNA的质量,采用NanoDrop2000测定DNA浓度和纯度。
土壤基因组DNA提取试剂盒说明书对酒醅样品中微生物群落宏基因组DNA进行抽提,使用1%的琼脂糖凝胶电泳检测抽提的基因组DNA的质量,采用NanoDrop2000测定DNA浓度和纯度。
1.3.3 PCR扩增和测序文库构建
以提取的宏基因组DNA为模板,使用携带Barcode序列的上游引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和下游引物ITS2R(5'-GCTGCGTTCTTCATCGATGC-3')[11]对真菌的内转录间隔区(internally transcribed spacer,ITS)1区基因序列进行PCR扩增,PCR扩增体系为:5×Trans Start FastPfu缓冲液4 μL,2.5 mmol/L脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphates,dNTPs)2 μL,上和下游引物(5 μmol/L)各0.8 μL,TransStart FastPfu DNA聚合酶0.4 μL,模板DNA 10 ng,双蒸水(ddH2O)补足至20 μL。PCR扩增程序:95 ℃预变性3 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸30 s,共27个循环;72 ℃再延伸10 min,最后在4 ℃进行保存。使用2%琼脂糖凝胶检测PCR扩增产物,并利用DNA凝胶回收纯化试剂盒回收、纯化产物后进行检测定量。纯化后的PCR产物进行建库,并利用Illumina Nextseq2000平台进行高通量测序。参照文献进行序列处理和分析[12]。
1.3.4 数据处理与统计分析
采用R语言(v4.4.3)中的“vegan”包计算α多样性指数,包括香农(Shannon)指数、辛普森(Simpson)指数、丰富度指数;采用SPSS 25软件进行单因素方差分析和多重比较;采用R语言(v4.4.3)中的“ggplot2”、“ggrepel”包进行主成分分析(principal components analysis,PCA),判断不同样品间真菌群落结构的相似性[5],并结合“vegan”包中相似性分析(analysis of similarities,ANOSIM)分析组间差异;使用“tidyverse”、“microeco”、“magrittr”、“patchwork”包进行线性判别分析效应值大小(linear discriminant analysis effect size,LEfSe),分析不同季节酒醅中的差异物种,并根据各差异物种的线性判别分析(linear discriminant analysis,LDA)得分大小,得到各季节酒醅中的生物标识[13]。采用“psych”包计算微生物之间的Spearman相关系数,并进行显著性检验,然后利用Gephi(v0.9.2)绘制微生物之间的共现性网络图[14]。
 白酒酒醅真菌群落的α多样性分析
白酒酒醅真菌群落的α多样性分析不同季节清香型大 白酒酒醅真菌群落的α多样性分析结果见表1。由表1可知,所有样品中真菌菌群高通量测序结果的覆盖率均为100%,说明测序结果能覆盖所有样品中的真菌群落,能真实反映样品中真菌菌群的多样性及丰度[15]。不同季节清香型大
白酒酒醅真菌群落的α多样性分析结果见表1。由表1可知,所有样品中真菌菌群高通量测序结果的覆盖率均为100%,说明测序结果能覆盖所有样品中的真菌群落,能真实反映样品中真菌菌群的多样性及丰度[15]。不同季节清香型大 白酒酒醅中真菌群落多样性具有一定差异。秋季是清香型白酒新一轮酿酒生产的开始,秋季酒醅中真菌菌群的多样性(Shannon指数、Simpson指数)和丰富度指数最高,略高于春季酒醅(P>0.05),显著高于冬季酒醅(P<0.05)。然而,有研究发现冬季是白酒酿造的最佳时节,冬季酿酒的出酒品质好[9]。在前人的研究中也发现,冬季清香型白酒真菌菌群的Chao1指数和Shannon指数显著低于其他季节[14]。分析原因可能是,冬季气温低,抑制环境中大多数微生物的活性,也减少了杂菌对酒醅的干扰,从而降低了整体的真菌菌群多样性;另外,春秋季节湿度高,会增加环境中真菌菌群的相对丰度和多样性[16]。
白酒酒醅中真菌群落多样性具有一定差异。秋季是清香型白酒新一轮酿酒生产的开始,秋季酒醅中真菌菌群的多样性(Shannon指数、Simpson指数)和丰富度指数最高,略高于春季酒醅(P>0.05),显著高于冬季酒醅(P<0.05)。然而,有研究发现冬季是白酒酿造的最佳时节,冬季酿酒的出酒品质好[9]。在前人的研究中也发现,冬季清香型白酒真菌菌群的Chao1指数和Shannon指数显著低于其他季节[14]。分析原因可能是,冬季气温低,抑制环境中大多数微生物的活性,也减少了杂菌对酒醅的干扰,从而降低了整体的真菌菌群多样性;另外,春秋季节湿度高,会增加环境中真菌菌群的相对丰度和多样性[16]。
表1 不同季节清香型大 白酒酒醅中真菌群落的α多样性分析结果Table 1 Analysis results of α-diversity of fungal community in the fermented grains of light-flavor Dacha Baijiu in different seasons
白酒酒醅中真菌群落的α多样性分析结果Table 1 Analysis results of α-diversity of fungal community in the fermented grains of light-flavor Dacha Baijiu in different seasons
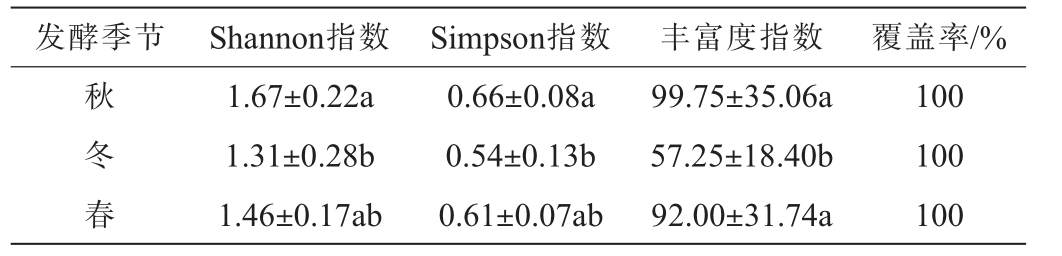
注:同列不同小写字母表示差异显著(P<0.05)。
 白酒酒醅真菌菌群结构分析
白酒酒醅真菌菌群结构分析不同季节清香型大 白酒酒醅中共注释到509个真菌属,包括9种共有优势真菌属(平均相对丰度>1%),分别为复膜孢酵母属(Saccharomycopsis)、伊萨酵母属(Issatchenkia)、曲霉属(Aspergillus)、哈萨克斯坦酵母属(Kazachstania)、嗜热子囊菌属(Thermoascus)、有孢汉逊酵母属(Hanseniaspora)、根霉属(Rhizopus)、威克汉逊酵母属(Wickerhamomyces)和毕赤酵母属(Pichia),9种优势真菌属相对丰度见图1。
白酒酒醅中共注释到509个真菌属,包括9种共有优势真菌属(平均相对丰度>1%),分别为复膜孢酵母属(Saccharomycopsis)、伊萨酵母属(Issatchenkia)、曲霉属(Aspergillus)、哈萨克斯坦酵母属(Kazachstania)、嗜热子囊菌属(Thermoascus)、有孢汉逊酵母属(Hanseniaspora)、根霉属(Rhizopus)、威克汉逊酵母属(Wickerhamomyces)和毕赤酵母属(Pichia),9种优势真菌属相对丰度见图1。
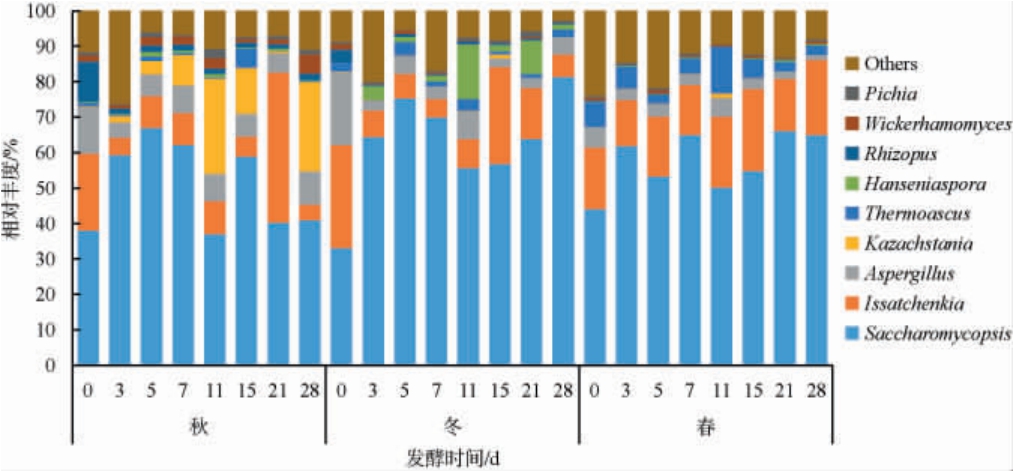
图1 不同季节清香型大 白酒酒醅真菌菌群结构分析
白酒酒醅真菌菌群结构分析
Fig.1 Analysis of fungal community structure in the fermented grains of light-flavor Dacha Baijiu in different seasons
复膜孢酵母属在不同季节酒醅中均为相对丰度最高的真菌,随着发酵的进行其相对丰度总体上呈现先升高后降低再升高的趋势。分析原因可能是,复膜孢酵母属可耐受体积分数7%~8%乙醇及pH为2~3的酸性环境[17]。进入地缸后,复膜孢酵母属迅速增殖发挥数量优势,消耗营养物质,继续生长,但是到发酵中期,其他微生物积累到一定程度,复膜孢酵母属相对丰度有所下降,然而随着发酵的进行,酒醅中酒精度和酸度的增加,氧气的缺乏,导致其他微生物的生长受到抑制,复膜孢酵母属的相对丰度又有所升高。复膜孢酵母属产生的淀粉酶、蛋白酶、β-葡萄糖苷酶等水解酶可以分解大曲、酒醅中的大分子物质,为其他参与酿酒的微生物提供营养;此外还可以产生β-苯乙醇、乙酸异戊酯、棕榈酸乙酯和苯乙酸乙酯等挥发性风味物质,影响白酒的风味[18-20]。伊萨酵母属在不同季节酒醅中的相对丰度是次高的,其在整个清香型白酒发酵期内稳定存在,尤其在春季生产中其相对丰度变化较小。伊萨酵母属属于高产酒酵母,耐热、耐酸性好[21],其在白酒发酵过程中主要致力于酒精发酵,通过糖酵解途径快速代谢糖类化合物,在获取能量的同时释放CO2和乙醇,并产生少量的高级醇等风味物质[19,22]。曲霉属在整个发酵过程中也均存在,但是发酵后期相对丰度有所降低。曲霉属主要来源于大曲,是白酒酿造中的糖化酶[19]。
其他优势菌属在不同季节酒醅中的相对丰度有所差异,冬季酒醅中有较多的有孢汉逊酵母属,尤其是在发酵11 d和21 d,但是在其他季节酒醅中相对丰度较小。秋季酒醅中有较多的哈萨克斯坦酵母属,尤其是在11 d、15 d和28 d时相对丰度比较高,然而在冬季和春季酒醅中较少。春季酒醅中有较多的嗜热子囊菌属,然而在其他季节酒醅中相对丰度较小。有孢汉逊酵母属不耐高乙醇、耐酸、耐高温[23],是一种非酿酒酵母,能够增加酒体香气[24],这可能是影响酿酒质量的关键性菌属。哈萨克斯坦酵母属在白酒酿造过程中能产生异戊酸乙酯、乙酸异戊酯、己酸乙酯、β-苯乙醇、丁二酸双乙酯、辛酸乙酯等风味物质[25]。哈萨克斯坦酵母属最适生长温度为25~30 ℃,在37 ℃或40 ℃生长受到限制[26]。3个季节0 d刚入缸时哈萨克斯坦酵母属相对丰度均极低,0 d的微生物主要受大曲影响,但是秋季环境中的哈萨克斯坦酵母属进入酒醅后逐渐增多,说明秋季酒醅中的哈萨克斯坦酵母属来源于环境。春季酒醅中有较多的嗜热子囊菌属,可能是因为春季使用的大曲中该菌属相对丰度高[5]。嗜热子囊菌属能产生具有良好热稳定性的酶,包括半纤维素,α-淀粉酶、葡萄糖淀粉酶、蛋白酶、脂肪酶等[26]。
 白酒酒醅真菌菌群结构差异分析
白酒酒醅真菌菌群结构差异分析为了进一步分析生产季节对清香型大 白酒酒醅真菌群落结构的影响,基于属水平对不同季节清香型大
白酒酒醅真菌群落结构的影响,基于属水平对不同季节清香型大 白酒酒醅样品进行PCA,结果见图2。由图2可知,主成分1(principal component 1,PC1)的方差贡献率为33.86%,PC2的方差贡献率为19.09%,前两个主成分的累计方差贡献率为52.95%,说明前两个主成分能代表大部分的真菌属信息。相同季节的酒醅样品距离相对较近,不同季节的酒醅样品距离相对较远,尤其是春季和冬季不同发酵时间的酒醅样品之间比较集中,但是秋季不同发酵时间的酒醅样品相对离散。这可能是因为秋季是新一周期生产刚开始,酒醅微生物群落结构还不稳定。此外,结合ANOSIM分析发现,不同季节清香型大
白酒酒醅样品进行PCA,结果见图2。由图2可知,主成分1(principal component 1,PC1)的方差贡献率为33.86%,PC2的方差贡献率为19.09%,前两个主成分的累计方差贡献率为52.95%,说明前两个主成分能代表大部分的真菌属信息。相同季节的酒醅样品距离相对较近,不同季节的酒醅样品距离相对较远,尤其是春季和冬季不同发酵时间的酒醅样品之间比较集中,但是秋季不同发酵时间的酒醅样品相对离散。这可能是因为秋季是新一周期生产刚开始,酒醅微生物群落结构还不稳定。此外,结合ANOSIM分析发现,不同季节清香型大 白酒酒醅真菌群落结构变化具有显著差异(P<0.05)。有研究发现,随着季节变化导致的环境因子变化会影响微生物的多样性和群落组成[27-29]。在清香型白酒酿造过程中,由于季节变化导致的环境温度、湿度、日照、紫外线强度等会影响空气中微生物种类和数量,导致由空气进入酒醅的微生物不同;另外由于季节变化导致的室温和地温变化,影响地缸内温度,导致发酵微生物的不同;此外,清香型白酒发酵工艺中的润糁过程也受环境变化影响,导致不同酸度、产生不同的底物等也会影响后续的地缸发酵。
白酒酒醅真菌群落结构变化具有显著差异(P<0.05)。有研究发现,随着季节变化导致的环境因子变化会影响微生物的多样性和群落组成[27-29]。在清香型白酒酿造过程中,由于季节变化导致的环境温度、湿度、日照、紫外线强度等会影响空气中微生物种类和数量,导致由空气进入酒醅的微生物不同;另外由于季节变化导致的室温和地温变化,影响地缸内温度,导致发酵微生物的不同;此外,清香型白酒发酵工艺中的润糁过程也受环境变化影响,导致不同酸度、产生不同的底物等也会影响后续的地缸发酵。
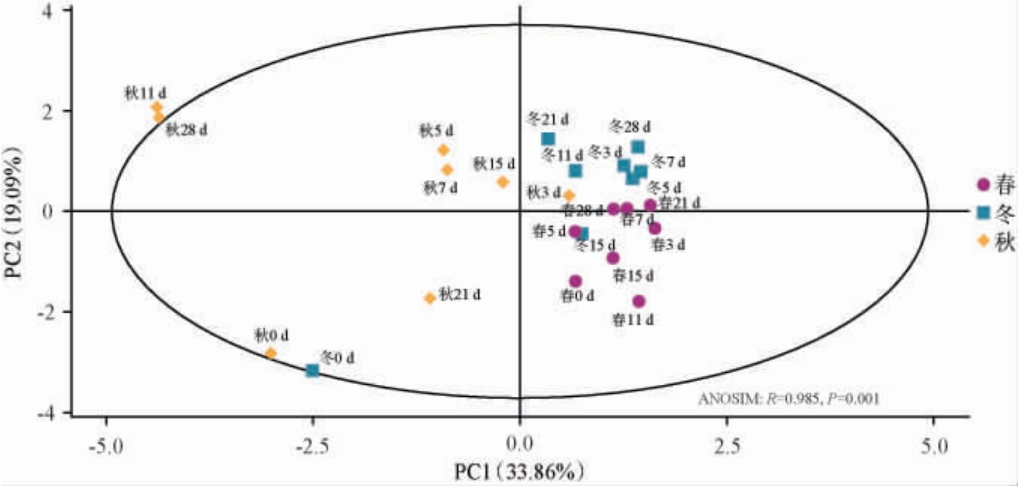
图2 基于属水平不同季节清香型大 白酒酒醅真菌群落主成分分析及相似性分析
白酒酒醅真菌群落主成分分析及相似性分析
Fig.2 Principal components analysis and analysis of similarities of fungal community in the fermented grains of light-flavor Dacha Baijiu in different seasons based on genus level
利用LEfSe方法进一步分析不同季节清香型大 白酒酒醅间的差异真菌,结果见图3。由图3可知,基于属水平,从不同季节清香型大
白酒酒醅间的差异真菌,结果见图3。由图3可知,基于属水平,从不同季节清香型大 白酒酒醅中共检出10种差异真菌(LDA得分>2,P<0.05)。秋季酒醅中具有显著差异的真菌属为哈萨克斯坦酵母属、根霉属、威克汉逊酵母属、根毛霉属(Rhizomucor)、Spiromyces(P<0.05);冬季酒醅中具有显著差异的真菌属为Naumovozyma。春季酒醅中具有显著差异的真菌属为Clavispora、鳞斑霉属(Malassezia)、红曲霉属(Monascus)、Lecanicillium。根霉属和根毛霉属均具有良好的产酶特性和热稳定性[30],根霉属也能产生乙醇、2-甲基-1-丁酮、3-甲基-1-丁酮等风味物质[19]。刚进入秋季,气温还比较高,根霉和根毛霉的热稳定性有利于它们在酒醅中分解更多的淀粉、脂肪、纤维素等,为系统中其他微生物的生长提供营养。Naumovozyma是浓香型白酒的核心菌群[31],在清香型白酒酿造车间内外环境中也分离到了Naumovozyma[32]。研究发现,Naumovozyma与丁酸的合成、酯类物质以及醇类物质的合成呈较强的正相关[31-33],说明Naumovozymay与产香有关,这可能是影响冬季酒质的关键性菌属。Clavispora在清香型[10,34]、浓香型[35]和酱香型白酒[36]的大曲或酒醅中均被发现,Clavispora是清茬曲的特有菌种[34]。Clavispora具有耐高温的特性,且能在pH 1~11范围内生存,但不耐酒精和己酸,能代谢产生己酸乙酯、β-苯乙醇和萜烯类物质[37]。鳞斑霉属在浓香型白酒的窖泥[38]、车间周围土壤[39]中均被发现,说明清香型白酒中的鳞斑霉属可能来源于环境。红曲霉能产生脂肪酶、糖化酶、蛋白酶与酯化酶[19]。真菌的生长繁殖依赖特定温湿度、溶氧量、营养等条件,季节变化会直接打破酒醅微生态的平衡,春季、秋季气温稍高,酒醅温度也随之较高,耐热性好的根霉属、根毛霉属、Clavispora就会被保留。冬季气温低,产香的Naumovozyma就会发挥竞争优势,产生更多的香气成分,改善酒质。真菌差异不仅反映了发酵微生态对季节变化的适应性响应,更直接关联白酒的出酒率、风味物质生成及酒体品质。
白酒酒醅中共检出10种差异真菌(LDA得分>2,P<0.05)。秋季酒醅中具有显著差异的真菌属为哈萨克斯坦酵母属、根霉属、威克汉逊酵母属、根毛霉属(Rhizomucor)、Spiromyces(P<0.05);冬季酒醅中具有显著差异的真菌属为Naumovozyma。春季酒醅中具有显著差异的真菌属为Clavispora、鳞斑霉属(Malassezia)、红曲霉属(Monascus)、Lecanicillium。根霉属和根毛霉属均具有良好的产酶特性和热稳定性[30],根霉属也能产生乙醇、2-甲基-1-丁酮、3-甲基-1-丁酮等风味物质[19]。刚进入秋季,气温还比较高,根霉和根毛霉的热稳定性有利于它们在酒醅中分解更多的淀粉、脂肪、纤维素等,为系统中其他微生物的生长提供营养。Naumovozyma是浓香型白酒的核心菌群[31],在清香型白酒酿造车间内外环境中也分离到了Naumovozyma[32]。研究发现,Naumovozyma与丁酸的合成、酯类物质以及醇类物质的合成呈较强的正相关[31-33],说明Naumovozymay与产香有关,这可能是影响冬季酒质的关键性菌属。Clavispora在清香型[10,34]、浓香型[35]和酱香型白酒[36]的大曲或酒醅中均被发现,Clavispora是清茬曲的特有菌种[34]。Clavispora具有耐高温的特性,且能在pH 1~11范围内生存,但不耐酒精和己酸,能代谢产生己酸乙酯、β-苯乙醇和萜烯类物质[37]。鳞斑霉属在浓香型白酒的窖泥[38]、车间周围土壤[39]中均被发现,说明清香型白酒中的鳞斑霉属可能来源于环境。红曲霉能产生脂肪酶、糖化酶、蛋白酶与酯化酶[19]。真菌的生长繁殖依赖特定温湿度、溶氧量、营养等条件,季节变化会直接打破酒醅微生态的平衡,春季、秋季气温稍高,酒醅温度也随之较高,耐热性好的根霉属、根毛霉属、Clavispora就会被保留。冬季气温低,产香的Naumovozyma就会发挥竞争优势,产生更多的香气成分,改善酒质。真菌差异不仅反映了发酵微生态对季节变化的适应性响应,更直接关联白酒的出酒率、风味物质生成及酒体品质。
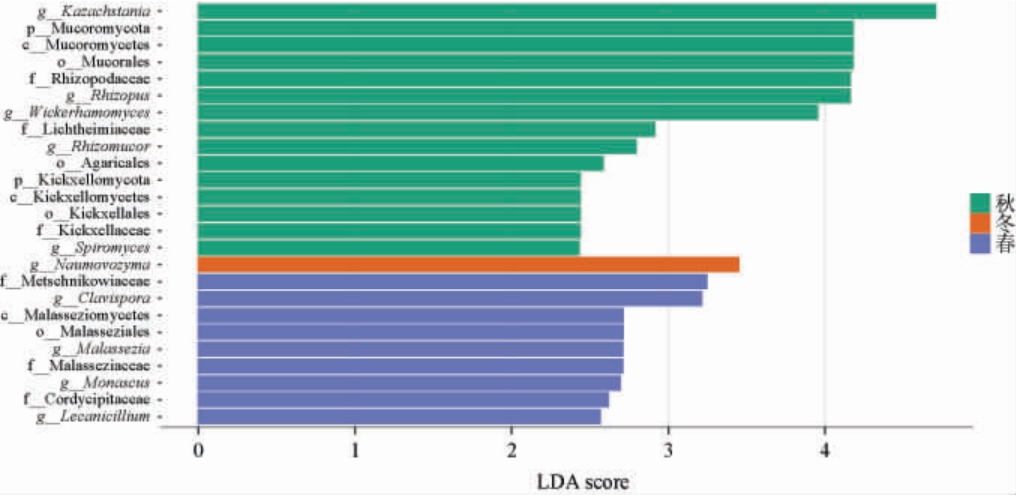
图3 不同季节清香型大 白酒酒醅真菌群落线性判别分析效应值大小分析结果
白酒酒醅真菌群落线性判别分析效应值大小分析结果
Fig.3 Results of linear discriminant analysis effect size analysis of fungal community in the fermented grains of light-flavor Dacha Baijiu in different seasons
 白酒酒醅真菌菌群间的相互作用分析
白酒酒醅真菌菌群间的相互作用分析微生物间相互作用是微生物群落构建的一个重要生物指标,基于Spearman相关性分析(|R|>0.6,P<0.05)对不同季节清香型大 白酒酒醅的真菌菌群进行共现网络分析[26],结果见图4及表2。由图4及表2可知,秋季酒醅中真菌菌群间的正相关关系(64.86%)高于负相关关系(35.14%);冬季酒醅中真菌菌群间的正相关关系占比升高至87.50%、负相关关系占比下降至12.50%;春季酒醅中真菌菌群间的正相关关系占比为51.16%、负相关关系占比为48.84%,两种关系占比相近。
白酒酒醅的真菌菌群进行共现网络分析[26],结果见图4及表2。由图4及表2可知,秋季酒醅中真菌菌群间的正相关关系(64.86%)高于负相关关系(35.14%);冬季酒醅中真菌菌群间的正相关关系占比升高至87.50%、负相关关系占比下降至12.50%;春季酒醅中真菌菌群间的正相关关系占比为51.16%、负相关关系占比为48.84%,两种关系占比相近。
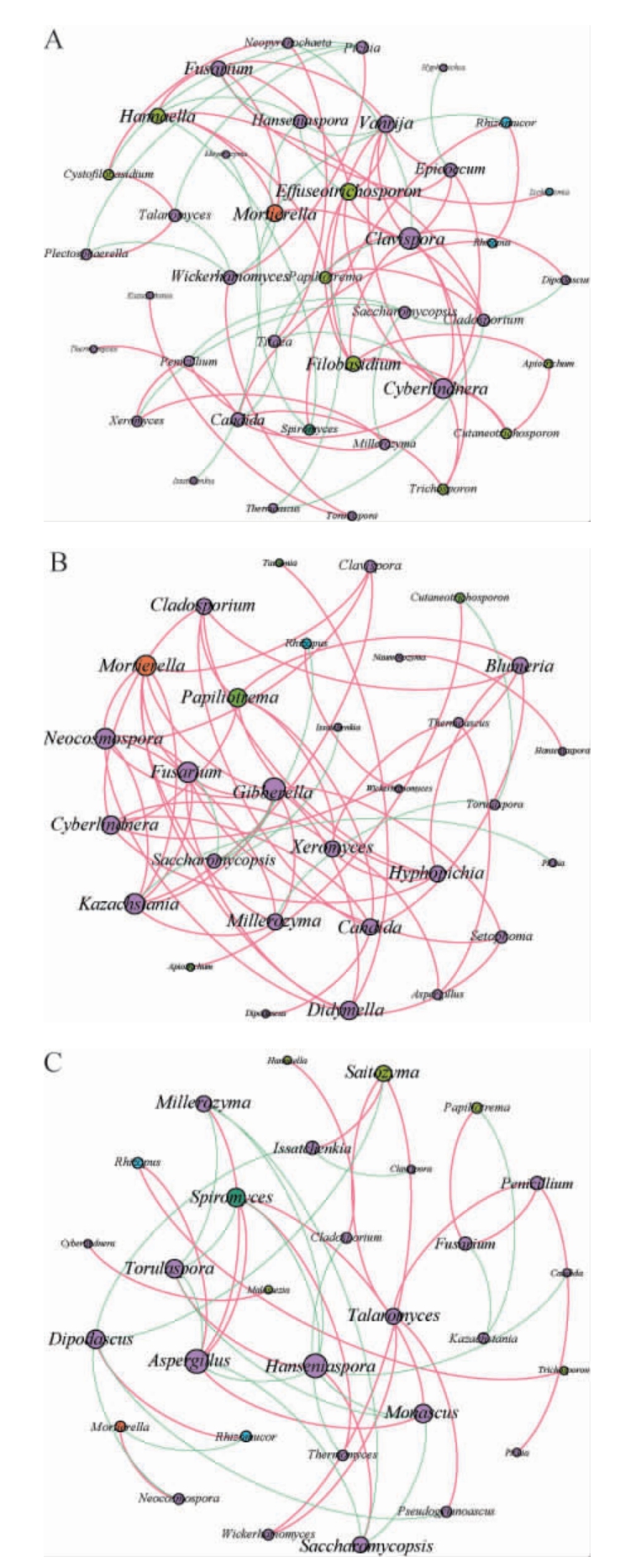
图4 秋(A)、冬(B)、春(C)季清香型大 白酒酒醅真菌群落间共现网络图
白酒酒醅真菌群落间共现网络图
Fig.4 Co-occurrence network diagrams of fungal communities in the fermented grains of light-flavor Dacha Baijiu in autumn (A),winter (B),and spring (C) seasons
红色的边代表正相关,绿色的边代表负相关。
表2 不同季节清香型大 白酒酒醅真菌群落间共现网络分析结果
白酒酒醅真菌群落间共现网络分析结果
Table 2 Analysis results of co-occurrence networks among fungal communities in the fermented grains of light-flavor Dacha Baijiu in different seasons
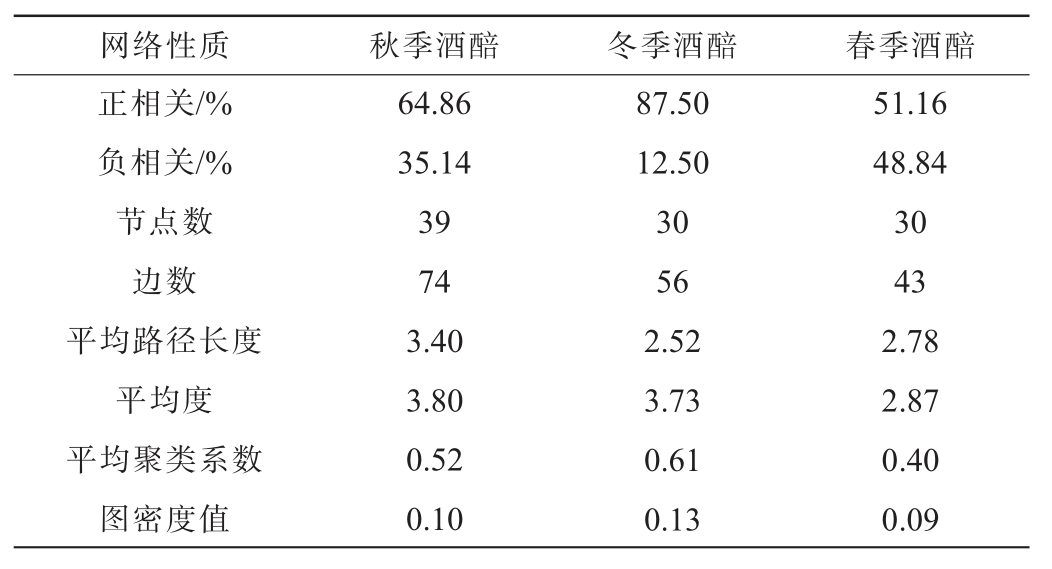
节点表示为酒醅真菌共现网络图中的真菌种类[40]。节点数为秋季(39)>冬季(30)=春季(30)。边是由酒醅真菌共现网络图中真菌间相关性所决定的[40]。边数为秋季(74)>冬季(56)>春季(43)。平均路径长度是任意两个节点之间距离的平均值,反映网络中各个节点间的分离程度,其值越小代表网络中节点的连接度越大[41]。平均路径长度为秋季(3.40)>春季(2.78)>冬季(2.52),意味着秋季酒醅中真菌之间的平均距离较长,冬季较短。图密度值反映微生物之间相互作用的紧密程度,值越大表明图中节点连接越紧密[40]。平均聚类系数表示共现网络图中各节点之间的聚集情况,反映网络节点间的亲密关系,其值越低,说明节点之间的连接比较稀疏[41]。图密度值和平均聚类系数均为冬季(0.13、0.61)>秋季(0.10、0.52)>春季(0.09、0.40),说明冬季酒醅真菌菌群间的相互作用比较紧密,其次为秋季酒醅。平均度反映共现网络图中微生物的平均相互作用强度[40]。平均度为秋季(3.80)>冬季(3.73)>春季(2.87)。综上,春季酒醅中真菌群落的节点数和边数较小,微生物分离程度大,连接稀疏,相互作用也较弱,说明其群落结构的复杂性和稳定性均最弱。秋季酒醅中真菌群落的节点数和边数最多,但是平均路径长度长,相互作用弱,说明群落结构复杂但不稳定。冬季酒醅中真菌群落的节点数虽少,但是边数较多,且平均路径长度最短,图密度值和平均聚类系数最高,说明其群落结构最稳定。微生物群落结构复杂性和稳定性的不同,会导致代谢产物的不同[42],直接影响白酒的品质,所以不同季节生产的白酒具有各自独特的特点。
本研究以清香型大 白酒酒醅为对象,探究生产季节对其真菌群落多样性、结构组成、复杂性和稳定性的影响。结果表明,生产季节影响酒醅真菌群落的多样性,秋季酒醅真菌群落的Shannon指数、Simpson指数及丰富度指数最高,冬季则最低。生产季节也会影响酒醅真菌群落组成,基于LEfSe从不同季节酒醅中共筛选出Kazachstania、Rhizopus、Wickerhamomyces、Rhizomucor等10种差异真菌属(LDA>2,P<0.05)。此外,生产季节还会影响群落复杂性与稳定性,通过微生物共现网络分析发现,秋季酒醅真菌群落结构复杂但不太稳定,冬季酒醅真菌群落结构虽然较简单但最稳定。
白酒酒醅为对象,探究生产季节对其真菌群落多样性、结构组成、复杂性和稳定性的影响。结果表明,生产季节影响酒醅真菌群落的多样性,秋季酒醅真菌群落的Shannon指数、Simpson指数及丰富度指数最高,冬季则最低。生产季节也会影响酒醅真菌群落组成,基于LEfSe从不同季节酒醅中共筛选出Kazachstania、Rhizopus、Wickerhamomyces、Rhizomucor等10种差异真菌属(LDA>2,P<0.05)。此外,生产季节还会影响群落复杂性与稳定性,通过微生物共现网络分析发现,秋季酒醅真菌群落结构复杂但不太稳定,冬季酒醅真菌群落结构虽然较简单但最稳定。
[1] 赵爽,杨春霞,窦屾,等.白酒生产中酿酒微生物研究进展[J].中国酿造,2012,31(4):5-10.
[2] PENG Q,ZHENG H,YU H F,et al.Environmental factors drive the succession of microbial community structure during wheat Qu fermentation[J].Food Biosci,2023,56:103169.
[3] MA S,LUO H,ZHAO D,et al.Environmental factors and interactions among microorganisms drive microbial community succession during fermentation of Nongxiangxing daqu[J].Bioresource Technol,2022,345:126549.
[4] SHANG Y,WU X,WANG X,et al.Factors affecting seasonal variation of microbial community structure in Hulun Lake,China[J]. Sci Total Environ,2022,805:150294.
[5] 曹苗文,相里加雄,杨凯环,等.清香型大曲白酒酿造中发酵微生物的分析研究[J].酿酒科技,2022(1):36-41.
[6] SUN W,XIAO H,PENG Q,et al.Analysis of bacterial diversity of Chinese luzhou-flavorliquor brewed indifferent seasons by Illumina Miseqsequencing[J].Ann Microbiol,2016,66(3):1293-1301.
[7] 尹小满,张宿义,敖宗华,等.不同季节对浓香型白酒发酵的影响[J].酿酒科技,2014(1):51-54,58.
[8] 张竞一,柴丽娟,高涛,等.不同季节浓香型白酒基酒风味物质差异分析[J].食品科学,2023,44(12):164-171.
[9] 刘全明,刘帅,甄攀.汾酒酿造工艺操作经验之浅见[J].酿酒,2014,41(5):83-85.
[10]曹苗文,杨凯环,孙海军,等.清香型白酒机械化酿造和传统手工酿造压醅前后出缸酒醅微生物群落结构对比[J].酿酒,2024,51(1):74-79.
[11] ADAMS R I,MILETTO M,TAYLOR J W,et al.Dispersal in microbes:fungi in indoor air are dominated by outdoor air and show dispersal limitation at short distances[J].ISME,2013,7(7):1460.
[12] 杨翼飞,徐桂瑶,王琴,等.芒柄花黄素对小鼠肠道菌群结构和丰度的影响[J].西南医科大学学报,2023,46(4):342-347.
[13] SEGATA N,IZARD J,WALDRON L,et al.Metagenomic biomarker discovery and explanation[J].Genome Biol,2011,12(6):R60.
[14] 王石垒.气候因子对清香型白酒酿造菌群驱动机制的解析及酿造菌群合成微生物组的构建[D].无锡:江南大学,2021.
[15] 王依文,田瑶瑶,张克粉,等.不同季节及层级浓香型白酒窖泥微生物群落多样性与风味物质的比较及相关性分析[J].食品科学,2025,46(4):100-109.
[16] 余琳,杜钢,钟慈平,等.季节变化对不同产地浓香型白酒大曲微生物菌群及风味的影响[J].中国酿造,2025,44(3):71-79.
[17] 王志男,杨佳,李新生,等.扣囊复膜酵母生物学性状及生理生化特性研究[J].陕西理工大学学报(自然科学版),2022,38(3):39-46.
[18] 王居伟,韩培杰,王雪薇,等.白酒发酵过程中常见酵母菌扣囊复膜酵母的研究进展[J].广西科学,2020,27(1):1-9.
[19] 韩冰玙,陈辉太,李宗军.酱、浓、清香型白酒酿造过程中真菌及其功能特性研究进展[J].中国酿造,2024,43(3):27-32.
[20] 王乃军,马美荣.扣囊复膜酵母在白酒生产中的应用研究进展[J].酿酒科技,2023(3):115-119.
[21] 刘超帝,缪礼鸿,陈瑾,等.耐高温酵母菌的筛选及其乙醇发酵特性[J].食品科学,2016,37(19):128-134.
[22] 彭远凤,杨阳,赵东,等.东方伊萨酵母对浓香型白酒酒醅微生物群落结构及挥发性风味物质合成的影响[J].食品科学,2024,45(16):97-104.
[23] 冯文倩,王倩,刘延琳,等.低产乙醇本土有孢汉逊酵母的筛选及酿造特性[J].食品与发酵工业,2021,47(21):9-17.
[24] SONG L,HAN D Y,LUO L J,et al.Exploring non-Saccharomyces yeasts from Daqu for beer production[J].LWT-Food Sci Technol,2024,209:116803.
[25] 游玲,周荣清,谭壹,等.Kazachstania属酵母在浓香型白酒糟醅中的分布特征及发酵功能[J].生物技术通报,2021,37(6):108-116.
[26] SHI W,CHAI L,ZHAO H,et al.Deciphering the effects of different types of high-temperature Daqu on the fermentation process and flavor profiles of sauce-flavor Baijiu[J].Food Biosci,2024,61:104917.
[27] LIPSON D A,SCHMIDT S K.Seasonal changes in an alpine soil bacterialcommunity in the Colorado Rocky Mountains[J]. Appl Environ Microbiol,2004,70(5):2867.
[28] SHARP K H,PRATTE Z A,KERWIN A H,et al.Season,but not symbiont state,drives microbiome structure in the temperate coral Astrangia poculata[J].Microbiome,2017,5(1):120.
[29] PRIEST T,OLDENBURG E,POPA O,et al.Seasonal recurrence and modular assembly of an Arctic pelagic marine microbiome[J].Nat Commun,2025,16(1):1326.
[30] 赵慧君,王玉荣,侯强川,等.滨州地区高温和中温大曲真菌类群解析及其感官品质关联性分析[J].食品工业科技,2025,46(11):163-173.
[31] 宋建阳,梁莉莹,岑定运,等.浓香型白酒发酵过程中酒醅微生物群落结构解析及其与风味物质的相关性[J].食品研究与开发,2023,44(14):86-92.
[32] 甄攀,尹政,高晓娟,等.汾酒酿造车间和车间外环境中酵母菌多样性研究[J].生物资源,2023,45(5):454-461.
[33] 刘凡,周新虎,陈翔,等.洋河浓香型白酒发酵过程酒醅微生物群落结构解析及其与有机酸合成的相关性[J].微生物学报,2018,58(12):2087-2099.
[34] 王薇,吴群,徐岩.清香型白酒固态酿造过程中酵母种群结构和多样性分析[J].微生物学通报,2012,39(9):1272-1279.
[35] 谭壹,赵东,陈敏,等.浓香型白酒发酵旺盛期糟醅中酵母菌菌群研究[J].食品研究与开发,2020,41(6):175-180.
[36] 吴成,程平言,谢丹,等.酱香型白酒高温大曲发酵过程中真菌多样性研究[J].食品与生物技术学报,2023,42(6):95-103.
[37] FAN G,LIU P,CHANG X,et al.Isolation and identification of a highyield ethyl caproate-producing yeast from Daqu and optimization of its fermentation[J].Front Microbiol,2021,12:663744.
[38] PU S,YAN S.Fungal diversity profiles in pit mud samples from Chinese strong-flavour liquor pit[J].Foods,2022,11(22):3544.
[39] 吕丽茹,王晓平,文静,等.浓香型白酒生产区土壤微生物群落结构的季节性变化[J].中国酿造,2022,41(2):60-68.
[40] 王梓橦.黄土高原退耕还林地土壤有机碳变化的微生物学机制[D].长春:东北师范大学,2023.
[41] KAJIHARA K T,HYNSON N A.Networks as tools for defining emergent properties of microbiomes and their stability[J]. Microbiome,2024,12(1):184.
[42] YUAN S,DU H,ZHAO D,et al.Stochastic processes drive the assembly and metabolite profiles of keystone taxa during Chinese strong-flavor Baijiu fermentation[J].Microbiol Spectrum,2023,11(2):e05103-22.
Differences analysis of fungal community structure of light-flavor Dacha Baijiu in different seasons during the fermentation process