牛肉酱作为一种广受欢迎的调味品,其品质直接影响消费者的接受度和产品的市场竞争力。据行业报告显示,2023年全球肉制品市场规模增长至6 195亿美元,其中调味酱类产品年增长率达8.20%,显著高于传统肉制品[1]。而传统牛肉酱多依赖自然发酵,存在品质不稳定,发酵周期长(14~21 d)及易受杂菌污染等问题[2-4],因此很难满足现代消费者的需求。人工接种的微生物发酵剂可用于引导发酵过程、抑制病原微生物的生长和潜在有害化合物(如生物胺)的合成[5-6],确保最终产品的安全性。同时,微生物发酵剂也可以改善产品的品质[1]。添加适宜的发酵菌剂,通过微生物发酵,不仅可以增强产品的风味和营养价值,并且能延长产品的保质期[7-8],对推动牛肉酱产业升级具有重要应用价值。所以发酵菌剂的种类尤为关键。
目前,发酵菌剂在肉制品中的应用主要通过微生物的代谢活动来提升肉制品的安全性、风味品质和营养功能等,且多集中于猪肉及水产品体系[9-10]。而牛肉因高肌红蛋白、低脂肪的特性,其微生物代谢路径与风味形成机制具有独特性[11]。乳酸菌和酵母菌是肉制品发酵剂中重要的菌种[12]。近年来已有多项研究证实采用乳酸菌和酵母菌能显著改善肉制品的pH、色泽、质构和风味[13]。现有研究多集中于复合菌剂的协同效应,王德宝[14]研究发现使用乳杆菌和葡萄球菌复合发酵剂可改善香肠色泽。赵改名等[15]添加发酵剂显著降低脂肪和蛋白质的氧化程度。但对单一菌种在牛肉酱基质中的功能解析研究还不够深入,难以指导工业化生产的精准菌种筛选[16-17]。如植物乳植杆菌(Lactiplantibacillus plantarum)的产酸特性可抑制致病菌,但其对风味协调性的影响尚不明确。酿酒酵母(Saccharomyces cerevisiae)的酯类合成能力在牛肉酱中的表达规律仍需系统验证。
发酵肉制品中用到的发酵菌剂(如乳酸菌、酵母菌等)在肉制品发酵和成熟的过程中,各自发挥其独特的作用[18-19],本研究旨在系统分析植物乳植杆菌、酿酒酵母及米曲霉(Aspergillus oryzae)3种菌种在牛肉酱发酵后对pH、质构、感官品质及风味物质的差异化影响。针对传统牛肉酱生产工艺中自然发酵品质不稳定、复合菌剂作用机制复杂等问题,通过建立单菌发酵组,结合气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)、电子鼻、感官评价,明确各菌种对牛肉酱鲜味提升、风味合成及质构优化的独立贡献。通过对比菌种功能优劣势,为工业化生产中的菌种定向筛选、工艺参数优化及复合菌剂开发提供理论依据,为牛肉酱风味多元化开发提供理论支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌株
新鲜无异味的牛后腿肉:市售;食盐:抚顺市盐业有限责任公司;味精、白糖:莲花健康产业集团股份有限公司;金龙鱼大豆油:益海嘉里金龙鱼粮油食品股份有限公司。
植物乳植杆菌(Lactiplantibacillusplantarum)BNCC187897、酿酒酵母(Saccharomyces cerevisiae)BNCC186060:北 纳生物河南省工业微生物菌种工程技术研究中心;米曲霉(Aspergillus oryzae)沪酿3.042孢子粉:沂水锦润生物科技有限公司。
1.1.2 化学试剂
牛肉膏、琼脂、酵母提取物:北京奥博星生物技术有限责任公司;乙酸钠、无水乙醇、氯化钠等:天津市科密欧化学试剂有限公司;葡萄糖、硫酸镁、硫酸锰、氢氧化钠等:天津市众联化学试剂有限公司;蛋白胨、磷酸氢二钾、柠檬酸二铵、吐温80、碳酸钙等:天津市致远化学试剂有限公司。本研究所用试剂均为分析纯或生化试剂。
1.1.3 培养基
MRS液体培养基:蛋白胨1.0 g,牛肉浸粉0.8 g,酵母提取物0.4 g,葡萄糖2.0 g,磷酸氢二钾0.2 g,柠檬酸氢二胺0.2 g,乙酸钠0.5 g,硫酸镁0.02 g,硫酸锰0.004 g,0.1 g吐温80,蒸馏水100 mL,pH值(5.7±0.2)。121 ℃高压蒸汽灭菌20 min。
MRS固体培养基:MRS液体培养基中加1.4 g琼脂。
LB固体培养基:胰蛋白胨1 g,酵母提取物0.5 g,NaCl 1 g,琼脂1.5 g,蒸馏水100 mL,121 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
FA224型电子天平:上海舜宇恒平科学仪器有限公司;WH25型恒温培养箱:Wiggens北京桑翌公司;PHS-3C型酸度计:成都世纪方舟科技有限公司;VS-1300U型净化工作台:上海苏净实业有限公司;ENS-iPRO型质构仪、C-PEN3型电子鼻:北京盈盛恒泰科技有限责任公司;7697A-8860-5977C型气相色谱仪:安捷伦科技(中国)有限公司。
1.3 方法
1.3.1 菌种分离纯化及冻干粉的制备
参照贾娜等[20]的方法,并适当进行修改。将植物乳植杆菌接种至MRS固体培养基上,酵母菌接种至LB固体培养基上。30 ℃条件下厌氧倒置培养36 h,挑取单菌落接种至各加入100 mL MRS液体培养基和LB液体培养基的三角瓶中,30 ℃条件下培养24 h,连续培养2次,备用。将上述活化后的菌株按1%的接种量接种至MRS液体培养基中扩大培养36 h后,离心(6 500 r/min,15 min)后收集沉淀(菌泥)。
向菌泥中加入10倍量无菌生理盐水后,离心(6500r/min,15 min)洗涤2次,收集沉淀。按2∶1的质量比将保护剂(3%甘油用于酵母菌、10%脱脂乳粉+5%蔗糖混合液用于植物乳植杆菌)与菌泥充分混合后,转移至一次性无菌培养皿中(倾倒厚度约0.5 cm),放入-80 ℃冰箱中预冻12 h后,冻干48 h,真空脱水,粉碎后收集菌粉备用。
1.3.2 牛肉酱制备工艺流程及操作要点
原料肉预处理→切块→大豆油加热→炒制→加入盐、糖→接入发酵菌种→发酵→牛肉酱
牛肉酱制备工艺参照赵岩等[21]的方法进行改进,操作要点如下:称取400 g牛肉,仔细剔除表面附着的筋膜与多余脂肪,修整成规整形状后进行清洗。清洗后的牛肉需浸泡15 min以充分渗出血水,随后再次清洗,沥干水分并擦干表面。处理好的牛肉被切成1 cm×1 cm×1 cm的小块,装入容器中备用。先将油预热,放入牛肉块,再加入牛肉质量1%的盐、糖以及适量味精进行调味,充分搅拌至调料均匀附着。调味完成后,各组样品依次装罐,向每罐中加入牛肉质量0.125%的发酵剂,搅拌均匀后进入发酵阶段。置于30 ℃条件下,恒温发酵7 d,发酵结束后取出样品进行检测[21,28]。
设置4个分组:(1)对照组:不添加发酵剂;(2)植物乳植杆菌发酵组:添加0.125%植物乳植杆菌冻干粉;(3)酵母菌发酵组:添加0.125%酵母菌冻干粉;(4)米曲霉发酵组:添加0.125%米曲霉孢子粉。
1.3.3 pH测定
参考GB 5009.237—2016《食品安全国家标准食品pH值的测定》方法和周建中等[22]的方法。将样品绞碎后,准确称取1.00 g,加入9 mL蒸馏水,搅拌振荡30 min后,先用标准溶液校正pH仪,用蒸馏水清洗后再使用。每个样品平行测定3次。
1.3.4 质构参数测定
参考张秋会等[23]的方法,使用质构仪测量牛肉酱的质构参数,以感应的受力测定牛肉酱的硬度、咀嚼性、弹性、胶粘性。具体参数设定为:触发类型Auto(Force)、触发力5.0 g,测试前速率1.0 mm/s,测试中速率5.0 mm/s,测试后速率5.0 mm/s,变形量10%,上升高度20 mm,暂停时间15 s。每个样品重复测定3次,取平均值。
1.3.5 挥发性风味物质的测定
参考孙光城等[24-25]的方法并进行修改。样品处理:称取样品2.0 g于20 mL顶空瓶中,加入3 mL饱和氯化钠,封口膜密封,摇匀。
GC条件:HP-5MS毛细管色谱柱(30 m×0.25 mm×0.25 μm);载气为高纯氦气(99.999%),流速1 mL/min,分流比5∶1,保持2 min。进样口温度250 ℃,升温程序:起始温度40 ℃,保持3 min,以3 ℃/min升温至60 ℃,保持1 min,再以6 ℃/min升温至140 ℃,保持1 min,最后以20 ℃/min升温至250 ℃,保持3 min。
MS条件:电子电离(electron ionization,EI)源,离子源温度230 ℃,电子能量70 eV,质量扫描范围35~550 m/z;全扫描模式。
定性定量分析:结果利用GC-MS数据分析软件处理,化合物经计算机检索,并与美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)和RTLPEST谱库相匹配,仅报道匹配度>800的结果。以环己酮(0.946 g/L,采用乙醇稀释)为内标,采用内标半定量的方法,通过待测组分与环己酮峰面积的比值计算各挥发性风味物质的相对含量[26]。
1.3.6 电子鼻分析
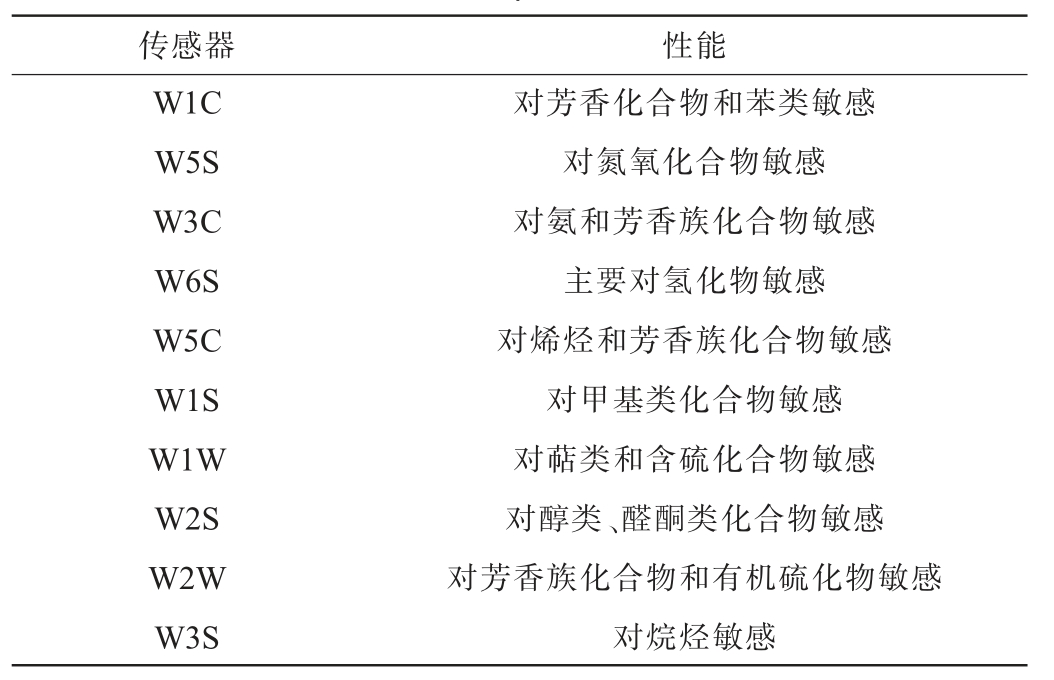
参照张丽华等[26-27]的研究方法进行改进。准确称量3.0 g样品,移至20 mL顶空进样瓶中,封口膜密封,盖上盖子,进行电子鼻测定。加热温度70 ℃,加热时间600 s,载气(空气)流量150 mL/s,进样量(顶空气体)500 μL,数据采集时间100 s,数据采集延迟150 s。不同样品重复测定3次,取第55秒的稳定测定结果进行分析,各传感器对应的敏感物质类型见表1。
表1 电子鼻不同传感器及性能
Table 1 Different sensors and performance of electronic nose
1.3.7 感官评价
成立8人感官评价小组,对牛肉酱的色泽、质地、气味和滋味进行评价。评价方法:称取10 g发酵成熟的牛肉酱于统一的器皿中,用水漱口后进行品尝,根据国标GB/T 22210—2008《肉与肉制品感官评定规范》,并参考徐君强等[28-29]的方法,设计牛肉酱感官评定标准,具体见表2(满分100分)。
表2 牛肉酱感官评价标准
Table 2 Sensory evaluation standard of beef sauce

1.3.8 数据处理与统计分析
采用SPSS 23.0软件对数据进行单因素方差分析,实验结果以“平均值±标准差”表示,对组间平均数进行差异比较。电子鼻传感器响应数据的采集使用设备自带的WinMuster软件进行。基于电子鼻响应值进行的主成分分析(principle component analysis,PCA)和电子鼻雷达图及结果可视化均使用Origin 2021软件完成。
2 结果与分析
2.1 3种发酵菌剂对牛肉酱pH的影响
适当的pH值可以保持牛肉的口感、色泽,并且可以改善产品的品质。3种发酵菌剂发酵后牛肉酱的pH值变化结果见图1。由图1可知,与对照组相比,添加发酵菌剂的牛肉酱pH显著降低(P<0.05),对照组牛肉酱pH值为5.59,植物乳植杆菌组pH值为4.64,酵母菌组pH值为4.87,米曲霉组pH值为5.01。植物乳植杆菌通过糖酵解途径快速代谢碳水化合物生成乳酸,乳酸菌可在肉制品中大量繁殖,并迅速成为肉制品中的优势菌株,符合乳酸菌的典型代谢特征[30-31]。pH值的降低有助于抑制有害微生物的生长,延长牛肉酱的保质期,同时赋予牛肉酱柔和的酸味,提升其风味。酵母菌通过乙醇发酵产生有机酸(如乙酸、琥珀酸),酸化能力弱于乳酸菌,也会使牛肉酱的pH值降低,但贡献独特风味前体。米曲霉分泌蛋白酶、淀粉酶水解大分子物质(蛋白质/淀粉),使得pH降低,抑制有害微生物的生长,为后期牛肉酱的风味提升作铺垫。然而,pH并非越低越好,过低的pH可能导致酸味过于尖锐,影响整体风味协调性。本研究结果表明,酵母菌组在维持适度pH的同时,也会调节风味,说明其在产酸与风味协调之间取得了最佳平衡。
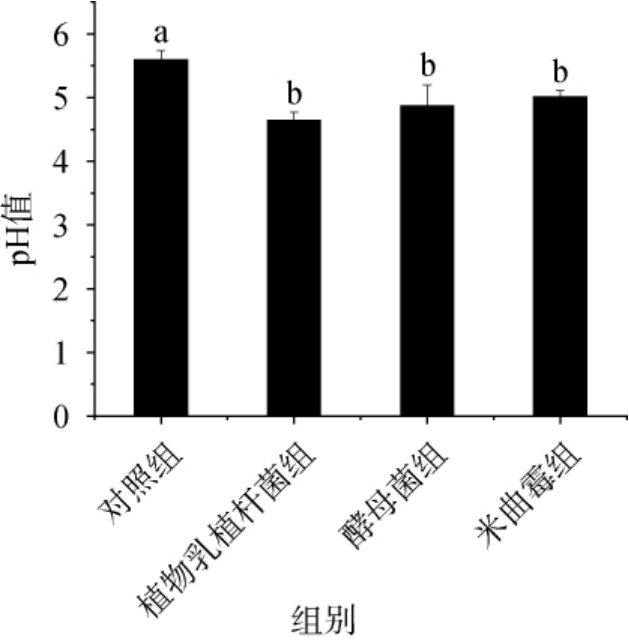
图1 3种发酵菌剂对牛肉酱pH的影响
Fig.1 Effect of three fermentation agents on the pH of beef sauce
不同字母表示差异显著(P<0.05)。下同。
2.2 3种发酵菌剂对牛肉酱质构的影响
发酵牛肉酱的硬度、弹性、咀嚼性和胶黏性测定结果见表3。由表3可知,3种发酵菌剂都能在一定程度上改善牛肉酱的质构特性,使其硬度、咀嚼性都显著降低(P<0.05),胶黏性变化较小。对照组硬度为(89.39±23.08)N,发酵组硬度均降低,植物乳植杆菌组硬度为(66.63±9.88)N,酵母菌组硬度为(74.96±13.03)N,米曲霉组硬度最低,原因可能是蛋白酶分解肌纤维蛋白,导致结构松散,对牛肉酱的品质有很大影响。中等程度的硬度,更有利于人们接受。对照组弹性为(4.18±1.41)mm,牛肉酱经发酵后弹性维持在2.90 mm左右,各组之间无显著性差异(P>0.05),可能各菌种对发酵牛肉酱弹性影响较为一致。对照组咀嚼性最高,而发酵后的牛肉酱咀嚼性都有降低,植物乳植杆菌组和酵母菌组差异不大,但米曲霉组咀嚼性最低,表明发酵使牛肉酱更易咀嚼。米曲霉分泌蛋白酶、淀粉酶水解大分子物质(蛋白质/淀粉)[32],但酶解过度导致口感过于绵软,缺乏消费者食用者的满足感。米曲霉组的胶黏性最低,可能因酶解作用破坏其结构,导致牛肉酱整体松散。从最终呈现的效果而言,相较于其他组别,采用酵母菌进行发酵,对牛肉酱质构品质的提升作用更为显著,赋予牛肉酱更佳的口感和更愉悦的食用体验,从而满足消费者对口感品质的追求,更易获得消费者的认可与接受。
表3 3种发酵剂对牛肉酱质构的影响
Table 3 Effect of three fermenting agents on the texture of beef sauce
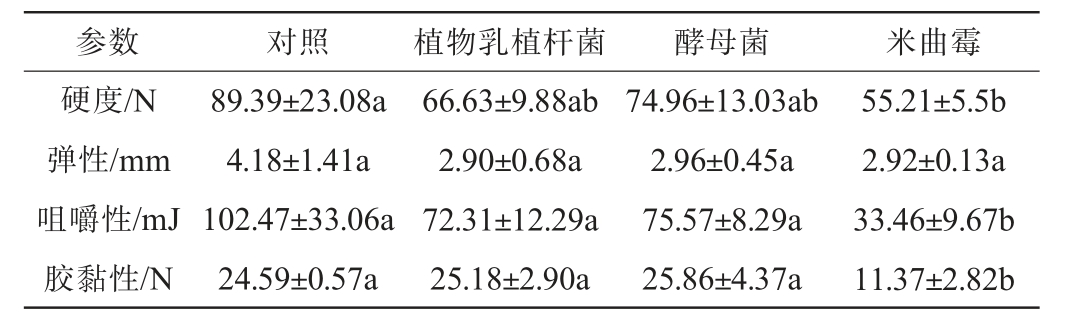
注:同行不同字母表示不同发酵组别所得各质构参数有显著性差异(P<0.05)。下同。
2.3 3种发酵菌剂对牛肉酱挥发性风味物质的影响
利用GC-MS测定了3种发酵菌剂发酵后牛肉酱中挥发性风味物质含量,结果见表4,不同类别挥发性风味物质结果见图2。
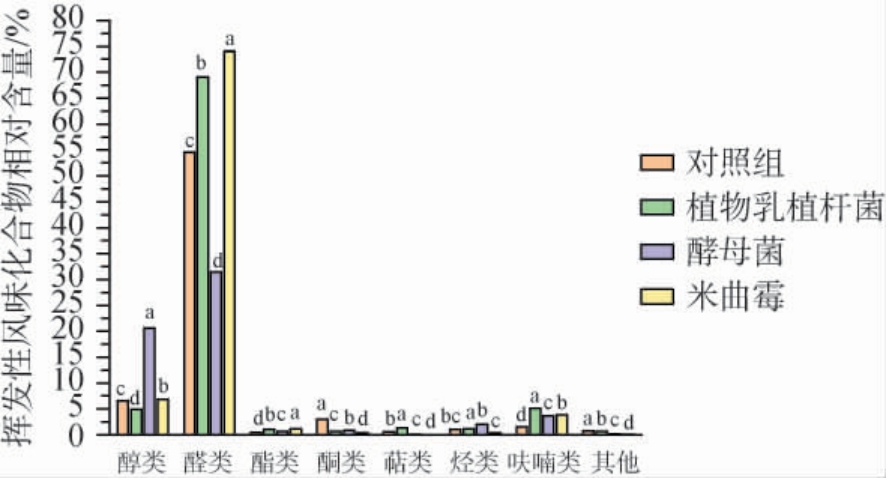
图2 3种发酵剂对牛肉酱不同类别挥发性风味化合物含量的影响
Fig.2 Effect of three fermentation agents on the volatile flavor compounds of beef sauce
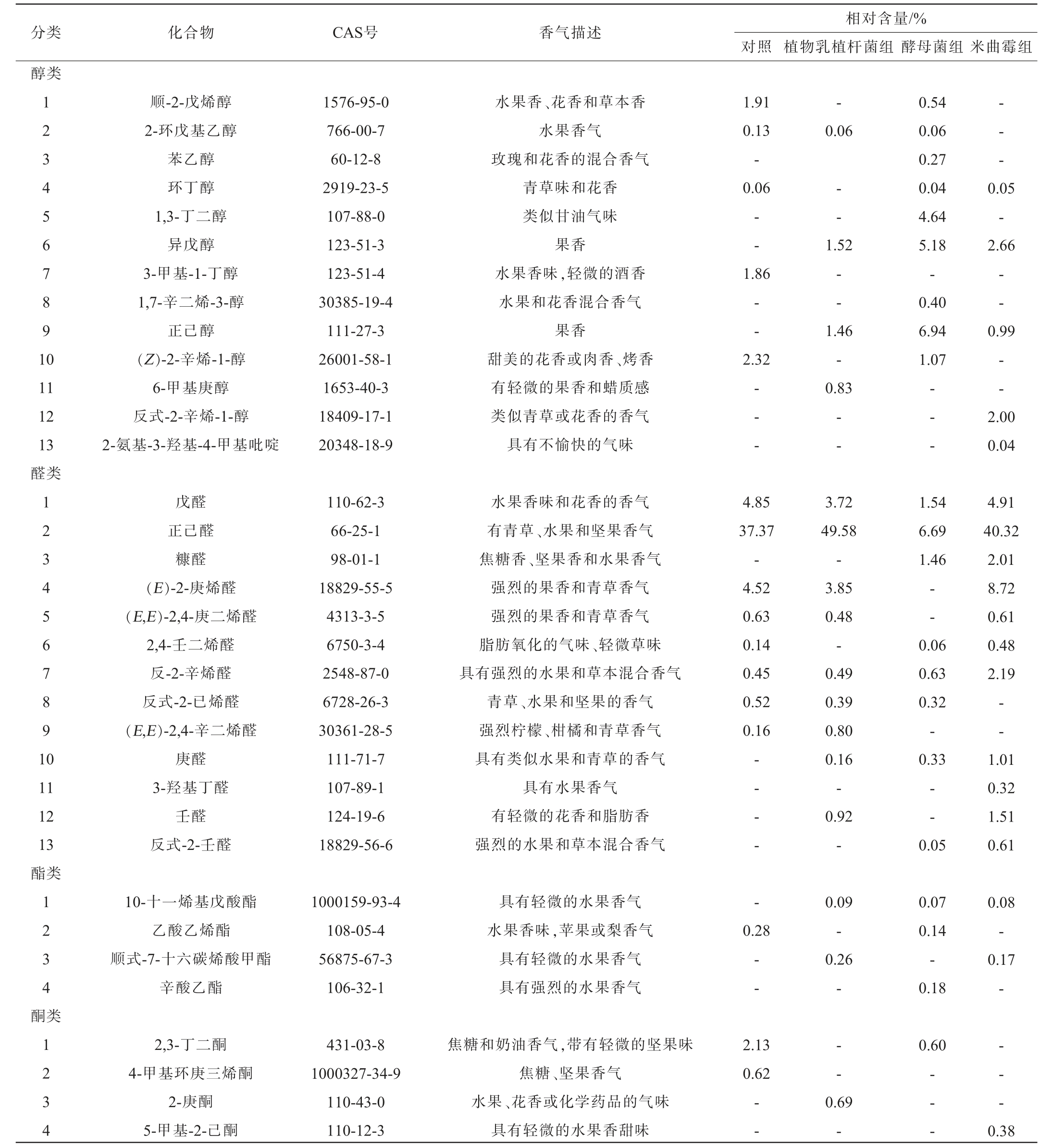
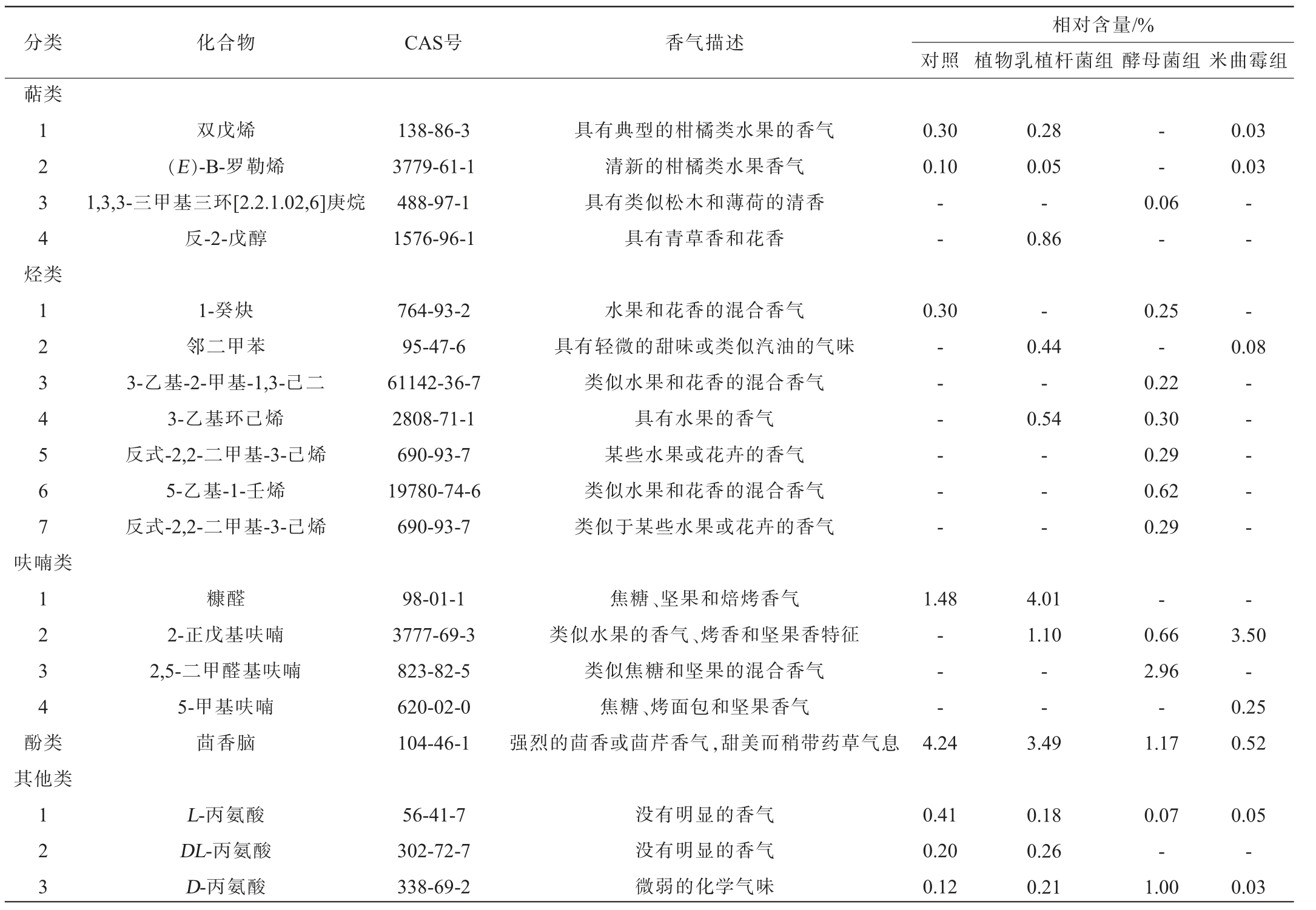
表4 牛肉酱中挥发性风味化合物气相色谱-质谱检测结果
Table 4 Determination results of volatile flavor compounds in beef sauce by GC-MS
续表
注:“-”表示未检出。
由表4可知,4种牛肉酱中共检出醇类、醛类、酯类、酮类、萜类、烃类、呋喃类、酚类及其他类化合物,共53种挥发性风味物质。发酵后的牛肉酱中醇类物质含量较对照组明显提高,其中酵母菌发酵组的醇类物质含量最高为19.14%。牛肉酱发酵后产生很多在自然发酵牛肉酱中未发现的醇类物质,如呈现玫瑰花香的关键物质苯乙醇(0.27%)、具有果香的异戊醇(5.18%)和正己醇(6.94%)等。酵母菌代谢均会产生大量醇类物质,因此,加酵母菌后产生的醇类的相对含量(19.14%)高于对照组的相对含量(6.28%)。植物乳植杆菌组的特征体现在醛类物质的显著积累,相对含量为69.03%,其中赋予水果、坚果香气的正己醛含量为49.58%,这可能与植物乳植杆菌促进脂质分解的作用有关。与植物乳植杆菌组相比,酵母菌发酵的牛肉酱中醛类物质(尤其是正己醛)相对含量显著降低。醛类由脂质氧化产生,阈值低,过量时会产生令人不悦的哈败味。酵母菌的代谢活动可能在一定程度上延缓或调控了脂肪氧化进程,避免了过多醛类物质的积累。米曲霉组含有独特的物质,如反式-2-辛烯-1-醇(2.0%),但同时也产生了微量的2-氨基-3-羟基-4-甲基吡啶,这种物质可能带来不愉快气味。米曲霉组的醛类物质含量最高(74.00%),但关键的风味醇、酯类物质含量均低于酵母菌组。此外,在各组中均检测出来自香辛料(如五香粉)的茴香脑,是一种大量存在于八角、茴香中的香味物质[36]。酮类、酯类、烃类等物质在不同组间虽均有检出,但相对含量变化不大。综上,酵母菌发酵能丰富牛肉酱的醇、酯类风味物质,并形成独特的气味。而植物乳植杆菌和米曲霉分别主导了醛类物质的积累,并产生独特的组分。
由图2可知,牛肉酱中醛类和醇类占比最高,而醛类、醇类和酯类是4个发酵组牛肉酱的主要风味物质。其中对照组、植物乳植杆菌发酵组、酵母菌发酵组、米曲霉发酵组的醛类物质的相对含量分别为54.55%、69.03%、31.46%和74.00%,添加酵母菌可以显著降低发酵牛肉酱的醛类物质(P<0.05),并且能够在一定程度上延缓了脂肪的氧化[33-34]。4个发酵组中醇类物质相对含量为6.58%、4.92%、20.62%和6.86%,酵母菌能够显著提高牛肉酱中的醇类物质含量,并能降低pH,产生酸类物质多有关联。酯类生成所需要的醇类大多来自碳水化合物、氨基酸的代谢以及脂质的氧化等,大多数的醇类化合物对风味的贡献不显著[35]。本研究中检测到的多种不饱和醇类对整体风味有重要贡献。如顺-2-戊烯醇呈现水果香、花香,异戊醇和正己醇具有果香,这些物质共同赋予了牛肉酱愉悦的水果、花香及甜香气息,所以对风味可能有一定的影响。牛肉酱经发酵后,相较于自然发酵牛肉酱,其醛类和酯类总量变多,酯类物质多具有果香味和甜味。结果表明,植物乳植杆菌组和米曲霉组发酵后,牛肉酱中醛类物质含量较对照组显著升高,但添加酵母菌组牛肉酱的醛类物质含量较对照组显著降低。3种发酵菌剂均能增加牛肉酱中酯类化合物的含量。酵母菌发酵组的醇类化合物含量显著高于其他组别,更有利于牛肉酱中挥发性物质的形成,在发酵牛肉酱过程中,展现出显著的潜在优势。
2.4 牛肉酱电子鼻分析结果
通过电子鼻分析不同发酵剂牛肉酱的气味,并根据响应值绘制雷达图,结果见图3。由图3可知,不同菌种发酵的牛肉酱其整体气味特征存在明显差异。酵母菌处理组在代表醇类、醛酮类、氮氧化合物及有机硫化物的传感器(W2S,W5S,W2W)上响应值普遍最高,显示出最为浓郁和复杂的香气特征。植物乳植杆菌组在上述多数传感器上的响应值次于酵母菌组,但高于米曲霉组和对照组。而米曲霉组与对照组在雷达图上的响应信号重叠较多,表明二者的气味特征较为相似。这些结果直观地反映出酵母菌在丰富牛肉酱香气方面效果最为显著。综上,不同发酵菌剂对牛肉酱的整体气味特征具有差异化影响。酵母菌在优化牛肉酱风味品质方面具有最大潜力,这与GC-MS的结果相互印证。
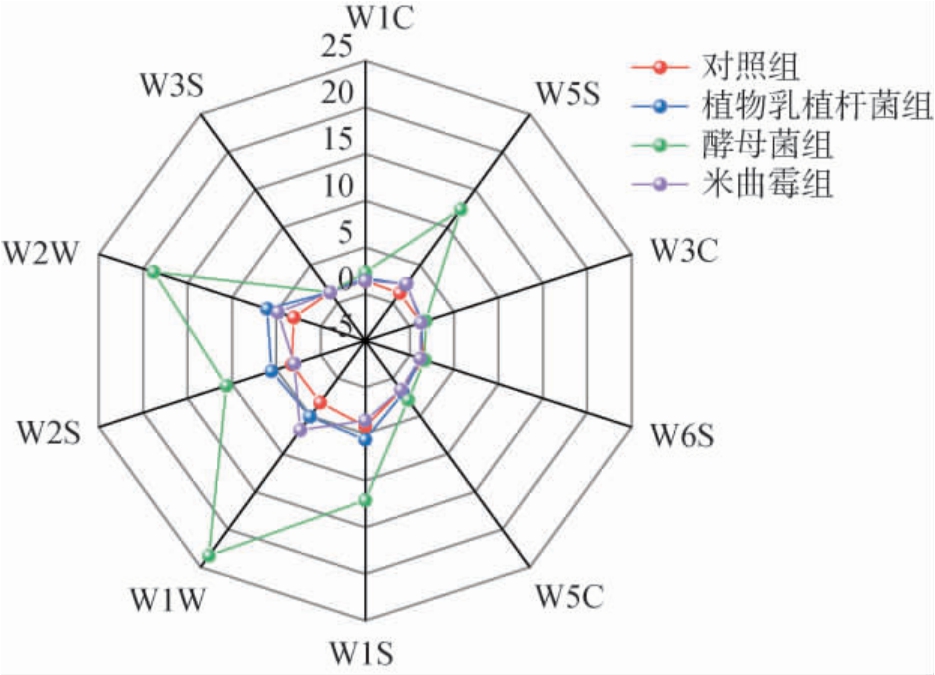
图3 牛肉酱的气味电子鼻响应值雷达图
Fig.3 Radar chart of the odor response value of beef sauce using electronic nose
2.5 基于电子鼻的传感器响应值牛肉酱主成分分析结果
采用主成分分析法基于电子鼻的传感器响应值,对不同发酵菌剂处理的牛肉酱样品的整体香气特征进行分析,结果见图4。
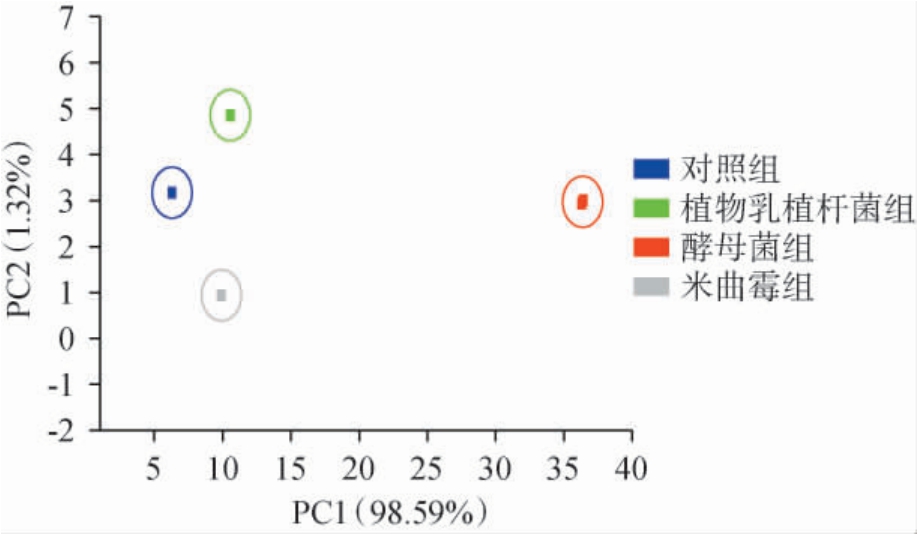
图4 基于电子鼻响应值的牛肉酱主成分分析
Fig.4 Principal component analysis of beef sauce based on the response value of electronic nose
由图4可知,第1主成分(principal component 1,PC1)(98.59%)和PC2(1.32%)的累计方差贡献率为99.91%(>80%),表明主成分可以反映样品的香气的整体信息[37]。不同发酵菌剂的牛肉酱的气味可以进行有效的区分,说明不同发酵菌剂的牛肉酱的香气特征存在明显的差异性。PC1方差贡献率远大于PC2,说明样品在横坐标距离越大,其差异性越大,样品的横坐标顺序从左到右为未添加发酵菌剂(对照组)、植物乳植杆菌、米曲霉、酵母菌,与传感器雷达信号强度大小一致。其中,对照组和样品添加植物乳植杆菌组总体在横坐标上距离较近,说明二者香气成分相似;对照组和样品添加米曲霉组总体在横坐标上距离也很近,说明二者香气成分也十分相似;样品添加植物乳植杆菌、样品添加酵母菌总体横坐标距离相对而言较远,说明二者香气成分有很大不同。
2.6 不同发酵剂对牛肉酱感官评价影响
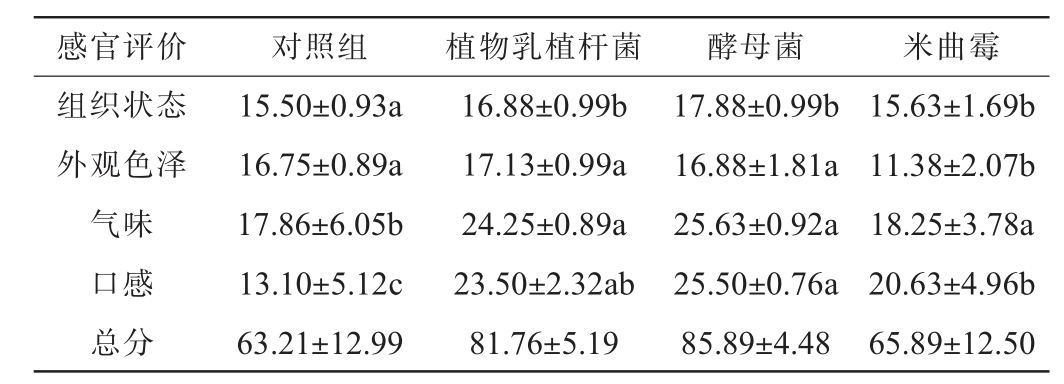
3种发酵剂对牛肉酱感官评价影响结果见表5。由表5可知,与自然发酵的对照组相比,经过发酵的牛肉酱在组织形态、气味和口感等感官品质上均表现出更优的特性。相比于自然发酵,发酵菌剂发酵能在一定程度上提高牛肉酱的感官品质。4组牛肉酱的组织形态差异不大,酵母菌发酵组在组织状态、外观色泽、气味和口感各个方面表现最佳。感官评价的结果与质构和风味的数据基本一致。感官评价结果有效印证了仪器分析的结果。
表5 牛肉酱的感官评价结果
Table 5 Sensory evaluation results of beef sauce
3 结论
本研究通过单菌发酵实验揭示了植物乳植杆菌、酵母菌和米曲霉对牛肉酱品质的差异化影响。植物乳植杆菌快速产酸使pH降低至4.64,有效抑制杂菌生长;酵母菌在风味提升方面表现突出,在发酵后期代谢生成酯类、醇类(如苯乙醇、异戊醇)等挥发性风味物质,显著增强香气,同时维持适中的硬度(74.96 N)和咀嚼性(75.57 mJ),感官评分最高,综合品质最优;米曲霉则通过分泌蛋白酶与淀粉酶,促进蛋白质降解,米曲霉通过酶解作用(如蛋白酶降解肌纤维)大幅降低硬度(55.21 N)和咀嚼性(33.46 mJ),但过度软化导致胶黏性下降53.8%,可能影响消费者对质构的接受度。综合结果表明,植物乳植杆菌、酵母菌和米曲霉3种发酵菌剂均能对牛肉酱品质产生影响,显著提升其风味;其中,酵母菌发酵组在香气物质生成、质构改善及感官体验等综合表现上最优,展现出对牛肉酱品质的全面优化潜力。
[1] 高娇娣.多元化的调味酱千亿级的大市场[N].中国食品报,2024-03-28(004).
[2] ZHOU Y J,ZHANG Y,PANG G Q,et al.Effect of inoculation of starter on physicochemical properties and texture characteristics of fermented beef jerky[J].J Food Process Preserv,2021,45(9):15744.
[3] 杨晓钢.低酸发酵牛肉发酵剂的筛选、工艺优化及效果评价[D].无锡:江南大学,2022.
[4] 于潇,马可心,潘德胤,等.三株乳酸菌对发酵牛肉干理化性质及蛋白质高级结构的影响[J].食品工业科技,2025,46(23):98-107.
[5] 鄢嫣,杨明柳,周迎芹,等.不同发酵剂对发酵牛肉品质、风味特性和安全性的影响[J].中国食品学报,2024,24(4):170-185.
[6] 张玉.发酵牛肉干发酵工艺优化及品质特性研究[D].长春:吉林大学,2021.
[7] 夏让,孔保华,张宏伟,等.不同发酵剂对发酵牛肉串品质的影响[J].食品与发酵工业,2010,36(6):196-200.
[8] 张丽,孙宝忠,魏晋梅,等.牦牛肉发酵过程中的品质变化分析[J].肉类研究,2014,28(5):20-24.
[9] 陈俊宏,王洋,李芹,等.乳酸菌发酵工艺对肉糜理化性质及品质的影响[J].中国调味品,2021,46(6):5-10.
[10] 杜宝.不同发酵剂和贮藏温度对发酵羊肉香肠品质的影响[D].呼和浩特:内蒙古农业大学,2018.
[11] 刘兰.不同发酵剂对发酵牛肉干品质的影响[D].呼和浩特:内蒙古农业大学,2018.
[12] 赵改名,李璇,祝超智,等.牛肉发酵香肠成熟过程中理化性质和微生物菌群变化[J].食品与发酵工业,2023,49(10):91-99.
[13] 张秋会,孟高歌,王晗,等.腊肉源酵母菌对发酵牛肉品质特性的影响[J].现代食品科技,2024,40(4):55-63.
[14] 王德宝.发酵剂对发酵羊肉香肠蛋白质、脂质分解代谢及风味物质生成机制影响的研究[D].呼和浩特:内蒙古农业大学,2020.
[15] 赵改名,焦阳阳,祝超智,等.发酵时间对半干型发酵牛肉干品质及蛋白质构象的影响[J].食品科学,2021,42(20):45-51.
[16] 王德宝,孙学颖,王柏辉,等.复合发酵剂对羊肉香肠发酵成熟过程中理化品质及安全性能的影响[J].中国食品学报,2020,20(6):137-145.
[17] 杨晓钢,赵鑫锐,堵国成.低酸牛肉发酵剂的筛选、工艺优化及品质特性研究[J].食品与发酵工业,2022,48(19):185-195.
[18] 高静,曹叶萍,郇延军.单一菌种和复合菌种发酵对猪肉脯挥发性风味物质的影响[J].食品与发酵工业,2019,45(1):128-136.
[19] ARIEF I I,WULANDARI Z,ADITIA E L,et al.Physicochemical and microbiological properties of fermented lamb sausages using probiotic Lactobacillus plantarum IIA-2C12 as starter culture[J].Proced Environ Sci,2014,20:352-356.
[20] 贾娜,马宏慧,刘登勇,等.直投式发酵剂对发酵牛肉干品质的影响[J].中国食品学报,2014,14(12):106-112.
[21] 赵岩,刘佳彤,吴都峰,等.块状牛肉发酵特性与工艺优化[J].肉类研究,2013,27(9):11-14.
[22] 周建中,高蕾,严宏孟,等.不同发酵方式对发酵马肉肠贮藏期品质劣变及食用安全性的影响[J].肉类研究,2022,36(10):29-34.
[23] 张秋会,孟高歌,王晗,等.特色腊肉源细菌发酵剂对发酵牛肉品质的影响[J].食品工业科技,2024,45(8):151-157.
[24] 孙光城,罗秀群,林丹,等.基于GC-MS分析牛肉不同部位对牛肝菌牛肉酱品质及挥发性香气成分的影响[J].食品工业科技,2024,45(19):216-227.
[25] 徐晔,张韬,夏玲燕,等.植物乳植杆菌JBP3和罗伊氏粘液乳杆菌JBR3对牛肉干品质的影响[J].食品工业科技,2025,46(22):225-234.
[26] 张丽华,王子阳,王文博,等.顶空固相微萃取-气相色谱-质谱联用结合气味活度值法分析不同脱腥方法对鸡爪挥发性风味物质的影响[J].肉类研究,2025,39(4):17-23.
[27] S′LIWI 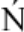 SKA M,WIS′NIEWSKA P,DYMERSKI T,et al.Applicationof electronic nose based on fast GC for authenticity assessment of polish homemade liqueurs called Nalewka[J]. Food Anal Meth,2016,9(9):2670-2681.
SKA M,WIS′NIEWSKA P,DYMERSKI T,et al.Applicationof electronic nose based on fast GC for authenticity assessment of polish homemade liqueurs called Nalewka[J]. Food Anal Meth,2016,9(9):2670-2681.
[28] 徐君强.发酵剂与木瓜蛋白酶对发酵牛肉干品质的影响[D].呼和浩特:内蒙古农业大学,2016.
[29] 焦阳阳.发酵对半干型牛肉干品质的影响研究[D].郑州:河南农业大学,2021.
[30] 陈曦,许随根,周彤,等.贵州酸肉中的植物乳杆菌对发酵香肠风味和品质特性的影响[J].中国食品学报,2018,18(6):174-182.
[31] 陈文碧,刘心发,史梅莓,等.乳酸菌接种发酵对泡榨菜风味品质的影响[J].食品与发酵科技,2025,61(1):25-33.
[32] 温馨.低温发酵微生物筛选及其对牛肉风味品质的影响研究[D].长沙:中南林业科技大学,2024.
[33] 周亚军,张玉,陈艳,等.发酵牛肉干加工中理化特性与风味品质分析[J].食品科学,2021,42(14):240-247.
[34] ZHANG W G,XIAO S,AHN D U.Protein oxidation: Basic principles and implications for meat quality[J].Crit Rev Food Sci Nutr,2013,53:1191-1201.
[35] LIU S L,LI Y H,WANG J G,et al.Effects of different protease-producing lactic acid bacteria on the oxidation of air-dried beef protein[J]. Food Ferment Ind,2021,47(20):68-74.
[36] ZHOU X,MA N,WANG X,et al.Changes in nutritional quality of fermented plant-protein meat during fermentation and storage[J].Food Res Develop,2024,45(17):86-94.
[37] 冯美琴,李天翊,孙健.复合发酵剂对发酵鱼肉香肠品质、风味及其多肽抗氧化活性的影响[J].食品科学,2023,44(24):138-145.