益生菌作为定植在人和动物体内能改变宿主健康状态的一类活性微生物,具有调节肠道菌群、增强肠道屏障功能等作用[1]。瑞士乳杆菌(Lactobacillus helveticus)是一种公认安全微生物(Generally Recognized as Safe,GRAS),具有抗高血压、抗菌、抗炎及免疫调节等作用[2]。瑞士乳杆菌2171对吸入性抗原具有抗敏感的活性,能产生免疫调节活性[3]。瑞士乳杆菌R0052能减少促炎因子、增加抗炎因子的生成,减轻肠炎症状[4]。其产生的抗菌肽、S层蛋白、胞外多糖(exopolysaccharide,EPS)都具有抑制致病菌的能力[5]。
EPS是益生菌生长代谢产生的次生代谢物,具有抗氧化、抗菌等活性。研究表明,植物乳杆菌MM89分泌的EPS通过增加淋巴细胞等的产生,对免疫抑制小鼠的免疫功能产生调节作用[6]。双歧杆菌分泌的SF-EPS具有抗氧化及调节肠道菌群的作用[7]。目前,EPS的研究主要集中在抗氧化、调节免疫功能等方面,对于抗菌方面的研究较少。ALI A H等[8]研究表明,粪肠球菌84B EPS对大肠杆菌、金黄色葡萄球菌等致病菌具有抑制作用。ZHANG J等[9]研究表明,嗜热链球菌GST-6 EPS对鼠伤寒沙门氏菌、金黄色葡萄球菌等致病菌最低抑制浓度(minimum inhibitory concentration,MIC)分别达10 mg/mL、6 mg/mL。
本研究以瑞士乳杆菌(Lactobacillus helveticus)MG0817-2为研究对象,通过抗生素敏感试验、溶血试验、耐酸耐胆盐试验、抑菌试验考察瑞士乳杆菌MG0817-2的安全性、耐受性及抑菌活性,对瑞士乳杆菌MG0817-2的胞外多糖进行提取、分离及纯化,利用傅里叶变换红外光谱解析多糖结构,并分析其抑菌性能。以期为益生菌的开发提供菌种资源,为EPS在食品等领域的开发利用提供技术支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
瑞士乳杆菌(Lactobacillus helveticus)MG0817-2:某牛场牛瘤胃内容物所分离出;大肠杆菌(Escherichia coli)ATCC25922、金黄色葡萄球菌(Staphylococcus aureus)ATCC6538:中国兽医微生物菌种保藏管理中心;鼠伤寒沙门氏菌(Salmonella typhimurium)SMO22:美国杜克大学分子遗传学和微生物学实验室惠赠。
1.1.2 试剂
木瓜蛋白酶、无水葡萄糖:上海源叶生物科技有限公司;3 500 Da透析袋:北京兰杰柯科技有限公司;药敏纸片:杭州微生物试剂有限公司;纤维素DEAE-52、葡聚糖凝胶G-100:北京索莱宝科技有限公司;血琼脂平板培养基:广东环凯生物科技有限公司。所用试剂均为分析纯。
1.1.3 培养基
MH液体培养基、LB液体培养基、MRS液体培养基、Baird-Parker琼脂基础培养基、沙门-志贺菌属(Salmonella Shigella,SS)琼脂培养基:海博生物股份有限公司。其中,MH培养基、LB培养基、MRS培养基:在液体培养基的基础上添加1.5%的琼脂。不同培养基灭菌方式参照培养基要求。
1.2 仪器与设备
THZ-82气浴恒温振荡器:金坛区金城春兰实验仪器厂;YB-FD-20D真空冷冻干燥机:上海亿倍仪器实业有限公司;Spouk 10M全波长酶标仪:瑞士帝肯公司;Nicolet iS10傅里叶红外光谱仪:Thermo Fisher Scientific Inc公司。
1.3 方法
1.3.1 菌株的活化及培养
将大肠杆菌ATCC25922、金黄色葡萄球菌ATCC6538、鼠伤寒沙门氏菌SM022、瑞士乳杆菌MG0817-2甘油冻存液接种于LB培养基平板上,37 ℃培养24 h后,挑取单菌落接种于LB液体培养基中,37 ℃、150 r/min振荡培养24 h。连续传代2次后,4 ℃保存备用。
1.3.2 菌株抗生素敏感性
采用纸片琼脂扩散法(K-B法)评估瑞士乳杆菌MG0817-2对10种抗生素(如青霉素、阿莫西林等)的敏感性,将活化后的菌株接种于MRS液体培养基中,37 ℃、150 r/min培养24 h,用磷酸盐缓冲液(phosphate buffer solution,PBS)配制成活菌浓度为1×109 CFU/mL菌悬液,取100 μL均匀涂布于MRS培养基平板。将药敏纸片均匀放置于平板上,经37 ℃培养24 h后,使用游标卡尺测测量各药敏纸片的抑菌圈直径,参照美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)对抗药物敏感性的最小抑菌圈直径大小来判定菌株的药敏性,判定结果分为敏感(S)、中度敏感(M)、抗性(R)。
1.3.3 菌株溶血试验
用接种环取一环活化后的瑞士乳杆菌的菌液,在血琼脂平板培养基上划线,观察比较溶血情况。若菌落四周出现草绿色环,则为α-溶血;若菌落四周出现透明溶血环,则为β-溶血;若菌落四周无任何变化,则为γ-溶血,即不溶血。
1.3.4 菌株耐酸、耐胆盐能力测定
(1)耐酸试验
菌株耐酸试验根据褚鑫龙等[10]描述的方法并稍作修改,将活化好的菌株接种于MRS液体培养基中,37 ℃、150 r/min培养12 h,将菌液OD600nm值调至1.0,按10%(V/V)接种量将菌液分别接种至pH值为2.0和3.0的MRS液体培养基(2 mol/L HCl调整pH),混匀后于37 ℃恒温培养箱静置培养2 h。测定0 h和2 h活菌数,以菌株存活率反映菌株的耐酸能力,存活率计算公式如下:
(2)耐胆盐试验
按10%(V/V)接种量将活化好的菌液分别接种至胆盐含量分别为0%、0.2%、0.4%的MRS液体培养基中,混匀后于37 ℃恒温培养箱静置培养2 h。测定0 h和2 h活菌数,以菌株存活率反映菌株的耐胆盐能力,存活率计算公式同上。
1.3.5 菌株抑菌试验
1.3.5.1 牛津杯琼脂扩散法
将培养至对数生长期的瑞士乳杆菌及致病菌(大肠杆菌、金黄色葡萄球菌、鼠伤寒沙门氏菌)经4 000 r/min、15 min离心,收集瑞士乳杆菌上清液,并将瑞士乳杆菌和致病菌菌液浓度调整至1×109 CFU/mL,备用。取100 μL致病菌均匀涂布于LB培养基平板上,分别加入200 μL瑞士乳杆菌菌液及其上清液于直径为8 mm的牛津杯中,37 ℃培养18 h,测量抑菌圈直径。
1.3.5.2 共培养实验
参考戴璐等[11]的方法并稍作修改,经4 000 r/min、15 min离心收集瑞士乳杆菌上清液,并将瑞士乳杆菌MG0817-2和致病菌(鼠伤寒沙门氏菌、金黄色葡萄球菌)的菌液浓度调整至1×109 CFU/mL,于800 μL LB液体培养基中分别加入100 μL瑞士乳杆菌菌液(上清液)和100 μL致病菌菌液,致病菌为对照,于37 ℃、150 r/min条件下培养0、4 h、8 h、12 h时测定致病菌活菌数,其中,SS培养基用于鼠伤寒沙门氏菌计数,在Baird-Parker琼脂基础培养基用于金黄色葡萄球菌计数,与对照组比较活菌数的差异。
1.3.6 胞外多糖的提取、分离纯化及含量测定
1.3.6.1 胞外多糖的提取
采用陈亮[12]的方法并进行适当修改,将活化后的瑞士乳杆菌菌液按按10%(V/V)接种量接种至MRS液体培养基,37 ℃培养24 h,菌液经离心(4 000 r/min、15 min)去除菌体后收集上清液,加入3倍体积的无水乙醇,在4 ℃冷藏静置12 h,离心(4 000 r/min、15 min)获得沉淀物,室温干燥至恒质量后称量,加入沉淀物质量2倍的木瓜蛋白酶及200倍的水于60 ℃处理1 h除去蛋白质后,100 ℃、10 min灭酶。进一步采用三氯乙酸(trichloroacetic acid,TCA)-正丁醇法再次去除蛋白质,TCA与正丁醇的质量体积比为1∶10,TCA-正丁醇的体积与多糖溶液的体积相等,充分振荡20 min于4 ℃静置分层,获取粗多糖溶液。将粗多糖溶液装入截留分子量为3 500 Da的透析袋,用超纯水透析72 h,透析期间每隔3 h全部更换一次超纯水,至透析完成,收集透析袋液体,经过浓缩、冷冻干燥以获得粗多糖。
1.3.6.2 胞外多糖分离纯化
称取600 mg胞外粗多糖溶于5 mL去离子水,将其滴入纤维素DEAE-52离子交换柱层析,依次以0(即去离子水)、0.2 mol/L、0.4 mol/L、0.6 mol/L和0.8 mol/L NaCl溶液为流动相进行洗脱,以0.5 mL/min流速20 min收集一管,每个梯度收集50管,采用苯酚-硫酸法跟踪检测胞外多糖含量,以管数为横坐标,波长490 nm处的吸光度值为纵坐标,绘制洗脱曲线。将相同浓度洗脱液洗脱得到吸光度值>0.1的多糖溶液进行合并,冷冻干燥得到初步纯化的EPS,计算多糖得率。随后,采用葡聚糖凝胶G-100层析,以超纯水为流动相,流速为0.5 mL/min,每管收集10 mL,采用苯酚-硫酸法测定胞外多糖含量,收集洗脱曲线中峰值位置的洗脱液,经过浓缩、透析和冷冻干燥后,最终分离得到纯化胞外多糖,计算胞外多糖得率,胞外多糖得率计算公式如下:
式中:A为纯化前粗多糖的质量,mg;B为纯化冻干后多糖的质量,mg。
1.3.6.3 胞外多糖测定
通过苯酚-硫酸法进行测定,取10 mg葡萄糖标准品配制成0.1 mg/mL的葡萄糖标准溶液。分别取葡萄糖标准溶液0、0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL于试管中,用纯水补足至2 mL,分别加入1 mL 6%苯酚和5 mL浓硫酸,混匀后室温反应30 min。在波长495 nm处测定吸光度值,葡萄糖质量浓度(X)为横坐标,吸光度值(Y)为纵坐标绘制葡萄糖标准曲线,获得葡萄糖标准曲线回归方程:Y=1.952 4X+0.078 4(相关系数R2=0.991 1),根据回归方程计算样品中的总胞外多糖含量。
1.3.7 胞外多糖红外光谱分析
采用傅里叶变换红外光谱仪测定多糖样品的红外光谱,取1 mg干燥至恒质量的胞外多糖与KBr粉末按1∶100混合,研磨5 min后用压片机压成KBr薄片,在4 000~400 cm-1范围内进行扫描,记录红外光谱。
1.3.8 胞外多糖的抑菌性能测定
1.3.8.1 最小抑菌浓度和最小杀菌浓度试验
将致病菌菌液接种于MH液体培养基,37 ℃培养24 h,将菌液浓度稀释至1×106 CFU/mL。在1~10管中分别加入100 μL MH液体培养基,取100 μL 320 mg/mL瑞士乳杆菌MG0817-2胞外多糖加至第1管中,混匀后依次梯度稀释,使其质量浓度分别为1.25mg/mL、2.5mg/mL、5mg/mL、10mg/mL、20 mg/mL、40 mg/mL、80 mg/mL、160 mg/mL,第9管加入100 μL 2.5 mg/mL卡那霉素(阳性对照),第10管加入MH液体培养基(阴性对照)。在1~10管中分别加入100 μL菌液混匀,37 ℃培养18 h。以无菌体生长所对应的最低质量浓度为(MIC),从清澈孔板中分别取100 μL样品涂布于MH琼脂平板,37 ℃孵育24 h,以生长的菌落数<3个所对应的最低质量浓度为最低杀菌浓度(minimum bactericidal concentration,MBC)。
1.3.8.2 滤纸片扩散法
采用滤纸片扩散法[13]测定多糖对致病菌的抑制效果,取20 mg/mL瑞士乳杆菌MG0817-2胞外多糖,加入蒸馏水依次稀释,配制成2.5 mg/mL、5 mg/mL、10 mg/mL的多糖溶液,取浓度为1×109 CFU/mL致病菌悬液100 μL接种于MH培养基平板。将灭菌圆滤纸片(6 mm)按“品”字形分布贴于MH培养基平板,PBS为空白对照,每片圆滤纸片滴加20 μL多糖溶液,37 ℃培养18 h后观察有无抑菌圈,形成透明的抑菌圈,则判断有抑菌活性,并用直尺测量抑菌圈直径,抑菌圈直径≥20 mm为极敏、抑菌圈直径15~20 mm高敏、抑菌圈直径10~15 mm为中敏、抑菌圈直径<10 mm为低敏。
1.3.9 数据处理
试验数据经Excel 2010初步处理后用SPSS 22.0进行单因素方差分析(analysis of variance,ANOVA),P<0.05表示差异显著。
2 结果与分析
2.1 菌株抗生素敏感试验
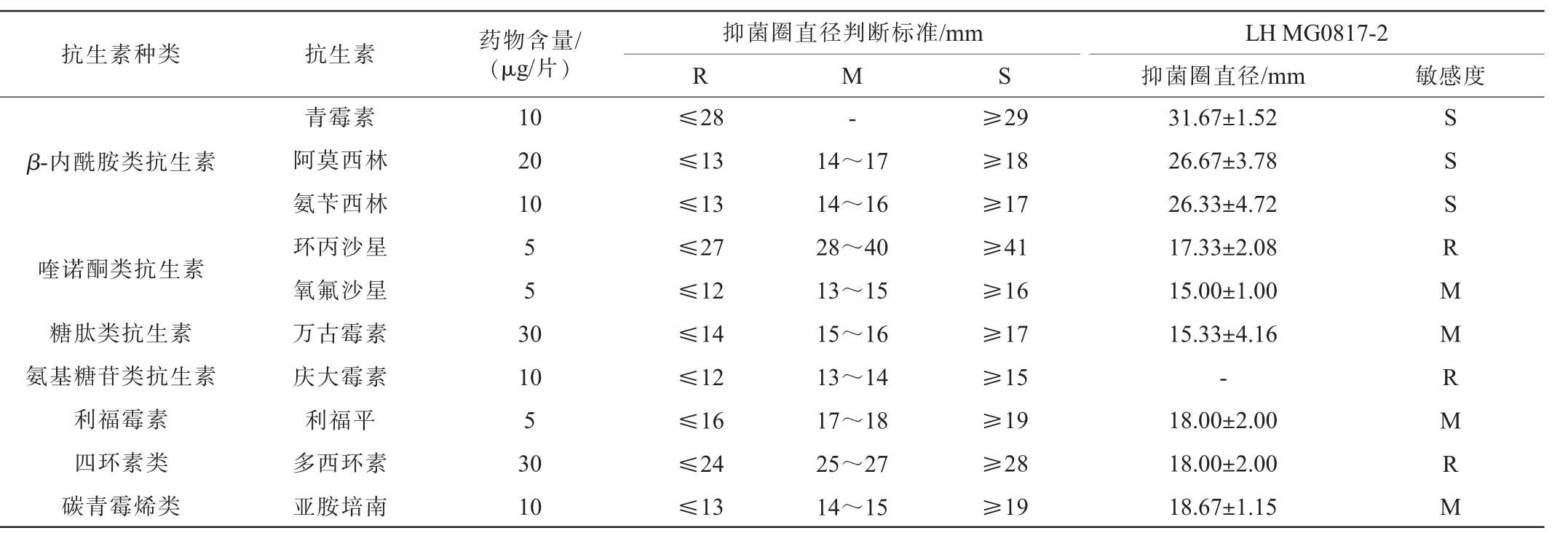
瑞士乳杆菌MG0817-2抗生素敏感药敏试验结果见表1。由表1可知,瑞士乳杆菌MG0817-2对青霉素、阿莫西林、氨苄西林等β-内酰胺类抗生素高度敏感;对氧氟沙星、万古霉素、利福平及亚胺培南中度敏感;对环丙沙星、庆大霉素及多西环素耐药。该菌株对11种抗生素中的6种抗生素敏感,与李晓颖等[14]分离出的5株植物乳杆菌相比,该菌株对抗生素的敏感性较高,表明菌株的耐药性低、安全性高。
表1 瑞士乳杆菌MG0817-2抗生素敏感试验结果
Table 1 Antibiotic sensitivity test results of Lactobacillus helveticus MG0817-2
2.2 菌株溶血试验
溶血特性是筛选益生菌的重要因素,不具有溶血特性的益生菌才安全[15]。菌株的溶血试验结果见图1。由图1可知,菌株瑞士乳杆菌MG0817-2未出现溶血圈,表明不产生溶血素,符合益生菌安全性要求。

图1 瑞士乳杆菌MG0817-2的溶血试验结果
Fig.1 Hemolytic test results of Lactobacillus helveticus MG0817-2
2.3 菌株耐酸、耐胆盐能力测定
益生菌应具有适应胃酸的低pH和肠液胆盐的高渗透压能力[16]。瑞士乳杆菌MG0817-2在pH 2.0、pH 3.0条件下的存活率分别为2%和75%,表明瑞士乳杆菌MG0817-2对可耐受pH值为3.0。这与马翠柳等[17]研究的唾液乳杆菌ZJBF005在pH 2.0条件下的存活率结果相似,高于汤伟等[18]研究的屎肠球菌Ef026在pH 3.0条件下的存活率(17.4%),与鼠李糖乳杆菌Z23在pH 3.0条件下的存活率(85.42%)相似[19],表明其对酸的耐受能力较强,有助于其作为活菌通过胃到达小肠发挥作用。
瑞士乳杆菌MG0817-2在胆盐含量为0.2%和0.4%条件下的存活率分别为88.89%和83.33%,明显高于聂阿真等[20]分离出的乳酸片球菌(Pediococcus acidilactici)、植物乳植杆菌(Lactiplantibacillus plantarum)、内氏液体乳杆菌(Liquorilactobacillus nagelii)3株乳酸菌的存活率(53.43%、75.78%、52.91%),与嗜酸乳杆菌GLA09[21]的存活率(75.21%)相似,表明瑞士乳杆菌MG0817-2对胆盐具有良好的耐受能力,对有助于其作为活菌到达小肠并发挥微生态制剂的作用。
2.4 菌株抑菌实验
瑞士乳杆菌MG0817-2的菌液及其上清液对鼠伤寒沙门氏菌的抑菌圈直径分别为11.67 mm、12.17 mm;瑞士乳杆菌MG0817-2的菌液及其上清液对金黄色葡萄球菌的抑菌圈直径分别为10.00 mm、9.83 mm。结果表明,瑞士乳杆菌MG0817-2的上清液抑菌性能更好,且对鼠伤寒沙门氏菌的抑制效果较好。与陈楠等[22]分离出的粪肠球菌ZJUIDS-D016相比,瑞士乳杆菌MG0817-2上清液对鼠伤寒沙门氏菌的抑制作用较高。
将瑞士乳杆菌MG0817-2和致病菌菌液进行共培养,结果见图2。由图2A可知,随着培养时间在0~12 h范围内的延长,鼠伤寒沙门氏菌菌液浓度呈先升高后趋于平稳的趋势,而瑞士乳杆菌MG0817-2菌液及其上清液菌体浓度呈下降趋势,且上清液菌体浓度下降较快,培养12 h时,其菌落数为4.52 lg(CFU/mL)。由图2B可知,随着培养时间在0~12 h范围内的延长,金黄色葡萄球菌菌液浓度呈先升高后趋于平稳的趋势,而瑞士乳杆菌MG0817-2菌液及其上清液菌体浓度呈下降趋势,且上清液菌体浓度下降较快,培养12 h时,其菌落数为4.90 lg(CFU/mL)。XUE X G等[23]研究表明,干酪乳杆菌KLS1上清液对金黄色葡萄球菌的抑菌直径为17.83 mm,高于瑞士乳杆菌MG0817-2,并且发现细菌素KLS1是其产生抑菌活性的关键。根据XU X Q等[24]的研究可知,干酪乳杆菌NA-2 EPS能通过抑制细菌生物膜的生长产生抑菌效果。表明瑞士乳杆菌MG0817-2的上清液中可能因含有细菌素、抗菌肽及EPS等物质产生抑菌效果。
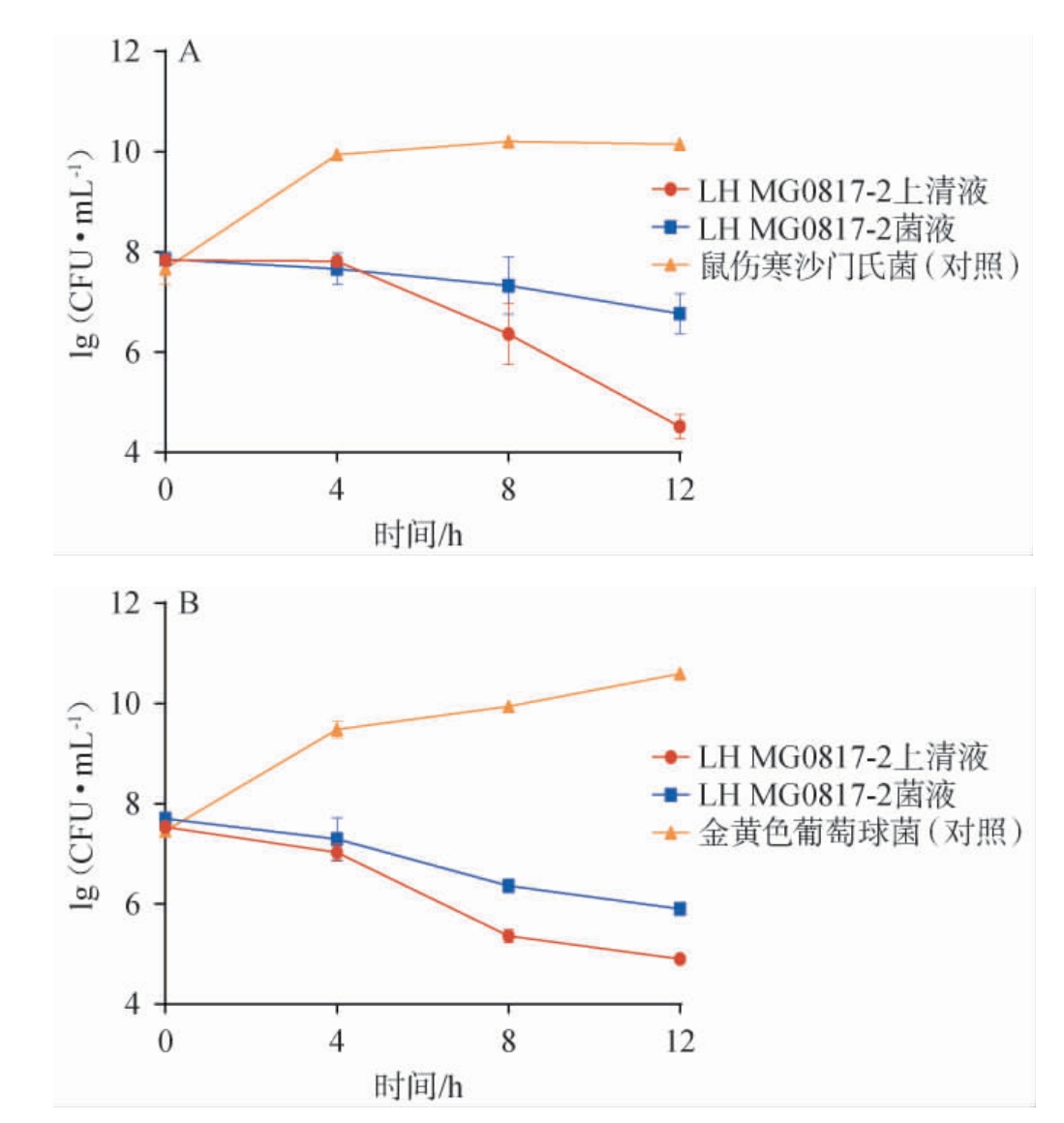
图2 瑞士乳杆菌MG0817-2菌液及其上清液对鼠伤寒沙门氏菌(A)及金黄色葡萄球菌(B)的抑菌能力测定结果
Fig.2 Determination results of antibacterial ability of Lactobacillus helveticus MG0817-2 bacterial solution and supernatant to Salmonella typhimurium (A) and Escherichia coli (B)
2.5 胞外多糖分离纯化
瑞士乳杆菌MG0817-2胞外多糖经纤维素DEAE-52及葡聚糖凝胶G-100分离纯化所得洗脱曲线见图3。由图3A可知,纤维素DEAE洗脱曲线出现两个明显单一峰,其中,采用纯水洗脱时,出现的峰宽而窄,峰高细长,表明洗脱的组分较集中,洗脱效果好,为中性胞外多糖,其得率为32.5%,采用0.2 mol/L、0.4 mol/L、0.6 mol/L、0.8 mol/L的NaCl溶液洗脱出来的组分较少。因此,选择去离子水洗脱得到的中性胞外多糖进行进一步纯化。
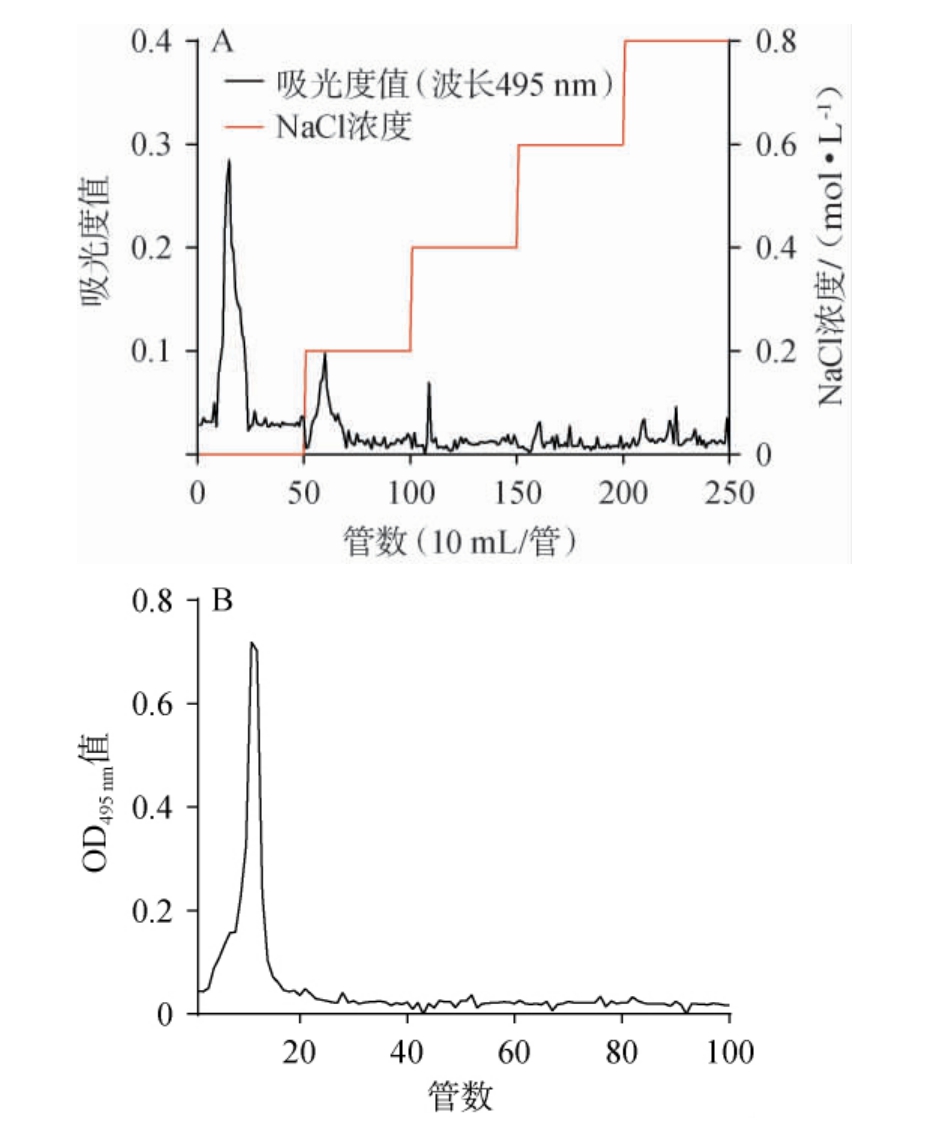
图3 瑞士乳杆菌MG0817-2纤维素DEAE-52洗脱曲线(A)及葡聚糖凝胶G-100洗脱曲线(B)
Fig.3 Elution curves of cellulose DEAE-52 (A) and glucan gel G-100 (B) for Lactobacillus helveticus MG0817-2
由图3B可知,葡聚糖凝胶G-100洗脱曲线出现单一峰,说明该洗脱得到的中性胞外多糖成分均一,胞外多糖得率为82.05%,经过冷冻干燥获得胞外多糖得率为71.9%,将纯化后胞外多糖命名为EPS-1。
2.6 胞外多糖红外光谱分析
瑞士乳杆菌MG0817-2EPS-1傅里叶变换红外光谱图见图4。由图4可知,瑞士乳杆菌MG0817-2EPS-1在3402.69cm-1、2 925.21 cm-1、1 654.78 cm-1、1 156.52 cm-1、1 020.48 cm-1、848.69 cm-1、762.60 cm-1处有吸收峰。其中,在3 402.69 cm-1处的吸收峰和2925.21cm-1处的吸收峰为EPS的特征吸收峰,O-H和C-H键伸缩振动产生的吸收峰[25]。1 654.78 cm-1处的吸收峰为COO-共振产生的吸收峰[26]。1 156.52 cm-1、1 020.48 cm-1处出现吸收峰,表明EPS-1中存在吡喃糖[27]。848.69 cm-1处出现吸收峰表明该糖具有β型糖苷键[28]。综上可知,瑞士乳杆菌MG0817-2 EPS-1是具有吡喃糖的β型杂多糖。
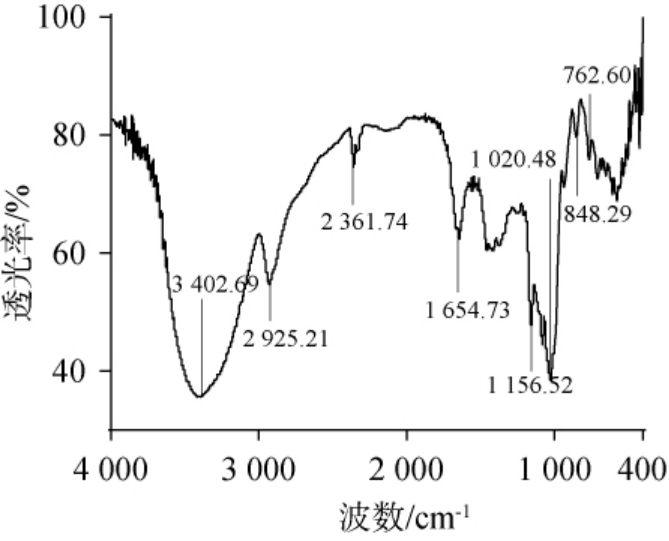
图4 瑞士乳杆菌MG0817-2胞外多糖傅里叶变换红外光谱图
Fig.4 Fourier transform infrared spectrum of extracellular polysaccharides of Lactobacillus helveticus MG0817-2
2.7 EPS-1抑菌活性
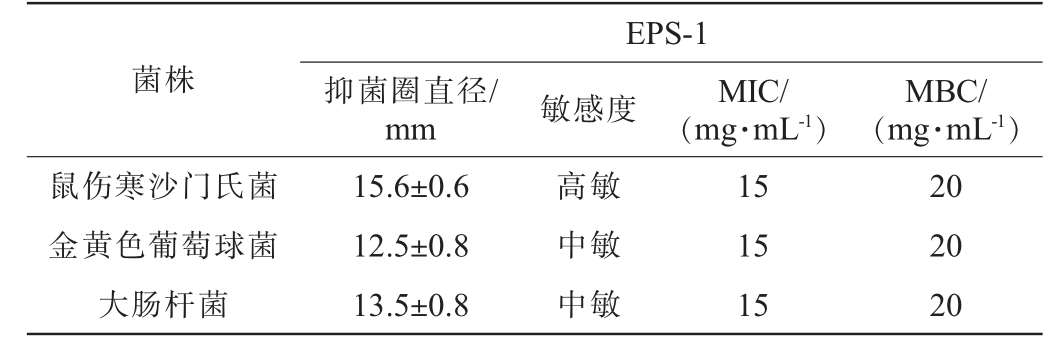
EPS抑菌活性是由多种机制协同作用的结果,主要包括促进益生菌肠道定植,抑制病原菌生长及促进益生菌生物膜的形成等[29]。EPS-1对致病菌的抑菌能力测定结果见表2。由表2可知,EPS-1对鼠伤寒沙门氏菌、大肠杆菌和金黄色葡萄球菌的抑菌能力分别为高敏、中敏、中敏,表明瑞士乳杆菌MG0817-2 EPS-1对鼠伤寒沙门氏菌的抑制效果更好,略高于普通小球藻(Chlorella vulgaris)224 EPS[30]。其MIC均为15 mg/mL,MBC均为20 mg/mL,表明EPS对致病菌具有一定的抑制效果。马蓝[31]的研究表明,干酪乳杆菌NA-2 EPS通过抑制E.coli O157∶H7表面的黏附特性达到抑制致病菌的作用。
表2 瑞士乳杆菌MG0817-2胞外多糖对致病菌的抑菌能力测定结果
Table 2 Determination results of antibacterial ability of Lactobacillus helveticus MG0817-2 extracellular polysaccharides to pathogenic bacteria
3 结论
瑞士乳杆菌(Lactobacillus helveticus)MG0817-2不产溶血素,对青霉素、阿莫西林、氨苄西林等β-内酰胺类抗生素高度敏感;对氧氟沙星、万古霉素、利福平及亚胺培南中度敏感,在pH 3.0培养液中的存活率为75%,在胆盐浓度为0.2%和0.4%时的存活率分别为88.89%、83.33%,其菌液及上清液均对致病菌具有抑菌效果,主要通过代谢产物抑制致病菌繁殖和生长。从瑞士乳杆菌MG0817-2上清液中分离出的EPS对致病菌具有一定抑制效果,经纯化后的胞外多糖EPS-1得率达71.9%,为具有吡喃糖的β型杂多糖,其中瑞士乳杆菌MG0817-2 EPS对鼠伤寒沙门氏菌的抑菌效果达到高度敏感,对鼠伤寒沙门氏菌、大肠杆菌和金黄色葡萄球菌的最低质量浓度(MIC)和最低杀菌浓度(MBC)分别为15 mg/mL和20 mg/mL。综上,瑞士乳杆菌MG0817-2具备良好的安全性,其产EPS抑菌活性较强,这可能是瑞士乳杆菌MG0817-2具有抗菌活性的原因之一,为益生菌在临床上的应用提供基础及EPS在食品、医疗领域的开发提供依据。
[1] SHAABAN S,HAMAD G M,GENENA S,et al.Evaluation of the antibacterial activity of Lactobacilli probiotics supernatants against Enterococcus faecalis(in-vitro study)[J].BMC Oral Health,2022,22(1):407.
[2] ÁLVAREZ-HERMS J,BURTSCHER M,CORBI F,et al.A narrative hypothesis:The important role of gut microbiota in the modulation of effort tolerance in endurance athletes[J].Nutrients,2025,17(17):2836.
[3] YAMASHITA M,UKIBE K,MATSUBARA Y,et al.Lactobacillus helveticus SBT2171 attenuates experimental autoimmune encephalomyelitis in mice[J].Front Microbiol,2017,8:2596.
[4] DE OLIVEIRA F L,SALGAÇO M K,DE OLIVEIRA M T,et al.Exploring the potential of Lactobacillus helveticus R0052 and Bifidobacterium longum R0175 as promising psychobiotics using SHIME[J]. Nutrients,2023,15(6):1521.
[5] 聂新.瑞士乳杆菌H11最适营养需求解析及培养条件优化[D].呼和浩特:内蒙古农业大学,2023.
[6] RAJOKA M S R,MEHWISH H M,KITAZAWA H,et al.Techno-functional properties and immunomodulatory potential of exopolysaccharide from Lactiplantibacillus plantarum MM89 isolated from human breast milk[J].Food Chem,2022,377:131954.
[7] LV H H,TENG Q,CHEN J H,et al.Probiotic potential of a novel exopolysaccharide produced by Bifidobacterium animalis subsp.Lactis SF[J].LWT-Food Sci Technol,2024,193:115764.
[8] ALI A H,BAMIGBADE G,TARIQUE M,et al.Physicochemical,rheological,and bioactive properties of exopolysaccharide produced by a potential probiotic Enterococcus faecalis 84B[J].Int J Biol Macromol,2023,240:124425.
[9] ZHANG J,CAO Y Q,WANG J,et al.Physicochemical characteristics and bioactivities of the exopolysaccharide and its sulphated polymer from Streptococcus thermophilus GST-6[J].Carbohydr Polym,2016,146:368-375.
[10] 褚鑫龙,马轲,高鹏程,等.羊肠道蒙氏肠球菌和屎肠球菌的分离鉴定及益生特性分析[J].微生物学通报,2024,51(7):93-101.
[11] 戴璐,袁亚宏,张宇翔,等.抗食源性致病菌益生菌的筛选及其抑菌活性评价(英文)[J].食品科学,2018,39(24):93-101.
[12] 陈亮.鼠李糖乳杆菌胞外多糖的分离纯化及其免疫调节作用研究[D].杭州:浙江工商大学,2023.
[13] 钱志瑶,罗永迪,李丽琼,等.半枝莲水提液体外抑菌及抑菌稳定性研究[J].中国现代医生,2023,61(21):69-72,80.
[14] 李晓颖,刘虹,张颜廷,等.5株植物乳杆菌生物学特性及安全性评价[J].食品工业科技,2017,38(20):115-119,24.
[15] 李秋月,杨雪娇,谭春艳,等.罗非鱼源肠道益生菌的分离鉴定及其体外益生特性分析[J].食品与生物技术学报,2023,42(12):1-9.
[16] MAKETE G,AIYEGORO O A,THANTSHA M S.Isolation,identification and screening of potential probiotic bacteria in milk from South African Saanen goats[J].Probiotics Antimicrob Proteins,2017,9(3):246-254.
[17] 马翠柳,蔡熙姮,刘超楠,等.北极狐源唾液乳杆菌ZJBF005的分离鉴定与体外益生功能的评价[J].动物营养学报,2023,35(5):3372-3381.
[18] 汤伟,李佳欣,唐涛,等.屎肠球菌Ef026的体外益生特性研究[J].中国饲料,2024(19):39-46.
[19] 何宇星,白高娃,于靖和,等.鼠李糖乳酪杆菌Z23的益生特性、安全性及全基因组关联分析[J].食品工业科技,2025,46(12):184-196.
[20] 聂阿真,倪子富,冯先阳,等.醋糟乳酸菌的筛选、鉴定及其益生特性研究[J].河南农业大学学报,2025,59(5):859-871.
[21] 张媛媛,赵梦迪,李悦垚,等.犬源嗜酸乳杆菌GLA09分离鉴定及其益生特性和安全性研究[J].中国畜牧杂志,2025,61(4):339-347.
[22] 陈楠,余泽旭,季暄,等.犬源抗氧化益生菌的筛选及功效评定[J].动物营养学报,2024,36(2):1303-1314.
[23] XUE X G,GAO Y F,LIU F,et al.Purification,characterization,and identification of a novel bacteriocin produced by Lacticaseibacillus casei KLS1,and its antimicrobial mechanism against Staphylococcus aureus[J].LWT-Food Sci Technol,2024,200:116207.
[24] XU X Q,PENG Q,ZHANG Y W,et al.Antibacterial potential of a novel Lactobacillus casei strain isolated from Chinese northeast sauerkraut andthe antibiofilm activity of its exopolysaccharides[J].Food Funct,2020,11(5):4697-4706.
[25] MAO Y R,WANG W X,MO W,et al.Purification,characterization,and hypoglycemic activity of exopolysaccharides from Lactiplantibacillus plantarum MY04[J].Int J Biol Macromol,2024,282:137008.
[26] WANG Z J,SHI Q,MIAO B,et al.Exopolysaccharide(EPS)synthesised from Azotobacter vinelandii and its characterisation and application in bioflotation[J].Minerals Eng,2024,211:108693.
[27] KONG Q,WANG D Z,CONG B L,et al.Structure characterization and cryoprotective activity of an exopolysaccharide from Pseudoalteromonas sp.LP6-12-2[J].Food Biosci,2024,57:103557.
[28] DE BRITO L P,DA SILVA E C,LINS L F,et al.Optimization,structural characterization,and biological applications of exopolysaccharide produced by Enterococcus faecium KT990028[J].Int J Biol Macromol,2024,282:136926.
[29] 李兆龙,闫露,肖学奎,等.植物乳杆菌胞外多糖对断奶仔猪生长性能、血清生化与免疫指标及肠道组织学的影响[J].畜牧与兽医,2024,56(8):32-37.
[30] 孙建瑞,赵君峰,符丹丹,等.响应面法优化Chlorella vulgaris 224胞外多糖积累及其抑菌和抗氧化活性[J].天然产物研究与开发,2020,32(3):489-497.
[31] 马蓝.干酪乳杆菌NA-2胞外多糖抑制大肠杆菌O157:H7生物膜形成的机制研究[D].北京:中国农业科学院,2022.